Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ejercicio 32 de Termo 2
Cargado por
jheisson kisimotoDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ejercicio 32 de Termo 2
Cargado por
jheisson kisimotoCopyright:
Formatos disponibles
32. Determine la temperatura máxima teórica de la e=1.
05
combustión del etano con un 30% de exceso de aire,
en un proceso en régimen estacionario. Los
reactantes entran a 25 °C y la reacción es completa. Balance de N:
SOLUCIÓN: 4.55∗3.76=d
C 2 H 6 +a ( O 2 +3.76 × N 2) ⟶ b∗C O 2 +c∗H 2 O+d∗N 2 d=17.108
Balance de C: Nos quedaría:
2=b C 2 H 6 + 4.55 ( O2 +3.76 × N 2) ⟶ 2 C O2+ 3 H 2 O+17.108 N 2+1.
Balance de H: Ahora que tenemos la ecuación con exceso balanceada
vemos que es un proceso de régimen estacionario y una
6=2∗c
reacción completa, por lo tanto, podemos aplicar la
3=c ecuación de la flama adiabática para poder de esa
manera encontrar la temperatura máxima teórica de la
Balance de O: combustión.
2∗a=2∗b+ c Aplicando la fórmula:
2∗a=4+ 3
a=3.5
Compuesto hT −h298 ,
Balance de N: s
º
△ hf , 298 h298 H 2O H2 O
P C O2 -393 520 9 364
3.76∗a=d
P H 2O -241 820 9 904
------
3.76∗3.5=d P/R O2 0 8682
d=13.16 P/R N2 0 8669
R C2 H6 -84 680 ------- 25 149
Nos quedaría:
C 2 H 6 +3.5 ( O2 +3.76 × N 2 ) ⟶ 2C O2 +3 H 2 O+13.16 N 2EN LOS PRODUCTO:
Ahora balanceamos con el 30% de exceso de aire Para el C O 2:
C 2 H 6 +1.3∗3.5 ( O2+3.76 × N 2 ) ⟶ b∗C O2 +c∗H 2 O+d∗N 2+ dH
O 2 =2 △ hº
CO f 2
[ CO 2 ,298 + hT −h298,
C O2 C O2
]
C 2 H 6 + 4.55 ( O 2 +3.76 × N 2) ⟶ b∗C O2 +c∗H 2 O+d∗N 2+ d O2
H C O =2 [−393 520+ hT −9 364 ]
2 C O2
Balance de C:
H C O =2 [−402 884+hT ]
2=b
2 C O2
Balance de H:
H C O =−805768+ 2 hT
2 C O2
6=2∗c Para el H 2 O :
3=c H H O =3 △ hf
2
[ º
H2 O ,298 +hT −h298 ,
H 2O H2 O
]
Balance de O:
H H O =3 [−241 820+hT −9 904 ]
4.55∗2=2∗b+ c+ 2e
2 H 2O
H H O =3 [−241 820+hT −9 904 ]
9.1=7+2 e 2 H 2O
2 e=2.1 H H O =3 [−251 724+hT
2 H 2O ]
H H O =−755 172+ 3 hT
2 H2 O
H ∏ ¿=69459.2084 kJ ¿
Para el N 2: Ahora vemos tablas del C O2 :
H N =17.108 △ hºf
2
[ N2 ,298 +hT −h298 ,
N2 N2
] T h u s∘
H N =17.108 [ hT −8669 ]
2 N2
H N =17.108 hT −148 309,252
2 N2
Para el O 2:
H O =1.05 △ h f
2
[ º
O2 ,298 +hT −h 298,
O2 O2
] Interpolamos:
H O =1.05 [ hT −8 682 ] 1460 ⟶ 68748
2 O2
T max ⟶ 69 459.2084
H O =1.05 hT −9116.1
2 O2
1480 ⟶ 69911
EN LOS REACTANTES:
T max −1460 69 459.2084−68 748
Para el C 2 H 6: =
1480−1460 69 911−68748
H C H = △ hºf
2 6
[ C 2H 6 ,298 + hT −h298 , C2 H 6 C 2H 6
] T max=1472.231 K
H C H =[ −84 680−25149 ]
2 6
Por lo tanto, la temperatura máxima de combustión del etano
es de 1 472.231 Kº
H C H =−109 829
2 6
Para el O 2:
H O = △ h ºf 2
[ O2 , 298 +h T −h298, O2 O2
]
H O =0 2
Para el N 2:
H N = △ hf 2
[ º
N2 , 298 +h T −h298 , N2 N2
]
H N =0 2
Luego sumamos todos lo obtenido y nos quedaría:
2 hT +3 hT +17.108 hT +1.05 hT =1 608 536.35
C O2 H 2O N2 O2
Pareciera que hubieran 4 incógnitas pero en verdad es una
T ∏ ¿¿ ya que h=H (T ) para gases ideales, entonces:
2 H ∏ ¿+3 H
∏ ¿+ 17.108 H∏ ¿ +1.05 H∏ ¿ =1608536.35 ¿ ¿ ¿ ¿
23.158 H ∏ ¿=1 608 536.35¿
23.158 H ∏ ¿=1 608 536.35¿
También podría gustarte
- Pregunta 7. Examen de Diseño de PlantasDocumento1 páginaPregunta 7. Examen de Diseño de PlantasKen Rojas FuentesAún no hay calificaciones
- Problema 7 - Reacciones QuímicasDocumento4 páginasProblema 7 - Reacciones QuímicasTony RodriguezAún no hay calificaciones
- Balances de Sistemas ReactivosDocumento17 páginasBalances de Sistemas ReactivosDavid Camilo Guerrero GonzalezAún no hay calificaciones
- Tarea Semana 8 Termo Compress PDFDocumento9 páginasTarea Semana 8 Termo Compress PDFRobert VDAún no hay calificaciones
- Trabajo de TermodinámicaDocumento10 páginasTrabajo de TermodinámicaDLPTAún no hay calificaciones
- Term Odin Á MicaDocumento10 páginasTerm Odin Á MicaDLPTAún no hay calificaciones
- 6.tarea Academica 06Documento4 páginas6.tarea Academica 06PIERO MATIAS HERRERA SUAREZAún no hay calificaciones
- Reacciones Químicas y CombustiónDocumento8 páginasReacciones Químicas y Combustiónjean ramos marin0% (1)
- Calculo de Temperatura de LlamaDocumento2 páginasCalculo de Temperatura de LlamaALBORNOZ ESCALANTE CARLOS EDUARDOAún no hay calificaciones
- Análisis de CalderaDocumento26 páginasAnálisis de CalderaomargelvezAún no hay calificaciones
- Tarea Semana 8 Termo Compress PDFDocumento13 páginasTarea Semana 8 Termo Compress PDFRobert VDAún no hay calificaciones
- Ejercicio de Temperatura de Llama AdiabáticaDocumento9 páginasEjercicio de Temperatura de Llama AdiabáticaJuan SandovalAún no hay calificaciones
- Tarea Termodinámica Semana 8Documento11 páginasTarea Termodinámica Semana 8sergio garciaAún no hay calificaciones
- Problema 13 - Reacciones QuímicasDocumento5 páginasProblema 13 - Reacciones QuímicasTony RodriguezAún no hay calificaciones
- Efectos TermicosDocumento6 páginasEfectos TermicosManuel RiegaAún no hay calificaciones
- Tarea Termodinámica Semana 1Documento5 páginasTarea Termodinámica Semana 1sergio garciaAún no hay calificaciones
- IQ.05.03 Taller 12Documento6 páginasIQ.05.03 Taller 12Silvana DotaAún no hay calificaciones
- Problemas Resueltos - TermoquímicaDocumento7 páginasProblemas Resueltos - TermoquímicaEva CaballeroAún no hay calificaciones
- Amy Zulema Velasco Bonilla - Ees2Documento4 páginasAmy Zulema Velasco Bonilla - Ees2amyzvbAún no hay calificaciones
- Procesos Químicos - Tema 2Documento14 páginasProcesos Químicos - Tema 2Jiajun XuAún no hay calificaciones
- Tarea N3 ReaccionesDocumento23 páginasTarea N3 ReaccionesKorayma CAAún no hay calificaciones
- Cinética ProblemasDocumento19 páginasCinética ProblemasCarmen RositaAún no hay calificaciones
- Seminario 1Documento18 páginasSeminario 1SEBASTIAN ALEJANDRO ARCE VILLARAún no hay calificaciones
- 2da ExposicionDocumento5 páginas2da ExposicionAlejandro Fuel67% (3)
- Ejer 8Documento17 páginasEjer 8Lenin A. GuevaraAún no hay calificaciones
- Asignación 30Documento8 páginasAsignación 30Fabrizio GiacobbeAún no hay calificaciones
- A) Benceno: 1) Determine La Entalpía de Combustión (KJ) Del Benceno y Del Octano A 25°CDocumento2 páginasA) Benceno: 1) Determine La Entalpía de Combustión (KJ) Del Benceno y Del Octano A 25°CTCAún no hay calificaciones
- Semana 08 TermodinamicaDocumento11 páginasSemana 08 TermodinamicaJames Lagos AcuñaAún no hay calificaciones
- PROBLEMA 6 7 8 9 y 10 para MileDocumento5 páginasPROBLEMA 6 7 8 9 y 10 para MileMarcelo Begazo MartínezAún no hay calificaciones
- FisicoquimicaDocumento2 páginasFisicoquimicaAdriana del Pilar Meza CalderonAún no hay calificaciones
- BustionDocumento11 páginasBustionJohn Erick CalsinAún no hay calificaciones
- Termidinamica Control3Documento7 páginasTermidinamica Control3Nicolas de la FuenteAún no hay calificaciones
- Aplicaciones de Propiedades ResidualesDocumento2 páginasAplicaciones de Propiedades ResidualesDer Gute Kerl RealAún no hay calificaciones
- Proyecto TermoDocumento6 páginasProyecto TermokevinAún no hay calificaciones
- Ejercicio 3.14Documento3 páginasEjercicio 3.14putes timmyAún no hay calificaciones
- Tarea Semana 8 TermoDocumento9 páginasTarea Semana 8 Termomiguel100% (1)
- Ejemplos Tema 2B HidrostáticaDocumento28 páginasEjemplos Tema 2B HidrostáticaBea NúñezAún no hay calificaciones
- Adriana Del Pilar Meza Calderón Problema. Termoquímica.: P VC Productos VC ReactivosDocumento2 páginasAdriana Del Pilar Meza Calderón Problema. Termoquímica.: P VC Productos VC ReactivosAdriana del Pilar Meza CalderonAún no hay calificaciones
- Determinar Cuál Es La Fórmula y Como Se Dedujo La Ecuación Fundamental de La Hidrostática Con Una Extensión Máxima de UnaDocumento5 páginasDeterminar Cuál Es La Fórmula y Como Se Dedujo La Ecuación Fundamental de La Hidrostática Con Una Extensión Máxima de Unatannia yeraldin suarez jimenezAún no hay calificaciones
- Ejercicios Equilibrio Químico y Le ChatelierDocumento3 páginasEjercicios Equilibrio Químico y Le ChatelierRocío PrelatoAún no hay calificaciones
- Reacciones 1-13-23-12Documento6 páginasReacciones 1-13-23-12Giuliana Estefany Alania LlanosAún no hay calificaciones
- Ayudantia 2Documento4 páginasAyudantia 2Cristóbal AppelgrenAún no hay calificaciones
- Miguel Honorato Tarea8termoDocumento8 páginasMiguel Honorato Tarea8termomiguel100% (1)
- Tarea 3.1Documento5 páginasTarea 3.1Deniz DenilsonAún no hay calificaciones
- Laboratorio 3 Procesos 2Documento13 páginasLaboratorio 3 Procesos 2Walter Crisólogo PérezAún no hay calificaciones
- Tarea Semana 8 TermodinámicaDocumento6 páginasTarea Semana 8 TermodinámicaOscar 1100% (3)
- Ejercicio 01Documento5 páginasEjercicio 01Daniel FuqueneAún no hay calificaciones
- Semana 1-2Documento43 páginasSemana 1-2LEONARDO PIERO TORRES HUAMANAún no hay calificaciones
- Fisicoquimica - Estudiante - 1 Sohana DavilaDocumento16 páginasFisicoquimica - Estudiante - 1 Sohana Davilasohana davilaAún no hay calificaciones
- MetanizadorDocumento6 páginasMetanizadorHugo MárquezAún no hay calificaciones
- Clase 020922Documento44 páginasClase 020922Diegho williamsAún no hay calificaciones
- CONO INVERTIDO FinalllllllllDocumento6 páginasCONO INVERTIDO Finalllllllllirving_mendoza_58Aún no hay calificaciones
- Anexo 1 - Esteban - MonguiDocumento11 páginasAnexo 1 - Esteban - MonguiDaniel FuqueneAún no hay calificaciones
- 13 16Documento17 páginas13 16Javier De la CruzAún no hay calificaciones
- Formula Empírica y MolecularDocumento3 páginasFormula Empírica y MolecularMelany Kuka VivasAún no hay calificaciones
- So Lucio NarioDocumento4 páginasSo Lucio NarioDante Bazan MartinezAún no hay calificaciones
- Video Diagrama PorubaixDocumento7 páginasVideo Diagrama PorubaixMatias OtárolaAún no hay calificaciones
- Claudio - Apablaza Tarea8Documento11 páginasClaudio - Apablaza Tarea8Claudio ApablazaAún no hay calificaciones
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Grupo 4 - Ejercicio 8Documento4 páginasGrupo 4 - Ejercicio 8jheisson kisimotoAún no hay calificaciones
- Trabajo Tarea 4Documento1 páginaTrabajo Tarea 4jheisson kisimotoAún no hay calificaciones
- Max y Min-Trabajo en GrupoDocumento5 páginasMax y Min-Trabajo en Grupojheisson kisimotoAún no hay calificaciones
- Grupo 1 - Ejercicio 10Documento5 páginasGrupo 1 - Ejercicio 10jheisson kisimotoAún no hay calificaciones
- Grupo 5 - Ejercicio 7Documento3 páginasGrupo 5 - Ejercicio 7jheisson kisimotoAún no hay calificaciones
- Importancia de La TermodinámicaDocumento4 páginasImportancia de La Termodinámicajheisson kisimotoAún no hay calificaciones
- Ejercicio 12 FluidosDocumento1 páginaEjercicio 12 Fluidosjheisson kisimotoAún no hay calificaciones
- Ejercicio 12 FluidosDocumento1 páginaEjercicio 12 Fluidosjheisson kisimotoAún no hay calificaciones
- Numero 9 FluidosDocumento1 páginaNumero 9 Fluidosjheisson kisimotoAún no hay calificaciones
- Ejercicio 8 FluidosDocumento1 páginaEjercicio 8 Fluidosjheisson kisimotoAún no hay calificaciones
- Tarea 02 Desarrollada, Grupo 04Documento36 páginasTarea 02 Desarrollada, Grupo 04jheisson kisimotoAún no hay calificaciones
- Numero 9 FluidosDocumento1 páginaNumero 9 Fluidosjheisson kisimotoAún no hay calificaciones
- Problema Fluidos 4Documento1 páginaProblema Fluidos 4jheisson kisimotoAún no hay calificaciones
- Ejercicio 14 - Tarea 1Documento3 páginasEjercicio 14 - Tarea 1jheisson kisimotoAún no hay calificaciones
- EJERCICIO 10 FluidosDocumento2 páginasEJERCICIO 10 Fluidosjheisson kisimotoAún no hay calificaciones
- Cuarta Lamina Terminada-Grupo 03Documento13 páginasCuarta Lamina Terminada-Grupo 03jheisson kisimotoAún no hay calificaciones
- Motor OttoDocumento16 páginasMotor Ottojheisson kisimotoAún no hay calificaciones
- Tarea 03 de Física - Tercer CicloDocumento10 páginasTarea 03 de Física - Tercer Ciclojheisson kisimotoAún no hay calificaciones
- Problema 2 - Termo IiDocumento3 páginasProblema 2 - Termo Iijheisson kisimotoAún no hay calificaciones
- Trabajo GrupalDocumento20 páginasTrabajo Grupaljheisson kisimotoAún no hay calificaciones
- Tarea de Semana 3Documento1 páginaTarea de Semana 3jheisson kisimotoAún no hay calificaciones
- Parte 1Documento19 páginasParte 1jheisson kisimotoAún no hay calificaciones
- Primer DibujoDocumento1 páginaPrimer Dibujojheisson kisimotoAún no hay calificaciones
- Del 1 Al 4Documento4 páginasDel 1 Al 4jheisson kisimotoAún no hay calificaciones
- Ejercicio 8 TermoDocumento3 páginasEjercicio 8 Termojheisson kisimotoAún no hay calificaciones
- Tarea Número 03Documento12 páginasTarea Número 03jheisson kisimotoAún no hay calificaciones
- Tarea Número 01Documento13 páginasTarea Número 01jheisson kisimotoAún no hay calificaciones
- Guía Ruta NVSDocumento150 páginasGuía Ruta NVSDaniel Felipe Florez GilAún no hay calificaciones
- Folleto Maestría en Gestión de TI UNADDocumento16 páginasFolleto Maestría en Gestión de TI UNADfranco1702Aún no hay calificaciones
- Marco TeóricoDocumento3 páginasMarco TeóricoMilena MesaAún no hay calificaciones
- Ficha Técnica CdiDocumento3 páginasFicha Técnica CdiMagali González100% (1)
- Arras y Joint VentureDocumento33 páginasArras y Joint VentureKenny Arriaga RodríguezAún no hay calificaciones
- Notebook Inspiron 14 3000 Core I3-5005u 4GB 500GB 14Documento2 páginasNotebook Inspiron 14 3000 Core I3-5005u 4GB 500GB 14Nico InfanteAún no hay calificaciones
- Plan de Saguridad Defensa CivilDocumento24 páginasPlan de Saguridad Defensa CivilAlvaro JosuéAún no hay calificaciones
- Herramientas para El Líder Del ProyectoDocumento4 páginasHerramientas para El Líder Del ProyectoMarielena Surco ApazaAún no hay calificaciones
- Como Desarrollar El FacultamientoDocumento11 páginasComo Desarrollar El FacultamientoDamaris VallejoAún no hay calificaciones
- 3 - DOP - Agregada - Ejemplos de Clase (3 Planes) - PlantillaDocumento3 páginas3 - DOP - Agregada - Ejemplos de Clase (3 Planes) - PlantillaJenny .Aún no hay calificaciones
- U8 - CondominiosDocumento4 páginasU8 - CondominiosCesar VeraAún no hay calificaciones
- Fonema Y - LL PLAN DE CLASE SEMANAL 2017Documento3 páginasFonema Y - LL PLAN DE CLASE SEMANAL 2017pfrancoh0567% (3)
- Ay 104Documento1 páginaAy 104Samuel Amilcar Infante LevaAún no hay calificaciones
- 3A Distribución NormalDocumento30 páginas3A Distribución NormalAlbert SotonAún no hay calificaciones
- Olimpiadas FTR 2023Documento6 páginasOlimpiadas FTR 2023Carlos SosayaAún no hay calificaciones
- Resumen Ejecutivo Diciembre 2018Documento65 páginasResumen Ejecutivo Diciembre 2018Daniela Rodriguez CuartasAún no hay calificaciones
- Guía de Aprendizaje 06 Tdimst-3 Comunicaciones DigitalesDocumento8 páginasGuía de Aprendizaje 06 Tdimst-3 Comunicaciones DigitalesjohanestevenAún no hay calificaciones
- Marco General y Proceso Constructivo Del Puente Allccomachay-1-25Documento25 páginasMarco General y Proceso Constructivo Del Puente Allccomachay-1-25Angelo Renato Lazo ParedesAún no hay calificaciones
- Taller-u2-Clase 2-s4 Cuento de BellisaDocumento5 páginasTaller-u2-Clase 2-s4 Cuento de BellisaMelissa Contreras Delgado100% (3)
- 5 - Los AdjetivosDocumento15 páginas5 - Los AdjetivosMaria Eugenia MiraAún no hay calificaciones
- Cuadernillo WASHDocumento43 páginasCuadernillo WASHdeyaniraAún no hay calificaciones
- Tarea Termo 1 PDFDocumento3 páginasTarea Termo 1 PDFLucero CárdenasAún no hay calificaciones
- Programa Analitico MicrobiologíaDocumento2 páginasPrograma Analitico MicrobiologíaPonce Alejandro LuisAún no hay calificaciones
- Plan Quinto AnualDocumento150 páginasPlan Quinto AnualOLIN ROSALINA GUDIEL GRIJALVAAún no hay calificaciones
- Ley TransitoriaaDocumento6 páginasLey TransitoriaaAnita EscalanteAún no hay calificaciones
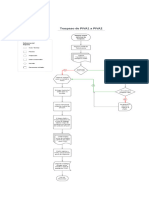
- Procesos de Envios de PIVA1 A PIVA2Documento1 páginaProcesos de Envios de PIVA1 A PIVA2casa.maravillas273Aún no hay calificaciones
- Absolucion Denuncia IndecopiDocumento3 páginasAbsolucion Denuncia IndecopiCristhian CarreonAún no hay calificaciones
- Cat - VW AutotodoDocumento96 páginasCat - VW AutotodoBernardo Salinas TeránAún no hay calificaciones
- HLM - ASM - Diri - Sem 02Documento2 páginasHLM - ASM - Diri - Sem 02Carlos Martín Medina TáberAún no hay calificaciones
- Séptimo 7Documento4 páginasSéptimo 7Joel HernandezAún no hay calificaciones