Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Determinacion de Datos de Equilibrio
Cargado por
Karen Siñani QuelaliDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Determinacion de Datos de Equilibrio
Cargado por
Karen Siñani QuelaliCopyright:
Formatos disponibles
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
PRACTICA Nº 7
DETERMINACIÓN DE DATOS DE EQUILIBRIO
7.1.- OBJETIVO
El objetivo del presente laboratorio es obtener los datos del equilibrio líquido vapor de
una mezcla binaria a la presión atmosférica de la ciudad de La Paz
7.2.- FUNDAMENTO TEÓRICO
El principio básico de la destilación es tan simple como antiguo; cuando se hierve una
solución el vapor usualmente difiere en composición del líquido residual. Si se tienen solo
dos componentes, uno se concentra en el condensado y el otro en el líquido residual. Si hay
más de dos componentes cada uno se concentra en el condensado o en el residuo,
exceptuando alguno ocasional que se puede encontrar en igual concentración en ambos
productos.
La facilidad con la cual se vaporiza un componente es llamada su volatilidad, y las
volatilidades relativas entre varios componentes determinan sus relaciones de equilibrio
líquido vapor.
El componente que se vaporiza con mayor facilidad de una solución en equilibrio es
llamado el más volátil o el más ligero. El componente que se vaporiza con menos facilidad
es llamado menos volátil o el mas pesado. Las volatilidades se expresan numéricamente
como cocientes de equilibrio, constantes de equilibrio y como volatilidades relativas
Cocientes de equilibrio
Un cociente de equilibrio expresa la relación que existe entre un vapor y un líquido en
ebullición en equilibrio físico mutuo. Para cada componente,
y K .x
y x
K
relaciones como componentes haya.
El cociente de equilibrio para cada componente depende de la temperatura, de la presión y
de las composiciones del líquido y del vapor. Puesto que un aumento de temperatura
favorece la vaporización y el aumento de la presión la dificulta, los cocientes de equilibrio
generalmente se hacen mas grandes conforma se aumenta la temperatura o se diminuye la
presión. Los cocientes de equilibrio no dependen de las cantidades presentes de líquido y
vapor. Si una solución se vaporiza parcialmente y se deja llegar al equilibrio, el retirar una
porción del liquido o del vapor (manteniendo la temperatura y la presión constantes) no
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
cambia la composición de ninguna de las fases
Constantes de equilibrio
La constante de equilibrio para cualquier componente en condiciones dadas solo dependerá
de las propiedades del componente puro; en consecuencia cualquier constante de equilibrio
queda fijada al señalar la presión y la temperatura, las constantes de equilibrio se denotan
Ko
Volatilidades relativas
La destilación separa en virtud de la diferencia de volatilidad, los cocientes de equilibrio
son menos importantes que sus relaciones mutuas. Estas relaciones secundarias se expresan
KA y A xB
A B .
KB x A yB
Conforme se aumenta la temperatura, las volatilidades de diferentes sustancias
generalmente se acercan entre si. Ya que el aumento de presión en cualquier sistema
aumenta su temperatura de ebullición, las volatilidades relativas generalmente Irán
disminuyendo conforme se aumenten las presiones
Relaciones de equilibrio
Sistemas ideales
Las constantes de equilibrio deben ser aplicables en sistemas ideales puesto que las
volatilidades son independientes de la composición. Para cada componente en un sistema
ideal, se tiene
y K o .x
Cuando las leyes de los gases perfectos se cumplen en un sistema ideal, las constantes de
equilibrio se pueden calcular a partir de las presiones de vapor. En una mezcla de gases
perfectos la presión parcial de cada componente es proporcional a su concentración
p . y (1)
Do P
Puesto que la cantidad de un componente que escapa de una solución ideal por unidad de
tiempo es proporcional a su concentración en el líquido, su presión parcial en el vapor será
también proporcional a su concentración en el líquido, o sea:
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
p C.x (2)
Donde C x 1 , la presión parcial de un componente es igual a
pv C pv
p p v .x (3)
Combinando las ecuaciones (1 y (3) se obtiene:
pv
y .x
De donde, si se cumplen las leyes de los gases perfectos
pv
Ko
Esta relación solo puede ser valida a bajas presiones ya que las leyes de los gases perfectos
se cumplen solo en esas condiciones. Cuando se cumplen las leyes de los gases perfectos, la
volatilidad relativa de un compone
ideal debe ser igual al cociente de sus presiones de vapor:
KA pvA
A B
KB pvB
Esta relación deriva de la definición de volatilidad relativa
Sistemas no ideales
Los sistemas vapor-liquido pueden desviarse de la idealidad debido a la no idealidad de la
solución liquida, de la mezcla de vapores o de ambas. Las desviaciones pueden provenir de
varias causas, como ser asociación entre las moléculas de diferentes componentes, por
ejemplo. Sea cual fuere
K .K o
Ko
Un coeficiente de actividad puede ser considerado como el factor que toma en cuenta el
cambio de ambiente de las moléculas de un compuesto puro cuando moléculas extrañas son
agregadas a el
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
El valor correspondiente a un componente puro debe ser 1,0. si solamente se añade una
pequeña cantidad de una sustancia extraña, el efecto sobre el compuesto original es
pequeño y su coeficiente de actividad permanece cercano a 1,0. Conforme la cantidad de
sustancias extrañas va en aumento el cambio en su medio se hace mayor y el coeficiente de
actividad se aleja más de 1,0. Para la mayoría de los sistemas no ideales tales desviaciones
conducen a valores numéricos del coeficiente de actividad mayores de 1,0.
factores:
L V ere a la no
L
Ecuaciones de equilibrio para sistemas binarios
A cada líquido en ebullición corresponde un vapor en equilibrio cuya composición queda
determinada por los cocientes de equilibrio de sus componentes. Para un sistema binario la
ecuación de equilibrio puede expresarse en función de la volatilidad relativa, esto es:
A B .x A
yA
1 ( A B 1).x A
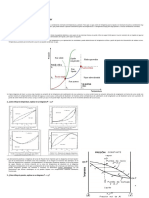
Esta ecuación se deriva directamente de la definición de volatilidad relativa. Las ecuaciones
de equilibrio para sistemas binarios se representan frecuentemente mediante graficas de
composición de vapor contra composición de líquido. Tales graficas reciben el nombre de
diagramas de equilibrio. Debido a que usualmente las destilaciones se conducen en
condiciones aproximadamente isobaricas, los diagramas de equilibrio se elaboran para
presión constante.
Cuando los componentes de un sistema binario son semejantes entre si, el sistema suele
acercarse a la idealidad. Aun cuando las volatilidades relativas en un sistema binario ideal
pueden cambiar con la composición, tales variaciones suelen ser pequeñas; cuando existen,
la volatilidad relativa aumenta conforme crece la concentración del componente más ligero.
Cualquier cambio ocurre en ese sentido, puesto que la temperatura de ebullición baja al
aumentar la proporción del componente ligero, y las volatilidades relativas son mayores a
bajas temperaturas
Cuando los componentes de un sistema binario no son semejantes entre si, este
normalmente no es ideal, en consecuencia es de esperarse que las volatilidades relativas
cambien sustancialmente conforme varían las proporciones de los componentes.
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
En casos extremos la volatilidad relativa puede cambiar tan drásticamente que el
componente más volátil en ciertas composiciones pase a ser el menos volátil en otras
7.3.- MATERIAL, EQUIPO Y REACTIVOS
- Un refractómetro de Abbe
- Un calderin tipo Othmer
- Termocuplas
- Termómetro digital
- Chaqueta eléctrica de calefacción
- 2 pipetas graduadas de 10 ml
- 2 pipetas graduadas de 5 ml
- Algodón (cada alumno debe traer)
- 10 Tubos de ensayo con sus respectivas tapas
- 5 vasos de precipitados de 100 ml
- 1 Probeta graduada de de vidrio de 50 ml
- 1 Balanza analitica
- 1 Picnómetro
- Material de limpieza (cada alumno debe traer)
- Etanol absoluto
- Acetona
- Benceno
- Agua destilada
7.4.- PROCEDIMIENTO EXPERIMENTAL
a) Utilizar un calderin tipo Othmer provisto de un termómetro (o termocuplas conectadas a
un termómetro digital) como el mostrado en la figura 1
b) Depositar en el calderin aproximadamente 25 ml de etanol absoluto, llevándolo
posteriormente a su punto de ebullición. Una vez que la temperatura de ebullición sea
estable, sacar una muestra tanto del destilado como del residuo y proceder a leer sus
respectivos índices de refracción
c) Adicionar en el calderin 5 ml de agua destilada y dejar que llegue y se estabilice en su
punto de ebullición, sacar una muestra del destilado y del residuo y leer sus índices de
refracción
d) Repetir la operación del punto anterior hasta que el punto de ebullición de la mezcla
liquida sea igual a la del agua pura en la ciudad de La Paz
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
Figura 1
7.5.- CALCULOS, GRAFICAS Y RESULTADOS
a) Con los datos obtenidos en la anterior practica, construir los siguientes diagramas de
- en papel milimetrado:
i) x y (Composición en la fase liquida Composición en la fase vapor )
ii) T x-y (Temperatura Composiciones)
iii) P x,y (Presión Composiciones)
iv) H x,y (Entalpia Composiciones)
b) Hallar el valor medio de la volatili
c) De manera teórica, a la presión atmosférica de 760 mmHg construir los siguientes
-
i) x y (Composición en la fase liquida Composición en la fase vapor )
ii) T x-y (Temperatura Composiciones)
iii) P x,y (Presión Composiciones)
iv) H x,y (Entalpía Composiciones)
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
7.6.- CONCLUSIONES Y RECOMENDACIONES
7.7.- CUESTIONARIO
1.- Diferencias entre gas y vapor
2.- Definir punto critico para una sustancia pura
3.- Como influye la temperatura, explicar en un diagrama P x,y
4.- Como influye la presión, explicar en un diagrama T x,y
5.- Indicar tres métodos de cálculo para establecer los datos de equilibrio en una mezcla
binaria ideal
6.- Diferencia entre presión y presión de vapor
7.- Como se calcula la presión y la temperatura critica de una mezcla gaseosa
multicomponente (tomar como ejemplo el gas natural)
8.- Definir volatilidad y fugacidad
9.- Definir solución liquida ideal y mezcla gaseosa ideal
10.- En una mezcla binaria ideal, en que rango de concentración se aplica la Ley de Raoult
11.- Describir y explicar las desviaciones de la Ley de Raoult
12.- Definir termodinámicamente el equilibrio liquido vapor
13.- Definir presión de convergencia para una mezcla gaseosa multicomponente
14.- Expresar una ecuación en la que se relacione la constante de equilibrio como función
del coeficiente de actividad
15.- Como se define factor de separación en destilación
16.- Que métodos teóricos se aplicarían para determinar la composición de una mezcla
ternaria ideal
17.- Explicar la ecuación de Antoine
18.- Para la mezcla binaria ideal (Agua - Etanol) que se encuentra a la presión atmosférica
de 495 mmHg. determinar los diagramas: x y ; T-x,y ; P-x,y ; H-x,y
Considerar los siguientes datos:
Constantes de antoine, rango de temperatura (0 100)ºC
Componente A B C
Agua 8,07131 1730,63 233,426
Etanol 8,1122 1592,864 226,184
19.- Las presiones de vapor del benceno y del heptano a distintas temperaturas son las
siguientes:
Ing. William Cusi Aruquipa
Universidad Mayor de San Andrés
Facultad de Ingeniería
Ingeniería Química, Ambiental, Alimentos y Petroquímica
Laboratorio de Especialidad
La Paz Bolivia
t ºC PC6 H1 4 mmHg PC7 H1 6 mmHg
69 760 295
70 780 302
75 915 348
80 1020 426
85 1225 498
90 1405 588
95 1577 675
99,2 1765 760
Determínese:
a) Los datos de equilibrio x y a la presión de 760 mmHg
b) La volatilidad relativa para cada temperatura
c) La relación analítica entre las composiciones de equilibrio vapor liquido de la mezcla,
tomando el valor medio de la volatilidad relativa
2.8.- BIBLIOGRAFIA
- Operaciones de Transferencia de Masa ROBERT TREYBAL
- Problemas de Ingeniería Química OCON TOJO
- Operaciones Básicas de Ingeniería Química MC CABE SMITH
- Introducción a la Ingeniería química BADGER BANCHERO
- Operaciones Básicas de la Ingeniería Química GRANGER BROWN
- Procesos de Transporte y Operaciones Unitarias J. GEANKOPLIS
Ing. William Cusi Aruquipa
También podría gustarte
- Ley de Accion de Masas FinalDocumento18 páginasLey de Accion de Masas FinalEdward PriceAún no hay calificaciones
- Tema5-Equilibrio en Fase GaseosaDocumento34 páginasTema5-Equilibrio en Fase Gaseosamahernan13Aún no hay calificaciones
- Práctica 7. Equilibrio Químico (Teoría)Documento10 páginasPráctica 7. Equilibrio Químico (Teoría)Panky Monteagudo RevolorioAún no hay calificaciones
- APUNTES - CINÉTICA UNIDAD SubrayadoDocumento5 páginasAPUNTES - CINÉTICA UNIDAD SubrayadojoaquinAún no hay calificaciones
- Equilibrio Manual Iniciación Química-1Documento69 páginasEquilibrio Manual Iniciación Química-1LUCIA GUADALUPEAún no hay calificaciones
- Definicion de EquilibrioDocumento11 páginasDefinicion de EquilibrioDalis RangelAún no hay calificaciones
- Practica 5 - Equilibrio Químico - Equipo 3Documento21 páginasPractica 5 - Equilibrio Químico - Equipo 3Martínez Alvarez EderAún no hay calificaciones
- Constante de EquilibrioDocumento10 páginasConstante de EquilibrioMD Cuqui RiveroAún no hay calificaciones
- Informe 10 Equilibrio QuímicoDocumento25 páginasInforme 10 Equilibrio QuímicoAnthony Ruiz ChavezAún no hay calificaciones
- Manual Aplicación QuímicaDocumento104 páginasManual Aplicación QuímicaJosé SalinasAún no hay calificaciones
- Mod 4 P2 Equilibrio Quimico 2021Documento16 páginasMod 4 P2 Equilibrio Quimico 2021Nico BarriosAún no hay calificaciones
- Apunte Unidad #4 - Equilibrio QuímicoDocumento14 páginasApunte Unidad #4 - Equilibrio QuímicoMarcos AgustinAún no hay calificaciones
- 3-4 Tipos de EquilibrioDocumento9 páginas3-4 Tipos de EquilibrioMax Bryan Rodriguez GarciaAún no hay calificaciones
- Tarea TermoDocumento13 páginasTarea TermodanielYT.Aún no hay calificaciones
- Termo 2 ExpoDocumento12 páginasTermo 2 ExpoADOLFO LOPEZ HERNANDEZAún no hay calificaciones
- Capitulo V. - Aplicaciones Del Equilibrio Químico IDocumento24 páginasCapitulo V. - Aplicaciones Del Equilibrio Químico IytkogAún no hay calificaciones
- Taller EquilibrioDocumento9 páginasTaller Equilibriolaura0% (1)
- Equilibrio QuímicoDocumento41 páginasEquilibrio QuímicoANDREA MUENTES CASADIEGOAún no hay calificaciones
- 8) 9.1 Equilibrio QuimicoDocumento11 páginas8) 9.1 Equilibrio QuimicomarianomcasellaAún no hay calificaciones
- Importante Trabajo de Equilibri Qui 1Documento19 páginasImportante Trabajo de Equilibri Qui 1Anonymous OrRURipAún no hay calificaciones
- Universidad Nacional Agraria La Molina: Facultad de Ciencias Departamento Académico de QuímicaDocumento16 páginasUniversidad Nacional Agraria La Molina: Facultad de Ciencias Departamento Académico de QuímicaLourdes LuqueAún no hay calificaciones
- Guia de Ejercicios y Problemas - Unidad 7Documento9 páginasGuia de Ejercicios y Problemas - Unidad 7hotmuysoyAún no hay calificaciones
- P2017 Equilibrio QuímicoDocumento4 páginasP2017 Equilibrio QuímicoRoberto FernandezAún no hay calificaciones
- Informe Punto BurbujaDocumento9 páginasInforme Punto Burbujalau2631Aún no hay calificaciones
- 9.1 Equilibrio QuimicoDocumento11 páginas9.1 Equilibrio QuimicofrancoAún no hay calificaciones
- TALLER 6-Equilibrio QuimicoDocumento8 páginasTALLER 6-Equilibrio QuimicoAlejandra Garcia RuizAún no hay calificaciones
- Clase Equilibrio Químico UJAP 2020Documento9 páginasClase Equilibrio Químico UJAP 2020Ivan VAún no hay calificaciones
- Equilibrio Químico Es La Denominación Que Se Hace A Cualquier Reacción Reversible Cuando Se Observa Que Las Cantidades Relativas de Dos o Más Sustancias Permanecen ConstantesDocumento8 páginasEquilibrio Químico Es La Denominación Que Se Hace A Cualquier Reacción Reversible Cuando Se Observa Que Las Cantidades Relativas de Dos o Más Sustancias Permanecen ConstantesZHARICK MIRANDAAún no hay calificaciones
- CONCEPTOS UNIDAD 2 - Flores - Acosta - SamaraDocumento8 páginasCONCEPTOS UNIDAD 2 - Flores - Acosta - SamaraFlores Acosta Karen SamaraAún no hay calificaciones
- Clase 3. Soluciones Ideales No IdealesDocumento6 páginasClase 3. Soluciones Ideales No IdealesGloria Beatriz Delvalle MAún no hay calificaciones
- Resumen Equilibrio QuímicoDocumento2 páginasResumen Equilibrio Químicoprobe13Aún no hay calificaciones
- Ilovepdf MergedDocumento75 páginasIlovepdf MergedIngrid Tahis Conforme MeraAún no hay calificaciones
- MEZCLASDocumento5 páginasMEZCLASCarla Lara SalgadoAún no hay calificaciones
- Glosario N°7Equilibrio QuimicoDocumento9 páginasGlosario N°7Equilibrio QuimicoBoris Milton Mamani IchutaAún no hay calificaciones
- Equilibrio Liquido VaporDocumento8 páginasEquilibrio Liquido VaporARNOLD BRAVO RAMIREZAún no hay calificaciones
- QG F-TEMA 9-2017-Equilibrio Fase GaseosaDocumento26 páginasQG F-TEMA 9-2017-Equilibrio Fase Gaseosaarmando fuentesAún no hay calificaciones
- Practica 5 Equilibrio QuimicoDocumento10 páginasPractica 5 Equilibrio QuimicoAlelí CovaAún no hay calificaciones
- Practico 3 - Sustancias Puras - Elias BarzonDocumento6 páginasPractico 3 - Sustancias Puras - Elias BarzonLuz Valentina Crispin MolloAún no hay calificaciones
- Equilibrio QuimicoDocumento19 páginasEquilibrio QuimicoIsmael A Cu NahAún no hay calificaciones
- Informe de DestilacionDocumento44 páginasInforme de DestilacionReina PinedoAún no hay calificaciones
- BinariosDocumento100 páginasBinariosOscar RodriguezAún no hay calificaciones
- Cinética QuímicaDocumento10 páginasCinética QuímicaLuz GodoyAún no hay calificaciones
- Elv Etanol AguaDocumento18 páginasElv Etanol AguaJuan Montalvo CerronAún no hay calificaciones
- Informe 10 Equilibrio - QuimicoDocumento17 páginasInforme 10 Equilibrio - QuimicoRonald Gomez OrellanaAún no hay calificaciones
- p4. Lab Termo 1Documento15 páginasp4. Lab Termo 1Castillo Pérez PaulinaAún no hay calificaciones
- Teoria EQUILIBRIO QUÍMICODocumento17 páginasTeoria EQUILIBRIO QUÍMICORoxana ChávezAún no hay calificaciones
- Volatilidad RelativaDocumento6 páginasVolatilidad RelativaAna Milena Castañeda Villamarin100% (1)
- Equilibrio Quimico FelixDocumento17 páginasEquilibrio Quimico FelixOlimpiada Ciencia Tabasco100% (1)
- Equilibrio LiquidoDocumento2 páginasEquilibrio LiquidoYarilithAún no hay calificaciones
- Resumen de La Unidad 2 - Equilibrio Quimico - Godoy BautistaDocumento9 páginasResumen de La Unidad 2 - Equilibrio Quimico - Godoy BautistaPAULINA JOSELINE GODOY BAUTISTAAún no hay calificaciones
- Presentaciónpq EquilibrioDocumento43 páginasPresentaciónpq EquilibrioCentzon TotochtinAún no hay calificaciones
- Equilibrio QuimicoDocumento49 páginasEquilibrio QuimicoRamiro BritoAún no hay calificaciones
- Tarea 2.2 EquilibrioDocumento8 páginasTarea 2.2 Equilibriopaola poma gutierrez0% (1)
- Influencia Del Efecto Salino en La Velocidad de ReaccionesDocumento36 páginasInfluencia Del Efecto Salino en La Velocidad de ReaccionesCris Hidalgo100% (2)
- Resumen para Teórico N°3Documento14 páginasResumen para Teórico N°3estefanisAún no hay calificaciones
- Diferencia Entre Gas y VaporDocumento8 páginasDiferencia Entre Gas y VaporJosé TorrezAún no hay calificaciones
- Informe Final Liquido - VaporDocumento8 páginasInforme Final Liquido - VaporMauricio Alejandro PadillaAún no hay calificaciones
- Lectura 11 Fisico QuimicoDocumento14 páginasLectura 11 Fisico QuimicoRuben AuronAún no hay calificaciones
- Soluciones IdealesDocumento10 páginasSoluciones IdealesJazz OramasAún no hay calificaciones
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- Aminoacidos EsencialesDocumento8 páginasAminoacidos EsencialesKaren Siñani QuelaliAún no hay calificaciones
- Que Es El PDCAASDocumento3 páginasQue Es El PDCAASKaren Siñani QuelaliAún no hay calificaciones
- Clasificación de Los AlimentosDocumento5 páginasClasificación de Los AlimentosKaren Siñani QuelaliAún no hay calificaciones
- Practica de PythonDocumento6 páginasPractica de PythonKaren Siñani QuelaliAún no hay calificaciones
- Elaboracion de Mermelada de PinaDocumento7 páginasElaboracion de Mermelada de PinaKaren Siñani QuelaliAún no hay calificaciones
- Practica 0Documento1 páginaPractica 0Karen Siñani QuelaliAún no hay calificaciones
- Elaboracion de MermeladaDocumento3 páginasElaboracion de MermeladaKaren Siñani QuelaliAún no hay calificaciones
- Producto de Escalar VectoresDocumento116 páginasProducto de Escalar VectoresKaren Siñani QuelaliAún no hay calificaciones
- Practica #5Documento7 páginasPractica #5Karen Siñani QuelaliAún no hay calificaciones
- ACTIVIDAD 6 ContinuacionDocumento12 páginasACTIVIDAD 6 ContinuacionKaren Siñani QuelaliAún no hay calificaciones
- Hielo InstantaneoDocumento2 páginasHielo InstantaneoKaren Siñani QuelaliAún no hay calificaciones
- Formulas de TriangulosDocumento39 páginasFormulas de TriangulosKaren Siñani QuelaliAún no hay calificaciones
- Formulas de CalculoDocumento249 páginasFormulas de CalculoKaren Siñani QuelaliAún no hay calificaciones
- Ecuaciones Del Movimiento ParabólicoDocumento1 páginaEcuaciones Del Movimiento ParabólicoKaren Siñani QuelaliAún no hay calificaciones
- Arreglos UnidimensionalesDocumento2 páginasArreglos UnidimensionalesKaren Siñani QuelaliAún no hay calificaciones
- IntroducciónDocumento2 páginasIntroducciónKaren Siñani QuelaliAún no hay calificaciones
- El CreacionismoDocumento9 páginasEl CreacionismoKaren Siñani QuelaliAún no hay calificaciones
- Evaporación de Un LíquidoDocumento2 páginasEvaporación de Un LíquidoarturoAún no hay calificaciones
- Manual 02 Operaciones UnitariasDocumento124 páginasManual 02 Operaciones UnitariasThaliz Rguez LautnerAún no hay calificaciones
- Termodinamica: Universidad de Las Fuerzas Armadas Espe Sede-LatacungaDocumento23 páginasTermodinamica: Universidad de Las Fuerzas Armadas Espe Sede-LatacungaJOB NICOLAS QUISHPE URRUTIAAún no hay calificaciones
- PRACTICA PARALELO Quimica ReformazamientoDocumento13 páginasPRACTICA PARALELO Quimica ReformazamientoagramontetrujilloAún no hay calificaciones
- Gases 1Documento13 páginasGases 1Daniel SaavedraAún no hay calificaciones
- Quimica General GasesDocumento20 páginasQuimica General GasesFederico David FloresAún no hay calificaciones
- Modelos de Primer Parcial de Química Del CBCDocumento19 páginasModelos de Primer Parcial de Química Del CBCclasesdequimicaAún no hay calificaciones
- Equilibrio Químico Es La Denominación Que Se Hace A Cualquier Reacción Reversible Cuando Se Observa Que Las Cantidades Relativas de Dos o Más Sustancias Permanecen ConstantesDocumento8 páginasEquilibrio Químico Es La Denominación Que Se Hace A Cualquier Reacción Reversible Cuando Se Observa Que Las Cantidades Relativas de Dos o Más Sustancias Permanecen ConstantesZHARICK MIRANDAAún no hay calificaciones
- Conceptos de Propiedades de GasesDocumento7 páginasConceptos de Propiedades de GasesYariela CedeñoAún no hay calificaciones
- Informe Determinacion de Bicarbonato en Alka-SelterDocumento5 páginasInforme Determinacion de Bicarbonato en Alka-SelterWilssonRamirez100% (1)
- Estado Gaseoso - Estequiometría - Problemas ResueltosDocumento25 páginasEstado Gaseoso - Estequiometría - Problemas ResueltosCane AbacaAún no hay calificaciones
- Leyes de Gases - Grupo 10Documento15 páginasLeyes de Gases - Grupo 10Michi CarpioAún no hay calificaciones
- Conceptos Básicos de DestilaciónDocumento20 páginasConceptos Básicos de DestilaciónvCPAún no hay calificaciones
- Seminario RespiratorioDocumento12 páginasSeminario RespiratorioDanae UrrutiaAún no hay calificaciones
- 1 Torres de Absorción, Importancia y Funcionamiento PDFDocumento46 páginas1 Torres de Absorción, Importancia y Funcionamiento PDFAle Toribio Gonzalez100% (1)
- Cuestionario de Fisica BásicoDocumento7 páginasCuestionario de Fisica BásicoAmaru Castro ParedesAún no hay calificaciones
- Informe Practica 2. Ley de Las Presiones Parciales David Barrios 29874777Documento2 páginasInforme Practica 2. Ley de Las Presiones Parciales David Barrios 29874777David JoseAún no hay calificaciones
- Tp2-Gases TT 2012Documento2 páginasTp2-Gases TT 2012Erica Correa100% (1)
- Disoluciones Clausius ClapeyronDocumento30 páginasDisoluciones Clausius ClapeyronArdila Alber80% (5)
- Casosde EstudioDocumento18 páginasCasosde EstudioGabriel AndrésAún no hay calificaciones
- Ley de DaltonDocumento2 páginasLey de DaltonPauly MuñozAún no hay calificaciones
- Presiones Parciales Alveolares de Oxígeno y de Dióxido de CarbonoDocumento2 páginasPresiones Parciales Alveolares de Oxígeno y de Dióxido de CarbonoEliana CadenaAún no hay calificaciones
- GasesDocumento33 páginasGasesDisofi ContrerasAún no hay calificaciones
- Informe de Laboratorio de Fisica DestilacionDocumento8 páginasInforme de Laboratorio de Fisica DestilacionMichael PachecoAún no hay calificaciones
- Determinación de La Densidad de Un GasDocumento8 páginasDeterminación de La Densidad de Un Gaswero221188Aún no hay calificaciones
- HematosisDocumento25 páginasHematosismanuelvaeAún no hay calificaciones
- Oxígeno HiperbáricoDocumento9 páginasOxígeno HiperbáricoDidi GAún no hay calificaciones
- Gases IdealesDocumento1 páginaGases IdealesGUIZAR PEREDIA DELIA LIZETTEAún no hay calificaciones
- Lucero Rodriguez Cruz Casos de Estudio Primera Fase - Lucero Rodriguez Cruz 23503 2091254651Documento25 páginasLucero Rodriguez Cruz Casos de Estudio Primera Fase - Lucero Rodriguez Cruz 23503 2091254651Solansh Arlet Ledezma PazAún no hay calificaciones
- Cuadernillo de MetodologiaDocumento61 páginasCuadernillo de MetodologiaCarina KriedelAún no hay calificaciones