Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Informe 1 Quimica 1 Fiqt Uni
Cargado por
Deysi RocaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Informe 1 Quimica 1 Fiqt Uni
Cargado por
Deysi RocaCopyright:
Formatos disponibles
INDICE:
1.- Fundamento teorico
1. FUNDAMENTO TEÓRICO:
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 1
El conocimiento de los materiales de laboratorio tiene como finalidad la correcta manipulación
de los mismos a la hora de realizar el experimento y así poder lograr una buena exactitud a la
hora de hacer los cálculos.
Instrumentos de medición:
I. TEMPERATURA
TERMÓMETRO DE Hg:
Es empleado para la medición de la temperatura con escalas en grados centígrados y
Fahrenheit.
Funciona por la dilatación del mercurio que es observado por medio de un capilar.
La variación del volumen del mercurio obedece la siguiente ecuación:
V = Vo (1+ α ∆t)
II. VOLUMEN
PROBETA:
Tubo de cristal o plástico alargado y graduado, cerrado por un extremo, usado como
recipiente de líquidos o gases, generalmente mide volúmenes de 25 o 50 mL.
VASO DE PRECIPITADO:
De forma cilíndrica, se encuentra en varias capacidades, se encuentran graduados. Son
de vidrio (pyrex) o plástico. Su objetivo principal es contener líquidos o sustancias
químicas de distinto tipo, normalmente es usado para transportar líquidos.
BURETA:
Se utiliza para emitir cantidades variables de líquido con gran exactitud y precisión.
Tubo graduado de gran extensión, está provista de una llave o adaptadas con una pinza
de Thor, que permite verter líquidos gota a gota
PIPETA:
Tuvo alargado que permite la transferencia de un volumen generalmente no mayor a 20
mL de un recipiente a otro de forma exacta, este medir proporciones de líquido con
bastante precisión, generalmente de vidrio y posee graduación.
Otros Instrumentos:
EMBUDO:
Es una pieza de vidrio o plástico que se utiliza para el trasvasijado de productos
químicos desde un recipiente a otro, también es usado para realizar fitraciones.
PROPIPETA:
Utensilio de goma, creada especialmente para asegurar la transferencia de líquidos de
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 2
topo tipo especialmente los que poseen propiedades específicas (infecciosos, corrosivos,
tóxicos, radiactivos o estériles).
SOPORTE UNIVERSAL:
Herramienta que se utiliza en el laboratorio para realizar montajes con los materiales
presentes en el laboratorio. Conformado por una base, el cual soporta una varilla que
permite sujetar materiales con ayuda de una pinza.
TUBOS DE ENSAYO:
Tubo de vidrio que resiste temperaturas muy altas, se utiliza para contener pequeñas
muestras de líquido.
PICETA:
Recipiente cerrado con una tapa de rosa, el cual posee un pequeño tubo con una gran
abertura capaz de entregar el líquido depositado (generalmente agua destilada o agua
desionizada). Su función principal es el lavado de recipientes y materiales de vidrio.
MECHERO DE BUNSEN:
Es un instrumento que proporciona energía en forma de calor para acelerar los procesos
de las reacciones químicas que se están llevando a cabo.
PARTES DEL MECHERO DE BUNSEN:
Vástago
Collarín
Entrada del aire
Llave de la entrada
de gas
1. OBJETIVOS GENERALES:
Familiarizarnos con los instrumentos de laboratorio.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 3
Tratar de medir correctamente las dimensiones con sus respectivas incertidumbres de
los materiales de laboratorio.
El uso responsable de los instrumentos dados por los docentes para llegar a nuestro
objetivo con éxito.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 4
2-. PARTE EXPERIMENTAL:
EXPERIMENTO N° 1
MEDICIÓN DE LA TEMPERATURA
OBJETIVO ESPECÍFICO:
Determinar la exactitud de la graduación del termómetro de Mercurio.
El uso correcto de la manera de medir la temperatura con el termómetro de Mercurio (Hg).
Determinar la temperatura del agua con el termómetro de Hg.
OBSERVACIONES:
Se observó como el termómetro de Mercurio era muy sensible a cambio de temperatura al
colocarlo del agua al ambiente
DIAGRAMA DEL PROCESO:
1. Llenamos el vaso precipitado con agua.
2. Introducimos el termómetro cuidadosamente.
3. Agitar con el termómetro el agua.
4. Mantener el termómetro a la mitad del vaso.
5. Con el termómetro aún en el vaso, observamos la
medición dada por el termómetro.
CONCLUSIONES
Luego de esta experiencia, pudimos notar que el Mercurio es un metal que se dilata con
facilidad pon ende es muy sensible a la temperatura ambiente.
RECOMENDACIONES
Tener mucho cuidado al medir temperaturas altas ya que al pasar de 100°C se puede quebrar
y derramar el Mercurio (Hg) y contaminar a aquellos que se encuentran alrededor de él.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 5
EXPERIMENTO N°2
MEDICIÓN DEL VOLUMEN
OBJETIVO ESPECÍFICO
Determinar de manera exacta el volumen de agua o líquido.
OBSERVACIONES
1. Se observa que se utiliza junto con la bombilla de succión luego al presionar la letra S el
líquido comienza a ascender en la pipeta de mohr.
2. Para medir el volumen se sube levemente la pipeta hasta que la vista esté en forma
tangente a la parte cóncava del agua o líquido.
DIAGRAMA DE PROCESOS
1. Colocar la propipeta en la pipeta para poder iniciar
2. Para succionar el líquido del vaso precipitado, presionar el
botón S (Succión) de la propipeta.
3. Una vez que tengamos la cantidad a medias, apretar el
botón E (Eyección) de la propipeta para llegar al volumen
deseado.
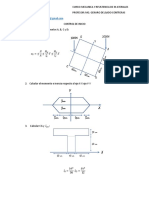
Mínima Volumen
Instrumento T(ºC) Tolerancia Incertidumbre
División dispensado (mL)
a. Probeta 0.5 25 - ±0.25 15±0.25
b. Pipeta de Mohr 0.1 20 - ±0.05 10±0.05
c. Bureta 0.1 20 - ±0.05 -
CÁLCULOS
CONCLUSIÓN
Se concluye del experimento que la bureta es más exacta que la pipeta ya que la bureta se
maneja con una llave y es más fácil regular.
RECOMENDACIONES
Al introducir la bombilla de succión en la pipeta debe hacerse con mucho cuidado ya que si
se le aplica con mucha fuerza se puede dañar la pipeta.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 6
EXPERIMENTO N° 3
DETERMINACIÓN DEL VOLUMEN DE LOS TUBOS DE ENSAYO
OBJETIVO ESPECÍFICO:
Determinar la capacidad de cada tubo de ensayo mediante el uso de la bureta y cierta
cantidad de agua.
OBSERVACIONES:
El volumen del agua expulsada e indicada por la probeta, es el volumen de cada tubo de
ensayo.
DIAGRAMA DEL PROCESO:
1. Colocar la bureta con ayuda de la pinza a una
altura adecuada en el soporte universal.
2. Llenamos la bureta 25 mL de agua y colocar
debajo un tubo de ensayo.
3. Abrir la bureta con cuidado y dejar salir el
agua hacia el tubo de ensayo, llenándolo al
ras.
4. Calcular el volumen del tubo de ensayo.
CÁLCULOS:
Tubo de Ensayo Dimensiones en mm Volumen total en mL
Pequeño 12 x 98.8 9.7 ± 0.05
Mediano 16 x 150 20.9 ± 0.05
Grande 17x150 27.7 ± 0.05
CONCLUSIÓN:
Con esta experiencia, podemos decir que la bureta es un instrumento más exacto en cuanto a
volumen respecta, aunque sea la mínima gota, la bureta es capaz de reconocer la pérdida del
volumen de esta.
RECOMENDACIONES:
Al momento de manipular la bureta, tener en cuenta si la llave de esta no esté floja pues el
líquido puede escaparse.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 7
EXPERIMENTO N° 4
DETERMINACIÓN DEL CAUDAL
OBJETIVO ESPECÍFICO:
Determinar la rapidez con la que la bureta expulsa el agua.
OBSERVACIONES:
No podemos encontrar una rapidez exacta en tres intentos, tomando tiempo con el
cronómetro se diferencian al menos por una milésima.
DIAGRAMA DEL PROCESO:
1. Colocar la bureta con ayuda de la pinza a una altura adecuada en el
soporte universal.
2. Llenamos la bureta 25 mL de agua y colocar el vaso precipitado.
3. Abrir la bureta y al instante iniciar el cronómetro.
4. Esperar que se vacíe la bureta y en el instante que ya esté vacía
pausar el cronómetro.
CÁLCULOS:
Volumen (mL) Tiempo (s) Caudal (mL/s)
25 09.43 2.6511
25 09.49 2.6343
25 09.45 2.6455
Caudal promedio: 2.6533 mL/s
CONCLUSIÓN:
Con esto pudimos calcular la velocidad promedio de la expulsión del agua de la bureta
cuando la llave está perpendicular.
RECOMENDACIONES:
Al momento de abrir la llave, hacerlo con cuidado pues el instrumento es muy delicado y un
movimiento brusco puede ocasionar que este se quiebre.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 8
EXPERIMENTO Nº5
DETERMINACIÓN DEL ERROR EN LA MEDICIÓN DEL VOLUMEN CON
EL VASO PRECIPITADO Y CON LA PROBETA
OBJETIVO ESPECÍFICO:
1. Relacionar los principales métodos de medición y sus respectivas unidades de medida
2. Medir la masa y sus respectivas incertidumbres de la probeta vacía, con agua y la masa
del vaso de precipitado vacía, con agua
3. Calcular las densidades respectivas
OBSERVACIONES:
1. Los materiales con los que se trabaja son de diferentes medidas cada una tiene su
medición y error
2. la balanza granataria es importante, mide masas de 2 a 2.5kg ideales para los materiales
a medir
DIAGRAMA DE PROCESOS:
1. Medimos el peso de la probeta vacía en su interior en la balanza granataria
2. Medimos el peso de la probeta con agua con un volumen de 10ml en su interior.
3. Medimos la masa del vaso de precipitado vacío en su interior en la balanza granataria.
4. Medimos la masa del vaso de precipitado con agua con un volumen de 10ml en su
interior en la balanza granataria.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 9
CÁLCULOS:
Vaso Precipitado Probeta
Volumen de agua a dispensar (mL) 10 mL 15 mL
Vaso Vaso con agua Probeta Probeta con agua
Masa (g)
100,5±0.05 177.8±0.05 14.8±0.05 24.4±0.05
Masa de agua (g) 17.75±0.15 0.6±0.1
Densidad real del agua (g/mL) 0.99868 0.99868
Volumen real del agua (mL) 17.8223 10.4333
Error (%) -43.890 -4,1530
CONCLUSIONES:
Las medidas hechas poseen ciertas incertidumbres pues cualquier medida que se haga nunca
es exacta
RECOMENDACIONES:
1. Tratar de calibrar bien la balanza.
2. Medir bien los volúmenes a medir del liquido.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 10
EXPERIMENTO N° 6
MECHERO DE BUNSEN Y EL ESTUDIO DE LAS LLAMAS
OBJETIVO ESPECÍFICO:
1. Aprender el funcionamiento del mechero y lograr un correcto uso para producir una
mejor eficiencia de la energía calorífica.
2. Identificar los productos de las reacciones químicas que ocurren durante la combustión
completa e incompleta
3. Identificar los tipos de llamas en ambas combustiones.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 11
OBSERVACIONES:
Al cerrar la entrada de aire del
mechero, se produce una llama muy
luminosa.
Al dejar la entrada de aire abierta del
mechero, se produce una llama no
luminosa de color azul pálido.
Al acercar una loseta a la llama muy
luminosa se observa un deposito solido
(hollín) producido por el carbono
Al acercar una loseta a la llama no
luminosa se observa que no queda
ningún residuo sólido en ella.
Al colocar una cartulina en una
posición vertical sobre la boca del
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 12
vástago con una llama no luminosa se
observa una silueta de la llama con una
división.
Al colocar una cartulina en una
posición horizontal sobre la boca del
vástago con una llama no luminosa se
observa la silueta de esta en forma de
un anillo.
Al introducir un cerillo, con la ayuda
de un alfiler, en la boca del vástago
con una llama no luminosa se observa
que el cerillo no se enciende.
ECUACIONES QUÍMICAS:
TIPOS DE COMBUSTIÓN:
1. Combustión Completa:
Ocurre cuando la combustión contiene la suficiente cantidad de oxígeno (O 2).
En esta combustión se obtienen como producto dióxido de carbono (CO2) y
agua gaseosa (H2O) además de una llama no luminosa de color azul pálido.
Se puede representar mediante la siguiente reacción química:
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g) + calor
2. Combustión Incompleta:
Ocurre cuando en la combustión existe una deficiencia de oxigeno (O 2).
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 13
En esta combustión se obtienen como producto, además de dióxido de carbono
(CO2) e agua gaseosa (H2O), carbono (C) y monóxido de carbono (CO).
Esta combustión genera una llama muy luminosa.
Se puede representar mediante la siguiente reacción química:
C3H8(g) + 3O2(g) C(s) + 2CO(g) + 4H2O(g) + calor
DIAGRAMAS:
Fig. N°1: Escala de la intensidad del calor en la llama no luminosa
1: Cono frio, no llega
el oxígeno.
2: Cono de reducción,
poco oxígeno.
3: Cono de oxidación,
abundancia de
oxígeno.
4: Zona de fusión,
alcanza los 1500°C
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 14
CONCLUSIONES:
1. Sobre las huellas que deja la llama en la cartulina se puede concluir que esta consta de
tres zonas, en donde la primera de ellas es la zona fría; ya que no existe combustión.
Con esto podemos demostrar el hecho de que el cerillo al ser introducido en la boca del
vástago no se enciende.
2. La llama no luminosa tiene la mayor intensidad calorífica en la zona del cono externo.
3. La llama no luminosa es más eficiente ya que produce mayor cantidad de energía a
comparación de la llama muy luminosa.
RECOMENDACIONES:
1. Para encender el mechero bunsen primero es preferible prender el fosforo y luego abrir
la llave del gas, ya que, una de las propiedades del gas es que se expande en todo el
ambiente pudiendo provocas daños graves dentro del laboratorio.
2. Evitar usar cabello suelto cerca del mechero ya que, por ser inflamable, puede quemarse
produciendo graves daños físicos.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 15
CUESTIONARIO N°1
1. Indique siete normas de seguridad en el laboratorio de Química y cinco
pictogramas con su explicación respectiva.
NORMAS DE SEGURIDAD DEL LABORATORIO:
a) Está prohibido fumar dentro del laboratorio ya que es un lugar
cerrado
b) Debe mantener el área de trabajo limpio y ordenado para evitar cualquier tipo de
accidentes y una mayor eficiencia en el trabajo que se está realizando.
c) Se debe tomar suma importancia a las etiquetas de productos desconocidos,
puesto que podría ser un producto altamente nocivo para la salud.
d) Se debe usar una bata antes de ingresar al laboratorio y verificar que esta esté
bien colocada.
e) Usar el cabello sujetado para evitar
accidentes físicos.
f) Antes de usar los instrumentos es necesario verificar su buen
estado.
g) Conocer las salidas de emergencia y la ubicación de las llaves generales de gas y de los
primeros auxilios.
PICTOGRAMAS:
C¬Corrosivo:
Clasificación:
Destrucción de la piel debido al contacto
directo
Precauciones:
Evitar el contacto directo con los ojos, no
inhalar los vapores producidos por esta
sustancia
T¬Toxico:
Clasificación:
La inhalación o ingestión puede provocar
daños graves para la salud.
Precauciones:
Evitar el contacto directo con cualquiera de
estas sustancia, en presencia de algún
malestar acudir inmediatamente al médico.
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 16
O¬Comburente:
Clasificación:
Sustancias que cuando tienen contacto con
otras sustancias inflamables producen una
reacción altamente exotérmica.
Precauciones:
Evitar el contacto con combustibles y tener un
correcto aislamiento de la sustancia.
N¬Peligroso para el medio ambiente:
Clasificación:
En el caso de ser liberado al medio ambiente
puede producir daños inmediatos o a largo
plazo.
Precauciones:
Observar las indicaciones de eliminación y
evitar la canalización en el suelo o medio
ambiente
E¬Explosivo:
Clasificación:
Sustancias que reaccionan exotérmicamente.
Precauciones:
Evitar el choque, fricción o ruptura de estos
productos
2.- ¿Cuál es el resultado de las operaciones siguientes, indicando la
incertidumbre absoluta y relativa?
5,34 ± 0,05 + 5,34 ± 0,03 – 3,78 ± 0,04
SOLUCION:
1 Medida:
T = 5,34 + 5,34 – 3,78 = 6,90
2 Incertidumbre:
2.1 Incertidumbre absoluta:
∆T = ∆(5,34) + ∆(5,34) + ∆(3,78)
∆T = 0,05 + 0,03 + 0,04
∆T = 0,12
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 17
2.2 Incertidumbre relativa
∆T
Incertidumbre relativa de T =
T
0.12
∆R(T) = = 0.017.39….. = 0.02
6.90
3.- Indique la formula y nombre de 5 productos controlados por la SUNAT.
Productos controlados pon la SUNAT.
PRODUCTO FORMULA FORMULA TOPOLOGICA
QUIMICO QUIMICA
CONTROLADO
Acetato de etilo CH3COOCH2CH3
(CH3)2CO
Acetona
Ácido antranilico (NH2)C6H4(COOH)
Ácido clorhídrico HCl
Ácido nítrico HNO3
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 18
3. REFERENCIAS BIBLIOGRÁFICAS:
Pérez y Juárez Arturo –(1972) Química al Día. Edición. Págs. 17-19
Daniel C Harris – Análisis Químico Cuantitativo. (2da Edición)
b. Fuentes electrónicas:
Tapia, C; Vega, C; Rojas, C (2015) IMPLEMENTACIÓN DEL LABORATORIO
CLÍNICO MODERNO. Recuperado de
http://www.sciencedirect.com/science/article/pii/S0716864015001558
http://orientacion.sunat.gob.pe/index.php/empresas-menu/insumos-
quimicos
APRESTAMIENTO PARA EL TRABAJO EN EL
LABORATORIO 19
También podría gustarte
- Informe 1 Química 1 Fiqt UniDocumento19 páginasInforme 1 Química 1 Fiqt UniJazmin GutierrezAún no hay calificaciones
- INFORME#1Documento11 páginasINFORME#1Eneine Barrera RAún no hay calificaciones
- Informe de Laboratorio - Docx 1 Punto de EbullicionDocumento6 páginasInforme de Laboratorio - Docx 1 Punto de EbullicionEdna Valentina Carranza ColoradoAún no hay calificaciones
- Reporte Práctica 1 Uso Del Material y Equipo de LaboratorioDocumento5 páginasReporte Práctica 1 Uso Del Material y Equipo de LaboratorioEva CruzAún no hay calificaciones
- Guia de Practica 3 Reconocimiento Materiales LaboratorioDocumento20 páginasGuia de Practica 3 Reconocimiento Materiales LaboratorioBrigith MayoAún no hay calificaciones
- Practico 01 - Instrumentos de LaboratorioDocumento33 páginasPractico 01 - Instrumentos de LaboratorioPatoCuak45Aún no hay calificaciones
- Conociendo el material de laboratorioDocumento19 páginasConociendo el material de laboratorioChelsea Mitch Diaz50% (2)
- Práctico de Laboratorio de Ingeniería QuímicaDocumento13 páginasPráctico de Laboratorio de Ingeniería QuímicaOrlando VegaAún no hay calificaciones
- Primer Informe de Quimica LaboratorioDocumento13 páginasPrimer Informe de Quimica LaboratorioMary Cielo CalderonAún no hay calificaciones
- Reconocimiento de materiales de laboratorio esencialesDocumento8 páginasReconocimiento de materiales de laboratorio esencialesSebastian AlejandroAún no hay calificaciones
- Guia de Quimica 2.0Documento9 páginasGuia de Quimica 2.0Daniel Valle PayneAún no hay calificaciones
- Práctica 2, Laboratorio Química GeneralDocumento12 páginasPráctica 2, Laboratorio Química GeneralAllan DuranAún no hay calificaciones
- Labortorio N°2Documento3 páginasLabortorio N°2Luis Alejandro Pico BurgosAún no hay calificaciones
- Aprestamiento laboratorio químicaDocumento28 páginasAprestamiento laboratorio químicasamuel reynero fernandez velaAún no hay calificaciones
- Trabajo Química AplicadaDocumento6 páginasTrabajo Química AplicadaGiancarlo Mendoza IbarraAún no hay calificaciones
- Instrumentos Más Usados en El Laboratorio de QuímicaDocumento37 páginasInstrumentos Más Usados en El Laboratorio de QuímicaLoida CáceresAún no hay calificaciones
- Informe P1Documento10 páginasInforme P1Andre PerezYTAún no hay calificaciones
- Presentación - Laboratorio DQUI 1034Documento31 páginasPresentación - Laboratorio DQUI 1034gustavo vargas diazAún no hay calificaciones
- Reporte MaterialesDocumento14 páginasReporte MaterialesGuadalupe del CAún no hay calificaciones
- Reporte #3Documento4 páginasReporte #3Bruno CovaAún no hay calificaciones
- Practica 1 Bioquimica de AlimentosDocumento14 páginasPractica 1 Bioquimica de AlimentosEstefania Parra UribeAún no hay calificaciones
- Práctica de Laboratorio No. 1Documento17 páginasPráctica de Laboratorio No. 1osman altamarAún no hay calificaciones
- Practica #1 Conocimiento Del Material y Operaciones Básicas de LaboratorioDocumento9 páginasPractica #1 Conocimiento Del Material y Operaciones Básicas de LaboratorioJuan David López QuinteroAún no hay calificaciones
- Práctica I. BioquímicaDocumento19 páginasPráctica I. BioquímicaItzel FigueroaAún no hay calificaciones
- lab.fisicoquimicvaDocumento12 páginaslab.fisicoquimicvaAyde muñoz ArispeAún no hay calificaciones
- Practica de LaboratorioDocumento8 páginasPractica de LaboratorioJuliana ZerpaAún no hay calificaciones
- MATERIAL DIDACTICO LABORATORIO. No 1Documento17 páginasMATERIAL DIDACTICO LABORATORIO. No 1Cristian OjedaAún no hay calificaciones
- Cuestionario FisicoquimicaDocumento5 páginasCuestionario FisicoquimicaClaudia Montoya SalazarAún no hay calificaciones
- UTP Laboratorio 1 Identificación HerramientasDocumento16 páginasUTP Laboratorio 1 Identificación HerramientasAlexander AlvaradoAún no hay calificaciones
- Informe 2 TermiDocumento16 páginasInforme 2 TermiBayron buenoAún no hay calificaciones
- Reporte Materiales de LaboratorioDocumento13 páginasReporte Materiales de LaboratorioGuadalupe del CAún no hay calificaciones
- GUÍA DE LABORATORIO Nº 1Documento14 páginasGUÍA DE LABORATORIO Nº 1Samuel Rojas AraujoAún no hay calificaciones
- Cuadernillo de Practicas Quimica IDocumento49 páginasCuadernillo de Practicas Quimica IMarai GarciaAún no hay calificaciones
- Laboratorio de Quimica 1.Documento6 páginasLaboratorio de Quimica 1.Edu MolinaAún no hay calificaciones
- Informe 6, Propiedades FisicasDocumento8 páginasInforme 6, Propiedades FisicasISABELA SIACHOQUE TORRESAún no hay calificaciones
- Presentación de Materiales de Laboratorio de Química OrganicaDocumento18 páginasPresentación de Materiales de Laboratorio de Química OrganicaAren HaddockAún no hay calificaciones
- Tornillo MicrometricoDocumento13 páginasTornillo MicrometricoMaicol YusedAún no hay calificaciones
- Materiales de Laboratorio y Normas de SeguridadDocumento16 páginasMateriales de Laboratorio y Normas de SeguridadAbel ArauzAún no hay calificaciones
- Material de LaboratorioDocumento18 páginasMaterial de LaboratorioMonica VanegasAún no hay calificaciones
- Intrumentos de LavoratorioDocumento3 páginasIntrumentos de LavoratorioYefri ReyesAún no hay calificaciones
- Guia de Laboratorio Q.organica I Impresion-13-22Documento10 páginasGuia de Laboratorio Q.organica I Impresion-13-22p75009033Aún no hay calificaciones
- Practica Nº1 Mediciones y Densidad (1.1)Documento6 páginasPractica Nº1 Mediciones y Densidad (1.1)raul rocha mejiaAún no hay calificaciones
- Practica 3Documento9 páginasPractica 3Gunnar DieGo0% (1)
- Práctica de Introducción Al Laboratorio de Bioquímica.Documento8 páginasPráctica de Introducción Al Laboratorio de Bioquímica.Dayana Guadalupe Medina MendozaAún no hay calificaciones
- Cuestionario BioquimicaDocumento6 páginasCuestionario BioquimicaGustavo AdolfoAún no hay calificaciones
- Temperatura crítica fenol-aguaDocumento10 páginasTemperatura crítica fenol-aguaAdrian Joseph Luzuriaga ChumbesAún no hay calificaciones
- Materiales de laboratorio y su clasificaciónDocumento18 páginasMateriales de laboratorio y su clasificaciónCarla Varinia GallardoAún no hay calificaciones
- Identificacion de Materiales de LaboratorioDocumento8 páginasIdentificacion de Materiales de LaboratorioArnulfo Rodriguez Paco100% (3)
- Reporte de Laboratorio 2Documento17 páginasReporte de Laboratorio 2Daniel CutimboAún no hay calificaciones
- Instrumentacion de LaboratorioDocumento6 páginasInstrumentacion de LaboratorioDRGM COPIADOAún no hay calificaciones
- Pre informe PrácticaDocumento8 páginasPre informe PrácticaHugo EspinosaAún no hay calificaciones
- Laboratorio 1 Fisica 2 Instrumentos, Máquinas y Elementos de Uso en El LaboratorioDocumento24 páginasLaboratorio 1 Fisica 2 Instrumentos, Máquinas y Elementos de Uso en El LaboratorioSchirmEdassAún no hay calificaciones
- Trabajo de Lab Oratorio Quimica 1Documento22 páginasTrabajo de Lab Oratorio Quimica 1DeibyAguilar0% (2)
- Practica 1_Manejo Equipo de Laboratorio. Determinacion de masas y volumenesDocumento7 páginasPractica 1_Manejo Equipo de Laboratorio. Determinacion de masas y volumenesmarina Alvarez RestrepoAún no hay calificaciones
- Informe Laboratorio Quimica General 17 - 03-2013Documento24 páginasInforme Laboratorio Quimica General 17 - 03-2013Miguel BermudezAún no hay calificaciones
- Conocimiento de Instrumentos de LaboratorioDocumento12 páginasConocimiento de Instrumentos de LaboratorioLily BarreraAún no hay calificaciones
- Cartilla de Evaluacion Implementos de LaboratorioDocumento30 páginasCartilla de Evaluacion Implementos de LaboratorioKeimirAsprillaMenaAún no hay calificaciones
- Equilibrios de Fases y Transiciones de Fases: Parte IDe EverandEquilibrios de Fases y Transiciones de Fases: Parte IAún no hay calificaciones
- UF0045 - Procesos de limpieza y puesta a punto de habitaciones y zonas comunes en alojamientosDe EverandUF0045 - Procesos de limpieza y puesta a punto de habitaciones y zonas comunes en alojamientosAún no hay calificaciones
- Microbiología médica II: esterilización, diagnóstico de laboratorio y respuesta inmuneDe EverandMicrobiología médica II: esterilización, diagnóstico de laboratorio y respuesta inmuneAún no hay calificaciones
- PC2 CostosDocumento1 páginaPC2 CostosDeysi RocaAún no hay calificaciones
- 5ta PCDocumento6 páginas5ta PCDeysi RocaAún no hay calificaciones
- PC2 CostosDocumento1 páginaPC2 CostosDeysi RocaAún no hay calificaciones
- Examen Final - Pi140 Ab-2020 2Documento2 páginasExamen Final - Pi140 Ab-2020 2Deysi RocaAún no hay calificaciones
- DEMOSTRACIÓN 3ertbDocumento4 páginasDEMOSTRACIÓN 3ertbDeysi RocaAún no hay calificaciones
- Roca ExaFinal PI 318 B 20202Documento6 páginasRoca ExaFinal PI 318 B 20202Deysi RocaAún no hay calificaciones
- Clase 10 22-06-21I Tratamientos TérmicosDocumento30 páginasClase 10 22-06-21I Tratamientos TérmicosDeysi RocaAún no hay calificaciones
- PC 2 - COSTOS Y PRESUPUESTOSDocumento1 páginaPC 2 - COSTOS Y PRESUPUESTOSDeysi RocaAún no hay calificaciones
- TALLERDocumento10 páginasTALLERDeysi RocaAún no hay calificaciones
- Clase 8 15-06-21I Diagrama de Fe-CDocumento20 páginasClase 8 15-06-21I Diagrama de Fe-CDeysi RocaAún no hay calificaciones
- Examen Final PI-142B - 2020-2Documento2 páginasExamen Final PI-142B - 2020-2Deysi RocaAún no hay calificaciones
- Control de InicioDocumento4 páginasControl de InicioDeysi RocaAún no hay calificaciones
- Practica Calificada No 5 - PI-524B - 2020-1Documento2 páginasPractica Calificada No 5 - PI-524B - 2020-1victorAún no hay calificaciones
- Clase 9 08-11-112 Propiedades Mecánicas 2Documento53 páginasClase 9 08-11-112 Propiedades Mecánicas 2Omar MuñozAún no hay calificaciones
- 3era PC Métodos Roca GutierrezDocumento3 páginas3era PC Métodos Roca GutierrezDeysi RocaAún no hay calificaciones
- Uni 23 DicDocumento2 páginasUni 23 DicDeysi RocaAún no hay calificaciones
- Combustion Calderos2021Documento62 páginasCombustion Calderos2021Deysi RocaAún no hay calificaciones
- Control Lectura 1Documento1 páginaControl Lectura 1Deysi RocaAún no hay calificaciones
- Expo MañanaDocumento2 páginasExpo MañanaDeysi RocaAún no hay calificaciones
- Ipq Grupo 3 PDFDocumento30 páginasIpq Grupo 3 PDFDeysi RocaAún no hay calificaciones
- Practica 02 Guia Lipidos Pi 721Documento6 páginasPractica 02 Guia Lipidos Pi 721Deysi RocaAún no hay calificaciones
- Informe 1 - Grupo 13 Analisis de CarbohidratosDocumento13 páginasInforme 1 - Grupo 13 Analisis de CarbohidratosDeysi Roca100% (1)
- PI-524B - 4pc 20-1 PDFDocumento3 páginasPI-524B - 4pc 20-1 PDFDeysi RocaAún no hay calificaciones
- Roca Gutierrez PC Resistencia de MaterialesDocumento8 páginasRoca Gutierrez PC Resistencia de MaterialesDeysi RocaAún no hay calificaciones
- Formato - EvaluacionDocumento1 páginaFormato - EvaluacionDeysi RocaAún no hay calificaciones
- Laboratorio de Lipidos - 2020-2Documento13 páginasLaboratorio de Lipidos - 2020-2Deysi RocaAún no hay calificaciones
- Control 20 - 1Documento1 páginaControl 20 - 1Deysi RocaAún no hay calificaciones
- Estructura Atómica y Prop MagneticasDocumento29 páginasEstructura Atómica y Prop MagneticasDeysi RocaAún no hay calificaciones
- Informe 1 - Grupo 13 Analisis de CarbohidratosDocumento13 páginasInforme 1 - Grupo 13 Analisis de CarbohidratosDeysi Roca100% (1)
- l03 InformeDocumento13 páginasl03 InformeDeysi RocaAún no hay calificaciones
- De Diagnostico: Tabla para ElDocumento2 páginasDe Diagnostico: Tabla para Elfrancisco cortes medinaAún no hay calificaciones
- Motor síncrono: introducción, funcionamiento y característicasDocumento4 páginasMotor síncrono: introducción, funcionamiento y característicasJuanLojaObregonAún no hay calificaciones
- Guia Del DeshidratadorDocumento10 páginasGuia Del DeshidratadorByron Sisa AAún no hay calificaciones
- Evaluación organoléptica de productos farmacéuticosDocumento2 páginasEvaluación organoléptica de productos farmacéuticospool jesus araujo cardoza100% (3)
- Claves descarga FTP programas radiosDocumento3 páginasClaves descarga FTP programas radiosDavid Josué Fernández PascualAún no hay calificaciones
- Ambatillo Alto TripticoDocumento2 páginasAmbatillo Alto TripticoDani VillacrésAún no hay calificaciones
- Universidad Nacional de Ingenieria FrancisDocumento29 páginasUniversidad Nacional de Ingenieria FrancisFrancisco MartinezAún no hay calificaciones
- Diseño de desbaste en plantas de tratamiento de agua: rejas y tamicesDocumento15 páginasDiseño de desbaste en plantas de tratamiento de agua: rejas y tamicesNadia RamosAún no hay calificaciones
- Laboratorio Física - Informe Experiencia 7 y 8Documento16 páginasLaboratorio Física - Informe Experiencia 7 y 8JoseAún no hay calificaciones
- Caso #2 Grana y MonteroDocumento28 páginasCaso #2 Grana y MonteroPaniura VivancoAún no hay calificaciones
- Manual Bomba de Infusion VP3Documento68 páginasManual Bomba de Infusion VP3Melissa AlvarezAún no hay calificaciones
- Abreviacion CañeriaDocumento8 páginasAbreviacion CañeriaGustavo MardonesAún no hay calificaciones
- Tolerancias en El Estudio de Tiempos.Documento2 páginasTolerancias en El Estudio de Tiempos.Joseph LeijaAún no hay calificaciones
- Protección de sistemas de potenciaDocumento24 páginasProtección de sistemas de potenciadiliana sotoAún no hay calificaciones
- Regla de Mezcla y AleaciónDocumento3 páginasRegla de Mezcla y AleaciónFrancisco ContrerasAún no hay calificaciones
- Manual de Señalización VialDocumento9 páginasManual de Señalización VialValeria BohórquezAún no hay calificaciones
- Valores Caracteristicos de Las Ondas SenoidalesDocumento12 páginasValores Caracteristicos de Las Ondas SenoidalesJeanPierSalloAún no hay calificaciones
- TEMA 8. Instalaciones Eléctricas en ViviendasDocumento4 páginasTEMA 8. Instalaciones Eléctricas en ViviendasFrancisco de Paula González RodríguezAún no hay calificaciones
- DISPAV-5-Versión 3.0. Actualización Del SistemaDocumento74 páginasDISPAV-5-Versión 3.0. Actualización Del SistemaLuiSilvestre Vaca OyolaAún no hay calificaciones
- Qué es la potencia eléctricaDocumento5 páginasQué es la potencia eléctricaEdwinAún no hay calificaciones
- Informe de ElectroquimicaDocumento22 páginasInforme de ElectroquimicaMilagros OlazabalAún no hay calificaciones
- Diseño de prácticas de laboratorio para enseñar NOSQLDocumento152 páginasDiseño de prácticas de laboratorio para enseñar NOSQLProfesor ivan ayalaAún no hay calificaciones
- Avance 3. Planteamiento Del Problema, JustificacionDocumento18 páginasAvance 3. Planteamiento Del Problema, JustificacionFreddy Wilmerson CajaAún no hay calificaciones
- PFC - Curso Superior en Dirección de Seguridad PrivadaDocumento27 páginasPFC - Curso Superior en Dirección de Seguridad PrivadaYessica PérezAún no hay calificaciones
- Examen de Conducir A2 y A4Documento19 páginasExamen de Conducir A2 y A4karen zierath100% (2)
- Guia Rapida para Usar ImageJ PDFDocumento19 páginasGuia Rapida para Usar ImageJ PDFSalvador Sanchez RosasAún no hay calificaciones
- Tratamiento Pulpa Guanabana PDFDocumento16 páginasTratamiento Pulpa Guanabana PDFSegundo Teofilo Cadenillas CabanillasAún no hay calificaciones
- Ficheros para El Examen Del DHCP PDFDocumento3 páginasFicheros para El Examen Del DHCP PDFLuis Jimenez PelazAún no hay calificaciones
- Problemas de Termodinámica: Trabajo de Frontera y Análisis de Energía en Sistemas Cerrados.Documento3 páginasProblemas de Termodinámica: Trabajo de Frontera y Análisis de Energía en Sistemas Cerrados.Miguel L. ToledanoAún no hay calificaciones
- Análisis estratégico con la matriz DOFA para la empresa NexusDocumento4 páginasAnálisis estratégico con la matriz DOFA para la empresa NexusWendy CardozoAún no hay calificaciones