Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Laboratorio de Fisica Experimento de Jou
Cargado por
alfredoTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Laboratorio de Fisica Experimento de Jou
Cargado por
alfredoCopyright:
Formatos disponibles
OBJETIVOS:
Determinar el equivalente mecánico del calor, es decir, la relación
entre la unidad de energía joule (julio) y la unidad de calor caloría,
mediante esta experiencia simulada,
MARCO TEÓRICO:
Un recipiente aislado térmicamente contiene una cierta cantidad de agua,
con un termómetro para medir su temperatura, un eje con unas paletas que
se ponen en movimiento por la acción de una pesa, tal como se muestra en la
figura.
La versión original del experimento, consta de dos pesas iguales que cuelgan
simétricamente del eje.
La pesa, que se mueve con velocidad prácticamente constante, pierde
energía potencial. Como consecuencia, el agua agitada por las paletas se
clienta debido a la fricción.
Experimento de Joule. Equivalente Mecánico del Calor
Página 1
Si el bloque de masa M desciende una altura h, la energía potencial
disminuye en Mgh, y ésta es la energía que se utiliza para calentar el agua
(se desprecian otras pérdidas).
Joule encontró que la disminución de energía potencial es proporcional al
incremento de temperatura del agua. La constante de proporcionalidad (el
calor específico de agua) es igual a 4.186 J/(g ºC). Por tanto, 4.186 J de
energía mecánica aumentan la temperatura de 1g de agua en 1º C. Se define
la caloría como 4.186 J sin referencia a la sustancia que se está calentando.
1 cal=4.186 J
En la simulación de la experiencia de Joule, se desprecia el equivalente en
agua del calorímetro, del termómetro, del eje y de las paletas, la pérdida de
energía por las paredes aislantes del recipiente del calorímetro y otras
pérdidas debidas al rozamiento en las poleas, etc.
Sea M la masa del bloque que cuelga y h su desplazamiento vertical
m la masa de agua del calorímetro
T0 la temperatura inicial del aguay T la temperatura final
g=9.8 m/s2 la aceleración de la gravedad
La conversión de energía mecánica íntegramente en calor se expresa
mediante la siguiente ecuación.
Mgh=mc(T-T0)
Se despeja el calor específico del agua que estará expresado en J/(kg K).
Como el calor especifico del agua es por definición c=1 cal/(g ºC), obtenemos
la equivalencia entre las unidades de calor y de trabajo o energía.
MATERIALES:
Experimento de Joule. Equivalente Mecánico del Calor
Página 2
Simulador
PROCEDIMIENTO:
Se introduce
La masa M del bloque que cuelga (en kg), en el control de edición
titulado Pesa que cuelga.
La masa m de agua (en g) o su volumen en ml, en el control de edición
titulado Masa de agua.
La temperatura inicial T0 se fijado en el programa interactivo en el
valor de 20ºC
Se pulsa el botón titulado Empieza.
Para detener el movimiento del bloque a una altura determinada se pulsa el
botón titulado Pausa y luego, varias veces Paso, para acercarnos a la altura
deseada paso a paso
Observamos la caída del bloque, que mueve unas aspas que están dentro del
calorímetro. El rozamiento de las aspas en movimiento con el agua eleva su
temperatura. Se deja caer el bloque una altura h y se apunta la
temperatura T final del agua calentada.
Ejemplo:
Se introduce
Masa del bloque M=50 kg
Masa del agua en g (o volumen del agua en ml), m=100 g=0.10 kg
Se apunta
Altura h=1 m
Temperatura inicial T0=20ºC, y la temperatura final T=21.2ºC
Experimento de Joule. Equivalente Mecánico del Calor
Página 3
Tenemos que aumentar la diferencia de temperaturas para obtener un
mejor resultado. En la experiencia real se consigue haciendo caer varias
veces el bloque. El trabajo total es n·Mgh, siendo n el número de veces que
se suelta el bloque. En la experiencia simulada conseguimos el mismo efecto
aumentando la masa M del bloque.
CÁLCULOS:
CAPTURA 1: REFERENCIA
Masa del bloque : M=50 kg
Masa del agua en g: m=100 g = 0.10 kg
Altura h=1 m
Temperatura inicial To = 20ºC
temperatura final T= 21.2ºC
𝑀𝑔ℎ
𝑐=
𝑚(𝑇 − 𝑇𝑜)
50 × 9,8 × 1
𝑐=
0,10(21,2 − 20)
𝑱
𝒄 = 𝟒𝟎𝟖𝟑, 𝟑
𝑲𝒈°𝑪
CAPTURA 2:
Masa del bloque : M=50 kg
Experimento de Joule. Equivalente Mecánico del Calor
Página 4
Masa del agua en g: m=200 g = 0.20 kg
Altura h=1 m
Temperatura inicial To = 20ºC
temperatura final T= 20.6ºC
𝑀𝑔ℎ
𝑐=
𝑚(𝑇 − 𝑇𝑜)
50 × 9,8 × 1
𝑐=
0,20(20,6 − 20)
𝑱
𝒄 = 𝟒𝟎𝟖𝟑, 𝟑
𝑲𝒈°𝑪
CAPTURA 3: MAYOR RADIO DEL DEPÓSITO
Masa del bloque : M=150 kg
Masa del agua en g: m=100 g = 0.10 kg
Altura h=1 m
Temperatura inicial To = 20ºC
Temperatura final T= 23.5ºC
𝑀𝑔ℎ
𝑐=
𝑚(𝑇 − 𝑇𝑜)
50 × 9,8 × 1
𝑐=
0,10(23,5 − 20)
𝑱
𝒄 = 𝟒𝟐𝟎𝟎
𝑲𝒈°𝑪
Experimento de Joule. Equivalente Mecánico del Calor
Página 5
CONCLUSIONES:
El calor es energía que es transferida desde un cuerpo a otro debido
a su diferencia de temperatura.
El calor no es una sustancia, ni una forma de energía, sino más bien
como una forma de transferencia de energía.
Se necesita transformar una gran cantidad de energía en calor para
elevar apreciablemente la temperatura de un volumen pequeño de
agua.
Si aumentamos la masa del agua, disminuye la temperatura final.
Si aumentamos la masa del bloque, aumenta la temperatura final.
La disminución de energía potencial es proporcional al incremento de
temperatura del agua
RECOMENDACIONES:
Cambiar las masas un número considerable de veces para así lograr
analizar el simulador y sacar conclusiones
Prestar atención a los aumentos de temperatura pues es la clave de
la práctica.
BIBLIOGRAFÍA:
http://www.quimicayalgomas.com/fisica/energia-cinetica-y-potencial
http://www.sc.ehu.es/sbweb/fisica/fluidos/dinamica/vaciado/vaciado.htm
http://www.youtube.com/watch?v=6LOgdOfFAbI
ANEXOS:
Experimento de Joule. Equivalente Mecánico del Calor
Página 6
CAPTURA 1:
Referencia
CAPTURA 2:
Experimento de Joule. Equivalente Mecánico del Calor
Página 7
Mayor masa de agua
CAPTURA 3:
Mayor masa del bloque
Experimento de Joule. Equivalente Mecánico del Calor
Página 8
También podría gustarte
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Laboratorio de Fisica Experimento de JouDocumento9 páginasLaboratorio de Fisica Experimento de JoualfredoAún no hay calificaciones
- Experimento de JouleDocumento4 páginasExperimento de JouleMancilla MathiusAún no hay calificaciones
- Experimento JouleDocumento3 páginasExperimento JouleZurisadai OrtegaAún no hay calificaciones
- JouleDocumento3 páginasJoulepablo vargasAún no hay calificaciones
- En El Experimento de Joule Se Determina El Equivalente Mecánico Del CalorDocumento4 páginasEn El Experimento de Joule Se Determina El Equivalente Mecánico Del CalorLuis Altamirano RafaelAún no hay calificaciones
- Experimento de JouleDocumento3 páginasExperimento de JouleEnidlarey FlowersAún no hay calificaciones
- Experimento de Joule. Equivalente Mecánico Del CalorDocumento3 páginasExperimento de Joule. Equivalente Mecánico Del CalorMiguel DiazAún no hay calificaciones
- Informe N 2 Prueba de JarrasDocumento5 páginasInforme N 2 Prueba de JarrasHayeDuranAún no hay calificaciones
- En El Experimento de Joule Se Determina El Equivalente Mecánico Del CalorDocumento7 páginasEn El Experimento de Joule Se Determina El Equivalente Mecánico Del CalorShawn McleanAún no hay calificaciones
- Calorimetro de JouleDocumento2 páginasCalorimetro de JouleAntonio J. Q. PalaciosAún no hay calificaciones
- Experimento de JouleDocumento10 páginasExperimento de JouleAliCiaAún no hay calificaciones
- Lab 1equivalente Mec Del CalorDocumento4 páginasLab 1equivalente Mec Del CalorDavid Paez GonzalezAún no hay calificaciones
- Práctica 1 Equivalente Mecánico Del CalorDocumento3 páginasPráctica 1 Equivalente Mecánico Del CalorFelipe Vinchery100% (1)
- Práctica 6 - Martinez - Badillo - MT3EDocumento14 páginasPráctica 6 - Martinez - Badillo - MT3ElUISIlloAún no hay calificaciones
- EL Calorímetro de JouleDocumento2 páginasEL Calorímetro de JouleJUAN DIEGO VASQUEZ HERRERAAún no hay calificaciones
- Equivalente Mecánico Del CalorDocumento9 páginasEquivalente Mecánico Del CalorMoller Calderon Sergio HAún no hay calificaciones
- Practica 6 Entalpia de TransformaciónDocumento7 páginasPractica 6 Entalpia de TransformaciónPadrón Resendiz Fernando RodolfoAún no hay calificaciones
- Informe 1. Fisica 2Documento6 páginasInforme 1. Fisica 2Liceth Páez100% (1)
- Determinación del equivalente mecánico de calorDocumento11 páginasDeterminación del equivalente mecánico de calorSamantaYoselimHuaranccaAún no hay calificaciones
- 8equivalente Mecanico Del CalorDocumento10 páginas8equivalente Mecanico Del CalorMiriam Vasquez BravoAún no hay calificaciones
- Equivalente Mecanico Del Calor VirtuallIIDocumento10 páginasEquivalente Mecanico Del Calor VirtuallIIOMAR ISIDRO RIVERA CANOAún no hay calificaciones
- LT. Reporte N°6. Entalpía de Transformación. Brigada N°1. Grupo 17. Semestre 2023-2Documento9 páginasLT. Reporte N°6. Entalpía de Transformación. Brigada N°1. Grupo 17. Semestre 2023-2Rosas Pérez Erika ArlethAún no hay calificaciones
- Termodinamica Practica 3Documento6 páginasTermodinamica Practica 3Cedric MonroyAún no hay calificaciones
- Práctica 7 TermodinámicaDocumento10 páginasPráctica 7 TermodinámicaFDGH133333100% (1)
- Experimento de Joule PDFDocumento1 páginaExperimento de Joule PDFJulio VásquezAún no hay calificaciones
- Informe6 - Equivalente Eléctrico Del CalorDocumento12 páginasInforme6 - Equivalente Eléctrico Del CalorMario Aguaguiña M.Aún no hay calificaciones
- Equivalente Mecanico Del Calor virtuallIIDocumento9 páginasEquivalente Mecanico Del Calor virtuallIIKatakuri CaceresAún no hay calificaciones
- Equivalente Mecanico Del CalorDocumento4 páginasEquivalente Mecanico Del CalorRubiany Gonzalez QuiñonezAún no hay calificaciones
- Universidad Autónoma Del Estado de México Facultad de CienciasDocumento10 páginasUniversidad Autónoma Del Estado de México Facultad de CienciasAguirre Acosta FernandaAún no hay calificaciones
- ENTALPÍA DE FUSIÓN DEL AGUADocumento8 páginasENTALPÍA DE FUSIÓN DEL AGUANaomy Stephany Muñoz FloresAún no hay calificaciones
- Equivalente eléctrico del calorDocumento6 páginasEquivalente eléctrico del calorJesusAún no hay calificaciones
- Calor latente de fusión y cambios de estadoDocumento15 páginasCalor latente de fusión y cambios de estadoSandy100% (1)
- LT - reporte5.EquivalenteMecánicoDelCalor - brigada4.Grupo13.Semestre2024 1Documento6 páginasLT - reporte5.EquivalenteMecánicoDelCalor - brigada4.Grupo13.Semestre2024 1Jorge Luis HernandezAún no hay calificaciones
- Experiencia de JouleDocumento2 páginasExperiencia de JouleJose Vilca NinaAún no hay calificaciones
- Guía 2 - Equivalente Mecánico Del CalorDocumento4 páginasGuía 2 - Equivalente Mecánico Del CalorAngie Viviana Sandoval CastilloAún no hay calificaciones
- Equivalente Mecanico Del CalorDocumento9 páginasEquivalente Mecanico Del CalorLen AbernathyAún no hay calificaciones
- LABORATORIO N 2 Calorimetria LisethDocumento9 páginasLABORATORIO N 2 Calorimetria Lisethliseth angela oña monzonAún no hay calificaciones
- Determina la capacidad calorífica de un sólidoDocumento7 páginasDetermina la capacidad calorífica de un sólidoKeviin ArronaAún no hay calificaciones
- Ejercicios Resueltos Quimica CalorimetriDocumento14 páginasEjercicios Resueltos Quimica CalorimetriIsmael Trejo NuñezAún no hay calificaciones
- WWW SC Ehu Es Sbweb Fisica Estadistica Otros Fusion Fusion HDocumento15 páginasWWW SC Ehu Es Sbweb Fisica Estadistica Otros Fusion Fusion HEduardo Daniel Zaragoza TejedaAún no hay calificaciones
- Laboratorio Equivalente Mecanico Del CalorDocumento9 páginasLaboratorio Equivalente Mecanico Del CalorKatakuri CaceresAún no hay calificaciones
- Upo13.semestre2024 1Documento8 páginasUpo13.semestre2024 1Jorge Luis HernandezAún no hay calificaciones
- Preguntas Resueltas FisicaDocumento4 páginasPreguntas Resueltas FisicaLincoln GarciaAún no hay calificaciones
- CALORIMETRIADocumento14 páginasCALORIMETRIAIsmael Trejo NuñezAún no hay calificaciones
- Teoría y Práctica Dirigida de TermodinamicaDocumento9 páginasTeoría y Práctica Dirigida de TermodinamicaPedro Gurmendi0% (1)
- Laboratorio N°7Documento11 páginasLaboratorio N°7Omar ObregónAún no hay calificaciones
- PRACTICA No 3 CalorimetriaDocumento9 páginasPRACTICA No 3 CalorimetriaAlexis Villalobos JacomeAún no hay calificaciones
- Practica 4 Aplicaciones de Propiedades de La Materia.Documento15 páginasPractica 4 Aplicaciones de Propiedades de La Materia.Nancy AEAún no hay calificaciones
- Lab - Virt - F2 - Equivalente CalorDocumento5 páginasLab - Virt - F2 - Equivalente CalorLeo CastilloAún no hay calificaciones
- Calor y Cambios de Fase Del AguaDocumento9 páginasCalor y Cambios de Fase Del AguaAna Luisa Tacanga RodriguezAún no hay calificaciones
- T13 Calor y TermodinámicaDocumento10 páginasT13 Calor y TermodinámicaXisca Muros MayansAún no hay calificaciones
- Laboratorio Efecto JouleDocumento3 páginasLaboratorio Efecto Joulejuan carlos0% (1)
- Calor AbsorbidoDocumento18 páginasCalor AbsorbidoRenzo Acevedo CanoAún no hay calificaciones
- Práctica de Laboratorio de Física N 8Documento10 páginasPráctica de Laboratorio de Física N 8Junior Quispe HuarcayaAún no hay calificaciones
- Calor AbsorbidoDocumento18 páginasCalor AbsorbidoSandy CisnerosAún no hay calificaciones
- 001 Nota TécnicaDocumento11 páginas001 Nota TécnicaFRANCISCO RAMÍREZ FLORESAún no hay calificaciones
- Determinación del Equivalente Mecánico del Calor (J/calDocumento7 páginasDeterminación del Equivalente Mecánico del Calor (J/calDieguito BravoAún no hay calificaciones
- DONOFRIODocumento3 páginasDONOFRIOalfredoAún no hay calificaciones
- Infrome de Aceite de OlivaDocumento13 páginasInfrome de Aceite de Olivaalfredo100% (1)
- Contabildad IIDocumento51 páginasContabildad IIalfredoAún no hay calificaciones
- Nectar de ZanahoriaDocumento16 páginasNectar de ZanahoriaalfredoAún no hay calificaciones
- Maíz en el PerúDocumento44 páginasMaíz en el PerúalfredoAún no hay calificaciones
- Vinos TRAB MAQUINARIASDocumento23 páginasVinos TRAB MAQUINARIASalfredoAún no hay calificaciones
- Fuerza Magnética Sobre Una Corriente EléctricaDocumento13 páginasFuerza Magnética Sobre Una Corriente EléctricaalfredoAún no hay calificaciones
- Tensinsuperficial 121110005236 Phpapp02Documento27 páginasTensinsuperficial 121110005236 Phpapp02alfredoAún no hay calificaciones
- PLANTEAMIENTO DEL PROBLEMA de Ing. de AlimentosDocumento1 páginaPLANTEAMIENTO DEL PROBLEMA de Ing. de AlimentosalfredoAún no hay calificaciones
- Cadenas de rodillos: características y montajeDocumento13 páginasCadenas de rodillos: características y montajealfredoAún no hay calificaciones
- Exposicion de KiwichaDocumento27 páginasExposicion de KiwichaalfredoAún no hay calificaciones
- Formulacion de Pan de Yema en Base SecaDocumento2 páginasFormulacion de Pan de Yema en Base SecaalfredoAún no hay calificaciones
- Protocolo de Tratamiento de AguaDocumento9 páginasProtocolo de Tratamiento de AguaalfredoAún no hay calificaciones
- Introduccion CafeDocumento9 páginasIntroduccion CafealfredoAún no hay calificaciones
- Diseoeimplementaciondel Plan HACCPparaunalineadebebidaslcteasDocumento10 páginasDiseoeimplementaciondel Plan HACCPparaunalineadebebidaslcteasCarla Modesta Cruz ChoquetomaAún no hay calificaciones
- Acc DinDocumento15 páginasAcc DinJavier Canto RiosAún no hay calificaciones
- Estudio de La Vida Útil de ChampiñonesDocumento17 páginasEstudio de La Vida Útil de ChampiñonesalfredoAún no hay calificaciones
- Problema 4-4 Santiago Mendez Marco AntonioDocumento3 páginasProblema 4-4 Santiago Mendez Marco Antoniomarco1mendez-829885Aún no hay calificaciones
- 3 Válvulas de EstrangulamientoDocumento3 páginas3 Válvulas de EstrangulamientoRenzo Vargas RamirezAún no hay calificaciones
- Ficha - 2020 GMV5Documento3 páginasFicha - 2020 GMV5Joaquin de la CruzAún no hay calificaciones
- Carlos Péndola Tarea 7.Documento11 páginasCarlos Péndola Tarea 7.marcelavalramAún no hay calificaciones
- Tecnológico - de-WPS - Office - Recuperar (1) (1) (Autoguardado)Documento8 páginasTecnológico - de-WPS - Office - Recuperar (1) (1) (Autoguardado)julioAún no hay calificaciones
- Potenciales Termodinámicos y Equilibrio Químico 2023-2Documento3 páginasPotenciales Termodinámicos y Equilibrio Químico 2023-2Hector Toledano EspinosaAún no hay calificaciones
- Ejercicios Resueltos QMC 1206 IIDocumento7 páginasEjercicios Resueltos QMC 1206 IIAna Luisa Garnica SalgadoAún no hay calificaciones
- PROYECTO CERTIFICACIÓN PROGRESIVA - Sistema de Refrigeración - V1.5Documento29 páginasPROYECTO CERTIFICACIÓN PROGRESIVA - Sistema de Refrigeración - V1.5ANTHONY FRANCESCO SAAVEDRA AGURTOAún no hay calificaciones
- Ficha Aeromax VM ES 2022 2Documento1 páginaFicha Aeromax VM ES 2022 2taponcete69Aún no hay calificaciones
- Unidad 3 TermDocumento20 páginasUnidad 3 TermElizabeth AguilarAún no hay calificaciones
- Proyecto Final - Termodinámica 2 - Arrocha, Ayarza, Mendoza, VasquezDocumento21 páginasProyecto Final - Termodinámica 2 - Arrocha, Ayarza, Mendoza, Vasquezian ayarzaAún no hay calificaciones
- Ejercicios Ciclo Rankine y Refrigerativo 2015-IDocumento8 páginasEjercicios Ciclo Rankine y Refrigerativo 2015-ILeoStyle16Aún no hay calificaciones
- Tarea, Ejercicios Transferencia de CalorDocumento4 páginasTarea, Ejercicios Transferencia de CalorRonny Salcedo LópezAún no hay calificaciones
- Balance Térmico Del Horno CementeroDocumento11 páginasBalance Térmico Del Horno CementeroDairo MontesAún no hay calificaciones
- Formulario y Diagramas - Transferencia de Calor PDFDocumento46 páginasFormulario y Diagramas - Transferencia de Calor PDFIgnacio SotoAún no hay calificaciones
- Flujo de Refrigerante y Funcionamiento Simple Del Sistema de RefrigeraciónDocumento9 páginasFlujo de Refrigerante y Funcionamiento Simple Del Sistema de RefrigeraciónJonayker Enrique Paredes AlvaradoAún no hay calificaciones
- Paper de ArleneDocumento16 páginasPaper de ArleneCmi IndepAún no hay calificaciones
- Problemas Tema 4 PDFDocumento2 páginasProblemas Tema 4 PDFAnonymous iVr7CfAún no hay calificaciones
- Balance de Energía - Problemario 1Documento9 páginasBalance de Energía - Problemario 1Marco TrejoAún no hay calificaciones
- 3.1-Thermal conceptsDocumento20 páginas3.1-Thermal conceptsThalia CerfAún no hay calificaciones
- Respuesta Total de Todos Los Quiz de TermidinamicaDocumento64 páginasRespuesta Total de Todos Los Quiz de TermidinamicaLevy FrancoAún no hay calificaciones
- Flujo IsentropicoDocumento8 páginasFlujo IsentropicoSofía Ariadna Castro GonzálezAún no hay calificaciones
- ENTALPÍADocumento6 páginasENTALPÍAAdiu Julian BonanzaAún no hay calificaciones
- Practica 4 QUIMICA APLICADA ESIMEZDocumento11 páginasPractica 4 QUIMICA APLICADA ESIMEZCamila Mendoza GaonaAún no hay calificaciones
- Transferencia de calor por convección: tipos, factores y ecuacionesDocumento34 páginasTransferencia de calor por convección: tipos, factores y ecuacionesAlejandro Miguel MacarenoAún no hay calificaciones
- Calor, Temperatura y Dilatación. Guía de EjerciciosDocumento3 páginasCalor, Temperatura y Dilatación. Guía de EjerciciosCota Flores BurbujaAún no hay calificaciones
- Taller. Trabajo de Frontera de Gases Ideales.Documento3 páginasTaller. Trabajo de Frontera de Gases Ideales.GARCIA PEREZ ANDRES FELIPEAún no hay calificaciones
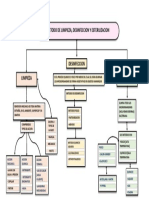
- Mapa Conceptual Delimpieza, Desinfeccion.Documento1 páginaMapa Conceptual Delimpieza, Desinfeccion.Yecenia Moreno Potenciano100% (6)
- Universidad de San Carlos de Guatemala Facultad de Ingeniería Escuela de Ingeniería QuímicaDocumento189 páginasUniversidad de San Carlos de Guatemala Facultad de Ingeniería Escuela de Ingeniería QuímicaRafael GomezAún no hay calificaciones
- Determinación de voltaje en proceso de evaporación con resistenciaDocumento8 páginasDeterminación de voltaje en proceso de evaporación con resistenciaJAVIER ANDRES PEREZ GARCIAAún no hay calificaciones