100% encontró este documento útil (3 votos)
4K vistas9 páginasFenomenos Practica CALORIMETRIA ESIQIE
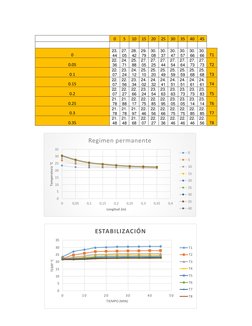
1. El documento describe un experimento de calorimetría para medir la transferencia de calor a través de una varilla de bronce. 2. Los estudiantes aplicarán la ley de Fourier para determinar la cantidad de calor que se transfiere a través del bronce y calcularán el coeficiente de transmisión de calor para encontrar la cantidad de calor perdida. 3. El experimento busca identificar cuando se alcanza el estado estacionario de transferencia de calor mediante la medición de un perfil de temperaturas a lo largo de la varilla.
Cargado por
JAUNDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
100% encontró este documento útil (3 votos)
4K vistas9 páginasFenomenos Practica CALORIMETRIA ESIQIE
1. El documento describe un experimento de calorimetría para medir la transferencia de calor a través de una varilla de bronce. 2. Los estudiantes aplicarán la ley de Fourier para determinar la cantidad de calor que se transfiere a través del bronce y calcularán el coeficiente de transmisión de calor para encontrar la cantidad de calor perdida. 3. El experimento busca identificar cuando se alcanza el estado estacionario de transferencia de calor mediante la medición de un perfil de temperaturas a lo largo de la varilla.
Cargado por
JAUNDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd