Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Practica 1 Cinetica y Reactores Homogeneos
Cargado por
Josue CarmonaDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Practica 1 Cinetica y Reactores Homogeneos
Cargado por
Josue CarmonaCopyright:
Formatos disponibles
lOMoARcPSD|7718551
Practica 1 Cinetica y reactores homogeneos
Cinética Y Reactores Homogéneos (Instituto Politécnico Nacional)
StuDocu no está patrocinado ni avalado por ningún colegio o universidad.
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
INSTITUTO
POLITECNICO
NACIONAL
ESCUELA SUPERIOR DE INGENIERIA
QUIMICA E INDUSTRIAS EXTRACTIVAS
ACADEMIA DE FISICOQUÍMICA
LABORATORIO DE CINÉTICA Y
REACTORES HOMOGÉNEOS
PRACTICA #1:
DILUCION DEL HIERRO EN UN MEDIO
ACIDO
PROF. MARTHA LETICIA HERNANNDEZ
PICHARDO
INTEGRANTES:
CRUZ MENDOZA RAQUEL
MOTA GARDUÑO VICTOR HUGO
RAMIREZ MARTINEZ JOSE GERARDO
3IM52
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
INTRODUCCION
ESTUDIO CINETICO DE LAS REACCIONES QUIMICAS
En el estudio termodinámico de una reacción nos interesa ver que los productos tienen
una energía libre menor que los reactivos, lo cual hará que la reacción sea espontanea.
Sin embargo, hemos puesto dos ejemplos de diagramas de dos reacciones químicas
distintas, ambas espontaneas.
A pesar de corresponder ambos a procesos energéticamente
favorables, tienen una diferencia muy clara: la montaña amarilla
que separa reactivos de productos no tiene la misma altura. La
diferencia entre la energía de reactivos
de los reactivos y la cima de la montaña
se denomina energía de activación, y
cuanta más pequeña sea mayor será la
velocidad de reacción. Es decir, la
magnitud de la energía de activación nos indica el aspecto
cinético de la reacción química, la velocidad a la cual transcurre
una reacción.
Así, podemos definir la cinética química como el estudio de la velocidad a la cual
transcurren las reacciones químicas y de los factores que influyen en ella, como
concentraciones, naturaleza de los reactivos o la presencia de catalizadores.
Podemos determinar con los tres diagramas siguientes cuál de las reacciones tendrá,
comparativamente, una velocidad menor y cual una velocidad mayor.
La variación de energía libre negativa de una reacción química nos indica que una
reacción será espontanea pero no a qué velocidad transcurrirá. Para saber la cinética
química de la reacción debemos fijarnos en la barrera de potencial es decir, menor será la
velocidad de reacción porque resulta más costoso para el sistema.
REACCION EN SOLUCION
Suelen ser bastante simples de analizar. Uno de los métodos tradicionales consiste en
dividir la solución en varias ampolletas y calentarlas a baño maría, posteriormente se van
retirando durante intervalos de tiempos constantes y se utilizan métodos analíticas
apropiados para obtener las concentraciones de interés.
CLASIFICACION DE LOS METODOS PARA LA OBTENCION DE DATOS CINETICOS
-METODO QUIMICO:
Se determina la concentración utilizando una reacción química
VENTAJAS:
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
Procedimientos simples y precisos.
Generalmente se basan en medidas absolutas.
-METODO FISICO:
Se determina alguna propiedad física de la reacción.
VENTAJAS:
Fácil determinación de propiedades físicas.
Determinación en corto tiempo.
- METODO FISICO-QUIMICO O INSTRUMENTAL:
Se evalúa una propiedad física a lo largo de una reacción.
VENTAJAS:
Determinación rápida.
Utiliza pequeñas muestras.
Posibilidad de obtener cambios de concentración sin sacar la celda de reacción del
aparato.
-METODO TITRIMETRICO:
Determinación del componente
analizado se hace por titulación con
una sustancia patrón que reacciona
químicamente con la sustancia
analizada hasta alcanzar el punto
de equivalencia estequiométrico.
-ESPECTROFOTOMETRIA:
La espectrofotometría es el método de análisis óptico más usado
en investigaciones biológicas. El espectrofotómetro es un
instrumento que permite comparar la radiación absorbida o
transmitida por una solución que contiene una cantidad
desconocida de soluto, y una que contiene una cantidad
conocida de la misma sustancia.
Todas las sustancias pueden absorber energía radiante, aun el vidrio que parece ser
completamente transparente absorbe longitud de ondas que pertenecen al espectro
visible; el agua absorbe fuertemente en la región del infrarrojo.
La absorción de las radiaciones ultravioleta, visibles e infrarrojas depende de la estructura
de las moléculas, y es característica para una sustancia química.
Cuando a luz atraviesa una sustancia, parte de la energía es absorbida; energía radiante
no puede producir ningún efecto sin ser absorbida. El color de las sustancias se debe a
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
que estas absorben ciertas longitudes de onda de la luz blanca que incide sobre ellas y
solo dejan pasar a nuestros ojos aquellas longitudes de onda no absorbidas.
DESARROLLO EXPERIMENTAL
METODO TITRIMETRICO
REACCIONES INVOLUCRADAS:
2 HCl(ac ) + Fe( s) → Fe Cl2( sol )+ H 2(g )
HCl( ac )+ NaOH ( s ) → NaCl( sol ) + H 2 O ( l)
Preparar y Valorar 15ml HCl 1M en Agregar 1g de clavos
1L de NaOH 1M vaso de precipitados o fibra
Alicuota de 2ml (to)
2 gotas de
en matraz Arrancar cronómetro
Anaranjado de metilo
Erlenmeyer
Vire de rosa a Alicuota de 1ml cada
Titular con NaOH 1M
amarillo 5minutos
Tabla 1.1 Hasta 30min
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
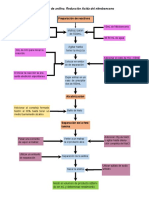
METODO ESPECTOFOTOMETRICO
REACCIONES INVOLUCRADAS:
2 HCl(ac ) + Fe( s) → Fe Cl2( sol )+ H 2(g )
3+ ¿→ Fe( SCN )3complejo café claro¿
Fe2+ ¿→ Fe ¿
15ml HCl 1M en
Preparar y Valorar Agregar 1g de
vaso de
1L de HCl 1M clavos o fibra
precipitados
Tomar alicuota de
Agregar 1ml de Arrancar
2ml (to) en matraz
H2O2 al 30%w cronómetro
Erlenmeyer
Agregar 1ml de Colocar en una Longitud de onda:
KSCN 0.1M celda 450nm
Alicuota de 3ml Lectura
Tabla 1.2
cada 3min espectofotométrica
Hasta 15min Tabla 1.2
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
METODO GRAVIMETRICO
REACCIONES INVOLUCRADAS:
2 HCl(ac ) +Fe( s) → Fe Cl2( sol )+ H 2(g )
3ml HCl 1M en vaso
Agregar 1 clavo de
de precipitados de Arrancar cronómetro
1/4´´ (pesado) (to)
100ml
Secar, pesar y
4 veces 10min sacar clavo
regresarlo
Combinacion 1: HCl
Combinacion 2: HCl Combinacion 3: HCl
conc y clavo
1M y clavo lacerado conc y clavo oxidado
lacerado
Combinacion 4: HCl
Tabla 1.3
1M y clavo oxidado
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
METODO GASOMETRICO
REACCIONES INVOLUCRADAS:
2 HCl(ac ) +Fe( s) → Fe Cl2( sol )+ H 2(g )
Manometro
3ml HCl concentrado
NO fugas suficiente líquido
matraz gasómetro
indicador
Líquido del
Si no, purgar Manómetro este en 0 manómetro nivelado
con papel mm
1 clavo oxidado Tapar Arrancar cronómetro
Cada 5seg hasta 7 Medir distancia (∆h)
Tabla 1.4
lect. al to
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
TABLA DE DATOS EXPERIMENTALES
METODO TITRIMÉTRICO
Corrida Tiempo (min) V NaOH (ml)
1 0 7
2 4 4.5
3 8 4
4 12 5.5
5 16 10
6 20 14.5
METODO ESPECTOFOTOMÉTRICO
Corrida Tiempo (min) Absorbancia (nm)
1 0 0.004
2 3 0.008
3 6 0.023
4 9 0.033
5 12 0.025
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
CÁLCULOS
METODO TITRIMÉTRICO
Para obtener la concentración de la solución de HCl es necesario aplicar el principio de
equivalencia.
¿
C NaOH V NaOH
C HCl =
V HCl
Sustituyendo los valores experimentales.
1 M∗7 ml
C HCl ,1=
2 ml
C HCl ,1=3.5 M
C HCl ,2=2.25 M
C HCl ,3=2 M
C HCl ,4 =2.75 M
C HCl ,5=5 M
C HCl ,6=7.25 M
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
CÁLCULOS
METODO ESPECTOFOTOMETRICO
Para el cálculo de la concentración se utiliza la ecuación de Lambert-Beer
As=ε b C
ε = Concentracion de absortividad de 200 L/mol cm
b= ancho de la celda (1cm)
C= Concentración (mol/L)
As
C=
εb
As
C=
L
200 ∗1 cm
mol cm
As
C=
L
200
mol
0.004
C 1=
L
200
mol
C 1=2 x 10−5 mol /L
C 2=4 x 10−5 mol /L
C 3=1.15 x 10− 4 mol/ L
C 4=1.65 x 10−4 mol /L
C 5=1.25 x 10−4 mol/ L
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
TABLA DE RESULTADOS
METODO TITRIMÉTRICO
Corrida Tiempo (min) V NaOH (ml) C HCl (ml)
1 0 7 3.5
2 4 4.5 2.25
3 8 4 2
4 12 5.5 2.75
5 16 10 5
6 20 14.5 7.25
METODO ESPECTOFOTOMÉTRICO
Corrida Tiempo (min) Absorbancia (nm) C FeCl 2 (mol/L)
1 0 0.004 2 x 10−5
2 3 0.008 4 x 10−5
3 6 0.023 1.15 x 10−4
4 9 0.033 1.65 x 10−4
5 12 0.025 1.25 x 10−4
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
GRAFICAS
METODO TITRIMÉTRICO
t vs C HCl
t vs Conc HCl
8
7.25
7
5 5
C HCl (M)
4
3.5
3
2.75
2.25
2 2
0
0 5 10 15 20 25
tiempo (min)
t vs Conc
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
METODO ESPECTOFOTOMETRICO
t vs C FeCl 2
t vs C FeCl2
0
0 0
0
0 0
C FeCl2 (mol/L)
0
0
0
0
0 0
0 0
0
0 2 4 6 8 10 12 14
tiempo (min)
t vs C
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
CUESTIONARIO
1. ¿Cuál de los métodos es más práctico y porque?
El método espectrofotométrico ya que es más rápido y con este método el equipo
realiza determinaciones más exactas las cuales contiene un margen de error a
diferencia del método titrimétrico en este pueden ocurrir errores visuales.
2. ¿Podría mejorarse alguno de los métodos, cómo?
El método titrimétrico y sería logrando una mejor titulación que fuese reproducible y
poder obtener un promedio, también la tolerancia del material de laboratorio ya que
unos materiales son más exactos que otros.
Y en el espectrofotómetro es difícil mejorar ya que el equipo al ser calibrado se
obtiene mejores resultados.
3. ¿Cuál crees que sean los errores más comunes en cada método?
En el método de espectrofotometría el error más común pueden ser que no se
registran los valores deseados en los tiempos exactos.
En el método titrimétrico el error más común es que al momento de titular la solución
nos pasamos del punto de equivalencia, lo cual genera errores a la hora de hacer los
cálculos respectivos; el preparar de forma correcta las soluciones representa un
aspecto fundamental, así como su correcta disposición para su almacenaje, ya que
estas condiciones determinan el resultado final del experimento.
4. En general, ¿Cuál fue el mejor método y porque?
El método espectrofotométrico resulta más preciso que los otros tres métodos,
además no lleva tanto tiempo su realización y es mucho más fácil el muestreo además
porque por el equipo que se emplea en este método es menos probable que se
obtengan errores tal como en el titrimétrico.
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
OBSERVACIONES
En la experimentación mientras más iba avanzando la reacción se podía apreciar en
datos que aumentaba la concentración de la sal y como se iba reduciendo el clavo en los
datos obtenidos en el método titrimétrico concordaba con el método de equivalencias.
Se utilizó un clavo oxidado y en el manual se propone un clavo NO oxidado pero no se
utilizó porque para la disolución del Fe sería muy tardado, debido a que la concentración
del ácido es muy baja y la velocidad de reacción seria lenta.
En el método espectrofotométrico tuvimos una pequeña variación al final de las
mediciones ya que nuestro valor disminuyó al punto anterior, esta variación la podemos
atribuir a que la celda posiblemente estaba mojada y eso disminuye la concentración de
nuestra alícuota y he ahí la variación en la medición.
En el método titrimétrico los valores no fueron como esperamos ya que la solución estaba
muy contaminada y no servía para realizar el experimento.
De acuerdo a la fundamentación teórica que se plantea en el manual y a la
información proporcionada por la profesora al inicio de la práctica, se pudieron
observar de una forma totalmente gráfica el distinto comportamiento numérico de
la reacción que se estaba llevando a cabo en ese momento.
En el primer método que fue el titrimétrico, el hecho de que las soluciones de las
cuales se estaba haciendo uso en ese momento, estuviesen contaminadas (lo cual
no nos pudimos percatar ya que el mismo envase en el cual estaban dispuestas
no lo permitía), y eso tuvo grandes repercusiones a la hora de esperar el vire de
nuestra solución, ya que ni presentaba el color representativo. Otra cuestión que
afecto éste método y que o hizo accidentado fue el cambio de bureta, ya que la
primera que se empleó no tenía un correcto flujo del líquido, y al cambiarla por otra
nueva, tuvimos un error de apreciación del menisco. Esto, inevitablemente se ve
reflejó en la gráfica que se anexa en el presente informe, su disposición está en
sentido contrario a lo que debió de ser.
En cuanto al método espectrofotométrico, considero que se cumplió con su
función, ya que los datos que se lograron recabar, ya plasmados en una gráfica (la
cual también se anexa en éste informe) tienen la tendencia que nos había
marcado la profesora, aunque en nuestra última determinación, el hecho de que
nuestra celda, en la cual se depositaría la solución a evaluar; estuviese
contaminada, arrojó un dato nada acertado.
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
CONCLUSIONES
El método espectrofotométrico es mejor que el titrimétrico debido a que en este hay más
probabilidad de cometer errores como detección del punto final de la titulación o
soluciones mal valoradas o contaminadas.
En las mediciones con el método titrimétrico tuvimos más errores, el volumen gastado de
NaOH gastado aumentaba y disminuía pero en general se ve como la concentración del
HCl disminuye con el tiempo. Esto es correcto ya que el ácido reacción con el fierro
disminuyendo la cantidad de HCl del sistema.
Nuestra experimentación del método titrimétrico no fue el mejor método esto fue debido a
que las soluciones que debíamos de usar estaban contaminadas e intuimos que de igual
forma no estaban bien preparadas por eso es que el experimento fue fallido.
Los reactivos tenían diferentes estados, ya que en el método espectrofotométrico usamos
un clavo lo menos oxidado posible mientras que en el titrimétrico fue un clavo no oxidado.
Esto pudo ocasionar menor velocidad de reacción y por lo tanto no podemos comparar
que método es mejor ya que se utilizaron diferentes estados del clavo, tal vez dejando
mucho más tiempo para tomar la alícuota en el método titrimétrico se pudieron haber
obtenido mejores resultados y un avance de reacción mayor como se nota en la gráfica
del método espectrofotométrico.
En el método espectrofotométrico se observan valores de concentración muy diferentes
ya que con respecto a la velocidad de reacción se confirma que la concentración
aumenta.
Cada uno de estos métodos son muy importantes ya que son métodos diferentes para
con ellos poder obtener la concentración.
Cruz Mendoza Raquel
2015321163
Se pudo cumplir el objetivo de esta práctica utilizando el método espectrofotométrico para
medir la concentración ya que este método tiene menor margen de error y es más rápido,
los pueden variar en este método si la celda no está bien seca, esto disminuye la
cancelación y obtendríamos un dato erróneo.
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
El método titrimétrico no dio buenos resultados ya que la solución estaba muy
contaminada.
Mota Garduño Victor Hugo
2014320599
El objetivo de la práctica se cumplió, ya que se pudo apreciar el avance de una reacción
por distintos métodos, y de ahí obtener parámetros medibles y contundentes para poder
establecer una relación de ellos con la cinética de esa misma reacción, Sin embargo, las
cuestiones enunciadas líneas más arriba, ponen de manifiesto los problemas que se
tuvieron para poder tener datos exactos.
Ramírez Martínez José Gerardo
2013320418
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
lOMoARcPSD|7718551
REFERENCIAS BIBLIOGRAFICAS
Skoog A.D. A Química Analítica
ISBN 7ta Edición
Ed. Mc Graw Hill México, 2003
Ayres HG Análisis Químico Cuantitativo
1ra Ed Harper &Row Publishers Inc.
Madrid 1970
DAY A.R. Jr. Química Analítica Cuantitativa
5ta Ed Pretence-hall hispanoamericana SA de CV
México, 1992
Harris C.D. Análisis Químico Cuantitativo
3ra Ed Grupo editorial Iberoamericana SA de CV
México 1992
WALTON F.H. Principios y método de análisis químico
2da Ed Reverte Mexicana SA
México 1970
Descargado por Carmona Jiménez Josué (xxxjoshuas117@gmail.com)
También podría gustarte
- Practica 1 CineticaDocumento16 páginasPractica 1 CineticaOmAr Aparicio Raw33% (3)
- Practica 10 EQUIPO 3 2IM44Documento16 páginasPractica 10 EQUIPO 3 2IM44Nadia Montero GonzálezAún no hay calificaciones
- Practicas AplicacionesDocumento39 páginasPracticas AplicacionesLiliana GonzálezAún no hay calificaciones
- Fotodegradacion de Anaranjado de Metilo Con Oxido de TitanioDocumento15 páginasFotodegradacion de Anaranjado de Metilo Con Oxido de Titaniousoppsky49100% (1)
- Practica 3 Obtencion Del Eter Metilnaftalico Equipo 7Documento9 páginasPractica 3 Obtencion Del Eter Metilnaftalico Equipo 7francisco rodriguezAún no hay calificaciones
- Practica 3 Termodinamica Del Equilibrio Quimico ESIQIE IPNDocumento9 páginasPractica 3 Termodinamica Del Equilibrio Quimico ESIQIE IPNAtax Mejia Medina50% (2)
- Reporte 10Documento19 páginasReporte 10alexadame2301100% (1)
- Reporte Practica 5 AplicacionesDocumento14 páginasReporte Practica 5 AplicacionesJesús Yair Mejía SánchezAún no hay calificaciones
- Termo 4 Práctica 2Documento10 páginasTermo 4 Práctica 2Erick Emma SánchezAún no hay calificaciones
- Practica 2. Organica Industrial Obtencion de La BenzoinaDocumento2 páginasPractica 2. Organica Industrial Obtencion de La BenzoinaOfelia RodriguezAún no hay calificaciones
- Practica 4 Reactores Homogeneos: INFLUENCIA DE LA CONCENTRACIÓN EN LA VELOCIDAD DE REACCIÓN EMPLEANDO COMO SISTEMA EL ALCOHOL ETILICO Y ACIDO CROMICODocumento7 páginasPractica 4 Reactores Homogeneos: INFLUENCIA DE LA CONCENTRACIÓN EN LA VELOCIDAD DE REACCIÓN EMPLEANDO COMO SISTEMA EL ALCOHOL ETILICO Y ACIDO CROMICOVanessa M.0% (2)
- Practica 6Documento11 páginasPractica 6Alfredo Enrique Vásquez GómezAún no hay calificaciones
- Practica No.6 Equiibrio Quimico SimultaneoDocumento7 páginasPractica No.6 Equiibrio Quimico SimultaneoAnnie Ávila100% (1)
- Practica 4 Cinética y Reactorés ESIQIEDocumento11 páginasPractica 4 Cinética y Reactorés ESIQIEAngell Glez Salgado100% (1)
- Practica No. 2 Cinetica y ReactoresDocumento10 páginasPractica No. 2 Cinetica y ReactoresEduardoQuirozCastilloAún no hay calificaciones
- Practica 3. Tubos AletadosDocumento9 páginasPractica 3. Tubos AletadosAlfredo Enrique Vásquez GómezAún no hay calificaciones
- ESIQIEDocumento5 páginasESIQIEAFachetiAún no hay calificaciones
- Practica 7 Termo 4Documento13 páginasPractica 7 Termo 4Luz María PeñafielAún no hay calificaciones
- Practica 1 PAC (2) Páginas 2,4 19Documento17 páginasPractica 1 PAC (2) Páginas 2,4 19Uriel LopezAún no hay calificaciones
- ESIQIE Práctica 5 Laboratorio Grupos Funcionales: Síntesis de BenzofenonaDocumento22 páginasESIQIE Práctica 5 Laboratorio Grupos Funcionales: Síntesis de BenzofenonaCesar Torres Boker50% (2)
- Obtencion Del Fenol, Equipo 7, 4IM53Documento13 páginasObtencion Del Fenol, Equipo 7, 4IM53Raul OrozcoAún no hay calificaciones
- Intercambiador VerticalDocumento8 páginasIntercambiador VerticalIrvin AdunaAún no hay calificaciones
- Reporte Practica 4 Aplicaciones EsiqieDocumento5 páginasReporte Practica 4 Aplicaciones EsiqieJesús Yair Mejía SánchezAún no hay calificaciones
- Práctica 2 - Cinética y Reactores HomogeneosDocumento16 páginasPráctica 2 - Cinética y Reactores HomogeneosVelázquez Aguilar Alan IgnacioAún no hay calificaciones
- Calculos Tubos Concentricos EsiqieDocumento4 páginasCalculos Tubos Concentricos EsiqieVanii Bellamy AllenAún no hay calificaciones
- Practica 5 Cinetica EsiqieDocumento8 páginasPractica 5 Cinetica EsiqieJesús Yair Mejía Sánchez100% (2)
- Practica 9 Obtencion Jabon Tocador 65690Documento13 páginasPractica 9 Obtencion Jabon Tocador 65690ALONSOAún no hay calificaciones
- Práctica 7 Quimica de Los Grupos FuncionalesDocumento14 páginasPráctica 7 Quimica de Los Grupos FuncionalesAngell Glez SalgadoAún no hay calificaciones
- Práctica 3 Equipo 6 Grupo 2IM47 Obtención de Un Shampoo Líquido Por Sulfatación Del Alcohol Láurico. Química de Grupos Funcionales PDFDocumento18 páginasPráctica 3 Equipo 6 Grupo 2IM47 Obtención de Un Shampoo Líquido Por Sulfatación Del Alcohol Láurico. Química de Grupos Funcionales PDFIrving Vazquez75% (4)
- Practica #2 Fuente Variable Regulada de Corriente Continua de 1.2-33VDocumento110 páginasPractica #2 Fuente Variable Regulada de Corriente Continua de 1.2-33VSebastián CastroAún no hay calificaciones
- Equilibrio Químico SimultaneoDocumento6 páginasEquilibrio Químico SimultaneoOscar Reyes Ruiz0% (1)
- Practica 3 Flujo Tubo RectoDocumento20 páginasPractica 3 Flujo Tubo RectoDaniel Alejandro Velazquez Toledo80% (5)
- Practica 5 Termodinamica Del Equilibrio QuimicoDocumento6 páginasPractica 5 Termodinamica Del Equilibrio QuimicoDiego SeCe100% (2)
- Tarea 12 EulerDocumento6 páginasTarea 12 EulerAngiells JessicaAún no hay calificaciones
- Practica 5Documento14 páginasPractica 5Ray AcostaAún no hay calificaciones
- Reporte 4 Cinetica y ReactoresDocumento8 páginasReporte 4 Cinetica y ReactoresIsrael Hernández MoralesAún no hay calificaciones
- LaboratoriosDocumento2 páginasLaboratoriosMau OrtegaAún no hay calificaciones
- Medidores de Flujo ESIQIEDocumento6 páginasMedidores de Flujo ESIQIEIrving RojasAún no hay calificaciones
- Practica Tuvo Recto EsiqieDocumento20 páginasPractica Tuvo Recto EsiqiePilar_Hernandez4Aún no hay calificaciones
- Practica 7 Termo 4Documento7 páginasPractica 7 Termo 4Iván Segura0% (2)
- Práctica 1 Rutinas de DiagnosticoDocumento15 páginasPráctica 1 Rutinas de DiagnosticoMau Mo100% (2)
- Practica 1 Cinetica FinDocumento21 páginasPractica 1 Cinetica FinAlfredoChritopherTorresCastilloAún no hay calificaciones
- Pract 3 ShampooDocumento7 páginasPract 3 ShampooCarito ParedesAún no hay calificaciones
- Practica No2 Balanza Analitica Ipn Esiqie AsDocumento6 páginasPractica No2 Balanza Analitica Ipn Esiqie AsAstrid Valverde DecaroAún no hay calificaciones
- Reporte 1 Dilucion de HierroDocumento13 páginasReporte 1 Dilucion de HierroIsrael Hernández MoralesAún no hay calificaciones
- Practica 6 Termo 4 TeoriaDocumento14 páginasPractica 6 Termo 4 TeoriaChristian Aquino100% (1)
- Practica - 10 - Dinitracion-2IM33-Equipo 1-Pareja 1Documento9 páginasPractica - 10 - Dinitracion-2IM33-Equipo 1-Pareja 1Pau AGAún no hay calificaciones
- Practica Determinación de Caídas de Presión en Tubo Recto y Accesorios.Documento18 páginasPractica Determinación de Caídas de Presión en Tubo Recto y Accesorios.Josselin Castro100% (2)
- Practica 6 Termo 4Documento5 páginasPractica 6 Termo 4Iván Segura0% (1)
- P8 Principios de Analisis CuantitativoDocumento16 páginasP8 Principios de Analisis CuantitativoNadia Montero GonzálezAún no hay calificaciones
- Tesina de TermodinamicaDocumento40 páginasTesina de TermodinamicaAlejandra Patsy Vázquez Ch100% (3)
- Condensador VerticalDocumento8 páginasCondensador VerticalIsaid Mendoza100% (1)
- Sin TítuloDocumento36 páginasSin TítuloDannie AstarothAún no hay calificaciones
- Práctica 4. Equilibrio Liquido - Vapor de Una Solucion No Ideal A Baja PresionDocumento20 páginasPráctica 4. Equilibrio Liquido - Vapor de Una Solucion No Ideal A Baja PresionPau AGAún no hay calificaciones
- Practica 3 PrincipiosDocumento4 páginasPractica 3 PrincipiosNadia Montero GonzálezAún no hay calificaciones
- Práctica 4 de Principios de Análisis CuantitativoDocumento4 páginasPráctica 4 de Principios de Análisis CuantitativoRay Acosta14% (7)
- Practica 3 Termo EsiqieDocumento33 páginasPractica 3 Termo Esiqier547Aún no hay calificaciones
- CRH - PRACTICA 1 (1) TerminadaDocumento21 páginasCRH - PRACTICA 1 (1) TerminadaAlondra Olvera GonzalezAún no hay calificaciones
- Informe-Acetato El BuenoDocumento13 páginasInforme-Acetato El BuenoNataliSotoRojasAún no hay calificaciones
- P3 - E4 - Cinetica de Reaccion Entre Cristal Violeta y NaOHDocumento23 páginasP3 - E4 - Cinetica de Reaccion Entre Cristal Violeta y NaOHLeslie Karina De León Sánchez100% (2)
- Actividad 3 Funciones Del Gerente de ProduccionDocumento6 páginasActividad 3 Funciones Del Gerente de ProduccionJosue CarmonaAún no hay calificaciones
- Con Dens AdoresDocumento17 páginasCon Dens AdoresJosue CarmonaAún no hay calificaciones
- Informe de Analisis Prac 3 CorrDocumento4 páginasInforme de Analisis Prac 3 CorrJosue CarmonaAún no hay calificaciones
- Con Dens AdoresDocumento17 páginasCon Dens AdoresJosue CarmonaAún no hay calificaciones
- Relacion de La Entropía y La Transferencia de CalorDocumento8 páginasRelacion de La Entropía y La Transferencia de CalorJosue Carmona50% (2)
- Diagrama de Bloques FOTODEGRADACION DE ANARANJADODocumento1 páginaDiagrama de Bloques FOTODEGRADACION DE ANARANJADOJosue CarmonaAún no hay calificaciones
- ETS Carmona Jimenez JosueDocumento4 páginasETS Carmona Jimenez JosueJosue CarmonaAún no hay calificaciones
- Actividad 4 Proceso de Ingenieria QuimicaDocumento11 páginasActividad 4 Proceso de Ingenieria QuimicaJosue CarmonaAún no hay calificaciones
- 8388 11890 1 PBDocumento14 páginas8388 11890 1 PBDaniel Pulido RojasAún no hay calificaciones
- Tarea 8 Minimos Cuadrados MultivariableDocumento7 páginasTarea 8 Minimos Cuadrados MultivariableJosue CarmonaAún no hay calificaciones
- Minimos Cuadrados Multivariable Ejercicios ResueltosDocumento7 páginasMinimos Cuadrados Multivariable Ejercicios ResueltosJosue Carmona100% (1)
- Ajuste MultivariableDocumento2 páginasAjuste MultivariableJosue CarmonaAún no hay calificaciones
- Minimos CuadradosDocumento6 páginasMinimos CuadradosJosue CarmonaAún no hay calificaciones
- Exponencial Minimos Cuadrados Univariable 1Documento4 páginasExponencial Minimos Cuadrados Univariable 1Josue CarmonaAún no hay calificaciones
- Minimos CuadradosDocumento6 páginasMinimos CuadradosJosue CarmonaAún no hay calificaciones
- TAREA 7 Exponencial Minimos Cuadrados Univariable 1Documento4 páginasTAREA 7 Exponencial Minimos Cuadrados Univariable 1Josue CarmonaAún no hay calificaciones
- PracticaDocumento10 páginasPracticaMariana Luna HdezAún no hay calificaciones
- Practica 7 Determinacion de La Curva de TitulacionDocumento9 páginasPractica 7 Determinacion de La Curva de TitulacionJosue CarmonaAún no hay calificaciones
- Practica 1 Lab PAC PDFDocumento7 páginasPractica 1 Lab PAC PDFJosue CarmonaAún no hay calificaciones
- Fórmulas de Simpson 1Documento1 páginaFórmulas de Simpson 1Josue CarmonaAún no hay calificaciones
- Minimos CuadradosDocumento7 páginasMinimos CuadradosJosue CarmonaAún no hay calificaciones
- Vertedor Parshall CalculosDocumento2 páginasVertedor Parshall CalculosJosue CarmonaAún no hay calificaciones
- Diagrama de Bloques Practica 4Documento1 páginaDiagrama de Bloques Practica 4Josue CarmonaAún no hay calificaciones
- Carbaniones ResumenDocumento3 páginasCarbaniones ResumenJosue CarmonaAún no hay calificaciones
- Diagrama de BloquesDocumento1 páginaDiagrama de BloquesJosue CarmonaAún no hay calificaciones
- Carbaniones ResumenDocumento3 páginasCarbaniones ResumenJosue CarmonaAún no hay calificaciones
- FactibilidadDocumento1 páginaFactibilidadJosue CarmonaAún no hay calificaciones
- Metodo de MohrDocumento9 páginasMetodo de MohrJosue CarmonaAún no hay calificaciones
- Diagrama Industrial AnilinaDocumento1 páginaDiagrama Industrial AnilinaJosue CarmonaAún no hay calificaciones
- Diagrama Industrial Practica 3 Diels AlderDocumento1 páginaDiagrama Industrial Practica 3 Diels AlderJosue CarmonaAún no hay calificaciones
- Ejercicios Dados Por El Arcángel Miguel para SerDocumento3 páginasEjercicios Dados Por El Arcángel Miguel para SerGuadalupe Miranda Gomez100% (1)
- Glosario de Marketing DigitalDocumento3 páginasGlosario de Marketing DigitalAlma JiménezAún no hay calificaciones
- Servicios SETECDocumento4 páginasServicios SETECedgar_estrada86_8012100% (2)
- Estructura Trabajo en Final Uci Adulto CoDocumento58 páginasEstructura Trabajo en Final Uci Adulto CoBrayan AlvarezAún no hay calificaciones
- El Fraude en La Ciencia. El Caso HwangDocumento8 páginasEl Fraude en La Ciencia. El Caso HwangAndrea Marcela AguirreAún no hay calificaciones
- Trabajo de Nuevo TestamentoDocumento5 páginasTrabajo de Nuevo TestamentoJimmy Fabian Acosta LunaAún no hay calificaciones
- El Sermón Del MonteDocumento7 páginasEl Sermón Del MonteQuispe Tintaya MoisésAún no hay calificaciones
- Taller de Investigacion BTDocumento15 páginasTaller de Investigacion BTDíaz MadeleineAún no hay calificaciones
- Triptico HistoriaDocumento2 páginasTriptico HistoriaJhunior Rodriguez Zambrano100% (1)
- Opinión Personal MotivacionDocumento1 páginaOpinión Personal MotivacionDani FreemanAún no hay calificaciones
- Diviones TanajDocumento2 páginasDiviones TanajHector del PeruAún no hay calificaciones
- Guia de Prototipado Emprendimiento Inclusivo Compressed 1 PDFDocumento70 páginasGuia de Prototipado Emprendimiento Inclusivo Compressed 1 PDFNelson Muñoz CerdaAún no hay calificaciones
- Bases Sociales y Culturales de La Educación SexualDocumento18 páginasBases Sociales y Culturales de La Educación SexualGrecia OrdazAún no hay calificaciones
- Vision de Mi Mismo - GedeonDocumento3 páginasVision de Mi Mismo - GedeonLUIS VILLALBAAún no hay calificaciones
- Elementos Constitutivos Del TributoDocumento8 páginasElementos Constitutivos Del TributoRonny Labrador100% (3)
- Level 3 T1 Desafíos Leer EscribirDocumento2 páginasLevel 3 T1 Desafíos Leer EscribirLuke GiglioAún no hay calificaciones
- Semana 3 CaDocumento5 páginasSemana 3 Camaria barrios78% (9)
- Rubrica-Ingles Vii HechoDocumento1 páginaRubrica-Ingles Vii HechoCrusvel Silva MedallaAún no hay calificaciones
- Kiyoshi Suzaki Gestion VisualDocumento3 páginasKiyoshi Suzaki Gestion VisualjocelynAún no hay calificaciones
- Informe de Servicio - 330-Kel11251Documento85 páginasInforme de Servicio - 330-Kel11251IBHET YHARIZA CRISPIN FLORESAún no hay calificaciones
- Agencia Metropolitana de TránsitoDocumento8 páginasAgencia Metropolitana de TránsitoKodi KodiAún no hay calificaciones
- Ética e Inteligencia Artificial - IA LatamDocumento16 páginasÉtica e Inteligencia Artificial - IA LatamSacrilegio SacrilexAún no hay calificaciones
- Actividad de Aprendizaje #1 Simbología Eléctrica para Control de Motores EléctricosDocumento1 páginaActividad de Aprendizaje #1 Simbología Eléctrica para Control de Motores EléctricosGilmer Bejarano EulogioAún no hay calificaciones
- Taller Simbolización de Argumentos Deductivos TEODocumento6 páginasTaller Simbolización de Argumentos Deductivos TEOSergio Pinchao0% (1)
- BiologiaDocumento180 páginasBiologiaAna UrbinaAún no hay calificaciones
- Raza, Etnia, Prejuicios, Estereotipos, Discriminación, Racismo, MinoríasDocumento4 páginasRaza, Etnia, Prejuicios, Estereotipos, Discriminación, Racismo, MinoríasStephanie Carolina MesaAún no hay calificaciones
- 1 - ACTIVIDAD - Introducción y Marco Legal Medicina Preventiva.Documento3 páginas1 - ACTIVIDAD - Introducción y Marco Legal Medicina Preventiva.PAOLAAún no hay calificaciones
- 008 Psiorg Sandra VargasDocumento3 páginas008 Psiorg Sandra VargasPilarGMAún no hay calificaciones
- Tarea 2 Mecanica Cuantica IIDocumento6 páginasTarea 2 Mecanica Cuantica IIDaniel Felipe Afanador RodriguezAún no hay calificaciones
- Esquema Período ClásicoDocumento2 páginasEsquema Período ClásicoIus-tavo ChaicojAún no hay calificaciones