Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Prev 6
Cargado por
Gabriela HernandezDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Prev 6
Cargado por
Gabriela HernandezCopyright:
Formatos disponibles
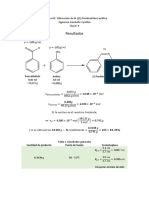
OBTENCIN DE p-NITROANILINA (NITRACIN E HIDRLISIS DE ACETANILIDA) Objetivo: Que el alumno efecte una reaccin de nitracin en el anillo de una amina
aromtica protegida como acetil derivado y elimine la proteccin por hidrlisis alcalina, como ejemplo del uso del concepto de grupo protector Investigacin Previa: Condiciones experimentales para nitrar una amina aromtica y diferentes agentes nitrantes La nitracin se origina ordinariamente tratando el compuesto aromtico con una mezcla de cido ntrico y sulfrico concentrado. + El agente nitrante es el in nitronio cargado positivamente (NO2) . El cido ntrico puede reaccionar consigo mismo de modo anlogo, por lo cual puede actuar por si solo como agente nitrante, aunque nicamente frente a determinados compuestos aromticos como el fenol Efecto del grupo acetamido en la reactividad y orientacin del anillo aromtico. El grupo acetamido es un grupo activante y en compuestos aromticos, se suele sobreentender que se refiere a activacin con respecto a la reaccin SEA. El mecanismo SEA en la anilina, explica mediante el modelo de resonancia la propiedad activante del grupo amino, y su condicin de orientador orto/para Indique qu ocurre si se nitra la anilina directamente. El mecanismo de la nitracin de la acetanilida es que un ion nitronio de la mezcla es el que efecta el ataque electroltico en el ncleo aromtico. La nitracin directa de la anilina y de otras aminas en solucin de cido sulfrico concentrado origina generalmente una mezcla de productos resinosos coloreados a menos que la solucin se diluya con un considerable exceso de cido sulfrico concentrado. En estas ltimas condiciones la nitracin de la acetanilida, suministra una mezcla de las 3 nitroacetanilidas ismeras (o, m y p).La nitracin directa de la anilina origina generalmente una mezcla de productos resinosos coloreados para obtener el ismero Para generalmente se refiere 2 etapas: 1. Nitracin de la Acetanilida2. 2. Hidrlisis de la Para- Nitroacetanilida a p -nitroanilida. Condiciones experimentales para efectuar la hidrlisis de amidas y mecanismo de reaccin. Las amidas se convierten por hidrlisis en cidos carboxlicos. La reaccin se puede realizar tanto en medios cidos como bsicos fuertemente concentrados y requiere calentar durante varias horas. Estas condiciones tan drsticas son necesarias dada escasa reactividad de las amidas frente a los ataques nuclefilos, debida principalmente a la cesin el par solitario del nitrgeno. Hidrlisis cida de amidas Las amidas se hidrolizan en medios cidos, bajo calefaccin, formando aminas y cidos carboxlicos.
La etanamida [1] se hidroliza en medio sulfrico para formar el cido etanoico [2].
El mecanismo de la reaccin transcurre en los siguientes pasos: Etapa 1. Protonacin del oxgeno carbonlico.
Etapa 2. Ataque nuclefilo del agua al carbono carbonilo
Etapa 3. Desprotonacin del agua y protonacin del grupo amino.
Etapa 4. Eliminacin de amoniaco
Etapa 5. Desprotonacin del oxgeno carbonlico
Hidrlisis bsica de amidas Las amidas se transforman en aminas y cidos carboxlicos por tratamiento con sosa acuosa bajo calefaccin.
La etanamida [1] se hidroliza en presencia de sosa acuosa, para formar etanoato de sodio [2]. El mecanismo de la reaccin transcurre en los siguientes pasos:
Etapa 1. Ataque nuclefilo
Etapa 2. Eliminacin
Etapa 3. Equlibrio cido base desplazado.
Indique otros agentes acetilantes de aminas. Los halogenuros de acilo, los cloruros y anhdridos de cido son usados comnmente como agentes acilantes para acilar aminas para formar amidas El cido succnico tambin es usado comnmente para un tipo especfico de acilacin denominado succinacin. Investigue mecanismos de reaccin involucrados en la prctica Etapa1: Reaccin de acetilacin
Etapa 2: Nitracin de acetanilida
Etapa 3: Nitracin de acetanilida
Investigue propiedades generales de aminas y amidas Amina: Las aminas son compuestos qumicos orgnicos que se consideran como derivados del amonaco y resultan de la sustitucin de los hidrgenos de la molcula por los radicales alquilo. Son compuestos con geometra piramidal. Presentan quiralidad aunque se encuentran en forma de racematos. Segn se sustituyan uno, dos o tres hidrgenos, las aminas sern primarias, secundarias o terciarias, respectivamente. Las aminas son compuestos muy polares. Las aminas primarias y secundarias pueden formar puentes de hidrgeno. Las aminas terciarias puras no pueden formar puentes de hidrgeno, sin embargo pueden aceptar enlaces de hidrgeno con molculas que tengan enlaces O-H o N-H. Las aminas primarias y secundarias tienen puntos de ebullicin menores que los de los alcoholes, pero mayores que los de los teres de peso molecular semejante. Las aminas terciarias, sin puentes de hidrgeno, tienen puntos de ebullicin ms bajos. Las aminas se comportan como bases a travs del par libre del nitrgeno. Tambin se comportan como cidos dbiles pudiendo desprotonarlas mediante el empleo de bases muy fuertes Amida: Una amida es un compuesto orgnico que consiste en una amina unida a un grupo acilo convirtindose en una amina cida. Se puede considerar como un derivado de un cido carboxlico por sustitucin del grupo OH del cido por un grupo NH2, NHR o NRR'. Son slidas a temperatura ambiente y sus puntos de ebullicin son elevados, ms altos que los de los cidos correspondientes. Presentan excelentes propiedades disolventes y son bases muy dbiles
Clculos de rendimiento Para calcular el rendimiento de una reaccin ha de tenerse en cuenta qu cantidad de producto se ha obtenido al final de la reaccin y cunto debera haberse producido en condiciones ideales (tericas). En qumica, el rendimiento, tambin referido como rendimiento qumico y rendimiento de reaccin, es la cantidad de producto obtenido en una reaccin qumica. El rendimiento absoluto puede ser dado como la masa en gramos o en moles (rendimiento molar). El rendimiento fraccional o rendimiento relativo o rendimiento porcentual, que sirve para medir la efectividad de un procedimiento de sntesis, es calculado al dividir la cantidad de producto obtenido en moles por el rendimiento terico en moles. Uno o ms reactivos en una reaccin qumica suelen ser usados en exceso. El rendimiento terico es calculado basado en la cantidad molar del reactivo limitante, tomando en cuenta la estequiometra de la reaccin. Para el clculo, se suele asumir que hay una sola reaccin involucrada Bibliografa Morrison, Robert Thornton. Qumica Orgnica. Ed. Addison-Wesley Iberoamericana, ed. 5, p.c 917-925 Ralph J. Fessenden y Joan S. Fessenden. Qumica Orgnica. Ed. Grupo Editorial Iberoamrica, ed. 2, p.c 605608 Prof. Hans Beyer. Manual de Qumica Orgnica. Ed. Reverte S.A, ed. 10, p.c 608-610
OBTENCIN DE P-NITROANILINA
Filtracin de acetanilida:
En un vaso de pp. coloque 1.25ml de cido actico glacial y luego 1.35g de acetanilida
Agitar y adicionar 2.5ml de H2SO4(cc)
Enfriar la mezcla en un bao de hielo-sal hasta una temperatura de 0-5C
Agregar gota a gota y agitando 0.75ml de HNO3
Despus de agragar todo el cido, la mezcla de reaccin se saca del hielo y se deja a temperatura ambiente por 10min
Vertir la solucin en 25ml de agua, precipitando el producto, filtrar, lavar y secar
Hidrlisis de la p-nitroacetanilida:
Los cristales obtenidos se colocan en un matraz de bola y se agregan 6ml de etanol y una solucin de 1.5g de NaOH en 4ml de agua
Se coloca el condensador en posicin de reflujo y se calienta en bao mara durante 10min
Se vierte la solucin en un vaso de pp. que contenga 10-15g de hielo y se enfra en un bao de hielo para que cristalice
Se filtra y se baja con las aguas madres el slido que queda adherido
Se lava con agua helada, se seca y recristaliza de etanol-agua
Determinar punto de fusin
También podría gustarte
- Informe 2 B NerolinaDocumento3 páginasInforme 2 B NerolinaVictor PerezAún no hay calificaciones
- Reporte Ácido FenoxiáceticoDocumento3 páginasReporte Ácido FenoxiáceticotertbutilAún no hay calificaciones
- AcetanilidaDocumento7 páginasAcetanilidaLiLiana Niño100% (1)
- AzocompuestosDocumento11 páginasAzocompuestosIsabel Centeno100% (1)
- Rio PREVIO 4 Fenolftaleina y Fluoresce in ADocumento5 páginasRio PREVIO 4 Fenolftaleina y Fluoresce in AJose Antonio Silva100% (9)
- Previo Ácido FenoxiacéticoDocumento6 páginasPrevio Ácido FenoxiacéticoJosh Tapia MuciñoAún no hay calificaciones
- BenzoínaDocumento13 páginasBenzoínadany_289Aún no hay calificaciones
- Ácido PícricoDocumento2 páginasÁcido PícricoViiry Salazar75% (4)
- Reporte de Ácido BencílicoDocumento5 páginasReporte de Ácido BencílicoZoledad Tavera100% (1)
- Previo Acido CinamicoDocumento9 páginasPrevio Acido CinamicoJose Emmanuel ChemaAún no hay calificaciones
- Azocompuestos Anaranjado de MetiloDocumento8 páginasAzocompuestos Anaranjado de MetiloChristian MontielAún no hay calificaciones
- Formación de PirazolonasDocumento4 páginasFormación de PirazolonasAdrian PIAún no hay calificaciones
- Reporte 5 PirazolonasDocumento4 páginasReporte 5 PirazolonasAnonymous enA4SSAún no hay calificaciones
- Síntesis de 2,4-Dietoxicarbonil 3,5 DimetilpirrolDocumento25 páginasSíntesis de 2,4-Dietoxicarbonil 3,5 DimetilpirrolEdgar ArmandoAún no hay calificaciones
- Ácido Pícrico-PrevioDocumento2 páginasÁcido Pícrico-PrevioScrolla BerserkerAún no hay calificaciones
- PirazolonasDocumento7 páginasPirazolonasFanny Venado HernandezAún no hay calificaciones
- Síntesis de DibenzalacetonaDocumento42 páginasSíntesis de DibenzalacetonaRoberto Viramontes100% (2)
- Previo para P-NitroanilinaDocumento10 páginasPrevio para P-NitroanilinaCarlos CastilloAún no hay calificaciones
- Acido Fenoxiacetico Previo y ReporteDocumento5 páginasAcido Fenoxiacetico Previo y Reportebrayan gutierrezAún no hay calificaciones
- Previo 4 M-NitroanilinaDocumento5 páginasPrevio 4 M-NitroanilinaAlan100% (3)
- Reporte - β-NerolinaDocumento4 páginasReporte - β-NerolinaKarla GarcíaAún no hay calificaciones
- Previo BenciloDocumento6 páginasPrevio BenciloHeber Daniel Andrade Rivera100% (1)
- Reporte DibenzalacetonaDocumento2 páginasReporte DibenzalacetonaluisAún no hay calificaciones
- Acido Picrico ReporteDocumento3 páginasAcido Picrico ReportePaul ValdezAún no hay calificaciones
- Síntesis de Alcohol Bencilico y Ácido BenzoicoDocumento35 páginasSíntesis de Alcohol Bencilico y Ácido BenzoicoGabrielVazquezOlvera100% (2)
- Obtencion de N - Z - Fenilmetilen AnilinaDocumento5 páginasObtencion de N - Z - Fenilmetilen AnilinaJuanDavidPBAún no hay calificaciones
- Reporte #6 - AcetanilidaDocumento3 páginasReporte #6 - AcetanilidaAna Karen Rodríguez ReyesAún no hay calificaciones
- Obtención Del Epóxido de Menadiona Apertura de 2-Metil-2,3-Epoxi-1,2-NaftoquinonaDocumento5 páginasObtención Del Epóxido de Menadiona Apertura de 2-Metil-2,3-Epoxi-1,2-NaftoquinonaAndres Polina ZuñigaAún no hay calificaciones
- Bencilo ReporteDocumento2 páginasBencilo ReporteDavid Ramirez50% (2)
- Practica 4 Condensación de Claisen-Schmidt. Obtencion de DibenzalacetonaDocumento18 páginasPractica 4 Condensación de Claisen-Schmidt. Obtencion de DibenzalacetonaLizeth Paola TellezAún no hay calificaciones
- B NerolinaDocumento10 páginasB NerolinaDiana MoedanoAún no hay calificaciones
- Previo 2-NitrotiofenoDocumento5 páginasPrevio 2-NitrotiofenoEdgar Armando100% (5)
- Condensación AldólicaDocumento7 páginasCondensación AldólicaGianfrancoAún no hay calificaciones
- Previo Difenil CarbinolDocumento7 páginasPrevio Difenil CarbinolOscar Correa100% (1)
- Cuestionario CanizzaroDocumento3 páginasCuestionario CanizzaroDalia Felix LopezAún no hay calificaciones
- DicinamalacetonaDocumento4 páginasDicinamalacetonaFanny Venado HernandezAún no hay calificaciones
- PRÁCTICA No. 4: OBTENCIÓN DE 5,5-DIFENILHIDANTOINADocumento7 páginasPRÁCTICA No. 4: OBTENCIÓN DE 5,5-DIFENILHIDANTOINADiana HMAún no hay calificaciones
- PREVIO6 PnitroanilinaDocumento7 páginasPREVIO6 PnitroanilinaLiLiana Niño100% (1)
- Previo de Orgánica P-NitroanilinaDocumento12 páginasPrevio de Orgánica P-NitroanilinaAngeles MendezAún no hay calificaciones
- P NitronilinaDocumento5 páginasP NitronilinaAdriana MarinAún no hay calificaciones
- Practica 1 Sintesis ParanitroanilinaDocumento5 páginasPractica 1 Sintesis ParanitroanilinaRocio100% (1)
- Sintesis de ParanitroanilinaDocumento2 páginasSintesis de ParanitroanilinaYara Hernandez0% (1)
- NitrotiofenoDocumento3 páginasNitrotiofenoGaby RodriguezAún no hay calificaciones
- Practica 4 Sintesis de Alcohol Bencilico y Acido BenzoicoDocumento5 páginasPractica 4 Sintesis de Alcohol Bencilico y Acido BenzoicoLiz RivasAún no hay calificaciones
- Reporte Practica 2 - Sintesis de AzocompuestosDocumento7 páginasReporte Practica 2 - Sintesis de AzocompuestosNicte Llanes0% (1)
- Muestra de Reporte. Síntesis de Colorante Azoico Sudan IDocumento3 páginasMuestra de Reporte. Síntesis de Colorante Azoico Sudan IIelena Bloox0% (1)
- Previo 6 Sintesis de Hantzsch para PiridinasDocumento3 páginasPrevio 6 Sintesis de Hantzsch para PiridinasJulio Cesar Venegas Muñoz50% (2)
- Investigacion Previa BenciloDocumento2 páginasInvestigacion Previa BenciloEve TenorioAún no hay calificaciones
- 2 NitrotiofenoDocumento5 páginas2 NitrotiofenoBrayan HEAún no hay calificaciones
- Obtencion de FurfuralDocumento3 páginasObtencion de FurfuralAdrian PIAún no hay calificaciones
- Reporte Práctica 10-Transposición BencílicaDocumento5 páginasReporte Práctica 10-Transposición BencílicaAndy Aldama100% (1)
- Difenil Carbinol Alumno FES-C V 2ggDocumento4 páginasDifenil Carbinol Alumno FES-C V 2ggDanGodAlvAún no hay calificaciones
- Previo HidantoínasDocumento9 páginasPrevio HidantoínasUriel RamosAún no hay calificaciones
- Previo Condensación AldolicaDocumento7 páginasPrevio Condensación AldolicaRodrigo Colin100% (1)
- Cuantificación Del Grado de Pureza Del Ácido AcéticoDocumento9 páginasCuantificación Del Grado de Pureza Del Ácido AcéticoFernanda GómezAún no hay calificaciones
- Organo Pre VioDocumento17 páginasOrgano Pre VioJonathan VillafañeAún no hay calificaciones
- Reporte Benzoína Bencilo Acido BencilicoDocumento3 páginasReporte Benzoína Bencilo Acido BencilicoAlan0% (1)
- Informe de Azlactona 2017Documento14 páginasInforme de Azlactona 2017yamily888Aún no hay calificaciones
- Practica 1-Obtencion de P-NitroanilinaDocumento10 páginasPractica 1-Obtencion de P-Nitroanilinassmrn100% (1)
- Informe de Azlactona 2017Documento14 páginasInforme de Azlactona 2017yamily888Aún no hay calificaciones
- Determinación de LA SATURACIÓN de AGUA Diagramas de StiffDocumento8 páginasDeterminación de LA SATURACIÓN de AGUA Diagramas de StiffJhonatan Chacon GutierrezAún no hay calificaciones
- Practica #5 QuímicaDocumento2 páginasPractica #5 QuímicaEduardo RubinAún no hay calificaciones
- P-3 Cuantitativa Ácidos en Medio No AcuosoDocumento43 páginasP-3 Cuantitativa Ácidos en Medio No AcuosoBC NandoAún no hay calificaciones
- Tabla de Aniones y CationesDocumento2 páginasTabla de Aniones y CationesEmmi Visant SandovalAún no hay calificaciones
- Articulo QuimicaDocumento9 páginasArticulo QuimicaSantiago ChagualaAún no hay calificaciones
- Quimica Mi Espe Evaluacion 2 ParcialDocumento4 páginasQuimica Mi Espe Evaluacion 2 ParcialKlever AcaroAún no hay calificaciones
- Tema de TesisDocumento18 páginasTema de TesisJose Carlos Huamani QuicañoAún no hay calificaciones
- Los Compuestos InorgánicosDocumento11 páginasLos Compuestos InorgánicosJosue GonzalezAún no hay calificaciones
- Composición LemongrassDocumento69 páginasComposición LemongrassbrayansagAún no hay calificaciones
- Práctica 14 - Digestión 2022Documento44 páginasPráctica 14 - Digestión 2022Ale QYAún no hay calificaciones
- Cert. Metales Pesados - PEBDDocumento2 páginasCert. Metales Pesados - PEBDJackeline Serrano Del CarpioAún no hay calificaciones
- Cuestionario TP1 - Revisión Del IntentoDocumento21 páginasCuestionario TP1 - Revisión Del IntentoGianella DagunAún no hay calificaciones
- SINTESIS de Williamson (Obtencion de Acido FenoxiaceticoDocumento16 páginasSINTESIS de Williamson (Obtencion de Acido Fenoxiacetico.:("*"BLacK BuLLeT"*"):.93% (28)
- Taller Quimica OrganicaDocumento25 páginasTaller Quimica OrganicaSantiago España GutierrezAún no hay calificaciones
- Reporte de La Práctica de Ácido BenzoicoDocumento3 páginasReporte de La Práctica de Ácido BenzoicoRamses DRHOAún no hay calificaciones
- Cálculos Balance de Energía Del Proceso de Tostación de Concentrados de Sulfuro de Zinc 1Documento5 páginasCálculos Balance de Energía Del Proceso de Tostación de Concentrados de Sulfuro de Zinc 1Jose CarlosAún no hay calificaciones
- DESASFALTIZACIONDocumento40 páginasDESASFALTIZACIONHernan ArizaAún no hay calificaciones
- Protocolo Emulsión - Equipo 5Documento31 páginasProtocolo Emulsión - Equipo 5JORGE OMAR CABALLERO CAMPOS100% (1)
- Actividad 1Documento2 páginasActividad 1Manuel MesonesAún no hay calificaciones
- Ejercicios 1 y 2 PDFDocumento16 páginasEjercicios 1 y 2 PDFGelber GarcíaAún no hay calificaciones
- Alcohol IsopropilicoDocumento25 páginasAlcohol IsopropilicoLizbeth GalvanAún no hay calificaciones
- Unidad 5. Soluciones AcuosasDocumento10 páginasUnidad 5. Soluciones AcuosasMelissa Alejandra Sanhueza ArévaloAún no hay calificaciones
- Tema: Caracteristica Fisicoquimica, Sensorial Y Funcional Del Yogurt de Noni Y Arandano Usando Stevia Como EndulcoranteDocumento4 páginasTema: Caracteristica Fisicoquimica, Sensorial Y Funcional Del Yogurt de Noni Y Arandano Usando Stevia Como EndulcoranteMelissa Rivera CaballeroAún no hay calificaciones
- Refinación y FundiciónDocumento5 páginasRefinación y FundiciónEdwin Huacanchi SotoAún no hay calificaciones
- Prelab 1 QDocumento18 páginasPrelab 1 Qapi-576334472Aún no hay calificaciones
- IMcehudDocumento117 páginasIMcehudangeloAún no hay calificaciones
- Proyecto Cientifico de JabonesDocumento75 páginasProyecto Cientifico de JabonesEmmy LimaAún no hay calificaciones
- Titulacion Acido-BaseDocumento12 páginasTitulacion Acido-BaseEmiliano RodríguezAún no hay calificaciones
- 4ta Clase 2016Documento15 páginas4ta Clase 2016SergioMachadoGarciaAún no hay calificaciones