Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ace Ton A
Ace Ton A
Cargado por
Jossi Maggali Soriano PomayaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ace Ton A
Ace Ton A
Cargado por
Jossi Maggali Soriano PomayaCopyright:
Formatos disponibles
UNIDAD 2
ALDEHDOS Y CETONAS
UNIDAD 2 ALDEHDOS Y CETONAS
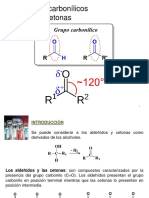
Aldehdos y cetonas son los compuestos carbonlicos ms simples, las cetonas en su estructura cuentan con dos grupos alquilo o arilo enlazados. Dichos compuestos son similares en estructura y tienen propiedades parecidas, sin embargo tienen algunas diferencias en su reactividad. En la mayora de los casos, los aldehdos son ms reactivos que las cetonas, esto se ver en el transcurso de esta unidad.
2.1 NOMENCLATURA DE ALDEHDOS Y CETONAS
2.1.1 Aldehdos Segn la UIQPA se toma la cadena ms larga que contiene el C del grupo CHO y se sustituye la terminacin o del alcano por el sufijo -al. El C del CHO es el nmero uno. Para los compuestos con dos grupos CH=O, al nombre del alcano se le aade el sufijo dial. Cuando otros grupos funcionales tienen prioridad en la nomenclatura, el grupo CHO se denomina formilo. Los nombres comunes sustituyen el sufijo ico (oico u oxlico) y la palabra cido de los cidos carboxlicos correspondientes por -aldehdo. La posicin de los sustituyentes en las cadenas se designa con letras griegas; como se ejemplifica a continuacin:
C C
C C
C C O
El carbono terminal de una cadena larga se denomina por (omega). Enseguida se muestran algunos nombres comunes de aldehdos.
O H C H
O H3C C H
H3C CH2
acetaldehdo
O C H
propionaldehdo
formaldehdo
Portillo Alva Benjamn, Leticia Coln Izquierdo.
37
UNIDAD 2
ALDEHDOS Y CETONAS
O
O CH3 CH2 CH2 C H
benzaldehdo
butiraldehdo
El compuesto se nombra como aldehdo (o carbaldehdo) cuando el CHO est unido a un anillo aromtico. Ejemplos:
O
O butanal (butiraldehdo) 2-metilbutanal (alfa-metilbutiraldehdo)
OH 3hidrohi-3metil pentanal (beta-hidroxi,beta-metil valrico)
OHCCH2CH2CH2CH(CH3)CHO
2-metil-1-6-hexanodial
CHO
3-ciclohexenocarbaldehdo
2.1.2 Cetonas
Para nombrar las cetonas, segn el sistema UIQPA, tambin se consideran derivados de los alcanos, por consiguiente, se sustituye la terminacin o del alcano por la terminacin ona; as, del propano se origina la propanona. Se debe fijar la posicin del carbono donde est la funcin carbonlica por lo que se debe dar el menor nmero en la numeracin de la cadena principal. Para nombrar a las cetonas por el nombre comn, se indican los nombres de los grupos alifticos o aromticos unidos al carbono carbonilo, seguido de la palabra cetona. Ejemplos:
O O O CH3 Br
1-bromo-2-metil-3-pentanona etil(1-bromo)isopropilcetona
1-fenil-1-propanona (etilfenilcetona)
3-metilciclopentanona
CH3
Portillo Alva Benjamn, Leticia Coln Izquierdo.
38
UNIDAD 2
ALDEHDOS Y CETONAS
CCH3 O C
OH
acetofenona (fenilmetilcetona) benzofenona (difenilcetona)
4-hidroxi-4-metil-2-hexanona (2-hidroxi-2-metil) butil-metilcetona
2.2 CARACTERSTICAS DEL GRUPO CARBONILO
Estructura del grupo carbonilo
El grupo funcional
C O
se conoce con el nombre de funcin carbonlica. Existe un
gran nmero de compuestos orgnicos importantes que contienen en su estructura esta funcin tales como los aldehdos, las cetonas, los cidos, los derivados de cido como steres, haluros de acilo, amidas y anhdridos. En los aldehdos y las cetonas, esta funcin reacciona como tal, es decir, presenta una serie de reacciones especficas, mientras que en los dems compuestos no reacciona como grupo carbonilo, por encontrarse interferido por otros grupos y no reacciona por s sola, sino que forman otras funciones. En esta unidad se hace referencia al estudio de las dos estructuras, aldehdo y cetona. La primera de stas muestra un hidrgeno unido al carbono carbonilo y su frmula estructural se representa como RCHO (no R-COH), mientras que las cetonas en lugar del hidrgeno se unen ya sea a un grupo alquilo o arilo; su frmula general se designa como RCOR, en donde R puede ser un grupo alquilo o arilo. En los aldehdos, la funcin es terminal sobre un carbono primario y en las cetonas se presenta en un carbono secundario.
O R C
aldehdo
O
H
C
cetona
El grupo carbonilo es planar; esto significa que los tomos de oxgeno, carbono carbonilo, y los dos tomos unidos a l (el hidrgeno y el carbono en el caso del
Portillo Alva Benjamn, Leticia Coln Izquierdo.
39
UNIDAD 2
ALDEHDOS Y CETONAS
aldehdo y los dos carbonos vecinales al C de la funcin en las cetonas) estn en el mismo plano. Es decir, los enlaces entre estos tomos corresponden a un ngulo de 120.
Grupo carbonilo planar
El grupo carbonilo est polarizado. La presencia del oxgeno, ms electronegativo que el carbono, hace que tienda a desplazarse la densidad electrnica de la molcula y los electrones del grupo carbonilo hacia su ncleo, rodendose de una mayor densidad electrnica, y creando una dbil carga positiva sobre el carbono alfa, vecino al carbono carbonilo.
electrones "pi"
C C1 C2 O
C C C O
Polarizacin del grupo carbonilo
Por efecto inductivo del oxgeno, el carbono alfa, origina una carga positiva; esto hace que los hidrgenos unidos a l sean de carcter cido. El carbono positivamente, hace que el H+ unido a l, se rechace, se debilite el enlace y pueda fcilmente ser abstrado por bases como el hidrxido de sodio.
2.3 PROPIEDADES FSICAS DE ALDEHDOS Y CETONAS
El grupo carbonilo es un grupo polar, por tanto, los aldehdos y las cetonas poseen temperaturas de ebullicin mayores que las de los hidrocarburos del mismo peso
Portillo Alva Benjamn, Leticia Coln Izquierdo.
40
UNIDAD 2
ALDEHDOS Y CETONAS
molecular. Aunque debido a que aldehdos y cetonas no pueden formar enlaces de hidrgeno fuertes entre sus molculas, tienen temperaturas menores que los alcoholes correspondientes. El tomo del oxgeno del carbonilo permite que las molculas de aldehdos y cetonas formen enlaces de hidrgeno fuertes con las molculas de agua. Como resultado los aldehdos y cetonas de bajo peso molecular, presentan solubilidades apreciables en agua. La cetona y el acetaldehdo se disuelven en agua en cualquier proporcin. Por su polaridad, los aldehdos y cetonas son solubles en solventes polares como el H2O y solventes orgnicos. Las molculas de alto peso molecular son poco o no solubles en agua, tienen olores y sabores caractersticos. Los miembros entre 8 y 14 tomos de carbono se usan fundamentalmente en perfumera. En la Tabla 2.1 se muestran algunas propiedades de los aldehdos y cetonas. Algunos aldehdos aromticos que se obtienen de fuentes naturales como las siguientes poseen aromas muy agradables.
O CH CHCH
CHO
HO H3CO
CHO
benzaldehdo (de almendras amargas)
vainillina (de vainas de vainilla)
cinamaldehdo (de la canela)
La acetona, es de gran uso en la industria como solvente o para obtener otros productos qumicos como la isobutilmetilcetona, metalonato de metilo (disolvente de la acetocelulosa o lacas y resinas); as mismo es el caso de muchos otros compuestos como la etilmetilcetona, que se utiliza como disolvente, para desparafinar aceites lubricantes.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
41
UNIDAD 2
ALDEHDOS Y CETONAS
Tabla 2.1 Propiedades fsicas de aldehdos y cetonas
Nombre UIQPA Aldehdos
metanal etanal propanal butanal 2 metil propanal pentanal 3 metilbutanal hexanal heptanal propenal 2-butenal benzaldehdo CH2O CH3CHO CH3CH2CHO CH3(CH2)2CHO (CH3)2CHCHO CH3(CH2)3CHO (CH3)2CHCH2CHO CH3(CH2)4CHO CH3(CH2)5CHO CH2=CH-CHO CH3-CH=CHO C6H5CHO CH3COCH3 CH3COCH2CH3 CH3COCH2CH2CH3 CH2CH2COCH2CH3 CH3CO(CH2)3CH3 CH3CH2CO(CH2)2CH3 CH3CO(CH2)4CH3 CH3 CH2CO(CH2)3CH3 (CH3CH2CH2)2CO (CH3)2C=CHCOCH3 CH2=CHCOCH3 C6H5COCH3 C6H5COC6H5
O
Estructura
P.F. (C)
-92 -123 -81 -97 -66 -91 -51 -56 -45 -88 -77 -56 -95 -86 -78 -41 -57 -36 -39 -34 -59 -6 21 48 -16 21
P.E. (C)
-21 21 49 75 61 103 93 129 155 53 104 179 56 80 102 101 127 124 151 147 144 131 80 202 305 157 218
Densidad (g/cm3)
0,82 0,78 0,81 0,82 0,79 0,82 0,80 0,83 0,85 0,84 0,86 10,05 0,79 0,81 0.81 0,81 0,83 0,82 0,81 0,82 0,82 0,86 0,86 1,02 1,08 0,94 -
Solubilidad en H2O (%)
55 20 7,1 11 0,1 0,02 30 18 0,3 25,6 5,5 4,8 1,6 1,4 0,4 0,5 15 -
Cetonas
2-propanona 2-butanona 2-pentanona 3-pentanona 2-hexanona 3-hexanona 2-heptanona 3-heptanona4-heptanona 4-metil-3penten-2-ona 3-buten-2-ona acetofenona benzofenona ciclohexanona propiofenona
C6H5COCH2CH3
Fuente: WADE JR., L. G. 2004. Qumica orgnica. Ed. Prentice-Hall, Madrid, Espaa, Pg.778.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
42
UNIDAD 2
ALDEHDOS Y CETONAS
2.4 MTODOS DE OBTENCIN DE ALDEHDOS
2.4.1 Oxidacin de alcoholes primarios
O R CH2OH
oxidante H
C
aldehdo
Los agentes oxidantes en medio cido H2SO4, comnmente usados son dicromato de potasio K2Cr2O7, permanganato de potasio KMnO4, cido ntrico caliente, trixido de cromo CrO3 disuelto en cido actico glacial. En el caso de aldehdos de bajo punto de ebullicin, estos deben destilarse de inmediato, para evitar que la oxidacin contine y se produzca el cido bien se puede utilizar clorocromato de piridinio (PCC) que es un oxidante suave.
2.4.2 Oxidacin de metilbencenos
Este mtodo es usado para la preparacin de benzaldehdo, se trata de la oxidacin controlada de los metilbencenos, que involucra la cloracin por radicales libres de un metilbenceno, seguido por el aislamiento del ismero dicloro, que se hidroliza. La reaccin de hidrlisis del gem-diol es inestable, y se pierde agua para formar el aldehdo.
Cl Ar C Cl H
(ms otros ismeros)
Ar CH3
metilbenceno (debe tener un grupo metilo)
Ctz
H2O CaCO3
OH Ar CH OH
gem-diol, inestable
O Ar C H + H2O
2.4.3 Reduccin de cloruros de acilo
Los cloruros de acilo o cloruros de cido, son derivados reactivos de los cidos carboxlicos en los cuales, el grupo hidroxilo o cido se reemplaza por un tomo de cloro. La reduccin se realiza al dejar que reaccione el cloruro de acilo con tricloruro de fsforo (PCl3) o cloruro de tionilo (SOCl2), dicha reduccin de cloruros de acilo se realiza mediante el uso de H2/Pd (BaSO4) desactivado o usando hidruro de litio y
Portillo Alva Benjamn, Leticia Coln Izquierdo.
43
UNIDAD 2
ALDEHDOS Y CETONAS
aluminio desactivado LiAlH4 en forma de hidruro tri-terbutoxi de litio y aluminio, LiAlH[O-C(CH3)3]3.
O R (Ar) C Cl
cloruro de acilo H2 Pd(BaSO4)
O R (Ar) C H
aldehdo
O R (Ar) C Cl
LiAlH[O-C(CH3)3]3
O R (Ar) C H
aldehdo
cloruro de acilo
2.4.4 Hidrocarbonilacin de alquenos (reaccin 0X0)
Uno de los procesos para la sntesis de aldehdos se llama hidroformilacin o reaccin oxo. En esta reaccin un alqueno reacciona con monxido de carbono e hidrgeno, en presencia del catalizador de cobalto, HCo(CO4), como se presenta a continuacin:
R HC CH2 + CO + H2
HCo(CO)4 2000psi, 110-150C
RCH2CH2CHO + ismeros
2.4.5 Oxidacin de alquenos (proceso wacker)
Los alquenos pueden oxidarse a varios productos, dependiendo del reactivo que se use. Por lo que las reacciones de oxidacin de un doble enlace C=C se pueden clasificar en 2 tipos, el primer tipo corresponde a la oxidacin del enlace pi sin ruptura del enlace, el segundo tipo se refiere a la oxidacin del enlace pi con ruptura del enlace sigma; este ltimo es el de inters para este punto ya que cuando en la oxidacin se rompen los enlaces y se obtienen como productos a los aldehdos, cetonas cidos carboxlicos.
C C
O3 Zn/ H+
O R C H
aldehdo
Portillo Alva Benjamn, Leticia Coln Izquierdo.
44
UNIDAD 2
ALDEHDOS Y CETONAS
El rompimiento del doble enlace se lleva a cabo con ozono y seguido de zinc con un cido para as producir un aldehdo, como lo indica la reaccin.
2.5 MTODOS DE OBTENCIN DE CETONAS
2.5.1 Oxidacin de alcoholes secundarios
Los alcoholes secundarios pueden oxidarse a cetonas. La oxidacin de un alcohol secundario o primario se puede llevar a cabo con un gran nmero de reactivos como el KMnO4, CrO3 y Na2Cr2O7. Es fcil oxidar alcoholes secundarios y el rendimiento de produccin de cetonas es elevado, por ello para oxidaciones en gran escala se usa como reactivo al Na2Cr2O7 en cido actico acuoso, debido a que es de un costo menor.
OH
Na2Cr2O7
O RCR
RCHR H2O, CH3COOH, calor
En el caso de los alcoholes ms sensibles, se utiliza frecuentemente el clorocromato de piridinio, debido a que la reaccin es ms suave y se efecta a temperaturas ms bajas.
2.5.2 Acilacin de friedel-crafts
O
Recibe el nombre de reaccin de acilacin debido a que el grupo R C se llama acilo y la reaccin por medio de la cual se introduce un grupo acilo en un compuesto adopta dicho nombre. Los grupos acetilo y benzoilo son dos grupos acilos comunes. La reaccin de acilacin de Friedel-Crafts es un medio efectivo para introducir un grupo acilo en un anillo aromtico. Con frecuencia la reaccin se lleva a cabo mediante el tratamiento del compuesto aromtico con un haluro de acilo. A menos que el compuesto aromtico sea muy reactivo, la reaccin tambin requiere de la adicin de por lo menos un equivalente de un cido de lewis. El producto de la reaccin es una alquilaril cetona diaril cetona.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
45
UNIDAD 2
ALDEHDOS Y CETONAS
O Ar + R C Cl
AlCl3
O
Ar
C R +
HCl
alquilaril cetona
Ar + Ar
O C Cl
AlCl3
O Ar C Ar +
diaril cetona
HCl
2.5.3 Cloruros de acilo con reactivos organocadmio
Dos reactivos organometlicos verstiles de uso constante en la sntesis orgnica son el reactivo de grignard y el reactivo de organocadmio. Cuando se trata el reactivo de grignard con el cloruro de cadmio seco (CdCl2) se produce un intercambio metal-metal, por lo que el Mg se reemplaza por el Cd, obteniendo de esta forma el reactivo de organocadmio R2Cd:
2R-X + 2Mg
R es alquilo arilo primario ter anhdro
2R-MgX
reactivo de grignard
CdCl2
R2Cd +
reactivo de organocadmio
2MgXCl
Los reactivos organocadmio son utilizados para la sntesis de cetonas. La principal limitacin del reactivo de organocadmio consiste en que pueden prepararse slo de haluros o arilos primarios. De los compuestos organometlicos comunes, el organocadmio es uno de los menos reactivos con respecto a varios grupos funcionales y el hecho de que reaccione exclusivamente con los cloruros de acilo lo pone como un reactivo muy til para introducir un grupo ceto en molculas que ya contienen un aldehdo, ster u otra cetona como sustituyente. O R2Cd +
reactivo de organocadmio
O
mezcla H H2O
R C Cl
cloruro de acilo
R C R
cetona
CdCl2
Portillo Alva Benjamn, Leticia Coln Izquierdo.
46
UNIDAD 2
ALDEHDOS Y CETONAS
2.5.4 Oxidacin de alquenos (proceso wacker)
Esta reaccin se lleva a cabo tratando un alqueno con ozono para ponerlo posteriormente en contacto con dimetilsulfuro y as obtener una cetona, como lo muestra la siguiente reaccin.
R C H
2.5.5 Ozonlisis
R C R
O3 (CH3)2S
R C H O + O C
R R
El mtodo ms comn para la localizacin del enlace doble de un alqueno requiere del uso de ozono (O3). El ozono reacciona enrgicamente con los alquenos formando compuestos inestables llamados oznidos iniciales, los cuales se reacomodan en forma espontnea produciendo compuestos conocidos como oznidos, estos por s mismos, son compuestos muy inestables y los de bajo peso molecular con frecuencia explotan en forma violenta. Debido a esta propiedad, por lo general no se les asla, si no que se reducen directamente tratndolos con zinc y agua. La reduccin produce compuestos carbonilo (aldehdos o cetonas) que pueden aislarse e identificarse con seguridad.
C + O
C O
C O O
C O
O C O C O
O C O C O + Zn
H2O
O + O
Zn(OH)2
Portillo Alva Benjamn, Leticia Coln Izquierdo.
47
UNIDAD 2
ALDEHDOS Y CETONAS
El proceso anterior equivale a desconectar el enlace doble C=C de la siguiente manera:
R C C R H R R C R O + O C H R
1)O3, CH2Cl2,-78C 2) Zn/H2O
2.6 REACCIONES DE ALDEHDOS Y CETONAS
2.6.1 Reacciones de adicin nucleoflica
Se considera que estos compuestos son muy reactivos debido a que presentan en su estructura funcional, una estructura plana polar y en consecuencia, se facilita el ataque de partculas nucleoflicas (escasas en protones o rica en electrones). As, como se observa en la siguiente figura, quien inicia el ataque es una partcula negativa llamada agente nucleoflico. De ah que, este tipo de reacciones se denominan de adicin nucleoflica, y al originarse sobre el oxgeno una carga negativa, sta se neutraliza por adicin de una parte positiva del agente nucleoflico. Es decir, al hacer reaccionar un aldehdo o cetona con HCN por ejemplo, ste primero se disocia en H+ y CN- , enseguida estas partculas se adicionan al aldehdo. En sntesis, estos compuestos dan reacciones tpicas de adicin nucleoflica.
2 1
base de Lewis (agente nucleoflico) Ataque de un agente nucleoflico
C N
Una de las reacciones ms caractersticas de los aldehdos y cetonas es la adicin nucleoflica en el enlace doble carbono-oxgeno, que se muestra a continuacin:
R C H
Portillo Alva Benjamn, Leticia Coln Izquierdo.
Nu O + H Nu R C H
48
OH
UNIDAD 2
ALDEHDOS Y CETONAS
2.6.2 Reacciones de condensacin 2.6.2.1 Condensacin catalizada con base
Los hidrgenos unidos al tomo de carbono adyacente al doble enlace C-O son cidos y pueden eliminarse fcilmente con una base; si se trata de un aldehdo o una cetona con una base en presencia de un halgeno, entonces ocurre la halogenacin. Pero en el caso de que un compuesto carbonlico entre en contacto con una base acuosa diluida y no se encuentre presente algn halgeno; en presencia de una base diluida existir una reaccin de condensacin que involucra dos molculas del compuesto carbonilo. El producto se trata de un -oxialdehdo cuando se usa un aldehdo, o -oxicetona cuando se emplea una cetona: O C OH C C O C
C H
OH H2O
aldehdo
-oxialdehdo
OH R
OH H2O
O C H
cetona
O C C R
C H
-oxicetona
Las reacciones anteriores llevan por nombre condensaciones aldlicas, trmino que surgi debido a que el producto proveniente de un aldehdo, contiene un grupo aldehdo y uno alcohlico, aldol se trata de una contraccin de las palabras aldehdo y alcohol. El trmino condensacin aldlica se emplea ampliamente para las reacciones de condensacin de los aldehdos y cetonas en solucin bsica.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
49
UNIDAD 2
ALDEHDOS Y CETONAS
2.6.2.2 Condensacin catalizada con cido
Las condensaciones aldlicas simples ocurren, tanto en condiciones bsicas como cidas. Considerando la reaccin catalizada con cido utilizando como ejemplo al acetaldehdo, se tiene la siguiente reaccin:
O 2CH3 C H
acetaldehdo H H2O
OH CH3 CH CH2
O C H
H
O CH3 C C C H
3 oxibutanal(inestable)
buten-2al(producto)
Una desventaja que presenta la condensacin aldlica catalizada con un cido, radica en que la eliminacin generalmente ocurre de modo que un compuesto carbonilo , -insaturado sea el producto observado, dicho que es particularmente cierto cuando un aldol contiene un grupo oxidrilo terciario.
2.6.3 Reacciones de sustitucin
La accin del pentacloruro de fsforo (PCl5) supone el reemplazamiento del tomo del oxigeno del grupo carbonilo por dos tomos de cloro, obteniendo derivados gemdiclorados de hidrocarburos.
O R C H
+PCl5 - POCl3
O R CHCl2 R C R
+PCl5 - POCl3
R CCl2 R
En una sustitucin de halgenos en la cadena hidrocarbonada, el Cl y Br reaccionando en condiciones convenientes, dan con aldehdos y cetonas, derivados halogenados de sustitucin en la cadena; donde el halgeno sustituye a los que se encuentran en posicin (contigua) al grupo carbonilo. Entre estos compuestos, con la forma R-CO-CH3, obtenidos a partir de las metilcetonas, dan una reaccin con bases alcalinas o alcalino-trreas. De esta manera el derivado clorado R-CO-CCl3 tratado con leja de sosa produce cloroformo y la sal de sodio (R-CO.ONa):
Portillo Alva Benjamn, Leticia Coln Izquierdo.
50
UNIDAD 2
ALDEHDOS Y CETONAS
R-CO-CCl3
+ OH
R.COO + CHCl3
En el caso de una metilcetona, como la acetona, tratada por hipoclorito de sodio (NaClO) en un medio alcalino (Cl en solucin de sosa) permite obtener cloroformo.
2.7 MECANISMOS DE REACCIN
Mecanismo general
La explicacin simblica del mecanismo de reaccin es la siguiente: 1.- Disociacin del reactivo, origen del reactivo de Lewis.
ZY
+ Y
2.- Ataque de la partcula nucleoflica al carbonilo.
2 3
OY C Y
estado de transicin
O
1
+ Z Y
C Z
compuesto de adicin
Algunos ejemplos de reactivos nucleoflicos que pueden reaccionar como adicin nucleoflica, siguiendo el mecanismo anterior son: cido cianhdrico, reactivos de grignard, alcoholes, amoniaco, derivados de amoniaco (aminas primarias, secundarias), hidroxilamina, hidracina, fenilhidracina, entre otros.
2.7.1 Reactividades relativas de aldehdos y cetonas
La polaridad del grupo carbonilo en los aldehdos y cetonas es la causa primordial de la reactividad de dichos compuestos. Lo anterior significa, que en una reaccin un tomo de carbono parcialmente positivo se une al anillo aromtico y ste desactiva el anillo al eliminar electrones haciendo que el electrfilo entrante ocupe la posicin meta; solo que sta reaccin tiene una limitante, consiste en que slo se puede llevar
Portillo Alva Benjamn, Leticia Coln Izquierdo.
51
UNIDAD 2
ALDEHDOS Y CETONAS
a cabo la halogenacin, nitracin y la sulfonacin en los aldehdos y cetonas aromticas. A continuacin se muestra la reaccin general:
O C R R + E E
aldehdo o cetona electrfilo ismero meta
O C
Existen cuatro tendencias a cerca de las reactividades relativas de los aldehdos y cetonas y se justifican con base en los siguientes mecanismos: A. Los aldehdos son ms reactivos que las cetonas. B. Los aldehdos y las cetonas con sustituyentes menos voluminosos unidos al grupo carbonilo son ms reactivos. C. Las cetonas cclicas son ms reactivas que las no cclicas. D. Los aldehdos y cetonas aromticos son menos reactivos que los compuestos alifticos. A medida que se produce la adicin, los sustituyentes se acercan entre s y el ngulo de enlace respecto al carbono cambia de 120 a 109.5 en el grupo carbonilo del producto. Entre ms sustituyentes sean, se dificulta su acercamiento entre s; ahora, el impedimento estrico creciente con respecto al grupo carbonilo tambin dificulta el ataque por parte del grupo nuclefilo. Por lo que de acuerdo a lo anterior, se puede decir que los aldehdos son ms reactivos que las cetonas ya que el hidrgeno siempre es uno de los sustituyentes en un aldehdo.
O CH3CH2CH
propanal(propanaldehdo)
ms reactivo que
O C H3C CH3
propanona(acetona)
Portillo Alva Benjamn, Leticia Coln Izquierdo.
52
UNIDAD 2
ALDEHDOS Y CETONAS
Existe menos amontonamiento en el producto y el ataque nucleoflico sobre el carbono de los compuestos cclicos es ms sencillo, ya que el grupo carbonilo se mantiene en su lugar por el anillo; mientras que en los sustituyentes, es decir los de cadena abierta, se mantienen fuera. Los factores electrnicos tambin influyen en la determinacin de la reactividad de los aldehdos y cetonas.
2.7.2 Estereoqumica de la adicin a compuestos carbonlicos
El grupo carbonilo es aquiral dado que slo posee un plano de simetra, por lo que no puede proporcionar propiedades quirales a una molcula, como se muestra: R C R Aunque las molculas que contienen al grupo carbonilo pueden ser quirales, logran existir en formas enantimeras debido a los centros asimtricos existentes en alguna parte de la molcula. Por lo que todos los compuestos carbonlicos con excepcin de las cetonas simtricas y el formaldehdo, generan un nuevo centro asimtrico cuando experimentan una adicin nucleoflica. Como el precursor carbonilo es simtrico, el ataque se puede dar en cualquier lado de las especies planas, dando como resultado una mezcla equimolar de enantimeros, que es ptimamente inactiva, como se muestra en seguida:
ataque en (1) (1)
R C R
Nu O
R
H
Nu C OH +
R C R
(2) ataque en (2)
Nu R C R Nu O R
H
OH C Nu
Portillo Alva Benjamn, Leticia Coln Izquierdo.
53
UNIDAD 2
ALDEHDOS Y CETONAS
2.7.3 Adicin de cido cianhdrico
El cido cianhdrico, ataca a las cetonas y a los aldehdos formando productos de adicin denominados cianohidrinas; estas se pueden producir empleando cido cianhdrico (HCN), lquido que contiene una cantidad cataltica de cianuro de sodio o de potasio. Sin embargo, como el HCN es peligroso, muchos mtodos emplean un equivalente de cianuro de potasio o de sodio disuelto en algn solvente donador de protones.
O R C C N R R
O C C R N H C N R
O C C
H R N
cetona o aldehdo
intermediario
cianohidrina
Esta reaccin es reversible y la constante de equilibrio puede no favorecer la formacin de cianohidrina. La tendencia general en reactividad de cetonas y aldehdos es la siguiente: formaldehdo > otros aldehdos > cetonas. Ejemplos:
O C
propanal
HO + H HCN C
CN H
propanal cianohidrina (100%)
O C
2-butanona
+ CH3
HCN
HO
CN CH3
2-butanona cianohidrina (95%)
O C
di-t-butilcetona
OH + HCN C CN
reaccin lenta, bajo rendimiento (<5%)
Portillo Alva Benjamn, Leticia Coln Izquierdo.
54
UNIDAD 2
ALDEHDOS Y CETONAS
2.7.4 Adicin de alcoholes
Los aldehdos y las cetonas reaccionan con los alcoholes para formar acetales. En la formacin de un acetal, se agregan dos molculas de alcohol al grupo carbonilo y se elimina una molcula de agua. O R C + H 2R OH
H
RO R C
acetal
OR + H
H2O
O R C R + 2R OH
RO R C
OR + R acetal H2O
2.7.5 Adicin de amoniaco y aminas sustitudas
En condiciones adecuadas, el amoniaco y las aminas primarias reaccionan con los aldehdos y cetonas para formar iminas. Estas son anlogos nitrogenados de las cetonas y de los aldehdos, con un doble enlace carbono nitrgeno en lugar del grupo carbonilo. Como las aminas, las iminas son bsicas; a una imina sustituida tambin se le llama
base de schiff.
OH + R NH2
H
O C
N C + H2O
C R N H
cetona o aldehdo
amina primaria
carbinolomina
imina (base de shift)
2.7.6 Adicin de reactivos de grignard
Los aldehdos y cetonas reaccionan con reactivos de grignard para formar alcxidos que se protonan con cido diluido para formar el alcohol correspondiente.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
55
UNIDAD 2 Mg ter
ALDEHDOS Y CETONAS
Br
BrMg
reactivo de grignard
O C + BrMg R
BrMgO C
alcxido
H3O
HO C
alcohol
aldehdo o cetona
2.7.7 Reduccin del grupo carbonilo
Este tipo de reaccin se refiere a una desoxigenacin, reemplazando el tomo de oxgeno del carbonilo de una cetona o aldehdo con dos tomos de hidrgeno, reduciendo al grupo carbonilo completamente, pasando por la etapa de alcohol y llegando hasta un metilo.
Zn(Hg), HCl H2NNH2.KOH
O R C R
aldehdo o cetona
NaBH4 LiAlH4
H R C
OH R
(1) TsCl (2) LiAlH4
H R C
H R
metilo
alcohol
2.7.8 Reacciones en las que intervienen los hidrgenos cidos
Un comportamiento qumico de los aldehdos y cetonas est dado, por la presencia de una ligera carga positiva que se origina en el carbono alfa (C2) vecino del carbono carbonilo, debido al efecto inductivo provocado por el oxgeno. Los hidrgenos unidos a l son de carcter cido y pueden reaccionar con bases, formando un carbanin.
O H H H C H OH C H
carbanin
CH C
O H
H C C
O + H H2O
Portillo Alva Benjamn, Leticia Coln Izquierdo.
56
UNIDAD 2
ALDEHDOS Y CETONAS
El hidrgeno alfa puede eliminarse fcilmente como protn a travs de una base adecuada; el carbanin formado se encuentra como un hbrido de resonancia, estabilizado por la deslocalizacin de los electrones sobre el enlace carbonocarbono-oxgeno, dicha estabilizacin es la causa de la acidez de los hidrgenos alfa de un compuesto carbonilo.
2.7.9 Acidez del hidrgeno de los compuestos carbonlicos
El grupo carbonilo afecta la acidez de los hidrgenos, permitiendo el acomodo de la carga negativa del anin. Comparados con el hidrgeno de un grupo -COOH, los tomos de hidrgeno de un aldehdo o de una cetona son dbilmente cidos; el aspecto importante es que son considerablemente ms cidos que los hidrgenos en cualquier otra parte de la molcula, y suficientemente cidos como para generar concentraciones significativas, aunque muy bajas de carbaniones.
2.7.10 Equilibrio cetoenol (tautomerizacin)
Los compuestos carbonlicos que tienen tomos de hidrgeno en sus carbonos alfa se interconvierten en forma rpida con sus correspondientes enoles. Esta rpida interconversin entre dos especies qumicamente distintas es una clase especial de isomera conocida como tautomera. A los ismeros individuales se les llama
tautmeros.
O C C
tautmero ceto
H H
equilibrio rpido
O C C
tautmero enol
En el equilibrio, la mayora de los compuestos carbonlicos existen casi exclusivamente en la forma ceto, y suele ser difcil aislar el enol en forma pura. Por ejemplo, a temperatura ambiente la ciclohexanona contiene slo alrededor de 0.0001% de su tautmero enol, y la acetona slo alrededor de 0.0000001% de su enol.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
57
UNIDAD 2
ALDEHDOS Y CETONAS
Si bien los enoles son difciles de aislar y en el equilibrio estn presentes slo en pequea cantidad, son extremadamente importantes e intervienen en gran parte de la qumica de los compuestos carbonlicos. ciclohexanona
O H
acetona
O
H3C
C O
CH3
H3C
C O
CH2 H
99.9999%
0.0001%
99.999999%
0.000001%
Hidratacin catalizada por in mercrico. Los alquinos llevan a cabo la adicin de
agua, al triple enlace en una reaccin catalizada por cido, en presencia de in mercrico como catalizador. La hidratacin de los alquinos es semejante a la de los alquenos, y tambin se lleva a cabo con orientacin Markovnikov. Sin embargo, los productos no son los alcoholes que cabra esperar.
R R C C H + H2O
HgSO4 H2SO4
H C C
H
R C O
H C H H
HO
alcohol vinlico ("enol")
El producto inicial de la hidratacin es un alcohol vinlico, al que se le llama enol. Por lo general los enoles son inestables y se isomerizan para dar las cetonas correspondientes. La isomerizacin simplemente implica la prdida del protn del hidroxilo del enol y la ganancia del protn en la posicin metilo, con una transposicin del enlace . Este tipo de equilibrio rpido entre dos grupos funcionales isomricos se llama
tautomera, el que se muestra en el ejercicio anterior se llama tautomera cetoenol. En solucin cida, la tautomera ceto-enol se lleva a cabo por la adicin de un
protn en la posicin metlica, seguida de la prdida del protn del hidroxilo.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
58
UNIDAD 2
ALDEHDOS Y CETONAS
Equilibrio ceto enol catalizado por cido: dentro del mecanismo para la
halogenacin catalizada por cido de un compuesto carbonilo, se encuentra el equilibrio ceto-enol. El compuesto protonado en el carbonilo es el intermediario importante del equilibrio debido a que puede perder el protn del oxgeno y regenerar el compuesto carbonilo, perder un protn del tomo de carbono alfa para producir la forma enlica (generalmente el equilibrio favorece a la forma ceto), partiendo de:
H O C C H + H C C
H
H O C C
H
OH C C
forma enol
forma ceto
La reaccin opuesta es decir, la conversin catalizada con cido de un enol a un compuesto ceto, involucra la protonacin del enol para producir el carbocatin ms estable, esto a travs de la carga positiva colocada en el tomo de carbono que est en el tomo de oxgeno; obteniendo as un carbocatin muy estable, debido a que el oxgeno puede aceptar la carga positiva, de modo que todos los tomos cuenten con su octeto de electrones completo.
H
HO C C + H
OH C C H
O C C H ;
OH C C
estable (los tomos tienen un octeto de electrones)
menos estable
2.7.10.1 Mecanismos del equilibrio ceto-enol
La tautomera ceto-enol de los compuestos carbonlicos est catalizada tanto por cidos como por bases. La catlisis cida implica la protonacin del tomo de oxgeno del carbonilo (una base de Lewis), para formar un catin intermediario que puede perder un protn del carbono y producir enol neutro.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
59
UNIDAD 2
ALDEHDOS Y CETONAS
La formacin de un enol catalizada por base ocurre va una reaccin cido-base entre el catalizador y el compuesto carbonlico. Este ltimo acta como un cido prtico dbil y dona a la base uno de sus hidrgenos . Entonces el anin resultante -un ion enolato- vuelve a protonarse para producir un compuesto neutro.
Mecanismo de la formacin del enol catalizada por cido.
O O C H C
H3O
C H O C
H C
O C H C
tautmero ceto
tautmero enol
H C H2O
Mecanismo de la formacin del enol catalizada por Base.
O C O C H C O C C
OH
C
H2O
O C C
tautmero ceto
tautmero enol
2.7.10.2 Factores que influyen en el porcentaje de las formas ceto-enol en el equilibrio
Existen algunos factores que intervienen en la determinacin del contenido enlico de los compuestos que contienen el grupo carbonilo, como los que se enuncian a continuacin:
Portillo Alva Benjamn, Leticia Coln Izquierdo.
60
UNIDAD 2
ALDEHDOS Y CETONAS
A. La naturaleza de los sustituyentes unidos a los grupos carbonilo. Por ejemplo, el acetato de etilo contiene cerca de 8% de enol, mientras que el benzoilacetato de etilo constituye casi el 23% de la forma ceto. B. La cantidad de enol depende del disolvente en el que el compuesto se disuelve, as mismo la temperatura y la concentracin de la mezcla representan otras variables. C. La mayor fuerza directriz para la formacin del enol para compuestos dicarbonlicos, es la conversin de una forma no conjugada (forma ceto) en una forma conjugada (forma enol), sta ltima se encuentra ms estabilizada por la formacin de un anillo de seis miembros, el cual involucra el puente de hidrgeno. Un mayor porcentaje de enol significa, en trminos relativos, que el enol es ms estable. La estabilidad del enol est marcada por un lado, por la estabilidad relativa del enlace C=C, y por otro, en la posibilidad del grupo O-H de estabilizarse formando enlaces de hidrgeno inter o intramoleculares.
2.7.10.3
Reacciones
travs
de
enoles
(isomerizacin,
racemizacin,
halogenacin) Isomerizacin: Los aldehdos y las cetonas existen como mezclas de equilibrio en
dos formas isomricas, la forma ceto y la forma enol. Este tipo de isomerismo, en el que slo el ismero difiere en la colocacin de un protn y la ubicacin correspondiente de un enlace doble se llama tautomerismo, de esta manera los ismeros se llaman tautmeros. Si se habla rigurosamente, el trmino tautomerismo se emplea slo cuando se trata de un isomerismo en que est presente un tomo hetero (azufre, nitrgeno u oxgeno), como se muestra en los siguientes ejemplos.
H N OH N O
nitrosociclohexano oxima de de ciclohehanona
Portillo Alva Benjamn, Leticia Coln Izquierdo.
61
UNIDAD 2
ALDEHDOS Y CETONAS
O H3C N O H2C N
OH O
nitrometano
aci-nitrometano
El caso de la isomerizacin del enlace doble simple, no se considera como un caso de tautomerismo.
CH3CH
CHCH3
CH3CH2CH
CH2
Racemizacin: La racemizacin tiene lugar en presencia de cidos o bases porque
la cetona cambia de manera lenta pero reversible, a su forma enol, y dicho enol es aquiral. Cuando el enol retorna a la forma ceto, se producen cantidades iguales de los dos enantimeros.
C2H5 O H3C C H CC6H5
OH H3O
C2H5 OH C C CH3 C6H5
forma enol (aquiral)
C2H5 O H3C C H
C2H5 O CC6H5 H CC6H5 + H3C C
(R)-(+)-sec-butil fenil cetona (quiral)
(+) -y (-)-sec-butil fenil cetona (forma racmica)
Enolizacin catalizada por base.
H OH C C
O C HO C C C H cetona
(quiral)
OH + OH
anin enolato (aquiral)
enol (aquiral)
Enolizacin catalizada por cido.
O C H C H O H H H C C OH C C H O H + H + O H H
enol (aquiral)
O H
cetona (quiral)
Portillo Alva Benjamn, Leticia Coln Izquierdo.
62
UNIDAD 2
ALDEHDOS Y CETONAS
Halogenacin: el carbanin puede reaccionar con halgenos. Este tipo de
reacciones se le conoce con el nombre de reacciones de sustitucin en el carbono alfa. H H C
2
O C H
1
H + OH
X-X
O C H + X-X
H H C X
O C H
H C
2.7.10.4 Condensacin aldlica
Esta reaccin se realiza por idnticas razones a la anterior, los aldehdos y cetonas que tengan hidrgenos en el carbono alfa provocan este tipo de reacciones en presencia de una base como NaOH. Consiste en la unin de dos molculas carbonlicas: aldehdo-aldehdo, aldehdo-cetona, cetona-cetona; a travs de la formacin de un enlace sencillo CC por eliminacin de una molcula de agua. Los productos de estas reacciones se llaman -hidroxicetona o -hidroxialdehdo. Ejemplos: Cetona + NaOH
O 2CH3 C CH3 Aldehdo + NaOH
NaOH
OH H3C C CH2 C CH3
O CH3
O 2CH3 C H
NaOH
OH H3C C CH2 C CH3
O H
Si los aldehdos o cetonas no tienen hidrgenos alfa, la reaccin no se lleva a cabo. Es el caso de compuestos como los siguientes, que no dan este tipo de reaccin aldlica:
Portillo Alva Benjamn, Leticia Coln Izquierdo.
63
UNIDAD 2
ALDEHDOS Y CETONAS
O C H
H C
O H
O C
Portillo Alva Benjamn, Leticia Coln Izquierdo.
64
UNIDAD 2
ALDEHDOS Y CETONAS
2.8 EJERCICIOS PROPUESTOS
A.- Escriba el nombre de las siguientes estructuras qumicas.
O
1.- H3C C H
O H3C HC C H
2.-
Cl O
3.- H3C HC
HC C H
O
4.-
H2C H2C C H
O H3C HC C H
5.-
Br
OH
6.- CH2
OH O HC C H
O
7.- CH3 CH2 CH2 CH2 CH2 CH2 C H
O
8.- H C H
O
9.- H2C HC C H
B.- Escriba las estructuras de los siguientes compuestos qumicos. 1.- Pentanona 2.- Fenilacetaldehdo 3.- Fenilmetilcetona
Portillo Alva Benjamn, Leticia Coln Izquierdo.
65
UNIDAD 2
ALDEHDOS Y CETONAS
4.- 3,5-dimetilbenzaldehdo 5.- 2-hidroxi-3-pentanona C.- Indique otro nombre aceptable para cada uno de los siguientes compuestos. 1.- Dimetilcetona 2.- 1-fenil-2-butanona 3.- Etilisopropilcetona 4.- Dibencilcetona 5.- Etilvinilcetona D.- Indique algunas semejanzas entre los aldehdos y las cetonas. E.- Cmo se pueden distinguir los aldehdos de las cetonas? F.- Complete las siguientes reacciones 1.+ H2
Pd(BaSO4)
(CH3)2CHCHO
CH3 H3C
2.-
CH3 +
NaIO
CH3 O O + H2O
HgSO4 H2SO4
3.-
G.- Indique los pasos en las siguientes sntesis: 1.- Cloruro de acetilo a acetal 2.- Etanol a 2-buteno H.- Los aldehdos reaccionan con el reactivo de Tollens [Ag(NH3)+2] pero no con las cetonas, escriba un ejemplo y explique este hecho. I.- Escriba la reaccin de: (1) la butanona y (2) el butanal con HCN. Establezca el mecanismo de estas reacciones. J.- Complete las siguientes reacciones.
Portillo Alva Benjamn, Leticia Coln Izquierdo.
66
UNIDAD 2
ALDEHDOS Y CETONAS
O
1.-
+ CH3OH
O
2.-
+ CH3OH
3.- CH3CH2COH
O
+ Br2
NaOH
4.-
+ Br2 NaOH
O CH2CH
O
1.-NaBH4 2.-H3O+
5.-
6.-
CH2CH
Ag2O NH4OH
O
7.-
CH2CH O
2.-H3O+
1.-CH3MgBr
8.-
CH2CH O
H2NNH2 KOH
9.-
CH2CH
O
HCN KCN
10.-
CH2CCH3 2.-H O+ 3 O
1.-NaBH4
11.-
CH2CCH3 2.-H O+ 3 O
1.-CH3MgBr
12.-
CH2CCH3
HCN KCN
Portillo Alva Benjamn, Leticia Coln Izquierdo.
67
UNIDAD 2
ALDEHDOS Y CETONAS
O C 2 13.NaOH
Portillo Alva Benjamn, Leticia Coln Izquierdo.
68
También podría gustarte
- ESTADO DEL ARTE DE LA VOLADURA by Cameron McKenzieDocumento107 páginasESTADO DEL ARTE DE LA VOLADURA by Cameron McKenzieRobertAún no hay calificaciones
- Propiedades Químicas AlcanosDocumento37 páginasPropiedades Químicas AlcanosFatima Viviana Sacta Paida87% (15)
- Métodos de Obtención de EsteresDocumento8 páginasMétodos de Obtención de EsteresXanath PotAún no hay calificaciones
- AlquenosDocumento45 páginasAlquenosSebastian Sanchez Franco100% (1)
- Estructura de LewisDocumento15 páginasEstructura de LewisAmadaAún no hay calificaciones
- Aldehídos y CetonasDocumento19 páginasAldehídos y CetonasAlvaro J Manosalva Angarita100% (1)
- Ejercicios - Capítulo4 - L.G. Wade, Jr. - Quimica Organica. 1-Pearson - 7ed - (2012)Documento4 páginasEjercicios - Capítulo4 - L.G. Wade, Jr. - Quimica Organica. 1-Pearson - 7ed - (2012)Luisa Fernanda MartinezAún no hay calificaciones
- Los HidrocarburosDocumento16 páginasLos HidrocarburosJose EnriqueAún no hay calificaciones
- 02 ÉsteresDocumento9 páginas02 ÉsteresJose Chamorro100% (3)
- Halogenuros de Alquilo. PropiedadesDocumento10 páginasHalogenuros de Alquilo. PropiedadesAndrea PachecoAún no hay calificaciones
- Acidos CarboxílicosDocumento43 páginasAcidos CarboxílicosYourladys Elena100% (3)
- Alcoholes y FenolesDocumento41 páginasAlcoholes y Fenolesclubdelquimico.blogspot.com90% (42)
- Hidrocarburos AromaticosDocumento30 páginasHidrocarburos AromaticosManuel Cedeño81% (64)
- ALCOHOLESDocumento25 páginasALCOHOLESJorge Luis Castañeda CobeñasAún no hay calificaciones
- AlquenosDocumento50 páginasAlquenosandri67% (3)
- Nomenclatura de FenolesDocumento6 páginasNomenclatura de Fenolesvanessa100% (2)
- Deshidrohalogenación de AlquinosDocumento6 páginasDeshidrohalogenación de AlquinosGiovanny Giraldo100% (1)
- Proceso de Reduccion Directa HylDocumento4 páginasProceso de Reduccion Directa Hyljherry100% (1)
- Acidos Carboxilicos ReaccionesDocumento13 páginasAcidos Carboxilicos ReaccionesKevinFernandez100% (1)
- Aldehídos y CetonasDocumento40 páginasAldehídos y Cetonasluisgabrielvivaldo70% (10)
- Cuestionario de AldehÍdos y CetonasDocumento6 páginasCuestionario de AldehÍdos y CetonasIgnacio Rodriguez Robles100% (4)
- AromaticidadDocumento32 páginasAromaticidadAlex Sotelo ContrerasAún no hay calificaciones
- Laboratorio 5 Aldehidos y CetonasDocumento11 páginasLaboratorio 5 Aldehidos y CetonasStefanny Londoño Amaya89% (9)
- ALCOHOLESDocumento26 páginasALCOHOLESPaul Paz Cieza100% (3)
- Tema 2 Alcanos y Cicloalcanos (Elier Galarraga)Documento55 páginasTema 2 Alcanos y Cicloalcanos (Elier Galarraga)Juan Alejandro Guerrero TeranAún no hay calificaciones
- Aldehidos y CetonasDocumento8 páginasAldehidos y Cetonasdavid mateusAún no hay calificaciones
- Sintesis de Aldehidos y CetonasDocumento18 páginasSintesis de Aldehidos y CetonasJesus Alberto MendozaAún no hay calificaciones
- Hidrocarburos AromáticosDocumento8 páginasHidrocarburos AromáticosAlejandra GualdronAún no hay calificaciones
- Propiedades Físicas y Químicas de Los AldehídosDocumento8 páginasPropiedades Físicas y Químicas de Los Aldehídoslia100% (1)
- ETERESDocumento21 páginasETERESJnthn AyalaAún no hay calificaciones
- 2015 Solucionario Clase 20 Química Orgánica II Propiedades Del Carbono e HidrocarburosDocumento9 páginas2015 Solucionario Clase 20 Química Orgánica II Propiedades Del Carbono e Hidrocarburosjorge0% (2)
- Haluros de Arilo RealDocumento10 páginasHaluros de Arilo RealAnDreAún no hay calificaciones
- AlquenosDocumento49 páginasAlquenosMaría Armijo Delgado0% (1)
- EpóxidosDocumento16 páginasEpóxidosMarielena100% (1)
- Derivados HalogenadosDocumento3 páginasDerivados HalogenadosJuan Marcelo Tenorio Barboza100% (1)
- Síntesis Del FenantrenoDocumento6 páginasSíntesis Del FenantrenoWilbert Rivera MuñozAún no hay calificaciones
- Alquenos PDFDocumento5 páginasAlquenos PDFAllison Aldoradin ReyesAún no hay calificaciones
- Propiedades Químicas de Ácidos CarboxílicosDocumento7 páginasPropiedades Químicas de Ácidos CarboxílicosCarlosAún no hay calificaciones
- Reacciones de Los FenolesDocumento3 páginasReacciones de Los FenolesLizandro Galleguillos Diaz33% (3)
- Cuestionario Quimica OrganicaDocumento2 páginasCuestionario Quimica Organicaapi-282235724100% (7)
- Propiedades Físicas y Químicas de Los Aldehídos y CetonasDocumento4 páginasPropiedades Físicas y Químicas de Los Aldehídos y CetonasMay WhiteAún no hay calificaciones
- ArenosDocumento21 páginasArenosAlex PallesAún no hay calificaciones
- Métodos de Obtención de Los HidrocarburosDocumento5 páginasMétodos de Obtención de Los Hidrocarburosluis alcivarAún no hay calificaciones
- ANILINADocumento11 páginasANILINANahomiAún no hay calificaciones
- Reacciones de AlquenosDocumento18 páginasReacciones de AlquenosRoger ManzanarezAún no hay calificaciones
- NitrilosDocumento19 páginasNitrilosIsis zaretAún no hay calificaciones
- Aldehidos y CetonasDocumento11 páginasAldehidos y Cetonaspaula67% (3)
- Metodos de Obtencion de Aldehidos y CetonasDocumento57 páginasMetodos de Obtencion de Aldehidos y CetonasMarco Antonio Moreno0% (1)
- Cuestionario PROPIEDADES FÍSICAS Y QUÍMICAS DE LOS ÁCIDOS CARBOXÍLICOSDocumento8 páginasCuestionario PROPIEDADES FÍSICAS Y QUÍMICAS DE LOS ÁCIDOS CARBOXÍLICOSFernanda Mateus0% (1)
- Practica Alcoholes QuimicaDocumento13 páginasPractica Alcoholes QuimicaSherri Barr64% (11)
- Síntesis OrgánicaDocumento67 páginasSíntesis OrgánicaYuri Jesus V.100% (1)
- Taller Reacciones de AdiciónDocumento3 páginasTaller Reacciones de AdiciónTatiana CastañoAún no hay calificaciones
- Aldehídos y CetonasDocumento16 páginasAldehídos y CetonasZero MadsAún no hay calificaciones
- Aldehidos y Cetonas Primera ParteDocumento34 páginasAldehidos y Cetonas Primera PartePaolaAlejandraRodriguezAún no hay calificaciones
- Aldehidos y CetonasDocumento21 páginasAldehidos y CetonasCamila Ximena Anaya AlarcónAún no hay calificaciones
- c11 Aldehidos y CetonasDocumento43 páginasc11 Aldehidos y CetonasOscarJoseAún no hay calificaciones
- Compuestos CarbonílicosDocumento61 páginasCompuestos CarbonílicosDuvan Benavides San JuanAún no hay calificaciones
- 21 Aldehidos y Cetonas 2023Documento27 páginas21 Aldehidos y Cetonas 2023Santos Anibal Tuj ToAún no hay calificaciones
- Aldehídos y Cetonas - Org II-UAB 2020Documento43 páginasAldehídos y Cetonas - Org II-UAB 2020ChemistryAún no hay calificaciones
- Aldehidos Y CetonasDocumento37 páginasAldehidos Y CetonasLin NietoAún no hay calificaciones
- Aldehidos y Cetonas 09Documento36 páginasAldehidos y Cetonas 09Alison RoaAún no hay calificaciones
- Aldehidos y Cetonas 2019 1Documento57 páginasAldehidos y Cetonas 2019 1Elvis David Olivera MerloAún no hay calificaciones
- Unidad 3 Compuestos CarbonílicosDocumento61 páginasUnidad 3 Compuestos Carbonílicosronni bermudezAún no hay calificaciones
- ModelosDocumento4 páginasModelosFranciscoAún no hay calificaciones
- Herramientas de Porosidad CAPITULO 1Documento3 páginasHerramientas de Porosidad CAPITULO 1hu55hAún no hay calificaciones
- Universidad Autonoma Gabriel René MorenoDocumento13 páginasUniversidad Autonoma Gabriel René Morenoale.dorado16Aún no hay calificaciones
- Quimica GeneralDocumento24 páginasQuimica GeneralRafael Fonseca MartinezAún no hay calificaciones
- Trabajo Quimica.Documento7 páginasTrabajo Quimica.Eduardo GordilloAún no hay calificaciones
- Oxidación de Aceites y Grasas - Original (Autoguardado)Documento10 páginasOxidación de Aceites y Grasas - Original (Autoguardado)luz karina ynoñan videaurrAún no hay calificaciones
- Semana 5 Reporte de Resultados - Laboratorio Q. InorgánicaDocumento3 páginasSemana 5 Reporte de Resultados - Laboratorio Q. InorgánicaLlerena VictorAún no hay calificaciones
- Alcohol-Isopropilico para SamobaresDocumento8 páginasAlcohol-Isopropilico para SamobaresLUCY YANETH CANO RINCONAún no hay calificaciones
- Nomenclatura de QuimicaDocumento15 páginasNomenclatura de Quimicarucham8Aún no hay calificaciones
- Masa Equivalente Marco TeoricoDocumento1 páginaMasa Equivalente Marco TeoricoNatalyGallosoSanchezAún no hay calificaciones
- 02.2 Dyeing Methods For Wool Notes 1 75.en - EsDocumento75 páginas02.2 Dyeing Methods For Wool Notes 1 75.en - EsMiryan VilatuñaAún no hay calificaciones
- Taller Quimica GeneralDocumento2 páginasTaller Quimica GeneralOriana Torres RodriguezAún no hay calificaciones
- Practica 1 ESTELADocumento12 páginasPractica 1 ESTELAMaria trinidad reyes tapiaAún no hay calificaciones
- Ejercicios de Formulación (Química Inorgánica) 23-Sept-2020Documento6 páginasEjercicios de Formulación (Química Inorgánica) 23-Sept-2020Sonsoles EncinarAún no hay calificaciones
- Quim I 17644 Ecuaciones y Reacciones Quimicas Sab 29-04Documento20 páginasQuim I 17644 Ecuaciones y Reacciones Quimicas Sab 29-04ERICK JHONATAN MEDINA LLANCAAún no hay calificaciones
- Cálculo Exergia QuimicaDocumento9 páginasCálculo Exergia QuimicamarzinusAún no hay calificaciones
- Alion 500 SCDocumento6 páginasAlion 500 SCsupermarco744735Aún no hay calificaciones
- Curso de h2s BasicoDocumento31 páginasCurso de h2s BasicoRafael Oswaldo Valladares VargasAún no hay calificaciones
- Introduccion Al Petroleo en ColombiaDocumento41 páginasIntroduccion Al Petroleo en Colombiaelmer yomar angarita castroAún no hay calificaciones
- Adobe Scan 29 Feb 2024Documento24 páginasAdobe Scan 29 Feb 2024damiandelacruz62Aún no hay calificaciones
- Reactividad de Elementos MetálicosDocumento9 páginasReactividad de Elementos MetálicosYuri Carolina LOPEZ ROJASAún no hay calificaciones
- Ejercicios Enlace Químco 3º EsoDocumento3 páginasEjercicios Enlace Químco 3º EsoBeatriz ArroyoAún no hay calificaciones
- Ciencias III-ejercicios de Pisa para El Bloque 3Documento4 páginasCiencias III-ejercicios de Pisa para El Bloque 3Qfb Mario Lopez MezaAún no hay calificaciones
- Artes VisualesDocumento4 páginasArtes VisualesAngel Moreno PaicoAún no hay calificaciones
- Exámenes Parciales:: Udb - Química Química GeneralDocumento9 páginasExámenes Parciales:: Udb - Química Química GeneralMati GoldmanAún no hay calificaciones
- Digestor UvDocumento10 páginasDigestor UvHaydEe Hamna Ramos RamosAún no hay calificaciones