Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Modelo de Stewar
Modelo de Stewar
Cargado por
Cristian Johan Castillo FierroTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Modelo de Stewar
Modelo de Stewar
Cargado por
Cristian Johan Castillo FierroCopyright:
Formatos disponibles
medigraphic Artemisa
en línea
Anestesiología
E A N ES
NO D T ES
Mexicana de M
EX
ICA IO
L
Revista
O
IO
GÍ
C
EG
AA
COL
.C.
ANT
GÍA
ES
LO
SO
IO
CI
ED ES
AD ST
MEXI NE
CANA DE A
ARTÍCULO DE REVISIÓN
Vol. 29. No. 4 Octubre-Diciembre 2006
pp 240-244
Teoría ácido-básico de Stewart, un nuevo paradigma
en medicina crítica
Dr. Carlos Häubi S,* Dr. Armando Moreno-Santillán,* Dr. Manuel Díaz de León-Ponce,*
Dr. Carlos Gabriel Briones-Vega,* Dr. José Meneses-Calderón,* Dra. María Elena Orenday-Aréchiga,*
Dr. Juan Torres-Pérez,* Dr. Jesús Carlos Briones-Garduño*
* Unidad de Investigación Instituto Mater- RESUMEN
no Infantil del Estado de México.
La vida humana es posible sólo dentro de parámetros estrechos de pH sanguí-
Solicitud de sobretiros: neo por lo que el organismo está dotado de mecanismos para mantener esta
Dr. Carlos Häubi S constante biológica. En condiciones normales los procesos metabólicos origi-
Paseo Colón esquina Gral. Felipe Ángeles. nan sustancias ácidas, esto pone en evidencia una tendencia del organismo a
Toluca México, 52140. producir ácidos, sin embargo el pH sanguíneo se mantiene en rangos fisiológi-
Tel. y Fax 01 722 280 92 12 cos, debido a que las concentraciones de iones hidrógeno en los compartimen-
E-mail: drcarlosbriones@hotmail.com tos extra e intracelulares es controlada estrechamente en el organismo, pues
cambios muy pequeños llevan a disfunciones celulares. Las alteraciones del
equilibrio ácido-básico son neutralizadas por sistemas buffer, explicados tradi-
Recibido para publicación: 10-07-06 cionalmente en base al trabajo de Henderson y Hasselbach mediante el uso del
Aceptado para publicación: 30-08-06 bicarbonato y de la presión parcial de bióxido de carbono, partiendo de la base
que estas dos variables son independientes de los factores que determinan el
pH. El método propuesto por Stewart propone que el comportamiento y concen-
tración de ciertos iones está determinado por las leyes de la química sobre las
variables independientes; la diferencia de iones fuertes, la presión parcial de
bióxido de carbono y el total de aniones débiles. El presente trabajo tiene como
propósito describir los aspectos importantes de ambos métodos y presentar las
bases de futuros trabajos de investigación relacionados con estos aspectos.
Palabras clave: Ácido-base, Stewart, Henderson-Hasselbach.
SUSTRAÍDODE-M.E.D.I.G.R.A.P.H.I.C
SUMMARY
Human life is:ROP ODAROBALE
only possible FDPrange of pH. Consequently, the body
within a narrow
has different and complex mechanisms to maintain this balance. In normal cir-
cumstances,VC metabolic
ED AS,processes yield a number of acid by-products, reflecting
CIDEMIHPARG
a natural trend in pH towards acidity. However, blood pH is kept within physiolog-
ical range because concentrations of hydrogen ions in both the extra- and intra-
ARAP are closely controlled by the body, since very slight changes
cellular compartments
may lead to cell dysfunction. In order to maintain pH within normal ranges and
avoid cell damage, hydrogen ARUTARETIL
ACIDÉMOIB ions move across :CIHPARGIDEM
the intra and extracellular com-
partments. Acid-base disturbances are controlled by different buffer systems,
described by Henderson and Hasselbalch using bicarbonate and carbon dioxide
as independent variables. The acid-base model described by Stewart proposes
edigraphic.com
that ion concentration is determined by the of laws chemistry acting upon inde-
pendent variables, such as strong ion difference, carbon dioxide partial pres-
sure, and weak anions. This paper describes important features of both methods,
in order to set the basis for future research in this field.
Key words: Acid-base balance, Stewart moder, Henderson-Hasselbalch model.
240 Revista Mexicana de Anestesiología
Häubi SC y cols. Teoría ácido-básico de Stewart, un nuevo paradigma en medicina crítica
BREVE RECUENTO HISTÓRICO partimentos extra e intracelulares es controlada estrechamente
en el organismo, pues cambios muy pequeños podrían llevar
La palabra ácido viene de la raíz latina “acere” que quiere a disfunciones celulares mayores(1). Las alteraciones del equi-
decir agriarse y la palabra “álcali” proviene del árabe “al- librio ácido-básico son neutralizadas en condiciones norma-
quili” que significa ceniza vegetal. A pesar de que los áci- les por tres sistemas buffers: 1) proteínas intracelulares (he-
dos se conocían desde la antigüedad, especialmente por su moglobina), 2) componentes titulares (carbonato de calcio,
sabor y su capacidad para corroer metales y enrojecer la fosfato de calcio), 3) el sistema bicarbonato-ácido carbónico.
tintura de tornasol, la historia del equilibrio ácido-base Entender las alteraciones en el equilibrio ácido-base es clíni-
puede remontarse al siglo XVI cuando Paracelso planteó la camente fundamental para diagnosticar y realizar un trata-
teoría de que algunas enfermedades eran causadas por de- miento adecuado(2).
pósitos alcalinos y necesitaban ácidos para su curación. En los últimos años se ha publicado diversos trabajos
En 1692 Newton planteó que “los ácidos se caracterizaban que en forma general plantean una controversia sobre dos
por tener una gran fuerza de atracción y por tanto todo lo modelos para entender las alteraciones en el equilibrio áci-
que atrae y es atraído con fuerza puede ser llamado ácido”. do-base, estos modelos se conocen como método tradicio-
SUSTRAÍDODE-M.E.D.I.G.R.A.P.H.I.C
Ya en el Siglo XVIII Antoine Lavoisier, Bertholet, Hum- nal (tradicional approach) y el método moderno (mordern
phry Davy, Gay Lussac y otros contribuyeron a un mejor approach) (3,4).
:ROP ODAROBALE FDP
conocimiento de los ácidos y las bases. En 1877 Friedrich El método tradicional fue desarrollado en base al trabajo
Walter midió por primera vez el dióxido de carbono en el de
VCHenderson Hasselbach y continúa siendo el más utiliza-
ED AS, CIDEMIHPARG
plasma y trató exitosamente con bases una acidosis meta- do en la práctica clínica. Una ventaja de este método es que
bólica. En la misma década Kussmaul describió la hiper- es relativamente fácil de entender y de aplicar, sin embargo
ARAP
ventilación en la acidosis metabólica del diabético y pos- se han identificado algunos problemas con su interpreta-
teriormente Bernard Naunyn introdujo el término de acidosis ción. HCO3- y de la PCO
El uso delARUTARETIL
ACIDÉMOIB 2 para describir diferentes
:CIHPARGIDEM
y lo definió como una producción excesiva de ácidos. En tipos de alteraciones ácido base ha generado la suposición
1887 el sueco Svante Arrhenius, en su teoría de la disocia- de que estas dos variables son independientes de los facto-
ción electrolítica, fue el primero en asociar la acidez a la res que finalmente determinan el pH; es decir, que la diso-
disociación de los iones H+. A finales del Siglo XIX y Höber ciación de equilibrio para el ácido carbónico es el sistema
dieron a conocer el primer electrodo para medir concentra- de control para el ajuste del pH(2-4).
ciones de H+. Entre 1901 y 1909 Sorensen introdujo el térmi- El método moderno fue inicialmente propuesto por
no y la escala logarítmica de pH. En 1912 Hasselbach de- Stewart a principios de los 80 y propone que el comporta-
mostró la relación entre la PCO2 y la acidez, un año después miento y concentración de ciertos iones y moléculas ([H+],
Henderson postuló que la acidosis metabólica está princi- [OH], [HCO3-], [CO32-], [HA], [A]) en un medio acuoso está
palmente determinada por el déficit de bases y no por el determinado por la acción de las leyes de la química sobre
exceso de ácidos. Tres años más tarde, el propio Hasselba- las variables independientes: la diferencia de iones fuertes
ch, aplicó el término de pH y una fórmula logarítmica a la (Strong Ion Difference: SID), presión parcial de bióxido de
ecuación que Henderson había enunciado en 1908, relacio- carbono (PCO2) y el total de aniones débiles en la solución
nada con el sistema amortiguador del H2CO3/HCO3, esta (ATOT)(2-5).
ecuación es la ya clásica ecuación de Henderson Hasselba- El presente trabajo tiene como finalidad describir los as-
ch(1-3). pectos importantes de ambos métodos.
INTRODUCCIÓN EL MÉTODO TRADICIONAL
La vida humana es posible sólo dentro de parámetros estre- Muchas reacciones en los sistemas biológicos son reversi-
chos del pH sanguíneo (6.8 a 7.8) por lo que el organismo bles y alcanzan su equilibrio. El equilibrio constante de-
está dotado de mecanismos homeostáticos muy sensibles pende de un número de factores entre los cuales se incluye
encargados de mantener esta constante biológica. En condi- la temperatura.
ciones normales los procesos metabólicos originan sustan-
cias ácidas como el ácido carbónico, el sulfúrico, el fosfóri- A + B <=> C + D
edigraphic.com
co, el láctico, el pirúvico y otros más. Incluso la degradación
de alimentos habitualmente libera sustancias ácidas. Esto En 1909 Henderson aplicó la ley de acción de masas (ver
pone en evidencia una tendencia del organismo a producir adelante) para equilibrar la reacción del ácido carbónico:
ácidos; sin embargo el pH sanguíneo no se modifica, debido
a que la concentración de iones de hidrógeno en los com- CO2 + H2O <=> H2CO3 <=>H+ + HCO3-
Volumen 29, No. 4, octubre-diciembre 2006 241
Häubi SC y cols. Teoría ácido-básico de Stewart, un nuevo paradigma en medicina crítica
Reorganizó la ecuación para permitir el cálculo del pH: de base y la brecha aniónica. En 1960 Siggard-Andersen &
Ángel propusieron el termino “exceso de base”, el cual se
_
[H + ] X [HCO 3 ] define como la concentración de [H+] requerida para regre-
K1 =
[H2 CO 3 ] sar el pH a 7.4, siempre y cuando la PCO2 se mantenga cons-
tante en 40 mmHg(3,4).
Entonces: La brecha aniónica se basa en el principio de electroneu-
tralidad y se calcula:
+ K1 X [H2 CO3 ]
[H ] = _
[HCO 3 ] ([Na+] + [K+]) – ([Cl-] + [HCO3-])
[CO2 ] X [H 2 O ] Su valor es usualmente positivo y refleja los aniones que
K2 =
[H2 CO 3 ] no son tomados en cuenta en la fórmula, como proteínas,
fosfatos y sulfatos(3,6). Este bemol en la fórmula puede cau-
[CO2 ] X [H 2 O ] sar errores de interpretación en el paciente crítico que gene-
[H2 CO 3 ] = ralmente presenta disminución en la concentración de albú-
K2
mina plasmática.
Y si el H2O se considera como constante:
EL MÉTODO MODERNO O MÉTODO
[H2 CO 3 ] = K3 X [CO2 ] DE STEWART
Después se sustituye el H2CO3: La teoría de Stewart se basa en las siguientes leyes de la
química:
+ K4 X [CO2 ]
[H ] = _ 1. Ley de conservación de la materia. La masa (o la energía)
[HCO3 ]
no puede ser creada ni destruida, sólo convertida a otras
formas de materia o energía(2).
K1, K2, K3 y K4 son constantes numéricas diferentes.
2. Ley de acción de masas. Toda sustancia incompleta-
Posteriormente Hasselbach reorganizó logarítmicamente la
mente disociada alcanza un equilibrio de disociación.
ecuación de Henderson:
El equilibrio se da cuando las reacciones de izquierda a
_ derecha se complementan con las reacciones de dere-
[HCO3 ]
pH = pK + log cha a izquierda, es decir, las moléculas siguen reaccio-
[CO2 ] nando al mismo ritmo, pero por cada molécula que reac-
ciona en una dirección hay otra que reacciona en la
Introdujo la PCO2 dentro de la ecuación en lugar del CO2: dirección opuesta. El punto en que se logra este equili-
_ brio (constante de equilibrio, K) está determinado por
[HCO3 ] las características de las moléculas y del medio en el
pH = pK + log
S CO 2 X pCO 2 que están disueltas(2).
3. Ley de electroneutralidad del agua. La suma de cargas
La SCO2 es el coeficiente de solubilidad para el dióxido positivas y negativas en el agua debe ser siempre de
de carbono y pK es el logaritmo negativo del equilibrio cero. El incremento de cargas positivas (cationes) pro-
constante de K4. ducirán incrementos en la disociación natural del agua
En base a lo anterior inferimos que el dióxido de carbono para compensar con la creación de iones hidroxilo (OH-).
y el HCO3- son variables que determinan el sistema que De modo opuesto el incremento de cargas negativas
corrige las alteraciones de la [H+]; sin embargo, hoy en día (aniones) aumentará la disociación para elevar la con-
está claro que cualquier cambio en la PaCO2 causará cam- centración de hidrogeniones (H+)(2).
bios en la HCO3-, motivo por el cual la concentración de
edigraphic.com
HCO3- no puede ser utilizada per se como un indicador de
alteraciones metabólicas. Es por esto que se desarrollaron
El modelo de Stewart incluye el análisis y la relación de
varios componentes de los fluidos humanos con las leyes
métodos que estimaran el componente metabólico que se previamente expuestas. Los componentes son: 1) agua, 2)
produce con los cambios ácido-base. En el presente trabajo iones fuertes en el agua, 3) ácidos débiles en el agua y 4)
mencionaremos los dos métodos más empleados, el exceso dióxido de carbono (Figura 1).
242 Revista Mexicana de Anestesiología
Häubi SC y cols. Teoría ácido-básico de Stewart, un nuevo paradigma en medicina crítica
El gas CO2 tiene una baja solubilidad en el agua y cuatro
VARIABLES INDEPENDIENTES
reacciones pueden ocurrir:
1. Disolución en el agua
2. Reacción en el agua para formar ácido carbónico
Diferncia entre Presión parcial Total de aniones 3. Disociación del ácido carbónico para formar el ión bicar-
iones fuertes de bióxido de débiles
carbono bonato
4. Disociación del bicarbonato para formar el ión carbonato
Las cuatro reacciones se pueden ejemplificar con la si-
Ley de conservación de la materia guiente reacción:
Ley de acción de masas CO2 + H2O <=> H2CO3 <=> H + HCO3 <=> H + H+CO32-
SUSTRAÍDODE-M.E.D.I.G.R.A.P.H.I.C
Principio de electroneutralidad
Total de aniones débiles (ATOT)
del agua :ROP ODAROBALE FDP
Un ácido débil, por definición, es aquel que se disocia
parcialmente en sus iones constituyentes hasta llegar a su
VC ED AS, CIDEMIHPARG
VARIABLES DEPENDIENTES equilibrio. El total de aniones débiles (ATOT) representa la
cantidad
ARAP total de ácidos débiles diferentes al CO2 en el sis-
tema. Los ácidos no disociados son descritos como HA y los
[H+], [OH], [HCO3-], [CO32-], [HA], [A] disociados A-(2)ARUTARETIL
. Entonces la reacción de disociación de áci-
ACIDÉMOIB :CIHPARGIDEM
dos débiles es:
Figura 1. El método de Stewart(2).
HA <=> H+ + A-
DIFERENCIA DE IONES FUERTES. STRONG ION En base a la ley de conservación de la materia, si HA y A
DIFFERENCE (SID) no participan en otras reacciones en la solución, la suma de
[HA] y [A] permanecerá constante, entonces:
La diferencia entre iones fuertes (SID por sus siglas en
inglés) es la primera y más importante variable indepen- [ATOT] = [HA] + [A-]
diente de Stewart.
SID = [todos los cationes fuertes en la solución] – [todos Los ácidos débiles más importantes en el plasma son las
los aniones fuertes en la solución]. proteínas y los fosfatos. La albúmina es la proteína más im-
Stewart realizó la distinción entre iones fuertes y débiles portante que actúa como un ácido débil. Los fosfatos, regu-
en base a sus constantes de disociación, entonces los catio- ladores del calcio en el cuerpo, constituyen el 5% del ATOT
nes fuertes son: Na, K, Ca y Mg; mientras que los aniones cuando sus niveles son normales. Por lo tanto la concentra-
fuertes son: Cl, SO4 y lactato. La entrada de un ión positivo ción de albúmina puede ser utilizada para estimar el ATOT en
o negativo altera la carga eléctrica del agua y obliga a ésta a plasma(2,3).
disociarse produciendo iones negativos (hidroxilo) o posi-
tivos (ión de hidrógeno) según sea el caso. Cuando las con- IMPLICACIONES DEL MODELO DE STEWART
centraciones de cationes y aniones son equimolares, la SID
es igual a cero, por lo tanto [H+] y [OH-] son iguales, y el pH Si el modelo de Stewart es correcto, entonces podemos afir-
tiende a 7(2,6). mar que cualquier manipulación en alguna de las tres varia-
bles independientes cambiará la [H+], sin embargo hay que
PRESIÓN PARCIAL DE BIÓXIDO DE CARBONO: tomar en cuenta que el dióxido de carbono difunde libre-
PCO2 mente a través de todas las membranas, por lo que no puede
La presión parcial de bióxido de carbono afecta a todos los
edigraphic.com
ser usado para regular el pH. Las proteínas no cruzan intac-
tas las membranas biológicas y el fosfato es regulado en el
sistemas biológicos y su valor es determinado por factores riñón y el intestino para mantener la homeostasis de calcio
externos al sistema químico de los fluidos corporales(3,7). Es más que para regular el pH. Entonces, el SID es el mecanis-
por esto que se le conoce como variable independiente. mo para generar ajustes en el pH(3,4,6,7).
Volumen 29, No. 4, octubre-diciembre 2006 243
Häubi SC y cols. Teoría ácido-básico de Stewart, un nuevo paradigma en medicina crítica
CLASIFICACIÓN DE LAS ALTERACIONES CONCLUSIÓN
ÁCIDO-BASE USANDO EL MÉTODO DE STEWART
Los procesos metabólicos generan la producción de áci-
La división de las alteraciones ácido-base se basa en los dos orgánicos y en consecuencia se requiere de mecanis-
cambios de las variables independientes. La alcalosis o aci- mos que mantengan un equilibrio en la concentración de
dosis respiratoria son aquéllas cuya variable afectada es la hidrogeniones, tanto fuera como dentro de las células,
PCO2. La respuesta compensadora se debe a cambios en la estos procesos a lo largo de un siglo los hemos entendido
SID plasmática(3,6). y explicado mediante la ecuación de Henderson y Has-
La acidosis metabólica puede ser considerada como un selbach, sin embargo se han identificado algunos proble-
aumento en las condiciones que causan reducción del SID o mas con su interpretación por lo que hace más de veinte
incremento de la [ATOT]. A la inversa la alcalosis metabólica años, Stewart propuso una teoría novedosa replanteando
se define como un proceso en donde el SID plasmático au- algunos conceptos químicos aplicados a la teoría ácido-
menta o la [ATOT] disminuye(3,6). base.
REFERENCIAS
1. Equilibrio ácido-básico. En: Herman Villarreal. Riñón y Electro- 5. Stewart PA. Moderns quantitative acid-base chemistry. Can J
lítos. México: Librería de Medicina; 1979:77-91. Physiol Pharmacol 1983;61:1441-1461.
2. La teoría de Stewart. En: Häubi SC. Teoría ácido-básico de Stewart: 6. Corey HE. Stewart and beyond: New models of acid-base ba-
Aplicaciones prácticas de una nueva teoría de la regulación del lance. Kidney International 2003;64:777-787.
pH en los sistemas biológicos. México: Editorial Cigome S.A. de
7. Story DA, Morimatsu H, Bellomo R. Strong ions, weak acids
C.V.; 2004:35-67.
and base excess: a simplified Fencl-Stewart approach to clini-
3. Sirker AA, Rhodes A, Grounds RM, Bennett ED. Acid-base phy-
siology: the “traditional” and the “modern” approaches. Anaes- cal acid-base disorders. British Journal of Anaesthesia 2004;92:
thesia 2002;57:348-356. 54-60.
4. Carreira F, Anderson RJ. Assessing metabolic acidosis in the in- 8. Fisiología y fisiopatología del equilibrio ácido-base. En: Díaz de
tensive care unit: Does the method make a difference? Crit Care León PM, Briones GJC, Vázquez AFG. Medicina Aguda. México
Med 2004;32:2131-2132. Editorial Prado; 2006:111-136.
edigraphic.com
244 Revista Mexicana de Anestesiología
También podría gustarte
- Manual Alteraciones Del Equilibrio Acido Base 2020pdfpdfDocumento42 páginasManual Alteraciones Del Equilibrio Acido Base 2020pdfpdfsonia isanami75% (4)
- Sindrome Diarreico - 2022Documento2 páginasSindrome Diarreico - 2022Emerson Chasis Calibre CalibreAún no hay calificaciones
- Cirugia Toracica GeneralidadesDocumento40 páginasCirugia Toracica GeneralidadesILIA DA SILVA CARVALHOAún no hay calificaciones
- Gold 2020 Report PDFDocumento141 páginasGold 2020 Report PDFKaren100% (1)
- Anestesia y Electrofisiologia IDocumento15 páginasAnestesia y Electrofisiologia IJohnnie SmithAún no hay calificaciones
- Aranalde - Bases Fisiopatológicas Del EAB PDFDocumento21 páginasAranalde - Bases Fisiopatológicas Del EAB PDFcesar alonsoAún no hay calificaciones
- Tecnología PetroquímicaDocumento18 páginasTecnología PetroquímicamauriceAún no hay calificaciones
- Tren de Fuerza Camion 795F AcDocumento111 páginasTren de Fuerza Camion 795F AcGabo Gabo100% (1)
- Interpretacion Gasometrica RazaDocumento8 páginasInterpretacion Gasometrica RazaEnrique Vazquez RodriguezAún no hay calificaciones
- Retroperitoneo e Inervación de Vejiga y UretraDocumento5 páginasRetroperitoneo e Inervación de Vejiga y UretraFranco ConfalonieriAún no hay calificaciones
- Hemodinamia Básica 2012Documento5 páginasHemodinamia Básica 2012TJHORNAAún no hay calificaciones
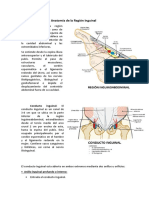
- Anatomía de La Región InguinalDocumento4 páginasAnatomía de La Región InguinalNachy SalcedoAún no hay calificaciones
- Exploracion Neurologica en UrgenciaDocumento4 páginasExploracion Neurologica en Urgenciaarielb08100% (2)
- Resumen GoicDocumento103 páginasResumen GoicIgnacioNacho ReyesAún no hay calificaciones
- Posibles Complicaciones Tras La Cirugia Con Circulacion ExtracorporeaDocumento5 páginasPosibles Complicaciones Tras La Cirugia Con Circulacion ExtracorporeaAndrés Flores Fornés100% (1)
- Manejo Inicial Shock SépticoDocumento48 páginasManejo Inicial Shock SépticoFrancisco Javier Gonzalez NomeAún no hay calificaciones
- Monitorizacion HemodinamicaDocumento10 páginasMonitorizacion Hemodinamicareinaldo valdes iznagaAún no hay calificaciones
- DR Barreto UCI PediátricaDocumento27 páginasDR Barreto UCI PediátricaAmira Cortés100% (3)
- Semiología Neurológica IIDocumento25 páginasSemiología Neurológica IINicolas GangasAún no hay calificaciones
- Tomografia CerebralDocumento39 páginasTomografia CerebralCarlosYovadSaldamandoCruz100% (1)
- Manual de PediatriaDocumento11 páginasManual de PediatriaLucia CoxAún no hay calificaciones
- Eco para Dgo.Documento74 páginasEco para Dgo.Carlos AlvaAún no hay calificaciones
- Biosíntesis Del Péptidoglicano de MureínaDocumento8 páginasBiosíntesis Del Péptidoglicano de MureínaRUTH MIRIAM TORRES SILVAAún no hay calificaciones
- Parte13 Alteraciones Del Equilibrio Acido Base - Cruz MenaDocumento13 páginasParte13 Alteraciones Del Equilibrio Acido Base - Cruz MenaJavier Ignacio Urrutia FigueroaAún no hay calificaciones
- Sindrome de Lisis TumoralDocumento16 páginasSindrome de Lisis TumoralVilma GerardoAún no hay calificaciones
- Total Burn Care 2018-266-281Documento16 páginasTotal Burn Care 2018-266-281Talia OrtizAún no hay calificaciones
- Caso Clinico de GastroenterologiaDocumento13 páginasCaso Clinico de GastroenterologiaJose Andres Villavicencio CallisayaAún no hay calificaciones
- Actualizacion Separ Diagnostico Tratamiento Derrame Pleural 2022Documento29 páginasActualizacion Separ Diagnostico Tratamiento Derrame Pleural 2022Ale JimenezAún no hay calificaciones
- Captíulo Cefaleas ImagenDocumento26 páginasCaptíulo Cefaleas Imagenjeporta100% (1)
- Protocolo MAPA MONITOREO AMBULATORIO DE PRESION ARTERIAL ABPM 3A PDFDocumento6 páginasProtocolo MAPA MONITOREO AMBULATORIO DE PRESION ARTERIAL ABPM 3A PDFJavier LagunaAún no hay calificaciones
- Fondo de Ojo Parte IDocumento20 páginasFondo de Ojo Parte IBegoña Molina SamosAún no hay calificaciones
- 8 - Sistema de Conduccion Del Corazon PDFDocumento23 páginas8 - Sistema de Conduccion Del Corazon PDFJehonnesAún no hay calificaciones
- Metabolismo Del Agua y ElectrolitosDocumento16 páginasMetabolismo Del Agua y ElectrolitosEricka Danuskka SandovalAún no hay calificaciones
- Electrocardiograma en PediatriaDocumento56 páginasElectrocardiograma en PediatriaestradivarioAún no hay calificaciones
- Taquiarritmias 150831013130 Lva1 App6892Documento43 páginasTaquiarritmias 150831013130 Lva1 App6892karla lozada100% (1)
- Laboratorio N°2 Fisiologia PDFDocumento23 páginasLaboratorio N°2 Fisiologia PDFPineda Perdomo José MiguelAún no hay calificaciones
- Avances en El Tratamiento de La Tuberculosis MultirresistenteDocumento39 páginasAvances en El Tratamiento de La Tuberculosis MultirresistentewachobestAún no hay calificaciones
- Ultrasonido PulmonarDocumento36 páginasUltrasonido Pulmonaryudi lopez100% (3)
- Electrocardiograma PDFDocumento4 páginasElectrocardiograma PDFMayrelis BohorquezAún no hay calificaciones
- Pericarditis AgudaDocumento27 páginasPericarditis AgudaCesar Giovanni Cordova100% (1)
- Trauma AbdominalDocumento12 páginasTrauma AbdominalSimonGonzalezAponteAún no hay calificaciones
- Generalidades en ColoproctologiaDocumento115 páginasGeneralidades en ColoproctologiaBlas Eduardo Quintero SadaAún no hay calificaciones
- Gradiente Alveolo ArterialDocumento2 páginasGradiente Alveolo Arterialcelecoxib200Aún no hay calificaciones
- Metodos Estudio CV HOLTER PDFDocumento13 páginasMetodos Estudio CV HOLTER PDFJ Sebastian SepulvedaAún no hay calificaciones
- VPP y Oclusion de La Arteria PulmonarDocumento8 páginasVPP y Oclusion de La Arteria PulmonarPedro SalamancaAún no hay calificaciones
- Protocolo de GasometriaDocumento4 páginasProtocolo de GasometriayurilsAún no hay calificaciones
- 1219 Presentación Electrónica Educativa 1308 1-10-20190222Documento24 páginas1219 Presentación Electrónica Educativa 1308 1-10-20190222Angie Lizeth VillamarinAún no hay calificaciones
- Hemorragia Cerebral HipertensivaDocumento26 páginasHemorragia Cerebral HipertensivaYuliana Rubi CastilloAún no hay calificaciones
- Fracturas Diafisarias de La Pierna, Maleolares, Supramaleolares y Lesiones de TobilloDocumento13 páginasFracturas Diafisarias de La Pierna, Maleolares, Supramaleolares y Lesiones de TobilloLuis José López OsiliaAún no hay calificaciones
- Piso Pelvico FemeninoDocumento7 páginasPiso Pelvico FemeninofernandezAún no hay calificaciones
- Resumen Transferencia Placentaria de FarmacosDocumento7 páginasResumen Transferencia Placentaria de FarmacosJ_r_f_mAún no hay calificaciones
- 7ma Clase Neuro Degraba - CerebeloDocumento10 páginas7ma Clase Neuro Degraba - CerebeloHinO - ArturoAún no hay calificaciones
- Planos de HodgeDocumento24 páginasPlanos de HodgeEstephanie Perez EscobarAún no hay calificaciones
- Teoria Stewart Rma - DesbloqueadoDocumento8 páginasTeoria Stewart Rma - DesbloqueadoJosé Luis CeballosAún no hay calificaciones
- 07 Estado ÁcidoDocumento63 páginas07 Estado ÁcidoCarla Gisela GutierrezAún no hay calificaciones
- Equilibrio Ácido-BaseDocumento18 páginasEquilibrio Ácido-BaseMiguel Angel Rodas HerreraAún no hay calificaciones
- Acido Base Conceptos ActualesDocumento9 páginasAcido Base Conceptos ActualesLuna Sanchez SAún no hay calificaciones
- Revista Española de Anestesiología y ReanimaciónDocumento8 páginasRevista Española de Anestesiología y Reanimacióngonzalezelizondo22Aún no hay calificaciones
- Seminario de PHDocumento8 páginasSeminario de PHJohn ConnorAún no hay calificaciones
- Metodo Stewart PDFDocumento8 páginasMetodo Stewart PDFAddii M. CervantesAún no hay calificaciones
- Informe de BioquímicaDocumento8 páginasInforme de Bioquímicaarelismartinez931Aún no hay calificaciones
- Facultad de MedicinaDocumento5 páginasFacultad de Medicinajohnnie “johnnie el crack” contrerasAún no hay calificaciones
- TESLA y Las Piramides de BosniaDocumento6 páginasTESLA y Las Piramides de BosniaAdriana NovilloAún no hay calificaciones
- Procedimiento de Trabajo Desmontaje, Transporte e Instalación Del Lavador de Gases de IntradevcoDocumento20 páginasProcedimiento de Trabajo Desmontaje, Transporte e Instalación Del Lavador de Gases de IntradevcoFreddy PorrasAún no hay calificaciones
- Instalacion Solar Fotovoltaica para El Bombeo de AGUADocumento57 páginasInstalacion Solar Fotovoltaica para El Bombeo de AGUAjavier100% (1)
- Laboratorio Fisica 2-6Documento8 páginasLaboratorio Fisica 2-6Luigyen MejiaAún no hay calificaciones
- Introducción OladeDocumento11 páginasIntroducción OladeJavier Antonio Cardenas OliverosAún no hay calificaciones
- Teorema TorricelliDocumento12 páginasTeorema TorricelliDaniela PachecoAún no hay calificaciones
- Tablas de SAP Ventajas y DesventajasDocumento10 páginasTablas de SAP Ventajas y DesventajasCinthia RayaAún no hay calificaciones
- Cm2 Act4 EhmDocumento12 páginasCm2 Act4 EhmEdgar Hernadez MezaAún no hay calificaciones
- TransformadorDocumento23 páginasTransformadorElePirataAún no hay calificaciones
- Electromagnetismo Generador Transformador PDFDocumento8 páginasElectromagnetismo Generador Transformador PDFRicardo Aparicio MontemayorAún no hay calificaciones
- Evaluación DiagnósticaDocumento8 páginasEvaluación DiagnósticaChristian Vergara FernándezAún no hay calificaciones
- Manual de Usuario TS F100Documento6 páginasManual de Usuario TS F100MarkochinoAún no hay calificaciones
- Cuadro Comparativo Modulo 4Documento5 páginasCuadro Comparativo Modulo 4Najhomy RamirezAún no hay calificaciones
- El Pensador SistémicoDocumento82 páginasEl Pensador SistémicocindyAún no hay calificaciones
- Pendulo SimpleDocumento3 páginasPendulo SimpleWilliam Taipe50% (2)
- Equipo Workover FrankDocumento3 páginasEquipo Workover FrankJosé Timaná75% (4)
- FisicaA Aintradora3Documento5 páginasFisicaA Aintradora3Alan Ruben EspinozaAún no hay calificaciones
- Cotización CamionetaDocumento11 páginasCotización CamionetaSemat SacAún no hay calificaciones
- Integrantes:: O Coronel Tarazona Ana O Navarro Monje BlancaDocumento20 páginasIntegrantes:: O Coronel Tarazona Ana O Navarro Monje BlancaJohnatan ChinininAún no hay calificaciones
- 5 - Termometros Termostatos Digitales AkoDocumento5 páginas5 - Termometros Termostatos Digitales AkoAngel Pérez SantiagoAún no hay calificaciones
- Valoracion de Los Recursos NaturalesDocumento21 páginasValoracion de Los Recursos NaturalesC Alemán JhosuaAún no hay calificaciones
- Tarea 3. Programa de MantenimientoDocumento8 páginasTarea 3. Programa de MantenimientoARZETA GOMEZ EDITHAún no hay calificaciones
- Energía y Potencia EléctricasDocumento3 páginasEnergía y Potencia EléctricasLito RamìrezAún no hay calificaciones
- Baño MariaDocumento12 páginasBaño MariaLuis M. Chamoso100% (1)
- Mobil Delvac 1320-1330-1340-1350 - ESPDocumento2 páginasMobil Delvac 1320-1330-1340-1350 - ESPMaxAún no hay calificaciones
- Cel Consulta 2Documento174 páginasCel Consulta 2Aristegui NoticiasAún no hay calificaciones
- Sesion 1 - Planta de Generación de VaporDocumento64 páginasSesion 1 - Planta de Generación de VaporGary Manuel Rodriguez RodriguezAún no hay calificaciones
- Pe3 XX YyestabDocumento11 páginasPe3 XX YyestabMefu NaronAún no hay calificaciones