Documentos de Académico
Documentos de Profesional
Documentos de Cultura
cristalización 3
Cargado por
AficiompDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
cristalización 3
Cargado por
AficiompCopyright:
Formatos disponibles
Instituto Sagrado Corazón A-111
Química 4ºA y B- Prof. Barreneche, Ignacio
TRABAJO PRÁCTICO DE LABORATORIO Nº2
CRISTALIZACIÓN- REDES CRISTALINAS
Fundamentos de la Cristalografía
Un cristal de una determinada sustancia o material tiene caras planas que presentan
siempre los mismos ángulos con sus vecinas, así como todas las otras propiedades regulares,
debido a que está formado por átomos, iones o moléculas dispuestas de una manera muy
ordenada. Este ordenamiento estructural se encuentra en casi toda la materia sólida,
aunque unas sustancias muestran una disposición más ordenada que otras. Una sustancia
formada a partir de cristales se denomina cristalina.
El fenómeno de la cristalización puede darse a través de diversas vías y es, en general, un
proceso lento que depende de factores tales como la temperatura, la velocidad de
evaporación del solvente, la pureza de las sustancias, étc.
Ensayo Nº1: Cristales de Naftaleno a partir de sus vapores
Materiales: Mortero; pilón; naftaleno; vaso de precipitados pequeño; vidrio de reloj;
mechero
Técnica:
Cuando el naftaleno se calienta suavemente pasa rápidamente a estado vapor (su punto de
fusión es de 80° C y su punto de ebullición es de 218° C). Su fuerte tendencia a pasar al
estado vapor es una de las propiedades que le hacen útil para proteger la ropa frente a las
polillas.
Una forma conveniente de hacer crecer cristales de naftaleno es la siguiente:
introduzca una pequeña cantidad de naftaleno sólido (media cucharadita) en el fondo
de un frasco alto de vidrio. Coloque una tapa amplia sobre el frasco.
Muy pronto (si ilumina con la linterna de su celular) podrá observar que empiezan a
formarse pequeños cristales en la parte superior del frasco, donde el invisible y cálido
vapor de naftaleno se enfría y la atracción mutua entre las partículas de naftaleno las
junta en la disposición ordenada de un cristal.
En este ensayo hemos obtenido pequeñísimos cristales a partir de los vapores de la
sustancia. (Podríamos experimentar lo mismo con Yodo).
Instituto Sagrado Corazón A-111
Química 4ºA y B- Prof. Barreneche, Ignacio
Ensayo Nº2: Obtención y crecimiento de un monocristal de
Sulfato (VI) de Cobre (II) pentahidratado. (CuSO4.5 H2O).
Materiales: Vaso de precipitados, termómetro, sulfato cúprico, espátula, mechero, varilla,
cristalizador o caja de Petri, balanza, probeta, embudo, papel de filtro, soporte universal,
hilo o tanza
Técnica:
Antes de iniciar propongo que veamos este pequeño video que se encuentra en la página
http://www.cristalografia.com.ar:
https://www.youtube.com/watch?time_continue=126&v=cNyQ_pMGxWs
En primer lugar, debemos preparar una solución saturada. Para ello será necesario contar
con los datos de solubilidad de ese sólido a distintas temperaturas:
Tener en cuenta que esta tabla de valores expresa qué masa de
sulfato de cobre puede disolverse, a cierta temperatura, en 1
litro de agua (es decir 1000 g o 1000 ml de agua).
Calculemos:
a) ¿Qué masa de soluto podemos disolver, a 20 ºC, en 25 ml de
agua?
b) ¿Qué masa de soluto podemos disolver, a 60ºC, en 25 ml de
agua?
¿Qué sucedería si a la solución saturada a 60 ºC la dejamos
enfriar hasta llegar a temperatura ambiente?
Disolver, en un vaso de precipitados, la masa de sulfato de cobre que sea capaz de
disolverse en 25 ml de agua a 60ºC. A continuación se filtran las impurezas con un
embudo y papel de filtro de café y se vierte la disolución en un cristalizador, colocado
en un lugar muy estable (sin vibraciones). Unas horas después aparecerán varios cristales
pequeños en el fondo del cristalizador (nosotros deberemos verlo la próxima clase).
Se extrae de la disolución el de mayor tamaño y se ata al hilo o a la tanza, que debe estar
muy limpio; el otro extremo del hilo se ata al palito o al lápiz. Con la balanza determinar la
masa de ese cristal apartado del sistema (cristal “semilla”).
Preparar una solución sobresaturada a 60ºC; en ella debemos añadir una masa de sulfato
que, aproximadamente, duplique la masa admitida para esa temperatura. Se filtra la
disolución y se vierte en un vaso limpio. Transcurrido el tiempo necesario para que la
disolución se enfríe, se introduce el cristal en la disolución. En un día el cristal de sulfato
de cobre (II) se hará mucho más grande, agotando su “combustible”. Retirar el cristal,
determinar su masa y comparar con la masa del cristal “semilla”. ES UN PROCESO LENTO
QUE LLEVARÁ AL MENOS 2 o 3 SEMANAS.
Podemos ver el siguiente video…https://vimeo.com/136989392
También podría gustarte
- Mi Primer Pecera Todo lo que Necesitas Saber para Iniciarte en el Cuidado de los PecesDe EverandMi Primer Pecera Todo lo que Necesitas Saber para Iniciarte en el Cuidado de los PecesAún no hay calificaciones
- Laboratorio 3ºDocumento9 páginasLaboratorio 3ºYamix QuispeAún no hay calificaciones
- Reporte Sal RochelleDocumento9 páginasReporte Sal RochelleVictor CarreraAún no hay calificaciones
- CristalizaciónDocumento2 páginasCristalizaciónMario MartinAún no hay calificaciones
- Formacion de CristalesDocumento2 páginasFormacion de CristalesgloriababysupapaesgaAún no hay calificaciones
- Exposición CristalizaciónDocumento11 páginasExposición CristalizaciónAlexis PokepulgaAún no hay calificaciones
- Determinación de La Curva de Solubilidad y Formación de CristalesDocumento6 páginasDeterminación de La Curva de Solubilidad y Formación de CristalesRoy Michael Guerra Aranda100% (1)
- Cristalización de sustancias por disolución y sublimaciónDocumento4 páginasCristalización de sustancias por disolución y sublimaciónSantiago CuellarAún no hay calificaciones
- Cristalización: Purificación de compuestosDocumento10 páginasCristalización: Purificación de compuestosSabrina PestanaAún no hay calificaciones
- CristalizacionDocumento11 páginasCristalizacionAnto LatgAún no hay calificaciones
- CristalizacionDocumento7 páginasCristalizacionAraceli Gp GRAún no hay calificaciones
- Estado SolidoDocumento5 páginasEstado SolidoAndrés ParedesAún no hay calificaciones
- Cuestionario de CristalizacionDocumento7 páginasCuestionario de CristalizacionMario Hernandez100% (3)
- Experimento 3. Propiedades Del Estado SólidoDocumento9 páginasExperimento 3. Propiedades Del Estado SólidoELVIS MORENOAún no hay calificaciones
- Informe de CriztalizacionDocumento9 páginasInforme de CriztalizacionCristhian UrbanoAún no hay calificaciones
- Cristalizacinnnnennlab 5060a68d71a221fDocumento5 páginasCristalizacinnnnennlab 5060a68d71a221fsusana tamayo0% (1)
- Siembra de Cristales de Cloruro de SodioDocumento5 páginasSiembra de Cristales de Cloruro de SodioOscar .SoberanoAún no hay calificaciones
- Informe 5 - Recristalizacion de Productos OrganicosDocumento10 páginasInforme 5 - Recristalizacion de Productos OrganicosCarlos MenesesAún no hay calificaciones
- Determinacion de CristalizacionDocumento9 páginasDeterminacion de CristalizacionCristian Orozco ChavezAún no hay calificaciones
- Atomos y Moleculas CristalizaciónDocumento13 páginasAtomos y Moleculas CristalizaciónMauricio AlvaradoAún no hay calificaciones
- Cristalizacion QuimicaDocumento5 páginasCristalizacion QuimicaDevis UrbaezAún no hay calificaciones
- Practica Nº2 Operaciones BasicasDocumento5 páginasPractica Nº2 Operaciones BasicasQUÍMICA0% (1)
- Manual Kit Cristal I Zac I OnDocumento12 páginasManual Kit Cristal I Zac I OnsusiferreyraAún no hay calificaciones
- Diapositivas Materiales de IngenieriaDocumento20 páginasDiapositivas Materiales de Ingenieriadebbie tatiana blanco plazasAún no hay calificaciones
- Cristalización de sustancias inorgánicas en el laboratorio de Química General IIDocumento44 páginasCristalización de sustancias inorgánicas en el laboratorio de Química General IIRonal Blari Chambi Mamani100% (1)
- Recristalizacion 18 BDocumento14 páginasRecristalizacion 18 BMiranda DanielAún no hay calificaciones
- Practice 3 Separation of Mixtures (Separacion de Mezclas)Documento10 páginasPractice 3 Separation of Mixtures (Separacion de Mezclas)Сау-л Сантьяго РуисAún no hay calificaciones
- Informe de Cristalografía Con Sulfato de CobreDocumento9 páginasInforme de Cristalografía Con Sulfato de CobreJuan SejasAún no hay calificaciones
- Estereoisomería CisDocumento4 páginasEstereoisomería CisMaria JaraAún no hay calificaciones
- Práctica #2Documento7 páginasPráctica #2Mio PhamthomAún no hay calificaciones
- Crsitalizacion de Sulfato de CobreDocumento6 páginasCrsitalizacion de Sulfato de CobreStefany HerreraAún no hay calificaciones
- Informe 3 de InorganicaDocumento7 páginasInforme 3 de InorganicaSergio Leonardo Elias Carbajal DiazAún no hay calificaciones
- Lab Métodos de CristalizacionDocumento11 páginasLab Métodos de CristalizacionJonás Correa PérezAún no hay calificaciones
- Bitacora Del Sulfato de CobreDocumento9 páginasBitacora Del Sulfato de Cobrejose paoloAún no hay calificaciones
- INFORME 4 - RecristalizacionDocumento12 páginasINFORME 4 - RecristalizacionJhimiChavezOAún no hay calificaciones
- Manual de Fotografía y Elementos de Qu-3Documento50 páginasManual de Fotografía y Elementos de Qu-3Instituto de Estudios Críticos en HumanidadesAún no hay calificaciones
- Practica de CristalizaciónDocumento10 páginasPractica de CristalizaciónJoanna HernándezAún no hay calificaciones
- Informe No. 3 Separación de Mezclas. Recristalización y Destilación, CompletoDocumento7 páginasInforme No. 3 Separación de Mezclas. Recristalización y Destilación, CompletoMelissa Andrea Villalobos VásquezAún no hay calificaciones
- Laboratorio Recristalizacion UnmsmDocumento8 páginasLaboratorio Recristalizacion UnmsmElizabethVargasAún no hay calificaciones
- Practica 2 Cristalización SimpleDocumento7 páginasPractica 2 Cristalización SimpleGiovanny Tapia Carlos0% (1)
- PratocaDocumento5 páginasPratocaDavid CaalAún no hay calificaciones
- Informe Cristalización Química OrgánicaDocumento10 páginasInforme Cristalización Química OrgánicaCamilaTrilloAún no hay calificaciones
- Manual Separa y Purifica 2024Documento20 páginasManual Separa y Purifica 2024EderthAún no hay calificaciones
- Practica de CrislaizacionDocumento5 páginasPractica de CrislaizacionARTURO BUENROSTRO GALLEGOSAún no hay calificaciones
- Informe Cristalización LL y LLLDocumento10 páginasInforme Cristalización LL y LLLAtescatenco Maldonado Jorge LuisAún no hay calificaciones
- Lab 3 RecristalizacionDocumento8 páginasLab 3 RecristalizacionDavid AriasAún no hay calificaciones
- UntitledDocumento27 páginasUntitledGisell Yadhira Mariño ParionaAún no hay calificaciones
- QuimmicaDocumento26 páginasQuimmicaAdrian C LermoAún no hay calificaciones
- Informe Sobre AspirinaDocumento26 páginasInforme Sobre AspirinaHenry TrujilloAún no hay calificaciones
- Laboratorio Quimica 7Documento7 páginasLaboratorio Quimica 7Patrick Jara cruzadoAún no hay calificaciones
- Balance de Materia InforDocumento12 páginasBalance de Materia InforPillco PillcoAún no hay calificaciones
- Informe Practica 6Documento14 páginasInforme Practica 6Ivan AlquiciraAún no hay calificaciones
- Destilador casero económico y fácilDocumento13 páginasDestilador casero económico y fácilana velazcoAún no hay calificaciones
- Lab 02 InorganicaDocumento5 páginasLab 02 InorganicaCamila Marmolejo VergaraAún no hay calificaciones
- Prereporte W10Documento4 páginasPrereporte W10gg tttAún no hay calificaciones
- 365 curiosidades asombrosas de la Historia, la Ciencia y las ReligionesDe Everand365 curiosidades asombrosas de la Historia, la Ciencia y las ReligionesAún no hay calificaciones
- El ambiente acuoso para el tratamiento de obras polìcromasDe EverandEl ambiente acuoso para el tratamiento de obras polìcromasAún no hay calificaciones
- Patología Vegetal y TerapeúticaDocumento45 páginasPatología Vegetal y TerapeúticaAficiompAún no hay calificaciones
- Todo sobre egagrópilasDocumento75 páginasTodo sobre egagrópilasAficiompAún no hay calificaciones
- Plantas estresadasDocumento17 páginasPlantas estresadasAficiompAún no hay calificaciones
- Ficha Clostridium TetaniDocumento4 páginasFicha Clostridium TetanijaimeSanchezQAún no hay calificaciones
- Sexo BacteriasDocumento23 páginasSexo Bacteriasalemartin000Aún no hay calificaciones
- PCRDocumento22 páginasPCRAnnie PérezAún no hay calificaciones
- Aplicaciones de NitrosomonasDocumento65 páginasAplicaciones de NitrosomonasAficiompAún no hay calificaciones
- Sexo BacteriasDocumento23 páginasSexo Bacteriasalemartin000Aún no hay calificaciones
- SARS-CoV-2 y Pandemia de Síndrome Respiratorio Agudo (COVID-19)Documento17 páginasSARS-CoV-2 y Pandemia de Síndrome Respiratorio Agudo (COVID-19)Cami MenesesAún no hay calificaciones
- GlucolisisDocumento3 páginasGlucolisisYuritzi QuintanaAún no hay calificaciones
- Inmunidad Celular y HumoralDocumento18 páginasInmunidad Celular y HumoralDavid MirandaAún no hay calificaciones
- InmunitariaDocumento19 páginasInmunitariaMax RossiAún no hay calificaciones
- Guía COVID-19 incubación y transmisiónDocumento8 páginasGuía COVID-19 incubación y transmisiónAficiompAún no hay calificaciones
- LevaduraS CerevisiaeylaproduccindealcoholDocumento25 páginasLevaduraS CerevisiaeylaproduccindealcoholAficiompAún no hay calificaciones
- Cinética Crecimiento LactobacillusDocumento14 páginasCinética Crecimiento LactobacillusAficiompAún no hay calificaciones
- EP4 - Guia DidacticaDocumento15 páginasEP4 - Guia DidacticaElizabeth VillavicencioAún no hay calificaciones
- InmunitariaDocumento19 páginasInmunitariaMax RossiAún no hay calificaciones
- 4 - Capítulo I. Las Enzimas PDFDocumento99 páginas4 - Capítulo I. Las Enzimas PDFyulleyAún no hay calificaciones
- It Corona VirusDocumento111 páginasIt Corona VirusJuan Bada CañibanoAún no hay calificaciones
- 4 - Capítulo I. Las Enzimas PDFDocumento99 páginas4 - Capítulo I. Las Enzimas PDFyulleyAún no hay calificaciones
- EP4 - Guia DidacticaDocumento15 páginasEP4 - Guia DidacticaElizabeth VillavicencioAún no hay calificaciones
- Inmunidad Celular y HumoralDocumento18 páginasInmunidad Celular y HumoralDavid MirandaAún no hay calificaciones
- PCRDocumento22 páginasPCRAnnie PérezAún no hay calificaciones
- Inmunoglobulinas PDFDocumento23 páginasInmunoglobulinas PDFClaudia Patricia Ballen GarzonAún no hay calificaciones
- SARS-CoV-2 y Pandemia de Síndrome Respiratorio Agudo (COVID-19)Documento17 páginasSARS-CoV-2 y Pandemia de Síndrome Respiratorio Agudo (COVID-19)Cami MenesesAún no hay calificaciones
- Inmunoglobulinas PDFDocumento23 páginasInmunoglobulinas PDFClaudia Patricia Ballen GarzonAún no hay calificaciones
- Guía COVID-19 incubación y transmisiónDocumento8 páginasGuía COVID-19 incubación y transmisiónAficiompAún no hay calificaciones
- Tecnicas Clonación BovinosDocumento25 páginasTecnicas Clonación BovinosAficiompAún no hay calificaciones
- It Corona VirusDocumento111 páginasIt Corona VirusJuan Bada CañibanoAún no hay calificaciones
- Practica Calificada 1 y RubricamayrolDocumento13 páginasPractica Calificada 1 y RubricamayrolMayrol MbqfAún no hay calificaciones
- Taller Sustancias Puras-Ingenieras-grupo 3Documento10 páginasTaller Sustancias Puras-Ingenieras-grupo 3Katerin MedinaAún no hay calificaciones
- 8) Ecuaciones DiferencialesDocumento15 páginas8) Ecuaciones DiferencialesJana Vecchio RomeroAún no hay calificaciones
- Partículas elementales: Simplificaciones para calcular tasas de decaimiento de muon y neutrónDocumento14 páginasPartículas elementales: Simplificaciones para calcular tasas de decaimiento de muon y neutrónariadna100% (1)
- Moreno Huerta Jose de Jesus: Rmu: 58290 20-07-20 XAXX-010101 005 CFEDocumento2 páginasMoreno Huerta Jose de Jesus: Rmu: 58290 20-07-20 XAXX-010101 005 CFEpapeleria el arbolAún no hay calificaciones
- FT Botín KI 303Documento1 páginaFT Botín KI 303solita_soleiAún no hay calificaciones
- Supervisor MonofasicoDocumento2 páginasSupervisor MonofasicoshamirAún no hay calificaciones
- Taller Soluciones AcuosasDocumento3 páginasTaller Soluciones AcuosasJuanesteban Montiel RiveraAún no hay calificaciones
- AST (Analisis de Trabajo Seguro)Documento2 páginasAST (Analisis de Trabajo Seguro)Belkis Salazar LagosAún no hay calificaciones
- Analisis 1Documento18 páginasAnalisis 1Euler Gonzalo LoarteAún no hay calificaciones
- Limpieza CroissomatDocumento24 páginasLimpieza CroissomatCarlos PerezAún no hay calificaciones
- Perfil Del Cargo SoldadorDocumento2 páginasPerfil Del Cargo SoldadorJavier Lojo100% (1)
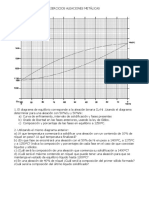
- Problemas ALEACIONES METÁLICASDocumento17 páginasProblemas ALEACIONES METÁLICASkoko10000Aún no hay calificaciones
- Informe de Equilibrio TermicoDocumento4 páginasInforme de Equilibrio TermicoBrayan VlAún no hay calificaciones
- ANÁLISIS ESTRUCTURASDocumento64 páginasANÁLISIS ESTRUCTURASJuancho CalaAún no hay calificaciones
- Procedimiento de Trabajo de Carga y DescargaDocumento14 páginasProcedimiento de Trabajo de Carga y DescargaCamila G9nzalezAún no hay calificaciones
- El Filtro de Grafeno - DiaposDocumento9 páginasEl Filtro de Grafeno - DiaposCristhian Argollo SapacayoAún no hay calificaciones
- Medidas eléctricas UNNE corrientes Foucault medidores energíaDocumento9 páginasMedidas eléctricas UNNE corrientes Foucault medidores energíarogelio de oliveraAún no hay calificaciones
- Examen de Maquinas Termicas IDocumento9 páginasExamen de Maquinas Termicas Ijhonny talledoAún no hay calificaciones
- TrabajoGrupo#12-CamposMagnetico CompressedDocumento12 páginasTrabajoGrupo#12-CamposMagnetico CompressedFiorela RodríguezAún no hay calificaciones
- Tarea Grupal 3Documento24 páginasTarea Grupal 3Jhina Maritza Garcia67% (3)
- Colada de Resina de Poliester PDFDocumento7 páginasColada de Resina de Poliester PDFNelson VargasAún no hay calificaciones
- Funcion Del Ingenio AzucareroDocumento16 páginasFuncion Del Ingenio AzucareroGustavo Chavez CalderonAún no hay calificaciones
- Polymobil Plus Brochure Español PDFDocumento8 páginasPolymobil Plus Brochure Español PDFMonica FajardoAún no hay calificaciones
- Curso-Basicodeinstalacionalarmas-111114084757-Phpapp02 (1) .PPSXDocumento72 páginasCurso-Basicodeinstalacionalarmas-111114084757-Phpapp02 (1) .PPSXMario Antonio Gonzalez PaineAún no hay calificaciones
- Taller 6 - Compuertas LógicasDocumento4 páginasTaller 6 - Compuertas Lógicasyanira perezAún no hay calificaciones
- Reparación aires acondicionados BBVA Of. SucreDocumento6 páginasReparación aires acondicionados BBVA Of. Sucrewilliam molinaAún no hay calificaciones
- Gas ideal vs real: leyes y conceptosDocumento24 páginasGas ideal vs real: leyes y conceptosangelkick42100% (2)
- Ensayo EstaticaDocumento8 páginasEnsayo EstaticaOctavioAún no hay calificaciones
- Planificadores Fisica 1BGU U3Documento7 páginasPlanificadores Fisica 1BGU U3luis jugadorAún no hay calificaciones