Documentos de Académico
Documentos de Profesional
Documentos de Cultura
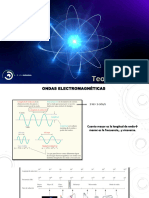
Teoría de MAX WELL
Cargado por
xolam0 calificaciones0% encontró este documento útil (0 votos)
4 vistas14 páginasTítulo original
teoría de MAX WELL (1)
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
4 vistas14 páginasTeoría de MAX WELL
Cargado por
xolamCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 14
El modelo de átomo planetario propuesto por
Rutherford mostró pronto algunos inconvenientes teóricos que
lo hacían inviable:
•Contradecía la teoría electromagnética de
Maxwell. Según esta teoría una carga eléctrica acelerada
debería de emitir ondas electromagnéticas. Un electrón al
girar en círculos alrededor del núcleo debería emitir, por tanto,
ondas electromagnéticas. Dicha emisión provocaría una
pérdida de energía que haría que el electrón
describiera órbitas de radio decreciente hasta caer sobre el
núcleo. El modelo atómico de Rutherford era, por tanto,
inviable desde el punto de vista de la física clásica.
•No daba una explicación
satisfactoria a los espectros
atómicos. Si encerramos en un tubo
hidrógeno o helio y sometemos el gas
a voltajes elevados, el gas emite luz. Si
hacemos pasar esa luz a través de un
prisma, los colores que la constituyen
se separan dándonos el espectro de la
luz analizada.
Pronto se concluyó que la emisión de luz podría deberse a
que los electrones absorbían energía de la corriente
eléctrica y saltaban a órbitas superiores para, a
continuación, volver a caer a las órbitas más próximas al
núcleo emitiendo el exceso de energía en forma de
energía luminosa.
Esta interpretación conducía, sin embargo, a afirmar que
los espectros deberían de ser continuos, ya que al existir
órbitas de cualquier radio (y energía) todos los saltos son
posibles. La experiencia, por el contrario, mostraba que
los espectros de los átomos son discontinuos. Constan de
rayas de diversos colores sobre un fondo negro
Arriba: espectro del hidrógeno (discontinuo)
Abajo: espectro de la luz solar (continuo)
EFECTO FOTOELÉCTRICO
Al incidir luz ultravioleta sobre el cátodo metálico (fotocátodo) se detecta el paso de una
corriente eléctrica. Se trata de electrones que abandonan el cátodo (colector) y se
dirigen al ánodo a través del vacío dentro del tubo. Los electrodos se hallan conectados a
una diferencia de potencial de sólo unos pocos voltios. La teoría electromagnética
clásica considera que la radiación de mayor intensidad (o brillo, si es visible), que
corresponde a ondas de mayor amplitud, transporta mayor energía. Esta energía se halla
distribuida uniformemente a lo largo del frente de onda. La intensidad es igual a la
energía que incide, cada unidad de tiempo, en una unidad de superficie.
Con radiación ultravioleta de diferentes intensidades, los electrones salen del metal con
la misma velocidad. La radiación más intensa arranca mayor número de electrones. Esta
observación también resultaba inexplicable
El principio de incertidumbre desempeñó un importante papel en el desarrollo de la
mecánica cuántica y en el progreso del pensamiento filosófico moderno. En mecánica
cuántica, la relación de indeterminación de Heisenberg o relación de incertidumbre de
Heisenberg afirma que no se puede determinar, simultáneamente y con precisión arbitraria,
ciertos pares de variables físicas, como son, por ejemplo, la posición y el momento lineal
(cantidad de movimiento) de un objeto dado. En otras palabras, cuanta mayor certeza se
busca en determinar la posición de una partícula, menos se conoce su cantidad de
movimiento lineal. Este principio fue enunciado por Werner Heisenberg en 1927. Si se
preparan varias copias idénticas de un sistema en un estado determinado las medidas de la
posición y el momento variarán de acuerdo con una cierta distribución de probabilidad
característica del estado cuántico del sistema. Las medidas del objeto observable sufrirá
desviación estándar Δx de la posición y el momento Δp verifican entonces el principio de
incertidumbre que se expresa matemáticamente como:
Números cuánticos. Las expresiones matemáticas de la mecánica
ondulatoria indican que el estado de energía de un electrón en un átomo se
puede describir por medio de un set de cuatro números, llamados números
cuánticos. Estos números describen el orbital espacial en el que el electrón
se mueve en términos de (1) su posición con respecto al núcleo, (2) su
forma, (3) su orientación espacial y (4) la dirección del spin (giro alrededor
del propio eje) del electrón en el orbital.
El número cuántico principal, simbolizado por n, indica la distancia
promedio del electrón desde el núcleo. Es una integral positiva, con valores
1, 2, 3, 4,...... y es la designación del nivel de energía principal de un orbital.
El primer nivel de energía es más cercano al núcleo y los otros se
encuentran a distancias crecientes. Los electrones del primer nivel de
energía tienen las energías más bajas, mientras que los de los niveles más
altos tienen niveles de energía crecientes. En algunos textos, los niveles de
energía se designan por las letras K, L, M, N, etc.
El número cuántico principal, n, determina el tamaño del orbital. Puede tomar
cualquier valor natural distinto de cero: n = 1, 2, 3, 4. Varios orbitales pueden
tener el mismo número cuántico principal, y de hecho lo tienen, agrupándose
en capas. Los orbitales que tienen el mismo número cuántico principal forman
una capa electrónica. Cuanto mayor sea el número cuántico principal, mayor
será el tamaño del orbital y, a la vez, más lejos del núcleo estará situado.
El número cuántico orbital, indica la forma del orbital en el que se mueve el
electrón. El número de posibles formas es igual al valor del número cuántico
principal n. En el enésimo nivel de energía hay orbitales de n formas posibles.
En el primer nivel es posible un orbital de una sola forma, en el segundo son
posibles de dos formas, en el tercero de tres, etc. Como ya se indicó las
designaciones de los cuatro primeros números cuánticos orbitales es s, p, d, y
f. Están escritos en orden de energía creciente. Así, para un nivel de energía
particular, el orbital s tiene menor energía que el p, el p menor que el d y el d
menor que el f. .
El número cuántico magnético: Indica la orientación
del orbital, cuya forma está dada por el número
cuántico orbital, en relación a los tres ejes del
espacio, en un campo magnético. Hay sólo una
orientación para un orbital s, mientras que hay tres
para el orbital p, cinco para el orbital d y siete para el
f. El número cuántico magnético, m, determina la
orientación del orbital. Los valores que puede tomar
depende del valor del número cuántico azimutal, m,
variando desde - l hasta + l.
Distribución electrónica en sistemas polielectrónicos La ecuación
de onda de Schrodinger no tiene solución exacta. Hay que
introducir soluciones aproximadas: Los orbitales atómicos son
semejantes a los del hidrógeno. También se pueden emplear los
mismos números cuánticos (n, l, m l) para describir los orbitales
Sistemas con más de 1 electrón, hay que tener en cuenta:
Cuarto número cuántico (ms) Limitar nº electrones por orbital (P.
Exclusión Pauli) Conjunto de niveles de energía más complejo La
configuración electrónica de un átomo es la distribución de los
electrones en los subniveles de energía del átomo. La
configuración electrónica de un átomo se obtiene escribiendo en
orden ascendente de energía los símbolos de los subniveles
ocupados indicando el número de electrones que contiene.
El número de electrones que ocupan los subniveles de un átomo
neutral debe ser igual al número atómico del elemento. Para escribir la
configuración electrónica de un átomo es necesario observar el
principio de Aufbau, el cual establece que los electrones del átomo se
van añadiendo a los subniveles en orden ascendente de energía. Es
decir, cada electrón entra en el subnivel de menor energía disponible
hasta que este nivel esté lleno, entonces el próximo electrón entra en
el subnivel que le sigue en energía. El arreglo así obtenido corresponde
al estado de más baja energía posible del átomo y se conoce como el
estado raso. Cualquier otro arreglo de los electrones produce un
estado de mayor energía y se le llama, en este caso, estado excitado. La
secuencia correcta de los subniveles en orden ascendente de energía
es: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
También podría gustarte
- Apuntes Numeros Cuanticos Conf. ElectronicaDocumento16 páginasApuntes Numeros Cuanticos Conf. Electronicacarlos antonioAún no hay calificaciones
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Apuntes de Estructura Atómica. Tercera ParteDocumento17 páginasApuntes de Estructura Atómica. Tercera ParteBrandon PaichoAún no hay calificaciones
- Modelo Atómico de La Mecánica Cuántica OndulatoriaDocumento13 páginasModelo Atómico de La Mecánica Cuántica OndulatoriaPaúl MartínezAún no hay calificaciones
- Modelo Nuclear Del Atomo.Documento44 páginasModelo Nuclear Del Atomo.Joselyn OrtegaAún no hay calificaciones
- QUIMICA CinvestavDocumento107 páginasQUIMICA CinvestavBerenice Acevedo HerreraAún no hay calificaciones
- Estructura Atómica 2020 p2Documento156 páginasEstructura Atómica 2020 p2Luciano Matias Garrido SosaAún no hay calificaciones
- Modelo Actual Del AtomoDocumento56 páginasModelo Actual Del AtomoCarlos Vicente100% (1)
- Configuración electrónicaDocumento18 páginasConfiguración electrónicaMoniik Alelii EspAún no hay calificaciones
- Orbital EsDocumento27 páginasOrbital EsMonica OramasAún no hay calificaciones
- Configuración electrónica y números cuánticosDocumento21 páginasConfiguración electrónica y números cuánticosYuleiny Arteaga PereiraAún no hay calificaciones
- 2 Teoria Est AtomicaDocumento9 páginas2 Teoria Est AtomicaCami Arce GariAún no hay calificaciones
- Cuestionario de FocalizaciónDocumento8 páginasCuestionario de FocalizaciónpotterheadAún no hay calificaciones
- Números Cuánticos PDFDocumento25 páginasNúmeros Cuánticos PDFJorgeAún no hay calificaciones
- Modelos AtómicosDocumento8 páginasModelos AtómicosLeilaAún no hay calificaciones
- TEORIA CUANTICA Configuracion ElectronicaDocumento17 páginasTEORIA CUANTICA Configuracion ElectronicaMaría elizabeth Díaz DíazAún no hay calificaciones
- Estructura Atómica y Números CuánticosDocumento15 páginasEstructura Atómica y Números CuánticosSTEFFANNYAún no hay calificaciones
- Módulo 1 - Lectura 4 - Orbitales Atómicos y Con Guración ElectrónicaDocumento15 páginasMódulo 1 - Lectura 4 - Orbitales Atómicos y Con Guración ElectrónicaIvanPascuaAún no hay calificaciones
- Quimica ParcialDocumento40 páginasQuimica ParcialRonaldoAún no hay calificaciones
- Guia Modelo Mecano Cuantico y Configuracion ElectronicaDocumento8 páginasGuia Modelo Mecano Cuantico y Configuracion ElectronicaLily baeza galvezAún no hay calificaciones
- Los Números Cuánticos PDFDocumento30 páginasLos Números Cuánticos PDFMilma CermeñoAún no hay calificaciones
- Modelo atómico actualDocumento4 páginasModelo atómico actualLeo SAún no hay calificaciones
- 3-Teoría Cuántica-VfinalDocumento48 páginas3-Teoría Cuántica-VfinaljuanixgenoAún no hay calificaciones
- Configuracion ElectronicaDocumento7 páginasConfiguracion ElectronicaBrayan De La CruzAún no hay calificaciones
- Tema 1.el Atomo Mecano-CuánticoDocumento9 páginasTema 1.el Atomo Mecano-CuánticojavierAún no hay calificaciones
- SommerfeldDocumento5 páginasSommerfeldFernando ChavezAún no hay calificaciones
- Atomo CuanticoDocumento9 páginasAtomo CuanticoVilchis Granados Axel MaximilianoAún no hay calificaciones
- Metodo de La LluviaDocumento7 páginasMetodo de La Lluviagabriel0900Aún no hay calificaciones
- Quimica DuvanDocumento9 páginasQuimica DuvanDiego BoadaAún no hay calificaciones
- Examen 2 de QuimicaDocumento7 páginasExamen 2 de QuimicaRicardo SantiagoAún no hay calificaciones
- Modelo de SchrodingerDocumento2 páginasModelo de SchrodingerGabriel CárdenasAún no hay calificaciones
- 6-Configuración ElectrónicaDocumento8 páginas6-Configuración ElectrónicaYuber RomañaAún no hay calificaciones
- Configuración Electrónica QUIMICA TAREADocumento3 páginasConfiguración Electrónica QUIMICA TAREAGibran MendozaAún no hay calificaciones
- Numeros Cuanticos (Clase 6)Documento5 páginasNumeros Cuanticos (Clase 6)Almonte NabilAún no hay calificaciones
- Espin Del ElectronDocumento7 páginasEspin Del ElectronMARIA ISABEL MESA PEREZAún no hay calificaciones
- Resumen EstructuraDocumento2 páginasResumen EstructurateresacamposcalvoAún no hay calificaciones
- Base Experimental de La Teoria Cuantica.Documento11 páginasBase Experimental de La Teoria Cuantica.Karen Alavez100% (1)
- Teoría de DALTON.: Rayos CatódicosDocumento8 páginasTeoría de DALTON.: Rayos Catódicosvictor MarceloAún no hay calificaciones
- Estructura atómicaDocumento5 páginasEstructura atómicaYanid Díaz SánchezAún no hay calificaciones
- Mecánica Cuántica Electrones OrbitalesDocumento5 páginasMecánica Cuántica Electrones OrbitalesMarcos Anguita SAún no hay calificaciones
- Numeros Cuanticos Guia 2022Documento7 páginasNumeros Cuanticos Guia 2022HUGO IBAÑEZAún no hay calificaciones
- Configuración electrónica átomosDocumento8 páginasConfiguración electrónica átomosEloy Alembert Fernandez HonoratoAún no hay calificaciones
- Max PlanckDocumento8 páginasMax PlanckISMAEL MORONESAún no hay calificaciones
- Guía - 02 - Números Cuánticos y Configuración ElecrónicaDocumento13 páginasGuía - 02 - Números Cuánticos y Configuración ElecrónicaYayo Pizarro AlarconAún no hay calificaciones
- Quimica Inorganica - Config ElectronicaDocumento2 páginasQuimica Inorganica - Config ElectronicaMaria Florencia AlbarelloAún no hay calificaciones
- Números CuánticosDocumento7 páginasNúmeros CuánticosJuanCho BastidasAún no hay calificaciones
- Mecánica Cuántica y Orbitales AtómicosDocumento9 páginasMecánica Cuántica y Orbitales AtómicosBrenda CaroAún no hay calificaciones
- Química General T7-14Documento49 páginasQuímica General T7-14Ilian GilAún no hay calificaciones
- El Modelo Mecánico Cuántico Del ÁtomoDocumento4 páginasEl Modelo Mecánico Cuántico Del ÁtomoDaniel ValdezAún no hay calificaciones
- Qué Son Los Niveles de EnergíaDocumento8 páginasQué Son Los Niveles de EnergíaAnthony JG100% (2)
- Conceptos para Selectividad Química 2ºbachDocumento9 páginasConceptos para Selectividad Química 2ºbachvialmapa5Aún no hay calificaciones
- Materia y Energía. Estructura Atómica. (Segunda Parte) .Documento25 páginasMateria y Energía. Estructura Atómica. (Segunda Parte) .Fabricio RodríguezAún no hay calificaciones
- Modelo Atomico CuanticoDocumento7 páginasModelo Atomico CuanticoMariano Ambrosio100% (1)
- Configuración Electrónica (O Periódica) : Modelo Atómico GeneralDocumento15 páginasConfiguración Electrónica (O Periódica) : Modelo Atómico GeneralDaimely GonzalezAún no hay calificaciones
- OrbitalesDocumento6 páginasOrbitalesJericka Cruz VargasAún no hay calificaciones
- Cap. 6. Estructura Electrónica ÁtomosDocumento54 páginasCap. 6. Estructura Electrónica ÁtomosMarcia JaraAún no hay calificaciones
- Orbitales Atómicos y MolecularesDocumento7 páginasOrbitales Atómicos y Molecularesashley0balcazarAún no hay calificaciones
- QuimicaDocumento29 páginasQuimicaIs Morales0% (1)
- Hoja de Trabajo No. 1Documento2 páginasHoja de Trabajo No. 1Jenifer LópezAún no hay calificaciones
- Gráfica de Campos EscalaresDocumento17 páginasGráfica de Campos EscalaresHernán Chaverra SuarezAún no hay calificaciones
- El Titánico Efecto de La RetrocausalidadDocumento3 páginasEl Titánico Efecto de La RetrocausalidadLuchoAún no hay calificaciones
- Larson y Edwar Calculo Del Volumen Con Integrales MultiplesDocumento6 páginasLarson y Edwar Calculo Del Volumen Con Integrales MultiplesIsrael Panimboza100% (1)
- METODONUMERICOSPARAEDPDocumento9 páginasMETODONUMERICOSPARAEDPALVARO DIEGO MACHACA CONDORIAún no hay calificaciones
- Lab 4 TermoDocumento10 páginasLab 4 TermosofiaAún no hay calificaciones
- El desarrollo de los modelos atómicos a través de la historiaDocumento10 páginasEl desarrollo de los modelos atómicos a través de la historiadowntango100% (2)
- Cartas Abstractas, Compatibilidad de Cartas, AtlasDocumento12 páginasCartas Abstractas, Compatibilidad de Cartas, AtlasE Alex Zambrano Guillermo100% (1)
- Derivadas ParcialesDocumento9 páginasDerivadas ParcialesÁngel Varón CalderónAún no hay calificaciones
- Longitud de Arco en Diferentes Sistemas de CoordenadasDocumento3 páginasLongitud de Arco en Diferentes Sistemas de CoordenadasLeonardo Sáenz BaezAún no hay calificaciones
- Computadora Cuantica PDFDocumento9 páginasComputadora Cuantica PDFJoel RojasAún no hay calificaciones
- Orbitales AtomicosDocumento8 páginasOrbitales AtomicosgermanAún no hay calificaciones
- Taller Curva Espiral-G02Documento20 páginasTaller Curva Espiral-G02Gabriela Fonseca cruzAún no hay calificaciones
- Taller 5 PDFDocumento2 páginasTaller 5 PDFAndres BenitezAún no hay calificaciones
- Matematicas Resueltos (Soluciones) Derivadas 2º Bachillerato Opción B-COUDocumento52 páginasMatematicas Resueltos (Soluciones) Derivadas 2º Bachillerato Opción B-COUmanuel_valle_4100% (5)
- 1°sec - Niveles, Subniveles y OrbitalesDocumento3 páginas1°sec - Niveles, Subniveles y OrbitalesHenry Daniel Ascencio FallaAún no hay calificaciones
- Taller Vect 2018Documento51 páginasTaller Vect 2018July KristenAún no hay calificaciones
- MantillaCristianD1 Taller4 2Documento10 páginasMantillaCristianD1 Taller4 2Cristian Giovanani Mantilla MorenoAún no hay calificaciones
- Mejoramiento CVVDocumento19 páginasMejoramiento CVVSweet TeamAún no hay calificaciones
- Movimiento Relativo TeoriaDocumento6 páginasMovimiento Relativo TeoriaAndres LopezAún no hay calificaciones
- Fórmula de Liouville (Mecánica) PDFDocumento1 páginaFórmula de Liouville (Mecánica) PDFAndii HerediaAún no hay calificaciones
- Informe de Laboratorio FisicaDocumento8 páginasInforme de Laboratorio Fisicabrendajuranny ramirezpardoAún no hay calificaciones
- Historia Del TensorDocumento2 páginasHistoria Del TensorRoberto Martinez Rodriguez100% (1)
- Subtema 2 - Estructura Atómica-Modelo ActualDocumento25 páginasSubtema 2 - Estructura Atómica-Modelo ActualAnderson GuarnizoAún no hay calificaciones
- James Clerk MaxwellDocumento13 páginasJames Clerk MaxwellHeriberto DiazAún no hay calificaciones
- Operador Diferencial Vectorial NablaDocumento14 páginasOperador Diferencial Vectorial NablaXiomara ACAún no hay calificaciones
- Derivada DireccionalDocumento11 páginasDerivada DireccionalSmith CórdovaAún no hay calificaciones
- Geometría Diferencial CosmologíaDocumento10 páginasGeometría Diferencial CosmologíaNiuk zzz100% (1)
- La Naturaleza Del Espacio y TiempoDocumento10 páginasLa Naturaleza Del Espacio y TiempoJulio CacedaAún no hay calificaciones
- Ejemplos de Matrice Contabilidad PDFDocumento4 páginasEjemplos de Matrice Contabilidad PDFJhanet Ampuero50% (2)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (200)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- La invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleDe EverandLa invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleCalificación: 4.5 de 5 estrellas4.5/5 (15)
- Psiconeuroinmunología para la práctica clínicaDe EverandPsiconeuroinmunología para la práctica clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDe EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreCalificación: 5 de 5 estrellas5/5 (3)
- Nunca fuimos modernos: Ensayos de antropología simétricaDe EverandNunca fuimos modernos: Ensayos de antropología simétricaAún no hay calificaciones
- Anatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasDe EverandAnatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasCalificación: 4.5 de 5 estrellas4.5/5 (21)
- Estoicismo y dureza mental: Descubre los secretos psicológicos de la filosofía estoica en la vida moderna. Construir una autodisciplina inquebrantable y hábitos diarios que garanticen el éxitoDe EverandEstoicismo y dureza mental: Descubre los secretos psicológicos de la filosofía estoica en la vida moderna. Construir una autodisciplina inquebrantable y hábitos diarios que garanticen el éxitoCalificación: 4 de 5 estrellas4/5 (23)
- Borges y la memoria: De "Funes el memorioso" a la neurona de Jennifer AnistonDe EverandBorges y la memoria: De "Funes el memorioso" a la neurona de Jennifer AnistonCalificación: 5 de 5 estrellas5/5 (4)
- Fisiopatología de las enfermedades cardiovascularesDe EverandFisiopatología de las enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Cálculo infinitesimal: El lenguaje matemático de la naturalezaDe EverandCálculo infinitesimal: El lenguaje matemático de la naturalezaCalificación: 5 de 5 estrellas5/5 (3)
- Resumen de Pensar rápido pensar despacio de Daniel KahnemanDe EverandResumen de Pensar rápido pensar despacio de Daniel KahnemanCalificación: 4.5 de 5 estrellas4.5/5 (11)
- Investigación de operaciones: Conceptos fundamentalesDe EverandInvestigación de operaciones: Conceptos fundamentalesCalificación: 4.5 de 5 estrellas4.5/5 (2)
- Desastres y emergencias. Prevención, mitigación y preparaciónDe EverandDesastres y emergencias. Prevención, mitigación y preparaciónCalificación: 4 de 5 estrellas4/5 (5)
- Zensorialmente : Dejá que tu cuerpo sea tu cerebroDe EverandZensorialmente : Dejá que tu cuerpo sea tu cerebroAún no hay calificaciones
- Reconstrucción de dientes endodonciados: Pautas de actuación clínicaDe EverandReconstrucción de dientes endodonciados: Pautas de actuación clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones
- Estadística básica: Introducción a la estadística con RDe EverandEstadística básica: Introducción a la estadística con RCalificación: 5 de 5 estrellas5/5 (8)
- En busca de la mente: El largo camino para comprender la vida mental (y lo que aún queda por descubrir)De EverandEn busca de la mente: El largo camino para comprender la vida mental (y lo que aún queda por descubrir)Calificación: 4.5 de 5 estrellas4.5/5 (3)