Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Preparación de soluciones ácidas y básicas para análisis químico
Cargado por
Sara Alejandra Buenaventura QuirogaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Preparación de soluciones ácidas y básicas para análisis químico
Cargado por
Sara Alejandra Buenaventura QuirogaCopyright:
Formatos disponibles
1.
En medio neutro, los iones plata reaccionan con el ion carbonato para formar un
precipitado de carbonato de plata:
a) cuántos gramos de carbonato sódico son necesarios para reaccionar completamente con 0,65 g
de nitrato de plata;
Na2CO3 + 2AgNO3 🡪 Ag2CO3 + 2NaNO3
Peso carbonato de sodio Na2CO3= 106 g/mol
Peso nitrato de plata 2AgNO3= 169,9 g/mol
Peso carbonato de plata 2AgCO3= 275,8 g/mol
Peso nitrato de sodio 2NaNO3 = 85 g/mol
3∗1 mol AgNO 3
∗1 mol Na2 CO 3
169,9 g AgNO 3
∗106 g Na2 CO 3
2 mol AgNO 3
g Na2 CO 3=0,65 g AgNO =0,2028 g Na2 CO 3
1 mol Na2 CO 3
b) cuántos gramos de nitrato de plata son necesarios para reaccionar con 250,0 mL de una
disolución de carbonato sódico 1,150 M;
3∗1 L Na2 CO 3
250 mL Na 2CO =0,25 L Na2 CO 3
1000 mL Na2 CO 3
Moles
Mo r a l idad=
Litro de solución
Moles=M∗V
1,150 MOL
Moles= ∗0,25 L=0,2875 mol de Na 2CO 3
L
3∗2 mol AgNO 3
∗169,9 g AgNO 3
1 mol Na2 CO 3
g AgNO 3=0,288 mol Na2 CO =97,86 g AgNO 3
1 mol AgNO 3
c) cuántos gramos de carbonato de plata se forman cuando 30 g de carbonato de sodio se
mezclan con 45 g de nitrato de plata;
Na2CO3 + 2AgNO3 🡪 Ag2CO3 + 2NaNO3
30 g 45 g x
3∗1 mol AgNO 3
45 g AgNO =0,2649 mol AgNO 3
169,9 g AgNO 3
3∗1 mol Na2 CO 3
30 g Na 2 CO =0,2830 mol Na 2CO 3
106 g Na2 CO 3
3∗1 mol Ag 2CO 3
∗275,8 g Ag 2CO 3
2 mol AgNO 3
g AgCO 3=0,2649 mol AgNO =36,53 g AgCO 3
1 mol Ag 2CO 3
d) cuántos gramos de carbonato de plata se forman cuando 24 g de carbonato de sodio se
mezclan con 12 g de nitrato de plata;
Na2CO3 + 2AgNO3 🡪 Ag2CO3 + 2NaNO3
24 g 12 g x
3∗1 mol AgNO 3
12 g AgNO =0,0706 mol AgNO 3
169,9 g AgNO 3
3∗1 mol Na 2CO 3
24 g Na2 CO =0,2263 mol Na2 CO 3
106 g Na 2CO 3
3∗1mol Ag 2CO 3
∗275,8 g Ag 2CO 3
2 mol AgNO 3
g AgCO 3=0,0706 mol AgNO =9,70 g Ag 2 CO 3
1mol Ag 2CO 3
e) cuántos gramos de carbonato de plata se forman cuando se mezclan 30 mL de
carbonato de sodio 2 M con 35 mL de nitrato de plata 1,3 M.
3∗1 L Na2 CO 3
30 mL Na2 CO =0,030 L Na2 CO 3
1000 mL Na2 CO 3
Moles
Moralidad=
Litro de solución
Moles=M∗V
2 MOL
Moles= ∗0,030 L=0,06 mol de Na2 CO 3
L
3∗1 L AgNO 3
35 mL AgNO =0,035 L AgNO 3
1000 mL AgNO 3
Moles
Moralidad=
Litro de solución
Moles=M∗V
1,3 MOL
Moles= ∗0,035 L=0,0455 mol de AgNO 3
L
3∗1 mol AgCO 3
∗275,8 g AgCO 3
2 mol AgNO 3
g AgCO 3=0,0455 mol AgNO =6,27 g AgCO 3
1mol AgCO 3
2. Se supone que una disolución de NaOH se encuentra a 1,3 M. Para determinar su
verdadera moralidad se valora esta disolución de NaOH utilizando biftalato ácido de
potasio, KHC8H4O4. Se disuelve una muestra de 0,7 gramos de biftalato en agua y se
valora con 44,50 ml de la disolución de NaOH. ¿Cuál es la molaridad real del NaOH?
NaOH + KHC8H4O4 🡪NaKC8H4O4 + H2O
1,3 M 0,7g
44,50 mL = 0,04450 L
Peso KHC8H4O4=204,22 g/mol
4∗1 mol KHC 8 H 4 O 4
∗1 mol de NaOH
204,22 g KHC 8 H 4 O 4
Mol NaOH=0,7 g KHC 8 H 4 O =0,003428 mol de NaOH
1mol KHC 8 H 4 O 4
Moles
Moralidad=
Litro de solución
0,003420 mol NaOH
Moralidad= =0,08 M NaOH
Litro de solución 0,0445 L NaOH
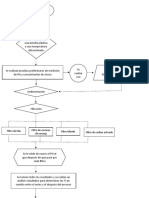
3. Un estudiante encuentra un frasco de NaOH sólido que alguien dejó destapado. El
hidróxido de sodio, que es higroscópico, absorbe humedad del aire. El estudiante desea
determinar cuánto NaOH existe realmente en la muestra humedecida. Proponga un
procedimiento para verificar la pureza del NaOH
● Pesar biftalato ácido de potasio.
● Realiza la relación estequiométrica de moles.
● Hallar el número de moles de hidróxido de sodio NaOH
● Se halla la concentración en molaridad con los litros valorados.
4. En el laboratorio se tiene un ácido de batería el cual se requiere determinar el contenido de
H2SO4. Una muestra de 1 ml de ácido de batería pesa 5,239 g. Esta muestra se diluye
hasta 500 ml con agua. De esta solución se toma una alícuota de 20 ml la cual es titulada
con solución de Na(OH) de concentración 15,85x10 -3 M. En la titulación se gastaron 70,7
ml de solución Na(OH). Calcular el % en peso de H 2SO4 en el ácido de la batería.
2Na(OH) + H2SO4 🡪 Na2SO4 + H2O
• 70,7 mL • 20mL
•15,85x10-3M
Peso H2SO4= 98,08 g/mol
0,011203 mol/L NaOH * 0.707 L = 0.11203 m
( OH )∗1 mol H 2 SO 4
∗1 mol H 2 SO 4
2 mol NaOH
g H 2 SO 4=0.011203 Na =0,0280075 moles de H 2 SO 4
0.020 L H 2 SO 4
4∗0,5 L H 2 SO 4
0.0280075 M H 2 SO =14 moles de H 2 SO 4
0.001 m H 2 SO 4
14 moles * 98 g/mol = 1372g
1000ml * 5,239 g/ml = 5239 g
g Soluto
%P /P= ∗100
g Solución
P 1372 g H 2 SO 4
% = ∗100=26,18 % H 2 SO 4
P 5239 g H 2 SO 4
5. Describa la preparación de 250,0 mL de disolución de H 2SO4 0,410 mol/L, a partir del
reactivo comercial concentrado (98% P/P y densidad 1,84 g/mL). H 2SO4 = 98,00 g/mol.
Suponga que en el laboratorio sólo hay: beaker, Erlenmeyer, buretas de 25,00 mL,
probetas de todo tipo, pipetas graduadas de 10,00 mL y balones aforados de 100,00 mL.
0,410mol H 2 SO 4
∗98 g H 2 SO 4
1 L H 2 SO 4
∗100 %
0,10 L H2SO4 * 1 MOL H 2 SO 4
∗1 mL
98 %
=2,2 mL H 2 S 04
1,84 g
1. Tomar una alícuota de 2,2 mL con la pipeta graduada.
2. Agregar en un beaker, luego agregar 20 mL de agua destilada teniendo
precaución por el choque térmico que se genera.
3. Esperar que la solución se enfríe para no descalibrar el material volumétrico
debido al calor que produce, ya que esto dilata el material.
4. Llevar la solución a un balón de 100 mL y aforar
5. Realizar este procedimiento por triplicado para obtener 300 mL de la solución.
6. Estandarizar las soluciones para saber su concentración real con alícuotas de 10
o 20 mL.
6. Para un análisis se requiere una solución patrón de HCl 0,3 mol/L, pero en el laboratorio
sólo hay una solución de HCl 1 mol/L. ¿Qué volumen de la disolución concentrada
requiere diluir para preparar 100,0 mL de la disolución de interés?
C 1∗V 1=C 2∗V 2
1 m∗X =0,3 m∗100 Ml
0,3 m∗100 ml /1
30 ml
R// Se deben tomar 30mL de la solución diluida al 1M y aforar en un balón de 100mL
7. Se añaden 15 g de hidróxido de sodio, NaOH al 95,0%, a 250 mL de una disolución acuosa
de ácido clorhídrico, HCl 1,5 M.
A) Determine cuál es el reactivo limitante
15g NaOH + 250 ml HCL 🡪 NaCL + H2O
39.97 36.45
1 mol NaOH
15g NaOH = 0.37 mol NaOH
39.97 g NaOH
0,375 mol 🡪 100%
0, 351 mol 🡪 95%
Limitante
1L
250ml * = 0.25 L
1000 ml
0.25 L HCL
mol
Molaridad=
V
mol
1,5 m =
0,25 L
mol
Mol= 1,5 * 0,25 L= 0,375 mol
L
B) Determine la reacción resultante y cuantos gramos de producto se formaron.
NaCL + H2O 🡪 Reacción resultante
58,43 g + 18 g = 76,43 g
🡪 Producto formado en gramos
C) En el caso de que se duplique la cantidad de NaOH, el reactivo limitante ¿sigue
siendo el mismo? ¿Cuánto producto se producirá?.
● El reactivo limitante no es el mismo, ya que se duplica. Por ende se produciría el
doble producto.
8. Se realiza una práctica de laboratorio donde se pesan 5,156 g de KCl (peso molecular:
74.5 g/mol) y se disuelven en 80 mL de agua (solución #1). De esta solución se toman 15
mL para llevarlos a un volumen total de 50 mL completando con agua (solución #2), y
finalmente de esta última solución se toman 15 mL para ser evaporados y llevados hasta
sequedad en una cápsula de porcelana. ¿Cuántos gramos de sal se recuperan al final en la
cápsula de porcelana? b. Cual es la concentración molar (M) y la concentración peso a
volumen (%p/v) de las soluciones #1 y 2
KCl∗1 mol Kcl
5,156 g =0.069301 mol KCl
74.4 g KCl
m 0.069301 mol KCl
Solución 1 M = M = =0.8662625 M
L 0.08 L
74.4 g KCl
0,069301 mol KCl * =5.16 g de KCl
1 mol KCl
P 5.16 g
% ∗100 ∗100=6.40 %
v 80 ml
Solución 2 0.8662625∗0.015=0.0129moles
0.0129 moles
M= =0.258 M
0.05 L
74.4 g KCl
0,0129 mol KCl * =0,9598 g de KCl
1 mol KCl
P 0,9598 g
% ∗100 ∗100=1.20 %
v 80 ml
Solución 3 0.258 * 0.015 = 0.00387 moles
mol∗74.4 g
0.00358 =0.2663 g
1mol
A// Se recuperan 0.2663g de KCl.
B// Concentración de solución 1 es de 0.8663M y de la solución 2 es de 0.258M
C// Concentración p/v de la solución 1 6.45% y la concentración p/v de la solución 2 es
de 1.20%.
También podría gustarte
- Materiales para ingeniería 1: Introducción a las propiedades, las aplicaciones y el diseñoDe EverandMateriales para ingeniería 1: Introducción a las propiedades, las aplicaciones y el diseñoCalificación: 5 de 5 estrellas5/5 (3)
- Ejercicios de Gravimetría ResueltosDocumento8 páginasEjercicios de Gravimetría Resueltosnano75% (4)
- Tarea I Hidrocarburos IngDocumento8 páginasTarea I Hidrocarburos IngManuel MendozaAún no hay calificaciones
- TAREA #7-P2 ESTEQUIOMETRIA-ResueltoDocumento4 páginasTAREA #7-P2 ESTEQUIOMETRIA-ResueltoSamantha Valdivia100% (2)
- Ejercicios Resueltos de QuimicaDocumento7 páginasEjercicios Resueltos de Quimicaraulix20% (5)
- CAOÍTULO 5-Hidrocarburos AromaticosDocumento83 páginasCAOÍTULO 5-Hidrocarburos AromaticosOscar F. C ReAún no hay calificaciones
- Grupo 1 - Ope III - Secado Por AtomizaciónDocumento30 páginasGrupo 1 - Ope III - Secado Por AtomizaciónErick Isaac CalleAún no hay calificaciones
- Problemario D2 - Equipo - 3 - 3BV2Documento11 páginasProblemario D2 - Equipo - 3 - 3BV2jesus raymundo ceballos torresAún no hay calificaciones
- Mostos Naturales, Concentrados y Rectificados PDFDocumento26 páginasMostos Naturales, Concentrados y Rectificados PDFOmar UculmanaAún no hay calificaciones
- Actividad 27 y 28Documento20 páginasActividad 27 y 28Xavier Villon100% (4)
- Ejercicios Quimica EstequiometriaDocumento6 páginasEjercicios Quimica EstequiometriaEnmanuel De la PazAún no hay calificaciones
- Metodos de Analisis GravimetricosDocumento6 páginasMetodos de Analisis GravimetricosCarolina Gomez Serna100% (1)
- Ejercicios de Complejometria AxelDocumento4 páginasEjercicios de Complejometria Axeljesus raymundo ceballos torres100% (1)
- Manual de Cristralografia PDFDocumento106 páginasManual de Cristralografia PDFMaria GonzalezAún no hay calificaciones
- Evidencia 7 Respuesta A Preguntas Sobre Volumetrías de PrecipitaciónDocumento4 páginasEvidencia 7 Respuesta A Preguntas Sobre Volumetrías de PrecipitaciónDavid Cubillos Gómez100% (1)
- Actividad 22Documento7 páginasActividad 22Xavier VillonAún no hay calificaciones
- Pract 6 DisolucionesDocumento5 páginasPract 6 DisolucionesMarQuizzéAún no hay calificaciones
- EJERCICIOS CHANG ANALISIS GRAVIMETRICO Y VOLUMETRICODocumento3 páginasEJERCICIOS CHANG ANALISIS GRAVIMETRICO Y VOLUMETRICOAlexis CushicondorAún no hay calificaciones
- Ejercicios para Resolver ESTEQUIOMETRIA CON SOLUCIONESDocumento3 páginasEjercicios para Resolver ESTEQUIOMETRIA CON SOLUCIONESYanchatipan Gutierres Elvis Alexander100% (1)
- Cantidades de Reactivos y Productos en Reacciones QuímicasDocumento9 páginasCantidades de Reactivos y Productos en Reacciones QuímicasThe_buzzcutAún no hay calificaciones
- Estequiometría 1Documento8 páginasEstequiometría 1Nicolas CastilloAún no hay calificaciones
- Parcial 2 Taller 4Documento24 páginasParcial 2 Taller 4Richard ApazaAún no hay calificaciones
- Informe de Práctica 2Documento9 páginasInforme de Práctica 2lauraAún no hay calificaciones
- Tarea de AnaliticaDocumento8 páginasTarea de AnaliticaOrlando Sayago Rafael100% (1)
- Guia de Gravimetria Resuelta OKDocumento18 páginasGuia de Gravimetria Resuelta OKcaruuswagAún no hay calificaciones
- Quimica InformeDocumento5 páginasQuimica InformeDaniel Gomez AgredoAún no hay calificaciones
- EstequiometriaDocumento26 páginasEstequiometriaWilmer LopezAún no hay calificaciones
- Pract 3 BalanceDocumento3 páginasPract 3 BalanceMarQuizzéAún no hay calificaciones
- Cuestionario Sobre Mol - Masa Molar Y Reactivo LimitanteDocumento4 páginasCuestionario Sobre Mol - Masa Molar Y Reactivo LimitanteRuvens Angola FernandezAún no hay calificaciones
- Formula EmpiricaDocumento6 páginasFormula EmpiricaEduardo Zamorano100% (1)
- Ejercicio QuimicaDocumento5 páginasEjercicio QuimicaAlexander SamAún no hay calificaciones
- U4 - S6 - Fichadetrabajo6 - CalculosEstequiométricos FinalDocumento6 páginasU4 - S6 - Fichadetrabajo6 - CalculosEstequiométricos FinalGisela Vera100% (2)
- Masa/ MolDocumento8 páginasMasa/ MolMary PalacesAún no hay calificaciones
- Reacciones químicas AgNO3 Na2CO3Documento2 páginasReacciones químicas AgNO3 Na2CO3Javier Luengo MoleroAún no hay calificaciones
- Ejercicios de EstequiometriaDocumento8 páginasEjercicios de Estequiometrianuñezgonzalo kevinAún no hay calificaciones
- Ejercicios Resueltos Tema 5Documento36 páginasEjercicios Resueltos Tema 5Ismael Zerouali ZeroualiAún no hay calificaciones
- Taller de EstequiometríaDocumento3 páginasTaller de EstequiometríaJesús Alfonso Castro ParraAún no hay calificaciones
- Practica - 3 - Estequiometria en Reacciones FALTADocumento3 páginasPractica - 3 - Estequiometria en Reacciones FALTAfelix gonzalesAún no hay calificaciones
- Taller Química Análitica Gravimétrica EjerciciosDocumento3 páginasTaller Química Análitica Gravimétrica EjerciciosLauraMilenaJaramilloRodriguezAún no hay calificaciones
- Taller de Química GeneralDocumento8 páginasTaller de Química GeneralAndres GuerreroAún no hay calificaciones
- Carlitos XDDocumento8 páginasCarlitos XDJulio Poma TorresAún no hay calificaciones
- Tarea Individual 3Documento8 páginasTarea Individual 3pamela garciaAún no hay calificaciones
- Cuestionario sobre reacciones químicas que liberan oxígenoDocumento1 páginaCuestionario sobre reacciones químicas que liberan oxígenogieremy gutierrezAún no hay calificaciones
- NoseDocumento4 páginasNoseDerek MAún no hay calificaciones
- Cálculos EstequiométricosDocumento4 páginasCálculos EstequiométricosKaren Meneses CorzoAún no hay calificaciones
- Informe BiologiaDocumento6 páginasInforme Biologiajuan diegoAún no hay calificaciones
- EJERCICIOS TITULACIONES 19 FebDocumento16 páginasEJERCICIOS TITULACIONES 19 Febmaria fernanda tous marrugoAún no hay calificaciones
- Tarea 4. Desarrollar El Componente Práctico VirtualDocumento7 páginasTarea 4. Desarrollar El Componente Práctico VirtualMauricio Suarez67% (3)
- Métodos volumétricos por precipitaciónDocumento27 páginasMétodos volumétricos por precipitaciónHerwin MoraAún no hay calificaciones
- Clase Práctica N7Documento7 páginasClase Práctica N7Johary SevillaAún no hay calificaciones
- INFORME 4 QuimicaDocumento7 páginasINFORME 4 Quimicasterlingquintero546Aún no hay calificaciones
- Ejercicios de Unidades en Masa y EstequiometríaDocumento28 páginasEjercicios de Unidades en Masa y EstequiometríaJunnior Santamaria RiveraAún no hay calificaciones
- SOLUCIONES EJERCICIOS (Masa Atómica, Molecular y Mol) PDFDocumento5 páginasSOLUCIONES EJERCICIOS (Masa Atómica, Molecular y Mol) PDFJhan'n CrhAún no hay calificaciones
- Semana 01Documento10 páginasSemana 01Akatsuki RoAún no hay calificaciones
- Tarea 1Documento4 páginasTarea 1Marta A. NuñezAún no hay calificaciones
- Informe Estequiometria.bDocumento8 páginasInforme Estequiometria.bDAIRON POPO SABOGALAún no hay calificaciones
- EspinosaSolis EjerEstequiometriaDocumento3 páginasEspinosaSolis EjerEstequiometriaAntonio ESAún no hay calificaciones
- Estequiometría ReaccionesDocumento4 páginasEstequiometría ReaccionesALICIA TITUAÑAAún no hay calificaciones
- Apuntes Quimica IDocumento10 páginasApuntes Quimica IMomo RosarioAún no hay calificaciones
- Nacl 0.36705 G M Bacl: + Fe 1mol 2 Mol 1molfes2 2 0,0087466 0,0087466 Mfes2 119,98Documento2 páginasNacl 0.36705 G M Bacl: + Fe 1mol 2 Mol 1molfes2 2 0,0087466 0,0087466 Mfes2 119,98GERARDO SILVESTRE MELENDEZ MACALOPUAún no hay calificaciones
- Informe Lab 02Documento4 páginasInforme Lab 02NicolasAún no hay calificaciones
- Quimica TDocumento5 páginasQuimica TAngel Jesus Alvarez SierraAún no hay calificaciones
- Tarea Semana 2Documento4 páginasTarea Semana 2Panela PierreAún no hay calificaciones
- Buenas Prácticas Del ServicioDocumento3 páginasBuenas Prácticas Del ServicioSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Electiva Profesional PDFDocumento4 páginasElectiva Profesional PDFSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- El ADN Es Un Tipo de Acido NucleicoDocumento3 páginasEl ADN Es Un Tipo de Acido NucleicoSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- El ResplandorDocumento3 páginasEl ResplandorSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- La Infinitud AfirmativaDocumento3 páginasLa Infinitud AfirmativaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Lisinopril en Acoplamiento Con Vitaminas PDFDocumento11 páginasLisinopril en Acoplamiento Con Vitaminas PDFSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Proyecto Ciencias EscritoDocumento5 páginasProyecto Ciencias EscritoSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- La Medicina en El Antiguo EgiptoDocumento2 páginasLa Medicina en El Antiguo EgiptoSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Gráficas y Técnicas EstadísticasDocumento4 páginasGráficas y Técnicas EstadísticasSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- AcetilcolinaDocumento10 páginasAcetilcolinaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Exposicion MicroDocumento5 páginasExposicion MicroSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Gestión Del Sistema de InformaciónDocumento4 páginasGestión Del Sistema de InformaciónSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Amor de Mi VidaDocumento8 páginasAmor de Mi VidaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Las Apariencias y EmpatíaDocumento1 páginaLas Apariencias y EmpatíaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Taller Prueba de Esterilidad SalesianaDocumento7 páginasTaller Prueba de Esterilidad SalesianaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- La Medicina Occidental Inicia en El Antiguo EgiptoDocumento2 páginasLa Medicina Occidental Inicia en El Antiguo EgiptoSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- ElectivaDocumento5 páginasElectivaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Ensayos proteínicos guía laboratorio bioquímicaDocumento2 páginasEnsayos proteínicos guía laboratorio bioquímicaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- CorreciónDocumento1 páginaCorreciónSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Parcial de MatemáticasDocumento8 páginasParcial de MatemáticasSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Resultados PDF AC202043604709Documento3 páginasResultados PDF AC202043604709Sara Alejandra Buenaventura QuirogaAún no hay calificaciones
- InformacionDocumento4 páginasInformacionSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Taller Control de Calidad Medios de Cultivo 06022023 PDFDocumento4 páginasTaller Control de Calidad Medios de Cultivo 06022023 PDFSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- LeerrrrrrrrrDocumento4 páginasLeerrrrrrrrrSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Benedict ReactivoDocumento4 páginasBenedict ReactivoAlexandra Oyarce MeléndezAún no hay calificaciones
- Revolución Científica: Cambio ParadigmasDocumento4 páginasRevolución Científica: Cambio ParadigmasSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- AcetilcolinaDocumento10 páginasAcetilcolinaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Diagrama FlujoDocumento2 páginasDiagrama FlujoSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- BioestadísticaDocumento7 páginasBioestadísticaSara Alejandra Buenaventura QuirogaAún no hay calificaciones
- Ejercicios Aminoacidos y SecuenciacionDocumento4 páginasEjercicios Aminoacidos y SecuenciacionDaniel Gomez GalindoAún no hay calificaciones
- Ivc2b0 Guc3ada Ejercicios Electrostc3a1tica 1Documento7 páginasIvc2b0 Guc3ada Ejercicios Electrostc3a1tica 1Ivan Fernando Caicedo PerezAún no hay calificaciones
- Determinación de acidez y alcalinidadDocumento18 páginasDeterminación de acidez y alcalinidadpatricia xiomaraAún no hay calificaciones
- Xxvii. - Centrales Que Queman BasurasDocumento30 páginasXxvii. - Centrales Que Queman BasurasPAPALOS007Aún no hay calificaciones
- Módulo de Young Barra FlexiónDocumento6 páginasMódulo de Young Barra FlexiónWillySurcoCoaguilaAún no hay calificaciones
- TP1 - Ejercicio 13Documento5 páginasTP1 - Ejercicio 13Carolina Paulino100% (1)
- 2 Lovatt Facts About Foliar Nutrition in Avocado (Spanish)Documento28 páginas2 Lovatt Facts About Foliar Nutrition in Avocado (Spanish)Jesus PeredaAún no hay calificaciones
- Actividades Estructura de La TierraDocumento48 páginasActividades Estructura de La TierraBea CalvoAún no hay calificaciones
- Elementos QuimicosDocumento87 páginasElementos QuimicosJuan ViscarraAún no hay calificaciones
- Soluciones 4to Año 11-5-20Documento2 páginasSoluciones 4to Año 11-5-20Douglas TesilloAún no hay calificaciones
- Ensayos No Destructivos Mediante Inspección VisualDocumento9 páginasEnsayos No Destructivos Mediante Inspección VisualanyeloAún no hay calificaciones
- Tipos pilasDocumento6 páginasTipos pilasbdematteiAún no hay calificaciones
- Extracion Del Video de FuncionamientoDocumento4 páginasExtracion Del Video de FuncionamientoUSUARIO1218Aún no hay calificaciones
- Nociones ElectronicaDocumento46 páginasNociones ElectronicaserlainAún no hay calificaciones
- Informe FISICOQUIMICA N°2Documento3 páginasInforme FISICOQUIMICA N°2Carolina Alejandra Cardenas JametAún no hay calificaciones
- ContinueDocumento2 páginasContinueBoescu SimonaAún no hay calificaciones
- Ingeniería industrial: contaminación atmosféricaDocumento75 páginasIngeniería industrial: contaminación atmosféricaAlejandro VasquezAún no hay calificaciones
- BitumenDocumento4 páginasBitumenborisov2009Aún no hay calificaciones
- Clasificacion de ReactivosDocumento4 páginasClasificacion de Reactivosfernando martinezAún no hay calificaciones
- Destilación Simple y FraccionadaDocumento31 páginasDestilación Simple y FraccionadaRocioAún no hay calificaciones
- Gfpi-F-019 - Gtaw Ejecucion Soldar 1Documento14 páginasGfpi-F-019 - Gtaw Ejecucion Soldar 1JUAN PABLO POSTIGLIONI CANALAún no hay calificaciones
- Historia de Un PesoDocumento17 páginasHistoria de Un PesoLuis AngelesAún no hay calificaciones
- Modulo de ReaccionDocumento4 páginasModulo de Reaccioneleazar albiterAún no hay calificaciones
- QUÍMICA 2o BACHILLERATO EJERCICIOS SELECTIVIDADDocumento4 páginasQUÍMICA 2o BACHILLERATO EJERCICIOS SELECTIVIDADAlejandro RenuncioAún no hay calificaciones
- HT 95xx Clasica Anticorrosivo Fast Dry Eid 300 v02 1Documento2 páginasHT 95xx Clasica Anticorrosivo Fast Dry Eid 300 v02 1Lesther Coloch GonzálezAún no hay calificaciones