Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Documento
Cargado por
Roberto Arias Flores0 calificaciones0% encontró este documento útil (0 votos)
9 vistas2 páginasEste documento describe los procedimientos de titulación para determinar las concentraciones de carbonato, bicarbonato e hidróxido en mezclas alcalinas. Explica que la titulación con ácido clorhídrico permite monitorear los cambios de las sustancias mediante el uso de indicadores de color como la fenolftaleína y la heliantina. También cubre los métodos para determinar el carbonato en presencia de bicarbonato y la alcalinidad total de una mezcla usando diferentes indicadores y condiciones de titulación.
Descripción original:
knknlk
Título original
Documento (1)
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento describe los procedimientos de titulación para determinar las concentraciones de carbonato, bicarbonato e hidróxido en mezclas alcalinas. Explica que la titulación con ácido clorhídrico permite monitorear los cambios de las sustancias mediante el uso de indicadores de color como la fenolftaleína y la heliantina. También cubre los métodos para determinar el carbonato en presencia de bicarbonato y la alcalinidad total de una mezcla usando diferentes indicadores y condiciones de titulación.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
9 vistas2 páginasDocumento
Cargado por
Roberto Arias FloresEste documento describe los procedimientos de titulación para determinar las concentraciones de carbonato, bicarbonato e hidróxido en mezclas alcalinas. Explica que la titulación con ácido clorhídrico permite monitorear los cambios de las sustancias mediante el uso de indicadores de color como la fenolftaleína y la heliantina. También cubre los métodos para determinar el carbonato en presencia de bicarbonato y la alcalinidad total de una mezcla usando diferentes indicadores y condiciones de titulación.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
Palabras clave:Indicador, Valoración, NaOH, HCl, Titulación, Mezclas.
Introducción
Una titulación es un procedimiento en el que se añade un patrón (reactivo
titulante) a un analito (sustancia a determinar) hasta que se considere completa la
reacción entre ellos. Podemos determinar que se ha completado la reacción entre
el titulante y el analito al evidenciar el punto final de la titulación, el cual está
cercano al punto de equivalencia de la misma. El punto de
equivalencia de una titulación es el punto en que la cantidad de titulante patrón
añadido es químicamente equivalente a la del analito. Y, el punto final de una
titulación, es el cambio físico
observado que se asocia con una condición de equivalencia química. En una
titulación es común añadir un indicador químico a la solución del analito para
obtener un
cambio físico apreciable (el punto final) en o cerca del punto de equivalencia como
se señaló anteriormente. Los cambios más grandes en la concentración relativa
del analito o del titulante se
dan, precisamente, en la zona del punto de equivalencia. Estos cambios de
concentración son los que hacen que cambie la forma del indicador siendo los
más típicos la aparición o desaparición de
calor, el cambio de color, o la aparición o desaparición de turbiedad.
Se denominan mezclas alcalinas a las formadas por combinaciones compatibles
de sosa. carbonato v carbonato ácido. Estas mezclas tienen gran importancia
tanto en Ouímica Industrial. como Medio-Ambiental. Alimentaria o Clínica. por lo
que su determinación analítica tiene un gran interés.
El carbonato y el carbonato ácido (bicarbonato ó hidrógenocarbonato) pertenecen
al sistema ácido-base:
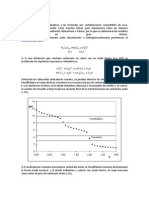
1) Si una disolución que contiene carbonato se valora con un acido fuerte
(p.e.HCl) se producirán las siguientes reacciones volumétricas:
Utilizando los adecuados indicadores visuales. se pueden detectar los dos puntos
finales: Con Fenolftaleina el viraie de Rosa a Incoloro nos marcara el paso de
carbonato a carbonato ácido. Si a la disolución incolora se le añade Heliantina
(Narania o Anaranjado de metilo) y se valora, el cambio de Amarillo a Rojo
localizará el punto final de la transformación de carbonato ácido a a CO2.
2) Si la disolución contiene únicamente carbonato ácido, la Fenolftaleína
tomaría directamente la forma ácida incolora, y al añadir Heliantina y valorar
un ácido fuerte, el viraje marcaría cómo antes el paso de carbonato de
ácido a a CQ.
3) Por su parte, si una disolución que contenga hidróxido sódico se valora
utilizando el mismo procedimiento, sólo hay una reacción volumétrica, que
será detectada tanto por la Fenolftaleína (que vira de Rosa a incoloro) como
por la Heliantina (que vira de amarillo a rojo)
Las mezclas de carbonato y bicarbonato y las mezclas de de carbono e hidróxido
pueden valorarse usando una solución estandarizada de HCl.
El método clásico para valorar carbonato en presencia de bicarbonato es
titulándolo con HCl hasta convertirlo cuantitativamente en bicarbonato (primero en
la titulación de CO3-2). El pH de las soluciones de HCO3- es 8,3 – 8,4 y varía
poco con la concentración; puede usarse Fenolftaleína, como indicador y para
disminuir el error comparar el color con el de una solución de NaHCO3: en un
segundo Erlenmeyer se coloca una solución de NaHC03 de concentración
cercana a la de carbonato se adiciona igual cantidad de indicador, y se titula la
muestra hasta obtener un tono rosado similar al que produce la solución de
bicarbonato. Mejores resultados se obtienen usando Azul de Timol (amarillo 8.0 -
9.6 azul) y titulando hasta color verde amarillento (pH~ 8.5). Para determinar la
alcalinidad total (CO3-2 + HCO3-) se titula con HCI hasta conversión total a
H2C03. El pH en el pe es aproximadamente 4 y puede usarse Heliantina como
indicador, aunque mejores resultados se obtienen por el método que usa Verde de
Bromocresol y ebullición.
Referencias:
Titulación De Mezclas Alcalinas - Ensayos - 2085 Palabras. (s. f.). Buenas Tareas.
Recuperado 25 de octubre de 2022,
de https://www.buenastareas.com/ensayos/Titulaci%C3%B3n-De-Mezclas-
Alcalinas/3996285.html
Leona, L. (s. f.). mezclas alcalinas. Scribd. Recuperado 25 de octubre de 2022,
de https://es.scribd.com/doc/96839889/mezclas-alcalinas
También podría gustarte
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Guia de Ejercicios Sobre PHDocumento5 páginasGuia de Ejercicios Sobre PHaestay89% (18)
- Determinación-Gravimetrica Del Níquel Con Dimetilglioxima-Carlos-Bayle-FrancoDocumento5 páginasDeterminación-Gravimetrica Del Níquel Con Dimetilglioxima-Carlos-Bayle-FrancoCarlos Bayle FrancoAún no hay calificaciones
- Valoracion CH3COOHDocumento14 páginasValoracion CH3COOHAdriana PérezAún no hay calificaciones
- Practica N 2 Titulacion Quimica Ii 222222222Documento4 páginasPractica N 2 Titulacion Quimica Ii 222222222Cristo CQ0% (1)
- Mezclas AlcalinasDocumento2 páginasMezclas AlcalinasLin Leon100% (1)
- Mezclas AlcalinasDocumento7 páginasMezclas AlcalinasAntonio Aviles Gudiño0% (2)
- Informe Número 5 (Aplicación Del Método Volumétrico para Determinar La Composición de Soluciones Acuosas Con Mezclas de Carbonatos)Documento7 páginasInforme Número 5 (Aplicación Del Método Volumétrico para Determinar La Composición de Soluciones Acuosas Con Mezclas de Carbonatos)Yefrei SierraAún no hay calificaciones
- Analitica Identificacion de CarbonatosDocumento4 páginasAnalitica Identificacion de CarbonatosFlorez Cabarcas BryamAún no hay calificaciones
- Practica 8 PACDocumento6 páginasPractica 8 PACAdolfo ContlaAún no hay calificaciones
- Practica 10Documento8 páginasPractica 10Roberto Arias FloresAún no hay calificaciones
- Determinacion de La Acidez Del VinagreDocumento10 páginasDeterminacion de La Acidez Del VinagreRudy Mamani CuellarAún no hay calificaciones
- Practica 1 - Quimica AnalíticaDocumento16 páginasPractica 1 - Quimica AnalíticaBryan A. Rios VelásquezAún no hay calificaciones
- Mezclas AlcalinasDocumento5 páginasMezclas AlcalinasTiffany Bernard100% (1)
- Resumen Analitca 2do ParcialDocumento9 páginasResumen Analitca 2do Parcialtotojul1Aún no hay calificaciones
- 7mo Informe de Analisis QuimicoDocumento15 páginas7mo Informe de Analisis QuimicoSamir Lima100% (1)
- Informe AlcalinidadDocumento13 páginasInforme AlcalinidadMaria Del MarAún no hay calificaciones
- Fundamento TeóricoDocumento4 páginasFundamento TeóricoMelisa DanisiAún no hay calificaciones
- PRACTICA 3. Mezcla Carbonatos y Acidez en JugoDocumento8 páginasPRACTICA 3. Mezcla Carbonatos y Acidez en Jugogreyllom9791Aún no hay calificaciones
- Titulaciones QuimicasDocumento5 páginasTitulaciones QuimicasNeldon CapillaAún no hay calificaciones
- TPL3 PARTE 1 AnaliticaDocumento4 páginasTPL3 PARTE 1 AnaliticaLu guzmanAún no hay calificaciones
- Determinacion de Muestras Alcalinas.Documento11 páginasDeterminacion de Muestras Alcalinas.lili46140% (1)
- Informe 1 Estandarización de HCLDocumento26 páginasInforme 1 Estandarización de HCLDame100% (12)
- Informe Lab. 2Documento9 páginasInforme Lab. 2Sol PolitanoAún no hay calificaciones
- Volumetrías de Neutralización NormalidadDocumento6 páginasVolumetrías de Neutralización NormalidadCututui CardenasAún no hay calificaciones
- 7 Informe de Analisis QuimicoDocumento20 páginas7 Informe de Analisis QuimicowillyballAún no hay calificaciones
- 0a020037 A64a 7041Documento9 páginas0a020037 A64a 7041mako2189Aún no hay calificaciones
- Marco Teorico de Acido - BaseDocumento13 páginasMarco Teorico de Acido - Basewuili Diaz AlbornozAún no hay calificaciones
- ACIDIMETRIADocumento16 páginasACIDIMETRIAJose Luis PalacioAún no hay calificaciones
- Practica 4 QuimicaDocumento7 páginasPractica 4 QuimicaMarlon GaliciaAún no hay calificaciones
- TITULACIÓNDocumento27 páginasTITULACIÓNhuerfansAún no hay calificaciones
- Notas Química Analítica 3Documento32 páginasNotas Química Analítica 3Hanna CirodAún no hay calificaciones
- Carbonatos y BicarbonatosDocumento3 páginasCarbonatos y BicarbonatosAlejandro Ramirez AlpizarAún no hay calificaciones
- Equilibrio Quimico 1Documento14 páginasEquilibrio Quimico 1Arthur Marcos Macedo AndiaAún no hay calificaciones
- Determinacion CarbonatosDocumento11 páginasDeterminacion CarbonatosCarlos Llona0% (1)
- Acido FuerteDocumento9 páginasAcido FuerteOSNAIDER JOSE PEÑA CUETO ESTUDIANTEAún no hay calificaciones
- 1 ANALISIS VOLUMETRICO Practica IDocumento9 páginas1 ANALISIS VOLUMETRICO Practica IRodrigo FloressAún no hay calificaciones
- Volume TriaDocumento4 páginasVolume TriaCeciliaCavesAún no hay calificaciones
- Determinacion de Carbonatos y BicarbonatosDocumento4 páginasDeterminacion de Carbonatos y BicarbonatosEstebanAún no hay calificaciones
- Acidimetria y Alcalimetria1Documento10 páginasAcidimetria y Alcalimetria1Jimmy FiestasAún no hay calificaciones
- Curva de TitulacionDocumento7 páginasCurva de TitulacionStefanyQuisbertDiazAún no hay calificaciones
- Constante de AcidezDocumento18 páginasConstante de AcidezMilagros Osorio Tábraj100% (1)
- NeutralizaciónDocumento12 páginasNeutralizaciónMiguel CarmonaAún no hay calificaciones
- Imprimir Informe 1 AnaliticaDocumento14 páginasImprimir Informe 1 AnaliticaMariam Cabellos SAún no hay calificaciones
- Titulacion de SolucionesDocumento6 páginasTitulacion de SolucionesAlejandra Guadalupe AcostaAún no hay calificaciones
- Introducción Titulacion Acidos BasesDocumento5 páginasIntroducción Titulacion Acidos BasesBetty SantiagoAún no hay calificaciones
- Cálculo de CarbonatosDocumento10 páginasCálculo de CarbonatosireneAún no hay calificaciones
- Punto EquivalenciaDocumento12 páginasPunto EquivalenciaCassandra YatesAún no hay calificaciones
- Química Reporte de PrácticaDocumento16 páginasQuímica Reporte de PrácticaNicoole HernandezAún no hay calificaciones
- Informe de Laboratorio, Titulacion de Soluciones Acido-BaseDocumento6 páginasInforme de Laboratorio, Titulacion de Soluciones Acido-BaseLina LarrotaAún no hay calificaciones
- Informe - Lab Quimica G2 Juan Camilo Cardona - Juan Felipe Ramirez Garcia #6Documento9 páginasInforme - Lab Quimica G2 Juan Camilo Cardona - Juan Felipe Ramirez Garcia #6Felipe RamirezAún no hay calificaciones
- Repo#3 Jose Arellano AguirreDocumento5 páginasRepo#3 Jose Arellano AguirreJose Arellano AguirreAún no hay calificaciones
- Métodos VolumétricosDocumento8 páginasMétodos VolumétricosEmanuel MoralesAún no hay calificaciones
- Conferencia 2Documento10 páginasConferencia 2Denis Lopez MartinezAún no hay calificaciones
- Titulación de Un Ácido Fuerte Con Una Base FuerteDocumento6 páginasTitulación de Un Ácido Fuerte Con Una Base FuerteValentina CalleAún no hay calificaciones
- Practica 2 Valoracion Acido BaseDocumento4 páginasPractica 2 Valoracion Acido BaseAnthonio MothaAún no hay calificaciones
- TitulaciónDocumento4 páginasTitulaciónJair CordovaAún no hay calificaciones
- Estandarizacion y TitulacionDocumento7 páginasEstandarizacion y TitulacionMaría Alejandra GuerreroAún no hay calificaciones
- PR Ctica N 3-Titulaci N Cido-BaseDocumento12 páginasPR Ctica N 3-Titulaci N Cido-BaseMaría ContrerasAún no hay calificaciones
- Práctica 13Documento5 páginasPráctica 13elirc25Aún no hay calificaciones
- Análisis de Mezclas de Álcalis-1Documento15 páginasAnálisis de Mezclas de Álcalis-1Loli PabuenaAún no hay calificaciones
- Practica Determinacion de Hidroxido de Sodio, Carbonato y Bicarbonato de Sodio-2Documento5 páginasPractica Determinacion de Hidroxido de Sodio, Carbonato y Bicarbonato de Sodio-2Roberto Arias FloresAún no hay calificaciones
- Calibración de Un PotenciómetroDocumento3 páginasCalibración de Un PotenciómetroRoberto Arias FloresAún no hay calificaciones
- Rompecabezas PlanisferioDocumento2 páginasRompecabezas PlanisferioRoberto Arias FloresAún no hay calificaciones
- A#11 Raf,.Documento11 páginasA#11 Raf,.Roberto Arias FloresAún no hay calificaciones
- Practica 10Documento8 páginasPractica 10Roberto Arias FloresAún no hay calificaciones
- Reporte No 4 5 Control Calidad de FarmacosDocumento14 páginasReporte No 4 5 Control Calidad de FarmacosRoberto Arias FloresAún no hay calificaciones
- A#11 Raf.Documento7 páginasA#11 Raf.Roberto Arias FloresAún no hay calificaciones
- A#2 RafDocumento4 páginasA#2 RafRoberto Arias FloresAún no hay calificaciones
- A#1 RafDocumento4 páginasA#1 RafRoberto Arias FloresAún no hay calificaciones
- Mapa ConceptualDocumento2 páginasMapa ConceptualRoberto Arias FloresAún no hay calificaciones
- Act# 4rafDocumento5 páginasAct# 4rafRoberto Arias FloresAún no hay calificaciones
- Práctica No2 Sin PortadaDocumento9 páginasPráctica No2 Sin Portadamikihibito1994Aún no hay calificaciones
- Phypoh: H / Oh H /ohDocumento3 páginasPhypoh: H / Oh H /ohhector lopezAún no hay calificaciones
- Examenes Pasados Tercer Parcial 2021 y 2020 Fqb-102 1-2022Documento5 páginasExamenes Pasados Tercer Parcial 2021 y 2020 Fqb-102 1-2022Natalia CarreraAún no hay calificaciones
- Informe Determinación de La Estequiometría de Una Reacción Química Por Análisis GravimétricoDocumento2 páginasInforme Determinación de La Estequiometría de Una Reacción Química Por Análisis GravimétricoElor TorrotoAún no hay calificaciones
- PRACTICA15Documento7 páginasPRACTICA15Frida Gtz'Aún no hay calificaciones
- Calor Diferencial de SoluciónDocumento4 páginasCalor Diferencial de SoluciónLuis Cifuentes IIAún no hay calificaciones
- Determinación de Nitrito en AguaDocumento4 páginasDeterminación de Nitrito en AguaLiz Karen Valdez SosaAún no hay calificaciones
- ComplexometriaDocumento17 páginasComplexometriaHeliAún no hay calificaciones
- Acidez en LecheDocumento3 páginasAcidez en LecheRubén Rueda AmayaAún no hay calificaciones
- Meza Ramos - Tarea7 - QuimicaDocumento5 páginasMeza Ramos - Tarea7 - QuimicaGris MezaAún no hay calificaciones
- Determinación Colorimétrica Del PHDocumento13 páginasDeterminación Colorimétrica Del PHhanscortesAún no hay calificaciones
- Práctica N°9Documento4 páginasPráctica N°9JcAún no hay calificaciones
- Equilibrio de SolubilidadDocumento27 páginasEquilibrio de SolubilidadHanz Pichilingue CruzAún no hay calificaciones
- Práctica 5 Obtención de Indicadores Con Productos CaserosDocumento11 páginasPráctica 5 Obtención de Indicadores Con Productos CaserosCarlaAún no hay calificaciones
- Potenciometria Docx-259384599Documento9 páginasPotenciometria Docx-259384599MaríaAntezanaAún no hay calificaciones
- Clase 6.1 Volumetría Por Formación de Complejos - IDocumento16 páginasClase 6.1 Volumetría Por Formación de Complejos - IBC NandoAún no hay calificaciones
- Clase 09 Equilibrio Iónico DipróticosDocumento33 páginasClase 09 Equilibrio Iónico DipróticosDANA VALEZKA VASQUEZ GUTIERREZAún no hay calificaciones
- Analitica6 SDocumento9 páginasAnalitica6 SJuan David AlegriaAún no hay calificaciones
- Equilibrio QuímicoDocumento2 páginasEquilibrio Químicohector lopezAún no hay calificaciones
- Elementos de La Tabla PeriodicaDocumento6 páginasElementos de La Tabla PeriodicaOSWALDO GUTIERREZ STERLINGAún no hay calificaciones
- Método Espectrométrico PDFDocumento2 páginasMétodo Espectrométrico PDFYoandy RodriguezAún no hay calificaciones
- Olguín Carranza - Diana Laura - M15S1AI1Documento12 páginasOlguín Carranza - Diana Laura - M15S1AI1luna pereAún no hay calificaciones
- Tema 7 23-24Documento83 páginasTema 7 23-24Miguel Ángel Morán VianaAún no hay calificaciones
- 3.3 Cromatografía de Líquidos de Alta ResoluciónDocumento7 páginas3.3 Cromatografía de Líquidos de Alta ResoluciónMalpica Flores Yosabeth AbigailAún no hay calificaciones
- Serie 6. Volumetrias Por Precipitación 2C 2022Documento4 páginasSerie 6. Volumetrias Por Precipitación 2C 2022lucianaramirezmalikAún no hay calificaciones
- Prueba 3 Medio Quimica CineticaDocumento1 páginaPrueba 3 Medio Quimica CineticaMarisol CabelloAún no hay calificaciones
- Prueba de CianuraciónDocumento13 páginasPrueba de CianuraciónJuan Pablo Ortiz HernandezAún no hay calificaciones
- 12 Acidos y Bases PDFDocumento20 páginas12 Acidos y Bases PDFbenavidesAún no hay calificaciones