Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Sesión 04. Espectroscopia Con Llama
Cargado por
Stacy Ruddy Flores MacedoDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Sesión 04. Espectroscopia Con Llama
Cargado por
Stacy Ruddy Flores MacedoCopyright:
Formatos disponibles
ESCUELA PROFESIONAL DE
INGENIERÍA QUÍMICA
ESPECTROSCOPIA CON
LLAMA
CURSO : ANÁLISIS INSTRUMENTAL
DOCENTE : Ing. Mg. RICARDO RODRIGUEZ VILCHEZ
SEMESTRE ACADÉMICO
Setiembre del 2021 2021 B
1
INTRODUCCIÓN
• Los métodos de espectroscopia atómica incluyen aquellos métodos de análisis
que se basan en la absorción, emisión y fluorescencia por las partículas
atómicas (atomización).
• Las radiaciones involucradas en estos procesos son: rayos X, UV y Visible.
• Está basada en la utilización de átomos al estado de vapor activados mediante
energía electromagnética o energía térmica, Midiendo la energía absorbida o
emitida por los átomos al pasar a un estado activado o al volver del estado
activado.
2
Ing. Mg. Ricardo Rodriguez Vilchez 1
3
ESPECTROSCOPIA ATÓMICA
• La absorción y emisión, supone la excitación de electrones que se encuentran
en las capas o niveles internos del átomo.
• La absorción y emisión de radiación en las regiones UV y VIS supone la
excitación de electrones de valencia.
• Es necesario convertir los constituyentes de la muestra en partículas
monoatómicas gaseosas, atomización.
• El espectro de emisión así como el de absorción consiste en varias líneas que
aparecen a longitudes de onda características del elemento.
4
Ing. Mg. Ricardo Rodriguez Vilchez 2
• Las técnicas de análisis basadas en espectroscopia atómica, difieren en:
• Radiación electromagnética envuelta
• Método utilizado par atomizar las muestras
• Llama
• Arco
• Chispa.
Ing. Mg. Ricardo Rodriguez Vilchez 3
ATOMIZACIÓN:
FLAMAS, HORNOS Y PLASMAS
• En espectroscopia atómica, el analito es atomizado en una llama, calentado
eléctricamente en un horno o con un plasma de radio frecuencia.
• La sensitividad analítica e interferencias dependerán de la atomización.
ATOMIZACIÓN DE LA MUESTRA
• Atomizador continuo
La solución de la muestra se convierte en una niebla de pequeñas gotas
finamente divididas mediante un chorro de gas comprimido = nebulización. El
flujo de gas transporta la muestra a una región calentada, desolvatación, donde
tienen lugar la atomización
• Atomizador discreto
El volumen medido de una disolución se introduce en el dispositivo.
Ing. Mg. Ricardo Rodriguez Vilchez 4
La desolvatación ocurre al aumentar la temperatura hasta la evaporación del
solvente.
- La temperatura aumenta drásticamente.
- La señal adquiere forma de pico.
PROCESOS DE ATOMIZACIÓN
Muestra (solución)
Nebulización
Aerosol líquido / gas
Evaporación de disolvente (desolvatación)
Aerosol sólido / gas
Volatización
Moléculas (g) M+ hn Atómico
Disociación (reversible)
Vapor atómico átomos excitados hn Atómico
Ionización (reversible)
Ion atómico iones excitados hn Atómico 10
Ing. Mg. Ricardo Rodriguez Vilchez 5
ATOMIZACIÓN CON FLAMA
• Cuando una solución de una sal inorgánica se rocía dentro de una flama de un
mechero, una fracción de los iones metálicos se reduce a su estado elemental y
se forman algunos iones monoatómicos en menor grado.
• En la flama se forma una solución gaseosa (plasma) de partículas elementales
(no hay iones complejos o moléculas).
11
ATOMIZADORES DE FLAMA
• Se emplean en medidas de emisión, absorción y fluorescencia atómica
• Consiste en un nebulizador neumático que transforma la muestra en solución
en un aerosol.
• El tipo de nebulizador más común es el de tubo concéntrico, donde la muestra
se aspira a través de un tubo capilar mediante un flujo de gas a alta presión
alrededor de la punta del capilar (efecto Venturi).
• El combustible y el oxidante, en general se combinan en una proporción
estequiométrica.
• Los metales que forman óxidos estables emplean flamas con exceso de
combustible.
12
Ing. Mg. Ricardo Rodriguez Vilchez 6
ATOMIZACIÓN CON FLAMA
13
ESTRUCTURA DE LA FLAMA
• Zona de combustión primaria
- Presenta luminiscencia azul que proviene de los espectros de bandas de C2,
CH y otros radicales.
- Esta zona no alcanza el equilibrio térmico.
- Rara vez se utiliza en espectroscopia de flama.
• Región Interconal
- Rica en átomos libres.
- Más utilizada en espectroscopia.
14
Ing. Mg. Ricardo Rodriguez Vilchez 7
• Cono exterior
• Zona de reacción secundaria.
• Se forma óxidos moleculares estables.
15
ATOMIZACIÓN CON FLAMA
16
Ing. Mg. Ricardo Rodriguez Vilchez 8
ATOMIZACIÓN CON FLAMA
• Emisión atómica
• La muestra se rocía en la flama y el calor de la flama es suficiente para
excitar las partículas de la solución gaseosa a estados electrónicos más
energéticos.
• Cuando las partículas regresan al estado raso emiten radiación, la cual es
detectada y da lugar a un espectro de líneas.
• La localización de las líneas provee información cualitativa y la intensidad de
las líneas permiten la determinación cuantitativa.
17
ESQUEMA BÁSICO DE LA INSTRUMENTACIÓN
18
Ing. Mg. Ricardo Rodriguez Vilchez 9
19
20
Ing. Mg. Ricardo Rodriguez Vilchez 10
Carcasa metálica
EDL Ar
Sólo para elementos fácilmente vaporizables
(As, Se, Sb, Pb, Sn, Hg…)
Ventana de cuarzo
I(EDL) > I(LCH)
Bovina generadora Analito en estado metálico o en forma de sal
de radiofrecuencias
Proceso de emisión de rem en una EDL
M* M*
Ar0 Ar+ + e- hδ
M0 Ar+
M0
1. Ionización del Ar 2. Excitación de los átomos 3. Relajación de los
del metal analito átomos
Acción del campo de
microondas o radiofrecuencias
21
Monocromador
Espejos cóncavos
Red de Plano
reflexión focal
Ranura Ranura
de entrada de salida
22
Ing. Mg. Ricardo Rodriguez Vilchez 11
Espectrometría de absorción atómica con atomización en llama (FAAS)
Fuente de
Modulador LLAMA Monocromador Detector Registrador
radiación
Lámpara
Nebulizador
Quemador
ATOMIZADOR
Modulador rotatorio
FUNCIÓN Lámpara
Discriminar entre:
Quemador
luz procedente de la fuente
y
luz procedente de la llama
Lámpara + llama Llama
Señal del detector
Señal
analítica
Tiempo
23
Quemador de flujo turbulento o de consumo total
Oxidante, combustible y muestra
se mezclan de forma turbulenta: RUIDO
Oxidante
Combustible
Mayor nº de interferencias
El 100% de la muestra aspirada alcanza el quemador
24
Ing. Mg. Ricardo Rodriguez Vilchez 12
25
Espectrometría de absorción atómica con atomización electrotérmica
(ETAAS)
CALENTAMIENTO
LONGITUDINAL
Tubo de grafito
Inyección de muestra
Camino
óptico
Camino
óptico
CALENTAMIENTO
Contactores eléctricos
TRANSVERSAL enfriados con agua
26
Ing. Mg. Ricardo Rodriguez Vilchez 13
CALENTAMIENTO
TRANSVERSAL
Inyección de muestra
hasta 40 µL Camino
Camino
óptico
óptico
Tubo de grafito
en el interior
Pared Contactores eléctricos
del tubo Camino
Plataforma de enfriados con agua
óptico
L´vov curvada
27
28
Ing. Mg. Ricardo Rodriguez Vilchez 14
OTROS MÉTODOS
ESPECTROFOTOMÉTRICOS
29
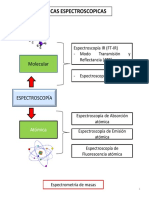
MÉTODOS
• Espectrometría de Absorción Atómica.
• Espectrometría de Emisión Atómica.
• Espectrometría de Masa Atómica.
• Espectrometría Atómica de Rayos X.
• Espectrometría de Absorción Molecular UV, VIS.
• Espectrometría de Luminiscencia Molecular.
• Espectrometría de Absorción en el IR.
• Espectroscopia Raman.
• Espectroscopia de Resonancia Magnética Nuclear.
• Espectroscopia de Masas Molecular.
30
Ing. Mg. Ricardo Rodriguez Vilchez 15
¿En qué se basa la Espectrofotometría Atómica?
• Es la absorción, emisión y/o fluorescencia de radiación electromagnética por las
partículas atómicas.
¿Qué regiones del espectro proporcionan datos atómicos espectrales?
• Región del UV-Visible
• Región de Rayos X
31
¿Cómo se obtienen los Espectros Atómicos del UV-Visible?
• Atomizando las muestras: las moléculas constituyentes se descomponen y se
convierten en partículas gaseosas elementales.
• Los espectros obtenidos están constituidos por una cantidad limitada de líneas
discretas de λ características de cada elemento.
¿Cuáles son las ventajas de los métodos analíticos basados en la Espectrofotometría
Atómica?
• Son específicos.
• Amplio rango de aplicación.
• Excelente sensibilidad.
• Rapidez y conveniencia.
32
Ing. Mg. Ricardo Rodriguez Vilchez 16
INTRODUCCIÓN A LA ESPECTROFOTOMETRÍA DE
EMISIÓN ATÓMICA
¿Cómo obtenemos los Espectros Ópticos Atómicos?
• Los componentes de la muestra deben convertirse en átomos o iones en estado
gaseoso, que pueden determinarse mediante medios espectrales de emisión,
absorción, fluorescencia o masa: ATOMIZACIÓN.
33
TIPOS DE ATOMIZADORES USADOS EN
ESPECTROFOTOMETRÍA ATÓMICA
• Llama.
• Vaporización electrotérmica.
• Plasma de argón (ICP)
• Plasma de corriente continua (DCP)
• Plasma por microondas (MIP)
• Plasma de descarga luminiscente (CD)
• Arco eléctrico.
• Chispa eléctrica.
34
Ing. Mg. Ricardo Rodriguez Vilchez 17
ESPECTROFOTOMETRÍA DE EMISIÓN CON FUENTES
DE PLASMA
• En la actualidad, las fuentes de plasma son las más importantes y usadas (ICP,
DCP, MIP).
¿Cuáles son las ventajas de la emisión de plasma vs. Llama?
• Menor interferencia entre elementos (altas temperaturas);
• Buenos espectros de emisión para muchos elementos en las mismas
condiciones de excitación;
• Registro simultáneo para una gran número de elementos (análisis
multielemental). 35
• Fuente de energía controlable para la excitación necesaria para excitar
todos los elementos sin ionización apreciable.
• Un medio químico inerte que impida la formación de especies
moleculares no deseables (e.g. óxidos, carburos, etc.) que puedan
afectar la precisión de las medidas.
Una fuente perfecta de emisión atómica tiene que presentar las siguientes
características:
1. Eliminación completa de la muestra desde su matriz original con el fin
de minimizar interferencias.
36
Ing. Mg. Ricardo Rodriguez Vilchez 18
2. Atomización completa, pero mínima ionización de los elementos a
analizar.
3. Fuente de energía controlable para la excitación necesaria para excitar
todos los elementos sin ionización apreciable.
4. Un medio químico inerte que impida la formación de especies
moleculares no deseables (e.g. óxidos, carburos, etc.) que puedan
afectar la precisión de las medidas.
37
5. No tiene que existir radiación de fondo (background) desde la fuente.
La radiación background se define como aquella emisión atómica y/o
molecular no deseable que podría interferir con las longitudes de onda
analíticas.
6. Una fuente que abarque un amplio rango de solventes (tanto orgánicos
como inorgánicos).
7. Ajustable a cualquier tipo de muestras.
8. Barato en su adquisición y mantenimiento.
9. Fácil de operar.
38
Ing. Mg. Ricardo Rodriguez Vilchez 19
¿QUÉ ES UN PLASMA?
Mezcla gaseosa conductora de la electricidad que contiene una concentración
significativa de cationes y electrones, con carga neta cero. Se usa ARGÓN. Las
especies conductoras son los iones argón, electrones y, en menor concentración,
cationes de la muestra.
Existen tres tipo de plasma:
(1) Plasma de acoplamiento inductivo.
(2) Plasma de corriente continua.
(3) Plasma inducido por microondas.
39
40
Ing. Mg. Ricardo Rodriguez Vilchez 20
41
¿CUÁLES SON LAS CARACTERÍSTICAS ACTUALES DE
UN ESPECTROFOTÓMETRO DE EMISIÓN ATÓMICA?
Abarcan el espectro UV-Visible (170-800 nm).
En condiciones de vacío, pueden alcanzar 150-160 nm (de interés para P, S, C..):
Son de tres tipos:
1º Secuenciales (para ir de una línea de emisión a otra en pocos segundos, hasta
obtener una buena relación señal/ruido).
2º Multicanal simultáneos (medida simultánea o cuasi simultánea de las líneas de emisión
de una gran número de elementos).
3º De transformada de Fourier (los menos utilizados).
Tanto 1º como 2º son de dos tipos: uno emplea un monocromador clásico y el otro un
monocromador en escalera. 42
Ing. Mg. Ricardo Rodriguez Vilchez 21
APLICACIONES DE LAS FUENTES DE PLASMA
¿Cuáles son las características de las fuentes de plasma?
Son ricas en líneas de emisión características.
Útiles para el análisis elemental (cualitativo y cuantitativo).
ICP y DCP aportan datos analíticos cuantitativos mejores que otras fuentes de
emisión, debido a su estabilidad, bajo ruido, poca radiación de fondo y ausencia
de interferencias cuando se trabaja en condiciones adecuadas.
Límites de detección aceptables.
43
ESPECTROFOTOMETRÍA DE MASA ATÓMICA
• La espectrometría de masa atómica es una herramienta versátil y muy utilizada
para identificar los elementos presentes en muestras de materia y determinar
sus concentraciones.
• Casi todos los elementos del Sistema Periódico se pueden determinar por
espectrometría de masas.
44
Ing. Mg. Ricardo Rodriguez Vilchez 22
VENTAJAS EN RELACIÓN A LOS MÉTODOS ANTERIORES
• Mejores límites de detección
• Espectros notablemente sencillos que generalmente son únicos y con frecuencia
de fácil interpretación.
• Capacidad para medir relaciones isotópicas atómicas.
Desventajas
• El costo del instrumento es de dos a tres veces más caro que el de los
instrumentos ópticos atómicos.
• Sufre interferencias.
45
ASPECTOS GENERALES DE LA ESPECTROFOTOMETRÍA
DE MASA ATÓMICA
Implica las siguientes etapas:
• Atomización.
• Ionización de una fracción de los átomos formados en la etapa 1.
• Separación de los iones formados en la segunda etapa.
• Recuento del número de iones de cada tipo o medida de la corriente iónica
producida cuando los iones formados a partir de la muestra inciden en un
detector adecuado.
46
Ing. Mg. Ricardo Rodriguez Vilchez 23
TIPOS DE ESPECTROFOTOMETRÍA DE MASA
ATÓMICA
47
COMPONENTE DE UN ESPECTROFOTÓMETRO DE MASA
48
Ing. Mg. Ricardo Rodriguez Vilchez 24
ESPECTROFOTOMETRÍA ATÓMICA DE RAYOS X
• Al igual que la espectrofotometría óptica, se basa en la medida de la emisión,
absorción, dispersión, fluorescencia y difracción de la radiación
electromagnética.
• Los métodos de fluorescencia y de absorción de rayos X son muy utilizados
para la determinación cualitativa y cuantitativa de todos los elementos de la
tabla periódica con números atómicos superiores al del sodio.
49
RAYOS X
• Rayos X: radiación electromagnética de longitud de onda corta producida por el
frenado de electrones de elevada energía o por transiciones de electrones que se
encuentran en los orbitales internos de los átomos.
PRODUCCIÓN DE RAYOS X
• Si un electrón interior es expulsado, el hueco que se produce puede ser ocupado por
otro electrón mas externo.
• La diferencia de energía se pone de manifiesto como una radiación X
• Esta diferencia se relaciona con el tipo de átomo, por lo que se relaciona siempre con
el número atómico Z .
50
Ing. Mg. Ricardo Rodriguez Vilchez 25
VENTAJAS
• Espectros sencillos.
• Método no destructivo.
• Análisis desde partículas a grandes objetos.
• Velocidad.
• Exactitud y precisión.
Desventajas
• Sensibilidad inferior que los método ópticos (0.01 a 100 %).
• No adecuado para elementos ligeros.
• Cosos elevados.
51
TRATAMIENTO DEL MÉTODO ADICION
PATRÓN
52
Ing. Mg. Ricardo Rodriguez Vilchez 26
TRATAMIENTO DEL MÉTODO ADICIÓN PATRÓN
𝑥 𝐴𝑥
= ... (1)
𝑥+𝑠 𝐴𝑠+𝑥
Donde:
𝑥 = Conc. del problema.
𝑠 = Conc. del patrón agregado.
Ax = Absorbancia (intensidad) del problema.
As = Absorbancia (intensidad) del problema ( + ) el patrón.
53
• Método Gráfico de Y Adición Patrón ... (2)
54
Ing. Mg. Ricardo Rodriguez Vilchez 27
𝐴𝐶 Con el eje Y indica la intensidad de emisión en la
(mg/ml) I muestra (28 unidades)
F Estará a una intensidad de 28+28 o sea 56
00 28
G Se encuentra en 28 de intensidad.
0.2 37
0.4 46 Se requiere una concentración 0.62 mg 𝐶𝐺 para
0.6 55
producir 28 unidades, la muestra desconocida 𝐷𝐸
también debe tener 0.62 mg.
0.8 63
𝐶𝐷𝐸 = 𝐹𝐶𝐺
55
Una muestra de una solución de Reemplazando:
mineral analizada por Zn2+ 𝑍𝑛2+ 0.179
=
empleando E. A. muestra una A de 𝑍𝑛2+ +3 0.261
0.179. A una alícuota de esta 0.179 𝑍𝑛2+ + 0.537 = 0.26 𝑍𝑛2+
solución se le agrega Zn2+ para 0.261 𝑍𝑛2+ − 0.179 𝑍𝑛2+ = 0.537
incrementar su concentración por 𝑍𝑛2+ =
0.537
0.082
3.00 ppm. La alícuota fue analizada
𝑍𝑛2+ = 6.548 𝑝𝑝𝑚
y dio una A de 0.261.
𝑥 𝐴𝑥
=
𝑥+𝑠 𝐴𝑠 + 𝑥
56
Ing. Mg. Ricardo Rodriguez Vilchez 28
PROBLEMAS
57
Problema N° 1
Para determinar la concentración de analito en una muestra, se realizó una adición
patrón. Se añadieron cantidades sucesivas de 0.10 ml de un patrón que contenía
600 ppb del analito. Se analizó una porción de 5.00 ml de la muestra, un análisis
tras cada adición se practicaron obteniéndose los resultados siguientes.
Datos en la gráfica para la graficación correspondiente.
58
Ing. Mg. Ricardo Rodriguez Vilchez 29
59
Problema N° 2
El Cromo en una muestra acuosa se determinó introduciendo alícuotas de 10 ml
de la muestra en 5 matraces de 50.0 ml. Antes de enrasar los matraces se
añadieron a cada uno de ellos volúmenes distintos de un patrón de 12.2 ppm de
Cr.
Muestra ml Estándar ml A
10 0.0 0.201
10 10 0.292
10 20 0.376
10 30 0.467
10 40 0.554
60
Ing. Mg. Ricardo Rodriguez Vilchez 30
Hallando concentraciones:
12.2 𝑥 10
𝑃𝑎𝑟𝑎: 10 𝑚𝑙 = = 2.44 𝑝𝑝𝑚
50
12.2 𝑥 20
𝑃𝑎𝑟𝑎: 20 𝑚𝑙 = = 4.88 𝑝𝑝𝑚
50
12.2 𝑥 30
𝑃𝑎𝑟𝑎: 30 𝑚𝑙 = = 7.32 𝑝𝑝𝑚
50
12.2 𝑥 40
𝑃𝑎𝑟𝑎: 40 𝑚𝑙 = = 9.76 𝑝𝑝𝑚
50
𝑉𝐴 50
𝑓𝑑 = = = 5
𝑉𝑎 10
𝐶𝑝𝑝𝑚𝐶𝑟 = 5.6 𝑥 5 = 28 𝑝𝑝𝑚
61
62
Ing. Mg. Ricardo Rodriguez Vilchez 31
APLICACIÓN DE LA TÉCNICA DE
TITULACIÓN FOTOMÉTRICA
63
El Magnesio se puede determinar por titulación fotométrica con EDTA (Na2H2Y),
la reacción se efectúa en relación estequiométrica 1 a 1. 𝑀𝑔+2 + 𝑦 4− ⇆
𝑀𝑔𝑀𝑔𝑌 2−
Se toman 50 ml de una solución de magnesio de un matraz volumétrico de 250
ml y se titulan con una solución de Na2H2Y 0.1000 M. Los datos son:
µL sol de y4- 0.0 6.0 12 18 24 30 36 42 48 54 60 70 80
Ac (540 nm), 1 cm 0.227 0.256 0.287 0.318 0.349 0.375 0.406 0.433 0.455 0.459 0.462 0.465 0.464
¿Cuántos miligramos de Magnesio se encuentran presentes en el matraz
volumétrico de 250 ml.?
64
Ing. Mg. Ricardo Rodriguez Vilchez 32
𝑚𝑜𝑙
10.50𝑥10−3 𝑙𝑡𝑠 1.00𝑥10−1 = 10.50𝑥10−4 𝑚𝑜𝑙
𝑙𝑡𝑠
Moles de Mg es 250 ml
5 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 𝑀𝑔 𝑒𝑛 50 𝑚𝑙
(5)(10.50𝑥10−4 𝑚𝑙 )
𝐶 ⇒ 5.25𝑥10−3 𝑚𝑙
250
𝑓𝑑 = =5
50
103 𝑚𝑔
𝑚𝑔 𝑑𝑒 𝑀𝑔 = 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 𝑀𝑔 𝑒𝑛 250 𝑚𝑙 𝑃. 𝑎𝑡. 𝑀𝑔 𝑔𝑟
𝑚𝑔 𝑑𝑒 𝑀𝑔 = 127.638 𝑚𝑔 𝑑𝑒 𝑀𝑔
65
⇒ Otro método:
𝑚𝑜𝑙 1 𝑙𝑡 24.312 𝑔𝑟 103 𝑚𝑔
𝑚𝑔 𝑑𝑒 𝑀𝑔 = 0.100 𝑥 𝑥 10.50 𝑚𝑙 𝑥 𝑥
𝑙𝑡 103 𝑚𝑙 1 𝑚𝑜𝑙 𝑀𝑔 1𝑔
25.5276 𝑥 𝑓𝑑 5 = 127.638 𝑚𝑔 𝑑𝑒 𝑀𝑔
66
Ing. Mg. Ricardo Rodriguez Vilchez 33
Gráfica para la determinación del Volumen
Equivalente en la Titulación de Magnesio con EDTA
67
68
Ing. Mg. Ricardo Rodriguez Vilchez 34
69
Link de video:
https://www.youtube.com/watch?v=xomiBHPluH4&t=102s
70
Ing. Mg. Ricardo Rodriguez Vilchez 35
También podría gustarte
- Absorción AtómicaDocumento23 páginasAbsorción AtómicaMaria Chavez JuarezAún no hay calificaciones
- Elementos de Un EspectrosDocumento37 páginasElementos de Un EspectrosPreu UnprgAún no hay calificaciones
- Absorcion AtomicaDocumento44 páginasAbsorcion AtomicaErika Itzel C AAún no hay calificaciones
- Análisis Instrumental Cuestionario Unidad IiDocumento11 páginasAnálisis Instrumental Cuestionario Unidad IiAzael Cortes LopezAún no hay calificaciones
- Clase 7 - 210417Documento42 páginasClase 7 - 210417Jorge Alejandro Lara GodoyAún no hay calificaciones
- CUESTIONARIO UNIDAD II 2a. PARTE AGO-DIC 2016Documento9 páginasCUESTIONARIO UNIDAD II 2a. PARTE AGO-DIC 2016Azael Cortes LopezAún no hay calificaciones
- EspectAbsorcAtomica F GH HGDocumento80 páginasEspectAbsorcAtomica F GH HGRafael GonzálezAún no hay calificaciones
- Absorción AtómicaDocumento62 páginasAbsorción AtómicaJulián GiménezAún no hay calificaciones
- ESPECTROSCOPIA ATOMICA ESPOSICION JVCDocumento16 páginasESPECTROSCOPIA ATOMICA ESPOSICION JVCYoshimar Carrasco SoriaAún no hay calificaciones
- Química AnalíticaDocumento28 páginasQuímica AnalíticaOLGA VEGAAún no hay calificaciones
- 5-Absorcion AtomicaDocumento41 páginas5-Absorcion AtomicaElizabeth HrAún no hay calificaciones
- Atomic Absorption and Atomic Fluorescence SpectrosDocumento36 páginasAtomic Absorption and Atomic Fluorescence SpectrosKheley Axis Evaristo CopitanAún no hay calificaciones
- DETERMINACIÓN DE ZN EN CONSERVAS DE PESCADO POR ABSORCION ATÓMICA EN LLAMADocumento6 páginasDETERMINACIÓN DE ZN EN CONSERVAS DE PESCADO POR ABSORCION ATÓMICA EN LLAMAValeriaAún no hay calificaciones
- PRACTICA No4 ANALITICADocumento12 páginasPRACTICA No4 ANALITICAdoncuev0% (2)
- Unidad III - Esp. de Absorcion Atómica - 2019 - IBQDocumento44 páginasUnidad III - Esp. de Absorcion Atómica - 2019 - IBQGómez Ruiz MaximilianoAún no hay calificaciones
- Espectros de Emision y AbsorcionDocumento27 páginasEspectros de Emision y AbsorcionAldo Richard Lopez CordovaAún no hay calificaciones
- Espectrofotometria de Absorcion AtomicaDocumento44 páginasEspectrofotometria de Absorcion Atomicajulio100% (1)
- Fotometria LlamaDocumento73 páginasFotometria LlamaHéctor Fernández100% (2)
- EspectrosDocumento31 páginasEspectrosKaren Angie Avalos100% (1)
- Semana 4 - Lab. Virtual Espectros de Emisión - Química - 2021-20.Documento14 páginasSemana 4 - Lab. Virtual Espectros de Emisión - Química - 2021-20.JairMedinaAún no hay calificaciones
- Semana 2 - Lab. Virtual Espectros de Emisión - Química 1 - 2022-10Documento14 páginasSemana 2 - Lab. Virtual Espectros de Emisión - Química 1 - 2022-10Armando Calcina ColquiAún no hay calificaciones
- Espectroscopía de Absorción AtómicaDocumento21 páginasEspectroscopía de Absorción AtómicaPekkaSwamplordAún no hay calificaciones
- Método de Espectrofotometría de Absorción Atómica Principio Físico y Tipos de LlamaDocumento22 páginasMétodo de Espectrofotometría de Absorción Atómica Principio Físico y Tipos de LlamamattkidoAún no hay calificaciones
- Exposicion de Absorcion Atomica IIDocumento35 páginasExposicion de Absorcion Atomica IIAna ColinaAún no hay calificaciones
- Espectroscopia de Absorcion AtomicaDocumento35 páginasEspectroscopia de Absorcion Atomicadavidanzoleaga100% (1)
- E Spectro Fabs Orc I On Atomic ADocumento44 páginasE Spectro Fabs Orc I On Atomic ARafael GonzálezAún no hay calificaciones
- Espectroscopia AtomicaDocumento26 páginasEspectroscopia AtomicaJurix MaxAún no hay calificaciones
- Absorción Atómica FinalDocumento44 páginasAbsorción Atómica FinalMauro VanarelliAún no hay calificaciones
- Conferencia 2 Unidad IIIDocumento33 páginasConferencia 2 Unidad IIIGa HerlindaAún no hay calificaciones
- Generador de Hidruros - Interferencia de IonizaciónDocumento22 páginasGenerador de Hidruros - Interferencia de IonizaciónLili RosalesAún no hay calificaciones
- Protocolo para La Determinacion de HierroDocumento8 páginasProtocolo para La Determinacion de HierroFabían Díaz Jhordan JhampierdAún no hay calificaciones
- Espectroscopia de Absorcion AtomicaDocumento21 páginasEspectroscopia de Absorcion AtomicaEdd Camilo MorenoAún no hay calificaciones
- Análisis de Minerales Por Absorción AtómicaDocumento25 páginasAnálisis de Minerales Por Absorción AtómicaDanna LópezAún no hay calificaciones
- Informe 2 Ana InstruhhhDocumento19 páginasInforme 2 Ana InstruhhhNilton Cj100% (1)
- 007 Espectroscopia Atómica Con LlamaDocumento52 páginas007 Espectroscopia Atómica Con LlamaCésar Fernando Melquiades BravoAún no hay calificaciones
- Espectroscopia de Abs AtomicaDocumento8 páginasEspectroscopia de Abs Atomicaalex garciaAún no hay calificaciones
- Métodos de Análisis de Metales Pesados en Agua TerminadoDocumento20 páginasMétodos de Análisis de Metales Pesados en Agua TerminadoPatricia Pereda SimoniAún no hay calificaciones
- Qan U3 Ea IstnDocumento8 páginasQan U3 Ea IstnIsmael Trejo nuñezAún no hay calificaciones
- Absorción AtómicaDocumento17 páginasAbsorción AtómicaAlessandro ZapataAún no hay calificaciones
- Absorcion Atomica FinalDocumento14 páginasAbsorcion Atomica FinalAngie Alyssa MendozaAún no hay calificaciones
- Espectrofotometría de Absorción AtómicaDocumento52 páginasEspectrofotometría de Absorción AtómicaCarolina GarcíaAún no hay calificaciones
- Adsorción AtómicaDocumento12 páginasAdsorción AtómicaAngel RomeroAún no hay calificaciones
- Flamometria Absorciony Ion SelectivoDocumento7 páginasFlamometria Absorciony Ion SelectivoAdelheint Bernstein75% (4)
- Conferencia de Emisión AtómicaDocumento25 páginasConferencia de Emisión AtómicaLuis David Cedeño IntriagoAún no hay calificaciones
- TP #2 Tecnicas Analiticas Instrumentales. Profesor Ricardo PereyraDocumento94 páginasTP #2 Tecnicas Analiticas Instrumentales. Profesor Ricardo PereyraLeo AgüeroAún no hay calificaciones
- Absorcion AtomicaDocumento63 páginasAbsorcion AtomicaKathyBonitaPAAún no hay calificaciones
- Cromatografía de Gases Química Analítica III - Semestre 2017-2Documento46 páginasCromatografía de Gases Química Analítica III - Semestre 2017-2Emiliano CastroAún no hay calificaciones
- Presentación Espectroscopía AtómicaDocumento53 páginasPresentación Espectroscopía AtómicaAna Florencia NadalAún no hay calificaciones
- Práctica 6Documento11 páginasPráctica 6Arthurrd AquinoAún no hay calificaciones
- Interferencia de Ionizacion (Final)Documento17 páginasInterferencia de Ionizacion (Final)Lili RosalesAún no hay calificaciones
- Trabajo QuimicaDocumento25 páginasTrabajo QuimicaAngie Lizeth Pancho PoloAún no hay calificaciones
- PDF Practica 6 DLDocumento11 páginasPDF Practica 6 DLJuanAún no hay calificaciones
- Clase 8. Espectroscopia de Absorción AtómicaDocumento33 páginasClase 8. Espectroscopia de Absorción AtómicaLUIS DAVID ZAVALETA GUTIERREZAún no hay calificaciones
- Métodos Espectroquímicos - Parte IIDocumento50 páginasMétodos Espectroquímicos - Parte IIYaniHuayguaAún no hay calificaciones
- Cuestionario 4Documento7 páginasCuestionario 4Brayan GahetaAún no hay calificaciones
- Espectroscopia Atómica, de Emisión y AbsorciónDocumento41 páginasEspectroscopia Atómica, de Emisión y AbsorciónAlejandro De la RosaAún no hay calificaciones
- Informe #2 Longuitud de OndaDocumento11 páginasInforme #2 Longuitud de OndaStacy Ruddy Flores MacedoAún no hay calificaciones
- 01-Estructura de Presentación Del Informe Laboratorio - Proyecto de InvestigaciónDocumento1 página01-Estructura de Presentación Del Informe Laboratorio - Proyecto de InvestigaciónStacy Ruddy Flores MacedoAún no hay calificaciones
- Informe 1 - Normas de Seguridad y Primeros Auxilios en El LaboratorioDocumento19 páginasInforme 1 - Normas de Seguridad y Primeros Auxilios en El LaboratorioStacy Ruddy Flores MacedoAún no hay calificaciones
- Informe N°4 - 91 G - Q.A INSTRUMENTALDocumento14 páginasInforme N°4 - 91 G - Q.A INSTRUMENTALStacy Ruddy Flores MacedoAún no hay calificaciones
- Sesión 3. Infrarrojo 2021BDocumento44 páginasSesión 3. Infrarrojo 2021BStacy Ruddy Flores MacedoAún no hay calificaciones
- Sesión 01. EspectrofotometríaDocumento50 páginasSesión 01. EspectrofotometríaGabriela Acosta DeledesmaAún no hay calificaciones
- Sesión 02. Metodos Espectoscopicos de Análisis 2021BDocumento28 páginasSesión 02. Metodos Espectoscopicos de Análisis 2021BStacy Ruddy Flores MacedoAún no hay calificaciones
- Sesión 05. Absorción Atómica Sin Llama y PlasmaDocumento22 páginasSesión 05. Absorción Atómica Sin Llama y PlasmaStacy Ruddy Flores MacedoAún no hay calificaciones
- Catalizadores No BiologicosDocumento9 páginasCatalizadores No BiologicosYuritziAún no hay calificaciones
- Clase 2Documento9 páginasClase 2Maximiliano PieroniAún no hay calificaciones
- Análisis de Precios Unitarios: PartidaDocumento40 páginasAnálisis de Precios Unitarios: PartidaP. Apaza EdwinAún no hay calificaciones
- CarbonoDocumento7 páginasCarbonoYhon Teylor CasafrancaAún no hay calificaciones
- Seleccion Refrigerante PowerPointDocumento38 páginasSeleccion Refrigerante PowerPointMelissa Tufiño Ochoa100% (1)
- 04 Diseño de Conexiones SoldadasDocumento45 páginas04 Diseño de Conexiones SoldadasEnrique AlonsoAún no hay calificaciones
- Guia Practica Determinacion Del Contenido de HumedadDocumento5 páginasGuia Practica Determinacion Del Contenido de HumedadJallesa Turizo CentenoAún no hay calificaciones
- Practica de Solubilidad de Las Aminas.Documento17 páginasPractica de Solubilidad de Las Aminas.Alejandra Palacios100% (1)
- Avance Labo de Ensayo de Carga PuntualDocumento8 páginasAvance Labo de Ensayo de Carga PuntualChristian Aliaga MejíaAún no hay calificaciones
- Tipos EmpujeDocumento9 páginasTipos EmpujeGonza ReyesAún no hay calificaciones
- Instructivo para El Lavado de Limpieza y Desinfeccion Del Tanque de AlmacenamientoDocumento5 páginasInstructivo para El Lavado de Limpieza y Desinfeccion Del Tanque de Almacenamientosaludambitolaboral ancuyaAún no hay calificaciones
- CongelacionDocumento7 páginasCongelacionRobby BenitesAún no hay calificaciones
- Colores Identificacion Tuberias NTE 44 1984 PDFDocumento9 páginasColores Identificacion Tuberias NTE 44 1984 PDFJoseluiarmijossAún no hay calificaciones
- Calculo de Muros para BodegaDocumento5 páginasCalculo de Muros para BodegaAndres LosadaAún no hay calificaciones
- Tipos de Suelos de GuatemalaDocumento2 páginasTipos de Suelos de GuatemalaJavier SolisAún no hay calificaciones
- Apuntes Sobre Oxidacion y ReducciÓnDocumento6 páginasApuntes Sobre Oxidacion y ReducciÓnaestay100% (3)
- Especificaciones Tecnicas IissDocumento18 páginasEspecificaciones Tecnicas Iissgigi180683Aún no hay calificaciones
- Examen Final - Semana 8 - Inv - Primer Bloque-Procesos Industriales - (Grupo1)Documento10 páginasExamen Final - Semana 8 - Inv - Primer Bloque-Procesos Industriales - (Grupo1)Nilson Ariza0% (1)
- Metodologia Adobe AntecedentesDocumento16 páginasMetodologia Adobe AntecedentesVictor Sulca Puca100% (1)
- Bloque IiDocumento7 páginasBloque IiFallo Re DoAún no hay calificaciones
- La Leche y Sus Puntos de Generación de ResiudosDocumento10 páginasLa Leche y Sus Puntos de Generación de ResiudosAlyssa EurestyAún no hay calificaciones
- Norma Covenin 1753-2003Documento10 páginasNorma Covenin 1753-2003Raúl RiveraAún no hay calificaciones
- Cap 01 Introducción PDFDocumento13 páginasCap 01 Introducción PDFjorgeAún no hay calificaciones
- Usos de Los AnhídridosDocumento3 páginasUsos de Los AnhídridosShannon Thompson56% (32)
- Cordillera Ficha Tecnica 33x33 Granito Gris CGRANIT13CIDocumento2 páginasCordillera Ficha Tecnica 33x33 Granito Gris CGRANIT13CIJuan MoyaAún no hay calificaciones
- Antapite PDFDocumento123 páginasAntapite PDFNelson Torres FloresAún no hay calificaciones
- Reporte 1Documento17 páginasReporte 1AmilcarAún no hay calificaciones
- Pavi MentosDocumento9 páginasPavi MentosBrayan SanchezAún no hay calificaciones
- 10aislador Post Line69Documento3 páginas10aislador Post Line69jcmagraAún no hay calificaciones
- Antique Bra DurasDocumento2 páginasAntique Bra DurasCarlos Condori AvilaAún no hay calificaciones
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (201)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Zensorialmente : Dejá que tu cuerpo sea tu cerebroDe EverandZensorialmente : Dejá que tu cuerpo sea tu cerebroAún no hay calificaciones
- Homo antecessor: El nacimiento de una especieDe EverandHomo antecessor: El nacimiento de una especieCalificación: 5 de 5 estrellas5/5 (1)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDe EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreCalificación: 5 de 5 estrellas5/5 (3)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones
- Las Cinco Leyes Biológicas De La Naturaleza: La Nueva Medicina (Color Edition) SpanishDe EverandLas Cinco Leyes Biológicas De La Naturaleza: La Nueva Medicina (Color Edition) SpanishCalificación: 4.5 de 5 estrellas4.5/5 (3)
- Anatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasDe EverandAnatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasCalificación: 4.5 de 5 estrellas4.5/5 (21)
- Manual técnico para la interpretación de análisis de suelos y fertilización de cultivosDe EverandManual técnico para la interpretación de análisis de suelos y fertilización de cultivosCalificación: 4 de 5 estrellas4/5 (1)
- El concepto Mulligan de terapia manual (Color)De EverandEl concepto Mulligan de terapia manual (Color)Calificación: 5 de 5 estrellas5/5 (3)
- La causa raiz de los accidentes: Historias de accidentes en la industriaDe EverandLa causa raiz de los accidentes: Historias de accidentes en la industriaCalificación: 5 de 5 estrellas5/5 (1)
- La invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleDe EverandLa invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleCalificación: 4.5 de 5 estrellas4.5/5 (15)
- Proyectos Arduino con Tinkercad: Diseño y programación de proyectos electrónicos basados en Arduino con TinkercadDe EverandProyectos Arduino con Tinkercad: Diseño y programación de proyectos electrónicos basados en Arduino con TinkercadCalificación: 5 de 5 estrellas5/5 (1)
- 50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaDe Everand50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaCalificación: 4 de 5 estrellas4/5 (37)
- El péndulo de sanación: Péndulo hebreo. Investigación y sistematización de la técnicaDe EverandEl péndulo de sanación: Péndulo hebreo. Investigación y sistematización de la técnicaCalificación: 4.5 de 5 estrellas4.5/5 (27)
- Guía de cálculo y diseño de conductos para ventilación y climatizaciónDe EverandGuía de cálculo y diseño de conductos para ventilación y climatizaciónCalificación: 5 de 5 estrellas5/5 (1)
- Cardiología y enfermedades cardiovascularesDe EverandCardiología y enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- Neuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaDe EverandNeuroanatomía: Fundamentos de neuroanatomía estructural, funcional y clínicaCalificación: 4 de 5 estrellas4/5 (16)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)De EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Calificación: 5 de 5 estrellas5/5 (9)