Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Consideraciones Importantes en El Equilibrio Líquido
Cargado por
Janexi Yamileth0 calificaciones0% encontró este documento útil (0 votos)
19 vistas2 páginasTítulo original
Consideraciones importantes en el equilibrio líquido
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
19 vistas2 páginasConsideraciones Importantes en El Equilibrio Líquido
Cargado por
Janexi YamilethCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
Consideraciones importantes en el equilibrio líquido-vapor:
-La fase vapor se considera como una mezcla de gases ideales.
-La fase líquida es considerada como una solución ideal.
El estado de equilibrio se da cuando se llega a la presión de vapor (presión
ejercida cuando la fase de vapor está en equilibrio con la fase líquida). Esta,
además de depender de la temperatura, dependerá de la naturaleza de los
componentes y la composición de cada fase.
En una solución ideal, la presión de vapor será proporcional a la fracción molar de
cada uno componente en la fase líquida y a la presión de vapor del componente
puro a una temperatura dada, de acuerdo con Raoult.
Punto de burbuja
Se refiere a la temperatura y presión a las que en una mezcla líquida se ha
formado la primera partícula de vapor, es decir, empieza a hervir. Además, el
punto del cambio de fase en el que existe la mayor presión.
Punto de rocío
Se conoce como punto de rocío a la temperatura y presión a la cual la mezcla de
vapor empezará a condensar. Además, es el punto de menor presión durante el
cambio de fase.
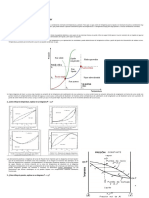
Diagramas de equilibrio líquido vapor a Presión y Temperatura constante
En una mezcla binaria de equilibrio líquido-vapor se pueden determinar las
composiciones molares tanto de la fase gaseosa como de la fase líquida en
función de la presión o de la temperatura, cuando se grafican estos datos
obtenidos experimentalmente, se obtienen diagramas de fases como los
mostrados en la figura 1.
Coeficiente de fugacidad: En condiciones ideales, la fugacidad del componente i en la fase vapor es
igual a su presión parcial, pi. Sin embargo, en el presente trabajo no se ha considerado la idealidad
de la fase vapor, por lo que se hace necesario introducir una variable que represente la desviación
respecto a la idealidad de la fugacidad de la fase vapor. Así pues, se define el coeficiente de
fugacidad, ̂i , como la relación entre la fugacidad de un componente y su presión parcial. Para un
componente i en fase vapor, se expresa como:
También podría gustarte
- Ley de Dalton y HenryDocumento62 páginasLey de Dalton y HenryLaura ReyesAún no hay calificaciones
- Equilibrio Liquido Vapor - InformeDocumento36 páginasEquilibrio Liquido Vapor - InformeCristhianPalaciosAún no hay calificaciones
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDe EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesAún no hay calificaciones
- EVL Benceno-ToluenoDocumento10 páginasEVL Benceno-ToluenoMiguel Jiménez FloresAún no hay calificaciones
- Equilibrio Gas LiquidoDocumento5 páginasEquilibrio Gas LiquidoRenzo Acevedo Cano100% (1)
- Punto de Rocio y BurbujaDocumento23 páginasPunto de Rocio y Burbujamanutws71% (7)
- Propiedades Termodinámicas de Las Sustancias PurasDocumento5 páginasPropiedades Termodinámicas de Las Sustancias PurasHugo Sanchez HuertaAún no hay calificaciones
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- Equilibrio Liquido-VaporDocumento10 páginasEquilibrio Liquido-VaporMiguelAún no hay calificaciones
- Ley de Raoult ModificadaDocumento8 páginasLey de Raoult ModificadaMilagrosCabanillasInfantesAún no hay calificaciones
- Equilibrio Vapor LiquidoDocumento13 páginasEquilibrio Vapor LiquidoERCI100% (1)
- IntroducciónDocumento4 páginasIntroducciónDavid Ramirez GutierrezAún no hay calificaciones
- Fisico QuimicaDocumento17 páginasFisico QuimicaGianfranco Yucra RojasAún no hay calificaciones
- Operacion UnitariaDocumento5 páginasOperacion UnitarialioAún no hay calificaciones
- Tarea 2.2 EquilibrioDocumento8 páginasTarea 2.2 Equilibriopaola poma gutierrez0% (1)
- Destilacion Ing 3Documento14 páginasDestilacion Ing 3winnyAún no hay calificaciones
- Diferencia Entre Gas y VaporDocumento8 páginasDiferencia Entre Gas y VaporJosé TorrezAún no hay calificaciones
- Exposicion Transferencia de Materia Unidad 6 y 7Documento5 páginasExposicion Transferencia de Materia Unidad 6 y 7Orestes GonzalezAún no hay calificaciones
- Tarea 2.2Documento2 páginasTarea 2.2Giovanny NuñezAún no hay calificaciones
- UNIDAD 2 Operacion UnitariasDocumento6 páginasUNIDAD 2 Operacion UnitariasCHUPA CABRAAún no hay calificaciones
- Practica 4Documento9 páginasPractica 4IsraelAngelesAún no hay calificaciones
- Equilibrio Liquido VaporDocumento6 páginasEquilibrio Liquido VaporAlexChacónAún no hay calificaciones
- Presentacion DestilacionDocumento108 páginasPresentacion DestilacionFrancisco SanchezAún no hay calificaciones
- Marco Teorico TxyDocumento4 páginasMarco Teorico TxyCraven HorrorsAún no hay calificaciones
- Aqui Editar111Documento14 páginasAqui Editar111SHsaavedraAún no hay calificaciones
- FugacidadDocumento3 páginasFugacidadRichard FloresAún no hay calificaciones
- Conceptos 2-TermodinamicaDocumento10 páginasConceptos 2-TermodinamicaDavid alonso SilvaAún no hay calificaciones
- 1.4 Sustancias PurasDocumento15 páginas1.4 Sustancias Purasjose luisAún no hay calificaciones
- Tema 6 OU3Documento16 páginasTema 6 OU3Sebastián Varga SchwindtAún no hay calificaciones
- Ley de RaoultDocumento6 páginasLey de RaoultGiuseppe Luigi Nuñez AguilarAún no hay calificaciones
- Modulo 02 - Propiedades Fase LíquidaDocumento10 páginasModulo 02 - Propiedades Fase LíquidaAnthony FariasAún no hay calificaciones
- Sesion 14mezcla Gas-VaporDocumento18 páginasSesion 14mezcla Gas-VaporJACINTO WILLCAMASCCOAún no hay calificaciones
- Calculo de Fugacidad en Sistemas No IdealesDocumento13 páginasCalculo de Fugacidad en Sistemas No IdealesLucio David Ramírez GarcíaAún no hay calificaciones
- Benceno Vs ToluenoDocumento11 páginasBenceno Vs ToluenoNicole Orellana PintoAún no hay calificaciones
- Informe de Gas Natural 2Documento20 páginasInforme de Gas Natural 2Salustria Cabezas SánchezAún no hay calificaciones
- Marco Teórico 4Documento2 páginasMarco Teórico 4Mariana PerezAún no hay calificaciones
- Unidad 5Documento7 páginasUnidad 5Arturo SerranoAún no hay calificaciones
- Práctica No. 4 Equilibrio Líquido-VaporDocumento15 páginasPráctica No. 4 Equilibrio Líquido-VaporAlex MartezeeAún no hay calificaciones
- Trabajo de Humidificación InvestigaciónDocumento8 páginasTrabajo de Humidificación InvestigaciónElia Castro LopezAún no hay calificaciones
- Informe 2-Mezcla MulticomponentesDocumento19 páginasInforme 2-Mezcla MulticomponentesSalustria Cabezas SánchezAún no hay calificaciones
- Propiedades de Las Sustancias PurasDocumento25 páginasPropiedades de Las Sustancias PurasrubenAún no hay calificaciones
- Informe T BurbujaDocumento14 páginasInforme T BurbujaRicardo Felipe Cortes CruzAún no hay calificaciones
- Termo III (Práctica 4)Documento37 páginasTermo III (Práctica 4)Jesus Vazquez60% (5)
- 2.3 ExposicionDocumento11 páginas2.3 ExposicionbethsyAún no hay calificaciones
- Tarea 3 Resumen de La Unidad 2Documento8 páginasTarea 3 Resumen de La Unidad 2fabian vazquez santanaAún no hay calificaciones
- Diagrama TDocumento8 páginasDiagrama TLissette CastilloAún no hay calificaciones
- Ud.1.4-Tsf - Equilibrio de Fases PDFDocumento8 páginasUd.1.4-Tsf - Equilibrio de Fases PDFAdrian Rodriguez DiazAún no hay calificaciones
- Equilibrio L VDocumento8 páginasEquilibrio L Vcarlina hernandezAún no hay calificaciones
- Captulo 4 Procesos de Humidificacin y SecadoDocumento46 páginasCaptulo 4 Procesos de Humidificacin y Secadoijil87Aún no hay calificaciones
- Equilbrio de FasesDocumento4 páginasEquilbrio de FasesRosalba González MéndezAún no hay calificaciones
- TermodinámicaDocumento11 páginasTermodinámicaAdriana CalderínAún no hay calificaciones
- IntroducciónDocumento20 páginasIntroducciónAevorg IrodnocAún no hay calificaciones
- Curvas de EquilibrioDocumento3 páginasCurvas de EquilibrioLizz SaavedraAún no hay calificaciones
- Punto de BurbujaDocumento4 páginasPunto de BurbujaguanakhoAún no hay calificaciones
- Presión de VaporDocumento4 páginasPresión de Vapormariana.ramirezmendozaAún no hay calificaciones
- Proceso de DestilacionDocumento58 páginasProceso de DestilacionfzulleAún no hay calificaciones
- Sustancia PurasDocumento14 páginasSustancia PurasRossy CarAún no hay calificaciones
- Equilibrio Liquido VaporDocumento8 páginasEquilibrio Liquido VaporARNOLD BRAVO RAMIREZAún no hay calificaciones
- TEMA 5 Termo 2017-2018Documento8 páginasTEMA 5 Termo 2017-2018Maria BallesterosAún no hay calificaciones