Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Diagrama T
Cargado por
Lissette Castillo0 calificaciones0% encontró este documento útil (0 votos)
382 vistas8 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
382 vistas8 páginasDiagrama T
Cargado por
Lissette CastilloCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 8
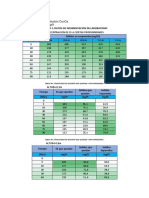
Diagrama T-v
El diagrama T-v se obtiene de la proyeccin de la superficie PvT
(Figura 1.28) en el plano T-v. La proyeccin resultante sobre un plano
paralelo a los ejes T-v se muestra en la Figura 1.29. En este diagrama
tanto las regiones de una y dos fases aparecen como reas.
Fig. 1.28 Superficie P-v-T de una sustancia que se expande al
congelarse (como el agua).
Es comn que dos fases estn en equilibrio, pero en algunas
condiciones las tres fases de una sustancia pura coexisten en
equilibrio. En los diagramas P-v o P-T, estos estados de fase triple
forman la lnea triple. Los estados de una sustancia sobre la lnea
triple tienen la misma presin y temperatura, pero diferentes
volmenes especficos. La lnea triple aparece como un punto sobre
los diagramas P-T y, por tanto, suele denominarse punto triple.
Fig. 1.29 Figura T-v de una sustancia pura.
Los estados de lquido saturado en la Figura 1.29 pueden
conectarse mediante una lnea, lnea de lquido saturado, y los
estados de vapor saturado en la misma figura pueden conectarse
mediante la lnea de vapor saturado. Estas dos lneas se alcanzan en
el punto crtico, formado un domo como muestra la Figura 1.29. El
punto crtico se define como el punto al cual los estados de lquido
saturado y de vapor saturado son idnticos. La temperatura, la
presin y el volumen especfico de una sustancia en el punto crtico se
denominan, temperatura crtica Tcr , presin crtica Pcr y volumen
especfico crtico vcr. Las propiedades del punto crtico del agua son
Pcr=22.09 Mpa, Tcr=374.14 C y vcr=0.003155 m3/kg.
Debemos familiarizarnos muy bien con estos dos diagramas; pues
sern muy tiles cuando se analicen problemas de esta naturaleza.
FIGURA 2.4 Diagramas p-v, T-v y p-T.
El inters prctico principal est en situaciones que comprenden las
regiones lquido, liquido vapor y vapor. Un vapor saturado se
encuentra sobre la lnea de vapor saturado y un lquido saturado sobre
la lnea de lquido saturado. La regin a la derecha de la lnea de
vapor saturado es la regin sobrecalentada; la regin a la izquierda de
la lnea de liquido saturado es la regin de liquido comprimido
(tambin llamada regin de liquido subenfriada). Se
Encuentra un estado supercrtico cuando la presin y temperatura son
mayores a los valores crticos.
REGION LIQUIDO-VAPOR
En cualquier estado (T, v) entre los puntos saturados f y g, mostrados
en la figura 2.5, liquido y vapor existen como una mezcla en equilibrio.
Representemos por vf y vg, respectivamente, los volmenes
especficos de liquido saturado y vapor saturado. Sea m la masa total
de un sistema (como el que se muestra en la figura 2.1c), mf cantidad
de masa en la fase liquida y mg la cantidad de masa en la fase de
vapor. Entonces, para un estado del sistema representado por
cualquier (T, v), por ejemplo el estado 1, el volumen total de la mezcla
es la suma del volumen ocupado por el lquido y el ocupado por el
vapor, o sea:
FIGURA 2.5 Diagrama T-v que muestra los puntos de liquido saturado
y vapor saturado
La razn entre la masa de vapor saturado y la masa total se denomina
calidad de la mezcla, designada por el smbolo x; es:
Con frecuencia nos referimos a la regin bajo las lneas de saturacin
como la regin de calidad, la regin de mezcla, o la regin hmeda; es
la nica regin donde la calidad x tiene significado. Si reconocemos
que mf = m - mg, podemos escribir la ecuacin 2.1, con el uso de
nuestra definicin de calidad, como:
Como la diferencia en valores de vapor saturado y lquido saturado
aparece con frecuencia en clculos, regularmente denotamos esta
diferencia con el subndice "fg"; esto es:
Por lo tanto, la ecuacin 2.3 es:
Las palabras gas y vapor a menudo se utilizan como sinnimos y
comnmente a la fase de vapor de una sustancia se le llama gas
cuando su temperatura es ms alta que la temperatura critica. El vapor
normalmente implica un gas que no se encuentra muy alejado del
estado de condensacin.
DEFINICIONES
Punto crtico
El lmite superior de la lnea de presin de vapor es el punto
crtico indicado por el punto C indicado en la figura 1.
Para un sistema formado por un solo componente, el punto
crtico implica el estado crtico de un componente puro y
representa el estado lmite (mximos valores de presin y
temperatura) para la coexistencia de dos fases (por ejemplo,
lquido y gas).
PROPIEDADES DE LAS SUSTANCIAS PURAS
LIQUIDO COMPRIMIDO O LIQUIDO SUBENFRIADO
En una sustancia pura significa que est en estado lquido y
que no est a punto de evaporarse sino que le falta una
adicin de calor o un cambio negativo en la presin para
hacerlo. Si hablamos de lquido subenfriado entendemos que
la sustancia est como lquida a una temperatura menor que
la temperatura de saturacin ( T < Tsat) para una presin
determinada. Si hablamos de lquido comprimido entendemos
que la sustancia est como lquida a una presin mayor que
la presin de saturacin (P > Psat) a una temperatura
determinada.
LIQUIDO SATURADO
Es aquel que est a punto de evaporarse. Es importante notar
que cuando una sustancia pura est como lquido saturado
sta se halla totalmente en ese estado, como lquido, nada de
vapor ya que est a punto de comenzar a crearse a partir del
agua lquida saturada.
VAPOR SATURADO O VAPOR SATURADO SECO
Es un vapor que est a punto de condensarse. En esta fase
la sustancia est toda como vapor y es necesario retirar calor
o aumentar la presin para provocar que se generen gotas de
lquido.
VAPOR SOBRECALENTADO
Es vapor que est a una temperatura ms alta que la
temperatura de vapor saturado, por lo cual la sustancia sigue
estando toda como vapor pero ya no estar a punto de
condensarse o de formar pequeas gotas de lquido. Si
hablamos de vapor sobrecalentado entendemos que la
sustancia est como toda vapor a una temperatura mayor que
la temperatura de saturacin ( T > Tsat) para una presin
determinada.
TEMPERATURA DE SATURACIN Y PRESIN DE
SATURACIN
La forma ms simple de entender estos conceptos es por
medio de un ejemplo: Siempre hemos sabido que el agua
ebulle, o se comienza a evaporar, a 100C, pero lo hace a
esa temperatura porque la presin a la que se encuentra es la
presin atmosfrica que es 1 atmsfera. Conclusin: la
temperatura a la cual una sustancia pura comienza a cambiar
de fase, bien sea comenzando a transformarse de agua a
vapor (lquido saturado) o de vapor a lquido (vapor saturado),
se llama temperatura de saturacin, y esta temperatura de
saturacin siempre va a tener ligada una presin que se
llamar presin de saturacin. Ahora, volviendo al ejemplo, si
preguntan en una clase cual es la temperatura de saturacin
para el agua a una presin de 1 atm = 101.325 kPa, la
respuesta correcta sera 100C. Y si preguntan sobre la
presin de saturacin para una temperatura de 100C la
respuesta correcta sera 1 atmsfera. En pocas palabras,
presin de saturacin es la temperatura de ebullicin para
una presin determinada y la presin de saturacin es la
presin de ebullicin para una temperatura determinada.
PUNTO CRTICO
Lquido + Vapor en equilibrio con sus valores de presin y
temperatura mximos. Se da en la punta superior de la
campana de lquido + vapor en un diagrama T-v (Temperara
vs. Volumen especfico).
VAPOR SATURADO + LIQUIDO SATURADO
Es un estado en donde dentro de un sistema tenemos lquido
al mismo tiempo que tenemos vapor. Un ejemplo de esto es
la preparacin de una sopa en una olla a presin en donde al
cabo de algunos minutos habr agua y vapor dentro de ella a
cierta presin nica para ambas fases de la sustancia.
Cuando hablamos de lquido ms vapor se sobreentiende que
existe la CALIDAD. La calidad es la cantidad de masa de
vapor con respecto a la cantidad de masa total de la
sustancia. Es decir, si est como toda vapor, calidad = 1, si
est como todo lquido, calidad = 0, porque no hay nada de
masa en fase vapor debido a que toda la masa est como
lquido.
También podría gustarte
- Tema 3 Propiedades de Una Sustancia PuraDocumento29 páginasTema 3 Propiedades de Una Sustancia Puradiana gAún no hay calificaciones
- Diagramas de FaseDocumento19 páginasDiagramas de FaseKleyjarh CorreaAún no hay calificaciones
- Guía de Estudio - Parte 3Documento33 páginasGuía de Estudio - Parte 3Juan Jay CasalAún no hay calificaciones
- Curso Termodinamica de Las Sustancia PurasDocumento32 páginasCurso Termodinamica de Las Sustancia PurasMonica Cornejo GonzalezAún no hay calificaciones
- Cap 3 Propiedades Sustancias PurasDocumento15 páginasCap 3 Propiedades Sustancias PurasjorgeAún no hay calificaciones
- Presentación 5 Final TermoDocumento25 páginasPresentación 5 Final Termoperezlobito2.0Aún no hay calificaciones
- Sustancia PurasDocumento14 páginasSustancia PurasRossy CarAún no hay calificaciones
- 2-Sustancia-Pura-Resumen 2Documento44 páginas2-Sustancia-Pura-Resumen 2Michelle LunaAún no hay calificaciones
- Campana de Saturación - Sistemas Termicos 1Documento6 páginasCampana de Saturación - Sistemas Termicos 1Khristian Vinicio0% (1)
- Guia 3 Sustancia Pura 2018Documento10 páginasGuia 3 Sustancia Pura 2018Ivanny NaranjoAún no hay calificaciones
- Sustancias PurasDocumento7 páginasSustancias PurasCarlosCarrilloAún no hay calificaciones
- Nota TécnicaDocumento33 páginasNota TécnicaAlejandro De AvilaAún no hay calificaciones
- IntroducciónDocumento20 páginasIntroducciónAevorg IrodnocAún no hay calificaciones
- 3 Propiedades de Las Sustancias Puras y Ecuaciones de EstadoDocumento20 páginas3 Propiedades de Las Sustancias Puras y Ecuaciones de EstadoAldo CisnerosAún no hay calificaciones
- Ensayo de Termodinámica 112-135Documento5 páginasEnsayo de Termodinámica 112-135damianAún no hay calificaciones
- Unidad 2 TermodinamicaDocumento10 páginasUnidad 2 TermodinamicaFilix QMAún no hay calificaciones
- Semana 3Documento26 páginasSemana 3DiinoGarcía100% (1)
- Resumen Capitulo 3 Cengel 8 EdicionDocumento13 páginasResumen Capitulo 3 Cengel 8 EdicionpepepepeAún no hay calificaciones
- Mediacion Pedagogica Unidad No9 2020termodinamicaDocumento16 páginasMediacion Pedagogica Unidad No9 2020termodinamicaLuciano RosalesAún no hay calificaciones
- Propiedades de Las Sustancias PurasDocumento15 páginasPropiedades de Las Sustancias PurasOmar SarmientoAún no hay calificaciones
- 1.4. Sustancias PurasDocumento55 páginas1.4. Sustancias PurasMr. vAún no hay calificaciones
- Fisico QuimicaDocumento17 páginasFisico QuimicaGianfranco Yucra RojasAún no hay calificaciones
- Propiedades de Las Sustancias PurasDocumento25 páginasPropiedades de Las Sustancias PurasrubenAún no hay calificaciones
- Material de Estudio - IIM504Documento237 páginasMaterial de Estudio - IIM504pedroAún no hay calificaciones
- Sustancias PurasDocumento10 páginasSustancias PurasSebastian Andre DuqueAún no hay calificaciones
- 1.4 Sustancias PurasDocumento15 páginas1.4 Sustancias Purasjose luisAún no hay calificaciones
- Propiedades Termodinámicas de Las Sustancias PurasDocumento5 páginasPropiedades Termodinámicas de Las Sustancias PurasHugo Sanchez HuertaAún no hay calificaciones
- Capitulo #3 Parte B Diagramas TermodinamicosDocumento6 páginasCapitulo #3 Parte B Diagramas TermodinamicosRodrigoAún no hay calificaciones
- Conceptos 2-TermodinamicaDocumento10 páginasConceptos 2-TermodinamicaDavid alonso SilvaAún no hay calificaciones
- Entalpia de Sustancias PurasDocumento38 páginasEntalpia de Sustancias PurasWilber X Siempre50% (2)
- Equilibrio Vapor LiquidoDocumento13 páginasEquilibrio Vapor LiquidoERCI100% (1)
- Clase 03 Sustancias Puras. Tablas TermodinamicasDocumento62 páginasClase 03 Sustancias Puras. Tablas TermodinamicasGilberto Salas ColottaAún no hay calificaciones
- Sesion 14mezcla Gas-VaporDocumento18 páginasSesion 14mezcla Gas-VaporJACINTO WILLCAMASCCOAún no hay calificaciones
- Un III - Sustancias PurasDocumento31 páginasUn III - Sustancias PurasRaul Gerardo PerezAún no hay calificaciones
- Sustancias PurasDocumento6 páginasSustancias PurasJesús MartínezAún no hay calificaciones
- Puto El Que Lo AbraDocumento15 páginasPuto El Que Lo AbraRaúl Núñez GonzálezAún no hay calificaciones
- Capítulo 2 - La Sustancia Pura - Termodinamica-2018-IDocumento36 páginasCapítulo 2 - La Sustancia Pura - Termodinamica-2018-IdanielAún no hay calificaciones
- LabFIQUI-I-"PRESIÓN DE VAPOR DE LÍQUIDOS PUROS"BDocumento9 páginasLabFIQUI-I-"PRESIÓN DE VAPOR DE LÍQUIDOS PUROS"Bcefiqt100% (2)
- TermodinámicaDocumento11 páginasTermodinámicaAdriana CalderínAún no hay calificaciones
- Propiedades de Sustancia Pura - Teoría PDFDocumento17 páginasPropiedades de Sustancia Pura - Teoría PDFxiomi2017100% (1)
- 1.3 Prop Termod de Sustancias PurasDocumento23 páginas1.3 Prop Termod de Sustancias PurasJaime G V Riquez100% (1)
- Unidad I - Sustancias PurasDocumento38 páginasUnidad I - Sustancias PurasJeremy CastilloAún no hay calificaciones
- Fundameto Teorico Presion de VaporDocumento5 páginasFundameto Teorico Presion de VaporSmithAnthonyBlasMAún no hay calificaciones
- 04 Presion de VaporDocumento14 páginas04 Presion de VaporMauricio Montaño SaavedraAún no hay calificaciones
- Disoluciones Clausius ClapeyronDocumento30 páginasDisoluciones Clausius ClapeyronArdila Alber80% (5)
- TEMA 5 Termo 2017-2018Documento8 páginasTEMA 5 Termo 2017-2018Maria BallesterosAún no hay calificaciones
- Modulo 02 - Propiedades Fase LíquidaDocumento10 páginasModulo 02 - Propiedades Fase LíquidaAnthony FariasAún no hay calificaciones
- Secado 3Documento19 páginasSecado 3Flor CerquinAún no hay calificaciones
- Propiedades de Sustancias PurasDocumento34 páginasPropiedades de Sustancias Purassigrid quesadaAún no hay calificaciones
- Tarea 3 Resumen de La Unidad 2Documento8 páginasTarea 3 Resumen de La Unidad 2fabian vazquez santanaAún no hay calificaciones
- Comport A Mien To PVT de Sustancias PurasDocumento8 páginasComport A Mien To PVT de Sustancias Puraspaisa solo paisa100% (2)
- Unidad 2Documento14 páginasUnidad 2Olivia LopezAún no hay calificaciones
- Capítulo Ii Comportamiento P-V-T de Las Sustancias PurasDocumento11 páginasCapítulo Ii Comportamiento P-V-T de Las Sustancias Purasnikolle12Aún no hay calificaciones
- Clase 02. Sustancias Puras. Tablas TermodinamicasDocumento62 páginasClase 02. Sustancias Puras. Tablas TermodinamicasGilberto Salas ColottaAún no hay calificaciones
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDe EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesAún no hay calificaciones
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Jabón de Glicerina AromáticoDocumento16 páginasJabón de Glicerina AromáticoLissette CastilloAún no hay calificaciones
- Valores Del PolicíaDocumento8 páginasValores Del PolicíaLissette CastilloAún no hay calificaciones
- EMPAREJAMIENTODocumento11 páginasEMPAREJAMIENTOLissette CastilloAún no hay calificaciones
- EMPAREJAMIENTODocumento11 páginasEMPAREJAMIENTOLissette CastilloAún no hay calificaciones
- Diseno Instruccional Sgos d2Documento8 páginasDiseno Instruccional Sgos d2Lissette CastilloAún no hay calificaciones
- Caracterosticas OrganolepticasDocumento11 páginasCaracterosticas OrganolepticasLissette CastilloAún no hay calificaciones
- EMPAREJAMIENTODocumento11 páginasEMPAREJAMIENTOLissette CastilloAún no hay calificaciones
- Diseno Instruccional Sgos d2Documento8 páginasDiseno Instruccional Sgos d2Lissette CastilloAún no hay calificaciones
- Sediment Ac I OnDocumento4 páginasSediment Ac I OnLissette CastilloAún no hay calificaciones
- Benditas GraficasDocumento15 páginasBenditas GraficasLissette CastilloAún no hay calificaciones
- Lab VertederosDocumento16 páginasLab VertederosLissette CastilloAún no hay calificaciones
- Informe InteraguaDocumento11 páginasInforme InteraguaLissette Castillo0% (1)
- CálculoDocumento14 páginasCálculoLissette CastilloAún no hay calificaciones
- Invest 1 402Documento12 páginasInvest 1 402Lissette CastilloAún no hay calificaciones
- Pretamiento de Aguas ResidualesDocumento14 páginasPretamiento de Aguas ResidualesLissette CastilloAún no hay calificaciones
- Lab VertederosDocumento16 páginasLab VertederosLissette CastilloAún no hay calificaciones
- Pretamiento de Aguas ResidualesDocumento13 páginasPretamiento de Aguas ResidualesLissette CastilloAún no hay calificaciones
- Cálculo&Fracciones Parciales PDFDocumento18 páginasCálculo&Fracciones Parciales PDFLissette CastilloAún no hay calificaciones
- Expo 403Documento68 páginasExpo 403Lissette CastilloAún no hay calificaciones
- ProyectoDocumento1 páginaProyectoLissette CastilloAún no hay calificaciones
- Deber1 403Documento5 páginasDeber1 403Lissette CastilloAún no hay calificaciones
- La Ciencia Que Se Ocupa de RecogerDocumento6 páginasLa Ciencia Que Se Ocupa de RecogerLissette CastilloAún no hay calificaciones
- Examen 403Documento2 páginasExamen 403Lissette CastilloAún no hay calificaciones
- Informe MezcladorDocumento9 páginasInforme MezcladorLissette CastilloAún no hay calificaciones
- DiazotaciónDocumento9 páginasDiazotaciónLissette CastilloAún no hay calificaciones
- Cuestionario 403Documento1 páginaCuestionario 403Lissette CastilloAún no hay calificaciones
- Resumen Convección - PTCDocumento31 páginasResumen Convección - PTCJorge Luis FigueroaAún no hay calificaciones
- Sustancias Puras SDFDocumento25 páginasSustancias Puras SDFDANIEL PIEDRAHITA RIOSAún no hay calificaciones
- Taller MFDocumento3 páginasTaller MFPipe VillegasAún no hay calificaciones
- Desafio 1 y 2 - QuimicaDocumento21 páginasDesafio 1 y 2 - QuimicavallenautaAún no hay calificaciones
- Presión de Vapor Reid (ASTM D 323) : Ángel Contreras - 1950176 Yisell X. Sánchez - 1950181Documento18 páginasPresión de Vapor Reid (ASTM D 323) : Ángel Contreras - 1950176 Yisell X. Sánchez - 1950181MAYRA FERNANDA CARVAJAL CRIOLLOAún no hay calificaciones
- Propiedades Fisicoquímicas de Los LíquidosDocumento1 páginaPropiedades Fisicoquímicas de Los LíquidosIker CedeñoAún no hay calificaciones
- Comportamiento Fluyente 02 ModificadoDocumento120 páginasComportamiento Fluyente 02 ModificadoGustavo Espinosa BarredaAún no hay calificaciones
- Practica 4Documento9 páginasPractica 4IsraelAngelesAún no hay calificaciones
- Practica 4 Quimica Aplicada EsimeDocumento8 páginasPractica 4 Quimica Aplicada EsimeLuis AngelAún no hay calificaciones
- Equilibrio Liquido VaporDocumento20 páginasEquilibrio Liquido VaporDavid Alemán SánchezAún no hay calificaciones
- Informe Del Rio ZapatillaDocumento30 páginasInforme Del Rio ZapatillaAlexis Leonardo SolizAún no hay calificaciones
- (Acv-S03) Autoevaluación 3 - Fisicoquimica (5952)Documento7 páginas(Acv-S03) Autoevaluación 3 - Fisicoquimica (5952)CYNTHIA FELICITA CALLAN CONTRERASAún no hay calificaciones
- Documento 1Documento9 páginasDocumento 1MARIANA MUGICA RUIZAún no hay calificaciones
- Cálculo Central de GLPDocumento22 páginasCálculo Central de GLPfernando100% (2)
- Serie 5Documento1 páginaSerie 5lester33100% (2)
- REMEDIACIÓN DE SUELOS 2do ParcialDocumento60 páginasREMEDIACIÓN DE SUELOS 2do ParcialFabricio GavilanesAún no hay calificaciones
- Tarea1 Liquidos 2020B 01Q PDFDocumento1 páginaTarea1 Liquidos 2020B 01Q PDFSOLIS ARONE MARISABELAún no hay calificaciones
- Evaporacion e InfiltracionDocumento37 páginasEvaporacion e InfiltracionRoger David Carhuamanta HuamanAún no hay calificaciones
- Presentación Tema 3 - DisolucionesDocumento76 páginasPresentación Tema 3 - Disolucionesvictor.b.i.villadeaspeAún no hay calificaciones
- Cuestionario Informe 1 y 2Documento3 páginasCuestionario Informe 1 y 2Erika BenavidesAún no hay calificaciones
- DESTILACIÓNDocumento16 páginasDESTILACIÓNJuan Julio BadaracoAún no hay calificaciones
- Aplicaciones de Las Propiedades ColigatiDocumento16 páginasAplicaciones de Las Propiedades ColigatiEDILBERTO GUTIERREZ CHICOMAAún no hay calificaciones
- Guia Equipos Operaciones UnitariasDocumento98 páginasGuia Equipos Operaciones UnitariasAlfree Baltazar75% (4)
- Descenso de La Presión de VaporDocumento9 páginasDescenso de La Presión de VaporAbel DiazAún no hay calificaciones
- Facultad de Ingenieria Ambiental Y SanitariaDocumento2 páginasFacultad de Ingenieria Ambiental Y SanitariaMarisol Solsticio Gutiérrez PuertaAún no hay calificaciones
- Temas Selectos de QuimicaDocumento4 páginasTemas Selectos de QuimicaIsaias Sanches LopezAún no hay calificaciones
- Tesis VMSV - GEMU PDFDocumento156 páginasTesis VMSV - GEMU PDFvictor1603Aún no hay calificaciones
- PsicrometriaDocumento56 páginasPsicrometriaJorgenis Gentile CavalliAún no hay calificaciones
- Propiedades de Los LiquidosDocumento12 páginasPropiedades de Los Liquidoslaura barrigaAún no hay calificaciones
- Obtención de Aceites Esenciales Por Arrastre de VaporDocumento4 páginasObtención de Aceites Esenciales Por Arrastre de VaporJ EAún no hay calificaciones
- Guía I ParcialDocumento5 páginasGuía I ParcialJose Daniel Ballestero MontielAún no hay calificaciones