Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Inversion Sacarosa
Cargado por
Andres Fernando Silvestre SuarezDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Inversion Sacarosa
Cargado por
Andres Fernando Silvestre SuarezCopyright:
Formatos disponibles
1
Cinética enzimática: inversión de la sacarosa.
Enzyme kinetics sucrose inversion.
Daniel Andrés Galvis Ortiz, Oscar Iván Sepulveda L.
Escuela de química, Universidad Tecnológica de Pereira, Pereira, Colombia
Resumen— Este artículo contiene los resultados de la práctica una de las sustancias de una mezcla sin necesidad de
sobre la Determinacion de la cinética de la inversión de la separar. Para la cuantificación de sustratos se pueden utilizar
sacarosa, además de comprobar mediante gráficas las hipótesis dos métodos generales:
planteadas por algunos autores en cuanto al orden de reacción
de la catálisis enzimática, comparar la cinética entre una
reacción catalizada enzimáticamente y otra catalizada por
a. Métodos de cambio total, de equilibrio o de punto final.
ácido y finalmente hallar la energía de activación para cada En este tipo de métodos (los más utilizados en la práctica) se
tipo de catálisis. permite que la reacción enzimática se complete o llegue al
equilibrio y se mide la variación producida en la
Palabras clave— Enzima, catálisis enzimática, Cinética, concentración de un producto de reacción o de un reactivo
Hidrólisis, invertasa, sacarosa. presente inicialmente en exceso.
Abstract— his article contains the results of the practice on the b. Métodos cinéticos, en los que se utilizan medidas de la
Determination of the kinetic one of the investment of the velocidad inicial de la reacción enzimática para deducir la
saccharose, beside verifying by means of graphs the hypotheses
concentración inicial de sustrato. Los procedimientos de
raised by some authors as for the order of reaction of the
enzymatical catalysis, compares the kinetic one between a medida son idénticos a los utilizados para reacciones
catalyzed reaction enzimáticamente and other one catalyzed by catalíticas en general.
acid and finally to find the energy of activation for every type
of catalysis. Hoy en día no se dispone de una teoría que explique la
actividad y especificidad de la catálisis enzimática. No
Key Word — Enzyme, enzymatic catalysis, kinetics, hydrolysis, obstante, existen numerosas ideas soportadas por los hechos
invertase, sucrose. experimentales que indican la existencia del complejo
enzima-sustrato formado por unión del sustrato al centro
I. INTRODUCCIÓN activo de la enzima. Mientras está enlazado a la enzima, el
sustrato se transforma en producto, momento en el cual se
La sacarosa es un disacárido de glucosa y fructosa. Se libera de la enzima. Existen cuatro características
sintetiza en plantas pero no en animales superiores. No diferenciadoras de las reacciones enzimáticas con respecto a
contiene ningún átomo de carbono anomérico libre, puesto las reacciones químicas catalizadas:
que los carbonos anoméricos de sus dos unidades
monosacáridos constituyentes se hallan unidos entre sí 1. La enzima es altamente específica y cataliza solo una o
covalentemente mediante un enlace O-glucosídico. Por esta pocas reacciones químicas. Los catalizadores sólidos no
razón, la sacarosa no es un azúcar reductor y tampoco posee suelen ser específicos y pueden intervenir en reacciones
un extremo reductor. diferentes que tengan el mismo grupo funcional. Dada la
gran variedad de enzimas descubiertas actualmente (unas
3300), se pueden llevar a cabo un gran número de
reacciones químicas empleando enzimas específicas como
catalizadores.
2. La velocidad de una reacción catalizada por una enzima
es mucho mayor que la velocidad de una reacción catalizada
por productos no biológicos. Solo es necesaria la presencia
de una pequeña cantidad de enzima para acelerar la
reacción.
3. Las condiciones de reacción (temperatura, presión, pH,
El análisis enzimático o análisis mediante el empleo de etc.) de las reacciones enzimáticas son suaves. A bajas
enzimas puede ser utilizado en: temperaturas la actividad de las enzimas es más elevada que
la de los catalizadores sólidos. A temperaturas altas los
1. La determinación de los sustratos de la reacción catalizadores ordinarios suelen aumentar su actividad,
enzimática, siendo posible determinar específicamente cada mientras que las enzimas disminuyen pudiendo perderla
totalmente a partir de cierta temperatura.
2
reacciona con agua para obtener el producto deseado P1
4. Las enzimas son moléculas sensibles e inestables que (fructosa y glucosa) y P2 (la invertaza libre) como se
requieren cuidado en su uso. Las enzimas pierden muestra en la anterior reacción.
fácilmente su actividad catalítica al cambiar su
conformación estructural (desnaturalización) en el La velocidad de desaparición es:
transcurso de algunas reacciones.
La importancia del estudio de la cinética enzimática no
solamente radica en el hecho de que las enzimas actúan en
el proceso metabólico de los microorganismos sino que
gracias a su posible inmovilización, pueden emplearse cada
vez más en reacciones específicas de aplicación industrial.
En bioquímica, el diagrama de Lineweaver-Burk se emplea
como herramienta gráfica para calcular los
parámetros cinéticos de una enzima.
Su utilidad consiste en que el recíproco de la cinética de Como la concentración del agua no cambia
Michaelis-Menten es fácilmente representable y que de él significativamente en la reacción, ya que la mezcla de
emanan mucha información de interés. reacción está muy diluida, entonces podemos asumir que:
Para seguir el avance de la reacción se usó el anión del
ácido 3,5- dinitrosalicílico que posee la capacidad de
reducir varios azucares. Así, que al medir la capacidad
reducción en la reacción de la mezcla (fructosa y glucosa)
se estará midiendo el alcance de la conversión de la
sacarosa a glucosa y a fructosa en la mezcla de reacción.
En el procedimiento usado, se preparó en primer lugar una
mezcla con una cantidad apropiada de sacarosa, enzima y
solución buffer. Esta mezcla se hidroliza en diferentes
FIG. 1. DIAGRAMA DE LINEWEAVER-BURK tiempos especificados y luego la reacción es inhibida por la
adición de NaOH (contenido en el reactivo adicionado 3,5-
dinitrosilicato); A partir de la forma oxidada y reducida del
anión del 3,5- dinitrosalicílico que posee una diferencia
significativa en el espectro visible y, midiendo las
Cuyo recíproco es: absorbancia a una longitud de onda 540nm se puede medir
dicho alcance.
Posteriormente las soluciones fueron calentadas en un baño
maría realizado en una estufa para revelar el color producido
por el reactivo en presencia de la actividad reductora en la
solución y la intensidad de color es evaluado en el
II. METODOLOGIA
espectrofotómetro. Las lecturas en el espectrofotómetro nos
permiten saber directamente los moles presentes de glucosa
PROCEDIMIENTO
y fructosa en la solución. Entonces, conociendo el tiempo
de duración para que ocurra la reacción, podremos
Para la reacción de la inversión de la sacarosa se usó la
establecer la velocidad media en la cual la sacarosa fue
Enzima invertaza, como lo muestra la reacción.
convertida en glucosa y fructosa.
Corrida del blanco
Se prepararon las mezclas como indica la tabla 1, para la
determinación de la absorbancia del reactivo de
dinitrosalicilato en ausencia de azúcares reductores. Luego
de adicionar la sacarosa, la mezcla se dejó reaccionar 5
Se aplicó el método cinemática de Michaelis-Mentel minutos, se adicionó el reactivo y se colocó en un baño
asumiendo la formación de un complejo intermedio María por cinco minutos, se enfrió, se agregaron 15 mL de
conformado por sacarosa-invertaza. Luego, este complejo agua destilada y se midió la absorbancia a 540 nm.
3
(Procedimiento llevado a cabo para todos los ensayos). Para
el ensayo A0 como para los demás ensayos marcados con *
se adicionó primero el reactivo de dinitrosalicilato y luego
la sacarosa.
Tabla 4. Soluciones realizadas para los ensayos del ítem
Tabla 1. Corrida del blanco E
Hidrolisis no enzimática de la sacarosa.
Ensayo de estandarización
Un bloque de concentraciones sugeridas con las cuales este
Se prepararon las soluciones enlistadas de la tabla 2. Con el experimento puede llevarse a cabo está dado en la tabla 5. El
fin de realizar una curva de calibración que permita conocer ensayo F0 es un blanco, el cual permitirá ver cuanta
la concentración de glucosa y fructosa a un dato de hidrólisis se da en ausencia de cualquier catálisis.
absorbancia obtenido.
Ensayo Sacarosa 0.3M, mL Agua, mL HCl 1M, mL
F0 2.0 2.0 0.0
F1 1.0 2.0 1.0
F2 1.0 1.0 2.0
F3 2.0 1.0 1.0
F4 2.0 0.0 2.0
Tabla 5. Ensayos hidrolisis no enzimática
Tabla 2. Ensayo de estandarización Dependencia de la Velocidad con la
Temperatura.
Progreso de la reacción con el tiempo
Elegir desde los ensayos E un paquete de concentraciones
Para el segundo de los siguientes dos bloques de ensayos,
iníciales que den una absorbancia cerca de 0.5 a temperatura
prepare algo de solución de sacarosa 0.03 M por dilución de
ambiente después del procedimiento estándar. Las
1 mL de la solución stock 0.3 M con 9 mL de agua
temperaturas convenientes para estos ensayos, nombrados
destilada. Corra la serie C usando la solución de sacarosa
como ensayos G son 0ºC (baño de hielo), 12, 25, 35 y 45 ºC.
concentrada y en la serie D use la solución diluida.
RESULTADOS
Verificación de la Actividad Enzimática
La mezcla realizada en la actividad enzimática fue:
1ml Enzima + 0,5 ml H2O + 0,5 ml de s/n Buffer + 1 ml
Sacarosa. (Para la primera muestra), posterior a esto se
procedió con las indicaciones que aparecen en la tabla 1
hasta obtener todas las soluciones.
Se determinó la absorbancia de la solución a 540 nm de A0,
A1, A2 y A3, siguiendo con las condiciones de las guías de
trabajo ninguno de los blancos corridos deberá revelar una
mayor absorbancia que 0,05 a 540 nm, con las absorbancias
Tabla 3. Ensayos de progreso de la reacción en el tiempo. obtenidas se verifico que la solución estaba en buen estado
para ser trabajada.
Dependencia de la velocidad inicial con la
concentración de sustrato Ensayo Absorbancia
A0 0,014
Se preparó una solución 0,03 M en sacarosa a partir de la A1 0,019
solución stock. Se prepararon las mezclas resumidas en la A2 0,024
tabla 3. El ensayo E0 era un blanco a tiempo cero por lo
A3 0,017
que el reactivo de dinitrosalicilato se adicionó antes de la
sacarosa. Tabla 6. Corridas del blanco.
4
Ensayo de estandarización d3 0,013 120
d5 0,036 180
Ensayo Absorbancia (540nm)
B1 0,108 d10 0,057 240
d20 0,107 300
B2 0,204
B3 0,318 TABLA 8. RESULTADOS ENSAYOS C y D
B4 0,330 Con estos datos realizamos la siguiente gráfica:
B5 0,452
Tabla 6. Ensayo de estandarización
A partir de los datos tabulados en la tabla anterior se C
determinó los moles de fructosa y glucosa producidas. D
Posteriormente se realizó una curva de calibración para
hallar el valor de α (coeficiente de calibración).
Absorbancia (N1+N2)/2
0,108 1,998*10-6
0,204 3,497*10-6
0,318 4,995*10-6
0,330 5,995*10-6
0,452 7,493*10-6
Tabla 7 Concentración y absorbancia de las muestras.
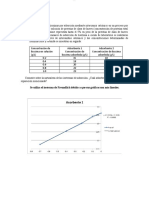
Fig. 3 tiempo vs absorbancia ensayos C y D
Simplificamos la expresión (n1 + n2)/2, como n para Cuya ecuación es:
efectos prácticos. Para C
y = -0,0001x + 0,053
R² = 0,9757
Para esto tenesmo que k0=0,0001
Para D
y = 0,0004x - 0,03
R² = 0,916
k0=0,0004
Por lo tanto las concentraciones serán:
Usando (x/0.003) = k0t
Fig. 2. Curva de calibración de la absorbancia vs. n
CONCENTRACIÓ CONCENTRACIÓN TIEMPO
La ecuacion de la recta es: NC D (s)
Abs = 0,0608ne-6 - 0,0094 1,8e-5 mol* l-1 7,2e-5 mol* l-1 60
R² = 0,982 3,6e-5 mol* l-1 1,44e-4 mol* l-1 120
5,4e-5 mol* l-1 2,16e-4 mol* l-1 180
-1
Con la pendiente de la anterior gráfica, obtenemos que la 7,2e-5 mol* l 2,88e-4 mol* l-1 240
constante de calibración es: 60840,18 mol-1. 9e-5 mol* l-1 3,6e-4 mol* l-1 300
Tabla 9. Concentraciones ensayos C y D en el tiempo
Progreso de la reacción con el tiempo
Con estos datos podemos observar que la concentración
ENSAYO ABSORBANCIA tiempo aumenta con el tiempo.
c1 0,046 60
c3 0,034 120 Dependencia de la velocidad inicial con la
c5 0,026 180 concentración de sustrato.
c10 0,02 240
c20 0,044 300 Ensayo Absorbancia Concentración Velocidad r0
ENSAYO ABSORVANCIA TIEMPO S0 (mol /L) (mol/L*s)
d1 0,006 60 Sacarosa 0.3 M
E0 0,046 2,5203*10-4 8,4009*10-7
5
E1 1,695 9,287*10-3 3,0955*10-5 R² = 1
E2 2,658 0,0146 4,8542*10-5 Del intercepto de la gráfica se obtiene el valor de k2
Sacarosa 0.03 M Dónde:
E3 1,228 6,728*10-3 2,2427*10-5 1
E4 0,787 4,312*10-3 1,4373*10-5 =30,91 s∗L/mol
k 2 (E)
E5 0,384 2,116*10-3 7,0129*10-6 0
E6 0,337 1,846*10-3 6,1546*10-6 (E)0 es la concentración inicial de la enzima siendo el valor
Tabla 10. Concentración de sustrato y velocidades nominal del peso molecular de la enzima 100000 g/mol.
halladas en el ensayo E. (E)0= 7*10-4 mol/L
K2= 46,2171 s-1.
[s0] = A/αV (3.4.1)
A partir del valor de K2 y de la pendiente de la gráfica ,
[s0] = (0,046)/ (60840, 18 mol-1) *(0,003L) podemos encontrar el valor de Km:
[s0] = 2, 5*10-4 mol /L
Km
ro = δ[ ]/δt = 299, 96 s
k 2 ( E)0
ro = (2,52*10-4 mol/L)/300 s
K
ro= 8,4*10-7 mol/L*s m= 9, 7043 mol/L (3.4.5)
Ecuación de la recta de lineweaver-burk
Ensayo r0/s0(s-1) r0(mol/l*s)
Km Sacarosa 0.3 M
∗1 E0 3,3333*10-3 8,4009*10-7
1 1 k 2 ( E)0
= + E1 3,3332*10-3 3,0955*10-5
r 0 k 2(E ) 0
(S)0 E3 3,3248*10-3 4,8542*10-5
Sacarosa 0.03 M
1/[S0](L/mol) 1/r0 (L*s/mol) E4 3,3334*10-3 2,2427*10-5
Sacarosa 0.3 M E5 3,3333*10-3 1,4373*10-5
3968,2539 1190348,653 E6 3,3142*10-3 7,0129*10-6
E3 3,3340*10-3 6,1546*10-6
107,6773 32304,9588 Tabla 12. Datos para la gráfica de Eadie-Hofstee
68,4932 20600,7169
Para la construcción de la gráfica 5 se usó los datos de la
Sacarosa 0.03 M tabla 12, con eliminación previa de los datos de los ensayos
148,6326 44589,1113 E0, E4 y E5. La razón por la cual se eliminó los datos es
para obtener una mejor correlación de los datos (línea recta).
231,9109 69574,8974
472,5898 142594,3618
541,7118 162480,0962
Tabla 11. Datos para graficar la lineweaver-Burk
Grafica 4. Representación gráfica de lineweaver-Burk Grafica 5. Representación gráfica de Eadie-Hofstee
para la conversión de la sacarosa 0.3M. para la conversión de la sacarosa 0.3M.
Ecuación de la recta:
1 299,96∗1 Ecuación de la recta:
=30,91+
r0 ( S)0 r0 /s0= - 1706,2 r0 + 0,0861
6
R2=1
Con el valor de la pendiente se obtiene Km, sabiendo que
esta es igual a -1/Km:
−1
=−1706,2 L /mol
Km
Km = 5,8610*10-4 mol/L
Ahora, conocida Km se puede hallar K2:
Grafica 7 Representación gráfica de Eadie-Hofstee para la
conversión de la sacarosa 0.03M.
K 2∗E 0
= 0,0861 / s
Km
Ecuación de la recta:
K2 = 0,0721 /s
r0 /s0= - 23,069 r0 + 0,0035
R2=0,7495
Con el valor de la pendiente se obtiene Km, sabiendo que
esta es igual a -1/Km:
−1
=−23,069 L/mol
Km
Km = 0,0433 mol/L
Ahora, conocida Km se puede hallar K2:
K 2∗E 0
Grafica 6. Representación gráfica de lineweaver-Burk para la = 0,0035 / s
Km
conversión de la sacarosa 0.03M.
Ecuacion de la recta K2 = 0,2167 / s
1 299,97∗1 III. CONCLUSIONES
=5,3748+
r0 (S )0
Se determinó la cinética de la inversión de la
R² = 1 sacarosa, además se comprobó por medio de
graficas las hipótesis planteadas por lineweaver-
1
=5,3748 s∗L /mol Burk en cuanto al orden, el cual para esta práctica
k 2 (E) 0
es de primer orden en la reacción de la catálisis
enzimática; además tiene la ventaja de que permite
1 una determinación más exacta del valor de la
= (5,3748 s∗L/mol )*(7*10-4 mol/L)
k2 velocidad máxima.
K2 = 3, 7624*10-3 / s En términos más específicos, la energía de
K2 = 3, 7624*10 / s-3 activación para una reacción que está siendo
catalizada por una enzima es mucho menor que la
K2= 46,2171 /s energía de activación para la misma reacción
Km cataliza por un ácido, de allí su importancia a nivel
=299,97s bioquímico, puesto que reacciones que a nivel de
k 2 ( E)0 laboratorio tardan varios días u horas, en la célula
ocurren en fracciones de segundo.
Km = 7, 9002*10-4 mol /L
La invertaza es una enzima es una enzima que
convierte la sacarosa en glucosa y fructosa, como
se presentó en las reacciones realizadas en la sesión
7
de laboratorio se determinó la cinética de la
reacción y la capacidad de la enzima como
catalizador de esta reacción biológica.
La representación de lineweaver-Burk tiene la
ventaja de que permite una determinación más
exacta del valor de la velocidad máxima, ya que en
la representación sencilla r0 frente a s0 solo se
obtiene su valor aproximado, puesto que es un
valor limite a una concentración de sustrato
infinita
La representación gráfica de Eadie-Hofstee, no
solamente da los valores de velocidad máxima y de
Km en forma sencilla, sino que también amplia las
desviaciones de carácter lineal que pueden no
parecer en la representación de lineweaver-Burk.
IV. BIBLIOGRAFIA
[1] Fisicoquímica aplicada, fundamentación experimental;
Jorge Eliecer Alba,Melvin Aroldo Dura,Hoover Alberto
valencia
[2] P.W atkins; sexta edición; universidad de Oxford.
8
También podría gustarte
- Quesos Viri PracticaDocumento13 páginasQuesos Viri PracticaTann MoralesAún no hay calificaciones
- Equipo 3 DIFUSIVIDAD EN GASESDocumento4 páginasEquipo 3 DIFUSIVIDAD EN GASESJesus HernandezAún no hay calificaciones
- Practica 2 Cromatografia Por AdsorcionDocumento5 páginasPractica 2 Cromatografia Por AdsorcionJordan Josue TorresAún no hay calificaciones
- Determinacion de RiboflavinaDocumento4 páginasDeterminacion de Riboflavinaalan50% (2)
- Disertacion 1 Depredadores Roman Escobedo Luis Carlos 9IM1Documento2 páginasDisertacion 1 Depredadores Roman Escobedo Luis Carlos 9IM1LiriamAún no hay calificaciones
- Caracterizacion de La Cinetica de Hidrolisis de La Sacarosa Por Invertasa Libre e InmovilizadaDocumento53 páginasCaracterizacion de La Cinetica de Hidrolisis de La Sacarosa Por Invertasa Libre e InmovilizadaFernando Gutiérrez100% (2)
- ACIDO BORICOfinalDocumento48 páginasACIDO BORICOfinalGustavo Cardona100% (5)
- Curva Tipo de Azúcares ReductoresDocumento2 páginasCurva Tipo de Azúcares ReductoresMar Dz HAún no hay calificaciones
- Informe Mejorado 1Documento16 páginasInforme Mejorado 1Andre Herbas FernandezAún no hay calificaciones
- aNA 4Documento5 páginasaNA 4Ana Patricia VillegasAún no hay calificaciones
- Ley de BeerDocumento10 páginasLey de Beermedun2009Aún no hay calificaciones
- EvaporaciónDocumento11 páginasEvaporaciónCarla Itzel AstorgaAún no hay calificaciones
- Potencial NormalDocumento8 páginasPotencial Normaladriana lizeth arzate guillenAún no hay calificaciones
- Hio Hi HoDocumento71 páginasHio Hi HojoeAún no hay calificaciones
- Discusión Halofílicos AmilolíticosDocumento14 páginasDiscusión Halofílicos AmilolíticosOz HdzAún no hay calificaciones
- P8 Mermelada Ok Ok OkDocumento45 páginasP8 Mermelada Ok Ok OkOz HdzAún no hay calificaciones
- Práctica 8 (Bioquímica) Efecto de La Temperatura en La Velocidad EnzimáticaDocumento3 páginasPráctica 8 (Bioquímica) Efecto de La Temperatura en La Velocidad EnzimáticaCeli Silva VillanuevaAún no hay calificaciones
- Fundamento Refractómetro AbbeDocumento2 páginasFundamento Refractómetro AbbeDaniel Alejandro Rojas ToroAún no hay calificaciones
- CafeinaDocumento4 páginasCafeinaAndresDuranAún no hay calificaciones
- Determinación Del Peso Molecular de Una Proteína Usando Cromatografía Por Exclusión Molecular.Documento8 páginasDeterminación Del Peso Molecular de Una Proteína Usando Cromatografía Por Exclusión Molecular.FernandoVTAún no hay calificaciones
- Tarea 3Documento2 páginasTarea 3Kagney UralesAún no hay calificaciones
- Diagrama de Purificación Parcial de Lisozima de Clara de HuevoDocumento1 páginaDiagrama de Purificación Parcial de Lisozima de Clara de HuevoXimena SánchezAún no hay calificaciones
- Problema Dos EvaporadoresDocumento1 páginaProblema Dos EvaporadoresNati FernandezAún no hay calificaciones
- Aajr Rep P2 Opu2Documento8 páginasAajr Rep P2 Opu2Jenny AlvaradoAún no hay calificaciones
- Contenido de Nitrógeno Total y Determinación de Sal en QuesosDocumento26 páginasContenido de Nitrógeno Total y Determinación de Sal en QuesosRichard MelgarejoAún no hay calificaciones
- Glucosidos CianogenicosDocumento4 páginasGlucosidos CianogenicosT PerezAún no hay calificaciones
- Practica de YogurthDocumento12 páginasPractica de YogurthGabriela HuazoAún no hay calificaciones
- HIDROLISISDocumento4 páginasHIDROLISISYurian vanegasAún no hay calificaciones
- Instructivo Ingeniería de BiorreacciónDocumento44 páginasInstructivo Ingeniería de BiorreacciónOz HdzAún no hay calificaciones
- Modelado de Cinetica de FermentacionesDocumento19 páginasModelado de Cinetica de FermentacionesjhoseceAún no hay calificaciones
- Pruebas Colorimétricas para AnfetaminasDocumento3 páginasPruebas Colorimétricas para AnfetaminasMonika OlguinAún no hay calificaciones
- Solubilidad de Las ProteinasDocumento16 páginasSolubilidad de Las ProteinasAnabel cruz crisantoAún no hay calificaciones
- Pre-Informe 1 (Inversión de La Sacarosa en Medio Ácido)Documento14 páginasPre-Informe 1 (Inversión de La Sacarosa en Medio Ácido)CarolinaMedranoAún no hay calificaciones
- Porta 3 Procesos 3Documento28 páginasPorta 3 Procesos 3Ari Rojas RamirezAún no hay calificaciones
- Absorción de Ácido Acético Con Carbón ActivadoDocumento8 páginasAbsorción de Ácido Acético Con Carbón ActivadoMariaElizabethSanchezAún no hay calificaciones
- ProblemasDocumento2 páginasProblemasjovanaAún no hay calificaciones
- Práctica 1 FenómenosDocumento8 páginasPráctica 1 FenómenosMonserrat Enamorada VargasAún no hay calificaciones
- Determinacion de Proteinas Por El Metodo de Lowry Y BradfordDocumento3 páginasDeterminacion de Proteinas Por El Metodo de Lowry Y BradfordMiriam N. Rivera Pinedo0% (3)
- Perfiles de Velocidad de Flujo PDFDocumento19 páginasPerfiles de Velocidad de Flujo PDFCAROLINAAún no hay calificaciones
- Practica 6: Determinación Del Índice de Refracción y Su Aplicación en El Procesamiento de Los AlimentosDocumento22 páginasPractica 6: Determinación Del Índice de Refracción y Su Aplicación en El Procesamiento de Los AlimentosPedro Antonio Cardenas ValdezAún no hay calificaciones
- Tarea 3 SeguridadDocumento12 páginasTarea 3 SeguridadAlejandra Fabiola CadenasAún no hay calificaciones
- Práctica 6Documento5 páginasPráctica 6Rodrigo Manuel Bravo PachecoAún no hay calificaciones
- Practica 5 Lineas de DuhringDocumento9 páginasPractica 5 Lineas de DuhringAlan Gerardo Aguirre GonzalezAún no hay calificaciones
- Problemario 3er ParcialDocumento11 páginasProblemario 3er ParcialOz HdzAún no hay calificaciones
- Dif. MemDocumento5 páginasDif. MemJavier AnguianoAún no hay calificaciones
- Biosintesis de DesoxirribonucleotidosDocumento23 páginasBiosintesis de DesoxirribonucleotidosingristabAún no hay calificaciones
- Reporte de Practica 4Documento5 páginasReporte de Practica 4GabrielVazquezOlveraAún no hay calificaciones
- Determinación de Azúcares Reductores Por El Método DNSDocumento9 páginasDeterminación de Azúcares Reductores Por El Método DNSlindaAún no hay calificaciones
- Polisacaridos EspañolDocumento50 páginasPolisacaridos EspañolDariel Malagón PerrusquiaAún no hay calificaciones
- Bioquimica Efecto PH y EnzDocumento3 páginasBioquimica Efecto PH y EnzGuerrillaScribdAún no hay calificaciones
- Reporte AireaciónDocumento2 páginasReporte AireaciónJenniferAún no hay calificaciones
- Práctica 4 - Friccion en Tubería RectaDocumento4 páginasPráctica 4 - Friccion en Tubería RectaCesr Paulino0% (1)
- Criterios de Selección de EquipoDocumento3 páginasCriterios de Selección de EquipoVictoria MonteroAún no hay calificaciones
- Práctica No.2 AnaliticaDocumento9 páginasPráctica No.2 AnaliticaLeonardo De la CruzAún no hay calificaciones
- Informe Cinetica EnzimaticaDocumento6 páginasInforme Cinetica EnzimaticaMayerli Tello BorjaAún no hay calificaciones
- Efecto de La Concentración Del Sustrato Sobre La Velocidad de Reacción Documento Nuevo 8 de DiciembreDocumento5 páginasEfecto de La Concentración Del Sustrato Sobre La Velocidad de Reacción Documento Nuevo 8 de DiciembreRosario JessAún no hay calificaciones
- V Prac 7Documento4 páginasV Prac 7Isaac VeraAún no hay calificaciones
- Actividad Enzimatica....Documento7 páginasActividad Enzimatica....Gladys González González100% (1)
- Bitacora 3Documento5 páginasBitacora 3Itzel Yamile Sandoval MendozaAún no hay calificaciones
- Aplicación de La Refractometria de Arco Iris (EXPOSICIÓN) 1Documento16 páginasAplicación de La Refractometria de Arco Iris (EXPOSICIÓN) 1Andres Fernando Silvestre SuarezAún no hay calificaciones
- Informe 8, Analisis de Mezclas BinariasDocumento10 páginasInforme 8, Analisis de Mezclas BinariasAndres Fernando Silvestre SuarezAún no hay calificaciones
- YodinacionDocumento5 páginasYodinacionAndres Fernando Silvestre SuarezAún no hay calificaciones
- Ejercicios Vía HúmedaDocumento1 páginaEjercicios Vía HúmedaAndres Fernando Silvestre SuarezAún no hay calificaciones
- Potencial de Electrodo.Documento6 páginasPotencial de Electrodo.Andres Fernando Silvestre SuarezAún no hay calificaciones
- Numero de Transporte Por El Método de Frontera MóvilDocumento3 páginasNumero de Transporte Por El Método de Frontera MóvilAndres Fernando Silvestre SuarezAún no hay calificaciones
- Electrolisis Del AguaDocumento3 páginasElectrolisis Del AguaAndres Fernando Silvestre SuarezAún no hay calificaciones
- Informe (Lab 4) Ondas Estacionarias en Una Columna de AireDocumento7 páginasInforme (Lab 4) Ondas Estacionarias en Una Columna de AireAndres Fernando Silvestre SuarezAún no hay calificaciones
- Informe Cinetica 1Documento29 páginasInforme Cinetica 1Andres Fernando Silvestre SuarezAún no hay calificaciones
- Cinética Del Cristal VioletaDocumento8 páginasCinética Del Cristal VioletaAndres Fernando Silvestre SuarezAún no hay calificaciones
- Preinforme (Lab 7) Difracción de La LuzDocumento4 páginasPreinforme (Lab 7) Difracción de La LuzAndres Fernando Silvestre SuarezAún no hay calificaciones
- Informe Cinetica Del Hierro IIDocumento6 páginasInforme Cinetica Del Hierro IIAndres Fernando Silvestre SuarezAún no hay calificaciones
- AlmacenamientoDocumento2 páginasAlmacenamientoAndres Fernando Silvestre SuarezAún no hay calificaciones
- ElectroquimicaDocumento5 páginasElectroquimicaAndres Fernando Silvestre SuarezAún no hay calificaciones
- Calor de Disolucion y NeutralizacionDocumento8 páginasCalor de Disolucion y NeutralizacionAndres Fernando Silvestre SuarezAún no hay calificaciones
- PolarimteriaDocumento4 páginasPolarimteriaAndres Fernando Silvestre SuarezAún no hay calificaciones
- Informe (Lab 10) Espectroscopía ÓpticaDocumento8 páginasInforme (Lab 10) Espectroscopía ÓpticaAndres Fernando Silvestre SuarezAún no hay calificaciones
- Informe (Lab 12) Medición de La Carga Del ElectrónDocumento13 páginasInforme (Lab 12) Medición de La Carga Del ElectrónAndres Fernando Silvestre SuarezAún no hay calificaciones
- Aplicación de La Refractometria de Arco Iris (EXPOSICIÓN)Documento16 páginasAplicación de La Refractometria de Arco Iris (EXPOSICIÓN)Andres Fernando Silvestre SuarezAún no hay calificaciones
- Área 2 Examen Simulacro PDFDocumento19 páginasÁrea 2 Examen Simulacro PDFMaria Elena SandovalAún no hay calificaciones
- Evaluaciones TCCDocumento2 páginasEvaluaciones TCCDominique VegaAún no hay calificaciones
- HomologacionDocumento25 páginasHomologacionChristian Medina RodríguezAún no hay calificaciones
- El TraucoDocumento4 páginasEl TraucoWladimir Rodrigo Brito RivasAún no hay calificaciones
- R. ASEGURAMIENTO DE VEHICULO Con Aviso A MPDocumento3 páginasR. ASEGURAMIENTO DE VEHICULO Con Aviso A MPguzz_161192Aún no hay calificaciones
- BD+C StudyGuide-ESDocumento246 páginasBD+C StudyGuide-ESredalfsAún no hay calificaciones
- Manual Configuracion ZXDSL 831 IIDocumento7 páginasManual Configuracion ZXDSL 831 IIohrzamudio100% (1)
- Indicadores Reproductivos RegionalesDocumento14 páginasIndicadores Reproductivos Regionalesjose ortizAún no hay calificaciones
- MATE - TAREA 2 - Expresiones AlgebraicasDocumento4 páginasMATE - TAREA 2 - Expresiones Algebraicase-JOSE MIGUEL MARTINEZ VINTIMILLAAún no hay calificaciones
- Tipos de Puertos S (1) - FusionadoDocumento118 páginasTipos de Puertos S (1) - FusionadoMichelle CastilloAún no hay calificaciones
- Doble RadiacionDocumento24 páginasDoble RadiacionMichaelVelasquezAún no hay calificaciones
- Taller Teoria Contable FORO DE DISCUSIÓN LOS PARADIGMAS DE TOMAS KUHNDocumento5 páginasTaller Teoria Contable FORO DE DISCUSIÓN LOS PARADIGMAS DE TOMAS KUHNAndrés Camilo LozRuAún no hay calificaciones
- Lineas de FulcroDocumento22 páginasLineas de FulcroMary Adco MoralesAún no hay calificaciones
- Tinciones SangreDocumento10 páginasTinciones SangrejhrpaulAún no hay calificaciones
- Guía de GeografíaDocumento8 páginasGuía de GeografíaPollo HernandezAún no hay calificaciones
- Temario Beca UTECDocumento4 páginasTemario Beca UTECJaqueline MariaAún no hay calificaciones
- 09-10 Marca TrueDocumento44 páginas09-10 Marca TrueAnonymous xTxId5fqqWAún no hay calificaciones
- 1 TallerGeomorfologíadeColombiaDocumento5 páginas1 TallerGeomorfologíadeColombiaOS ROAAún no hay calificaciones
- Sintesis Del Acidp P-AminobenzoicoDocumento11 páginasSintesis Del Acidp P-AminobenzoicoJaime Velásquez100% (1)
- Estudio Oceanográfico de La Playa Cedeño FinalDocumento32 páginasEstudio Oceanográfico de La Playa Cedeño FinalCindy RuizAún no hay calificaciones
- Certificado de Tuberia Estructurada 2020Documento2 páginasCertificado de Tuberia Estructurada 2020Leonardo MonteroAún no hay calificaciones
- Plano de Jumbo DetallesDocumento23 páginasPlano de Jumbo DetallesPedro Espinoza Huahuacondori100% (1)
- Corte Fugado Detalle ConstructivoDocumento1 páginaCorte Fugado Detalle ConstructivoHector HernandezAún no hay calificaciones
- Nelcy Robles 1Documento124 páginasNelcy Robles 1Carlos AncasiAún no hay calificaciones
- Glosario de InvestigacionDocumento3 páginasGlosario de InvestigacionMARIA CECILIA GARCIA RODRIGUEZAún no hay calificaciones
- Practica de Sensibilidad + Casos ClinicosDocumento12 páginasPractica de Sensibilidad + Casos Clinicosalison.barreraAún no hay calificaciones
- Cuestionarios Álgebra Geometría y TrigonometriaDocumento37 páginasCuestionarios Álgebra Geometría y TrigonometriaWilmarMendozaAún no hay calificaciones
- La Inteligencia HumanaDocumento4 páginasLa Inteligencia HumanaDaniel Abraham LopezAún no hay calificaciones
- Des CargoDocumento4 páginasDes CargoVladimir Fuentes CalderónAún no hay calificaciones
- Aspecto Físico PedroDocumento10 páginasAspecto Físico PedroGuido Sargiotto0% (1)