Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Gases Reales e Ideales
Gases Reales e Ideales
Cargado por
Silvia LLancaleoDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Gases Reales e Ideales
Gases Reales e Ideales
Cargado por
Silvia LLancaleoCopyright:
Formatos disponibles
2.- Gases ideales y reales.
Ecuaciones trmicas de estado.
2.1. Gas ideal. Ley de Boyle (45); 2.2. Ecuacin trmica de estado del gas ideal. Ley de
Avogadro (46); 2.3. Densidad de un gas perfecto. Densidad relativa al aire (50);
2.4. Mezcla de gases perfectos no reaccionantes. Ley de Dalton (50); 2.5. Superficies
PVT de un gas ideal (52); 2.6. Gases reales (52); 2.7. Determinacin de las coordenadas
crticas. Tubos de Natterer (57); 2.8. Ecuacin de estado de Clausius (58); 2.9. Ecuacin
de estado de Van der Waals (60); 2.10. Isotermas de Van der Waals (63); 2.11. La
ecuacin de Van der Waals y las coordenadas crticas (64); 2.12. Otras ecuaciones de
estado (65); 2.13. Ecuacin de estado reducida. Ley de los estados correspondientes (68);
Problemas (70)
2.1. Gas ideal. Ley de Boyle.- En la leccin anterior, se indic que los
valores de los coeficientes de dilatacin isobrico () y piezotrmico () de los gases
dependen de la presin y de la naturaleza del gas y que los valores de dichos
coeficientes tienden a un valor comn
1
273.15
0.003 661 K
[2.1]
con independencia de la naturaleza del gas,
cuando la presin tiende a cero. De acuerdo con
esta situacin, se define el gas ideal o perfecto
como un sistema ideal cuyos coeficientes y
tienen valores constantes e iguales a
1/273.15 K-1 para cualquiera que sea su presin
y que, adems, est caracterizado porque satisface exactamente la llamada ley de Boyle-Mariotte, de la que trataremos a continuacin.
Figura 2.1.- Robert BOYLE (1627-1691).
Los estudios experimentales realizados en
1661 por el qumico irlands Robert BOYLE1
(1627-1691) y en 1676 por el fsico francs Edme MARIOTTE (1620-1684) permiten
afirmar que
Robert BOYLE (1627-1691); qumico ingls. En su obra The Sceptical Chymist (1661)
estableci el concepto moderno de elemento y supuso que en nmero de estos debera ser muy
superior a los tres de los alquimistas o a los cuatro aristotlicos.
Manuel R. Ortega Girn
45
46
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
Ley de BOYLE-MARIOTTE: los volmenes ocupados por una misma masa
gaseosa son inversamente proporcionales a las presiones a la que est
sometida, siempre que la temperatura se mantenga constante; esto es
pV
[2.2]
donde k es exclusivamente funcin de la temperatura; de modo que si el proceso es
isotermo, tal como se considera en el enunciado de la ley, k es una constante.
Diferenciando la expresin [2.1] se obtiene la forma diferencial de la ley de BoyleMariotte:
p dV
V dp
dp
p
dV
V
[2.3]
A principios del siglo XIX se demostr que la ley de Boyle-Mariotte slo tiene
una validez aproximada para los gases reales, aunque estos la satisfacen tanto mejor
cuanto menor es su presin. En consecuencia, se defini un gas ideal o perfecto como
un fluido no licuable tal que
a) satisface exactamente las leyes de Gay-Lussac y de Charles (vide ec.
[1.83] y [1.84]).
b) obedece exactamente la ley de Boyle-Mariotte a cualquier temperatura.
Aunque el gas ideal no existe, todos los gases reales a bajas presiones lo
aproximan muy bien. Desde un punto de vista prctico, en las condiciones ordinarias
de presin y temperatura, pueden considerarse como gases ideales los llamados gases
permanentes (que no puede licuarse ms que a muy bajas temperaturas), tales como
el hidrgeno, el helio, el oxgeno, el nitrgeno y el aire, ... entre otros.
2.2. Ecuacin trmica de estado del gas ideal. Ley de Avogadro.- La
ecuacin de estado de un sistema simple, cuyo acoplamiento con los alrededores se
realiza a travs del volumen, tal como el caso que ahora nos ocupa, es de la forma
p(V,T)
o bien
f (p,V,T)
[2.4]
donde f(p,V,T)=0 es la ecuacin de una superficie en el espacio termodinmico
(p,V,T), para cuyo estudio se suele recurrir a considerar cortes de la misma con
planos paralelos a los tres planos coordenados (Figura 2.5). De esta forma, se obtienen
las curvas planas isotermas (temperatura constante), isobaras (presin constante) e
isocoras o isoteras (volumen constante). Todas estas transformaciones se pueden
representar mediante el diagrama p-V o de Clapeyron y corresponden, respectivamente, a las leyes de Boyle-Mariotte (que relaciona el volumen de un gas con su
presin cuando se mantiene constante la temperatura) y a las leyes de Gay-Lussac y
Charles (que relacionan el volumen y la presin con la temperatura, mantenindose
constante bien sea la presin o el volumen). Estas leyes indican que el estado del gas
queda inequvocamente definido al dar valores a dos cualesquiera de las variables
termodinmicas (p,V,T), ya que el valor de la otra quedar determinado a partir de
la ecuacin de estado [2.4].
Para una temperatura fija, todas las transformaciones de un gas ideal vienen
definidas por la ecuacin [2.2], que en el diagrama de Clapeyron se representa
2.2.- Ecuacin trmica de estado del gas ideal. Ley de Avogadro.
47
mediante una hiprbola equiltera (Figura 2.2). Para una temperatura distinta de la
anterior, se tendr otra hiprbola diferente, de tal suerte que tendremos toda una
familia de hiprbolas o red de isotermas, correspondiendo una de tales hiprbolas a
cada temperatura.
Ahora, consideremos una cierta masa de gas
perfecto que se encuentre inicialmente en el estado
(p0,V0,T0) representado por el punto A en el diagrama de la Figura 2.2, y supongamos que dicha masa
gaseosa evoluciona hasta alcanzar el estado (p,V,T),
representado por el punto C en el mismo diagrama.
Esta evolucin puede tener lugar en dos etapas. En
la primera etapa, el gas mantiene constante su volumen (evolucin isocora) y pasa de la temperatura
T0 a la T, en tanto que su presin aumenta desde el
Figura 2.2.- Determinacin de la
valor p0 al p, viniendo determinada esta ltima por ecuacin trmica de estado del gas
ideal.
la ecuacin
p0
T0
p
T
[2.5]
En la segunda etapa, el gas evoluciona de forma isoterma, hasta alcanzar el estado
final (p,V,T), por lo que, de acuerdo con la ley de Boyle-Mariotte,
pV0
[2.6]
pV
de modo que, multiplicando miembro a miembro las dos ecuaciones anteriores, se
sigue
p 0 V0
T0
pV
T
[2.7]
donde r es una constante para el gas que se est considerando, que depende
nicamente de la masa del mismo. La ecuacin [2.7] es la ecuacin trmica de estado
para la masa m de gas y establece que, cualquiera que sea la transformacin que
experimente el gas (a masa constante), el producto de la presin por el volumen
dividido por la temperatura absoluta permanece constante en todos los estados. De
la ec. [2.7] se desprende la imposibilidad de tener valores negativos para la
temperatura absoluta T, ya que ello requerira un valor negativo para el producto pV.
Ejemplo I.- Deducir la ecuacin [2.7] por diferenciacin y posterior integracin de la ecuacin de
estado escrita en la forma V=V(p,T), habida cuenta de la definicin dada para el gas ideal.
La diferenciacin de la ecuacin trmica de estado en la forma que se indica en el enunciado
nos conduce a
dV
V
dp
p T
V
dT
T p
[2.8]
48
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
Como un gas ideal est caracterizado por satisfacer exactamente las leyes de Boyle-Mariotte
y de Gay-Lussac, calcularemos las derivadas parciales que intervienen en la ec. [2.8] con el
concurso de estas leyes. As, de la ley de Boyle-Mariotte diferenciada [2.3] se sigue
V
p T
V
p
[2.9]
mientras que de la 1 ley de Gay-Lussac [1.83], V/T=k, cuando p es constante, se obtiene
V
T p
V
T
[2.10]
Sustituyendo las expresiones [2.9] y [2.10] en la [2.8] resulta
V
dp
p
dV
V
dT
T
dp
p
dV
V
dT
T
[2.11]
que es una ecuacin diferencial de variables separadas que, por integracin, conduce a
ln V
ln p
ln T
cte
pV
T
[2.12]
que es la ecuacin [2.7], tal como queramos demostrar.
Ahora, introduciremos una ley que fue
formulada en 1811 por AVOGADRO2:
LEY DE AVOGADRO.- A igualdad de
presin, volumen y temperatura, todos
los gases contienen el mismo nmero
de molculas y, como consecuencia de
ello, tienen masas proporcionales a sus
Figura 2.3.- Amedeo AVOGADRO, conde
respectivas masas moleculares.
de Quaregna e Ceretto (1776-1856).
En particular, si tomamos 1 mol de gas (i.e.,
un nmero de gramos igual al nmero que
expresa su masa molecular), el nmero de molculas es
NA
6.02251023 molculas/mol
[2.13]
que se denomina nmero de Avogadro. En definitiva, se cumple que
1 mol de cualquier gas, en las mismas condiciones de presin y de temperatura, ocupa siempre el mismo volumen.
En condiciones normales (p0=1 atm y T0=273.15 K), un mol de cualquier gas
perfecto ocupa un volumen de 22.4136 L (volumen molar).
Amedeo AVOGADRO, conde de Quaregna e Ceretto (1776-1856). Fsico y qumico italiano.
Aunque tambin realiz investigaciones en electricidad y sobre las propiedades fsicas de los
lquidos, es ms conocido por sus trabajos sobre los gases, que le llev a formular en 1811 la ley
que ahora lleva su nombre (actualmente reconocida como cierta, aunque no fue aceptada
universalmente hasta 1850).
2.2.- Ecuacin trmica de estado del gas ideal. Ley de Avogadro.
49
La ley de Avogadro permite escribir la ecuacin trmica de estado de un gas
perfecto de un modo ms general. En efecto, si consideramos 1 mol de gas ideal en
condiciones normales de presin (1 atm) y de temperatura (0C), el valor de la
constante r que aparece en [2.7] tomar un valor determinado (referido a 1 mol de
sustancia) que designaremos por R y que podemos calcular a partir del conocimiento
del volumen molar; i.e.,
R
p 0 v0
T0
1 atm 22.4136 L/mol
273.15 K
0.082 05
atm L
mol K
[2.14]
siendo R una constante independiente de la naturaleza del gas, conocida con el
nombre de constante universal de los gases perfectos, con dimensiones de
trabajo/(gradomol). En el Sistema Internacional de Unidades (S.I.), teniendo en
cuenta que 1 atm = 1.013105 Pa y 1 L=10-3 m3,
R
1.013105 Pa 22.413610 3 m 3/mol
273.15 K
8.314 97
J
mol K
[2.15]
Teniendo en cuenta [2.14], reescribimos la expresin [2.7] para el caso de un mol
de gas perfecto
pv
T
p 0 v0
T0
pv
RT
[2.16]
siendo v el volumen molar. Si en lugar de un mol de sustancia consideramos n moles,
el volumen correspondiente ser V=nv, y obtenemos finalmente la ecuacin de estado
del gas ideal en la forma
pV
nRT
[2.17]
que es la llamada ecuacin de Clapeyron.
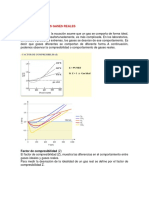
Tanto la ec. [2.16] como el valor de la constante R pueden establecerse experimentalmente a
partir de los datos obtenidos para los gases reales. Como estos gases slo se comportan como
ideales a presiones reducidas, es preciso
obtener datos experimentales a presiones
finitas y extrapolarlos para presiones
nulas. Esto es lo que hizo el fsico
francs Emile Hilaire AMAGAT (18411915) al representar el trmino pv/T
frente a p. Obtuvo as diferentes curvas,
aun trabajando con un mismo gas,
correspondiendo cada una de ellas a la
temperatura a la que se realizaba la experiencia. De este modo, observ que para
gases de diferente naturaleza se obtenan
familias de curvas ms o menos
semejantes a la que se muestra en la
Figura 2.4 (correspondientes al dixido de
carbono, CO2); pero que siempre, al
Figura 2.4.- Isotermas de Amagat para el dixido de
extrapolar a presin nula, todas las
carbono.
50
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
isotermas tienen la misma ordenada en el origen, cuyo valor es 8.31497 J mol-1 K-1, que es el valor
de la constante R de los gases perfectos.
Ahora podemos definir el gas perfecto como aqul para el que el trmino pv/T
es igual a R a cualquier temperatura, por lo que su grfica en el diagrama de la
Figura 2.4 es la lnea recta paralela al eje de presiones, tal como se indica.
De cuanto hemos dicho, se infiere que
los gases reales a muy bajas presiones se comportan de forma muy similar
a como lo hace un gas ideal,
por lo que, en estas circunstancias, la ecuacin de Clapeyron constituye una excelente
aproximacin a la ecuacin trmica de estado de los gases reales.
2.3. Densidad de un gas perfecto. Densidad relativa al aire.- En la
ecuacin [2.17] se puede hacer aparecer la masa m del gas, sin ms que tener en
cuenta que n=m/M, siendo M la masa molecular del mismo; i.e.,
pV
m
RT
M
[2.18]
Esta ecuacin puede escribirse en trminos de densidad del gas () sin ms que tener
presente la definicin de sta, i.e., =m/V, de modo que
pM
RT
[2.19]
En algunas ocasiones es conveniente considerar la densidad relativa (rel) de un
gas respecto de otro que se toma como referencia, que generalmente es el aire. Si
designamos por a la densidad del aire, en las mismas condiciones de presin y
temperatura que el gas que se considere, y por Ma la masa molecular media del
mismo (aproximadamente 28.8 g/mol), y admitimos un comportamiento ideal para
ambos gases, se sigue inmediatamente que
rel
M
Ma
[2.20]
de modo que la densidad relativa depende nicamente del peso molecular del gas, lo
que constituye una consecuencia inmediata de la ley de Avogadro.
2.4. Mezcla de gases perfectos no reaccionantes. Ley de Dalton.Consideremos una mezcla de N gases perfectos e inertes, que ocupan un volumen V
a una temperatura T, y sea p la presin total de la mezcla. Designaremos por pi la
presin parcial correspondiente al gas i-simo, definida como la que ejercera el
componente i-simo de la mezcla si estuviese l slo ocupando todo el volumen de
la mezcla, a la temperatura a la que sta se encuentra. Evidentemente, por tratarse de
un gas perfecto, se cumplir
piV
ni RT
(i
1, 2, ... , N)
siendo ni el nmero de moles del componente i-simo.
[2.21]
51
2.4.- Mezcla de gases perfectos no reaccionantes. Ley de Dalton.
Nuestro objetivo es establecer una relacin entre las presiones parciales (pi, con
i=1,2,...,N) y la presin total de la mezcla (p). Para conseguirlo, sumaremos miembro
a miembro las N ecuaciones [2.21] y obtendremos
N
pi V
i 1
N
ni RT
i 1
[2.22]
Puesto que los componentes de la mezcla son gases no reaccionantes, la ec. [2.17]
puede aplicarse a la mezcla en su conjunto, tenindose
N
ni RT
i 1
pV
[2.23]
cuyo segundo miembro coincide con el de [2.22], por lo que la identificacin de los
primeros miembros nos conduce a este importante resultado
N
p
i 1
[2.24]
pi
LEY DE DALTON.- La presin total de una mezcla de gases ideales no
reaccionantes es la suma de las presiones parciales de sus componentes.
Dividiendo miembro a miembro las ecuaciones [2.21] y [2.23] y despejando pi,
obtenemos
pi
ni
ni
i p
con i
ni
[2.25]
ni
donde i representa la fraccin molar3 del componente i-simo en la mezcla. La
ecuacin [2.25] expresa que
la presin parcial de cualquier componente es proporcional a su fraccin
molar en la mezcla,
siendo la presin total la constante de proporcionalidad.
Ejemplo II.- Una mezcla de nitrgeno (N2) y oxgeno (O2) con una composicin porcentual en peso
del 40% de nitrgeno, se encuentra a una temperatura de 270 C y est sometida a una presin de
700 mmHg. a) Determinar la presin parcial de cada gas en la mezcla. b) Determinar la densidad
de la mezcla en las condiciones consideradas.
a) Obtendremos en primer lugar la fraccin molar de cada gas. Teniendo en cuenta las masas
moleculares del N2 (28 g/mol) y del O2 (32 g/mol), el nmero de moles de N2 y de O2 en 100 g
de mezcla, ser
n (N2)
40 g
28 g/mol
1.429 moles de N2
n (O2)
60 g
32 g/mol
1.875 moles de O2
Obsrvese que la suma de las fracciones molares de todos los componentes de la mezcla es
igual a la unidad.
52
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
El nmero total de moles en 100 g de mezcla ser n=n(N2)+n(O2)=3.304 moles; por tanto, las
correspondientes fracciones molares sern
(N2)
n(N2)
n
1.429
3.304
0.4325
(O2)
(N2)
0.5675
Las correspondientes presiones parciales sern
p (N2)
(N2) p
302.75 mmHg
p(O2)
(O2) p
p(N2)
397.25 mmHg
b) La ecuacin de Clapeyron nos permite obtener el volumen correspondiente a una masa de
100 g de mezcla. Habida cuenta de que T=543.15 K y p=700/760 atm, se tiene
V
nRT
p
3.3040.08205543.15
700/760
m
V
100
159.77
0.626
159.77 L
g
L
2.5. Superficies PVT de un gas ideal.- Dado que la ecuacin termodinmica
de estado para una masa fija de gas es una relacin entre las tres variables p, V y T,
dicha relacin define una superficie en el espacio termodinmico (p,V,T), llamada
superficie caracterstica, correspondiendo un punto de esa superficie a cada estado
de equilibrio del sistema. En consecuencia, en cualquier proceso que implique una
evolucin del sistema a travs de una sucesin de estados de equilibrio, el punto
representativo del estado del sistema en el espacio termodinmico se mueve sobre
una curva contenida en la superficie caracterstica.
Para un gas ideal, la superficie caracterstica es un paraboloide hiperblico
rectangular, asinttico a los planos coordenados (p,T) y (V,T), del que se ha
representado una seccin en la Figura 2.5a. Los procesos isotermos corresponden a
intersecciones de los planos T=cte. con la superficie caractersticas, resultando
hiprbolas equilteras cuyas proyecciones sobre el plano (p,V) se muestran en la
Figura 2.5b. Anlogamente, las intersecciones de los planos V=cte. con la superficie
caracterstica corresponden a procesos isocoros que vienen representados por lneas
rectas cuyas proyecciones sobre el plano (p,T) se refleja en la Figura 2.5c. De la misma
forma, los procesos isobaros (p=cte.) estn representados por rectas sobre la
superficie caracterstica.
2.6. Gases reales.- Hemos dicho anteriormente que los gases reales slo
obedecen la ecuacin de Clapeyron, con suficiente aproximacin, en el dominio de
las bajas presiones. Cuando se eleva la presin, el comportamiento de los gases reales
puede ser muy diferente del de los gases ideales; las discrepancias son tan notables
que no pueden pasarse por alto. De ah proviene el inters en el estudio de los gases
reales que, por otra parte, proporciona valiossima informacin acerca de la estructura
molecular de la materia y de la naturaleza de las fuerzas intermoleculares.
Cuando un gas perfecto se comprime isotrmicamente, contina siendo gas por
muy grande que sea la presin a la que se le someta; su volumen disminuye
2.6.- Gases reales.
53
Figura 2.5.- Superficie pVT para el gas ideal.
continuamente al aumentar la presin, de acuerdo con la ley de Boyle-Mariotte. Por
el contrario, los gases reales no se comportan de ese modo y pueden pasar al estado
lquido por compresin, siempre que su temperatura no sea muy alta.
A fin de obtener informacin acerca de las discrepancias en el comportamiento
de gases ideales y reales, vamos a considerar la experiencia llevada a cabo en
1869 por el cientfico ingls Thomas ANDREWS (1813-1885) con dixido de carbono,
consistente en estudiar a temperatura constante las variaciones del volumen molar de
dicho gas en funcin de la presin a la que estaba sometido.
Andrews comprimi 1 mol de CO2 en un tubo de paredes transparentes y midi
simultneamente la presin (p) y el volumen (v). Al comienzo de la experiencia, el
estado del sistema est representado por el punto A en el diagrama p-v de la Figura 2.6
corresponde a la posicin inicial del mbolo. A continuacin, el mbolo se desplaza
lentamente hacia la izquierda, comprimindose el gas encerrado en el cilindro. Al
principio, se observa que el volumen del gas disminuye mucho y que el punto
representativo del estado del mismo recorre el arco AB, mantenindose prcticamente
constante el producto pv.
Cuando se alcanza el estado representado por el punto B, al que corresponde una
cierta presin pv, si se contina disminuyendo el volumen mediante el movimiento
del mbolo, se observa que la presin indicada por el manmetro permanece
constante y que, al mismo tiempo, comienzan a aparecer gotas de lquido sobre las
54
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
paredes del tubo; i.e., se ha iniciado la
condensacin (licuacin) del gas,
convirtindose ste en vapor saturante.
Si continuamos desplazando el
mbolo hacia la izquierda, la cantidad
de fase lquida aumenta sin que la
presin vare (pv, presin de vapor
saturante), ya que al ser el volumen
molar del lquido ms pequeo que el
del vapor, el volumen de la mezcla va
disminuyendo a medida que progresa la
condensacin y as contina el proceso
mientras quede algo de gas. En consecuencia, la curva de evolucin isotrmica presenta un tramo horizontal
isbaro, denominado tramo de licuaFigura 2.6.- Experiencia de Andrews.
cin (tramo BD).
Una vez alcanzado el punto D,
todo el sistema se encuentra en el estado lquido y, como los lquidos son poco
compresibles, ser necesario un aumento muy grande de la presin para reducir
apreciablemente el volumen, por lo que en esta zona, correspondiente al estado
lquido, las curvas isotermas presentarn una gran pendiente.
Cuando se repite la experiencia de Andrews para una
misma masa gaseosa a diferentes temperaturas T1, T2, ...
crecientes, se obtiene una red
de isotermas como la que se
muestra en la Figura 2.7, donde
puede apreciarse que el comportamiento del gas es el
mismo que se ha descrito en
el prrafo anterior, con la
nica diferencia de que el
tramo de licuacin es cada
vez ms corto, conforme la
temperatura es ms alta. Para
una cierta temperatura TC
(30.9 C, para el CO2), el
intervalo de equilibrio lquido-vapor se reduce a un punto
Figura 2.7.- Isotermas de un gas real.
de inflexin con tangente
horizontal, que Andrews denomin punto crtico (PC),
siendo sus coordenadas las llamadas coordenadas crticas del gas. La isoterma que
pasa por ese punto se llama isoterma crtica.
55
2.6.- Gases reales.
En las proximidades del punto crtico, no se distingue el menisco de separacin
entre las fases lquida y vapor, pues ambas tienen densidades muy prximas que se
hacen idnticas en el punto crtico. Para temperaturas superiores a la crtica, toda
disminucin de volumen va siempre acompaada por un aumento de presin y el gas
no puede licuarse por simple compresin, por muy elevadas que sean las presiones
a las que se le someta.
As pues, vemos que tenemos establecida una diferencia entre gases y vapores,
que no es una diferencia de estado de agregacin, sino de estado termodinmico,
siendo vapor la fase gaseosa correspondiente a temperaturas inferiores a la
crtica y gas la correspondiente a temperaturas superiores a sta.
Tambin queda patente que para licuar un gas es necesario enfriarlo previamente
a temperaturas inferiores a la crtica y luego comprimir el vapor.
Los resultados indicados anteriormente son completamente generales, de modo
que cualquier gas real presenta una red de isotermas de aspecto anlogo a la del
dixido de carbono.
Por consiguiente, podemos afirmar que las isotermas de los gases reales son de
dos tipos, segn que la temperatura sea inferior o superior a la temperatura crtica:
en el primer caso, existe un tramo horizontal que corresponde a la transicin
vapor-lquido; en el segundo caso, las isotermas se aproximan cada vez ms a la
forma hiperblica equiltera y el gas obedece aproximadamente a la ley de BoyleMariotte, tanto mejor cuanto mayor es su temperatura. As pues, podemos afirmar que
Tabla 2.1.- Coordenadas crticas de algunos gases.
gas
aire
Tc (K)
132.4
pc (atm)
37.2
vc (cm3/mol)
92.4
acetileno (C2H2)
30.9
61.6
amonaco (NH3)
405.5
111.3
butano (C4H10)
425.
37.5
dixido de azufre (SO2)
430.7
77.8
122.
dixido de carbono (CO2)
304.1
72.9
94.
helio (He)
5.19
113.
72.5
2.26
58.
hidrgeno (H2)
33.3
12.80
65.
metano (CH4)
190.7
45.8
99.
monxido de carbono (CO)
132.9
34.5
93.
nitrgeno (N2)
126.2
33.5
90.
oxgeno (O2)
154.8
50.1
78.
propano (C3H8)
370.
42.
vapor de agua (H2O)
647.4
218.3
vapor de mercurio (Hg)
1900.
3554.
56.
40.
56
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
un gas se acerca tanto ms al estado perfecto cuanto ms alejado se encuentra de su
temperatura crtica, cuyo valor depende de la naturaleza del gas, como puede
apreciarse en la Tabla 2.1, donde tambin figuran los valores de la presin crtica y del
volumen molar crtico para diferentes gases.
El lugar geomtrico de los puntos extremos de los tramos de licuacin es una
curva con vrtice en el punto crtico, tal como se ha representado con trazo
discontinuo en la Figura 2.7. Esta curva, llamada curva lmite de saturacin, delimita
una regin del plano (p,v) donde coexisten las fases lquida y gaseosa, denominada
zona de mezcla. En esta zona, en un punto tal como el C (en la Figura 2.7), las dos
fases estn en equilibrio, siendo sus volmenes molares respectivos los correspondientes a los puntos B y D, situados en los extremos del tramo de licuacin que pasa
por el punto C.
Para establecer la relacin existente entre las masas de las fases coexistentes en el punto C,
designaremos por n1 el nmero de moles de lquido en el estado representado por el punto C, de
modo que su volumen ser n1vD, siendo vD el volumen molar del sistema en el estado D. Como
estamos considerando un mol de sustancia, el nmero de moles de vapor ser (1-n1), y su
correspondiente volumen ser (1-n1)vB, siendo vB el volumen molar en el punto B. El volumen
molar en C, i.e., vC, ser la suma de los volmenes de ambas fases, o sea
vC
n1 vD
(1
n1) vB
vB
vC
n1 (vB
v D)
[2.26]
Ahora bien, vB-vC es la longitud del segmento CB, y lo mismo ocurre con vB-vD, que
corresponde al segmento DB. As pues, la ecuacin [2.26b] queda en la forma
CB
n1 DB
[2.27]
De manera anloga, escribiendo [2.26a] en funcin de n2=1-n1, se sigue
DC
n2 DB
[2.28]
y, dividiendo miembro a miembro las expresiones [2.27] y [2.28], se obtiene finalmente que
n1
CB
m1
n2
DC
m2
[2.29]
siendo m1 y m2 las respectivas masas de lquido y vapor en el punto C. La relacin anterior
establece que las masas de las fases en equilibrio estn en relacin inversa con las longitudes de
los segmentos determinados por el punto representativo del estado de la mezcla en el tramo de
licuacin (ley de la palanca). En B, toda la masa se encuentra en estado gaseoso; en tanto que en
D, toda la masa est en estado lquido.
El examen del diagrama de las isotermas de Andrews nos permite enunciar la
continuidad de los estados lquido y gaseoso. Es posible hacer pasar una masa fluida
desde un estado representado por el punto B (Figura 2.7) hasta el estado lquido representado por el punto D, sin que la licuacin se manifieste por la aparicin de una
fase distinta, como ocurrira si el sistema evolucionase a lo largo de la isoterma que
pasa por los puntos B y D. Para conseguirlo, bastar con hacer que la masa fluida
evolucione a lo largo de la lnea BMND, como se indica en la Figura 2.7. Tal
evolucin consiste en un calentamiento isocrico del vapor para pasarlo a gas a una
temperatura superior a la crtica (tramo BM), seguido de una compresin isotrmica
(tramo MN) y de un enfriamiento isocrico (tramo ND). En este ltimo proceso, el
sistema pasa del estado N (gas) al estado D (lquido) sin perder homogeneidad, ya
2.6.- Gases reales.
57
que al cruzar la isoterma crtica en el punto Q se pasa sin transicin alguna a la
isoterma de lquido inmediatamente inferior, de tal forma que ninguna de las variables (p,v,T) interesadas en la transformacin del gas en lquido presenta un comportamiento irregular que ponga de manifiesto el cambio de estado de agregacin.
En el diagrama de la Figura 2.7 se pone
tambin de manifiesto que para cada temperatura inferior a la crtica existe una nica presin
para la que existe equilibrio entre las fases
lquida y gaseosa. A esa presin se le llama
presin de vapor saturante, y a ella nos volveremos a referir en la leccin que dedicaremos al
estudio de los cambios de fase. De momento,
slo diremos que los valores de las presiones de
vapor saturante y sus correspondientes temperaFigura 2.8.- Curva de presin de vapor
turas definen una curva en el plano (p,T) que,
saturante.
como se infiere de la Figura 2.7, est limitada
superiormente en el punto crtico; con otras
palabras, las curvas de presin de vapor en funcin de la temperatura no son
indefinidas, sino que terminan en un punto cuyas coordenadas corresponden a la
presin y a la temperatura del punto crtico (Figura 2.8).
En relacin con lo dicho en el prrafo anterior, hay un aspecto que conviene
exponer. Cuando un gas est mezclado con vapor de agua, se dice que est hmedo.
Si el gas est saturado de vapor de agua, la presin parcial del vapor de agua en la
mezcla es igual a la presin de vapor saturante (pv) correspondiente a la temperatura
de la mezcla; en caso contrario, si la cantidad de vapor de agua slo representa un
porcentaje s de la correspondiente a la saturacin, la presin parcial del vapor de
agua en la mezcla ser (s/100)pv.
2.7. Determinacin de las coordenadas crticas. Tubos de Natterer.- La
determinacin de las coordenadas del punto crtico puede efectuarse mediante los
llamados tubos de Natterer que son unos tubos de vidrio, de paredes muy resistentes
para evitar que estallen al calentarlos. Supongamos que estos tubos contienen un gas
parcialmente licuado. Uno de los tubos (a) contiene poco lquido y mucho gas; i.e.,
la fraccin de lquido es pequea de modo que el punto correspondiente a la mezcla
(A1) est situado a la derecha del punto crtico (Figura 2.9). Al calentar el tubo, y
habida cuenta de la pequea dilatacin del vidrio, podemos admitir que el volumen
del sistema permanece constante; as pues, el sistema evolucionar siguiendo una
trayectoria vertical (proceso iscoro) desde el estado A1 al estado A2, pasando
totalmente al estado gaseoso al alcanzar este ltimo punto.
Si repetimos la experiencia con otro tubo (b), en el que la fraccin de lquido sea
importante, de modo que el punto representativo del estado del sistema (B1) est
situado a la izquierda del punto crtico, al elevar la temperatura aumentar el
volumen de la fase lquida y, antes de alcanzarse la temperatura crtica, todo el tubo
aparecer ocupado por el lquido (Figura 2.9).
Procediendo por tanteo, podemos preparar un tubo (c) con las proporciones
adecuadas de lquido y de gas, de tal suerte que el proceso de calentamiento se
realice a lo largo de la vertical C1C que pasa por el punto crtico. Al calentar este
58
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
tubo, el menisco que separa las dos
fases permanece prcticamente
estacionario, persistiendo las fases
lquida y gaseosa hasta que se
alcanza la temperatura crtica. Al
aproximarnos a la temperatura
crtica, se observa que la superficie
de separacin entre las dos fases se
va difuminando. Cuando se alcanza
la temperatura crtica, dicha superficie desaparece por completo y el
sistema presenta un aspecto
homogneo. Esto se debe a que la
densidad del vapor crece con la
temperatura, contrariamente a lo
que ocurre con la del lquido, hasta
alcanzarse el punto crtico; en ese
momento desaparecen todas las
Figura 2.9.- Experiencia de los tubos de Natterer.
diferencias entre las dos fases. En
las proximidades del punto crtico,
poco antes de la desaparicin del menisco, ste es muy movible, como si estuviese
en equilibrio inestable, y el fluido aparece afectado de una turbidez que se conoce
con el nombre de opalescencia crtica, debida a las fluctuaciones en el ndice de
refraccin provocadas por las variaciones de densidad en las fases lquidas y de
vapor, que se van acercando a la densidad correspondiente al punto crtico, y que
desaparece en el momento en que se supera la temperatura crtica (TC). La
opalescencia crtica reaparece al enfriar por debajo de la temperatura crtica; de este
modo es posible determinar con gran precisin el valor de esa temperatura.
El conocimiento del volumen del tubo y de la masa de fluido que contiene
permitiran, en principio, determinar el volumen crtico vC; sin embargo, el calibrado
del volumen de los tubos resulta difcil, recurrindose a mtodos indirectos que
determinan la densidad crtica y a partir de ella se obtiene vC. En cuanto a la presin
crtica (pC), sta no puede ser determinada mediante los tubos de Natterer; lo que se
hace es estudiar la variacin con la temperatura de la presin de vapor saturante del
fluido, se representan grficamente los resultados y, a partir de estas curvas experimentales, se deduce el valor de pC, extrapolando si fuese preciso.
De cuanto hemos dicho en los prrafos anteriores, podemos extraer las siguientes
conclusiones:
1.- En el punto crtico, los estados lquido y gaseoso se confunden en uno
slo, pasndose de un estado a otro de una forma continua.
2.- A medida que un lquido se aproxima a su punto crtico, su tensin
superficial disminuye rpidamente, hasta anularse en dicho punto.
2.8. Ecuacin de estado de Clausius.- La ecuacin trmica de estado de
los gases perfectos no da cuenta de los fenmenos de licuacin, puesto que no
proporciona las curvas isotermas angulosas que suministra la experiencia para
temperaturas inferiores a la crtica. Entonces, se plantea el problema de introducir una
59
2.8.- Ecuacin de estado de Clausius.
ecuacin que, adems de traducir con mayor fidelidad el comportamiento de los gases
reales alejados de las condiciones de licuacin, sea aplicable al intervalo de
condensacin y al estado lquido. En la actualidad, no se dispone de ninguna
expresin que satisfaga plenamente tan ambiciosas aspiraciones; pero, entre las
numerossimas que se han ideado (Kamerling Onnes, Van der Waals, Clausius,
Berthelot, Dieterici, ..., etc), la que mejor se adapta "cualitativamente" a los
fenmenos observados es la ecuacin de Van der Waals, aunque deja mucho que
desear en la interpretacin "cuantitativa" de esos fenmenos.
El fsico alemn Rudolf J. E. CLAUSIUS (1822-1888) introdujo una modificacin
en la ecuacin de Clapeyron, arguyendo que el volumen que se ha de considerar en
la ecuacin de estado no es el volumen del recipiente que contiene el gas, sino el
volumen til para las molculas; i.e., el volumen disponible para el movimiento de
las molculas. Dicho volumen debe ser menor que el del
recipiente, ya que las molculas ocupan de por s un
cierto volumen. La evaluacin de esta correccin puede
realizarse del modo que explicamos a continuacin.
Imaginemos que en un instante quedasen fijas todas
las molculas constituyentes de una masa gaseosa,
excepto una, que continuara movindose entre las otras
y chocando con ellas. Si consideramos las molculas
como esferas de radio r, la distancia entre los centros de
Figura 2.10.- Esfera de
dos molculas en el momento en que chocan es de 2r
exclusin.
(Figura 2.10). Por consiguiente, el centro de la molcula
mvil queda excluido de un volumen esfrico de radio
2r, denominado esfera de exclusin. Sin embargo, puesto que tan slo la semiesfera
que se enfrenta a la molcula mvil es eficaz para excluir a sta ltima, tomaremos
la mitad del volumen de las esferas de exclusin de todas las molculas como
volumen no efectivo para una molcula mvil cualquiera.
El nmero de molculas en un mol de gas es igual al nmero de Avogadro (NA);
de modo que el volumen no disponible por mol, que designaremos por b, es
b
1
4
N
(2r)3
2 A 3
4 N A r 3
3
[2.30]
llamada tambin covolumen. Puesto que el volumen total de un mol de molculas
esfricas de radio r es (4/3)r3NA, la ecuacin anterior indica que el covolumen es
cuatro veces el volumen molecular total en un mol.
El volumen disponible para el movimiento de las molculas es v-b (v, volumen
molar), siendo ste el volumen a considerar en la ecuacin de estado, que queda en
la forma
p (v
b)
RT
pv
T
pb
T
[2.31]
que es la ecuacin de estado de Clausius, que se escribe en la forma
p (V
nb)
nRT
[2.32]
60
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
para n moles de gas, como puede deducirse fcilmente de [2.31] sin ms que poner
v=V/n, siendo V el volumen total ocupado por el gas.
Obviamente, la correccin introducida por Clausius en la ecuacin de estado de
los gases ser tanto ms necesaria cuanto menor sea el volumen molar; i.e., cuanto
mayor sea la presin a que se haya sometido el gas.
De la ecuacin [2.31] se infiere que pV/T, a temperatura constante crece
linealmente cuando aumenta la presin. As, esta ecuacin responde, al menos
cualitativamente, a parte del comportamiento de los gases reales reflejado en la
Figura 2.4. Nos referimos concretamente a las curvas o a los tramos de curvas que
exhiben una pendiente positiva; i.e., a las curvas situadas por encima de la recta
horizontal correspondiente al gas ideal y a los tramos crecientes de las curvas que
exhiben inicialmente una disminucin de pv/T con p.
2.9. Ecuacin de estado de Van der Waals.- La interpretacin de los
tramos decrecientes de las curvas aludidas en el apartado anterior exige introducir una
nueva correccin en la ecuacin [2.31], que fue establecida en 1873 por Van der
Waals4, retomando una idea de Laplace, al considerar las fuerzas debidas a las
interacciones intermoleculares.
Entre las molculas existe una fuerza de
atraccin gravitatoria que se manifiesta entre
cualquier pareja de ellas; sin embargo, estas
fuerzas son demasiado dbiles como para que
puedan explicar las divergencias observadas
entre los gases ideales y los reales, as como el
hecho de que todos los gases se licuen cuando
se les comprime suficientemente a temperaturas
inferiores a la crtica.
La explicacin de estos hechos exige el
reconocimiento de la existencia de fuerzas
intermoleculares de naturaleza electromagntica, las llamadas fuerzas de Van der Waals,
Figura 2.11.- Johanes Diderik VAN DER
mucho ms intensas que las fuerzas gravitaWAALS (1837-1923).
torias, pero de muy corto alcance (del orden de
algunos dimetros moleculares). Cuando la
separacin entre las molculas es muy pequea, tales fuerzas dejan de ser atractivas
para convertirse en repulsivas. En la Figura 2.13, hemos representado la intensidad de
la fuerza de interaccin intermolecular en funcin de la distancia (r) de separacin
entre las molculas; observaremos que la fuerza pasa de ser atractiva (negativa) a ser
repulsiva (positiva) para distancias de separacin inferiores a r0. Tambin hemos
representado la energa potencial (Ep) asociada con cada pareja de molculas (lnea
de trazos) en funcin de la distancia r; recordemos que entre la fuerza y la energa
potencial existe la relacin F=-dEp/dr.
Johanes Diderik VAN DER WAALS (1837-1923); fsico holands. Galardonado con el Premio
Nobel de Fsica en 1910 por sus trabajos sobre la ecuacin de estado de los gases.
2.9.- Ecuacin de estado de Van der Waals.
61
Supongamos que las fuerzas intermoleculares sean
de tan corto alcance que solamente acten entre una
molcula y sus vecinas ms prximas (esfera de
influencia). En estas condiciones, las molculas situadas en el interior de la masa gaseosa sern atradas por
igual, en trmino medio, en todas las direcciones; pero
las molculas situadas en zonas perifricas experimentarn una atraccin unilateral procedente de las
dems molculas prximas. Esto es, el efecto neto de Figura 2.13.- Fuerzas intermoleculares.
las fuerzas de interaccin es nulo sobre cada molcula
situada en el interior de la masa gaseosa; pero sobre
las molculas situadas junto a las paredes la fuerza
resultante est dirigida hacia el interior de la masa gaseosa,
lo que provoca una disminucin de la velocidad de las
molculas en las zonas perifricas (Figura 2.12). Por consiguiente, para invertir la cantidad de movimiento de las
molculas que chocan contra las paredes del recipiente (que
en algunos casos ser la superficie libre del mercurio en un
manmetro), la fuerza dirigida hacia dentro que tienen que
ejercer aqullas ser menor que la calculada para un gas
Figura 2.12.- Concepto de
ideal.
sobrepresin.
As pues, las fuerzas intermoleculares atractivas dan
lugar a una reduccin en la presin que, en su ausencia (gas
ideal), se ejercera sobre las paredes del recipiente. En definitiva, la presin real o
verdadera en el seno de la masa gaseosa se calcular sumando a la presin observada
en la periferia (debida a los impactos moleculares sobre la membrana manomtrica)
un trmino correctivo que se denomina sobrepresin. Como la fuerza atractiva que
acta sobre una molcula determinada en el seno de la masa gaseosa es proporcional
al nmero de molculas por unidad de volumen, la presin tambin lo ser; pero sta,
a su vez, es proporcional a la frecuencia de choque de las molculas contra las
paredes del recipiente, la cual tambin es proporcional al nmero de molculas por
unidad de volumen. En consecuencia, podemos afirmar que la sobrepresin es
proporcional a (N/V)2, siendo N el nmero de molculas en el sistema y V el volumen
ocupado por ste. Si consideramos un mol de gas, la proporcionalidad de la
sobrepresin ser respecto del trmino (NA/v)2, de modo que sta podr escribirse de
la forma a/v2, donde a es un parmetro que depende de la intensidad de las fuerzas
intermoleculares y que vara de una sustancia gaseosa a otra.
El trmino de sobrepresin vara ampliamente, incluso para una misma sustancia gaseosa,
dependiendo de las condiciones de presin y temperatura. As, para el aire a 20 C y 1 atm, la
sobrepresin vale 0.0028 atm; en tanto que a 0 C y 100 atm, vale 26 atm; y a -75 C y 100 atm,
su valor es de 84.5 atm.
Teniendo en cuenta la correccin de Clausius para el volumen y la correccin de
Van der Waals para la presin, la ecuacin trmica de estado para el sistema queda
en la forma
p
a
(v
v2
b)
RT
[2.33]
62
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
que es la ecuacin de estado de Van der Waals.
Los valores de a y b pueden obtenerse experimentalmente. Se comprueba que el
parmetro b es del orden de 0.03 L/mol, con poca variacin de un gas a otro. Por el
contrario, el valor del parmetro a vara ampliamente de unas sustancias a otras. En
la Tabla 2.2 hemos indicado los valores de estos parmetros para algunos gases.
Para el caso de n moles de gas, la ecuacin de Van der Waals queda en la forma
an 2
(V
V2
nb)
[2.34]
nRT
siendo V el volumen total del sistema.
Para gases de baja densidad, i.e., a bajas presiones, la correccin de volumen de
la ecuacin de Van der Waals puede ser despreciada, reducindose sta a
p
a
v
v2
RT
pv
T
a
vT
[2.35]
lo que indica que, para una temperatura determinada, el trmino pv/T es menor que
R, disminuyendo a medida que aumenta la presin, ya que esto implica una
disminucin de v y, por consiguiente, un aumento del trmino a/vT. De esta forma
queda explicado el tramo decreciente en las curvas de la Figura 2.4, que no poda
justificarse mediante la ecuacin de Clausius. Por el contrario, cuando la presin es
elevada, el trmino de sobrepresin puede despreciarse frente a la presin, con lo que
la ecuacin de Van der Waals se reduce a la de Clausius.
Tabla 2.2. Parmetros de Van der Waals para algunos gases.
gas
a (atm L2/mol2)
b (L/mol)
aire
1.33
0.036
acetileno (C2H2)
4.39
0.051
amonaco (NH3)
4.17
0.037
anhdrido carbnico (CO2)
3.59
0.043
anhdrido sulfuroso (SO2)
6.71
0.056
argn (Ar)
1.35
0.037
cloro (Cl)
6.50
0.056
helio (He)
0.034
0.024
hidrgeno (H2)
0.24
0.027
metano (CH4)
2.25
0.043
monxido de carbono (CO)
1.49
0.040
nitrgeno (N2)
1.39
0.039
oxgeno (O2)
1.36
0.032
vapor de agua (H2O)
5.46
0.030
2.9.- Ecuacin de estado de Van der Waals.
63
Debemos entender que las correcciones introducidas en la ecuacin trmica de
estado del gas ideal para obtener la ecuacin de Van der Waals son muy simples. El
hecho de que esta ecuacin conduzca a resultados errneos, en algunos casos, es una
prueba fehaciente de que los supuestos de partida son demasiado simplificadores en
tales casos. No obstante, y por el momento, no se conoce ninguna frmula simple
que se pueda aplicar a todos los gases y en todas las condiciones.
2.10. Isotermas de Van der Waals.- Reescribiremos la expresin [2.33] en la
forma
RT
v b
a
v2
[2.36]
para obtener una relacin explcita entre la presin y el volumen cuando la
temperatura permanece constante. Esta expresin constituye la ecuacin de las
isotermas de Van der Waals, cuya representacin en el diagrama (p-v), para el
dixido de carbono (CO2) y varias temperaturas, superiores e inferiores a la
temperatura crtica (TC = 304 K), se muestra en la Figura 2.14.
Como puede verse, no se
trata de hiprbolas equilteras,
como ocurra con el gas ideal,
y la comparacin con la red de
isotermas experimentales de la
Figura 2.7 nos permite afirmar
que las previsiones tericas de
la ecuacin de Van der Waals
estn en buen acuerdo (al
menos cualitativamente) con
los resultados experimentales,
siempre que la temperatura del
gas sea superior a la crtica.
Sin embargo, para temperaturas inferiores a la crtica,
las isotermas de Van der
Waals difieren considerablemente de las isotermas de Andrews; la diferencia estriba
Figura 2.14.- Isotermas de Van der Waals.
fundamentalmente en que las
isotermas de Van der Waals no
reproducen el tramo horizontal (tramo de licuacin) de las isotermas de Andrews, que
aparece sustituido por una ondulacin; en cambio, existe un buen acuerdo en las
regiones correspondientes al lquido y al vapor.
La ecuacin de Van der Waals no responde en la regin de equilibrio de lquidovapor y, por tanto, no gobierna completamente el comportamiento de los gases reales.
No obstante, consideraciones termodinmicas indican que el tramo ondulado de las
isotermas de Van der Waals debe ser sustituido por un tramo rectilneo, paralelo al
eje v, situado de tal manera que delimite reas iguales con cada una de las ramas de
64
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
dicho tramo ondulado (zonas sombreadas en la Figura 2.14). Procediendo de esta forma,
se encuentra que las intersecciones del tramo rectilneo sustitutorio de la ondulacin
con la isoterma de Van der Waals corresponde a puntos de la curva lmite de
saturacin.
2.11. La ecuacin de Van der Waals y las coordenadas crticas.- Vamos
a centrar ahora nuestra atencin en la determinacin de las coordenadas crticas de
un sistema gobernado por la ecuacin de Van der Waals. Para ello, debemos recordar
que el punto crtico representa un punto de inflexin en el diagrama de Clayperon;
por consiguiente, debern ser nulas en dicho punto las derivadas primera y segunda
de la presin con respecto al volumen, a temperatura constante, esto es
2
p
2
v T
p
v T
[2.37]
Estas derivadas se obtienen fcilmente a partir de la expresin [2.36];
p
v T
2
p
2
v T
R TC
(vC
2a
2
b)
2R TC
(vC
6a
b)3
[2.38]
vC
4
C
[2.39]
donde el subndice C hace referencia al punto crtico. Las ecuaciones [2.38] y [2.39]
constituyen un sistema de dos ecuaciones con dos incgnitas (TC y vC) cuya
resolucin conduce a la obtencin de expresiones para estas coordenadas crticas en
funcin de los parmetros a, b y R:
vC
3b
TC
8a
27 bR
[2.40]
Sustituyendo ahora estos resultados en la expresin [2.36], obtenemos la expresin de
la presin crtica
pC
a
27 b 2
[2.41]
De las expresiones [2.40] y [2.41] se sigue inmediatamente que
pCvC
RTC
3
8
[2.42]
mientras que para el gas ideal se cumple pv/RT=1.
Las ecuaciones [2.40] y [2.42] pueden utilizarse para obtener expresiones de los
parmetros a, b y R en funcin de las coordenadas crticas, que como ya sabemos
pueden ser determinadas experimentalmente. Estas expresiones son las siguientes:
2.11.- La ecuacin de Van der Waals y las coordenadas crticas.
9
R vCTC
8
3 pCvC
vC
8 pCvC
3 TC
65
[2.43]
las cuales nos permiten establecer unos baremos de comparacin de la ecuacin de
Van der Waals con los valores experimentales de estos parmetros. La conclusin es
que la ecuacin de estado de Van der Waals no es aplicable en la regin prxima al
punto crtico, ya que las discrepancias que se observan son del orden del 30%.
2.12. Otras ecuaciones de estado.- Aparte de la ecuacin de Van der
Waals, se han propuesto un gran nmero de ecuaciones de estado para gobernar el
comportamiento de los gases reales; aunque ninguna de ellas ha conseguido
plenamente ese objetivo. Sera muy prolijo y casi imposible enumerarlas todas, por
lo que nos limitaremos a comentar brevemente las ms utilizadas.
a) Ecuacin de Berthelot.- En esta ecuacin, debida al qumico francs Marcelin
Pierre Eugne BERTHELOT (1827-1907), se pone explcitamente de manifiesto que las
interacciones moleculares son funcin de la temperatura, escribindose el trmino de
sobrepresin en la forma a/(v2T), donde el valor del parmetro a no tiene porqu
coincidir con el de la ecuacin de Van der Waals. Para un mol de sustancia, esta
ecuacin se escribe en la forma siguiente:
a
(v
T v2
b)
RT
[2.44]
Para volmenes molares elevados, esta ecuacin se reduce a la de Van der Waals.
b) Ecuacin de Clausius.- Esta ecuacin aade a las constantes a, b y R de
Berthelot una nueva constante (c), quedando de la forma
p
a
T (v
(v
c)
2
b)
RT
[2.45]
c) Ecuacin de Dieterici.- En 1899, Dieterici propuso la siguiente ecuacin
trmica de estado
a
[2.46]
p (v b) RT exp
R
Tv
que a bajas presiones (i.e., volmenes molares elevados), se reduce a la ecuacin de
Van der Waals.
d) Ecuacin de Beattie-Bridgman5.- Esta ecuacin engloba un mayor nmero
de parmetros que las anteriores (cinco, en total), por lo que gobierna mejor el
comportamiento de los gases en un amplio margen de temperaturas y presiones;
aunque, al igual que la de Van der Waals, es inexacta en las proximidades del punto
crtico. Esta ecuacin es de la forma
Percy Williams BRIDGMAN (1882-1961); fsico estadounidense. Galardonado con el Premio
Nobel de Fsica en 1946 por sus trabajos en el campo de la Fsica de Altas Presiones.
66
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
Tabla 2.3.- Constantes de la ecuacin de estado de Beattie-Bridgman.
c 10-3
Gas
A0
He
0.216
0.01400
+0.05984
H2
0.1975
0.02096
-0.00506
-0.04359
0.00504
O2
1.4911
0.04624
+0.02562
+0.004208
0.480
CO2
5.0065
0.10476
+0.07132
+0.07235
6.600
NH3
2.3930
0.03415
+0.17031
+0.19112
47.687
B0
b
0.0
0.00040
Nota: p en atm, v en L/mol, T en K y R = 0.08205 atm L/(mol K)
RT
(1
v2
donde
A0 1
) (v
A
v2
B)
B0 1
[2.47]
c
v T3
[2.48]
siendo A0, B0, a, b y c los parmetros caractersticos para cada gas.
e) Ecuaciones de estado del virial.- En estas ecuaciones, el producto pv se
expresa en forma de desarrollo en serie de potencias, bien de p o bien de 1/v, lo que
comporta un conjunto de coeficientes indeterminados que se pueden evaluar
experimentalmente para cada gas, dentro de unos lmites determinados de presin y
temperatura, de tal suerte que el acuerdo entre los resultados que proporcionan estas
ecuaciones y los resultados experimentales sea satisfactorio.
Por otra parte, estas ecuaciones presentan la ventaja de que al ser posible la
eleccin de un nmero de trminos tan grande como se desee, se puede conseguir
que el acuerdo de la ecuacin con los resultados experimentales sea casi perfecto
mediante la adicin de trminos suplementarios. De esta forma se obtienen excelentes
ecuaciones de estado para un gas dado en las condiciones que interesen.
Estas ecuaciones fueron introducidas en 1901 por Kammerling-Onnes6; su forma
general es la siguiente
pv
o bien
pv
RT 1
RT 1
B
v
Bp
C
v2
...
[2.49]
Cp 2
...
[2.50]
Las ecuaciones de estado del virial se aplican fundamentalmente a gases con
densidades medias y bajas, al objeto de no tener que considerar un nmero
Heike KAMMERLING-ONNES (1853-1929); fsico y qumico holands. Premio Nobel de Fsica
en 1913 por sus investigaciones sobre las propiedades de los cuerpos a bajas temperaturas.
67
2.12.- Otras ecuaciones de estado.
demasiado elevado de trminos en el desarrollo en serie; en caso contrario, estas
ecuaciones resultan difciles de manejar.
Los coeficientes de los desarrollos expresados en las ecuaciones [2.49] y [2.50] se
denominan coeficientes del virial y son funcin de la temperatura; de entre todos
ellos, el ms importante desde el punto de vista fsico es el segundo, ya que es el que
ms caracteriza la desviacin de los gases reales respecto a los gases ideales, debido
a que, al corresponder a una potencia de primer orden y al movernos en el dominio
de densidades moderadas, los trminos de orden superior al primero pueden
despreciarse. A ttulo puramente informativo, diremos que la temperatura a la que
este coeficiente se anula se le llama temperatura de Boyle; a esta temperatura, y
siempre que se consideren presiones que permitan despreciar los trminos de orden
superior al primero, los gases ideales exhiben un comportamiento ideal. Obsrvese
que, en la temperatura de Boyle, en las condiciones antedichas, los desarrollos [2.49]
y [2.50] se reducen a la ecuacin de estado de los gases perfectos.
Ejemplo III.- Escribir las ecuaciones del virial para un gas gobernado por la ecuacin de estado
de Berthelot.
a) De la ecuacin [2.44] despejamos el producto pv; as nos queda
RT
b
1
v
pv
a
Tv
[2.51]
y como b<v, ser b/v<1, de modo que 1/(1-b/v) representa la suma de una serie geomtrica
indefinida de razn b/v, por lo que tendremos
pv RT 1
b
v
b 2 b 3
...
v v
RT 1
a
Tv
1
v
a b 2
...
RT 2 v
[2.52]
que corresponde a la ecuacin [2.49], en la que el valor del segundo coeficiente es
B
a
RT 2
[2.53]
por lo que la temperatura de Boyle ser T= (a/bR)1/2. Para el tercer coeficiente se tiene C=b2, y as
sucesivamente.
b) En cuanto a la ecuacin del virial en trminos de la presin, la deduciremos a partir de la
ecuacin de Berthelot escrita en la forma
pv
RT
pb
a
Tv
ab
Tv 2
[2.54]
como se puede comprobar fcilmente. En esta ecuacin sustituiremos (1/v) por la expresin
aproximada que se obtiene despejando v de [2.44]; as se obtiene
v
RT
a
p
Tv 2
RT
p 1
Tv 2 p
[2.55]
68
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
Como el trmino de sobrepresin a/Tv2 es pequeo en comparacin con p, podemos desarrollar
en serie la inversa de (1+a/Tv2p), con lo que obtendremos en primera aproximacin
v
Tv 2p
RT
1
p
RT
1
p
bp
RT
a
Tv 2p
[2.56]
Como en primera aproximacin podemos considerar pv=RT, entonces
a
Tv 2p
ap
Tv 2p 2
ap
R 2T 3
]75
Si ahora introducimos esta ltima aproximacin en la expresin [2.56], invertimos el resultado as
obtenido y volvemos a desarrollar en serie, tendremos:
1
v
p
RT
bp
RT
ap
R 2T 3
[2.58]
Llevando este resultado a la expresin [2.54], resultar
pv
RT
ap
RT 2
pb
ap
R 2T 3
bp
RT
ab p 2
R 2T 3
ap
R 2T 3
b p 2
RT
[2.59]
que una vez desarrollada, limitndonos a los trminos de segundo orden, queda reducida a
pv RT 1
p
RT
RT 2
2a p 2
R 3T 4
2RT 2
[2.60]
que es la ecuacin del virial en trminos de presin y que identificada con [2.49] nos permite
establecer que
B
1
RT
RT 2
2a
R 3T 4
2RT 2
[2.61]
2.13. Ecuacin de estado reducida. Ley de los estados correspondientes.- Se definen las coordenadas reducidas asociadas a cierto estado de un gas como
el cociente entre sus coordenadas termodinmicas y los valores respectivos correspondientes a las coordenadas crticas; esto es,
pr
p
pc
vr
v
vc
Tr
T
Tc
[2.62]
El estado del sistema queda inequvocamente determinado por dos de estas
coordenadas reducidas.
Cuando se introducen las coordenadas reducidas en la ecuacin de estado
f(p,v,T)=0, se obtiene una relacin de la forma (pr,vr,Tr)=0, que se denomina
ecuacin de estado reducida, y que se caracteriza por ser una ecuacin donde no
intervienen parmetros caractersticos del sistema (i.e., los parmetros a y b de la
ecuacin de Van der Waals), por lo que dicha ecuacin tiene una validez universal,
en el sentido de que todos los gases gobernados por la misma ecuacin trmica de
estado poseen idntica ecuacin de estado reducida, independientemente de sus
69
2.13.- Ecuacin de estado reducida. Ley de los estados correspondientes.
peculiaridades. En lo que sigue, pondremos de manifiesto lo anteriormente dicho para
el caso concreto de la ecuacin de Van der Waals.
Si las expresiones de los parmetros a, b y R, dadas en [2.43], se introducen en
[2.33], se obtiene
2
3 pcvc
v2
vc
8 p cv c
T
3 Tc
[2.63]
Dividiendo los dos miembros de esta ecuacin por pcvc, tendremos
pr
3
vr
2
vr
8
T
3 r
[2.64]
donde, tal como se anunci anteriormente, ya no aparecen los parmetros a y b cuyos
valores son caractersticos de cada sustancia gaseosa.
Diremos que dos gases gobernados por la misma ecuacin de estado se
encuentran en estados correspondientes cuando poseen las mismas coordenadas
reducidas. Resulta obvio, a partir de [2.64], que
Ley de los estados correspondientes.- Si dos masas gaseosas con el mismo
nmero de moles poseen la misma presin reducida y la misma temperatura
reducida, tambin tendrn el mismo volumen reducido.
Por ejemplo, el nitrgeno a 19 C (Tr=2.3) estar en estado correspondiente con el dixido de
carbono a 427 C y con el dixido de azufre a 1032 C. Lo mismo ocurre con el dixido de azufre
a 19 C (Tr=0.68), que se corresponde con algunos gases a muy bajas temperaturas, tales como el
dixido de carbono a -66 C o el hidrgeno a -251 C.
Cuando dos gases se encuentran en estados correspondientes, tienen los mismos
coeficientes elsticos y en coordenadas reducidas, las mismas isotermas de
Andrews (tambin en coordenadas reducidas), los mismos volmenes especficos del
vapor y del lquido, ... etc. Por este motivo, y a modo de ejemplo, el estudio del
nitrgeno a 19 C da resultados que son vlidos para el dixido de azufre a 1032 C,
temperatura a la cual resulta muy difcil obtener medidas directas. De lo dicho, se
infiere claramente el inters de esta ley.
70
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
Problemas
2.1.- Una cierta masa de gas perfecto ocupa un
volumen de 250 cm3 cuando est sometido a
una presin de 770 mmHg y tiene una temperatura de 20 C. a) Determinar el volumen
que ocupara dicha masa gaseosa en condiciones normales. b) A qu temperatura ocupar un volumen de 200 cm3 a la presin normal?
2.2.- Un matraz de 2 L de capacidad, provisto
de una llave de paso, contiene oxgeno a
300 K y a la presin atmosfrica. Con la llave
abierta a la atmsfera, se calienta el sistema
hasta una temperatura de 400 K; a continuacin, se cierra la llave y se enfra el matraz
hasta la temperatura inicial. a) Cul es la
presin del oxgeno en el matraz? b) Que
masa de oxgeno quedar en el matraz?
2.3.- Un litro de helio, a 2 atm y 27 C, se
calienta hasta que su presin y volumen se
duplican. a) Cul es la temperatura final?
b) Determinar la masa de helio.
2.4.- A 20 C y 0.97105 Pa, 1.618 g de argn
ocupan el volumen de 1 L. Determinar: a) la
densidad del argn en condiciones normales y
b) su masa molecular.
2.5.- En la parte superior de la atmsfera, la
temperatura vara slo ligeramente con los
cambios de altura, por lo que podemos suponer
que la temperatura de la atmsfera sea uniforme en esta zona. Designaremos por n y n0 los
nmeros de las molculas por unidad de volumen a las alturas z y z0. a) Establecer la ley de
variacin de la densidad molecular n con la
altura z. b) Hallar la ley de variacin de la
presin en funcin de la altura. NOTA: Se
considerar el aire como si fuese un gas perfecto y se admitir que la intensidad del campo gravitatorio permanece constante en el
intervalo de alturas considerado.
2.6.- Un recipiente cerrado contiene 10 g de
nitrgeno a 12 atm y 50 C. Al cabo de un
cierto tiempo, la presin ha descendido a
5/8 de su valor inicial y la temperatura se ha
reducido a la mitad. a) Calcular el volumen
interior del recipiente. b) Determinar la masa
de nitrgeno que se ha escapado.
2.7.- Calcular el tanto por ciento en peso de
monxido de carbono contenido en una mezcla
de este gas y dixido de carbono, sabiendo que
la mezcla, a la temperatura de 50 C y presin
de 900 mmHg, tiene la misma densidad que el
oxgeno en condiciones normales.
2.8.- Demostrar que, en una mezcla de gases
perfectos no reaccionantes, el tanto por ciento
en volumen de cada gas es igual a la fraccin
molar del gas en la mezcla. Aplicar este resultado para obtener la presin parcial de los
diferentes componentes del aire a una presin
de 1 atm, considerando la siguiente composicin centesimal en volumen: nitrgeno,
78.06%; oxgeno, 21.00%; argn, 0.94%.
2.9.- Un cilindro provisto de un mbolo mvil
contiene 40 L de oxgeno a la presin de
2 atm. Si la temperatura permanece constante
y se desplaza el mbolo hasta duplicar el
volumen del gas, cul ser entonces la presin del gas?
2.10.- Una muestra de oxgeno hmedo, saturada de vapor de agua al 80%, ocupa un volumen de 486 cm3 a la presin de 790 mmHg y
a una temperatura de 20 C. Si la presin de
vapor del agua a la temperatura considerada es
17.5 mmHg, cul sera el volumen ocupado
por el oxgeno seco a 25 C y 800 mmHg?
2.11.- Una muestra de aire est saturada en un
50% con vapor de agua y se encuentra a una
temperatura de 30 C y una presin de
700 mmHg. Cul ser la presin parcial del
vapor de agua en la mezcla cuando la presin
total se reduzca a 100 mmHg? La presin del
vapor de agua a 30 C es 31.8 mmHg.
2.12.- Una cierta cantidad de aire, a 20 C y
1 atm, con una humedad relativa del 80%, se
comprime dentro de un tanque de 100 L de
capacidad hasta una presin de 6 atm, elevndose la temperatura durante el proceso
hasta 25 C. Las correspondientes presiones de
vapor del agua a 20 C y 25 C son
17.5 mmHg y 23.8 mmHg, respectivamente.
Considerando el gas como perfecto, y despreciando el volumen de agua que se condensa en
el tanque durante el proceso, calcular la masa
de la misma.
2.13.- Obtener los desarrollos del virial para la
ecuacin de estado de Van der Waals; primero,
en funcin de v; despus, en funcin de p;
71
Problemas
limitndose a los trminos de segundo orden.
Calcular numricamente los coeficientes del
virial de los desarrollos anteriores para el caso
del oxgeno a 25 C, sabiendo que los valores
experimentales de los parmetros caractersticos que intervienen en la ecuacin de Van der
Waals son los siguientes:
a
1.36
(atm L 2)
mol 2
0.032
L
mol
2.14.- Obtener los coeficientes de dilatacin
isobrico, piezomtrico y de compresibilidad
isoterma de una gas gobernado por la ecuacin
de Berthelot.
2.15.- Determinar las
correspondientes a una
ecuacin de Berthelot,
metros a, b, y R de la
aqullas.
coordenadas crticas
gas gobernado por la
expresando los parmisma en funcin de
2.16.- a) Demostrar que las constantes de la
ecuacin de Dieterici vienen dadas en funcin
de las coordenadas crticas por las expresiones
siguientes:
2
4R Tc
e 2 pc
RTc
e 2 pc
b) Calcular numricamente estas constantes
para el metano, el cual posee las siguientes
c o o rd en ad as c rtic a s : p c = 4 5.8 a tm,
vc=6.17 cm3/g y Tc= 190.95 K.
2.17.- a) Escribir la ecuacin de Dieterici para
n moles. b) Escribir esta ecuacin en forma
reducida. c) Determinar el primero y segundo
coeficientes del virial. Cul es la temperatura
de Boyle? d) Hallar una expresin para el
coeficiente de compresibilidad isotermo de un
gas gobernado por la ecuacin de Dieterici.
2.18.- La ecuacin trmica de estado para un
cierto vapor viene dada por
p (v
C)
RT
A
T
donde A y C son constantes caractersticas del
sistema y R es la constante de los gases perfectos. Hallar el coeficiente de dilatacin
isobrico en funcin de A, C, R y T.
2.19.- Los coeficientes de dilatacin isobrica
y de compresibilidad isotermo de cierto gas
vienen dados por las expresiones
b
vT
b
pv
siendo v el volumen molar y b una constante
caracterstica del gas. a) Determinar la ecuacin trmica de estado del gas, sabiendo que el
gas se comporta idealmente para valores altos
del volumen molar. b) Escribir la ecuacin
obtenida en el apartado anterior para n moles.
c) Escribir esa ecuacin en forma de desarrollo
del virial.
2.20.- Admitiendo que tanto el agua como el
dixido de carbono obedezcan a la misma
ecuacin trmica de estado y que, en esas
condiciones, los dos sistemas se encuentren en
estados correspondientes cuando se efecta un
cambio de fase, calcular la temperatura de
ebullicin del CO2 a la presin normal. Nota:
Consultar la Tabla 2.1 (pgina 55) para obtener las coordenadas crticas del agua y del
CO2.
Tabla Prob. 2.20.- Temperatura de
ebullicin del agua en funcin de la
presin.
p (kg/cm2)
T (K)
2.0
392.0
2.5
399.8
3.0
405.9
3.5
411.2
4.0
415.9
72
Lec. 2.- Gases ideales y reales. Ecuaciones trmicas de estado.
También podría gustarte
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDe EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesAún no hay calificaciones
- Sedimentacion Cepis Equipos Cap. 7 PDFDocumento61 páginasSedimentacion Cepis Equipos Cap. 7 PDFFernandoAún no hay calificaciones
- Ley de CharlesDocumento15 páginasLey de CharlesOmar PerezAún no hay calificaciones
- Ley de Los Gases IdealesDocumento14 páginasLey de Los Gases Idealesjuan david50% (2)
- Estado GaseosoDocumento20 páginasEstado GaseosoKerly WestAún no hay calificaciones
- Ley General de Los GasesDocumento8 páginasLey General de Los GasesEzequiel Conde GutierrezAún no hay calificaciones
- Energia y Altura de CargaDocumento20 páginasEnergia y Altura de CargaOscar Diaz100% (2)
- Ley General Del Estado GaseosoDocumento9 páginasLey General Del Estado GaseosoAleejandraa LhAún no hay calificaciones
- Parte 2 - Método Del Esfuerzo - VidaDocumento11 páginasParte 2 - Método Del Esfuerzo - VidaOscar ValderramaAún no hay calificaciones
- Antologia Unidad 5Documento29 páginasAntologia Unidad 5Erika Perez Fernando100% (1)
- Practica 2 Quimica ESIME ZacatencoDocumento15 páginasPractica 2 Quimica ESIME ZacatencoDavid Vl100% (1)
- Carga y Esfuerzo Critico en ColumnasDocumento7 páginasCarga y Esfuerzo Critico en ColumnasNícolas Carrasco0% (1)
- Gases IdealesDocumento25 páginasGases IdealesVictor PereaAún no hay calificaciones
- Tema 12Documento25 páginasTema 12Mortal ResiduoAún no hay calificaciones
- Lab #2Documento18 páginasLab #2Aldair Treviño Portillo0% (2)
- Práctica #02Documento18 páginasPráctica #02Luis Rolando Alvarez ChavezAún no hay calificaciones
- Práctica #02Documento8 páginasPráctica #02Bárbara RTAún no hay calificaciones
- Ecuación de Estado para Gases RealesDocumento13 páginasEcuación de Estado para Gases RealesCristian Ccaso MamaniAún no hay calificaciones
- Trabajo de FluidosDocumento82 páginasTrabajo de FluidosRoberto Martinez100% (1)
- Guia de Lab - Ley de CharlesDocumento7 páginasGuia de Lab - Ley de CharlesMaria JoseAún no hay calificaciones
- Ecuaciones de Estado para Gases NaturalesDocumento31 páginasEcuaciones de Estado para Gases NaturalesYusuf MohammedAún no hay calificaciones
- Ley de Boyle, Charles, Gay & Lussac y Ley CombinadaDocumento4 páginasLey de Boyle, Charles, Gay & Lussac y Ley CombinadaLucha PresaAún no hay calificaciones
- El Gas PerfectoDocumento17 páginasEl Gas PerfectoAgustin ValderramaAún no hay calificaciones
- Leyes de Los GasesDocumento5 páginasLeyes de Los GasesRoberto RiveraAún no hay calificaciones
- Unidad 02 Gases Ideales... Term.Documento9 páginasUnidad 02 Gases Ideales... Term.Mica Guadi PrietoAún no hay calificaciones
- Cap 7 Gases Ideales 19 Mayo 2013 PDFDocumento14 páginasCap 7 Gases Ideales 19 Mayo 2013 PDFKriiztal GodinezAún no hay calificaciones
- Laboratorio 1 - Leyes de Los GasesDocumento10 páginasLaboratorio 1 - Leyes de Los GasesRafael Gustavo Alfaro AlemanAún no hay calificaciones
- Gases IdealesDocumento23 páginasGases IdealesEduardo RobleroAún no hay calificaciones
- Gases Ideales y RealesDocumento13 páginasGases Ideales y RealesLee HansonAún no hay calificaciones
- LEY GasesDocumento6 páginasLEY GasesLeydii Yazz ArévaLoAún no hay calificaciones
- QG Tema6 OdtDocumento14 páginasQG Tema6 OdtGabriel Palomares HumanesAún no hay calificaciones
- Ley General de Los GasesDocumento10 páginasLey General de Los Gasesvanessamonserrat2007kawaiiAún no hay calificaciones
- Lectura 6 GASES FinalDocumento12 páginasLectura 6 GASES FinalBritney S.Aún no hay calificaciones
- Termodinámica Unidad 2Documento21 páginasTermodinámica Unidad 2Jael SanchezAún no hay calificaciones
- Ley de GasDocumento3 páginasLey de GasAbril DiazAún no hay calificaciones
- Resumen Gas IdealDocumento3 páginasResumen Gas Idealmargarita canoAún no hay calificaciones
- Tema 9. El Estado GASEOSO Y LÍQUIDO (Teoría)Documento21 páginasTema 9. El Estado GASEOSO Y LÍQUIDO (Teoría)Pablo Merino DeniaAún no hay calificaciones
- Ecuacion de EstadoDocumento6 páginasEcuacion de Estadogabriela amangandiAún no hay calificaciones
- Lectura 6.1 - GASESDocumento12 páginasLectura 6.1 - GASESMoises YepezAún no hay calificaciones
- Cuestionario Gases, Termoquímica y ElectroquímicaDocumento24 páginasCuestionario Gases, Termoquímica y ElectroquímicaEmily GonzalesAún no hay calificaciones
- Instituto Tecnológico Nacional de México Campus Villahermosa Alumno: Catedratica: Asignatura: Carrera: Semestre: FechaDocumento23 páginasInstituto Tecnológico Nacional de México Campus Villahermosa Alumno: Catedratica: Asignatura: Carrera: Semestre: FechaEduardo NiñoAún no hay calificaciones
- Relaciones Termodinamicas Parte 2Documento22 páginasRelaciones Termodinamicas Parte 2Maria caballeroAún no hay calificaciones
- INFORME DE Fisico Quimica (Reparado)Documento9 páginasINFORME DE Fisico Quimica (Reparado)Harold RiveraAún no hay calificaciones
- Leyes de Los Gases IdealesDocumento4 páginasLeyes de Los Gases IdealesFrancisco Javier Retamal SotoAún no hay calificaciones
- Gases IdealesDocumento7 páginasGases IdealesHenry Josué Condori QuillaAún no hay calificaciones
- Trabajo D GasotecniaDocumento28 páginasTrabajo D GasotecniaEdgar Sanchz100% (1)
- Ecuaciones de EstadoDocumento11 páginasEcuaciones de EstadoJadhira RamirezAún no hay calificaciones
- GasDocumento29 páginasGasDiego Armando OspinaAún no hay calificaciones
- Ley Combinada de Los GasesDocumento8 páginasLey Combinada de Los GasesLuisa BotiaAún no hay calificaciones
- Practica 2Documento8 páginasPractica 2AyrtonAún no hay calificaciones
- 20 Ejemplos de Gas Ideal y Gas Rea1Documento25 páginas20 Ejemplos de Gas Ideal y Gas Rea1Liddy WaldoAún no hay calificaciones
- Práctica ..Documento17 páginasPráctica ..Tito Mendoza Tito MendozaAún no hay calificaciones
- Semana 11Documento6 páginasSemana 11MISHELL JULISA MAMANI FLORESAún no hay calificaciones
- Leyes de Los GasesDocumento3 páginasLeyes de Los GasesEduardo Salgado GuerraAún no hay calificaciones
- Gases Ideales y RealesDocumento28 páginasGases Ideales y RealesLee HansonAún no hay calificaciones
- Practica 1 Quimica AplicadaDocumento10 páginasPractica 1 Quimica AplicadaAlfredoAún no hay calificaciones
- A - Estado GaseosoDocumento15 páginasA - Estado GaseosoRamy LudueñaAún no hay calificaciones
- Unidad 2 Gas IdealDocumento35 páginasUnidad 2 Gas IdealIndiraAún no hay calificaciones
- Estado GaseosoDocumento12 páginasEstado GaseosoandreaAún no hay calificaciones
- Informe Fisico Quimica 2019 1Documento39 páginasInforme Fisico Quimica 2019 1RICARDO ANGEL BERRIO PEREZAún no hay calificaciones
- Tarea de Lab Fis IDocumento8 páginasTarea de Lab Fis IErlinzon Estrella SantosAún no hay calificaciones
- Separata 3Documento19 páginasSeparata 3Price Sanchez JoseAún no hay calificaciones
- Teoria Elasticidad Leyes ConstitutivasDocumento21 páginasTeoria Elasticidad Leyes ConstitutivasErick MorrisAún no hay calificaciones
- Biomecánica Uap FiioDocumento21 páginasBiomecánica Uap FiioLIZ MENDOZA YUCRAAún no hay calificaciones
- Análisis Tridimensional de La DeformaciónDocumento14 páginasAnálisis Tridimensional de La DeformaciónAldo Carlos100% (1)
- Ensayo Ingenieria MecanicaDocumento5 páginasEnsayo Ingenieria MecanicaMaritza PanacualAún no hay calificaciones
- Cubiert-PolideportivoDocumento16 páginasCubiert-PolideportivoaeaxannoAún no hay calificaciones
- Repaso MRUVDocumento3 páginasRepaso MRUVSergio GaleraAún no hay calificaciones
- LABORATORIO #13 (Final)Documento5 páginasLABORATORIO #13 (Final)Vanessa De la hozAún no hay calificaciones
- Ite - Resumen Tps FinalDocumento43 páginasIte - Resumen Tps FinalGuadaa MourelosAún no hay calificaciones
- DMI T1. CuestionesDocumento6 páginasDMI T1. CuestionesVicente Pascual NavarroAún no hay calificaciones
- UNE 23500-2012 Sistema de BombeoDocumento21 páginasUNE 23500-2012 Sistema de BombeoJavier Alonso LosadaAún no hay calificaciones
- Informe de Física II - 7Documento10 páginasInforme de Física II - 7Michel JamcAún no hay calificaciones
- Informe de Laboratorio de FisicoquimicaDocumento9 páginasInforme de Laboratorio de FisicoquimicaLicho LapizAún no hay calificaciones
- Cambio de FaseDocumento11 páginasCambio de FaseMisael OrellanoAún no hay calificaciones
- Acoplamientos - Transmision de MovimientoDocumento15 páginasAcoplamientos - Transmision de MovimientoJohn Alejandro Perez PerezAún no hay calificaciones
- Solución PD1 PD2 2018 - 2Documento10 páginasSolución PD1 PD2 2018 - 2Jos AngeloAún no hay calificaciones
- T0000904 PDFDocumento589 páginasT0000904 PDFpeterboadaAún no hay calificaciones
- Capítulo 3 Estudio de Perdidas Saltos Entalpicos y Rendimientos PDFDocumento29 páginasCapítulo 3 Estudio de Perdidas Saltos Entalpicos y Rendimientos PDFAriel Alvaro Gomez CanaviriAún no hay calificaciones
- 1 Apuntes Electricidad y MagnetismoDocumento20 páginas1 Apuntes Electricidad y MagnetismoLibros Unitec PdfAún no hay calificaciones
- Problemas Propuestos Unidad 3 Volumenes de ControlDocumento16 páginasProblemas Propuestos Unidad 3 Volumenes de ControlRodrigo Felipe Cárdenas JaraAún no hay calificaciones
- Cuando Colocamos Un Medidor de ROE Entre El Transceptor y La Línea de TransmisiónDocumento3 páginasCuando Colocamos Un Medidor de ROE Entre El Transceptor y La Línea de TransmisiónGraciela ArchilaAún no hay calificaciones
- Modulo III - Fisica IDocumento41 páginasModulo III - Fisica ICristopher Nuñez CruzadoAún no hay calificaciones
- Análisis de EstructurasDocumento9 páginasAnálisis de Estructurasandrea rieraAún no hay calificaciones
- 1 CLASE DE FISICA 10 Segundo Peridodo MUDocumento17 páginas1 CLASE DE FISICA 10 Segundo Peridodo MUYiseth MuñozAún no hay calificaciones
- Bfi01 Valdivia Pe 21-1 WDocumento1 páginaBfi01 Valdivia Pe 21-1 WJennifer Gianella Orihuela OrihuelaAún no hay calificaciones