Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Diagrama de Fase
Cargado por
TeachmeonceagainTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Diagrama de Fase
Cargado por
TeachmeonceagainCopyright:
Formatos disponibles
Diagrama de fase
De Wikipedia, la enciclopedia libre Saltar a: navegacin, bsqueda
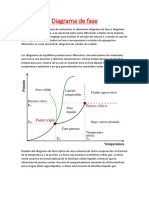
La lnea de puntos muestra el comportamiento anmalo del agua. La lnea verde marca el punto de congelacin y la lnea azul, el punto de ebullicin. Se muestra cmo varan con la presin. En termodinmica y ciencia de materiales se denomina diagrama de fase a la representacin grfica de las fronteras entre diferentes estados de la materia de un sistema, en funcin de variables elegidas para facilitar el estudio del mismo. Cuando en una de estas representaciones todas las fases corresponden a estados de agregacin diferentes se suele denominar diagrama de cambio de estado. En ciencia de materiales se utilizan ampliamente los diagramas de fase binarios, mientras que en termodinmica se emplean sobre todo los diagramas de fase de una sustancia pura.
[editar] Diagrama de fase de una sustancia pura
Los diagramas de fase ms sencillos son los de presin - temperatura de una sustancia pura, como puede ser el del agua. En el eje de ordenadas se coloca la presin y en el de abscisas la temperatura. Generalmente, para una presin y temperatura dadas, el cuerpo presenta una nica fase excepto en las siguientes zonas:
Punto triple: En este punto del diagrama coexisten los estados slido, lquido y gaseoso. Estos puntos tienen cierto inters, ya que representan un invariante y por lo tanto se pueden utilizar para calibrar termmetros. Los pares (presin, temperatura) que corresponden a una transicin de fase entre: o Dos fases slidas: Cambio alotrpico; o Entre una fase slida y una fase lquida: fusin - solidificacin; o Entre una fase slida y una fase vapor (gas): sublimacin - deposicin (o sublimacin inversa); o Entre una fase lquida y una fase vapor: vaporizacin - condensacin (o licuefaccin).
Es importante sealar que la curva que separa las fases vapor-lquido se detiene en un punto llamado punto crtico. Ms all de este punto, la materia se presenta como un fluido supercrtico que tiene propiedades tanto de los lquidos como de los gases. Modificando la presin y temperatura en valores alrededor del punto crtico se producen reacciones que pueden tener inters industrial, como por ejemplo las utilizadas para obtener caf descafeinado.
Es preciso anotar que, en el diagrama P-T del agua, la lnea que separa los estados lquido y slido tiene pendiente negativa, lo cual es algo bastante inusual. Esto quiere decir que aumentando la presin el hielo se funde, y tambin que la fase slida tiene menor densidad que la fase lquida.
[editar] Diagrama de fase binario
Cuando aparecen varias sustancias, la representacin de los cambios de fase puede ser ms compleja. Un caso particular, el ms sencillo, corresponde a los diagramas de fase binarios. Ahora las variables a tener en cuenta son la temperatura y la concentracin, normalmente en masa. En un diagrama binario pueden aparecer las siguientes regiones:
Slido puro o disolucin slida Mezcla de disoluciones slidas (eutctica, eutectoide, peritctica, peritectoide) Mezcla slido - lquido nicamente lquido, ya sea mezcla de lquidos inmiscibles (emulsin), ya sea un lquido completamente homogneo. Mezcla lquido - gas Gas (lo consideraremos siempre homogneo, trabajando con pocas variaciones da altitud).
Hay punto y lneas en estos diagramas importantes para su caracterizacin:
Lnea de lquidus, por encima de la cual solo existen fases lquidas. Lnea de slidus, por debajo de la cual solo existen fases slidas. Lnea eutctica y eutectoide. Son lneas horizontales (isotermas) en las que tienen lugar transformaciones eutcticas y eutectoides, respectivamente. Lnea de solvus, que indica las temperaturas para las cuales una disolucin slida () de A y B deja de ser soluble para transformarse en ()+ sustancia pura (A B). Concentraciones definidas, en las que tienen lugar transformaciones a temperatura constante
También podría gustarte
- Diagrama de FaseDocumento2 páginasDiagrama de FaseAuxiliadora BencomoAún no hay calificaciones
- Lectura Diagrama de Fases BinarioDocumento4 páginasLectura Diagrama de Fases BinarioJuan SotoAún no hay calificaciones
- Quimica (Diagrama y EnLaces)Documento3 páginasQuimica (Diagrama y EnLaces)Eduardo GarcíaAún no hay calificaciones
- Equilibrio de FasesDocumento3 páginasEquilibrio de FasesJudithAún no hay calificaciones
- 5.1 Diagrama de FaseDocumento6 páginas5.1 Diagrama de FaseAntonio HermidaAún no hay calificaciones
- Diagrama de Fase PuraDocumento6 páginasDiagrama de Fase Purajesus machinAún no hay calificaciones
- Actividad 10 Diagrama de FasesDocumento8 páginasActividad 10 Diagrama de FasesCitlaly Montalvo100% (1)
- Diagrama de FaseeDocumento27 páginasDiagrama de FaseeCarolyn BennettAún no hay calificaciones
- Practica #9 Diagrama de FasesDocumento6 páginasPractica #9 Diagrama de FasesAleinad FC83% (6)
- Diagramas de FacesDocumento21 páginasDiagramas de FacesferminhernandezAún no hay calificaciones
- Diagrama de FasesDocumento4 páginasDiagrama de FasesJAVIERAún no hay calificaciones
- Energía en Los Cambios QuímicosDocumento12 páginasEnergía en Los Cambios QuímicossofiaAún no hay calificaciones
- Diagrama de Fase y FisicoquimicaDocumento4 páginasDiagrama de Fase y FisicoquimicaRonal Vásquez BautistaAún no hay calificaciones
- Diagrama de FasesDocumento3 páginasDiagrama de FasesJorge MalmaAún no hay calificaciones
- Guía Diagramas de FaseDocumento5 páginasGuía Diagramas de FaseFelipe Peña PeñaAún no hay calificaciones
- Diagrama de fases y entropía en sistemas termodinámicosDocumento16 páginasDiagrama de fases y entropía en sistemas termodinámicosAlberto DuranAún no hay calificaciones
- Diagrama de FaseDocumento8 páginasDiagrama de FaseCristian valenzuela maciasAún no hay calificaciones
- Entalpía Entropía FasesDocumento3 páginasEntalpía Entropía FasesMauricio Avila100% (1)
- Diagrama de FasesDocumento6 páginasDiagrama de FasesNúria Tornay G.Aún no hay calificaciones
- Practica 9 Diagrama de Fases 1Documento5 páginasPractica 9 Diagrama de Fases 1grecia martinez ortizAún no hay calificaciones
- Regla de FasesDocumento16 páginasRegla de Faseskenyi8Aún no hay calificaciones
- Informe Equilibrio Liquido VaporDocumento25 páginasInforme Equilibrio Liquido VaporPaolo Guerra SteinAún no hay calificaciones
- Equilibrio QuimicoDocumento8 páginasEquilibrio QuimicoDennis LinoAún no hay calificaciones
- Diagrama de FaseDocumento9 páginasDiagrama de FaseSimarAún no hay calificaciones
- Diagramas de Propiedades para Procesos de Cambio de FaseDocumento4 páginasDiagramas de Propiedades para Procesos de Cambio de Faseernith david corrales fernandezAún no hay calificaciones
- Sistema binario paradiclorobenceno-naftalenoDocumento71 páginasSistema binario paradiclorobenceno-naftalenoMalu AisneAún no hay calificaciones
- U6 2C 2017Documento32 páginasU6 2C 2017Flor MalamudAún no hay calificaciones
- Diagrama de FaseDocumento5 páginasDiagrama de FaseKevin Perez YalleAún no hay calificaciones
- Critico Lo Nesesario de SaberDocumento6 páginasCritico Lo Nesesario de Saberfreddy noya plataAún no hay calificaciones
- Trabajo Diagrama de FaseDocumento5 páginasTrabajo Diagrama de FaseAndreina HernandezAún no hay calificaciones
- Sustancias puras: propiedades, fases y diagramasDocumento15 páginasSustancias puras: propiedades, fases y diagramascesarAún no hay calificaciones
- Cómo se alcanza el equilibrio material entre fasesDocumento7 páginasCómo se alcanza el equilibrio material entre fasesESTHER ISABEL CEBALLOS PORTILLOAún no hay calificaciones
- Diagrama PVT sustanciasDocumento4 páginasDiagrama PVT sustanciasNeilet Arias AgostiniAún no hay calificaciones
- Sustancias PurasDocumento73 páginasSustancias PurasMiliana LPAún no hay calificaciones
- Gases Reales y Cambios de FaseDocumento2 páginasGases Reales y Cambios de FaseJuan Pablo Gonzalez0% (1)
- Actividad 9Documento3 páginasActividad 9Serenity RicaldeAún no hay calificaciones
- Ses 5 Equilibrio de Fases y Endurecimiento Por Solucion SolidaDocumento40 páginasSes 5 Equilibrio de Fases y Endurecimiento Por Solucion SolidaMaria AquiseAún no hay calificaciones
- Trabajo de Invetigacion MontielDocumento12 páginasTrabajo de Invetigacion MontielAngel Alexis Hernandez RamirezAún no hay calificaciones
- Curva de CoexistenciaDocumento5 páginasCurva de CoexistenciaMariano HernandezAún no hay calificaciones
- Equilibrio de FasesDocumento34 páginasEquilibrio de FasesAndrea Gomez100% (1)
- Diagramas P-V y P-T de gases idealesDocumento4 páginasDiagramas P-V y P-T de gases idealesJose JesusAún no hay calificaciones
- UNIDAD 2 Operacion UnitariasDocumento6 páginasUNIDAD 2 Operacion UnitariasCHUPA CABRAAún no hay calificaciones
- DIAGRAMA DE PROPIEDADES PARA PROCESOS DE CAMBIOS DEDocumento11 páginasDIAGRAMA DE PROPIEDADES PARA PROCESOS DE CAMBIOS DEANDRES FABIAN CHARRY POVEDAAún no hay calificaciones
- Diagrama de Fase Presion TemperaturaDocumento6 páginasDiagrama de Fase Presion TemperaturaDevra GomezAún no hay calificaciones
- Equilibrio líquido-vapor en mezclas binariasDocumento11 páginasEquilibrio líquido-vapor en mezclas binariasRoberto GoncalvesAún no hay calificaciones
- Diagrama de FaceDocumento8 páginasDiagrama de FaceLeonardo Daniel Toledo PresaAún no hay calificaciones
- E2a J Microestructura y Propiedades de Los MaterialesDocumento27 páginasE2a J Microestructura y Propiedades de Los MaterialesJorge Martinez CamachoAún no hay calificaciones
- Diagrama de Fases PDFDocumento1 páginaDiagrama de Fases PDFjeanfrancoAún no hay calificaciones
- Equilibrio de Fases DiagramasDocumento10 páginasEquilibrio de Fases DiagramasAnonymous NIMKH6EqAún no hay calificaciones
- Superficie P V TDocumento12 páginasSuperficie P V TWilman Freddy Arista TafurAún no hay calificaciones
- Diagramas y Propiedades Termodinámicas Del AguaDocumento8 páginasDiagramas y Propiedades Termodinámicas Del AguaLuis Enrique Peñuela V.Aún no hay calificaciones
- Diagrama fasesDocumento9 páginasDiagrama fasesPaola Pallares ÁvilaAún no hay calificaciones
- Diagrama de Fase Presión-TemperaturaDocumento6 páginasDiagrama de Fase Presión-Temperaturaxyzabc987123Aún no hay calificaciones
- Diagrama TernarioDocumento3 páginasDiagrama TernarioSerenity RicaldeAún no hay calificaciones
- Sistema Termodinamica InformeDocumento22 páginasSistema Termodinamica InformeGénesis NrvzAún no hay calificaciones
- Investigacion FaseDocumento7 páginasInvestigacion FaseFlavio SiqueirosAún no hay calificaciones
- Sem7 MF Diagrama de Fases de Aleaciones JRCL 202220Documento24 páginasSem7 MF Diagrama de Fases de Aleaciones JRCL 202220José ZavalaAún no hay calificaciones
- Ensayo de Termodinámica 112-135Documento5 páginasEnsayo de Termodinámica 112-135damianAún no hay calificaciones
- Tarea 1 de Tecnologia de Los Materiales 1Documento36 páginasTarea 1 de Tecnologia de Los Materiales 1Danny Carrasquedo Muñoz100% (2)
- Catálogo Peças MotorDocumento218 páginasCatálogo Peças MotorJoão MacielAún no hay calificaciones
- Práctica 7 Equipo 3 LouDocumento13 páginasPráctica 7 Equipo 3 LouJhibran Perez PerezAún no hay calificaciones
- Trabajo 10Documento8 páginasTrabajo 10Cam GonzAún no hay calificaciones
- Sustentacion 3 Semana 7Documento3 páginasSustentacion 3 Semana 7camilo pea0% (1)
- Probl Resueltos - Tema 9 Din Fluid - 2019Documento19 páginasProbl Resueltos - Tema 9 Din Fluid - 2019PacoSanchezBorrego100% (1)
- Cap 29 - Welty - 5th-570-587 EspañolDocumento27 páginasCap 29 - Welty - 5th-570-587 EspañolEstefy GimenezAún no hay calificaciones
- Química - Unidades de masa y estequiometríaDocumento3 páginasQuímica - Unidades de masa y estequiometríaLuan Carrasco SayagoAún no hay calificaciones
- Sistemas e Instalaciones Hidráulicas: Propiedades de los FluidosDocumento3 páginasSistemas e Instalaciones Hidráulicas: Propiedades de los FluidosFrancisco RuizAún no hay calificaciones
- 18 Compresor NeumáticoDocumento39 páginas18 Compresor Neumáticojuanluis201277Aún no hay calificaciones
- Unidad N °7 Uso Del RevaporizadoDocumento7 páginasUnidad N °7 Uso Del Revaporizadobluesenmi100% (1)
- INTRODUCCIÓN Columnas de AbsorciónDocumento5 páginasINTRODUCCIÓN Columnas de AbsorciónSamanta SilvaAún no hay calificaciones
- Aplicacion Norma ISADocumento30 páginasAplicacion Norma ISAFFlipooxAún no hay calificaciones
- Actividad Virtual N°1 - Termodinamica 2Documento6 páginasActividad Virtual N°1 - Termodinamica 2jadyra53100% (1)
- Leyes VolumetricasDocumento10 páginasLeyes VolumetricasLuis Francisco Lizcano Guzman0% (1)
- GUIA DE PROBLEMAS No 3Documento5 páginasGUIA DE PROBLEMAS No 3Fernanda ZaldañaAún no hay calificaciones
- Bombeo NeumáticoDocumento11 páginasBombeo NeumáticoBrandon Alejandro Gómez PérezAún no hay calificaciones
- PRACTICA 2 - 4to ParcialDocumento5 páginasPRACTICA 2 - 4to ParcialRodriguez MamaniAún no hay calificaciones
- Catalogo Power Team SPXDocumento20 páginasCatalogo Power Team SPXmarceloAún no hay calificaciones
- Ciclo Rankine: Calentar agua para generar vapor y energíaDocumento7 páginasCiclo Rankine: Calentar agua para generar vapor y energíaEdisson TrujilloAún no hay calificaciones
- LXE10E136J o Posterior (DECOS J) : Unidad de Refrigeración de Contenedores para Transporte MarítimoDocumento191 páginasLXE10E136J o Posterior (DECOS J) : Unidad de Refrigeración de Contenedores para Transporte MarítimoHever Porto RoseroAún no hay calificaciones
- Gas Natural y Su Impacto AmbientalDocumento9 páginasGas Natural y Su Impacto AmbientalVictor MartinezAún no hay calificaciones
- Bomba de Ariete PDFDocumento46 páginasBomba de Ariete PDFfidelnixon100% (1)
- Métodos para evaluar la eficiencia de separación en destilación fraccionadaDocumento18 páginasMétodos para evaluar la eficiencia de separación en destilación fraccionadaMilagros SalazarAún no hay calificaciones
- Presiòn de Vapor ReidDocumento3 páginasPresiòn de Vapor ReidCarlos Alberto Jaimes BravoAún no hay calificaciones
- Trabajo 1 de ReaccionesDocumento3 páginasTrabajo 1 de ReaccionesJuan Sebastián Albán DomínguezAún no hay calificaciones
- Determinación del área de relleno sanitario y cálculo de generación de residuosDocumento19 páginasDeterminación del área de relleno sanitario y cálculo de generación de residuosFernanda FloresAún no hay calificaciones
- Producción de Oxígeno Mediante Un Sistema CriogénicoDocumento3 páginasProducción de Oxígeno Mediante Un Sistema CriogénicoJhordy Maycol Rodas QuirozAún no hay calificaciones
- Ecuacion de Los Gases IdealesDocumento6 páginasEcuacion de Los Gases IdealesJorge BenitezAún no hay calificaciones
- Plan de Superación Final Tercer Período 10° 2023Documento9 páginasPlan de Superación Final Tercer Período 10° 2023Juan Felipe Díaz LondoñoAún no hay calificaciones
- Diagramas TernariosDocumento7 páginasDiagramas TernariosGerson OrtizAún no hay calificaciones