Documentos de Académico
Documentos de Profesional
Documentos de Cultura
TIROSINA
TIROSINA
Cargado por
dalayna quirozDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
TIROSINA
TIROSINA
Cargado por
dalayna quirozCopyright:
Formatos disponibles
UNIDAD EDUCATIVA SAN VICENTE FERRER
Nombre: Dalayna Quiroz
Fecha: 26/10/23
Curso: 1ro D
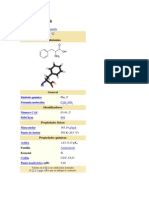
TIROSINA
La tirosina (abreviado en español como Tir o Y, y Tyr o Y en inglés) es uno de los veinte aminoácidos que forman las
proteínas. Se clasifica como un aminoácido no esencial en los mamíferos ya que su síntesis se produce a partir de la
hidroxilación de otro aminoácido: la fenilalanina. Esto se considera así siempre y cuando la dieta de los mamíferos
contenga un aporte adecuado de fenilalanina. Por tanto el aminoácido fenilalanina sí que es esencial. Como todos
los aminoácidos está formado por un carbono central alfa (Cα) unido a un átomo de hidrógeno (-H), un grupo
carboxilo (-COOH), un grupo amino (-NH2) y una cadena lateral. En la tirosina, la cadena lateral es un grupo fenólico.
La palabra tirosina proviene del griego tyros, que significa queso. Se llama así ya que este aminoácido fue
descubierto por un químico alemán llamado Justus von Liebig a partir de la proteína caseína, que se encuentra en el
queso. Se conocen tres isómeros distintos del aminoácido tirosina: para-tirosina, meta-tirosina y la orto-tirosina.
Aunque la forma más conocida y estudiada es la para-tirosina o también llamada L-tirosina. De forma general, las
propiedades de los aminoácidos se deben a la naturaleza de su cadena lateral, su reactividad y la conformación de
las cadenas proteicas que forman. Lo mismo sucede en la tirosina. La tirosina es un sólido que forma cristales y que
generalmente presenta un color blanquecino, aunque también puede ser incoloro. Se considera un aminoácido polar
y protonable. Aunque normalmente se clasifica como aminoácido hidrofóbico a causa de su anillo aromático, hay
que tener en cuenta que también contiene un grupo hidroxilo. Normalmente se encuentra sin carga, aunque a pH
muy básico presenta carga negativa. Por lo que respecta a su solubilidad sabemos que es soluble en agua y
ligeramente soluble en alcohol. También conocemos su insolubilidad en éter. Se trata de una molécula ópticamente
activa, lo cual significa que hace girar el plano de la luz polarizada. Como la mayoría de los aminoácidos (todos
excepto la glicina) presenta una asimetría en el carbono alfa, de manera que no puede superponerse a su imagen en
el espejo. Se dice que presenta quiralidad.
También podría gustarte
- Exposicion AminoacidosDocumento20 páginasExposicion Aminoacidosbrayan garcia100% (1)
- FenilalaninaDocumento13 páginasFenilalaninaJonathan CastellanosAún no hay calificaciones
- AminoácidoDocumento6 páginasAminoácidoDennisOrellanaAún no hay calificaciones
- AminoácidosDocumento13 páginasAminoácidosLalo BarcenasAún no hay calificaciones
- AminoácidoDocumento17 páginasAminoácidoandresleonliveAún no hay calificaciones
- AminoacidosDocumento34 páginasAminoacidosNatalie BravoAún no hay calificaciones
- Aminoácidos PDFDocumento13 páginasAminoácidos PDFLalo BarcenasAún no hay calificaciones
- TirosinaDocumento5 páginasTirosinaVenecia Francelli Villalobos GonzalezAún no hay calificaciones
- AminoácidoDocumento9 páginasAminoácidoDiego Alexander Ortiz AsprillaAún no hay calificaciones
- AMINOÁCIDOSDocumento9 páginasAMINOÁCIDOSNaylenAún no hay calificaciones
- AminoácidoDocumento9 páginasAminoácidoOliver Martínez BermúdezAún no hay calificaciones
- AminoacidoDocumento6 páginasAminoacidoVictor Eduardo Pozo EstradaAún no hay calificaciones
- Aminoacidos LaboratorioDocumento20 páginasAminoacidos LaboratorioCarlos Torres VelaAún no hay calificaciones
- Resumen AminoácidosDocumento6 páginasResumen AminoácidosElvisRojas972010Aún no hay calificaciones
- Produccion de Aminoacidos y BiopolimerosDocumento15 páginasProduccion de Aminoacidos y BiopolimerosJhan Montero100% (1)
- Naturaleza Química de Los AminoácidosDocumento17 páginasNaturaleza Química de Los Aminoácidosjuan carlosAún no hay calificaciones
- TEMA 3 Aminoácidos y PéptidosDocumento7 páginasTEMA 3 Aminoácidos y PéptidosYeniffer MontilvaAún no hay calificaciones
- Aminoácido - Wikipedia, La Enciclopedia LibreDocumento14 páginasAminoácido - Wikipedia, La Enciclopedia LibreAnnoli Lugo100% (1)
- AminoácidosDocumento3 páginasAminoácidosjosexuuAún no hay calificaciones
- Aminoacidos y PeptidosDocumento6 páginasAminoacidos y PeptidosRafael B. DiazAún no hay calificaciones
- Reacciones de Color para Identificacion de AaDocumento7 páginasReacciones de Color para Identificacion de AaRegina Flores PerezAún no hay calificaciones
- Amino Acid oDocumento8 páginasAmino Acid osantiago dazaAún no hay calificaciones
- Amino Acid oDocumento8 páginasAmino Acid osantiago dazaAún no hay calificaciones
- AMINOACIDOSDocumento24 páginasAMINOACIDOSDaniela SmithAún no hay calificaciones
- AminoácidosDocumento13 páginasAminoácidosluz Erika santiagoAún no hay calificaciones
- Aminoacidos y Peptidos I 2021Documento55 páginasAminoacidos y Peptidos I 2021paoka100% (1)
- Estructura Básica de Un AminoácidoDocumento6 páginasEstructura Básica de Un AminoácidoJesus DiazAún no hay calificaciones
- FENILALANINADocumento5 páginasFENILALANINAMónica Viviana Carabalí PortelaAún no hay calificaciones
- Metabolitos Secundarios 1 PDFDocumento91 páginasMetabolitos Secundarios 1 PDFLeonardo Giraldo67% (3)
- PROTEINASDocumento30 páginasPROTEINASFrancy Julieth Triviño BohorquezAún no hay calificaciones
- Metabolismo de ProteinasDocumento61 páginasMetabolismo de ProteinasprietalindaAún no hay calificaciones
- AminoácidosDocumento3 páginasAminoácidosMontse BolañosAún no hay calificaciones
- Aminoácidos Abril AguilarDocumento10 páginasAminoácidos Abril AguilarABRIL AGUILARAún no hay calificaciones
- Aplicación de Los Aminoácidos en La Química - DayaniDocumento18 páginasAplicación de Los Aminoácidos en La Química - DayaniMiguel Angel Campos MarcavillacaAún no hay calificaciones
- La TirosinaDocumento2 páginasLa TirosinaAngela QuispeAún no hay calificaciones
- AminoacidosDocumento45 páginasAminoacidosDavid ocampoAún no hay calificaciones
- Laboratorio de Aminoácidos 2Documento14 páginasLaboratorio de Aminoácidos 2Sandy Paola Villera TobonAún no hay calificaciones
- Resumen Semana 29 Aminoacidos y Peptidos Grupo 6Documento15 páginasResumen Semana 29 Aminoacidos y Peptidos Grupo 6Mariana Alejandra Lopez LopezAún no hay calificaciones
- AminoacidosDocumento7 páginasAminoacidosDyannie MedinaAún no hay calificaciones
- AminoacidosDocumento12 páginasAminoacidosCesarManuelCastilloCamachoAún no hay calificaciones
- Charla de Ac. ShikimicoDocumento9 páginasCharla de Ac. ShikimicoLizbethAún no hay calificaciones
- Trabajo AminoacidosDocumento38 páginasTrabajo AminoacidosYojackson Pastran100% (1)
- Unidad I - Semana 4 PROTEINAS Aminoácidos PÉPTIDOS-Teoría PDFDocumento14 páginasUnidad I - Semana 4 PROTEINAS Aminoácidos PÉPTIDOS-Teoría PDFchalyn romeyro fabian rojasAún no hay calificaciones
- Tarea3 Los20AminoácidosProteicos CarmenPontanillaDocumento3 páginasTarea3 Los20AminoácidosProteicos CarmenPontanillacarmen PontanillaAún no hay calificaciones
- FOSFORODocumento7 páginasFOSFOROSergio PerezAún no hay calificaciones
- AminoácidoDocumento10 páginasAminoácidoNestorAún no hay calificaciones
- REPASO 2do ParcialDocumento9 páginasREPASO 2do ParcialModesto CopiasAún no hay calificaciones
- Representacion de AminoácidosDocumento13 páginasRepresentacion de Aminoácidosvitochorolo100% (1)
- TeóRico QuímicaDocumento66 páginasTeóRico QuímicaJuli GrandAún no hay calificaciones
- AminoacidosDocumento6 páginasAminoacidosDiego Padilla SantosAún no hay calificaciones
- Las ProteinasDocumento8 páginasLas ProteinasCarlos Angel Contreras ZeballosAún no hay calificaciones
- Aminoacidos 2022Documento12 páginasAminoacidos 2022Sâmuel LópezAún no hay calificaciones
- Amino Acidos Aspecto Historico y ClasificacionDocumento4 páginasAmino Acidos Aspecto Historico y ClasificacionFerchuy KansaguiAún no hay calificaciones
- AminoácidoDocumento11 páginasAminoácidoAlexander GuadronAún no hay calificaciones
- AMINOÁCIDOSDocumento11 páginasAMINOÁCIDOSafuentesv211Aún no hay calificaciones
- Los AminoácidosDocumento5 páginasLos AminoácidosSebastian OliverosAún no hay calificaciones
- ProteínasDocumento48 páginasProteínasAdenis DesvarsAún no hay calificaciones