Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Problemas de Parciales
Cargado por
Paula LópezDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Problemas de Parciales
Cargado por
Paula LópezCopyright:
Formatos disponibles
PROBLEMAS DE PARCIALES
PROBLEMA (1º parcial año 2015). La reacción elemental AB en fase líquida se lleva a cabo en
una batería de tanques isotérmicos conectados en serie, tal como se muestra en la Figura.
El volumen de cada reactor es 100 L. La relación de reciclo usada en el segundo reactor es 1. El
primer tanque se alimenta con un caudal volumétrico de 10L/min y una concentración de reactivo
de 1mol/L. La conversión alcanzada en el primer tanque es del 45%.
a) Calcule la conversión alcanzada en el sistema de reactores.
b) Proponga una modificación al esquema de reactores existente que resulte en un aumento de la
conversión y la producción final alcanzadas.
PROBLEMA (1º parcial año 2016). Dada una reacción reversible elemental en fase líquida A ↔ B,
estime la máxima producción diaria que se puede obtener en una planta que cuenta con tres
reactores TAD de 100 L cada uno. A la temperatura de operación, la conversión de equilibrio es del
76% y la constante de velocidad de la reacción directa es 0.01 min-1. Cada reactor se carga
completamente con una solución 1 mol/L de reactivo A. El tiempo de limpieza, carga,
acondicionamiento y descarga de cada reactor es de 30 min.
PROBLEMA (1º parcial año 2017). La reacción de descomposición de azometano (CH3−N=N−CH3)
en fase gaseosa se lleva a cabo en un reactor tubular con flujo pistón (TUB) que opera
isotérmicamente a 150ºC y 1 atm de presión, según la reacción:
CH3−N=N−CH3⟶CH3−CH3+N2
La velocidad es de primer orden respecto al azometano y la constante de velocidad a 150ºC es
kr=0,15min− 1.
El reactor consta de 100 tubos de 2 cm de diámetro y 6m de longitud conectados en serie. La
alimentación consiste en una mezcla que contiene el 75% de reactivo A y 25% de inertes y un
caudal volumétrico de 15 L/min.
a) Calcule la producción de etano (CH3-CH3) alcanzada en el TUB.
b) Por cuestiones de mantenimiento, se deberá suspender la operación del reactor durante un
tiempo. En la planta se dispone de varios tanques agitados de 85 L cada uno que pueden operar de
manera discontinua (TAD). Calcule el mínimo número de tanques (TAD) que deberán usarse para
igualar la producción del reactor tubular, sabiendo que el tiempo muerto estimado para la
operación discontinua es de 45 minutos. Suponga que los reactores se cargan con la mezcla de
alimentación hasta que la presión es igual a 1atm y la temperatura es 150ºC.
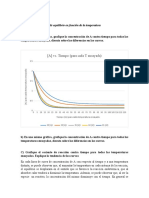
PROBLEMA (adaptado del 2º parcial año 2017). En dos reactores tipo TAC con flujo ideal de 40 L
cada uno conectados en serie, se lleva a cabo la reacción en fase líquida de primer orden A → 2B
de constante cinética 0.05 min-1 , a partir de una corriente de alimentación de 5L/min cuya
concentración (A0 ) es 0.5 mol/L. Suponga que los dos tanques se encuentran operando en estado
estacionario y que se produce un cambio abrupto en la concentración inicial del reactivo tal que
(A0´) es 0.75 mol/L. Encuentre la evolución temporal de la concentración durante este período
transitorio y determine el tiempo en el que se alcanzará la nueva concentración de EE (asumir un
error del 0.1%).
PROBLEMA (1º parcial 2018). La reacción elemental en fase gas 2AB se lleva a cabo en un TAD a
volumen constante de 100 litros. Para una temperatura de 200oC, una presión inicial de 5 at y una
mezcla equimolar de A e inertes se alcanza una producción de 0.045 mol/min y una presión final
de 3.8 at. ¿En cuánto podrá incrementarse la producción si el reactor se opera en las condiciones
óptimas, partiendo de la misma alimentación? Dato: El tiempo muerto se estima en 25 minutos.
PROBLEMA (1º parcial 2018). El reactivo líquido A se descompone según el siguiente sistema de
reacciones:
A R rR = k1CA2 siendo k1 = 0.02 m3/(mol min) (reacción deseada)
A S rS = k2CA siendo k2 = 0.1 min-1
La alimentación consiste en una solución acuosa cuya concentración es CA0 = 40 mol/m3.
a) Para un reactor TAC con flujo ideal, determine la conversión de A y el tiempo espacial que
maximizan la concentración de R. Calcule el rendimiento global de R en dicha condición.
b) Califique la siguiente expresión como “verdadera o falsa”: (Justifique)
Para la reacción dada, es posible obtener un mayor rendimiento global en un reactor TAC que en
un reactor TUB.
c) Suponga que el reactor diseñado en a) se encuentra operando en estado estacionario cuando se
duplica la concentración del reactivo A en la corriente de alimentación. Calcule el tiempo en el que
la concentración de R alcanzará el valor en el nuevo estado estacionario con un error del 0.05%.
Determine el rendimiento global de R, la conversión de A y la concentración de R en el nuevo
estado estacionario.
d) ¿Cuál es la conversión de A que maximiza la concentración del producto S en un TAC?
PROBLEMA (1º parcial 2018). La reacción en fase gas 2AB auto-catalítica cuya cinética es (-rA)=
k[A][B], se lleva a cabo en un rector tubular con flujo pistón de 100 litros. Para una temperatura de
200oC, una presión de operación de 5 at y una mezcla equimolar de A e inertes se alcanza una
producción de 0.305 mol/min cuando se utiliza una relación de reciclo (R) de 0.5 y un caudal de
alimentación de 15L/min ¿En cuánto podrá incrementarse la producción si se utiliza la relación de
reciclo óptima?
También podría gustarte
- A Touch of RuinDocumento314 páginasA Touch of Ruinkaren ham100% (4)
- Ejercicios Reactores 2023 1Documento12 páginasEjercicios Reactores 2023 1Arantxa RoblesAún no hay calificaciones
- DENSIDAD DE HARINASDocumento5 páginasDENSIDAD DE HARINASMariané Chávez100% (1)
- Manual de Frutas y HortalizasDocumento94 páginasManual de Frutas y HortalizasDaniel Cuauhtle NavaAún no hay calificaciones
- 02 Problemas Tema 2 BSTRDocumento6 páginas02 Problemas Tema 2 BSTRL222Aún no hay calificaciones
- Ejercicios de Equilibrio QuímicoDocumento8 páginasEjercicios de Equilibrio QuímicoFrancisco NoéAún no hay calificaciones
- Problemas de ReaccionesDocumento21 páginasProblemas de ReaccionesSteven kevin Choquihuayta letonaAún no hay calificaciones
- Modelamiento y casos especiales de la cinética química heterogéneaDe EverandModelamiento y casos especiales de la cinética química heterogéneaCalificación: 3 de 5 estrellas3/5 (1)
- Purificacion SalmueraDocumento127 páginasPurificacion SalmueraAugusto Ruben Colque AntonioAún no hay calificaciones
- Problemas Diseño de ReactoresDocumento7 páginasProblemas Diseño de Reactoreskari0% (1)
- 4-Sección IV - Monitoreo de Aguas y Ambientes. Validaciones Microbiológicas de ProcesosDocumento76 páginas4-Sección IV - Monitoreo de Aguas y Ambientes. Validaciones Microbiológicas de ProcesosPaula LópezAún no hay calificaciones
- Práctica Laboratorio QuímicaDocumento24 páginasPráctica Laboratorio QuímicaJosé Urday100% (1)
- Ejercicios Propuestos CSTR PFRDocumento3 páginasEjercicios Propuestos CSTR PFRJoseAún no hay calificaciones
- Guía 2 - 2018Documento13 páginasGuía 2 - 2018DarioTejerinaAún no hay calificaciones
- Módulo Balance Parte 1Documento66 páginasMódulo Balance Parte 1May APAún no hay calificaciones
- Problemas - Resueltos - de - Quimica - Analitica - ProblemasDocumento7 páginasProblemas - Resueltos - de - Quimica - Analitica - ProblemasSaraRamirezYepesAún no hay calificaciones
- 5 - Prob Asoc React 11-12 47-60Documento6 páginas5 - Prob Asoc React 11-12 47-60Arnaldo Enrique Rojas CortesAún no hay calificaciones
- Introducción Merged OrganizedDocumento5 páginasIntroducción Merged OrganizedpaulaAún no hay calificaciones
- Problemario Unidad 2 Reactores QuímicosDocumento2 páginasProblemario Unidad 2 Reactores QuímicosSarah LarkAún no hay calificaciones
- Boletin Tema 4Documento2 páginasBoletin Tema 4manu regueiroAún no hay calificaciones
- Primer Serie de ProblemasDocumento17 páginasPrimer Serie de ProblemasRuth HueyopaAún no hay calificaciones
- Series 09-10 - 9Documento17 páginasSeries 09-10 - 9obrani0% (2)
- Problemas de Diseno de Reactores IdealesDocumento5 páginasProblemas de Diseno de Reactores IdealesJose Demons Peña CarvajalAún no hay calificaciones
- Guia de Ejercicio de Reactores Batch y Mezcla Completa.Documento4 páginasGuia de Ejercicio de Reactores Batch y Mezcla Completa.Daniel LeonardezAún no hay calificaciones
- Tema6 EjerciciosDocumento4 páginasTema6 EjerciciosManolitoreyesAún no hay calificaciones
- Problemas-Tema Reactores 22Documento2 páginasProblemas-Tema Reactores 22claudiagAún no hay calificaciones
- 3 - Prob RFP 11-12 23-35Documento4 páginas3 - Prob RFP 11-12 23-35adonis aguero pajueloAún no hay calificaciones
- Tarea 1. Lista de Problemas Reactores Homogéneos IsotérmicosDocumento2 páginasTarea 1. Lista de Problemas Reactores Homogéneos IsotérmicosFrancisco Vicente0% (2)
- Listado Problemas ReactoresDocumento4 páginasListado Problemas ReactoresjorgeAún no hay calificaciones
- Propuestos T03Documento4 páginasPropuestos T03antonioAún no hay calificaciones
- Problemas Adicionales Teoria 2017Documento2 páginasProblemas Adicionales Teoria 2017Juan AparicioAún no hay calificaciones
- Unidad IV - Reactores E. EstacionarioDocumento7 páginasUnidad IV - Reactores E. EstacionarioAgustinaAún no hay calificaciones
- Guia ReactoresDocumento4 páginasGuia ReactoresMatias Ulloa SaavedraAún no hay calificaciones
- Repartido1 2009Documento3 páginasRepartido1 2009Roberto FigueroaAún no hay calificaciones
- Reactores cinética problemasDocumento10 páginasReactores cinética problemasFranz Tucta Huillca0% (1)
- Otros Problemas - reactoresMP - 2223 - SolDocumento8 páginasOtros Problemas - reactoresMP - 2223 - SolIvan FernandezAún no hay calificaciones
- TPNº5 Cinética Química 2018Documento3 páginasTPNº5 Cinética Química 2018Leonardo GimenezAún no hay calificaciones
- Segunda Practica de Cinetica GroverDocumento4 páginasSegunda Practica de Cinetica GroverAgni SelmanAún no hay calificaciones
- U3 ProblemasDocumento9 páginasU3 ProblemasmarianzavaAún no hay calificaciones
- H3-EFECTOS_TERMICOS_EN_REACTORES_IDEALES-2014-2015 campusDocumento5 páginasH3-EFECTOS_TERMICOS_EN_REACTORES_IDEALES-2014-2015 campusCenaida ColinaAún no hay calificaciones
- Serie Unidad 2Documento3 páginasSerie Unidad 2lorenaAún no hay calificaciones
- Examenes de Diseño de Reactores IIDocumento11 páginasExamenes de Diseño de Reactores IIDiogo Lopez MachacaAún no hay calificaciones
- TALLER Ingeniería de Las Reacciones Químicas 1 PDFDocumento4 páginasTALLER Ingeniería de Las Reacciones Químicas 1 PDFAndres LlorenteAún no hay calificaciones
- Guia Tema 2 Analisis de Reactores IdealesDocumento4 páginasGuia Tema 2 Analisis de Reactores Idealesjose carranza leonAún no hay calificaciones
- Guia Practica 1 Cinetica QuímicaDocumento4 páginasGuia Practica 1 Cinetica QuímicaKaticsa Olivera ValentinAún no hay calificaciones
- Problemes Reactors IsotermesDocumento4 páginasProblemes Reactors IsotermesAlbert VictoriAún no hay calificaciones
- Procesos Unitarios - Guía N°3Documento2 páginasProcesos Unitarios - Guía N°3Xime WalburgAún no hay calificaciones
- Serie 04 - Reactores No IsotermicosDocumento4 páginasSerie 04 - Reactores No IsotermicosLuciana NeirotAún no hay calificaciones
- DISEÑO DE REACTORES TALLER EN CLASE UNIVERSIDAD DE PAMPLONADocumento3 páginasDISEÑO DE REACTORES TALLER EN CLASE UNIVERSIDAD DE PAMPLONAAngelo VarelaAún no hay calificaciones
- Guia de Problemas - Reactores IdealesDocumento4 páginasGuia de Problemas - Reactores IdealesDianaMenchacaAún no hay calificaciones
- Guía de Estudio Unidad 4Documento2 páginasGuía de Estudio Unidad 4Ana Victoria Marquez ChaconAún no hay calificaciones
- 420509184Documento19 páginas420509184Cristhofer Renato Brigges LoayzaAún no hay calificaciones
- Problemas de Cinética Metalúrgica - 2Documento2 páginasProblemas de Cinética Metalúrgica - 2deus07Aún no hay calificaciones
- EXAMENSustit2020 1Documento1 páginaEXAMENSustit2020 1Reaven :3Aún no hay calificaciones
- SerieProblemas 16761Documento9 páginasSerieProblemas 16761andrea vargasAún no hay calificaciones
- Problemas Tema2Documento8 páginasProblemas Tema2Pelayo RodrigoAún no hay calificaciones
- Eva Reaqui Ad21Documento3 páginasEva Reaqui Ad21Luis Antonio Sánchez SánchezAún no hay calificaciones
- Enunciados Problemas ReactoresDocumento1 páginaEnunciados Problemas ReactoresAntonio Guexpal TepoxAún no hay calificaciones
- Guía de Ejercicios Reactores IsotérmicosDocumento3 páginasGuía de Ejercicios Reactores IsotérmicosJose David CastroAún no hay calificaciones
- Practico Idea Les 2010Documento14 páginasPractico Idea Les 2010Bartolome Garcia ReyAún no hay calificaciones
- Problemas de Diseno de Reacciones SimplesDocumento2 páginasProblemas de Diseno de Reacciones SimplesNicoleIsabelCifuentesMuñozAún no hay calificaciones
- Asociación de reactores químicosDocumento3 páginasAsociación de reactores químicosJonathan Xavi AguilarAún no hay calificaciones
- Guía de Ejercicios ReactoresDocumento8 páginasGuía de Ejercicios ReactoresAna Virginia MontoyaAún no hay calificaciones
- REACTORES CONTINUOS OPERACIÓN ISOTÉRMICA 2° ParteDocumento3 páginasREACTORES CONTINUOS OPERACIÓN ISOTÉRMICA 2° ParteVanesa acostaAún no hay calificaciones
- Ejercicios IrDocumento11 páginasEjercicios IrAriel FuenteAún no hay calificaciones
- Guía #3 - Reactores Continuos en Estado EstacionarioDocumento9 páginasGuía #3 - Reactores Continuos en Estado EstacionarioNicole Retamal YevenesAún no hay calificaciones
- Guía #4 - Reactores MultiplesDocumento7 páginasGuía #4 - Reactores MultiplesNicole Retamal YevenesAún no hay calificaciones
- Problemas de ParcialesDocumento2 páginasProblemas de ParcialesPaula LópezAún no hay calificaciones
- Cuadernillo-PRIMERA PARTE (Teoría)Documento28 páginasCuadernillo-PRIMERA PARTE (Teoría)Paula LópezAún no hay calificaciones
- TC - Introducción y Conceptos Básicos - 2021Documento19 páginasTC - Introducción y Conceptos Básicos - 2021Nicolas VentreAún no hay calificaciones
- TP 3 y 4 Volumetría de Precipitación - Volumetría de Formación de ComplejosDocumento8 páginasTP 3 y 4 Volumetría de Precipitación - Volumetría de Formación de ComplejosPaula LópezAún no hay calificaciones
- Ingeniería Química - Plan 2003 (Texto Ordenado) Sujeto A VerificacionDocumento1 páginaIngeniería Química - Plan 2003 (Texto Ordenado) Sujeto A VerificacionPaula LópezAún no hay calificaciones
- Trabajo Especial 1 - Calor 2023Documento1 páginaTrabajo Especial 1 - Calor 2023Paula LópezAún no hay calificaciones
- Transferencia de Calor 2023: - 13 A 15 HS: Teoría - 15 A 16:30 HS: Práctica I - 16:30 A 18 HS: Práctica IIDocumento3 páginasTransferencia de Calor 2023: - 13 A 15 HS: Teoría - 15 A 16:30 HS: Práctica I - 16:30 A 18 HS: Práctica IIPaula LópezAún no hay calificaciones
- Calendario de clases de Seguridad e HigieneDocumento1 páginaCalendario de clases de Seguridad e HigienePaula LópezAún no hay calificaciones
- 01 Guia Visual para La Medición de Corriente en DC (Pt100)Documento21 páginas01 Guia Visual para La Medición de Corriente en DC (Pt100)Paula LópezAún no hay calificaciones
- 00 Guia Protocolo de ProducciònDocumento2 páginas00 Guia Protocolo de ProducciònPaula LópezAún no hay calificaciones
- 02 Herramientas Manuales de Taller - Guía VisualDocumento32 páginas02 Herramientas Manuales de Taller - Guía VisualPaula LópezAún no hay calificaciones
- 01 Funcionamiento y Capacidades de Las Válvulas Reguladoras de PresiónDocumento4 páginas01 Funcionamiento y Capacidades de Las Válvulas Reguladoras de PresiónJésica HerreraAún no hay calificaciones
- Instalaciones y cañerías guía visualDocumento26 páginasInstalaciones y cañerías guía visualPaula LópezAún no hay calificaciones
- Guia ParticulasDocumento43 páginasGuia Particulasvalidacion1127100% (2)
- TC - CONDUCCION DE CALOR EE Clase 3 Conduccion 2020 Aletas No PresencialDocumento12 páginasTC - CONDUCCION DE CALOR EE Clase 3 Conduccion 2020 Aletas No PresencialPaula LópezAún no hay calificaciones
- Soluciones amortiguadoras: preparación y estudio de su capacidad reguladora del pHDocumento18 páginasSoluciones amortiguadoras: preparación y estudio de su capacidad reguladora del pHmelanieAún no hay calificaciones
- Reporte de SolucionesDocumento30 páginasReporte de SolucionesArnoldo DanielAún no hay calificaciones
- MA465 - S06 - S17 - CS06 - Caso 5 - Crisis Ambiental SJL - AlumnosDocumento11 páginasMA465 - S06 - S17 - CS06 - Caso 5 - Crisis Ambiental SJL - AlumnosSebastián MarceloAún no hay calificaciones
- Temas para El Examen ComplexivoDocumento270 páginasTemas para El Examen ComplexivoAlejandra LmaAún no hay calificaciones
- Calculo constante equilibrio función temperaturaDocumento3 páginasCalculo constante equilibrio función temperaturaFredy GomezAún no hay calificaciones
- Proyecto U4 Balances de MasaDocumento8 páginasProyecto U4 Balances de MasaDiego FloresAún no hay calificaciones
- Preparación de Soluciones QuímicasDocumento4 páginasPreparación de Soluciones QuímicasMiguel MelilloAún no hay calificaciones
- Cinetica (1) - EjerciciosDocumento4 páginasCinetica (1) - EjerciciosItala AlejandroAún no hay calificaciones
- Tema 1 Disoluciones y ColoidesDocumento39 páginasTema 1 Disoluciones y Coloides1111Aún no hay calificaciones
- Cuestionario de seguridad industrialDocumento23 páginasCuestionario de seguridad industrialSolansh Arlet Ledezma PazAún no hay calificaciones
- Informe Factores Que Afectan La Rapidez de Una ReacciónDocumento7 páginasInforme Factores Que Afectan La Rapidez de Una ReacciónMARIELBY RODRIUEZAún no hay calificaciones
- Merrill Crowe - ProcesamientosDocumento30 páginasMerrill Crowe - ProcesamientosTomás Esteban Espejo Cueva100% (1)
- Procesamiento Items de Ensayo Piccap 2020Documento4 páginasProcesamiento Items de Ensayo Piccap 2020coordinadora calidadAún no hay calificaciones
- Aloe Vera Proceso de ExtraccionDocumento4 páginasAloe Vera Proceso de ExtraccionLAún no hay calificaciones
- Determinación de Parámetros de Calidad en Aceites y GrasasDocumento17 páginasDeterminación de Parámetros de Calidad en Aceites y GrasasPaola Rivera0% (1)
- 2 APE QUIMICA ANEXO AS2022klever GuanotasigDocumento14 páginas2 APE QUIMICA ANEXO AS2022klever GuanotasigJuan ToazaAún no hay calificaciones
- Reaccion B-ZDocumento8 páginasReaccion B-ZJessica Rojas Carmona100% (1)
- 2 CN Química 2021Documento50 páginas2 CN Química 2021Natalia ForeroAún no hay calificaciones
- PD FQ 3 Eso 1011Documento30 páginasPD FQ 3 Eso 1011cienciasmcrespo2010Aún no hay calificaciones
- 5.4 Aplicacion en Evaporadores y CondensadoresDocumento43 páginas5.4 Aplicacion en Evaporadores y Condensadoresjorge mayAún no hay calificaciones
- Formato - de - Sílabo - Dga - (1) QUIMICA - NATHALY REYES 2024-Signed-SignedDocumento11 páginasFormato - de - Sílabo - Dga - (1) QUIMICA - NATHALY REYES 2024-Signed-Signedalexfreecash17Aún no hay calificaciones
- Práctica #10Documento6 páginasPráctica #10María Paula Carvajal NaviaAún no hay calificaciones
- Informe Coeficiente de DifusividadDocumento16 páginasInforme Coeficiente de Difusividadbarayanmg42Aún no hay calificaciones