Documentos de Académico
Documentos de Profesional
Documentos de Cultura
GPC Cardiopatias
Cargado por
Marcela RodriguezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
GPC Cardiopatias
Cargado por
Marcela RodriguezCopyright:
Formatos disponibles
FCV
GUIA MEDICA DE CARDIOPATIAS CONGENITAS Versión: 1 GPC-MA503-31
PROCESO: MÉDICO ASISTENCIAL – CUIDADO
Página 1 de 6
INTENSIVO NEONATAL
1. OBJETIVO
Brindar un adecuado diagnóstico de las cardiopatías congénitas en el recién nacido para mejorar con un
tratamiento inicial pertinente al pronóstico de estos pacientes.
Facilitar herramientas para la detección temprana de signos de cardiopatías congénitas para indicaciones
de estudios imagenológicos y un pronto manejo de los recién nacidos.
2. POBLACIÓN OBJETO
Todo recién nacido con patología cardiaca que ingrese a la unidad neonatal, remitidos o nacidos en la
institución.
3. USUARIOS A QUIENES SE DIRIGE Y ÁMBITO GENERAL DE APLICACIÓN
Esta guíaa será el patrón de manejo de todo neonato que presente cardiopatía congénita durante su
estancia en la unidad neonatal de la FCV y será revisada por personal médico, enfermería y terapia
respiratoria que labora en la Unidad Neonatal.
.
4. MÉTODO DE CONSENSO UTILIZADO
La guía fue basada en textos vesicos de Neonatología y artículos clínicos de temas de revisión de
cardiopatías congénitas.
5. ASPECTOS CLÍNICOS
a. Definición de la patología.
Anomalía estructural del corazón o de los grandes vasos intratorácicos que real o potencialmente tienen
significado funcional y que se origina durante el desarrollo embrionario cardiovascular. Se encuentra
presente al momento del nacimiento y puede ser diagnosticada ¨in utrero¨.
b. Etiología.
Anomalías cromosómicas
Trisomía 21 (40%) Canal auriculoventricular, Comunicación auricular, comunicación interventricular,
Fallot, Ductus arterioso.
Trisomia 13, 18 (85%): comunicación aurículoventricular, Coartación de la aorta, displasias
polivavulares y cardiopatías complejas.
Síndrome de Turner (35%) Coartación de la aorta, Valvulopatía aortica.
Síndromes no cromosómicos
Síndrome Noonan (50%): Comunicación auricular, Miocardiopatía.
Asociación Charge (80%): Comunicación interventricular, Comunicación auricular, Ductus arterioso
persistente.
Asociación VACTERL (70%): Comunicación interventricular, Tetralogía de Fallot.
Síndrome de Williams (75%): Estenosis supravalvular arterial.
Di George (85%): Interrupción Arco Aórtico, Truncus Arteriosus.
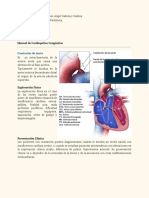
c. Signos y síntomas.
Hallazgos físicos que pueden dar indicios de cardiopatía congénita, no obstante, pueden estar ausentes
en los recién nacidos con cardiopatías ductus-dependientes.
Frecuencia cardiaca anormal: si presenta valores de frecuencia cardiaca de 90-160 latidos por minutos
en los primeros 6 días de vida, es necesario realizar un electrocardiograma para determinar si presenta
arritmia y para guiar conductas adicionales.
Impulso cardiaco: Nos ayuda a determinar si la ubicación del corazón se encuentra normalmente al lado
izquierdo y descartar dextrocardia. Impulso cardiaco en región paraesternal inferior izquierdo es
sugestivo de sobrecarga de presión o volumen.
Elaborado por: : Neonatólogo UCI Neonatal Aprobado por: Subgerente Medico ICF
Revisado por: Oficina de Calidad ICF Fecha de Aprobación: 2019-02-01
Todos los derechos reservados. FCV y FCV Zona Franca S.A.S
FCV
GUIA MEDICA DE CARDIOPATIAS CONGENITAS Versión: 1 GPC-MA503-31
PROCESO: MÉDICO ASISTENCIAL – CUIDADO
Página 2 de 6
INTENSIVO NEONATAL
Sonidos cardíacos anormales: los siguientes ruidos cardíacos adicionales pueden estar asociados con
anomalías cardíacas
Clics asistólicos: ocurren en la estenosis de la válvula semilunar, válvula aórtica bicúspide.
Clics mesodiastólicos: propaso de la válvula mitral y con anomalía de Ebstein de la válvula tricúspide.
Galope S3: disfunción ventricular o sobrecarga de volumen del ventrículo izquierdo.
Roce pericárdico: derrame pericardio y pericarditis.
Soplos patológicos
Hepatomegalia: Es un hallazgo inespecífico, se puede observar en recién nacidos con insuficiencia
cardiaca y aumento de la presión venosa central.
Pulsos disminuidos en las extremidades inferiores: Es parte esencial para identificar cardiopatía
congénita crítica.
Tensión arterial diferencial entre miembros superiores e inferiores
Factores prenatales asociados a cardiopatías
Diabetes gestacional: Hipertrofia septal asimétrica.
Lupus: Bloqueo AV completo.
Rubeola: Ductus arterioso persistente, estenosis pulmonar periférica.
Aspirina: Hipertensión pulmonar.
Trimetadiona: Comunicacion interauricular, Tetralogía de Fallot
Infección viral: Miocarditis.
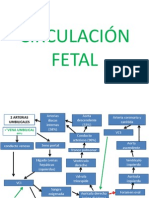
Clasificación
Cardiopatías no Cianógenas
1. Flujo pulmonar aumentado.
Ductus arteriosus.
Comunicación interventricular.
Comunicación interauricular.
Canal auriculoventiricular.
Ventana aortopulmonar.
2. Flujo pulmonar normal.
Estenosis Aórtica
Coartación aórtica
Estenosis mitral
Interrupción del Arco Aórtico
Cardiopatías Cianógenas
3. Flujo pulmonar aumentado.
Transposición de Grandes Arterias.
Corazón izquierdo hipoplásico.
Ventrículo único.
Truncus Arteriosus.
4. Flujo pulmonar disminuido.
Tetralogia de Fallot.
Atresia pulmonar.
Anomalía de Ebstein.
Estenosis pulmonar.
Atresia tricúspidea.
d. Abordaje diagnóstico
i. Historia clínica y examen físico
Elaborado por: : Neonatólogo UCI Neonatal Aprobado por: Subgerente Medico ICF
Revisado por: Oficina de Calidad ICF Fecha de Aprobación: 2019-02-01
Todos los derechos reservados. FCV y FCV Zona Franca S.A.S
FCV
GUIA MEDICA DE CARDIOPATIAS CONGENITAS Versión: 1 GPC-MA503-31
PROCESO: MÉDICO ASISTENCIAL – CUIDADO
Página 3 de 6
INTENSIVO NEONATAL
Fisiopatología.
No cianógenas:
Cortocircuitos de Izquierda a Derecha:
Tiene como factor común el hiperflujo pulmonar, el cual se asocia a hipertensión pulmonar cuando el
defecto es a nivel ventricular o arterial. Este hiperflujo se debe al incremento del retorno venoso a
cavidades izquierdas, con aumento de presión de final de diástole de estas cavidades, que lleva a
hipertensión venosa pulmonar e hipertensión hidrostática capilar pulmonar, favoreciendo el paso de
líquido al intersticio pulmonar. Esta acumulación produce inicialmente clínica de TTRN que puede
incrementar hasta edema pulmonar. El compromiso pulmonar lleva a una mayor hipertensión arterial
pulmonar, con incremento de la presión diastólica de las cavidades derechas y congestión venosa
sistémica con Hepatomegalia. La magnitud del corto circuito depende del tamaño del defecto cardiaco,
y más importante de la relación entre la resistencia vascular pulmonar y sistémica. A menor
resistencia pulmonar y mayor resistencia periférica, mayor corto circuito. Como el recién nacido tiene
una resistencia vascular pulmonar relativamente alta, solo con la caída de ésta, al final de la
10,11,12,13
segunda semana, aparecen los signos clínicos significativos.
Obstructivas
Habitualmente nacen en buenas condiciones sin manifestación de alteración cardiaca por horas y / o
días, siempre y cuando tengan Ductus permeable con buen corto circuito de der. a izq. para
mantener la circulación sistémica.
En el corazón izq. hipoplásico, el cortocircuito es obligadamente auricular (foramen oval) con
sobrecarga e hiperflujo pulmonar. Cuando el Ductus se contrae para cerrarse es cuando de forma
brusca se compromete severamente la circulación periférica, apareciendo insuficiencia cardiaca y
shock Cardiogénico. Las altas presiones en la aurícula izq. llevan a edema pulmonar, así como las
altas presiones diastólicas en corazón der. llevan a congestión sistémica y Hepatomegalia con
desarrollo de acidosis metabólica severa.
Cianógenas
En las cardiopatías por falla de mezcla entre circulaciones pulmonar y sistémica, la sangre
desaturada que retorna por las venas cava a la aurícula der., vuelve a la aorta y a la circulación
sistémica sin pasar por la circulación pulmonar. Por otro parte, la sangre oxigenada que regresa por
las venas pulmonares a la aurícula izquierda vuelve a dirigirse a la circulación pulmonar sin alcanzar la
circulación sistémica. Esto ocurre en la transposición de las grandes arterias. Se producen así dos
circuitos independientes, uno sistémico de sangre desaturada, que lleva a Hipoxemia marcada, y
uno de sangre oxigenada pulmonar, que no es utilizada. En vida intrauterina existen dos sitios de
mezcla, el foramen oval y el Ductus arterioso, donde se produce circuito bidireccional que permite la
sobrevida del neonato por algunas horas, estos corto circuitos son frecuentemente insuficientes por
cierre del Ductus en las primeras horas y del foramen en los primeros días. En las cardiopatías por
obstrucción al flujo pulmonar; no necesariamente a nivel valvular. La resultante común es que la
obstrucción al flujo pulmonar obliga a un corto circuito de derecha a izquierda entrando sangre
desaturada al territorio sistémico con la consecuente Hipoxemia. Cuando la obstrucción es total
"atresia pulmonar”, el flujo pulmonar depende de la persistencia del Ductus permeable.
ii. Ayudas diagnósticas y pruebas complementarias
Las ayudas diagnósticas a solicitar se encuentran relacionadas dentro de las guías y/o instructivos
específicos para cada patología.
iii. Formulación explícita de recomendaciones para el diagnóstico
Las recomendaciones se encuentran relacionadas dentro del desarrollo del presente documento y en
las guías y/o instructivos específicos para cada patología.
Elaborado por: : Neonatólogo UCI Neonatal Aprobado por: Subgerente Medico ICF
Revisado por: Oficina de Calidad ICF Fecha de Aprobación: 2019-02-01
Todos los derechos reservados. FCV y FCV Zona Franca S.A.S
FCV
GUIA MEDICA DE CARDIOPATIAS CONGENITAS Versión: 1 GPC-MA503-31
PROCESO: MÉDICO ASISTENCIAL – CUIDADO
Página 4 de 6
INTENSIVO NEONATAL
e. Abordaje terapéutico
i. Manejo médico
Conducta general frente a paciente cianótico con probable cardiopatía.
Ambiente térmico.
Hematocrito a 40 - 45 %.
Líquidos endovenosos 85 - 90 cc/kg/día.
Si la Hipoxemia es muy severa, administrar O2 hasta máximo 80% de SAO2 para evitar cierre del
Ductus.
Estabilización de alteraciones metabólicas.
Ventilación asistida si ph es menor de 7.25, po2 menor de 50 o apneas a repetición.
Uso de prostaglandinas
Cardiopatía Ductus dependiente estable con evidencia de buena permeabilidad ductal.
Cardiopatía Ductus dependiente en malas condiciones generales, con evidencia de cierre ductual y
con hipoxemia importante y acidosis metabólica.
ii. Cuidados de enfermería, terapias y nutrición.
DIAGNOSTICO DE
INTERVENCION ACTIVIDADES RESPONSABLE
ENFERMERIA
Realizar una valoración
exhaustiva de la circulación
periférica (comprobar pulsos
periféricos, edema, relleno
capilar, color y temperatura de
las extremidades.
Monitorizar los signos vitales
Disminución del gasto
con frecuencia
cardiaco
Cuidados cardiacos Observar signos y síntomas de
Riesgo de disminución de
Oxigenoterapia disminución del gasto cardiaco.
gasto cardiaco.
Regulación Mantener la permeabilidad de
Deterioro del intercambio
hemodinámica las vías aéreas.
de gases
Monitorización Administrar oxigeno
Perfusión tisular periférica
respiratoria suplementario según ordenes Pediatra
ineficaz
Monitorización de médicas. Enfermería
Deterioro de la ventilación
signos vitales Controlar la eficacia de la Psicología
espontanea
Manejo de la vía aérea oxigenoterapia (pulsoximetria, Terapia
Riesgo de disminución de
Administración de gasometría). respiratoria
la perfusión tisular
medicación Monitorizar la presencia y
Alteracion de la nutricion
Aumentar el calidad de los pulsos.
por defecto
afrontamiento Monitorizar si hay cambios de
Ansiedad de los padres
Prevención de las cianosis central y periférica.
Deterioro de la integridad
ulceras por presión. Correctos en la administración
cutanea
de medicamentos.
Anotar y valorar el balance
hídrico, peso diario y control de
diuresis.
Alentar a la familia a manifestar
sus sentimientos, percepciones
y miedos respecto a su hijo
enfermo.
Elaborado por: : Neonatólogo UCI Neonatal Aprobado por: Subgerente Medico ICF
Revisado por: Oficina de Calidad ICF Fecha de Aprobación: 2019-02-01
Todos los derechos reservados. FCV y FCV Zona Franca S.A.S
FCV
GUIA MEDICA DE CARDIOPATIAS CONGENITAS Versión: 1 GPC-MA503-31
PROCESO: MÉDICO ASISTENCIAL – CUIDADO
Página 5 de 6
INTENSIVO NEONATAL
Escucha activa
Proporcionar información
objetiva respecto del
diagnóstico, tratamiento y
pronóstico.
Fomentar la implicación familiar.
Vigilar y registrar el estado de la
piel diariamente. Eliminar la
humedad excesiva en la piel
causada por la transpiración,
drenaje de heridas y orina o
heces. Cambios posturales
cada dos horas.
Higiene e hidratación adecuada
de piel y mucosas
iii. Formulación explícita de recomendaciones para el tratamiento
Las recomendaciones se encuentran relacionadas dentro del desarrollo del presente documento y en
las guías y/o instructivos específicos para cada patología.
f. Criterios de egreso hospitalario y recomendaciones
Entrenamiento al padre/cuidador en el manejo del neonato, incluyendo medicamentos
Realización de ayudas diagnósticas para confirmar/descartar cardiopatía congénita según la sospecha
clínica inicial
No necesidad de soporte vasoactivo
Citas de seguimiento ambulatorio
Estabilidad hemodinámica
g. Educación
La educación al cuidador al momento del alta se realiza según las siguientes recomendaciones:
I-MA802-12 Educación a Padres para el Cuidado del Recién Nacido en Casa
6. INDICADORES O PUNTOS CLAVE PARA MEDIR LA ADHERENCIA.
La medición de adherencia a esta guía se realizará de forma anual de acuerdo con lo establecido en el
documento I-GCAL101-06 Elaboración, Adaptación y Adopción de Guías de Práctica Clínica en la FCV
junto con los resultados del perfil epidemiológico institucional.
7. REGISTRÓ DE CONFLICTO DE INTERESES.
No hay conflicto de interés. El grupo acepta las conductas establecidas basadas en evidencias actuales.
Elaborado por: : Neonatólogo UCI Neonatal Aprobado por: Subgerente Medico ICF
Revisado por: Oficina de Calidad ICF Fecha de Aprobación: 2019-02-01
Todos los derechos reservados. FCV y FCV Zona Franca S.A.S
FCV
GUIA MEDICA DE CARDIOPATIAS CONGENITAS Versión: 1 GPC-MA503-31
PROCESO: MÉDICO ASISTENCIAL – CUIDADO
Página 6 de 6
INTENSIVO NEONATAL
8. BIBLIOGRAFÍA.
CDC’s National Center on Birth Defects and Developmental Disabilities (NCBDDD). Improving the
Health of People Across the Lifespan: NCBDDD’S CONGENITAL HEART DEFECTS TRACKING
AND RESEARCH. Enero 8 , 2018.
Robert L Geggel, MD. Cardiac causes of cyanosis in the newborn - UpToDate 2018
Robert L Geggel, MD. Diagnosis and initial management of cyanotic heart disease in the newborn.
UpToDate 2018.
Carolyn A Altman, MD. Identifying newborns with critical congenital heart disease. UpToDate 2018.
Matt Oster, MD, MPH. Newborn screening for critical congenital heart disease using pulse oximetry
.UpToDate 2018.
Mihaela Patriciu. Et col. Pulse Oximetry During the First 24 Hours as a Screening Tool For
Congenital Heart Defects. The Journal of Critical Care Medicine 2017;3(1):12-17.
Philip Roth, MD, PhD*. Pulse Oximetry and the Neonate. Pediatrics in Review. Vol. 37 No. 9
SEPTEMBER 2016.
Guidelines for the Management of Congenital Heart Diseases. Cardiology in the Young (2017),
27(Suppl. 3), S1–S105.
Gabriel Diaz gongora et col. Cardiología pediatrica. Mc Graw- Hill interamericana
Geva T, Martins J, Wald R. Atrial septal defects. Lancet 2014;383:1921-193.
Goldberg S, et al. Atrial Septal Defects. Chapter 15. pp 159 – 167. En: Muñoz R. et al. (eds.). Critical
Care of Children with Heart Disease: Basic Medical and Surgical Concepts. Spreinger-Verlag.
London. 2010.
Mogullansky D, et al. Venricular Septal Defects. Chapter 16. pp 169 – 176. En: Muñoz R. et al.
(eds.). Critical Care of Children with Heart Disease: Basic Medical and Surgical Concepts. Spreinger-
Verlag. London. 2010
Kozik D, et al. Patent Ductus Arteriosus. Chapter 14. pp 145 – 157. En: Muñoz R. et al. (eds.).
Critical Care of Children with Heart Disease: Basic Medical and Surgical Concepts. Spreinger-Verlag.
London. 2010.
9. CONTROL DE CAMBIOS
VERSIÓN FECHA DE REVISIÓN DESCRIPCIÓN DEL PARTICIPANTES
CAMBIO
Emisión del documento. Jorge Alvarado – Neonatólogo UCI
0 2016-09-05 Proviene de G-UCINEO-13 Neonatal
(Versión 0)
Angélica Lucero Ortiz Córdoba –
1 2019-02-01 Revisión del documento Residente UCIP UDES 3º año
María Azucena Niño Tovar – Pediatra
Neonatóloga, Especialista en Bioética
Mary Yaneth Mendoza Carreño –
Enfermera
Leidy Andrea Manrique Toloza –
Enfermera.
Elaborado por: : Neonatólogo UCI Neonatal Aprobado por: Subgerente Medico ICF
Revisado por: Oficina de Calidad ICF Fecha de Aprobación: 2019-02-01
Todos los derechos reservados. FCV y FCV Zona Franca S.A.S
También podría gustarte
- Urgencias médicas en el consultorio odontológico: Conocimientos básicos odontológicos, #2De EverandUrgencias médicas en el consultorio odontológico: Conocimientos básicos odontológicos, #2Calificación: 5 de 5 estrellas5/5 (1)
- Sistema de CanalesDocumento475 páginasSistema de CanalesVictorianolopez100% (1)
- Cardiopatias Congenitas 2020Documento57 páginasCardiopatias Congenitas 2020Percy Vara CelisAún no hay calificaciones
- Cardiopatias Congénitas AcianóticasDocumento21 páginasCardiopatias Congénitas Acianóticasjoha corralesAún no hay calificaciones
- Clase 5 Cabeza y CuelloDocumento11 páginasClase 5 Cabeza y CuelloCristobal Alexander Alcantara YañezAún no hay calificaciones
- Pedriatrica, Casos Clinicos de CardiologiaDocumento10 páginasPedriatrica, Casos Clinicos de Cardiologiagiohanis caballeroAún no hay calificaciones
- Raul PrebischDocumento9 páginasRaul PrebischWilder Ccopa MamaniAún no hay calificaciones
- Cardiopatias CongenitasDocumento48 páginasCardiopatias CongenitasVerónica Ñacato Pincay0% (1)
- Manual para la prevención de la enfermedad coronaria: Consejos para mejorar la calidad de vidaDe EverandManual para la prevención de la enfermedad coronaria: Consejos para mejorar la calidad de vidaAún no hay calificaciones
- Cardiopatia CongenitaDocumento18 páginasCardiopatia Congenitadaniela vargasAún no hay calificaciones
- Ejercicios de IntervalosDocumento2 páginasEjercicios de IntervalosRaul V. Meza Ccorahua100% (1)
- Sindrome Ventriculo IzqDocumento20 páginasSindrome Ventriculo IzqJuan Krlos Escalante MontoyaAún no hay calificaciones
- Sindromes Cardiologicos PediatricosDocumento18 páginasSindromes Cardiologicos Pediatricosjimmy SaavedraAún no hay calificaciones
- Guia de Practica Clinica Del Recien Nacido Con Asfixia PerinatalDocumento9 páginasGuia de Practica Clinica Del Recien Nacido Con Asfixia PerinatalMarcela RodriguezAún no hay calificaciones
- Tetralogía de FallotDocumento6 páginasTetralogía de FallotnicolasAún no hay calificaciones
- PAE FinalDocumento30 páginasPAE FinalOwell IgorAún no hay calificaciones
- PAE Definitivo Caso CCDocumento24 páginasPAE Definitivo Caso CCOwell IgorAún no hay calificaciones
- ECCRI Hipertensión - PulmonarDocumento13 páginasECCRI Hipertensión - Pulmonarseba_garcia2003Aún no hay calificaciones
- Cardiopatías Congénitas.Documento12 páginasCardiopatías Congénitas.Cintia BonillaAún no hay calificaciones
- Repercusiones Del Embarazo Sobre Las Cardiopatías y VicersaDocumento68 páginasRepercusiones Del Embarazo Sobre Las Cardiopatías y VicersaSabrina YalliAún no hay calificaciones
- Diapos Cardio SinDocumento117 páginasDiapos Cardio SinDaniela GrauAún no hay calificaciones
- MQ2 - Tema 1.2Documento4 páginasMQ2 - Tema 1.2Maria Escarabajal FernándezAún no hay calificaciones
- 42 Cardiopatias Congenitas WordDocumento9 páginas42 Cardiopatias Congenitas WordElkins Guivar OrtizAún no hay calificaciones
- Cardiopatias Congenitas AcianoticasDocumento48 páginasCardiopatias Congenitas AcianoticasAlejandra PalaciosAún no hay calificaciones
- Cardiopatias CongenitasDocumento51 páginasCardiopatias Congenitascarlos y ashley selena mi unica familiaAún no hay calificaciones
- Cardiopatias CongénitasDocumento17 páginasCardiopatias CongénitasVitor FloreAún no hay calificaciones
- Trastornos CardiovascularesDocumento13 páginasTrastornos CardiovascularesPau RoblesAún no hay calificaciones
- Cardiopatía CongénitaDocumento4 páginasCardiopatía CongénitaJuan Carlos JimenezAún no hay calificaciones
- Insuficiencia Cardiaca AgudaDocumento21 páginasInsuficiencia Cardiaca Agudamariana virguezAún no hay calificaciones
- Presenta: Mariana Torres MoránDocumento21 páginasPresenta: Mariana Torres Morándaniel sanchezAún no hay calificaciones
- Cardiopatías Congénitas PediatríaDocumento44 páginasCardiopatías Congénitas PediatríaCitlaliAún no hay calificaciones
- Cardiopatía CongénitaDocumento11 páginasCardiopatía CongénitaNayerlyn CedanoAún no hay calificaciones
- IccDocumento12 páginasIccLety Flores OrtizAún no hay calificaciones
- Estenosis PulmonarDocumento6 páginasEstenosis Pulmonarcorazon mabelAún no hay calificaciones
- Cardiopatias CongenitasDocumento12 páginasCardiopatias CongenitasNicole MartínezzAún no hay calificaciones
- Cardiopatías CongénitasDocumento22 páginasCardiopatías CongénitasSary AtenciaAún no hay calificaciones
- Evidencia 3 - Hito 4Documento21 páginasEvidencia 3 - Hito 4Barbara Claudia Bracamonte MuñozAún no hay calificaciones
- Gccv09-01 Guia Enfermedad Valvular MitralDocumento9 páginasGccv09-01 Guia Enfermedad Valvular MitralAlexander Grimaldi E.Aún no hay calificaciones
- CardiologiaDocumento30 páginasCardiologiaWilliam Javier Tobar ErazoAún no hay calificaciones
- CardiovascularDocumento13 páginasCardiovascularHarold Cedeño EscalonaAún no hay calificaciones
- Libro Cardiopatias Dra Silva (17290)Documento75 páginasLibro Cardiopatias Dra Silva (17290)SALOME PANTOJAAún no hay calificaciones
- Conducto Arterioso PersitenteDocumento6 páginasConducto Arterioso PersitentePaloma GalindoAún no hay calificaciones
- Circulación FetalDocumento20 páginasCirculación FetalJorge Obetth CastellanosAún no hay calificaciones
- Valvulopatía MitralDocumento2 páginasValvulopatía MitralEduardo GonzálezAún no hay calificaciones
- Cardiopatías Congénitas ClaseDocumento49 páginasCardiopatías Congénitas ClaseEdward AlfonsoAún no hay calificaciones
- Cardiopatías Congénitas: Frecuencia Relativa de Las CCDocumento5 páginasCardiopatías Congénitas: Frecuencia Relativa de Las CCGala BruggeAún no hay calificaciones
- Cardiopatia y EmbarazoDocumento37 páginasCardiopatia y EmbarazoIsai GutierrezAún no hay calificaciones
- 11ava Clase Pediatría II Uc Cardiopatias Congenitas IDocumento36 páginas11ava Clase Pediatría II Uc Cardiopatias Congenitas IJesus Castro GonzalesAún no hay calificaciones
- Insuificiencia y CardiopatiasDocumento7 páginasInsuificiencia y Cardiopatiasleonardo daniel morales briceñoAún no hay calificaciones
- CardiopatiasDocumento57 páginasCardiopatiasYesidAún no hay calificaciones
- Cardiopatias Congenicas AcianoticasDocumento66 páginasCardiopatias Congenicas AcianoticasJUDITH INGAAún no hay calificaciones
- Fisiopatologia HumanaDocumento9 páginasFisiopatologia HumanaJimmy Alexis Lira HuamanAún no hay calificaciones
- Cardiopatias en El EmbarazoDocumento31 páginasCardiopatias en El Embarazoalbert540Aún no hay calificaciones
- HemodinamiaDocumento8 páginasHemodinamiaCatalinaAún no hay calificaciones
- Capitulo Pediatria: Dra. Ana Gariza SolanoDocumento61 páginasCapitulo Pediatria: Dra. Ana Gariza Solanoluis alonso moralesAún no hay calificaciones
- Trabajo Autonomo 11Documento5 páginasTrabajo Autonomo 11Andy Belen MonterosAún no hay calificaciones
- 9 Estenosis AorticaDocumento14 páginas9 Estenosis AorticaJulián David RodriguezAún no hay calificaciones
- Cardiopatias-Alumnos - 2015 (Imprimir) PDFDocumento89 páginasCardiopatias-Alumnos - 2015 (Imprimir) PDFnadiaAún no hay calificaciones
- Conducto Arterioso PersistenteDocumento25 páginasConducto Arterioso PersistenteMary QuilliAún no hay calificaciones
- Fisiopato NeiyerDocumento4 páginasFisiopato NeiyerOsmari MirandaAún no hay calificaciones
- Adulto MayorDocumento7 páginasAdulto Mayorlorena ruizAún no hay calificaciones
- Valvulopatías Estenosis AorticaDocumento3 páginasValvulopatías Estenosis AorticaSusana MenesesAún no hay calificaciones
- ICC en Pediatia 2018Documento12 páginasICC en Pediatia 2018saimar segoviaAún no hay calificaciones
- CardiopatiasDocumento14 páginasCardiopatiasana.kleangroupAún no hay calificaciones
- Manual de CardiopatíasDocumento26 páginasManual de CardiopatíasJohana BenitezAún no hay calificaciones
- Asistencia Ventilatoria en Neonatos: Proceso: Médico AsistencialDocumento8 páginasAsistencia Ventilatoria en Neonatos: Proceso: Médico AsistencialMarcela RodriguezAún no hay calificaciones
- GPC Atencion Del Niño SanoDocumento5 páginasGPC Atencion Del Niño SanoMarcela RodriguezAún no hay calificaciones
- Respuestas Test de Autoevaluaci N Cap Tulo 2 El Paciente NeonatalDocumento2 páginasRespuestas Test de Autoevaluaci N Cap Tulo 2 El Paciente NeonatalMarcela RodriguezAún no hay calificaciones
- GPC Convulsiones NeonatalesDocumento9 páginasGPC Convulsiones NeonatalesMarcela RodriguezAún no hay calificaciones
- Fresenius Injectomat MC Agilia Bomba de Jeringa Funciona Con Batera y Conectado A RedDocumento1 páginaFresenius Injectomat MC Agilia Bomba de Jeringa Funciona Con Batera y Conectado A RedMarcela RodriguezAún no hay calificaciones
- Respuestas Test de Autoevaluaci N Cap Tulo 1 Unidades de Cuidados IntensivosDocumento2 páginasRespuestas Test de Autoevaluaci N Cap Tulo 1 Unidades de Cuidados IntensivosMarcela RodriguezAún no hay calificaciones
- Estrategias Del Cuidado Humanizado Implementadas en Las Unidades de Cuidado Crítico Neonatal en Los Últimos 5 AñosDocumento60 páginasEstrategias Del Cuidado Humanizado Implementadas en Las Unidades de Cuidado Crítico Neonatal en Los Últimos 5 AñosMarcela RodriguezAún no hay calificaciones
- Medicamento NastacuasDocumento2 páginasMedicamento NastacuasMarcela RodriguezAún no hay calificaciones
- FR-GDU-64 Registro y Control de Muestras de OrinaDocumento1 páginaFR-GDU-64 Registro y Control de Muestras de OrinaMarcela RodriguezAún no hay calificaciones
- Fr-Gdup-01 Kardex de Enfermeria Pediatria-NeonatosDocumento2 páginasFr-Gdup-01 Kardex de Enfermeria Pediatria-NeonatosMarcela RodriguezAún no hay calificaciones
- PT GDC 11 Protocolo NavDocumento5 páginasPT GDC 11 Protocolo NavMarcela RodriguezAún no hay calificaciones
- FR-GDU-63 Apuntes de Turno de EnfermeriaDocumento1 páginaFR-GDU-63 Apuntes de Turno de EnfermeriaMarcela RodriguezAún no hay calificaciones
- EVIDENCIA 3 Contabilidad de SociedadesDocumento9 páginasEVIDENCIA 3 Contabilidad de SociedadesRaúl HerreraAún no hay calificaciones
- 2 Hacia El PRONACE 1. AguaDocumento33 páginas2 Hacia El PRONACE 1. AguaHector CastelanAún no hay calificaciones
- SeltecDocumento9 páginasSeltecWuilliam Danilo TorresAún no hay calificaciones
- Educación ArtisticaDocumento58 páginasEducación ArtisticaAdry RamirezAún no hay calificaciones
- Cuentas Por Cobrar e InventariosDocumento17 páginasCuentas Por Cobrar e InventariosAmérica Fernández Saavedra de LetonaAún no hay calificaciones
- GTA No 1 Ciencias 7Documento6 páginasGTA No 1 Ciencias 7Rafael Eduardo CordobaAún no hay calificaciones
- Aterramiento ElectricoDocumento8 páginasAterramiento ElectricoJaime Cors FlamburyAún no hay calificaciones
- Ejercicios Planeacion Agregada - CompressDocumento27 páginasEjercicios Planeacion Agregada - CompressselenaAún no hay calificaciones
- Bienes y Servicios Ambientales Del Bosque HumedoDocumento115 páginasBienes y Servicios Ambientales Del Bosque HumedoJulio Cesar Martinez OrtegaAún no hay calificaciones
- Comunicación S35 Almendra Sifuentes Saavedra 5to ADocumento5 páginasComunicación S35 Almendra Sifuentes Saavedra 5to ABRYAM ANTONIO PILLCO VALLADOLIDAún no hay calificaciones
- Diferencias Entre Uniones Empernadas y Uniones SoldadasDocumento7 páginasDiferencias Entre Uniones Empernadas y Uniones SoldadasMarquito34Aún no hay calificaciones
- Actividad 2. - Actividad ExperimentalDocumento8 páginasActividad 2. - Actividad ExperimentalMontserrat HerreraAún no hay calificaciones
- Aa4 IoDocumento10 páginasAa4 IoRonald SalazarAún no hay calificaciones
- Taller 17 y 18 Grado NovenoDocumento3 páginasTaller 17 y 18 Grado NovenoHaswledy Gonzalez CasallasAún no hay calificaciones
- Semana 24 C.SDocumento4 páginasSemana 24 C.SYobana TolentinoAún no hay calificaciones
- Relación Fútbol Con Resto de DeportesDocumento10 páginasRelación Fútbol Con Resto de DeportesMartin BeanatteAún no hay calificaciones
- Anexos Cuarentena Abril 2Documento2 páginasAnexos Cuarentena Abril 2Alfredo Quezada DomínguezAún no hay calificaciones
- Jaziel Flores Ortiz 5A ARH PDFDocumento31 páginasJaziel Flores Ortiz 5A ARH PDFJaziel OrtizAún no hay calificaciones
- Lenguaje de Las CienciasDocumento17 páginasLenguaje de Las Cienciasspring bonnie ArangoAún no hay calificaciones
- Situación Actual de La Producción de Frutas y HortalizasDocumento6 páginasSituación Actual de La Producción de Frutas y HortalizasKatlyn RoblesAún no hay calificaciones
- 3S (P) 2006 PDFDocumento3 páginas3S (P) 2006 PDFMaria_fernanda_paredesAún no hay calificaciones
- Actividad de Aprendizaje 4 Analisis FinancieroDocumento10 páginasActividad de Aprendizaje 4 Analisis FinancieroKaren Cecilia Cabarcas LoraAún no hay calificaciones
- Tipo de TejidosDocumento3 páginasTipo de TejidosFernández García LitzyAún no hay calificaciones
- PROY-NOM-017-STPS-2017 Equipo Proteccion Personal en El TrabajoDocumento22 páginasPROY-NOM-017-STPS-2017 Equipo Proteccion Personal en El TrabajoMiguel AngelAún no hay calificaciones
- Fraude Masivo en Estudios Científicos en ChinaDocumento3 páginasFraude Masivo en Estudios Científicos en Chinajhony1523Aún no hay calificaciones
- El Testamento de Don Gumercindo (ContinúaDocumento3 páginasEl Testamento de Don Gumercindo (ContinúaBlum LopezAún no hay calificaciones