Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Formato Informe Síntesis de (Co (NH3) 6) Cl3 G - 12
Cargado por
DaniiDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Formato Informe Síntesis de (Co (NH3) 6) Cl3 G - 12
Cargado por
DaniiCopyright:
Formatos disponibles
UNIVERSIDAD CENTRAL DEL ECUADOR
CENTRO DE QUÍMICA
QUÍMICA INORGÁNICA I
INFORME TALLER No.
NOMBRES Y
CARRERA FACULTAD NOTA/11
APELLIDOS
Bioquímica y
Ciencias Químicas
Farmacia
PARALELO FECHA
Daniela Toazo
Karen Torres
Christopher Toscano
BF3-001 26/07/2022
Steven Ullauri
Alondra Yanez
Alex Zura
GRUPO HORARIO
12 9:00-11:00
TEMA DE LA PRÁCTICA: Síntesis de [Co(NH3)6]Cl3
RESULTADOS (3pts):
a) Escribir la reacción de síntesis igualada con los estados de agregación y con los nombres de los
reactivos y productos
−¿ ¿
2 C o (aq) →2 C o (aq )+ 2e
+¿
−¿+2 H (aq) →2 H2 O (l ) ¿¿
H 2 O (aq) +2 e
_______________________________
Co +¿ +¿ 3+¿
(aq )+ H 2 O ( aq ) + 2 H (aq) →2 Co ( aq ) + H 2 O ¿ ¿¿
b) Calcular el porcentaje de rendimiento de la reacción
2 CoC l 2 ∙ 6 H 2 O+2 N H 4 Cl +10 N H 4 OH + H 2 O2 →2 ¿
g
msolución =1.7 ml ∙ 0.900
ml
msolución =1.53 g
Elaborado por: M Sc. Maribel Andrango
Revisado por: Dr. Wilmer Narváez
M Sc. José Cadena 2022
m
%
mN H OH ∙ m solución
mN H OH = 4
4
100 %
27.33 % ∙ 1.53 g
mN H OH =
4
100 %
mN H 4 OH =0.4181 g N H 4 OH
1 mol N a 2+ b2=c 2 H 4 OH
0.4181 g N H 4 OH ∙ ∙ 2 mol ¿ ¿
35.04 gN H OH4
1 mol CoC l 2 ∙ 6 H 2 O
0.80 g CoC l 2 ∙ 6 H 2 O ∙ ∙2 mol ¿ ¿
237.93 g CoC l 2 ∙ 6 H 2 O
1 mol N H 4 Cl
0.52 g N H 4 Cl ∙ ∙ 2 mol ¿ ¿
53.491 g N H 4 Cl
Reactivo limitante: N H 4 OH Reactivo en exceso: N H 4 Cl ; CoC l 2 ∙6 H 2 O
1 mol N H 4 OH
0.4181 g N H 4 OH ∙ ∙2 mol ¿ ¿
35.04 g N H OH
4
masa experimental
%rendimiento= ×100
masateórica
0,13 g
%rendimiento= × 100
0.59057 g
%rendimiento=22.013 %
DISCUSIONES (6pts)
1) Analizar cuál de las especies químicas involucradas en la reacción química actúa como ácido y base
de Lewis.
Co +¿ +¿ 3+¿
(aq )+ H 2 O ( aq ) + 2 H (aq) →2 Co ( aq ) + H 2 O ¿ ¿¿
+¿
Acido de Lewisà 2 H(aq) ¿
+¿
Base de Lewis àCo (aq ) ¿
+¿
Anfótero H 2 O (aq) +2 H(aq) ¿
2) Explicar cuál es el propósito de añadir carbón activado y exponer al aire la reacción.
Los complejos de hexaaminocobalto (III) son termodinámicamente inestables en disoluciones ácidas, en
el equilibrio, la concentración de dicho complejo es muy bajo por lo que la reacción puede llegar a tomar
incluso días en completarse, es decir, es un complejo inerte que experimenta reacciones de cambio muy
lentas. (Goldsby y Chang, 2017, p. 1015).
Elaborado por: M Sc. Maribel Andrango
Revisado por: Dr. Wilmer Narváez
M Sc. José Cadena 2022
Los carbones activados son excelentes adsorbentes debido a su extensa área específica, juega un papel
importante debido a que pueden actuar como sitios de anclaje del metal precursor durante su
impregnación y como sitios activos debido a sus propiedades ácido-base o redox. La superficie del
carbón activo puede atrapar las moléculas de la fase gaseosa o líquida provocando una elevada
concentración en superficie. (Robles, 2006). Por lo tanto, al agregar carbón activado al complejo
hexaaminocobalto (III), esté actuara como catalizador acelerando el proceso de la reacción. La
importancia de exponer al aire la reacción radica en el proceso de oxidación que se da con el oxígeno
atmosférico
3) Explicar las observaciones del proceso.
Al añadir 0,8 g de cloruro de cobalto (II) hexahidratado y 0,5 g de cloruro de amonio, en el reposo al aire
libre la solución café se tornó ligeramente roja, después cambio ligeramente a anaranjado. Además,
desprendiendo vapores, teniendo ciertos residuos que correspondientes al carbón. En el calentamiento a
baño maría, el carbón estuvo suspendido en la solución. Después de la destilación al vacío, la cual
consiste en separar los compuestos en función de las diferencias en los puntos de ebullición. Al colocar
los 4ml de HCl concentrado y dejarlo por 10 minutos en el baño de hielo se observó un precipitado que
se suspendía al fondo del vaso.
Al momento de dejar secar la muestra en la estufa debido a una mala manipulación, un compañero tiro
más de la mitad del producto seco, por lo que se presentó un rendimiento bajo. La síntesis para formar
este nuevo complejo resulto relativamente rápida en el proceso de calentar y esperar a que se forme el
complejo
4) Explicar las observaciones de las propiedades químicas.
Al colocar un poco de muestra en el tubo de ensayo se tardó un poco en disolver, pero al agitar por un
momento se disolvió totalmente. La solución tenía un color naranja. El Co(NH3)6]Cl3 según su hoja de
seguridad de Sigma-Aldrich es un compuesto ligeramente soluble (Sigma-Aldrich Inc, 2020).
Figura I. Cloruro de hexaamincobalto III
De acuerdo con su estructura atómica, puede ser considerado un compuesto iónico, por lo que, al
entrar en contacto con el agua, este se disociará. Los cationes y aniones disueltos, debido a su carga,
pueden interactuar con el agua por su carácter polar, y formarán fuerzas intermoleculares ion-dipolo.
Es por ello que [Co(NH3)6]Cl3 sería soluble en agua (House, 2013).
Por otro lado, se tiene la reacción del Cloruro de hexaamincobalto III con agua:
4[Co(NH3)6]Cl3(s) + 10H2O(l) → 4Co(OH)2(s) + O2(g) + 12NH4Cl(ac) + 12NH3(ac) (1)
Elaborado por: M Sc. Maribel Andrango
Revisado por: Dr. Wilmer Narváez
M Sc. José Cadena 2022
Según la reacción expuesta, en los productos se tendría un precipitado color rosado, el hidróxido de
cobalto II (Co(OH)2) el cual no se observó en el momento de disolución del [Co(NH3)6]Cl3 en agua.
El segundo tubo de ensayo que se expuso al calor presentó un cambio de color. Es probable que el
calor haya alterado el equilibrio en la solución con los productos de la reacción 1.
El cloruro de amonio, producto de la reacción 1, es altamente soluble en agua, por lo que se tendrá
presente especies como amonio y amoniaco en la solución.
NH3+ H+⇌ NH4+(ac) (2)
A mayor calor, el amoniaco se evapora, lo que produce desplazamiento en el equilibrio de la
reacción 2. Esto se traduce como mayor transformación de NH4+ en NH3.
La transformación de NH4+ en NH3 y la evaporación de este último por el calor pueden ser los
causantes del cambio de color en el segundo tubo de ensayo después de ser sometido al baño maría.
CONSULTA (2pts)
a) Propiedades físicas y químicas del complejo: tipo de cristal, color, solubilidad, reacción con HCl
llevando a ebullición, punto de fusión.
Tipo de cristal: Polvo, cristales sólidos.
Color: Rojo vino o marrón-naranja-rojo.
Solubilidad: En agua a 20°C ligeramente soluble, soluble en NH 3.
Reacción con HCl: Recristalización sin cambios.
Punto de fusión: 217°C.
BIBLIOGRAFÍA
Chang, R. y Goldsby, K. (2017). Química (12va. ed.). México D.F: Mc Graw Hill Education.
House, J. (2013). Inorganic Chemistry (2da ed). Normal, Estados Unidos: Elsevier.
Robles, S. (2006). Carbón activado modificado como soporte para catalizadores prototipo de HDS.
Revista Mexicana de Ingeniería Química, 5(3),279-284. ISSN: 1665-2738. Recuperado de:
https://www.redalyc.org/articulo.oa?id=62050314
Pubchem. (2012). Hexaamminecobalt (III) Clorhide (compound). Recuperado de:
https://pubchem.ncbi.nlm.nih.gov/compound/159295
Sigma-Aldrich. (2021). Ficha de datos de seguridad: Hexaamminecobalt (III) Clorhide. Versión 6.2.
Sigma-Aldrich Inc. (2020). Ficha de datos de seguridad Tricloruro de hexamincobalto
Co(NH3)6]Cl3 Sigma-H7891 , 1–9. Recuperado de
https://www.sigmaaldrich.com/EC/es/sds/sigma/h7891
Elaborado por: M Sc. Maribel Andrango
Revisado por: Dr. Wilmer Narváez
M Sc. José Cadena 2022
También podría gustarte
- Inorganica 2, Practica 4Documento3 páginasInorganica 2, Practica 4samantaAún no hay calificaciones
- Preparacion de Las Practicas de Laboratiorio Inorganica IiDocumento29 páginasPreparacion de Las Practicas de Laboratiorio Inorganica IiMONROY RAMIREZ ANDRES FELIPEAún no hay calificaciones
- LABORATORIO 8 JabonDocumento6 páginasLABORATORIO 8 JabonDiego GuayacanAún no hay calificaciones
- Obtención y Estudio de La Cinética de Conversación de Los Isómeros de EnlaceDocumento6 páginasObtención y Estudio de La Cinética de Conversación de Los Isómeros de EnlaceAlejandra Balaguera TorresAún no hay calificaciones
- Isomeros FinalDocumento5 páginasIsomeros FinalJohanna GalanAún no hay calificaciones
- Examen Preliminar P - CLOROANILINADocumento4 páginasExamen Preliminar P - CLOROANILINAAlejandra ZeaAún no hay calificaciones
- Nomenclatura de AlcoholesDocumento9 páginasNomenclatura de AlcoholesCristian Edwin Machaca RamosAún no hay calificaciones
- Compuestos de Coordinacion de Niquel PrácticaDocumento14 páginasCompuestos de Coordinacion de Niquel PrácticaUbariel BecerraAún no hay calificaciones
- Acidos Duros y BlandosDocumento2 páginasAcidos Duros y BlandosLyn Portilla GarciaAún no hay calificaciones
- INFORME 6. UV-VisDocumento8 páginasINFORME 6. UV-VisDany PandaAún no hay calificaciones
- BoranosDocumento17 páginasBoranosUriel VázquezAún no hay calificaciones
- Reactividad de PiridinasDocumento21 páginasReactividad de PiridinasIván Narváez AguilarAún no hay calificaciones
- COORDINACIÓN. Sintesis de Cloro Amin. Practica 2 - 1Documento6 páginasCOORDINACIÓN. Sintesis de Cloro Amin. Practica 2 - 1Francisco PeraltaAún no hay calificaciones
- REVISADO - Reporte Vainillina.Documento12 páginasREVISADO - Reporte Vainillina.Ale MontoyaAún no hay calificaciones
- Practica Nº7Documento18 páginasPractica Nº7Angela Chumioque GarciaAún no hay calificaciones
- Practica 3 OrganicaDocumento8 páginasPractica 3 OrganicaQuique RosasAún no hay calificaciones
- Compuesto de CobreDocumento3 páginasCompuesto de CobreJairArmandoGomezPerezAún no hay calificaciones
- Sintesis de Isomeros GeometricosDocumento19 páginasSintesis de Isomeros GeometricosJUAN DANIEL GIRALDO MUÑOZAún no hay calificaciones
- Informe 8 Quimica Organica IIDocumento3 páginasInforme 8 Quimica Organica IILUIS JAVIER RAMIRO SANCHEZAún no hay calificaciones
- ComplejosDocumento41 páginasComplejosAnthony Alexandere VivancoAún no hay calificaciones
- 23-02-2017 Síntesis de Un Material Luminiscente Por CoprecipitaciónDocumento2 páginas23-02-2017 Síntesis de Un Material Luminiscente Por CoprecipitaciónLuis CampuzanoAún no hay calificaciones
- Identificación de Muestra DesconocidaDocumento11 páginasIdentificación de Muestra DesconocidaVale AlarconAún no hay calificaciones
- Estudio Del Comportamiento Químico de Los Elementos Boro y AluminioDocumento10 páginasEstudio Del Comportamiento Químico de Los Elementos Boro y AluminioJorge RosalesAún no hay calificaciones
- InorganicaDocumento17 páginasInorganicaRicardo A RoweAún no hay calificaciones
- Reporte Experimental QuelatoDocumento9 páginasReporte Experimental QuelatoEdgar ArmandoAún no hay calificaciones
- PRÁCTICA 11, BromaciónDocumento2 páginasPRÁCTICA 11, BromaciónAlfre Contreras RamírezAún no hay calificaciones
- Preguntas SN1Documento2 páginasPreguntas SN1Kike PadillaAún no hay calificaciones
- +hno Cu (NO) + No + H ODocumento3 páginas+hno Cu (NO) + No + H OC'Denisse PalominoAún no hay calificaciones
- Síntesis de Co (Salen) y Estudio de Absorción de O2Documento5 páginasSíntesis de Co (Salen) y Estudio de Absorción de O2Andrea SilvaAún no hay calificaciones
- Lab #2 Terc-ButiloDocumento6 páginasLab #2 Terc-ButiloEliana picoAún no hay calificaciones
- Síntesis y Análisis de Un Compuesto de Oxalato de AluminioDocumento5 páginasSíntesis y Análisis de Un Compuesto de Oxalato de AluminioJulian Arango100% (2)
- INFODocumento6 páginasINFOsandraAún no hay calificaciones
- Isomeros de Enlace. Inorganica 2019 Modificado-1Documento6 páginasIsomeros de Enlace. Inorganica 2019 Modificado-1Herman Ruiz CalderinAún no hay calificaciones
- Informe 1 Inor 2Documento14 páginasInforme 1 Inor 2Heidy Beatriz HurtadoAún no hay calificaciones
- Cuestionario Previo de Práctica 4Documento3 páginasCuestionario Previo de Práctica 4Teresa EscobedoAún no hay calificaciones
- Practica 3 de CoordinaciónDocumento3 páginasPractica 3 de CoordinaciónElizabeth ChavanaAún no hay calificaciones
- Teoría Ácidos y Bases Blandos y DurosDocumento2 páginasTeoría Ácidos y Bases Blandos y Durosfama_20Aún no hay calificaciones
- Practica #4 Metodo de JobDocumento11 páginasPractica #4 Metodo de JobSERGIO ARMANDO BLANCO MERCADOAún no hay calificaciones
- CobaltoDocumento7 páginasCobaltoLuz Marina Peña MorajxkfjjkkzkfAún no hay calificaciones
- CompletoDocumento439 páginasCompletoJuan Carlos Vazquez80% (5)
- Reporte 1 de Organica IIDocumento3 páginasReporte 1 de Organica IIOrquideaAún no hay calificaciones
- Aislamiento de Un Ingrediente Activo en Una Droga AnalgésicoDocumento8 páginasAislamiento de Un Ingrediente Activo en Una Droga AnalgésicoJorge ContrerasAún no hay calificaciones
- Pasar inDocumento3 páginasPasar inAlexander LeónAún no hay calificaciones
- 1414-L Práctica 0 Pasta Cerámica CuestionarioDocumento3 páginas1414-L Práctica 0 Pasta Cerámica CuestionarioJonathan Saviñon de los SantosAún no hay calificaciones
- Diels AlderDocumento6 páginasDiels AlderLaura GuidoAún no hay calificaciones
- Preinforme Practica Isomeros Nitro y NitritoDocumento5 páginasPreinforme Practica Isomeros Nitro y Nitritoferney romerocaperaAún no hay calificaciones
- Síntesis de Trioxalatomanganato (III) de PotasioDocumento3 páginasSíntesis de Trioxalatomanganato (III) de PotasioGICELAAún no hay calificaciones
- Informe 8 RecristalizaciónDocumento14 páginasInforme 8 Recristalizaciónjairo guerreroAún no hay calificaciones
- Reporte Fisico QuimicaDocumento8 páginasReporte Fisico QuimicaFelipe VilchesAún no hay calificaciones
- Informe de Tris Oxalato de Aluminio y PotasioDocumento8 páginasInforme de Tris Oxalato de Aluminio y PotasioCesar Valencia75% (4)
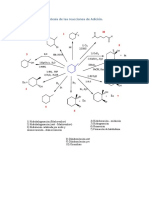
- Síntesis de Las Reacciones de AdiciónDocumento1 páginaSíntesis de Las Reacciones de AdiciónMiri AldreteAún no hay calificaciones
- P5 QO II-finalDocumento4 páginasP5 QO II-finalRodrigo de J. García ChimalAún no hay calificaciones
- Lab 6Documento17 páginasLab 6Ayrton Jimenez InfantesAún no hay calificaciones
- CICLO DE BORN HABER MgF2Documento2 páginasCICLO DE BORN HABER MgF2Lilian Olivos100% (1)
- ZanahoriaDocumento3 páginasZanahoriademefpAún no hay calificaciones
- Wuolah Free Informe Experimentacion en Quimica InorganicaDocumento67 páginasWuolah Free Informe Experimentacion en Quimica InorganicaMariajo FernándezAún no hay calificaciones
- Yoduros de EstañoDocumento4 páginasYoduros de EstañoF DAAún no hay calificaciones
- Anexo 3 ModificadoDocumento5 páginasAnexo 3 ModificadoYEFERSON MOSQUERAAún no hay calificaciones
- Anexo 3Documento4 páginasAnexo 3alfredo aaronAún no hay calificaciones
- Anexo 3Documento6 páginasAnexo 3YEFERSON MOSQUERAAún no hay calificaciones
- Ejercicios de CalculoDocumento5 páginasEjercicios de CalculoDaniiAún no hay calificaciones
- Tarea Individual 3Documento21 páginasTarea Individual 3DaniiAún no hay calificaciones
- Contraste - Hipotesis - AnovaDocumento23 páginasContraste - Hipotesis - AnovaDaniiAún no hay calificaciones
- Formato Informe Síntesis Del K (CR (C2O4) 2 (H2O) ) .3H2ODocumento6 páginasFormato Informe Síntesis Del K (CR (C2O4) 2 (H2O) ) .3H2ODaniiAún no hay calificaciones
- Diagrama de Flujo (Alumbre)Documento2 páginasDiagrama de Flujo (Alumbre)DaniiAún no hay calificaciones
- Trabajo Grupal 2 Analisis de ANOVADocumento10 páginasTrabajo Grupal 2 Analisis de ANOVADaniiAún no hay calificaciones
- Aplicacion de Los Compuestos de CoordinacionDocumento7 páginasAplicacion de Los Compuestos de CoordinacionDaniiAún no hay calificaciones
- Tarea Individual 2Documento21 páginasTarea Individual 2DaniiAún no hay calificaciones
- Técnicas de Análisis ModernasDocumento5 páginasTécnicas de Análisis ModernasDaniiAún no hay calificaciones
- Trabajo Grupal - Geometria MolecularDocumento6 páginasTrabajo Grupal - Geometria MolecularDaniiAún no hay calificaciones
- Informe Reacciones Químicas Grupo 12Documento9 páginasInforme Reacciones Químicas Grupo 12DaniiAún no hay calificaciones
- Deber Grupal 4 OrganicaDocumento23 páginasDeber Grupal 4 OrganicaDaniiAún no hay calificaciones
- Diagrama de Flujo Practica 11Documento1 páginaDiagrama de Flujo Practica 11DaniiAún no hay calificaciones
- Parasitologia Pruebas 2020 2020Documento78 páginasParasitologia Pruebas 2020 2020DaniiAún no hay calificaciones
- Ejercicios de CalculoDocumento4 páginasEjercicios de CalculoDaniiAún no hay calificaciones
- Tarea No 1 Quimica AnaliticaDocumento6 páginasTarea No 1 Quimica AnaliticaDaniiAún no hay calificaciones
- Prueba de La Unidad 2 - Revisión Del IntentoDocumento6 páginasPrueba de La Unidad 2 - Revisión Del IntentoDaniiAún no hay calificaciones
- Prueba de La Unidad 3 - Revisión Del IntentoDocumento8 páginasPrueba de La Unidad 3 - Revisión Del IntentoDaniiAún no hay calificaciones
- Prueba de La Unidad 1 - Revisión Del IntentoDocumento6 páginasPrueba de La Unidad 1 - Revisión Del IntentoDaniiAún no hay calificaciones
- Tarea 1 Estadística DescriptivaDocumento13 páginasTarea 1 Estadística DescriptivaDaniiAún no hay calificaciones
- Práctica 2 y 3Documento8 páginasPráctica 2 y 3BRYAN ALFREDO LINARES MARTINEZAún no hay calificaciones
- Visita Tecnica A La Planta de Segregacion de Minerales Rio Seco UNSADocumento9 páginasVisita Tecnica A La Planta de Segregacion de Minerales Rio Seco UNSAPiero Mendoza HurtadoAún no hay calificaciones
- Tambor Rotatorio-CompostDocumento20 páginasTambor Rotatorio-CompostGERMAN GUZMANAún no hay calificaciones
- Germinacion y LatenciaDocumento29 páginasGerminacion y LatenciaFabio Diaz LloccllaAún no hay calificaciones
- Jabones 1Documento17 páginasJabones 1Omar Antonio Sivira Jr.Aún no hay calificaciones
- Termino ImooooooooooDocumento11 páginasTermino ImooooooooooEylinAún no hay calificaciones
- Certificado de Calidad. Cemento CEMEX.Documento2 páginasCertificado de Calidad. Cemento CEMEX.Lucio BUSTAMANTE MARRUFO.Aún no hay calificaciones
- BiologiaDocumento3 páginasBiologiaJOSE ANTONIO CESAR CASTILLO MENDEZAún no hay calificaciones
- Operaciones de Acondicionamiento Del AguaDocumento31 páginasOperaciones de Acondicionamiento Del AguaGiancarlo Diosdado Castro MendizabalAún no hay calificaciones
- Minerales de Plomo, Zinc e Hierro.Documento3 páginasMinerales de Plomo, Zinc e Hierro.David Sanchez RmzAún no hay calificaciones
- Avance Capitulo 3 Obtencion de BiohidrogenoDocumento72 páginasAvance Capitulo 3 Obtencion de BiohidrogenoDiego Medrano HidalgoAún no hay calificaciones
- 2ºaño Físico Química 4ºposteoDocumento11 páginas2ºaño Físico Química 4ºposteoJxkd JdjdAún no hay calificaciones
- Ingeniería de Reacciones Químicas I: - Cinética de Las Reacciones - Velocidad de ReacciónDocumento25 páginasIngeniería de Reacciones Químicas I: - Cinética de Las Reacciones - Velocidad de ReacciónMORAN CABALLERO JUAN PABLOAún no hay calificaciones
- Analisis Cualitativo y Cuantitativo Del AtenololDocumento8 páginasAnalisis Cualitativo y Cuantitativo Del AtenololMarco Antonio Tarazona MoyaAún no hay calificaciones
- DestilaciónDocumento3 páginasDestilaciónIrving MoyanoAún no hay calificaciones
- Informe 4 - Quimica AnaliticaDocumento16 páginasInforme 4 - Quimica AnaliticaJOSE TAIPE SANCHEZAún no hay calificaciones
- Guia 7 Grado UndécimoDocumento8 páginasGuia 7 Grado UndécimoJhosua Ricardo pachecoAún no hay calificaciones
- Fertilización en CacaoDocumento33 páginasFertilización en CacaoGermán A DelgadoAún no hay calificaciones
- Inf. Nro 2-2019 - Res-Cues.Documento9 páginasInf. Nro 2-2019 - Res-Cues.Aylin JudithAún no hay calificaciones
- ARCILLADocumento6 páginasARCILLAFELIX ALEX CONDORI NINAAún no hay calificaciones
- 1CINETICADocumento2 páginas1CINETICANATALIA SALVADOR NICODEMOSAún no hay calificaciones
- Punto de Fusión y EbulliciónDocumento2 páginasPunto de Fusión y EbulliciónjopacopoAún no hay calificaciones
- Escaldado de FrutasDocumento21 páginasEscaldado de FrutasJuan Jose Gaytan AndradeAún no hay calificaciones
- Alcoholism oDocumento14 páginasAlcoholism oWINNY ERIKA CERENO ROSALESAún no hay calificaciones
- Pry. Inv. Manz y MatDocumento76 páginasPry. Inv. Manz y MatWily Oviedo CarpioAún no hay calificaciones
- Banco de PreguntasDocumento7 páginasBanco de PreguntasLUZ STELLA ARGUELLO VARGASAún no hay calificaciones
- Biosintesis de Histidina A Partir de Ribosa-5-Fosfato.Documento8 páginasBiosintesis de Histidina A Partir de Ribosa-5-Fosfato.LaaLiin B. MuÑoz0% (1)
- Capitulo 17 RUTHDocumento38 páginasCapitulo 17 RUTHnimer paredes quispeAún no hay calificaciones
- TP N°8 AGLOMERANTES YESO (Recuperado Automáticamente)Documento12 páginasTP N°8 AGLOMERANTES YESO (Recuperado Automáticamente)Tobias ScheurerAún no hay calificaciones
- 6 ZoeDocumento25 páginas6 ZoeGabriela Medina GomezAún no hay calificaciones