Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cecil 3
Cargado por
Sofía L.Descripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Cecil 3
Cargado por
Sofía L.Copyright:
Formatos disponibles
Cecil Medicina Interna, 5th Edition 21
3 ESTRUCTURA Y FUNCIÓN DEL CORAZÓN Y LOS
VASOS SANGUÍNEOS
Eric H. Awtry
Joseph Loscalzo
Anatomía microscópica
El tejido cardíaco (miocardio) está compuesto por varios tipos de células que
conjuntamente dan lugar a una contracción organizada del corazón. Las células
especializadas del miocardio comprenden el sistema eléctrico cardíaco (sistema de
conducción) y son las responsables de la generación del impulso eléctrico y de su
propagación organizada hacia las fibras del músculo cardíaco (miocitos), que, a su
vez, responden a través de una contracción mecánica. Los miocitos auriculares y
ventriculares son células musculares especializadas y ramificadas separadas entre sí
por placas intercalares término–terminales. Estas regiones engrosadas de la
membrana celular (sarcolema) ayudan en la transmisión de la tensión mecánica
entre las células. El sarcolema tiene funciones similares a otras membranas
celulares, incluyendo el mantenimiento de gradientes iónicos, la propagación de
impulsos eléctricos y la provisión de receptores para impulsos nerviosos y
hormonales. Además, el sarcolema está íntimamente implicado en la coordinación
entre la excitación y contracción miocárdica a través de pequeños túbulos
transversales (túbulos T) que se extienden desde el sarcolema hacia el espacio
intracelular. Los miocitos contienen otras organelas, incluyendo un núcleo;
múltiples mitocondrias responsables de la generación de la energía necesaria para la
contracción; una extensa red de túbulos intracelulares denominados retículo
sarcoplasmático, que funciona como almacén fundamental del calcio intracelular, y
las miofibrillas, los elementos contráctiles de la célula. Cada miofibrilla está
formada por unidades repetitivas llamados sarcómeros, que a su vez están
compuestos por delgados filamentos de actina y filamentos gruesos de miosina
superpuestos y por sus proteínas reguladoras troponina y tropomiosina (Figura 3-1).
Anatomía macroscópica
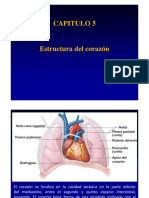
El corazón está compuesto por cuatro cámaras, dos aurículas y dos ventrículos, que
forman dos bombas separadas adosadas y con funcionamiento secuencial (Figura
3-2). Las aurículas son cámaras de presión baja que funcionan fundamentalmente
como almacén de sangre durante la contracción ventricular (sístole), y a
3 ESTRUCTURA Y FUNCIÓN DEL Página 1 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
continuación llenan los ventrículos con sangre durante su relajación (diástole). Las
dos aurículas están separadas por un delgado tabique interauricular. Los ventrículos
son cámaras de presión alta responsables del bombeo de la sangre hacia los
pulmones y los tejidos periféricos. Debido a que la presión generada en el
ventrículo izquierdo es mayor que la del ventrículo derecho, el miocardio del
ventrículo izquierdo es más grueso que el derecho. Los dos ventrículos están
separados por el tabique interventricular, que es una estructura membranosa en su
porción superior y de tipo muscular grueso en las porciones media y distal.
Las aurículas y ventrículos están separados por las válvulas auriculoventriculares
(AV). La válvula mitral está compuesta por dos valvas y separa la aurícula y
ventrículo izquierdos. La válvula tricúspide posee tres valvas y separa las cámaras
derechas. La superficie ventricular de estas válvulas está unida a estructuras
tendinosas fuertes (cuerdas tendinosas) que se continúan en los músculos papilares
de su ventrículo respectivo. Estos músculos papilares son extensiones del miocardio
normal que se proyectan en las cavidades ventriculares, y son importantes para
obtener un cierre valvular óptimo. Las válvulas semilunares separan los ventrículos
de las cámaras arteriales: la válvula semilunar aórtica separa el ventrículo izquierdo
de la aorta, y la válvula semilunar pulmonar separa el ventrículo derecho de l a
arteria pulmonar. Estas válvulas carecen de cuerdas tendinosas. En su lugar, se trata
de válvulas fibrosas cuyos extremos coaptan estrechamente,permitiendo con ello el
cierre adecuado de la válvula. Cada una de las cuatro válvulas está rodeada por un
anillo fibroso, que forma parte del soporte estructural del corazón. Cuando las
válvulas se abren, el flujo sanguíneo pasa libremente a su través hacia la cámara o
vaso adyacentes. Cuando se cierran, las válvulas impiden de forma eficaz el flujo
retrógrado de sangre. 21
3 ESTRUCTURA Y FUNCIÓN DEL Página 2 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
21
22
FIGURA 3-1
A, Un sarcómero tal y como aparece en la microscopia electrónica. B, esquema
que muestra la localización e interacción entre la actina y la miosina (véase el
texto).
El corazón está rodeado por el delgado pericardio, de doble capa. El pericardio
visceral está adherido al corazón y constituye su superficie externa o epicardio.
Esta capa está separada del pericardio parietal por el espacio pericárdico, que en
condiciones normales contiene menos de 50 ml de líquido. El pericardio parietal
está sujeto al esternón, columna vertebral y diafragma, para estabilizar el corazón
dentro de la caja torácica. El líquido pericárdico normal lubrifica las dos superficies
en contacto y limita el contacto tisular directo durante la contracción miocárdica.
3 ESTRUCTURA Y FUNCIÓN DEL Página 3 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
Además, el pericardio normal modula la interacción interventricular durante el ciclo
cardíaco.
La circulación sanguínea
La sangre desoxigenada procede de los tejidos periféricos y entra en la aurícula
derecha a través de la vena cava superior e inferior (véase la Figura 3-2). La sangre
que ha irrigado el propio corazón entra en la aurícula derecha a través del seno
coronario. Esta sangre se mezcla en la aurícula derecha durante la sístole ventricular
y a continuación fluye a través de la válvula tricúspide hacia el ventrículo derecho
durante la diástole ventricular. Cuando el ventrículo derecho se contrae, la sangre es
bombeada a través de la válvula pulmonar hacia la arteria pulmonar principal, que a
continuación se bifurca en las arterias pulmonares izquierda y derecha cuando estas
ramas penetran en el pulmón correspondiente. Después de múltiples bifurcaciones,
la sangre fluye en los capilares pulmonares donde el dióxido de carbono se
intercambia por oxígeno a través de la membrana alveolocapilar. La sangre
oxigenada sale así de los pulmones por las cuatro venas pulmonares, que van a
drenar en la aurícula izquierda. Durante la diástole ventricular, esta sangre fluye a
través de la válvula mitral abierta y pasa al ventrículo izquierdo. Con la contracción
ventricular, la sangre es bombeada a través de la válvula aórtica hacia la aorta y de
esta forma pasa a la circulación sistémica y los diferentes órganos, donde el
oxígeno y los nutrientes son intercambiados por dióxido de carbono y residuos
metabólicos.
El propio corazón recibe la irrigación sanguínea a través de las arterias coronarias
izquierda y derecha (Figura 3-3). Son las primeras ramas arteriales de la aorta y se
originan en unos espacios de la raíz aórtica denominados senos de Valsalva. La
arteria coronaria izquierda principal se origina en el seno de Valsalva izquierdo y es
un vaso de corto trayecto que se bifurca en las arterias descendente anterior (DA) y
circunfleja (C). La DA discurre a través de la superficie del corazón por el surco
interventricular anterior hacia el ápex cardíaco. Irriga a la porción anterior y
anterolateral del ventrículo izquierdo a través de sus ramas diagonales, así como a
los dos tercios anteriores del tabique interventricular a través de sus ramas septales.
La C discurre posteriormente por el surco AV izquierdo (entre la aurícula y el
ventrículo izquierdos), e irriga la superficie lateral del ventrículo izquierdo a través
de las ramas obtusas marginales, así como ramas para la aurícula izquierda. La
arteria coronaria derecha (CD) se origina en el seno de Valsalva derecho y discurre
hacia abajo por el surco AV derecho hasta el punto de encuentro de los surcos AV
izquierdo y derecho e interventricular inferior, o "cruz" del corazón. La CD
proporciona ramas para la aurícula derecha y ramas marginales agudas para el
3 ESTRUCTURA Y FUNCIÓN DEL Página 4 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
ventrículo derecho. La irrigación sanguínea de las caras diafragmática y posterior
del ventrículo izquierdo es variable. En el 85% de los sujetos, la CD se bifurca en la
cruz dando a la arteria coronaria descendente posterior (DP), que discurre por el
surco interventricular inferior para irrigar la pared inferior del ventrículo izquierdo
y el tercio inferior del tabique interventricular, y las ramas posteriores del
ventrículo izquierdo (RPVI) que irrigan esta zona. Esta distribución se denomina
circulación derecha dominante. En el 10% de los sujetos, la CD finaliza antes de
llegar a la cruz y la circunfleja irriga a las RPVI y la DP. Esta distribución se
denomina dominancia izquierda. En el resto de sujetos, la CD da lugar a la DP y la
circunfleja a las RPVI, denominándose distribución codominante. La irrigación
sanguínea del nódulo sinusal procede en un 60% de la CD y en un 40% de la
circunfleja, mientras que la arteria dominante irriga el nodo AV.
FIGURA 3-2
Esquema de los sistemas circulatorios sistémico y pulmonar. El sistema
venoso contiene la mayor cantidad de sangre y en un momento dado es
altamente distensible, alojando un amplio rango de volúmenes de sangre
(elevada capacidad). El sistema arterial comprende la aorta, las arterias y
arteriolas. Estas últimas son pequeñas arterias musculares que regulan la
presión arterial cambiando su tono (resistencia).
22
3 ESTRUCTURA Y FUNCIÓN DEL Página 5 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
22
23
FIGURA 3-3 Arterias coronarias principales y sus
ramificaciones.
Existen pequeños canales vasculares denominados vasos colaterales que
interconectan las arterias coronarias normales. Estos vasos no son funcionales en el
miocardio normal porque no existe un gradiente de presión entre ellos. Sin
embargo, en una situación de estenosis grave u oclusión completa de una arteria
coronaria, la presión existente en el vaso distal a la estenosis disminuye y se crea un
gradiente a través de los vasos colaterales, dando lugar a la aparición de flujo en
dichos vasos. El desarrollo de colaterales está directamente relacionado con la
gravedad de la estenosis coronaria y puede ser estimulado por isquemia, hipoxia y
por una serie de factores de crecimiento. Con el tiempo, estos vasos pueden
alcanzar una luz de hasta 1 mm y ser casi indistinguibles de las arterias coronarias
normales de tamaño similar.
La mayor parte del drenaje venoso del corazón se realiza a través del seno
coronario, que discurre por el surco AV y va a drenar en la aurícula derecha. Una
pequeña cantidad de sangre del corazón derecho desemboca directamente en la
aurícula derecha a través de las venas tebesianas y las pequeñas venas miocárdicas
anteriores.
3 ESTRUCTURA Y FUNCIÓN DEL Página 6 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
El sistema de conducción
El impulso eléctrico que inicia la contracción cardíaca se origina en el nodo sinusal,
una agrupación de células marcapaso especializadas que mide entre 1 y 2 cm de
longitud y que se localiza en la porción superior de la aurícula derecha, entre la
vena cava superior y la orejuela (Figura 3-4). A continuación el impulso se
disemina por todo el tejido auricular a través de unos trayectos internodales
preferentes y alcanza el nodo AV. Esta estructura está compuesta por una red de
células y se localiza en la cara inferior de la aurícula derecha, entre el seno
coronario y la valva septal de la válvula tricúspide. Tanto el nodo sinusal como el
AV están ricamente inervados por neuronas simpáticas y parasimpáticas,
permitiéndose así la regulación nerviosa de la frecuencia cardíaca.
El nodo AV proporciona la única conexión eléctrica normal entre aurículas y
ventrículos. Después de que un impulso eléctrico penetra en el nodo AV, la
conducción se enlentece transitoriamente y a continuación sigue hacia los
ventrículos a través del sistema de His-Purkinje. El haz de His se extiende desde el
nodo AV por el tabique interventricular membranoso y muscular, donde se divide
en las ramas izquierda y derecha. La rama derecha es una estructura discreta que se
extiende a lo largo del tabique interventricular y penetra en la banda moderadora en
su camino hacia el músculo papilar anterolateral del ventrículo derecho. La rama
izquierda está menos diferenciada, compuesta por una agrupación de fibras
organizadas en un fascículo anterior, que sigue su curso hacia el músculo papilar
anterolateral, y un fascículo posterior, que discurre posteriormente por el tabique
hacia el músculo papilar posteromedial. Las dos ramas finalizan en las células de
Purkinje, que son células grandes con conexiones intercelulares bien desarrolladas,
lo que permite la rápida propagación de los impulsos eléctricos. Estas células son
las que estimulan directamente a los miocitos. 23
3 ESTRUCTURA Y FUNCIÓN DEL Página 7 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
23
24
FIGURA 3-4 Representación del sistema de conducción del
corazón.
Inervación nerviosa
El miocardio normal está ricamente inervado por el sistema nervioso autónomo.
Las terminales simpáticas se encuentran distribuidas ampliamente por aurículas y
ventrículos, y un aumento del tono simpático implica un aumento de la fuerza de la
contracción miocárdica. El sistema parasimpático inerva las aurículas a través del
nervio vago, pero hay escasas proyecciones hacia los ventrículos. Los nodos sinusal
y AV están densamente inervados por neuronas simpáticas y parasimpáticas,
permitiendo la regulación nerviosa de la frecuencia cardíaca. El aumento del tono
simpático conduce a un aumento de la frecuencia cardíaca y a un acortamiento del
intervalo de conducción a través del nodo AV. El aumento del tono parasimpático
conduce a una disminución de la frecuencia cardíaca y al enlentecimiento de la
conducción a través del nodo AV.
Fisiología de la contracción
La contracción de los miocitos se inicia con la despolarización eléctrica del
sarcolema, dando lugar a una entrada de calcio dentro de las células a través de
canales en los túbulos T (Figura 3-5). La entrada inicial de calcio estimula la rápida
liberación de grandes cantidades de calcio del retículo sarcoplasmático hacia el
3 ESTRUCTURA Y FUNCIÓN DEL Página 8 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
citosol celular. Este calcio se une a la subunidad correspondiente de la troponina
(troponina C) en los filamentos de actina del sarcómero, dando lugar a un cambio
en la configuración del complejo troponina–tropomiosina. Dicho cambio favorece
la interacción actina–miosina, que da lugar a la contracción celular. A medida que
la onda de despolarización va pasando, el calcio es secuestrado de forma rápida y
activa en el retículo sarcoplasmático, donde queda almacenado en varias proteínas,
incluyendo la calsecuestrina, hasta que aparezca la siguiente onda de
despolarización. El calcio también es eliminado del citosol a través de varias
bombas presentes en el sarcolema. La fuerza de la contracción del miocito puede
regularse según la cantidad de calcio libre liberado en la célula por el retículo
sarcoplasmático: una mayor cantidad de calcio permite una mayor interacción actina
–miosina, provocando una contracción más potente.
La energía para la contracción del miocito procede del trifosfato de adenosina
(ATP), generado por la fosforilación oxidativa del difosfato de adenosina (ADP) en
las abundantes mitocondrias de la célula. El ATP es necesario tanto para la entrada
de calcio como para la generación de la fuerza en la interacción actina–miosina.
Durante la contracción, el ATP fomenta la disociación entre miosina y actina,
permitiendo con ello el deslizamiento de los filamentos gruesos sobre los delgados
a medida que el sarcómero se va acortando. En condiciones normales, los ácidos
grasos son la fuente de energía preferida, aunque también puede utilizarse la
glucosa como sustrato. Estos sustratos deben suministrarse de forma continuada al
corazón a través del torrente circulatorio, porque el corazón dispone de un almacén
de energía mínimo. El metabolismo miocárdico es aeróbico y por ello precisa un
aporte constante de oxígeno. En condiciones anaeróbicas, la glucólisis y el lactato
pueden convertirse en una fuente de ATP, aunque en cantidades insuficientes como
para mantener la función cardíaca.
Fisiología de la circulación sanguínea y el ciclo cardíaco
El ciclo cardíaco es una serie de eventos contráctiles y valvulares repetitivos
durante los cuales las válvulas se abren y se cierran en respuesta a gradientes de
presión entre las diferentes cámaras cardíacas (Figura 3-6). Este ciclo puede
dividirse en sístole, período de contracción ventricular, y diástole, período de
relajación ventricular. Con la aparición de la contracción ventricular, la presión de
los ventrículos aumenta y supera la existente en las aurículas, cerrándose entonces
las válvulas AV. La presión intraventricular continúa aumentando, inicialmente sin
producirse cambios en el volumen (contracción isovolumétrica) del ventrículo,
hasta que dicha presión supera a la existente en la aorta y la arteria pulmonar, en
cuyo momento las válvulas semilunares se abren y se produce la expulsión de
3 ESTRUCTURA Y FUNCIÓN DEL Página 9 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
sangre de los ventrículos. Con la aparición de la relajación ventricular, la presión en
los ventrículos cae hasta que la presión en las cámaras arteriales supera a la de los
ventrículos, y las válvulas semilunares se cierran. La relajación ventricular
continúa, inicialmente sin cambios en el volumen (relajación isovolumétrica) del
ventrículo. Cuando la presión en los ventrículos cae por debajo de la presión de las
aurículas, las válvulas AV se abren y aparece una fase de llenado ventricular rápido
a medida que se vacía la sangre de las aurículas y pasa a los ventrículos. Al final de
la diástole, la contracción auricular activa aumenta el llenado ventricular. Dicho
aumento es especialmente importante en pacientes con mala función ventricular y
desaparece en los pacientes con fibrilación auricular. 24
25
FIGURA 3-5
Dependencia del calcio de la contracción miocárdica. La despolarización
2+
eléctrica del miocito da lugar a la entrada de Ca al interior de la célula a
través de los canales en los túbulos T. Esta fase inicial de la entrada del calcio
2+
estimula la liberación de grandes cantidades de Ca del retículo
2+
sarcoplasmático (RS). A continuación el Ca se une al complejo troponina–
tropomiosina de los filamentos de actina, provocando un cambio en su
configuración que facilita la interacción entre la actina y la miosina. En
presencia de trifosfato de adenosina (ATP), la asociación actina–miosina se
disocia de forma cíclica cuando los filamentos gruesos y delgados se deslizan
2+
entre sí, dando lugar a la contracción. Durante la repolarización, el Ca es
bombeado activamente fuera del citosol y secuestrado en el RS. M:
mitocondria.
3 ESTRUCTURA Y FUNCIÓN DEL Página 10 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
En ausencia de una valvulopatía, no existe ningún impedimento para que el flujo
sanguíneo pase de los ventrículos al lecho arterial, y la presión arterial sistólica
aumenta de forma pronunciada hasta su valor máximo. Durante la diástole, la
presión arterial va disminuyendo progresivamente a medida que la sangre fluye
distalmente y aparece la retracción elástica de las arterias. Esta respuesta contrasta
con la respuesta a la presión en los ventrículos durante la diástole, que va
aumentando progresivamente a medida que la sangre fluye dentro de los ventrículos
desde las aurículas. La presión auricular puede medirse directamente en la aurícula
derecha, mientras que la presión auricular izquierda suele obtenerse indirectamente
a través de la oclusión de una pequeña rama de la arteria pulmonar y determinando
distalmente la presión (presión de "enclavamiento" capilar pulmonar). La Figura
3-6 muestra un trazado de presión en la aurícula, que está compuesto por varias
ondas de presión. La onda a representa a la contracción auricular. A medida que la
aurícula se va relajando, la presión en la aurícula disminuye y aparece el descenso x
en el trazado. El descenso x queda interrumpido por una pequeña onda c, que se
genera cuando la válvula AV abomba hacia la aurícula durante la sístole
ventricular. A medida que la aurícula se llena con el retorno venoso aparece la onda
v, después de la cual aparece el descenso y cuando las válvulas AV se abren y la
sangre de la aurícula se vacía en los ventrículos. La Tabla 3-1 muestra los rangos
normales de presión en las diferentes cámaras del corazón.
Función cardíaca
La cantidad de sangre expulsada por el corazón en cada minuto se conoce por gasto
cardíaco (GC) y es el producto entre el volumen latido (VL = cantidad de sangre
expulsada en cada contracción ventricular) y la frecuencia cardíaca (FC):
GC = VL X FC
El índice cardíaco (IC) es el GC dividido entre el área de superficie corporal, y se
mide en litros por minuto por metro cuadrado, y es una forma de normalizar el GC
en relación al tamaño corporal. El GC normal en reposo es de 5-6 l/min,aunque este
valor puede aumentar entre cuatro y seis veces durante un ejercicio extenuante
como resultado del incremento en la frecuencia cardíaca (cronotropía) y el VL
(inotropía). 25
3 ESTRUCTURA Y FUNCIÓN DEL Página 11 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
25
26
FIGURA 3-6
Trazados simultáneos del electrocardiograma (ECG) y de presión obtenidos en
la aurícula izquierda (AI), ventrículo izquierdo (VI), y presiones de la aorta y
la vena yugular durante el ciclo cardíaco. Por motivos de simplificación, se
han omitido las presiones derechas. La presión normal de la aurícula derecha
sigue un trazado paralelo al de la aurícula izquierda, y las presiones del
ventrículo derecho y la arteria pulmonar están estrechamente relacionadas en
el tiempo con las cavidades izquierdas correspondientes, existiendo
únicamente una reducción en su magnitud. El cierre normal de las válvulas
mitral y aórtica precede al cierre de las válvulas tricuspídea y pulmonar,
respectivamente, mientras que el orden de la abertura valvular está invertido.
3 ESTRUCTURA Y FUNCIÓN DEL Página 12 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
El pulso venoso yugular aparece retrasado detrás del pulso de la aurícula
derecha.
Durante el curso de un ciclo cardíaco, primero aparece la señal eléctrica
(ECG) y a continuación la contracción mecánica (presión), y esta última
precede a la auscultación (ruidos cardíacos) resultante. Poco después de la
aparición de la onda P, la aurícula se contrae produciendo la onda a; a
continuación aparece un cuarto ruido. El complejo QRS inicia la sístole
ventricular, seguido poco después por la contracción del VI y por la aparición
de presión rápida en dicha cavidad. Casi inmediatamente, la presión del VI
supera a la de la AI, cerrándose la válvula mitral y apareciendo el primer ruido
cardíaco. Después de un breve período de contracción isovolumétrica, la
presión del VI supera a la presión de la aorta y se abre la válvula aórtica
(AVA). Cuando la presión ventricular vuelve a caer por debajo de la presión
aórtica, la válvula se cierra produciendo el segundo ruido cardíaco y finaliza la
expulsión ventricular. La presión del VI disminuye durante una fase de
relajación isovolumétrica hasta que cae por debajo de la presión de la AI,
momento en que se abre la válvula mitral (AVM). Empieza entonces una fase
de llenado ventricular rápido, durante la cual puede oírse un tercer ruido
cardíaco. Véase el texto para la discusión sobre el pulso venoso yugular.
El VL es una medida de la función mecánica del corazón y depende de la
precarga, la poscarga y la contractilidad miocárdica (Tabla 3-2). La precarga es el
volumen de sangre presente en el ventrículo al final de la diástole y
fundamentalmente es un reflejo del retorno venoso. Dentro de unos límites, cuando
la precarga aumenta el ventrículo se distiende y la contracción ventricular resultante
es más rápida y potente. Este fenómeno se conoce como la ley de Frank–Starling.
Debido a que el volumen ventricular no se puede determinar fácilmente, se utiliza
la presión del llenado ventricular (presión ventricular telediastólica, presión
auricular o presión de enclavamiento pulmonar capilar) como medida sustitutiva de
la precarga.
La poscarga es la fuerza contra la que los ventrículos deben contraerse para
expulsar la sangre. Anivel práctico, se utiliza la presión arterial como medida de la
poscarga, aunque para ser estrictos la poscarga se determina a través de la presión
intraventricular, el tamaño de la cavidad ventricular y el grosor de las paredes del
ventrículo (ley de Laplace). Por ello, la poscarga está aumentada en la hipertensión
sistémica o cuando hay una estenosis de la válvula aórtica, así como también
cuando existe una dilatación o hipertrofia ventriculares.
3 ESTRUCTURA Y FUNCIÓN DEL Página 13 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
La contractilidad o capacidad inotrópica, aunque es difícil de definir, representa
la fuerza de la contracción ventricular independientemente de las condiciones de
carga. Por ejemplo, un aumento de la contractilidad da lugar a una contracción
ventricular más potente aun cuando la precarga y poscarga sean constantes. La
contractilidad puede alterarse en condiciones normales a través de la estimulación
directa de las terminaciones adrenérgicas en el miocardio y a través de las
catecolaminas circulantes liberadas por las glándulas suprarrenales. Existen varios
fármacos con efecto inotrópico positivo importante y con aplicación clínica, como
la digoxina y las catecolaminas (adrenalina, noradrenalina, dopamina). Otros
fármacos (p. ej., los β–bloqueantes, los antagonistas de los canales del calcio)
tienen efectos inotrópicos negativos y reducen la fuerza de la contracción
ventricular. 26
27
TABLA 3-1 Valores normales de los parámetros
hemodinámicos más frecuentes
Frecuencia cardíaca 60-100 latidos/minuto
Presiones
Venosa central ≤ 9 mmHg
Aurícula derecha ≤ 9 mmHg
Ventrículo derecho
Sístole 15-30 mmHg
Telediástole ≤ 9 mmHg
Arteria pulmonar
Sístole 15-30 mmHg
Diástole 3-12 mmHg
Capilar pulmonar de enclavamiento ≤ 12 mmHg
Aurícula derecha ≤ 12 mmHg
Ventrículo izquierdo
Sístole 100-140 mmHg
Telediástole 3-12 mmHg
Aorta
Sístole 100-140 mmHg
Diástole 60-90 mmHg
Resistencia
−5
Vascular sistémica (SVR) 800-1.500 dinas–s/cm
−5
Vascular pulmonar (PVR) 30-120 dinas–s/cm
Gasto cardíaco 4-6 l/min
Índice cardíaco 2,5-4 l/min
3 ESTRUCTURA Y FUNCIÓN DEL Página 14 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
Tabla 3-2 Factores que afectan al funcionalismo cadío
De forma general, la función ventricular sistólica se cuantifica con frecuencia a
través de la fracción de eyección, que es la relación entre el VL y el volumen
telediastólico, o sea, la fracción de sangre expulsada en cada contracción
ventricular. La fracción de eyección normal es de aproximadamente el 60% y puede
determinarse mediante métodos invasivos (ventriculografía radiológica) o no
invasivos (ecocardiografía, ventriculografía isotópica).
No hay ninguna duda de que la contracción sistólica constituye un componente
importante de la función ventricular; sin embargo, la relajación ventricular
diastólica (lusitropía) también juega un papel importante en la función cardíaca
global. Una alteración en dicha relajación (disfunción diastólica), como en el caso
de la hipertrofia o isquemia ventriculares, da lugar a un ventrículo rígido y no
distensible, con un mal llenado ventricular y un aumento de la presión ventricular
para cualquier volumen diastólico determinado.
Fisiología de la circulación coronaria
El corazón es un órgano aeróbico que precisa un aporte constante de oxígeno para
mantener su funcionamiento normal. En condiciones normales, el aporte de
oxígeno suministrado al corazón se equipara estrechamente con la cantidad de
oxígeno que aquél necesita (el consumo de oxígeno en el miocardio [MVO2]). Los
3 ESTRUCTURA Y FUNCIÓN DEL Página 15 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
principales factores determinantes del MVO2 son la frecuencia cardíaca, la
contractilidad y la tensión de pared. La tensión de pared, determinada por la ley de
Laplace, está directamente relacionada con la presión sistólica y el tamaño cardíaco:
Tensión de pared = (presión X radio)/(2 X grosor de pared).
Por ello, el MVO2 sigue cambios paralelos en la frecuencia cardíaca, presión
arterial, contractilidad y tamaño del corazón. Por lo general, el oxígeno
suministrado a un órgano puede aumentar a través del incremento del flujo
sanguíneo o por el incremento en la extracción de oxígeno de la sangre. Por razones
prácticas, la extracción de oxígeno por parte del corazón ya es máxima en reposo y,
consecuentemente, los incrementos en el MVO2 deben satisfacerse a través del
incremento del flujo sanguíneo coronario.
Debido a la compresión de los vasos sanguíneos intramiocárdicos durante la
sístole, la mayor parte del flujo coronario aparece durante la diástole. Por lo tanto,
la presión diastólica es la principal en la circulación coronaria. Una implicación
importante de este hecho es que la taquicardia, que fundamentalmente acorta la
duración de la diástole, da lugar a una disminución del tiempo de flujo coronario, lo
que aparece a pesar del incremento del MVO2 asociado al aumento de la frecuencia
cardíaca. La presión sistólica tiene un escaso impacto sobre el flujo sanguíneo
coronario, excepto en la medida en que los cambios en la presión arterial provoquen
cambios en el MVO2.
La regulación del flujo sanguíneo coronario se produce fundamentalmente a
través de cambios en la resistencia vascular coronaria. En respuesta a los cambios
en el MVO2, las arterias coronarias pueden dilatarse o estrecharse para ajustarse a
los cambios en el flujo coronario. Además, dentro del rango de 60-130 mmHg de la
presión de perfusión coronaria, el flujo sanguíneo coronario es constante a través
del proceso de autorregulación coronario. Dicha regulación de la resistencia arterial
aparece en las arteriolas y está mediada por varios factores. Amedida que el
trifosfato de adenosina se metaboliza durante el aumento de la actividad
miocárdica, la adenosina se libera y actúa como un potente vasodilatador. Durante
el aumento del metabolismo cardíaco aparecen una disminución de la tensión de
oxígeno y un aumento del dióxido de carbono, así como acidosis e hiperpotasemia,
y ello también puede mediar en la vasodilatación coronaria. 27
28
Las arterias coronarias están inervadas por el sistema nervioso autónomo, y la
activación de las neuronas simpáticas o parasimpáticas afecta al flujo sanguíneo
coronario a través de cambios en el tono vascular. La inervación parasimpática se
3 ESTRUCTURA Y FUNCIÓN DEL Página 16 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
realiza a través del nervio vago y, mediante el neurotransmisor acetilcolina, se
produce una vasodilatación. Las neuronas simpáticas utilizan noradrenalina como
neurotransmisor y producen efectos opuestos sobre la vascularización coronaria. La
estimulación de los receptores α produce una vasoconstricción, mientras que la
estimulación de los receptores β conduce a una vasodilatación.
La capacidad de los vasos coronarios para mediar en los cambios del flujo
sanguíneo a través de los cambios en el tono vascular depende en gran parte de un
endotelio íntegro y con funcionalismo normal. El endotelio produce varios
dilatadores potentes, incluyendo el factor relajante derivado del mismo (EDRF) y la
prostaciclina. El EDRF probablemente es óxido nítrico o un compuesto que lo
contiene, y es liberado por el endotelio en respuesta a la acetilcolina, trombina,
ADP, serotonina, bradicinina, la agregación plaquetaria y el aumento en las fuerzas
de rotura. Este último estímulo justifica la dilatación de las arterias coronarias en
respuesta al incremento del flujo sanguíneo en el contexto del aumento del MVO2
(la llamada vasodilatación dependiente del flujo).
El endotelio también produce factores vasoconstrictores, especialmente la
endotelina, y probablemente tienen un papel en la regulación del tono vascular. El
equilibrio entre los factores vasodilatadores y vasoconstrictores es importante en
situaciones como el espasmo coronario. Además de influir sobre el tono vascular, el
endotelio tiene otras funciones con importantes implicaciones para el flujo
sanguíneo y la perfusión tisular. Éstas incluyen el mantenimiento de una superficie
no trombótica a través de la inhibición de la actividad plaquetaria, el control de la
trombosis y la fibrinólisis y la modulación de la respuesta inflamatoria de los vasos.
Resulta probable que los trastornos de estas propiedades normales del endotelio
(disfunción endotelial) tengan un papel importante en la fisiopatología de la
aterosclerosis y trombosis coronarias.
Fisiología de la circulación sistémica
Las paredes de la aorta y de las arterias principales son ricas en fibras elásticas. Con
la expulsión de sangre durante la sístole ventricular, estas fibras permiten que
dichas arterias se distiendan y posteriormente se retraigan, dando lugar con ello a
un suministro paulatino de sangre hacia la periferia. Las grandes arterias se
ramifican convirtiéndose progresivamente en arterias menores y finalmente en
arteriolas, las ramas reguladoras terminales del árbol arterial. Las arteriolas
funcionan como "vasos de resistencia", debido a la presencia de esfínteres
musculares, y controlan el flujo de sangre hacia el sistema capilar. Las propias
arteriolas se encuentran bajo una regulación doble: centralmente a través del
3 ESTRUCTURA Y FUNCIÓN DEL Página 17 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
sistema nervioso y localmente a través de las condiciones en la vecindad inmediata
de los vasos sanguíneos. El sistema vascular está inervado por fibras simpáticas y
parasimpáticas. La estimulación del sistema α–adrenérgico da lugar a una
vasoconstricción, mientras que la estimulación β–adrenérgica o vagal provoca una
vasodilatación. Localmente, una PO2 baja, una PCO2 elevada y una acidosis
provocan una vasodilatación por relajación directa de los esfínteres arteriolares. La
resistencia vascular sistémica (SVR) es una medida del tono vascular total, y se
define por la caída de la presión a través del lecho capilar periférico dividido entre
el flujo sanguíneo que atraviesa dicho lecho. En la práctica, ello se calcula como la
presión arterial media menos la presión de la aurícula derecha dividido entre el
gasto cardíaco y normalmente se encuentra en el rango de las 800-1.500 dinas–
−5
s/cm .
La sangre abandona las arteriolas y fluye dentro del sistema capilar, donde el
oxígeno y los nutrientes son suministrados a las células y se recuperan el dióxido de
carbono y los residuos metabólicos. La sangre desoxigenada drena en las venas
periféricas, que contienen válvulas para evitar el flujo retrógrado. Estas venas
presentan paredes más delgadas que las arterias y funcionan como "vasos de
capacidad", capaces de acomodar un volumen de sangre significativamente superior
que en el sistema arterial. Con la ayuda de la acción de bombeo de la musculatura
esquelética y el movimiento respiratorio de la pared torácica, la sangre vuelve a la
aurícula derecha. Este retorno venoso puede alterarse por la constricción o
dilatación de las venas periféricas. Además del retorno venoso, existe un rico
sistema de vasos linfáticos que ayudan a evacuar el exceso de líquido intersticial de
la periferia. Los diferentes vasos linfáticos drenan en el conducto torácico y
posteriormente éste desemboca en la vena braquiocefálica izquierda.
Fisiología de la circulación pulmonar
De forma similar a lo que sucede con la circulación sistémica, la pulmonar está
compuesta por una red de ramificaciones progresivas de arterias pequeñas en
arteriolas, capilares y venas. Los capilares pulmonares están separados de los
alvéolos por una fina membrana alveolocapilar a través de la cual sucede el
intercambio gaseoso. El dióxido de carbono difunde desde la sangre capilar hacia el
alvéolo, y el oxígeno desde el alvéolo hacia la sangre. El flujo sanguíneo en los
diferentes segmentos pulmonares viene regulado por varios factores, siendo el más
importante la presión parcial de oxígeno en el alvéolo. De esta forma, la sangre es
cortocircuitada hacia segmentos pulmonares bien ventilados y alejada de segmentos
mal ventilados. De forma secundaria a la naturaleza extensa del sistema capilar
3 ESTRUCTURA Y FUNCIÓN DEL Página 18 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
pulmonar y a la distensibilidad de los vasos pulmonares, la resistencia a través del
sistema pulmonar (la resistencia vascular pulmonar [PVR]) es aproximadamente
una décima parte de la observada en la circulación sistémica. Debido a estas
características, el sistema pulmonar es capaz de tolerar incrementos significativos
del flujo sanguíneo con un efecto mínimo o nulo sobre la elevación de la presión
pulmonar. Por ello, los cortocircuitos intracardíacos (como los defectos del tabique
auricular) pueden asociarse a una presión pulmonar normal.
El pulmón recibe un suministro sanguíneo doble. La arteria pulmonar aporta la
inmensa mayoría del flujo sanguíneo pulmonar; sin embargo, el pulmón también
recibe sangre oxigenada a través de las arterias bronquiales. Estos vasos
suministran oxígeno al propio pulmón y desembocan en las venas bronquiales.
Dichas venas drenan en parte en las venas pulmonares; por lo tanto, una pequeña
cantidad de sangre desoxigenada penetra normalmente en la circulación sistémica y
justifica un cortocircuito derecha–izquierda fisiológico. En condiciones normales,
este cortocircuito es insignificante y representa solamente un 1% del flujo
sanguíneo sistémico total. 28
29
La respuesta cardiovascular frente al ejercicio
La respuesta del corazón frente al ejercicio es multifactorial e implica a muchos de
los mecanismos de control circulatorio previamente abordados (Tabla 3-3). En
previsión del ejercicio, los centros nerviosos del cerebro estimulan la retirada vagal
e incrementan el tono simpático, dando lugar a un incremento de la frecuencia
cardíaca y de la contractilidad (y con ello un aumento del GC) aun antes de iniciar
el ejercicio. Durante el mismo, la vasoconstricción simpática, la acción de bombeo
de la musculatura esquelética y el aumento de los movimientos respiratorios de la
pared torácica provocan un aumento del retorno venoso al corazón. A través de la
ley de Frank–Starling se produce un aumento de la contractilidad miocárdica,
elevándose con ello el GC. La activación simpática también aumenta la
contractilidad; sin embargo, la mayor parte del incremento en el GC durante el
ejercicio (hasta cuatro a seis veces la normalidad) es una consecuencia del
incremento de la frecuencia cardíaca. La frecuencia cardíaca máxima que puede
alcanzarse depende de la edad y puede estimarse a partir de la siguiente fórmula:
FC máxima = (220 − edad) ± (10-12) latidos/min.
3 ESTRUCTURA Y FUNCIÓN DEL Página 19 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
Cecil Medicina Interna, 5th Edition
TABLA 3-3 Respuestas fisiológicas frente al ejercicio
Respuesta Mecanismo
↑ Frecuencia ↑ Estimulación parasimpática
cardíaca
↓ Estimulación simpática
↑ Volumen latido
↑ ↑ Estimulación simpática
Contractilidad
↑ Retorno Vasoconstricción venosa mediada por el sistema simpático
venoso
Acción de bombeo de la musculatura esquelética
↓ Presión intratorácica con la inspiración profunda
Vasodilatación arteriolar en los músculos sometidos a ejercicio
↓Poscarga Vasodilatación arteriolar en los músculos sometidos a ejercicio (mediada
fundamentalmente por metabolitos locales)
↑ Presión arterial ↑ Gasto cardíaco
Vasoconstricción (estimulación simpática) en el lecho vascular no
sometido a ejercicio
↑Extracción de O2 Desplazamiento de la curva de disociación de la oxihemoglobina debido
a la acidosis local
Los factores locales del ejercicio muscular provocan una dilatación arteriolar,
dando lugar a un aumento del flujo en el lecho capilar. Esta vasodilatación origina
una disminución de la resistencia al flujo y, por lo tanto, la SVR disminuye con el
ejercicio. A pesar de este cambio en la resistencia, la presión arterial sistólica
aumenta, debido al aumento del GC y a la vasoconstricción simpática, dando lugar
a un cortocircuito preferente de sangre que sale de los lechos vasculares no
sometidos a ejercicio. La presión arterial diastólica, por el contrario, normalmente
permanece constante durante el ejercicio. El sistema pulmonar es capaz de tolerar el
incremento del flujo con solamente pequeños incrementos en la presión pulmonar.
El aumento de la frecuencia cardíaca y la contractilidad dan lugar a un marcado
incremento del MVO2 (de hasta un 300%), y consecuentemente el flujo sanguíneo
coronario también aumenta.
Diferentes tipos de ejercicio originan efectos distintos sobre el sistema
circulatorio. La respuesta descrita aquí aparece con el ejercicio isotónico, como
correr o ir en bicicleta. En el ejercicio isométrico, por ejemplo al levantar pesos, la
respuesta predominante es el aumento de la presión arterial, debido a una elevación
de la vasoconstricción periférica.
3 ESTRUCTURA Y FUNCIÓN DEL Página 20 de 20
CORAZÓN Y LOS VASOS SANGUÍNEOS
También podría gustarte
- Material para Estudiar Parcial de HistologiaDocumento79 páginasMaterial para Estudiar Parcial de Histologiamarihenny VallejoAún no hay calificaciones
- Repaso CircuDocumento42 páginasRepaso CircuJessica Andrea Alamilla GarcíaAún no hay calificaciones
- El Corazón Se Localiza en La Cavidad TorácicaDocumento4 páginasEl Corazón Se Localiza en La Cavidad TorácicaEstefania De Jesus Arrazate GonzalezAún no hay calificaciones
- Corazón - Fisiologia IDocumento58 páginasCorazón - Fisiologia IFernanda GarcíaAún no hay calificaciones
- BOA de Anatomia (Sistema Cardiovascular)Documento12 páginasBOA de Anatomia (Sistema Cardiovascular)Erick RamirezAún no hay calificaciones
- 4ta Sistema Circulatorio IDocumento10 páginas4ta Sistema Circulatorio IRoxana Kelly ManferAún no hay calificaciones
- Sistemas cIRCULDocumento14 páginasSistemas cIRCULkriss PerezAún no hay calificaciones
- Resumen de Cardiologia-1Documento5 páginasResumen de Cardiologia-1jennifer garciaAún no hay calificaciones
- Act 4 Sist Circulatorio CorazonDocumento17 páginasAct 4 Sist Circulatorio Corazoningrid gomezAún no hay calificaciones
- ANATOMIA-DEL-APUNTE WEB CORAZON-VASOS-Y-CIRCULACION-PEÑA-Mariana-MEDICINA-EN-EL-TRABAJODocumento28 páginasANATOMIA-DEL-APUNTE WEB CORAZON-VASOS-Y-CIRCULACION-PEÑA-Mariana-MEDICINA-EN-EL-TRABAJOMelisa AlbertoAún no hay calificaciones
- Universidad Anáhuac Mayab: Anatomía, Fisiología Y Exploración CardiologicaDocumento35 páginasUniversidad Anáhuac Mayab: Anatomía, Fisiología Y Exploración CardiologicaValeria PechAún no hay calificaciones
- CirculatorioDocumento17 páginasCirculatorioYanina GonzálezAún no hay calificaciones
- Trabajo CardiopulmonarDocumento21 páginasTrabajo CardiopulmonarGeovanny RiobuenoAún no hay calificaciones
- Irrigacion e Invervación Del ToraxDocumento27 páginasIrrigacion e Invervación Del ToraxWilson RenéAún no hay calificaciones
- 4ta Sistema Circulatorio IDocumento10 páginas4ta Sistema Circulatorio ICarlos Farro AscencioAún no hay calificaciones
- Sistema Circulatorio 1Documento28 páginasSistema Circulatorio 1Sam Amoretti RobledoAún no hay calificaciones
- Cuestionario V - FisiologiaDocumento11 páginasCuestionario V - FisiologiaMaria GarciaAún no hay calificaciones
- Circulacion Mayor y Circulacion MenorDocumento6 páginasCirculacion Mayor y Circulacion MenorInformes 2022Aún no hay calificaciones
- Aparato Cardio Vasculr. Manual de EnfermeriaDocumento10 páginasAparato Cardio Vasculr. Manual de EnfermeriaCiber GamAún no hay calificaciones
- Camaras CardiacasDocumento105 páginasCamaras CardiacasAlejandro SolisAún no hay calificaciones
- El CorazonDocumento5 páginasEl CorazonAylin GarciaAún no hay calificaciones
- Anatomía y Fisiología Del Aparato CirculatorioDocumento14 páginasAnatomía y Fisiología Del Aparato CirculatorioLeticia SantanaAún no hay calificaciones
- Cuestionario de Sistema CirculatorioDocumento3 páginasCuestionario de Sistema CirculatorioVantex UghAún no hay calificaciones
- Apuntes UT3 ERLDocumento19 páginasApuntes UT3 ERLAinhoaAún no hay calificaciones
- Sistema CardiovascularDocumento23 páginasSistema CardiovascularMay AlejandraAún no hay calificaciones
- Sistema Circulatori CorreoDocumento40 páginasSistema Circulatori CorreoLEIDY SEGUIL CASACHAHUAAún no hay calificaciones
- Anatomia Del Sistema CardiacoDocumento8 páginasAnatomia Del Sistema CardiacoLoren RamirezAún no hay calificaciones
- Fisiología Cardíaca-MedGeneralIIDocumento8 páginasFisiología Cardíaca-MedGeneralIIAndrea PaosulineAún no hay calificaciones
- Cuidado Del Sistema CardiovascularDocumento29 páginasCuidado Del Sistema CardiovascularJefferson Roa SantaAún no hay calificaciones
- 0.FISIO UD4 CardioDocumento16 páginas0.FISIO UD4 CardioalejandragarciagmmAún no hay calificaciones
- Anatomía Del CorazónDocumento5 páginasAnatomía Del CorazónCitlaliAún no hay calificaciones
- Fisiologia CardiacaDocumento7 páginasFisiologia CardiacaMercedes CanalesAún no hay calificaciones
- Anatomía y Fisiología CardíacaDocumento10 páginasAnatomía y Fisiología CardíacaDaniel García CamañesAún no hay calificaciones
- Biologia InvestigacionDocumento19 páginasBiologia Investigacionalexis josue salinas vizcarraaAún no hay calificaciones
- Ud5 AnattomíaDocumento31 páginasUd5 AnattomíaALEJANDRA DE LA CUESTAAún no hay calificaciones
- Anatomia y Fisiologia Del CorazónDocumento14 páginasAnatomia y Fisiologia Del CorazónAlberto Fernandez PinillaAún no hay calificaciones
- 1-ANATOMIA Y FISIOLOGÃ A CV Lic. Enf. Estela CardozoDocumento9 páginas1-ANATOMIA Y FISIOLOGÃ A CV Lic. Enf. Estela CardozoKariiniita SalciidoAún no hay calificaciones
- Sistema CardiovascularDocumento17 páginasSistema CardiovascularTHANIA MAGALY CAMPOS PEREZAún no hay calificaciones
- CAPITULO 5.2 Estructura CorazonDocumento26 páginasCAPITULO 5.2 Estructura CorazonMike Dávila100% (1)
- CorazonDocumento11 páginasCorazonBRITTMAR LUDWING QUISPE CCANAHUIREAún no hay calificaciones
- Sistema Cardiovascular PDFDocumento15 páginasSistema Cardiovascular PDFJulia AlfonsinAún no hay calificaciones
- Apuntes Sobre Aparato Circulatorio IDocumento9 páginasApuntes Sobre Aparato Circulatorio IRoberto Esteban Mandiola OpazoAún no hay calificaciones
- Taller AnatomiaDocumento9 páginasTaller Anatomiaapi-500170978Aún no hay calificaciones
- Marco Teorico CardiovascularDocumento10 páginasMarco Teorico CardiovascularKatinaGonzalesYovera100% (1)
- QC Enzimas CardiacasDocumento49 páginasQC Enzimas CardiacasQUIMICO CLINICO WILLIANS SANCHEZ97% (32)
- Ecc AdultosDocumento120 páginasEcc AdultosNelson JaldinAún no hay calificaciones
- UrgenciasDocumento12 páginasUrgenciasDario Cruz RosalesAún no hay calificaciones
- Anatomia Corazón y S. CirculatorioDocumento15 páginasAnatomia Corazón y S. CirculatorioJuanita MonterrosoAún no hay calificaciones
- Apuntes CorazonDocumento9 páginasApuntes CorazonatrompaAún no hay calificaciones
- Resumen Del CorazonDocumento6 páginasResumen Del CorazonLAURA GONZALEZAún no hay calificaciones
- Sistema Cardiovascular - LinfaticoDocumento13 páginasSistema Cardiovascular - LinfaticoItzy BernalAún no hay calificaciones
- TareaDocumento4 páginasTareaVivian MelendezAún no hay calificaciones
- Actividad 1-Fabiola GonzalezDocumento11 páginasActividad 1-Fabiola GonzalezFabiola ArizagaAún no hay calificaciones
- Sistema CirculatorioDocumento12 páginasSistema CirculatorioAndrea FernándezAún no hay calificaciones
- El Sistema Circulatorio ResumenDocumento14 páginasEl Sistema Circulatorio ResumenCastro Albina100% (5)
- Sistema CardiovascularDocumento10 páginasSistema CardiovascularEnos DEGBEAún no hay calificaciones
- Sistema Cardiovascular - Jesús GonzálezDocumento18 páginasSistema Cardiovascular - Jesús GonzálezJesús GonzálezAún no hay calificaciones
- Anatomia Del CorazonDocumento6 páginasAnatomia Del CorazonVioleta Tello MedinaAún no hay calificaciones
- Introducción Básica a la Microcirculación de la Sangre: La Siguiente Generación en Cuidados de la SaludDe EverandIntroducción Básica a la Microcirculación de la Sangre: La Siguiente Generación en Cuidados de la SaludAún no hay calificaciones
- Mejorar la Circulación Sanguínea de Forma Natural: Sanar el Sistema Circulatorio y inmunológico para Prevenir Enfermedades, Aumentar la Energía, Aliviar el Estrés y Sentirte Mejor que NuncaDe EverandMejorar la Circulación Sanguínea de Forma Natural: Sanar el Sistema Circulatorio y inmunológico para Prevenir Enfermedades, Aumentar la Energía, Aliviar el Estrés y Sentirte Mejor que NuncaCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Cecil 5Documento30 páginasCecil 5Sofía L.Aún no hay calificaciones
- Cecil 4Documento34 páginasCecil 4Sofía L.Aún no hay calificaciones
- Cecil 2Documento9 páginasCecil 2Sofía L.Aún no hay calificaciones
- Cecil 1Documento24 páginasCecil 1Sofía L.Aún no hay calificaciones
- Hiperónimo y HipónimosDocumento2 páginasHiperónimo y HipónimosMarco Antonio Limunao PurránAún no hay calificaciones
- PDF EspermatogénesisDocumento0 páginasPDF Espermatogénesisbeagj_15Aún no hay calificaciones
- Eponimos de IncisionesDocumento6 páginasEponimos de IncisionesJuan Miguel AlemanAún no hay calificaciones
- Aprenda A Tirar El Caracol PDFDocumento362 páginasAprenda A Tirar El Caracol PDFJose Ricardo Castellanos Garcia67% (3)
- Manual Formacion Primeros RespondientesDocumento83 páginasManual Formacion Primeros RespondientesAvril Franco MorenoAún no hay calificaciones
- Leucoreduccion de Los Concentrados EritrocitariosDocumento9 páginasLeucoreduccion de Los Concentrados EritrocitariosWilsonAún no hay calificaciones
- Virus - Bacterias Clase 2Documento27 páginasVirus - Bacterias Clase 2Alexita RuizAún no hay calificaciones
- Historia Clinica CardiologicaDocumento7 páginasHistoria Clinica CardiologicaMariel Sullón RamirezAún no hay calificaciones
- Hemostasia en Cirugía. AmhedDocumento30 páginasHemostasia en Cirugía. AmhedArabeAún no hay calificaciones
- Anatomia - Veterinaria - Dyce - 4ta - Edicion (Arrastrado) 4Documento1 páginaAnatomia - Veterinaria - Dyce - 4ta - Edicion (Arrastrado) 4Victoor PazAún no hay calificaciones
- Entomologia Forense NelsonDocumento25 páginasEntomologia Forense NelsonEdna PatriciaAún no hay calificaciones
- Guía de Práctica de Embriología General ScribdDocumento12 páginasGuía de Práctica de Embriología General ScribdAnel MamaniAún no hay calificaciones
- Curve in MathDocumento58 páginasCurve in Math王竣寬Aún no hay calificaciones
- Practica Medica I Unidad I Exploracion de Piel y CardiovascularDocumento276 páginasPractica Medica I Unidad I Exploracion de Piel y CardiovascularCarol JCAún no hay calificaciones
- Dulces SueñosDocumento174 páginasDulces SueñosIsa NegreiraAún no hay calificaciones
- Preguntas MIR, Examenes MIR, Test MIR, Preguntas de Medicina, Formación OnliDocumento12 páginasPreguntas MIR, Examenes MIR, Test MIR, Preguntas de Medicina, Formación OnliJaime AristiguetaAún no hay calificaciones
- Sistema-Respiratorio 1Documento4 páginasSistema-Respiratorio 1Valentina MoraAún no hay calificaciones
- Alimentacion para Epoca de Sequia - Pastos y ForrajesDocumento74 páginasAlimentacion para Epoca de Sequia - Pastos y ForrajesLinda RamosAún no hay calificaciones
- Distribución de Muestras BiológicasDocumento4 páginasDistribución de Muestras BiológicasMaria de los Angeles Morales OchoaAún no hay calificaciones
- Patologia Benigna de Colon y Recto UeesDocumento32 páginasPatologia Benigna de Colon y Recto UeesCristina Bran SarmientosAún no hay calificaciones
- Hemoglobina-1Documento18 páginasHemoglobina-1Djvans Samanamud OsorioAún no hay calificaciones
- Insuficiencia Renal Aguda MonografiaDocumento24 páginasInsuficiencia Renal Aguda MonografiaJuan Marcelo Escobar100% (2)
- Monografia Aparato RespiratorioDocumento42 páginasMonografia Aparato RespiratorioRiro Pezzo85% (20)
- ORNITORINCODocumento5 páginasORNITORINCOVictoria BritosAún no hay calificaciones
- Cuál Es El Agente Causal de La LeptospirosisDocumento23 páginasCuál Es El Agente Causal de La LeptospirosisTOMAS MARINAún no hay calificaciones
- Escuela de Capacitación para Conductores Profesionale1Documento2 páginasEscuela de Capacitación para Conductores Profesionale1Peluche VivancoAún no hay calificaciones
- Proteccion de Los SentidosDocumento20 páginasProteccion de Los SentidosMiguel Emilio GuelermanAún no hay calificaciones
- Suprovet LaboratorioDocumento2 páginasSuprovet LaboratorioMilagros Uzuriaga SánchezAún no hay calificaciones
- Resumen ATLSDocumento13 páginasResumen ATLSNadir al bu lah100% (2)
- Caries Clase 3Documento12 páginasCaries Clase 3Rosalinda MartínezAún no hay calificaciones