Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Monitoreo Hemodinámico y Gasométrico (MHEGAS
Cargado por
URGENCIAS MEDICAS-IMSS 46Descripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Monitoreo Hemodinámico y Gasométrico (MHEGAS
Cargado por
URGENCIAS MEDICAS-IMSS 46Copyright:
Formatos disponibles
Autores y profesores de curso:
DR. SERGIO EDGAR ZAMORA GOMEZ
Medicina de Urgencias CMN La Raza IMSS/Medicina del enfermo en Estado Crítico Hospital
Juárez de México SSA.
DR. ORLANDO RUBÉN PEREZ NIETO
Medicina de Urgencias Hospital Primero de Octubre, ISSSTE/ Medicina del enfermo en Estado
Crítico Hospital Juárez de México SSA.
DR. EDER IVÁN ZAMARRÓN LÓPEZ
Medicina de Urgencias Hospital General Regional #6 Cd. Madero, Tam. / Medicina del enfermo
en Estado Crítico Hospital Regional PEMEX Madero, Tam.
Prologo
El curso taller Monitoreo Hemodinámico y Gasométrico (MHEGAS) tiene como objetivo transmitir
de forma concisa conceptos fundamentales para la adecuada atención del paciente con
inestabilidad hemodinámica, por lo que se ha diseñado de forma practica y sencilla por un
equipo de especialistas en Urgencias y Medicina Crítica.
Sin duda la atención adecuada del paro cardiaco aumentará las posibilidades de mortalidad del
paciente, pero un porcentaje muy alto de estos presentan datos de inestabilidad en un periodo
previo de entre 6 a 24 horas, por lo que es muy importante no solo saber reconocer los signos
de inestabilidad, sino saber tratarlos. Aunque un porcentaje alto de pacientes críticos se
encontrarán en Departamentos de Urgencias o Unidades de Terapia Intensiva, otros estarán
en Hospitalización, Quirófano, área de recuperación y en Ambiente prehospitalario, por lo que
es indispensable que cualquier personal de la salud logre identificar e iniciar tratamiento de
este tipo de pacientes.
Las mejoras esperadas con la implementación del curso taller MHEGAS es reducir al mínimo el
tiempo entre la aparición de los signos y síntomas clínicos, correcto diagnostico y tratamiento
del paciente con inestabilidad hemodinámica, usando las herramientas diagnosticas acorde a
nuestro medio, implementando así las intervenciones individualizadas acorde a cada paciente.
Este curso tiene como profesores fundadores al Dr. Sergio Edgar Zamora Gómez, Dr. Orlando
Rubén Pérez Nieto y Eder Iván Zamarrón López, teniendo el primer curso en Hospital Central
de San Luis Potosí, el día 28 de Mayo de 2017.
Siguiendo la máxima: “Cuidados críticos no es un lugar, es una actitud” es que se transmite
conocimiento a todo el personal de salud que comparta nuestro interés… salvar vidas.
Los autores
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 1
INDICE
Tema Pag.
Capitulo 1
GASTO CARDIACO APLICADO A LA CLINICA……………………………………. 4
Sergio Edgar Zamora Gómez
Capitulo 2
CHOQUE. DEFINICIÓN, IDENTIFICACIÓN Y CLASIFICACIÓN………………………... 9
Orlando Rubén Pérez Nieto
Capitulo 3
EVALUACION HEMODINAMICA EN ESCENARIOS DE RECURSOS LIMITADOS………… 14
Sergio Edgar Zamora Gómez
Capitulo 4
EQUILIBRIO ÁCIDO-BASE…………………………………………………… 20
Orlando Rubén Pérez Nieto
Capitulo 5
MONITOREO HEMODINÁMICO ECOGUIADO Y OTRAS UTILIDADS EN AREAS CRÍTICAS... 29
Eder Iván Zamarrón López/ Héctor Valenzuela Suarez
Capitulo 6
INTEGRACIÓN DEL MANEJO DEL PACIENTE CON INESTABILIDAD HEMODINAMICA…... 46
Eder Iván Zamarrón López
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 2
Capitulo 1. GASTO CARDIACO APLICADO A LA CLINICA
“No importa el valor numérico del Gasto Cardiaco, sino si es adecuado o no para el paciente”
Sergio Edgar Zamora Gómez
Introducción
El gasto cardiaco (GC) puede ser analizado y estimado desde diferentes niveles de profundidad
fisiológica y tecnológica, sin embargo todos y cada uno de ellos carecen de perfección en su
abordaje, sobre todo por la utilización de variables inferidas estandarizadas que se aplican de
manera uniforme en aquellos que se basan solamente en obtención mediante cálculos o
“talleres”. El advenimiento de la tecnología ha permitido un abordaje más aproximado a la
fisiología cardiovascular, sin embargo los algoritmos por los cuales se rigen no están exentos
de alteraciones en sus estimaciones debido a varias situaciones clínicas que no son
infrecuentes en el paciente críticamente enfermo, además de la limitada disponibilidad, derivada
del alto costo de la mayoría de ellos. Ningún abordaje, cualquiera que sea, tiene un impacto en
la evolución del paciente si no tiene una aplicación clínica, el objetivo del presente texto es
brindar herramientas tangibles para realizar un abordaje clínico del gasto cardiaco.
Determinantes del gasto cardiaco
El abordaje más simplista del gasto cardiaco es la Fórmula:
Gasto Cardiaco (GC) = Volumen Sistólico (VS) x Frecuencia Cardiaca (FC)
Este abordaje nos permite considerar que el gasto cardiaco se va a mantener a expensas
principalmente del VS, y que cualquier alteración en éste, se verá reflejado en la FC. El volumen
VS que es eyectado del corazón determinado número de veces por minuto, es decir la FC, debe
generar como resultado de la interacción con la resistencia vascular sistémica (RVS) una
presión resultante, es decir la Presión Arterial Media (PAM), la cual debe asegurar la perfusión
de todos los órganos del cuerpo. Cuando un paciente tiene un VS reducido la respuesta
compensadora es el incremento de la FC, para mantener un GC constante y generar una PAM
perfusora, cuando ésta última no se logra, estamos hablando de un estado de choque. Cuando
un paciente tiene una función contráctil incrementada como en el caso de pacientes atletas, la
FC tiende a ser baja ya que no se requiere más para mantener un GC constante y una PAM
perfusora. Existe una condición particular en la cual el VS puede estar normal o incrementado,
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 3
sin embargo las RVS tan reducidas que el VS no genera una PAM perfusora, y conlleva a un
estado de choque, el ejemplo característico es el choque séptico.
Dado lo anterior, nos centraremos en los factores que determinan el VS, el primero de ellos es
el volumen de llenado de las cavidades cardiacas y que genera tensión y estiramiento de la
fibra miocárdica en condiciones de reposo; ese volumen de llenado es lo que conocemos como
precarga. La precarga por lo tanto genera tensión en la fibra miocárdica y tiene en condiciones
de normalidad relación directa con el VS, es decir a mayor volumen de precarga mayor el VS
eyectado, sin embargo cada corazón sano o enfermo tiene un límite de tolerancia de precarga,
el cual si es rebasado el VS ya no incrementa, incluso se reduce, generando caída del GC; esto
sucede en la falla cardiaca aguda.
Por otro lado la función ventricular también interviene en el VS eyectado; cuando el corazón
tiene disminución de la fuerza contráctil, aun incluso en condiciones de precarga normal, el VS
puede ser inferior a lo esperado, es la llamada Insuficiencia Cardiaca con Función Sistólica
alterada, la cual frecuentemente se acompaña de hipertrofia ventricular excéntrica o dilatada.
Cuando el corazón es sometido a incremento de las RVS de forma crónica como en los pacientes
con hipertensión arterial sistémica, en fases iniciales existe una hipertrofia ventricular
compensadora caracterizada por hipertrofia concéntrica, la cual mantiene la función sistólica
preservada, incluso incrementada, pero reduce el tamaño de la cavidad ventricular, y por lo
tanto el volumen de llenado máximo, lo que condiciona que el VS pueda verse reducido; éstos
pacientes usualmente presentan un corazón con disminución en su capacidad de relajación
miocárdica. En el último caso el mecanismo compensador esperado es el incremento de la FC
para mantener constante el GC, sin embargo, a medida que la FC se incrementa, el tiempo de
llenado del ventrículo se reduce y por lo tanto el volumen de llenado también se ve reducido y
por ende el VS también se verá reducido.
Finalmente cuando precarga y función ventricular están preservadas, la FC por si sola puede
generar alteración en el GC, cuando es muy alta la FC genera llenado ventricular escaso y VS
insuficiente, y cuando la FC es muy baja a pesar que el VS sea adecuado, el GC se encontrará
reducido a expensas de la FC.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 4
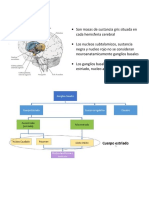
Esquema 1. Determinantes del gasto cardiaco
Valoración clínica del gasto cardiaco
Cuando se está frente a un paciente, sobre todo crítico, lo más importante no es conocer el
valor numérico del GC, sino determinar si el GC que está generando el sistema cardiovascular
del paciente es adecuado y suficiente para mantener la perfusión tisular sistémica.
La primera valoración es la clínica la cual se fundamenta en la exploración de tres “ventanas”
es decir datos que reflejan la perfusión sistémica, la primera es la ventana neurológica, e implica
que el paciente tenga integridad neurológica sobre todo del estado de conciencia. La segunda
ventana es la renal, la cual se valora mediante los flujos urinarios que deben de ser acorde al
volumen ingresado al paciente. La tercera ventana es la cutánea, la cual suele valorarse
mediante la temperatura dérmica y mediante la coloración de la piel, específicamente la
presencia de piel marmórea implica disminución de la perfusión tisular.
Imagen 1. Ventanas clínicas para detectar hipoperfusión tisular
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 5
Valoración bioquímica del gasto cardiaco y la perfusión tisular
En caso de que se cuente con datos clínicos francos de hipoperfusión o que no se tenga certeza
de la misma existen herramientas bioquímicas accesibles sobre todo en los pacientes críticos,
tales como el nivel sérico de lactato, el cual debe ser menor de 2 mmol/L, y el más certero en
la actualidad el cual es medir la diferencia de la presión parcial de CO2 a nivel venoso (de
preferencia medido en una muestra venosa central) y restarle el valor de la presión parcial de
CO2 a nivel arterial; la diferencia venoarterial de pCO2 no debe ser mayor de 6 mmHg, en caso
de ser superior a 6 mmHg existen tres posibilidades de hipoperfusión, la primera GC
inadecuado, la segunda disfunción mitocondrial, y la tercera la suma de la primera y la segunda.
Otra valoración bioquímica es la diferencia arteriovenosa de oxígeno, la cual se obtiene
restando al contenido arterial de oxígeno el contenido venoso de oxígeno; el valor normal es
de 3-5 mmHg, cuando es menor de 3 mmHg suele asociarse a un gasto cardiaco alto. Otra
herramienta bioquímica es la diferencia entre la saturación venosa central de oxígeno (SVcO2)
y la saturación arterial de oxígeno (SaO2), el valor normal es de 20-30%, cuando es menor de
20% se asocia a gasto cardiaco alto y cuando es mayor de 30% suele asociarse a gasto
cardiaco bajo.
Valoración paraclínica del gasto cardiaco
En la actualidad existen múltiples tecnologías que permiten la estimación del GC, cobran
importancia aquellas que se pueden realizar a la cabecera del paciente y con la menor invasión
posible, obteniendo la mayor cantidad de información posible; es así que la ultrasonografía se
ha convertido en un aliado fundamental para el médico que atiende pacientes críticos para
valorar GC y las determinantes del mismo, lo cual se explicará en capítulos posteriores con
detalle.
Conclusiones
El GC es el resultado de la interacción de múltiples variables, el VS es el determinante clínico
más útil en la valoración clínica. El entender que factores influyen en el comportamiento del VS
permite mediante un abordaje fisiológico y fisiopatológico elucidar los mecanismos subyacentes
implicados en el paciente en cuestión y facilitan el abordaje terapéutico. Existen herramientas
clínicas, bioquímicas y paraclínicas para lograr una valoración integral del GC, VS y sus
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 6
determinantes; en los siguientes capítulos se aprenderá la manera de detectar estado de
choque y abordajes de manejo basados en los principios fisiológicos citados en éste capítulo.
Bibliografía recomendada:
1. Cecconi M, De Backer D, Antonelli M, Beale R, Bakker J, Hofer C, et al. Consensus on circulatory shock
and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine. Intensive
Care Med (2014) 40:1795–1815DOI: 10.1007/s00134-014-3525-z
2. Guyton. Tratado de Fisiología Médica. 12Ed
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 7
Capitulo 2. ESTADO DE CHOQUE:
DEFINICIÓN, IDENTIFICACIÓN Y CLASIFICACIÓN.
“No hay un estado de choque en el paciente, sino pacientes con estados de choque”
Orlando Rubén Pérez Nieto
Introducción.
El estado de choque es una entidad muy frecuente en urgencias, hospitalización y terapia
intensiva, causado por un sinfín de patologías, y que pone en riesgo inminente de muerte al
paciente de no ser identificado y tratado de manera oportuna, de acuerdo a su clasificación,
dado que los diferentes tipos de shock, requieren de un tratamiento diferente, y de no ser
llevado a cabo adecuadamente, puede llevar a un desenlace fatal.
Definiciones.
Choque:
• Estado de disminución de energía, caracterizado por una disminución de producción de
ATP (trifosfato de adenosina), con aumento de la demanda metabólica celular.
• Estado de profunda y amplia reducción de perfusión tisular efectiva, ocasionando un
desbalance entre el aporte de Oxígeno (DO2) y el consumo del mismo (VO2), conocido
como disoxia, que lleva a daño celular reversible y posteriormente irreversible.
El oxígeno es el sustrato que las células ocupan para el metabolismo aerobio, del cual depende
la integridad celular. Los tejidos reciben una cantidad de oxígeno que iguala los requerimientos
metabólicos. Si el suplemento falla, la hipoxemia lleva a las células a realizar un metabolismo
anaeróbico parcialmente compensatorio, producción de Lactato y acumulación de metabolitos
que pueden llegar a ser citotóxicos.
Nota: El estado de choque no está definido ni determinado únicamente por variables
macrohemodinámicas (tensión arterial, frecuencia cardiaca), frecuentemente es causado por
hipotensión sostenida, sin embargo, puede existir hipotensión sin choque, así como choque,
sin hipotensión.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 8
Identificación
Se basa en parámetros clínicos obtenidos con la exploración física, y paraclínicos con estudios
de laboratorio.
Signos y síntomas:
• Estado mental alterado (Somnolencia, Estupor, Coma)
• Hipotermia
• Taquipnea (Frecuencia Respiratoria > 22 rpm)
• Taquicardia (Frecuencia Cardiaca > 100 lpm)
• Hipotensión arterial (Tensión Arterial Sistólica < 90 mmHg)
• Llenado capilar retardado (> 3 segundos)
• Oliguria (< 400 ml en 24 h)
Índice de choque: FC / TAS
> 0.8 = Choque
> 1.5 = Choque grave
Estudios paraclínicos.
• Lactato > 2 mmol/l = Choque
• Existen varios estudios complementarios que nos pueden ayudar a identificar el origen
del choque, sus complicaciones o su magnitud, tales como Hematócrito, Hemoglobina,
Creatinina, Presión arterial de Oxígeno (PaO2), Saturación venosa central de Oxígeno
(SvcO2), Capnografía, etc. sin embargo, ninguno de ellos se utiliza como diagnóstico.
Si el estado de choque se deja evolucionar libremente, conduce a falla orgánica múltiple (DOM)
y posteriormente a la muerte.
Clasificación
Clasificar el estado de choque es de gran utilidad, dado que nos orienta hacia el diagnóstico
etiológico desencadenante y al tratamiento que debemos utilizar para revertirlo, es de suma
importancia realizar este paso a la brevedad posible.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 9
El choque se clasifica en varios tipos, hipovolémico, cardiogénico, obstructivo y otros, que
generan falla circulatoria.
1. Hipovolémico
Determinado por una disminución en la precarga circulatoria, cuyas causas más frecuentes
son:
§ Hemorragia externa
§ Hemorragia interna
§ Deshidratación severa
2. Cardiogénico
Determinado por una falla o disminución en la contractilidad miocárdica o en su eficiencia,
dentro de su etiología más frecuente se encuentran:
§ Infarto Agudo al Miocardio
§ Disfunción ventricular izquierda
§ Disfunción ventricular derecha
3. Obstructivo
Determinado por una condicionante mecánica que aumenta la resistencia en la circulación
menor y cavidades cardiacas derechas, e impidiendo el paso de la precarga, sus causas
principales son:
§ Neumotórax a tensión
§ Tromboembolia pulmonar
§ Taponamiento cardiaco
4. Distributivo
Determinado por una disminución de las resistencias vasculares sistémicas por
vasodilatación no regulada, desencadenada por mecanismos inflamatorios, sus dos
etiologías son las siguientes:
§ Séptico
§ Anafiláctico
§ Inflamatorio (ej. pancreatitis)
5. Otros
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 10
Determinado por alteraciones disminución en el tono simpático (vasodilatación,
bradicardia) de diversas etiologías y combinación de los cuatro grupos anteriores, dentro
de los cuales se encuentran frecuentemente los siguientes:
Neurogénico (ej. lesión medular, tallo cerebral, etc.)
Farmacológico (ej. sedantes, antihipertensivos, intoxicaciones, etc.)
Endocrinológico (ej. crisis suprarrenal, coma mixedematoso, etc.)
Embolismos (ej. embolismo graso, amniótico, etc.)
Resistencias Presión de
vasculares aurícula
ESTADO DE CHOQUE Gasto cardiaco sistémicas derecha
Cardiogénico ↓ ↑ ↑
Hipovolémico ↓ ↑ ↓
Distributivo ↑ ↓ ↓
Obstructivo ↓ ↑ ↑
Tabla 2. Comportamiento hemodinámico de los tipos de estados de choque
Nota: Existen más estados de choque, mucho menos frecuentes, que comparten en su mayoría
los mismos determinantes anteriormente expuestos, y el tratamiento que se les debe otorgar
es similar.
Un algoritmo útil para realizar la clasificación del estado de choque, es la mnemotecnia SHOCK,
que abarca los tipos de choque mas frecuentes, para llegar al diagnóstico subyacente de forma
rápida.
Séptico
Hipovolémico
Obstructivo
Cardiogénico
K (combinación de los anteriores)
El identificar y clasificar el estado de choque, nos guía al tratamiento de soporte indicado (ej.
hipovolémico: reposición de volumen, cardiogénico: inotrópico, séptico: vasopresor, etc), si es
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 11
tratado de manera oportuna, puede lograrse una reversibilidad de dicho estado y un regreso
al estado basal, de no ser así, la hipoperfusion sostenida causará falla multiorgánica (renal,
cardiovascular, respiratoria, hepática, cerebral, suprarrenal, etc.) que condicionará la muerte
del paciente.
Bibliografía recomendada:
1. Cecconi M, De Backer D, Antonelli M, Beale R, Bakker J, Hofer C, et al. Consensus on circulatory shock
and hemodynamic monitoring. Task force of the European Society of Intensive Care MedicineIntensive
Care Med (2014) 40:1795–1815
DOI: 10.1007/s00134-014-3525-z
2. Vincent JL, De Backer D. Circulatory shock. N Engl J Med 2013; 369:1726-1734October 31, 2013
DOI: 10.1056/NEJMra1208943
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 12
Capitulo 3. EVALUACION HEMODINAMICA EN ESCENARIOS
DE RECURSOS LIMITADOS
“El recurso más valioso en la atención del paciente lo posee el médico en su mente”
Sergio Edgar Zamora Gómez
Introducción
El monitoreo hemodinámico avanzado suele ser de un coste alto, y en la mayoría de los lugares
de nuestro continente no es posible contar con él, sin embargo, esto no justifica en absoluto
un mal manejo. La limitación en recursos de conocimientos fisiológicos es la peor carencia que
un médico puede tener. En el presente capítulo utilizaremos toda la información que se ha
revisado en los capítulos previos para poder con base a un análisis fisiológico y fisiopatológico
realizar una evaluación hemodinámica y por ende un tratamiento dirigido individualizado.
Algoritmo de manejo
El algoritmo de manejo que presentamos en este capítulo está formulado para la mayoría de
los escenarios de la práctica médica cotidiana de atención de paciente crítico, donde se cuenta
usualmente con un acceso venoso central y una línea arterial, o la toma de gasometrías
arteriales por punción. Se basa en la estructuración ordenada de las siguientes interrogantes
a resolver:
1. ¿Mi paciente está chocado?......Establecer o descartar estado de hipoperfusión
El primer paso en el abordaje de un paciente bajo sospecha de inestabilidad
hemodinámica es determinar si cuenta con datos de hipoperfusión tisular. La valoración
de las ventanas clínicas (neurológica, renal y cutánea) más la correlación de la FC/TAS
(índice de choque) en conjunto con las variables bioquímicas (diferencia de CO2 va,
lactato y radio CO2 va/ Dav O2) nos permiten establecer si existe o no hipoperfusión
sistémica.
2. ¿La presión arterial es la adecuada?....... Valorar inicio de vasopresor temprano
Una vez establecido el diagnóstico de hipoperfusión tisular es muy importante
establecer si la presión arterial es adecuada o no para el paciente. No existe una
presión arterial estándar para todos los pacientes, en pacientes que no son hipertensos
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 13
crónicos se puede considerar una presión arterial media entre 60-70 mmHg como un
valor adecuado, sin embargo en pacientes con hipertensión arterial crónica es muy
importante interrogar sobre los valores que el paciente maneja de ordinario, ya que la
curva de autorregulación vascular se encuentra desplazada a la derecha y por lo tanto
valores “normales o estándar” de presión arterial media pueden representar
hipotensión y condicionar hipoperfusión en éstos pacientes, de acuerdo a literatura
internacional se recomienda que pacientes hipertensos crónicos un valor de TAM
objetivo puede ser 80-85 mmHg. Una vez detectada una presión arterial media
inadecuada para el paciente y considerarse causa de hipoperfusión, no debe retrasarse
el inicio de vasopresor a valorar la respuesta a la administración de volumen, sobre
todo cuando es muy marcada la hipotensión; debe iniciarse vasopresor de forma
temprana para lograr una presión arterial media perfusora, y reducir el tiempo de
hipoperfusión, para poder continuar con la evaluación hemodinámica. Mientras mayor
tiempo de hipoperfusión sostenida, mayor posibilidad de evolucionar a la
irreversibilidad.
3. ¿Cómo está el gasto cardiaco?.....Alto o bajo, sin medir Gasto Cardiaco.
Existen variables obtenidas a través del análisis de muestras de sangre venosa central
y arterial que nos ayudan a inferir el comportamiento del gasto cardiaco, con una
relevancia mayor que un valor absoluto del gasto cardiaco. Tales herramientas son el
valor de la saturación venosa central (SVcO2), la diferencia arteriovenosa de oxígeno
(DavO2) y la diferencia de saturación arterial de oxígeno menos saturación venosa
central de oxígeno (SaO2-SVcO2). La obtención de estas tres variables en conjunto no
lleva más de 2 minutos, una vez teniendo los resultados de las gasometrías procesadas.
Un gasto cardiaco alto se infiere por una SVcO2 >70%, una DavO2 <3 ml y una SaO2-
SVcO2 <20 %; un gasto cardiaco bajo se infiere por una SVcO2 < 60 %, una DavO2
>5 ml y una SaO2-SVcO2 >30%.
4. ¿Existe alguna causa mecánica de choque?.....Condiciones que ameriten resolución
inmediata antes de continuar el análisis.
Antes de continuar con el análisis del comportamiento hemodinámico es imprescindible
sobre todo cuando existen factores de riesgo para su desarrollo, descartar la presencia
de condiciones “mecánicas” que pueden por una parte por sí solas condicionar estado
de choque y por otra parte confundir o sesgar el análisis del comportamiento
hemodinámico. Estas condiciones en orden de frecuencia son: neumotórax, hemorragia
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 14
oculta intracavitaria (hemotórax masivo, hemorragia intrabdominal), tamponade
cardiaco y tromboembolia pulmonar. En caso de identificar cualquiera de ellas, deben
de resolverse de manera inmediata, en caso de baja sospecha o de descartarse debe
continuarse con el análisis.
5. ¿Una carguita?.....Buscar intencionadamente datos de tolerancia a volumen y de
potencial beneficio.
Una interrogante esencial a resolver es el esclarecer si el paciente mejorará su
inestabilidad hemodinámica a la administración de volumen, es decir si el gasto cardiaco
mejorará tras optimizar la precarga. Lo anterior implica valorar riesgos y beneficios de
administrar un volumen que puede llegar a ser beneficioso, pero que en caso de no
serlo tiene mucha posibilidad de ser dañino, sobre todo cuando el paciente tiene
alteración en la función renal y no es capaz de eliminar el volumen administrado. Existen
herramientas para valorar si el paciente se encuentra en una situación de tolerancia al
volumen, ya que lo primero es no generar más daño con una intervención diagnóstica
terapéutica. Cuando un paciente no tiene datos clínicos de sobrecarga hídrica como
ingurgitación yugular, datos de congestión pulmonar, y que se acompaña de una PVC
<5 mmHg, así como una pobre tolerancia hemodinámica a presiones del ventilador
cuando se encuentra bajo ventilación mecánica y se incrementa el PEEP a 15 cmH2O
(maniobra de potencial de reclutamiento pulmonar) manifestando hipotensión e
incremento en la variabilidad de la onda de pletismografía.
Así mismo cuando se realiza un reto de líquido con 100-150 ml máximo de solución
cristaloide o elevación pasiva de las piernas al menos 2 minutos, el registrar un
incremento en el valor de la SVcO2 de 5-10% es sugestivo de tolerancia y de beneficio
potencial al administrar volumen. Cuando el paciente cuenta con todo lo anterior
contrario, es decir datos de sobrecarga, PVC >8 mmHg, que el incrementar el PEEP a
15 no genera ninguna alteración hemodinámica o en la onda de pletismografía, y que
al realizar elevación pasiva de las piernas o realizar un reto de líquido no se genera un
incremento mayor a 4% en el valor de SVcO2.
6. Y ¿ahora qué hago?
a) En caso de cumplir con datos de tolerancia a volumen y un potencial beneficio en
su administración:
• Administrar una cantidad de cristaloide de preferencia soluciones
balanceadas, como la Solución Hartmann, que tienen menor contenido de
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 15
cloro con respecto a la Solución Salina al 0.9% en una cantidad de 250 ml
preferentemente, y como máximo 500 ml en un lapso de 15-20 minutos, y
valorar la optimización del sistema cardiovascular mediante: reducción en la
dosis de vasopresor necesaria para mantener TAM perfusora, acompañado
de una mejoría en el comportamiento de las variables que reflejan
comportamiento del gasto cardiaco y finalmente en mejoría de las variables
que reflejan hipoperfusión tisular. Valorar nuevamente si el paciente tiene
aún tolerancia y potencial beneficio en continuar la administración de
volumen, deteniéndose cuando se tengan datos de no encontrar mayor
beneficio en la administración de volumen.
b) En caso de cumplir con datos de intolerancia a volumen y un potencial perjuicio en
su administración:
• NO ADMINISTRAR VOLUMEN, el inicio de inotrópico (levosimendán,
dobutamina, epinefrina) es una opción viable y fisiológicamente respaldada
por el análisis desarrollado previamente, donde el volumen sistólico no
mejorará a la administración de volumen. Tras la administración del
inotrópico se debe valorar la optimización del sistema cardiovascular
mediante: reducción en la dosis de vasopresor necesaria para mantener
TAM perfusora, acompañado de una mejoría en el comportamiento de las
variables que reflejan comportamiento del gasto cardiaco y finalmente en
mejoría de las variables que reflejan hipoperfusión tisular. Valorar
nuevamente si el paciente tiene aún intolerancia y potencial perjuicio en la
administración de volumen, o si tras la mejoría hemodinámica y una mejoría
en los flujos urinarios, el paciente llega en algún momento a tener datos de
tolerancia y potencial beneficio en continuar la administración de volumen,
y realizando la intervención descrita en el inciso a.
El algoritmo presentado trata de facilitar el abordaje y manejo hemodinámica siguiendo los
principios de seguridad y manejo individualizado basado en un análisis meramente fisiológico
y fisiopatológico, abarcando la mayoría de las posibilidades diagnósticas en la mayoría de los
escenarios hospitalarios, considerando la utilización mínima de recursos, la realidad en nuestro
continente.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 16
Algoritmo 3. Algoritmo de abordaje y manejo del paciente inestable
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 17
Bibliografía recomendada:
1. E. Matijasevic, M. Jaramillo. Monitoreo hemodinámico. Cuidado crítico cardiovascular .
2. D. Nichols,D. Nielsen, Oxygen Delivery and Consumption: A Macrocirculatory Perspective. Crit Care Clin
26 (2010) 239–253.
3. Marino P. El libro de la UCI. 3° Edición. Editorial Lippincott Williams & Wilkins. Philadelphia 2008.
4. Hemodynamic Evaluation and Monitoring in the ICU, Michael R. Pinsky, MD, FCCP
5. Clinical review: Circulatory shock - an update: a tribute to Professor Max Harry Weil Jean-Louis
Vincent1,*, Can Ince2 and Jan Bakker2
6. N Engl J Med 2001;345:1368-77
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 18
Capitulo 4. EQUILIBRIO ÁCIDO-BASE.
“El médico es equilibrista en el organismo del paciente, pero si falla, no hay red.”
Orlando Rubén Pérez Nieto
Introducción.
El equilibrio ácido-base es un determinante fundamental en la hemodinamia, necesario para
una adecuada entrega de oxígeno a los tejidos y el mantenimiento del tono arterial de los
pacientes, tiene importancia para el funcionamiento hemostático, el estado neurológico, entre
otras muchas cosas de suma consideración en pacientes críticos, en este capítulo se indicará
paso por paso como se debe interpretar la gasometría para este propósito.
Conceptos básicos y determinantes del potencial de hidrogeniones.
El potencial de hidrogeniones (pH) nos habla de la concentración plasmática de H+ .
Dicho valor nos indica la gravedad del trastorno ácido-base (pH = –log[H± 1. ]).
Su rango normal: 7,35-7,45, lo que es equivalente a una [H+ ] de aproximadamente 40 ± 5
nM.
[H+ ] = 23,9 x (pCO2 / HCO3 -)
La presión de dióxido de carbono (pCO2) nos indica la respuesta respiratoria.
Su rango normal es: 35-45 mmHg. Su valor crítico: > 70 mmHg.
La concentración plasmática de bicarbonato (HCO3–) o CO2 total indica el estado de los
sistemas amortiguadores.
Su rango normal es: 22-26 mEq/l (mEq/l = mMol/l) Sus valores críticos: < 8 y > 40 mEq/l.
Parametro Valor de referencia Valor crítico
pH 7.35-7.45 <6.8 ó >7.6
PaCO2 35-45 mmHg >70 mmHg
HCO3 22-26 mmHg <8 ó >40 mEq/dL
Tabla 4. Valores normales en gasometría arterial
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 19
§ Cambio en la PCO2 = Trastorno acido basico respiratorio:
§ A) Aumento de PCO2: Acidosis respiratoria
§ B) Disminucion de PCO2: Alcalosis respiratoria
§ Cambio en el HCO3: Trastorno acido basico metabolico
§ A) Disminucion del HCO3: Acidosis metabolica
§ B) Aumento del HCO3: Alcalosis metabolica
Trastorno primario Cambio primario Respuesta secundaria
Acidosis respiratoria PCO2 Aumentado HCO3 Aumenta
Alcalosis respiratoria PCO2 Disminuido HCO3 Disminuye
Acidosis metabolica HCO3 Disminuido PCO2 Disminuye
Alcalosis metabolica HCO3 Aumentado PCO2 Aumenta
Tabla 4.1 Trastornos acido base y su respuesta secundaria esperada
PASOS PARA EL ANÁLISIS ACIDO BÁSICO.
Primera etapa: Identificar el trastorno acido basico primario
Regla 1: Si la PaCO2 y el pH, o ambos, no estan dentro del intervalo normal, existe un trastorno
acidobásico.
Regla 2: Si la PaCO2 y el pH están alterados, comparar el cambio direccional:
§ 2a) si el cambio de la PaCO2 y del pH van en la misma direccion, existe un trastorno
acidobasico metabolico primario
§ 2b) si el cambio en la PaCO2 y el pH van en direcciones opuestas, existe un trastorno
acidobasico respiratorio primario
Regla 3: Si solo esta alterado el pH o la PaCO2, el cuadro es un trastorno metabólico y
respiratorio mixto (trastornos iguales pero opuestos):
§ 3a) Si la PaCO2 esta alterada, el cambio direccional de la PaCO2 identifica el tipo de
trastorno respiratorio y el trastorno metabolico opuesto.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 20
§ 3b) Si el pH esta alterado, el cambio direccional en el pH identifica el tipo de trastorno
metabolico y el trastorno respiratorio opuesto
TRASTORNO ACIDO BÁSICO PRIMARIO
Alcalosis metabólica : pH ↑ y PCO2 ↑ Acidosis metabolica : pH ↓ y PCO2 ↓
Alcalosis respiratoria: pH ↑ y PCO2 ↓ Acidosis respiratoria: pH ↓ y PCO2 ↑
Tabla 4.3 Trastorno acido base primario
Segunda etapa: Evaluar las respuestas secundarias.
Regla 4: En caso de que exista un trastorno metabólico primario, si la PaCO2 medida es mayor
de lo esperado, hay una acidosis respiratoria secundaria, y si la PaCO2 medida es menor de la
esperada, existe una alcalosis respiratoria secundaria.
§ En la acidosis metabólica: Por cada mmol/l de descenso del HCO3– debe bajar 1 mmHg
la pCO2
§ PCO2 esperado: (HCO3 x 1.5 )+ 8
§ En la alcalosis metabólica: Por cada mmol/l de aumento de HCO3– debe subir 0,7
mmHg la pCO2
§ PCO2 esperado: (HCO3 x 0.7) + 20
Cifras de HCO3– inferiores a 5 mmol/l indican que la capacidad de tamponamiento se está
agotando.
Valores extremadamente bajos (<15 mmHg) de pCO2 indican que la respuesta respiratoria
está llegando al límite.
§ Compensación del Potasio
Por cada 0,1 unidades que aumenta el pH plasmático, la [K+ ]p disminuye en 0,6 mmol/l, y
viceversa.
Regla 5: En un trastorno respiratorio primario, una concentración de HCO3 normal o casi normal
indica que el trastorno es agudo.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 21
Regla6: En un trastorno respiratorio primario en el que la concentracion de HCO3 esta alterada,
hay que determiner la HCO3 esperada para un trastorno respiratorio cronico.
§ 6a) Para una acidosis respiratoria cronica, si el HCO3 es menor del esperado, existe
una respuesta renal imcompleta, y si el HCO3 es mayor del esperado, existe una
alcalosis metabolica secundaria.
§ 6b) Para una alcalosis respiratoria cronica, si el HCO3 es mayor del esperado, existe
una respuesta renal incompleta, y si el /hco3 es menor del esperado, hay una acidosis
metabolica secundaria.
Acidosis Respiratoria:
§ Tamponamiento intracelular (hemoglobina y proteínas). Constituye la única protección
frente a la hipercapnia aguda, ya que el bicarbonato no puede tamponar el ácido
carbónico. Realizada de 10 a 15 minutos tras el aumento de la pCO2.
§ En la hipercapnia aguda el bicarbonato plasmático aumenta en 1 mEq/l por cada 10
mmHg de aumento en la pCO2.
§ Respuesta renal. Tarda 3-4 días. Incremento en la excreción urinaria de amonio, acidez
titulable y pérdida de cloro, con el consiguiente aumento en la reabsorción de
bicarbonato, que aumenta en 3-4 mEq/l por cada 10 mmHg de aumento de la pCO2
Alcalosis Respiratoria:
§ Tamponamiento intracelular. La hemoglobina, los fosfatos y las proteínas liberan
hidrogeniones [H+ ] que se unen al HCO3– para forma H2CO3 . Consigue disminuir 2
mEq/l de HCO3– por cada 10 mmHg que desciende la pCO2 .
§ Respuesta renal. Tarda 3-4 días en producirse, disminución en la reabsorción proximal
de bicarbonato y la excreción urinaria de amonio y acidez titulable. Como consecuencia,
el bicarbonato disminuye 4 mEq/l por cada 10 mmHg que desciende la pCO2 .
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 22
Tercera etapa: En caso de acidosis metabólica, evaluar el hiato aniónico.
El hiato aniónico (brecha aniónica o anión gap), diferencía entre las principales cargas positivas
(cationes) y negativas (aniones) del plasma.
Nos orienta hacia el diagnostico diferencial de la acidosis metabólica.
Na + Cationes no medidos = (Cl + HCO3) + Aniones no medidos
Na - (Cl + HCO3) = Aniones no medidos – Cationes no medidos
Hiato aniónico = Na - (Cl + HCO3)
(Valores de referencia = 3 - 11 mEq/L)
Influencia de la Albumina: Debe corregirse en caso de hipoalbuminemia.
Hiato aniónico corregido = AG + 2,5 x (4,5-albumina g/dL).
Aniones no medidos Cationes no medidos
Albumina (15 mEq/L) Calcio (5 mEq/L)
Acidos organicos (5 mEq/L) Potasio (4,5 mEq/L)
Fosfato (2 mEq/L) Magnesio (1,5 mEq/L)
Sulfato (1 mEq/L)
TOTAL ANM:23 mEq/L TOTAL CNM: 11 mEq/L
Hiato Anionico (AG)=ANM-CNM=12 mEq/L
Tabla 4.4. Aniones y cationes plasmáticos
Hiato aniónico alto Hiato aniónico normal
Acidosis láctica Diarrea
Cetoacidosis Infusión de suero salino isotónico
(hipercloremia)
Insuficiencia renal terminal Insuficiencia renal en estadio precoz
Ingestión de metanol Acidosis tubular renal
Ingestión de etilenglicol Acetazolamida
Toxicidad por salicilatos Ureteroenterostomia
Tabla 4.5. Causas de acidosis metabólica con Anión GAP alto y normal
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 23
Bases de tratamiento de la acidosis metabólica de hiato aniónico amplio:
Cetoacidosis diabética
§ Insulina para frenar la producción de H+
§ Reexpansión del volumen extracelular.
§ Corrección del posible déficit de potasio.
Acidosis láctica
§ Tipo A o acidosis anaerobia: Debida a hipoxia y exceso de formación de ácido láctico.
Más común. Puede producirse por falta de aporte de oxígeno (enfermedad pulmonar o
cardíaca), falta de transporte de oxígeno a los tejidos (anemia) o exceso de
demanda/bloqueo de la respiración tisular (isquemia).
El tratamiento consiste en aumentar el aporte tisular de oxígeno.
§ Tipo B o acidosis aerobia: Debida a la disminución del metabolismo hepático del ácido
láctico en ausencia de hipoxia. Puede deberse a insuficiencia hepatocelular grave o a
interferencia con el metabolismo hepático.
Intoxicación por alcoholes: Metanol, etilenglicol, propilenglicol.
Tratamiento: Lavado gástrico, administración de Etanol o Fomepizol y hemodiálisis.
Calcular la osmolalidad es útil en la sospecha de intoxicación por alcoholes.
Osmolalidad calculada = 2 × [Na+ ]p + [glucosa] (mg/dl)/18 + [BUN] (mg/dl)/2,8
Un hiato osmolal >20 mOsm/l implica la existencia de un osmol no medido y no detectado por
los auto analizadores habituales, habitualmente alcoholes.
• Reposición de Bicarbonato
Cálculo de la reposición de bicarbonato Déficit de bicarbonato =
ΔHCO3 - x 0,5 a 0.8 x peso corporal
ΔHCO3 – = bicarbonato diana – [HCO3 -]p
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 24
Cociente Hiato/Hiato
Si existe acidosis metabólica de hiato aniónico elevado, es posible detectar otro trastorno acido
base metabólico concomitante oculto, como acidosis metabólica de hiato aniónico normal ó
alcalosis metabólica
Fórmula:
Exceso de hiato aniónico / Déficit de bicarbonato = Hiato aniónico / 24 – HCO3
(Valor normal: 1)
< 1 Significa Acidosis metabólica de hiato aniónico normal agregada (ej. cetoacidosis diabética
más acidosis hiperclorémica agregada).
> 1 Significa Alcalosis metabólica agregada (ej. cetoacidosis diabética más uso de diuréticos o
aspiración gástrica)
• Acidosis metabólica: Hiato aniónico normal
Si Cl- en orina > (Na+ en orina + K+ en orina): existe un catión acompañante, el NH4+, lo
que indica que el mecanismo de acidificación está intacto y que la causa de la acidosis es
extrarrenal (habitualmente gastrointestinal).
Si Cl- en orina < (Na+ en orina + K+ en orina): no hay excreción de NH4+, por lo que el
origen es renal. Una excepción es la presencia de otro anión no medido, por ejemplo el β-
hidroxibutirato,
• Alcalosis metabólica
Es generada por exceso en los aportes de bicarbonato, ó por pérdida de hidrogeniones.
Para que se mantenga en el tiempo debe existir una circunstancia que impida al riñón
deshacerse del exceso de bicarbonato plasmático:
§ Depleción del Cl– y/o K+.
§ Contracción de volumen circulante eficaz
§ Reabsorción de HCO3
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 25
§ Exceso de actividad mineralocorticoide (hiperaldosteronismo)
§ Insuficiencia Renal
Situaciones Predisponentes:
1) Perdida de volumen.
2) Perdida de ácidos gástricos.
3) Diuréticos.
Tratamiento: Aportar cloro en forma de suero salino hasta expandir el espacio extracelular.
Los casos resistentes al cloro son menos frecuentes, para ellos se requieren terapias más
específicas (espironolactona, indometacina, amilorida o triamtereno, potasio, etc.).
Exceso de bicarbonato = 0,6 x peso corporal x ΔHCO3 –
ΔHCO3 - x 0,5* x peso corporal
ΔHCO3 - = HCO3 - plasmático – 24
§ Infusión de solución salina:
1) Deficit de Cl- ( meq ) = 0,2 x peso ( kg ) x ( 100 - Cl plasmático )
2) Volumen de solución salina isotónica (L) = Déficit de C l/ 154
3) Ritmo de reposición: 100-125 ml/h
Infundir cloruro de potasio más concentrado en estados edematosos o pacientes que requieran
restricción hídrica.
Alcalosis resistente a cloururo.
§ Acetazolamida: Inhibe a la anhidrasa carbónica, dosis 5 - 10 mg/kg IV o VO.
§ Infusion de Acido Clorhidrico:
1) Calcular el deficit de hidrogeniones:
Deficit de H+ = 0,5 x peso ( kg ) x ( HCO3 plasma – 30 )
2) Determinar el volumen de reposicion de solucion salina:
Litros de HCl 0.1 N = Deficit de H+ / 100
3) Ritmo de reposicion < ó = 0.2 mEq/kg/h
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 26
Categoria Criterios Situaciones
Sensible al Cloruro [Cl-] orina<15 mEq/L Vomitos
Aspiración gástrica
Diuréticos clorureticos
Hipovolemia
Abuso de laxantes
Resistente al Cloruro [Cl-] orina >25 mEq/L Aldosteronismo primario
Ingestión de regaliz
Hipopotasemia grave
Tabla4.5. Alcalosis metabólica sensible y resistente a cloruro
Imagen 4. Nomograma de interpretación acido base simplificada
Bibliografía recomendada:
1. Tools to use to diagnose acid-base disorders. In: Halperin ML, Kamel S, Godstein MB. Fluid, Electrolyte
and Acid-Base Physiology. A problem based-approach. 4th Ed. Philadelphia, Saunders Elsevier 2010;
p. 39-59
2. Adrogue HJ, Gennari FJ, Galla JH, Madias NE. Assessing acid-base disorders. Kidney Int 2009; 76:
1239-47.
3. Trastornos del metabolismo acidobase. Alcázar R, Albalate M, De Sequera, P. Nefrología al día 2012.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 27
Capitulo 5. MONITOREO HEMODINAMICO ECOGUIADO Y
OTRAS UTIIDADES EN AREAS CRÍTICAS
“El corazón en inestabilidad hemodinámica: Unas veces es causante y otras es testigo”
Eder Iván Zamarrón López
Introducción
La ecografía a la cabecera del paciente (ECP) se utiliza con fines de situar hemodinámicamente
al enfermo así como determinar la causa que ha llevado a la inestabilidad hemodinámica o
incluso al paro cardiaco y de esta forma realizar intervenciones terapéuticas dirigidas.
Cuando está disponible, la ECP se utiliza en pacientes en los que el diagnóstico etiológico no
se ha logrado con la evaluación clínica y de laboratorio o en aquellos en los que las imágenes
radiológicas no son convincentes y como una herramienta complementaria para examinar la
respuesta a volumen. Cuando es realizada por personal capacitado como una herramienta de
diagnóstico en pacientes inestabilidad hemodinámica, aporta una valiosa información que
puede utilizarse para toma de decisión que les puede salvar la vida.
Algoritmo 5. Abordaje inicial del paciente con estado de choque.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 28
Le ECP en situaciones de urgencias constituye un procedimiento seguro, no invasivo y de
diagnóstico de gran utilidad. Su uso se ha extendido y es imprescindible en muchos ámbitos de
la práctica médica y en especialidades que lo utilizan como medio diagnóstico y de apoyo en
decisiones terapéuticas.
SONDA VELOCIDAD USOS
Lineal 5-10 MHz Evaluación y visualización de estructuras superficiales:
(Alta frecuencia) vasos sanguíneos, músculo esqueléticas, pleura, etc.
Convexo 2-5 MHz Estructuras de cavidad abdominal:
(Baja frecuencia) Obstetricia, FAST.
Sectorial 2-5 MHz Ecocardiografía transtorácica, Doppler transcraneal.
(Baja frecuencia y tamaño pequeño)
Tabla 5. Selección de la sonda para insonación
Es importante tener en cuenta que a mayor velocidad de onda sonora, la profundidad de
penetración a los tejidos será menor, pero con mayor definición…y visceversa.
ECOGRAFÍA CARDIACA
Una vez que contamos con un equipo de ultrasonido y el transductor adecuado, debemos
localizar los sitios que me permitirán evaluar el corazón.
Ventanas cardiacas
En cada paciente, la localización del corazón con respecto al tórax, así como la rotación sobre
su propio eje y su posición con respecto al plano horizontal/vertical son distintas. Por lo tanto
los sitios donde se obtendrán las ventanas ecocardiográficas son muy variables. Habitualmente
se obtienen imágenes del corazón desde 4 proyecciones:
1. Proyección paraesternal: sobre la línea paraesternal izquierda 4to espacio intercostal,
nos permite la obtención del eje largo del corazón cuando dirigimos la marca del
transductor hacia el hombro derecho y el eje corto, cuando dirigimos la marca hacia el
hombro izquierdo, explorando desde los grandes vasos en la porción basal del corazón,
posteriormente la válvula aórtica, válvula mitral y el ventrículo izquierdo (en sus tres
niveles: basal, medio y apical)
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 29
Imagen 5. Ventana paraestrenal eje largo
Imagen 5.1. Ventana paraestrenal eje corto
2. Proyección apical: alrededor del 5to espacio intercostal, línea axilar anterior, permite
obtener imágenes desde la punta del corazón, rotando el transductor sobre su propio
eje pueden obtenerse las vistas de cinco cámaras (5C), cuatro cámaras (4C), tres
cámaras (3C) y dos cámaras (2C)
Imagen 5.2. Ventana apical 4 cámaras
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 30
Imagen 5.3. Ventana apical 2, 3 y 5 cámaras respectivamente
3. Proyección subcostal: podemos obtener una imagen de 4 cámaras al dirigir la marca
hacía el espacio axilar izquierdo, rotando nuestro transductor hasta dirigir la marca
hacia el esternón obtenemos un eje corto, si inclinamos nuestro transductor hacia la
izquierda en esa posición podemos observar la desembocadura de la vena cava inferior
y parte de su trayecto.
Imagen 5.4. Ventana subcostal cuatro cámaras y vena cava inferior respectivamente.
4. Proyección supraesternal: si dirigimos la marca del transductor hacia la izquierda del
paciente podemos observar el cayado aórtico, los vasos supra aórticos y la arteria
pulmonar derecha pasando debajo del cayado aórtico, esta proyección es poco utilizada
por médicos no cardiólogos.
ECOGRAFÍA PULMONAR
Cuando realizamos una ecografía pulmonar se generan una serie de artefactos horizontales y
verticales de diferente ecogenicidad e intensidad en la escala de grises producto de la
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 31
interacción del ultrasonido con la pleura, el parénquima pulmonar y la interfase aire-líquido.
Son precisamente estos artefactos generados los que han llevado a la ecografía pulmonar a la
práctica clínica
Ventanas pulmonares
La exploración ecográfica inicia en la zona anterosuperior y acaba en la zona lateroinferior de
cada hemitórax.
Liechtenstein en su protocolo BLUE (Bedside Lung Ultrasound in Emergency) recomienda que
en situaciones críticas (de inestabilidad) nos enfoquemos en realizar un barrido ecográfico
inicial (que suele durar unos 5 minutos aproximadamente) enfocándonos en buscar la causa
principal que genera la insuficiencia respiratoria aguda y posteriormente al estabilizar la
situación se procede a una evaluación más detallada.
Un pulmón normal se caracteriza por la presencia de los siguientes signos ecográficos:
- Signo del deslizamiento pleural o “sliding”: Es la imagen en modo real del movimiento
de la pleural visceral (que acompaña al pulmón) sobre la pleura parietal. Este
deslizamiento es máximo en las bases y mínimo o nulo en los vértices pulmonares.
- Presencia de líneas A: Lineas hiperecogénicas horizontales, que aparecen de forma
repetida y paralelas a la pleura. Son artefactos de reverberación que se repiten
equidistantes a la línea pleural.
- Signo de la orilla de playa (en modo M): 2 zonas bien diferenciadas divididas por la
línea pleural. Una parte superior formada por líneas horizontales paralelas que
representan la pared torácica y una parte inferior de aspecto granulado como arena de
playa que representa el pulmón aereado.
- Pueden haber de forma aislada líneas B o colas de cometa (<3): Líneas
hiperecogénicas verticales (a modo de “laser”) que parten desde la pleura y atraviesan
y borran las líneas A.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 32
Imagen 5.5. Hallazgos normales en ecografía pulmonar y
zonas de exploración de la ecografía pulmonar. Puede
observarse una división de 4 zonas, 2 anteriores, la
superior e inferior y 2 zonas laterales igualmente la
superior e inferior. LAA, línea axilar anterior; AS, antero
superior; AI, antero inferior; LA, lateral superior; LI, lateral
inferior.
Para obtener datos ecográficos relevantes para tomar decisiones clínicas se deberá insonar
corazón y pulmón principalmente además de otras estructuras (grandes vasos, abdomen, etc.)
para situar el estado de choque y muchas de las veces su etiología, lo anterior sin olvidar que
lo mas importante es el contexto clínico del enfermo.
Los principales protocolos que se utilizan para obtener datos ecográficos fundamentales para
la toma de decisión ante un paciente crítico son los siguientes:
Protocolo FALLS (Fluid Administration Limited by Lung Sonography)
En este protocolo se establece de acuerdo al patrón ecográfico pulmonar su correlación con
los distintos estados de choque.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 33
Algoritmo 5.1. Protocolo FALLS
Para guiar la reanimación hídrica nos serán muy útiles las valoraciones repetidas de la cava
inferior (en cuanto disminuya la colapsabilidad/distensibilidad, es probable que el paciente no
requiera más líquidos) y el seguimiento de la ecografía pulmonar (en cuanto empiecen a
aparecer líneas B, se hace improbable que el paciente siga respondiendo a volumen).
Protocolo RADIUS (Rapid Assessment of Dyspnea with Ultrasound)
Este protocolo se utiliza para evaluar la disnea e incluye a la tromboembolia pulmonar. Tiene 4
componentes:
1. Examen cardiaco FOCUS (Focused cardiac ultrasound - ecografía cardiaca dirigida)
2. Examen de vena cava inferior
3. Evaluación de cavidad torácica a nivel pulmonar para identificar derrames pleurales
4. Evaluación de la línea pleural
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 34
En el examen pulmonar se debe buscara la presencia de neumotórax y de liquido intersticial.
En cuanto al examen cardiaco como ya hemos visto anteriormente debe hacerse enfocado a la
resolución de problemas, en el caso de este protocolo específicamente: Tamponade cardiaco,
presencia de derrame pericárdico se observara en la ventana subcostal o paraestrenal, esta
vista nos ayudará a diferenciar entre derrame pericárdico y pleural:
El derrame pericárdico se observa anecoico detrás de la aurícula izquierda y ventrículo
izquierdo, mientras que el derrame pleural se observa anecoico detrás de la aorta descendente.
Para cuantificar el derrame pericárdico se debe medir la distancia entre el corazón y el
pericardio parietal. Si la medición obtenida es <0.5 cm es leve, entre 0.5 a 2 cm es moderado
y > 2 cm es grave. Siguiendo valoración cardiaca se estudiara la función del ventrículo izquierdo
CUALITATIVAMENTE MAS QUE CUANTITATIVAMENTE. Lo normal es que se aproximen 50% y
que se engruese un 50% las paredes del VI.
Examen de Vena cava inferior (VCI): Realizando la medición del diámetro y colapsabilidad
(paciente en ventilación espontanea), se obtiene una estimación de la presión de la aurícula
derecha, lo que podría tener valor para el diagnostico hemodinámico y la necesidad de
administración de volumen intravascular aunado a otras mediciones y factores del paciente.
Entre mayor colapsabilidad, mayor posibilidad de responder a volumen.
Diámetro de la VCI Porcentaje de Presión estimada de Correlación clínica
colapso Aurícula derecha
inspiratorio
<15 mm 100% 0-5 mmHg Hipovolemia o choque distributivo
15-25 mm >50% 5-10 mmHg Choque
15-25 mm <50% 11-15 mmHg Choque cardiogénico o obstructivo
>25 mm <50% 16-20 mmHg Choque cardiogénico o obstructivo
Hipertensión pulmonar, insuficiencia
>25 mm 0% >20 mmHg cardiaca derecha, Síndrome de dificultad
respiratoria con PEEP alto.
Tabla 5.1. Interpretación de la evaluación de la vena cava inferior.
Es importante mencionar que la distensibilidad (paciente con ventilación controlada) de la VCI
tiene relevancia debido a que una distensibilidad de mas del 15% predice respuesta a volumen
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 35
del paciente crítico sin embargo la individualización del paciente y la obtención de otras pruebas
(VPP, VVS, ecografía de pulmón, prueba de levantamiento de piernas, etc.) aumentarán las
posibilidades de predecir respuesta a volumen.
Protocolo EGLS (Echo Guided Life Support)
Este protocolo fue ideado para realizar un diagnostico diferencial del estado de choque en
áreas críticas donde el tiempo resulta fundamental para iniciar el tratamiento adecuado en base
a una sistematización.
Se da respuesta a las siguientes interrogantes:
1. ¿Existe neumotórax?
2. ¿Tiene tamponade cardiaco?
3. ¿Esta hipovolémico el paciente?
4. ¿Esta deprimida la función del VI? (Si es así, es la causa del choque?)
5. ¿Existe alteración en el VD?
El protocolo EGLS responde sistemáticamente a estas preguntas previas con una secuencia:
A- Vía aérea, B- Ventilación y C- Circulación
El examen empieza en insonando pulmón donde se busca neumotórax, se evalúa el patrón de
las líneas pulmonares, posterior se obtiene una ventana subcostal de 4 cámaras cardiacas y
por ultimo la VCI. Esto para evaluar la presencia de Tamponade, estado hídrico del paciente y
la función cardiaca.
Diagnostico Datos ecográficos
Neumotórax a tensión Sin datos de “slinding”, no líneas B, imagen de código de barras en modo M
Tamponade cardiaco Derrame pericárdico con colapso de VD y AD, VCI dilatada, VI hiperdinámico.
Hipovolemia VI hiperdinamico, VCI colapsada, pulmones normales
Tromboembolia pulmonar masiva VD dilatado, VD en froma de “D”, movimiento septal paradójico, VCI dilatada.
Infarto del ventrículo izquierdo VI con función disminuida asociado con patrón B pulmonar y VCI dilatada,
siempre y cuando exista choque cardiogénico.
Trastornos electrolíticos, acido base e Se puede asociar con función cardiaca deprimida.
intoxicaciones
Tabla 5.2. Hallazgos ecográficos y diagnosticos
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 36
Tome en cuenta otras causas de ausencia de “slinding” o desplazamiento pleural; Neumonía,
SIRA, Enfisema pulmonar severo, obstrucción bronquial, intubación selectiva, apnea, derrame
pleural. El signo patognomónico de Neumotórax a tensión es la imagen de código de barras en
la modalidad M.
Algoritmo 5.2. Manejo del protocolo EGLS
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 37
Protocolo FATE (Focused Assesed Transthoracic Echo)
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 38
Protocolo RUSH (Rapid Ultrasound in Shock protocol)
Es uno de los protocolos mas completos donde se insona ordenadamente componentes del
gasto cardiaco y se busca dirigidamente la o las etiologías de la inestabilidad hemodinámica.
Paso 1.- La “Bomba” nos referimos a una terapia dirigida por metas empezando con la
exploración de las vistas clásicas paraesternal eje largo, eje corto, subxifoidea y apical. Se
buscan tres hallazgos específicos:
a. Derrame pericárdico y taponamiento cardiaco
b. Contractilidad de VI. Esto es muy importante para saber la fuerza de “la bomba” que
será crucial en la terapia de administración de fluidos. El corazón puede encontrarse
dilatado y esto lo podemos clasificar de acuerdo a su contractilidad en un corazón de
contractilidad normal, moderada o severamente disminuido. Una cuarta categoría
llamada hipercontráctil se observan cámaras pequeñas, aumento en la contractilidad.
Esto se puede observar en el choque distributivo o estados de hipovolemia.
c. Tamaño del ventrículo derecho. La evaluación del tamaño nos puede indicar la
presencia de un émbolo pulmonar en el contexto del paciente con estado de choque.
Cualquier condición que aumente de manera súbita la presión de la vasculatura
pulmonar resultará en una dilatación aguda del VD. Adicionalmente la depleción del
septum interventricular hacia el lado izquierdo son indicaciones de altas presiones del
lado derecho y de la Arteria Pulmonar; en estos casos se deberá de realizar un escaneo
de miembros pélvicos buscando trombosis venosa profunda.
Paso 2.- El “tanque” en este segundo paso del protocolo nos referimos al “tanque” como al
estado de volumen intravascular.
a. Llenado del tanque. (Vena Cava Inferior y venas yugulares internas). En este caso se
debe de observar el diámetro de estas venas y su respuesta a la dinámica de la
respiración. Ya hemos comentado previamente como medir la VCI y la presión de la
aurícula derecha con la que se corresponde. Las venas yugulares internas se pueden
observar elevando la cabeza del paciente a 30°; se debe de realizar el escaneo con un
transductor lineal y observar ambos lados. Una VYI pequeña sin colapsabilidad a los
movimientos respiratorios se correlaciona con una presión de la AD disminuida, por el
contrario una VYI dilatada más allá del ángulo de la mandíbula con pobre colapsabilidad
en la respiración se corresponde con una presión de AD aumentada.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 39
b. Fuga del tanque. Protocolo FAST y pulmonar. Una vez que se observó el estado de
volemia de nuestro paciente se deberá de buscar intencionadamente el compromiso
hemodinámico secundario a fuga de volumen. En pacientes politraumatizados se
deberá de reconocer rápidamente la presencia de hemotórax o hemoperitoneo. En
condiciones no traumáticas la presencia de un exceso de fluidos en las cavidades
abdominales y torácicas puede significar ascitis o derrame pleural que eventualmente
pueden llegar a ocasionar falla cardiaca, renal o hepática. Se inicia este escaneo
realizando el protocolo FAST ya descrito en capítulos anteriores para terminar
realizando el rastreo pulmonar también ya comentado ampliamente.
c. Compromiso del tanque. Neumotórax. En esta situación se deberá de colocar al paciente
en posición supina buscando la presencia de la pleura. La presencia del signo de
“sliding” o deslizamiento pleural con líneas B excluye el diagnóstico de neumotórax.
Paso 3.- Evaluación de “las tuberías”. Es la última parte del protocolo donde primero se
evaluará la parte arterial del sistema circulatorio y posteriormente el lado venoso. Algunas
causas de hipotensión son la ruptura de un aneurisma aórtico abdominal o una disección
aórtica; es por esto que se continúa con este tercer paso.
a. Disección aórtica y ruptura de aneurisma de aorta abdominal. El examen de la aorta
abdominal y todo su trayecto es esencial para localizar un posible aneurisma poniendo
especial interés en la parte infrarenal que es la localización más frecuente. El
diagnóstico se hace cuando el diámetro de la aorta >3cm. La ruptura de aneurismas
es más común cuando estos superan los 5cm. En un paciente inestable con el
diagnóstico de AAA (aneurisma de aorta abdominal) hecho por ultrasonido se deberá
de iniciar el tratamiento de manera inmediata. La segunda parte de esta sección
corresponde a la búsqueda de disección aórtica esta se mide observando la raíz aórtica
en un eje paraesternal largo, una raíz aórtica normal deberá de medir no más de 3.8cm.
Encontrar una raíz dilatada y un colgajo en la íntima nos puede hacer el diagnóstico. Se
puede utilizar Doppler color para observar dos lúmenes uno verdadero y uno falso
dentro del vaso, una disección aórtica tipo A suele acompañarse con derrame
pericárdico o insuficiencia aórtica.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 40
b. Obstrucción de la tubería. (Trombosis venosa profunda) Si se sospecha un
tromboembolia como causa del estado de choque se deberá de realizar un escaneo del
lado venoso de la “tubería”. Como la mayoría de los eventos trombóticos se originan
en los miembros inferiores el escaneo consiste en ejercer cierta presión en
determinados puntos de los mismos con un transductor lineal. Una vena normal se
colapsa con la compresión del transductor sin embargo cuando existe algún trombo
este se visualizará en el lumen de la vena. El signo patognomónico será la compresión
incompleta al aplicar la fuerza con el transductor.
Choque hipovolémico Choque Choque obstructivo Choque distributivo
cardiogénico
Bomba Corazón pequeño, Corazón Derrame pericárdico, Corazón hipercontráctil
hipercontráctil hipocontráctil, VD elongado, corazón (etapa temprana sepsis)
dilatado hipercontráctil Corazón hipocontráctil
(etapa tardía sepsis)
Tanque VCI aplanada VCI distendida VCI distendida VCI normal o pequeña
VYI aplanada VYI distendida VYI distendida VYI normal o pequeña
Líquido peritoneal y en Colas de cometa Ausencia de signo de Líquido pleural
pulmón-hemotórax Ascitis, derrame deslizamiento pleural (empiema)
(dependiendo de la etiología pleural Líquido peritoneal
del choque hipovolémico) (peritonitis)
Tuberías AAA Normal TVP Normal
Disección aórtica
Tabla 5.3. Hallazgos en protocolo RUSH
OTROS PROTOCOLOS DE ECOGRAFÍA EN AREAS CRÍTICAS:
- Protocolo CORE (Concentrated Overview of Resuscitative Efforts), Este protocolo tiene
por objetivo encausar la exploración ecográfica a identificar las causas y guiar la
reanimación oportuna del paciente en áreas críticas. Este protocolo incluye la valoración
de la vía aérea para colocación adecuada del tubo endotraqueal dentro de sus pasos,
- Protocolo FEER (Focused echocardiographic evaluation in resucitation management),
Durante la resucitación cardiopulmonar el ultrasonido ha venido a tomar parte
recientemente dentro de las guías de ACLS 2015 donde se establece su uso para
corroborar la correcta posición del tubo endotraqueal. El ultrasonido cardiaco o no
cardiaco puede ser considerado durante el manejo de la parada cardiaca (IIB). En este
contexto se utiliza dentro de la identificación de las causas siempre teniendo en cuenta
no interrumpir en el protocolo de reanimación del paciente en parada cardiaca. Es útil
en los ritmos no desfibrilables principalmente, se debe tomar el ultrasonido en pausas
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 41
menores a diez segundos o incluso durante las compresiones, la vista más útil es la
subcostal para no interferir.
Aunque los algoritmos varían en el orden de insonación, la mayoría coinciden en que lo
realmente impórtate son los datos ecográficos obtenidos para realizar una interpretación para
situar hemodinámicamente al paciente, así como buscar la etiología de la inestabilidad. Los
componentes del examen ecográfico en resumen se describen brevemente a continuación:
1. Insonación dirigida del corazón deben llevarse a cabo en busca de lo siguiente:
o Pericardio: La ecografía cardíaca puede detectar un derrame pericárdico (línea
anecoica); colapso de cavidades derechas pueden apoyar taponamiento como
una causa de choque. La ecografía cardíaca también puede ser usada para
guiar la pericardiocentesis y examinar la respuesta al drenaje.
o Ventrículo izquierdo: Un ventrículo izquierdo (VI) grande con la contractilidad
reducida puede sugerir falla de bomba y requerir intervención como
intervención coronaria percutánea, inotrópicos, etc. En contraste, cámaras
cardíacas pequeñas y un VI hiperdinámico pueden indicar choque distributivo
por sepsis o hipovolemia, que puede llevar una evaluación adicional para una
foco séptico o localizar la hemorragia, respectivamente.
o Ventrículo derecho: Reducción en la contractilidad del ventrículo derecho (VD)
puede sugerir infarto de miocardio del VD; aumento de tamaño del VD (por
ejemplo radio >1:1 VD/VI) puede sugerir una Tromboembolia pulmonar (TEP)
masiva o hipertensión pulmonar (imagen de cavidades derechas grandes); un
trombo flotante en la aurícula o ventrículo derecho también apoya de TEP.
o Vena cava inferior: Un colapso exagerado de la vena cava inferior (VCI) al final
de la espiración sugiere hipovolemia. La VCI dilatada puede apoyar a
insuficiencia cardiaca, taponamiento cardíaco o TEP.
2. Insonación dirigida del pulmón y abdomen se deben realizar para examinar lo siguiente:
- Pulmón y el espacio pleural - La ausencia de deslizamiento pulmonar apoya la presencia
de un neumotórax.
o Edema pulmonar como se evidencia por la presencia de líneas B puede apoyar
insuficiencia cardiaca o sobrecarga de volumen.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 42
o Derrame pleural (Línea anecoica) pueden apoyar empiema o hemotórax.
- Cavidad peritoneal - Evidencia de acumulación de líquido peritoneal significativa puede
sugerir una fuente de pérdida de sangre en un trauma o una fuente potencial de
infección (es decir, peritonitis bacteriana espontánea en el paciente con cirrosis).
3. Insonación de las principales arterias y venas:
•Aorta: Aunque se prefiere la tomografía computarizada (TC) de tórax o
ecocardiografía transesofágica, ECP puede detectar un aneurisma torácico o
abdominal. Alternativamente, la visualización de líquido libre o de un derrame
pericárdico o pleural también puede proporcionar una evidencia indirecta de rotura
o disección.
•Extremidades inferiores: La falta de compresibilidad de las venas popitleas o
femorales puede ser indicativo de la trombosis venosa profunda, elevando así la
sospecha de TEP.
Algunas de las veces resulta difícil situar al paciente en un tipo de choque, ya que se encuentran
mixtos (ej. Cardiogénico con séptico) y la toma de decisión para realizar una intervención se
torna un verdadero reto. En estas circunstancias se debe realizar un monitoreo hemodinámico
mas juicioso y profundo, por lo que se requiere otros sistemas o dispositivos invasivos o
mínimamente invasivos los cuales ya se describieron con anterioridad, y la ecografía podría
realizar un monitoreo tan dinámico como se desee.
Cuadro 5. Esquema Forrester Swan adaptado (MHEGAS) a ecografía a la cabecera del paciente
Clase I: Normal Clase II: Edema Pulmonar
•Pulmón seco •Pulmón húmedo
•VI contractilidad adecuada •VI contractilidad adecuada
•VCI normal •VCI dilatada
Tx: Diurético y vasodilatador
Clase III: Hipovolemia Clase IV: Choque Cardiogénico
•Pulmón seco •Pulmón húmedo
•VI contractilidad aumentada •VI contractilidad disminuida
•VCI colapsada •VCI dilatada
Tx: Volumen Tx: Vasopresor y/o inotrópico
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 43
No debemos de olvidar que al paciente críticamente enfermo debemos una vez que hayamos
realizado la exploración ecográfica siguiendo alguno de los protocolos previamente descritos y
ubicando el diagnóstico del mismo iniciar el tratamiento oportunamente y posteriormente si el
caso así lo amerita deberemos de apoyarnos en el ultrasonido para realizar los procedimientos
invasivos que así se requieran. Desde la colocación de accesos vasculares ecoguiados,
paracentesis, toracocentesis, etc. además de continuar con el monitoreo hemodinámico
posterior a intervenciones terapéuticas.
Bibliografía recomendada:
1. Urias Romo de Vivar Emma Gabriela, Ortega Salas Joel, Valenzuela Suárez Héctor. (2016). Ecografía crítica
Head To Toe. México D.F.: Prado
2. Toward an ultrasound curriculum for critical care medicine. Neri L, Storti E, Lichtenstein D. Crit Care Med.
2007 May;35 (5 Suppl):S290-304Motta-Ramírez GA, Bastida-Alquicira J, Béjar-Cornejo J, Craviotto AB,
Salgado-Camarillo J. El ultrasonido y su papel preponderante en situaciones de Urgencia. Anales de Radiología
México 2014;13:404-427.
3. Lucas Ochoa-Pérez, Alejandro Cardozo-Ocampo. Aplicaciones de la ultrasonografía en el sistema nervioso
central para neuroanestesia y cuidado neurocrítico. Rev Colomb Anestesiol . 2 0 1 5;4 3(4):314–320
4. Butts, Christine. The Speed of Sound. The RADiUS Protocol for Evaluating Shortness of Breath. Emergency
Medicine News: April 2014 - Volume 36 - Issue 4 - p 19 doi: 10.1097/01.EEM.0000446062.28899.91
5. Jean-Francois Lancto, Maxime Valois. EGLS: Echo-guided life support An algorithmic approach to
undifferentiated shock. Crit Ultrasound J (2011) 3:123–129 DOI 10.1007/s13089-011-0083-2
6. Dina Seif, Phillips Perera, Thomas Mailhot, David Riley, Diku Mandavia. Bedside Ultrasound in Resuscitation
and the Rapid Ultrasound in Shock Protocol. Critical Care Research and Practice Volume 2012, Article ID
503254, 14 pages doi:10.1155/2012/503254
7. Raoul Breitkreutz, MD; Felix Walcher, MD, PhD; Florian H. Seeger, MD. Focused echocardiographic evaluation
in resuscitation management: Concept of an advanced life support– conformed algorithm. Crit Care Med 2007
Vol. 35, No. 5 (Suppl.)
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 44
Capitulo 6. INTEGRACIÓN DEL MANEJO DEL PACIENTE CON
INESTABILIDAD HEMODINAMICA
“La terapia intensiva no es un lugar, es una actitud”
Cesar Cruz Lozano
Introducción
El estado de choque es una condición potencialmente mortal de insuficiencia circulatoria que
más comúnmente se presenta con hipotensión. También puede ser anunciado por otros
cambios de signos vitales o presencia de niveles altos de lactato sérico. Los efectos del choque
inicialmente son reversibles, pero rápidamente pueden llegar a ser irreversibles, lo que resulta
en un fallo multiorgánico (FOM) y muerte. Por lo tanto, cuando un paciente se presenta con
hipotensión indiferenciada, es importante que el médico identifique rápidamente la etiología de
modo que la terapia apropiada pueda ser administrada para prevenir FOM y muerte.
En este tema integra, resume y destacan los conceptos descritos anteriormente, desde la
presentación clínica, así como los enfoques diagnósticos y terapéuticos iniciales para el
paciente con inestabilidad hemodinámica.
Fisiología: Los principales determinantes fisiológicos de la perfusión tisular (y la presión arterial
sistémica [TA]) son el gasto cardíaco (Q) y la resistencia vascular sistémica (RVS):
TA= Q X RVS
Q es el producto de la frecuencia cardíaca (FC) y el volumen sistólico (VS):
Q= FC X VS
El volumen sistólico es determinado por:
Precarga, contractilidad miocárdica y poscarga
RVS está determinada por:
Longitud del vaso, viscosidad sanguínea y diámetro del vaso (tono de los vasos)
Por lo tanto, los procesos biológicos que cambian cualquiera de estos parámetros fisiológicos
pueden resultar en hipotensión y choque.
Definición y clasificación
Choque se define como un estado de hipoxia celular y tisular debido a la entrega reducida de
oxígeno y/o el aumento del consumo de oxígeno o la utilización inadecuada de oxígeno.
Mientras que los pacientes tienen a menudo una combinación de más de una forma de choque
(choque multifactorial), cuatro clases de choque son reconocidos:
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 45
TIPO DE CHOQUE Q* RVS¶ USG PULMON PADΔ
CARDIOGENICO ↓ ↑ Líneas B ↑
(congestión pulmonar)
HIPOVOLEMICO ↓ ↑ Líneas A ↓
(Pulmón normal)
DISTRIBUTIVO ↑ ↓ Líneas A ↓
OBSTRUCTIVO ↓ ↑ Líneas A o B ↑
Tabla 6. Características hemodinámicas de los estados de choque
* Q= Gasto cardiaco: Volumen que expulsa los ventrículos en un minuto. Es difícil medirlo cuantitativamente en Urgencias (Requiere Cateter de
Swan Ganz, monitoreo mínimamente invasivo y ecocardiografía avanzada), pero se puede evaluar si suficiencia con marcadores de perfusión tisular
como el lactato sérico.
¶ RVS= Resistencias vasculares periféricas: difícil medición, es resultado de Presión arterial media – Presión de aurícula derecha entre gasto
cardiaco.
Δ
PAD= Presión de aurícula derecha: Es prácticamente la presión venosa central, lo cual su valor histórico es de 8-12 mmHg, aunque actualmente
pdebemos individualizar al enfermo y tomar 4-6 mmHg como limites aceptables.
¿CUANDO SOSPECHAR CHOQUE?
Manifestaciones clínicas: Las características que son altamente sospechosos de choque
incluyen:
MANIFESTACIONES CLINICAS DE HIPOPERFUSIÓN TISULAR
Hipotensión Taquipnea
Taquicardia Piel fría, húmeda y cianótica
Oliguria Acidosis metabólica
Estado mental anormal Hiperlactatemia
Tabla 6.1 Características clínicas del estado de choque
La mayoría de los rasgos clínicos no son sensibles ni específicos para el diagnóstico de
choque. Sin embargo, muchas de las manifestaciones clínicas proporcionan “pistas” sobre la
etiología subyacente y se utilizan principalmente para realizar el diagnóstico diferencial de
modo que las terapias empíricas se pueden administrar de manera oportuna.
Características de shock: Las características clínicas típicas que elevan la sospecha de choque
incluyen lo siguiente:
• Hipotensión: Ocurre en la mayoría de los pacientes con shock. La hipotensión puede ser
absoluta (por ejemplo, presión arterial sistólica <90 mmHg; presión arterial media <65
mmHg), relativa (por ejemplo, una caída en la presión arterial sistólica> 40 mmHg) o
profunda (por ejemplo, vasopresores-dependiente).
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 46
Es importante destacar que, los pacientes en las primeras etapas de choque pueden ser
normotensos o hipertensos, de manera que la hipotensión no tiene que estar presente para el
diagnóstico. A la inversa, no todos los pacientes con hipotensión tienen shock (por ejemplo,
hipotensión crónica, hipotensión inducida por fármacos, disfunción autonómica, síncope
vasovagal, enfermedad vascular periférica).
Recuerde: “Existe choque sin hipotensión e hipotensión sin choque”
• Taquicardia: Es un mecanismo compensatorio precoz en pacientes con choque. Puede ser
aislado u ocurrir en asociación con hipotensión. Es importante destacar que, en
comparación con los pacientes de edad avanzada, los pacientes más jóvenes desarrollan
taquicardia grave y persistente antes de presentar hipotensión. Dada la frecuencia del uso
de bloqueadores beta y otros fármacos que controlan la frecuencia cardiaca, se debe tomar
en cuenta como “enmascaradores” de la taquicardia.
• Taquipnea: Es un mecanismo compensatorio precoz en pacientes con choque y acidosis
metabólica. Por lo tanto es una herramienta útil para identificar pacientes con riesgo de
deterioro clínico, como lo demuestra su incorporación al qSOFA.
• Oliguria: En estado de choque puede ser debido a la derivación del flujo sanguíneo renal a
otros órganos vitales, lesión renal directa (por ejemplo, toxicidad de los aminoglucósidos),
o debido a la reducción del volumen intravascular (por ejemplo, vómito, diarrea, o
hemorragia).
• Cambios en el estado mental: Alteración del sensorio en estado de choque por lo general
es debido a la mala perfusión o encefalopatía metabólica. Es un proceso continuo que
comienza con agitación, avanza a la confusión o delirio, y termina en la obnubilación o
coma.
• Alteraciones en la piel: Piel fría y húmeda es por una vasoconstricción periférica que redirige
la sangre, para mantener la perfusión de los órganos vitales (es decir, el flujo coronario,
cerebral y esplácnico). Un aspecto moteado cianótico es una característica preocupante de
hipoperfusión tisular. Sin embargo, la apariencia de la piel fría y húmeda o cianótica también
puede ser debido o exacerbada por isquemia de enfermedad vascular arterial periférica
subyacente. Es importante destacar que piel caliente, hiperémica no descarta estado de
choque debido a que estas características pueden estar presentes en pacientes con choque
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 47
distributivo temprano (antes de la aparición de la vasoconstricción compensatoria) o
choque terminal (debido a un fallo de la vasoconstricción compensatoria).
• Acidosis metabólica: En general, acidosis metabólica de anion GAP elevado debe plantear
siempre la sospecha clínica de choque. Es importante destacar que la presencia de una
acidosis metabólica en los estados de choque no es específica y también puede ser debido
a la lesión renal aguda o la ingestión de toxinas.
• Hiperlactatemia: Ya sea junto con acidosis metabólica o no, la presencia de un nivel elevado
de lactato sérico se ha asociado con resultados adversos, incluyendo el desarrollo de
choque. La relación entre hiperlactatemia tipo A y mortalidad se ha reproducido a través
de una serie de condiciones clínicas, incluyendo el trauma, sepsis y post-paro cardíaco.
Características debido a la causa subyacente: Debido a la amplia gama de etiologías del estado
de choque, las características iniciales pueden ser variables y con frecuencia se superponen. Sin
embargo, se facilitan la identificación temprana de la etiología causante, así como hipoperfusión
tisular cuando se realiza a adecuada anamnesis, exploración física, pruebas de laboratorio y
estudios de imagen.
APROXIMACIÓN INICIAL DEL ESTADO DE CHOQUE
El enfoque inicial para pacientes con estado de choque se debe realizar de manera
sistematizada con el ABCD. Cuando sea posible, se prefiere un enfoque multidisciplinario, ya
que permite la evaluación simultánea y administración de terapias dirigidas en los diferentes
estados de choque:
• La vía aérea debe estabilizarse y colocar acceso intravenoso para que los pacientes pueden
ser tratados inmediatamente con líquidos intravenosos, para restaurar la perfusión
tisular. Es importante destacar que los esfuerzos de reanimación, en particular líquidos por
vía intravenosa, no deberían ser retrasados para una evaluación clínica detallada, ni deben
ser los médicos “hidrofóbicos” en términos de reanimación con líquidos a pacientes con
insuficiencia cardíaca o insuficiencia renal crónica, pero siempre se debe estar a la cabecera
del enfermo para evaluar pre, trans y pos intervención.
• Pacientes críticamente enfermos que han sido estabilizados y en pacientes con hipotensión
leve deben someterse a un enfoque de diagnóstico más formal, mientras que las terapias
iniciales de resucitación siguen en curso.
Es importante destacar que, los pacientes pueden estar inestable hemodinámicamente durante
el período de evaluación y el tratamiento precoz, lo que puede requerir un rápido cambio de
dirección de la aproximación a la administración de terapias vitales.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 48
Evaluar vía respiratoria, ventilación y circulación: Las principales prioridades son estabilizar la
vía aérea y respiración con oxígeno y/o ventilación mecánica, cuando sea necesario. El acceso
intravenoso se debe garantizar que los pacientes pueden ser tratados inmediatamente con
líquidos intravenosos para restaurar la perfusión tisular adecuada.
Los pacientes con dificultad respiratoria y/o marcada inestabilidad hemodinámica suelen
requerir ser intubados. La excepción es aquellos con sospecha de neumotórax a tensión, donde
el drenaje rápido del aire del espacio pleural puede revertir rápidamente choque y evitar la
intubación (ventilación mecánica puede empeorar la tensión y precipitar paro cardíaco).
La secuencia rápida de intubación, por lo general con etomidato (0,3 mg / kg por vía
intravenosa) o ketamina (1 a 2 mg / kg por vía intravenosa), y un bloqueador neuromuscular
de acción rápida, por lo general la utilización de succinilcolina (1 mg / kg por vía intravenosa)
o rocuronio (de 1 a 1,5 mg / kg por vía intravenosa), es el enfoque preferido; agentes que
empeoran la hipotensión (por ejemplo, propofol, midazolam ) deben ser evitados.
Acceso periférico venoso (Calibre de 14 a 18) o el acceso intraóseo es suficiente para la
evaluación inicial y el manejo de muchos pacientes con shock e hipotensión. Sin embargo, el
acceso venoso central debe ser obtenido en aquellos en los que no se puede obtener acceso
periféricos, en los que necesitan infusiones grandes volúmenes de líquidos y/o hemoderivados,
o en aquellos que necesitan infusiones prolongadas de vasopresores. El acceso venoso central
también puede ser útil en pacientes que requieren extraer muestras sanguíneas con frecuencia
para los estudios de laboratorio y para la monitorización hemodinámica (ej: presión venosa
central, saturación de oxigeno venosa central). Es importante destacar que la administración
de líquidos y medicamentos de resucitación no debería ser retrasado porque un acceso venoso
central no está disponible. La evidencia sugiere que el uso de medicamentos vasoactivos
intravenosos periféricos se puede utilizar de forma segura durante horas a días, vigilando que
no se presente extravasación.
Los médicos deben obtener una breve historia y examen físico dirigido, junto con
electrocardiografía dinámica, para evaluar si requiere intervención inmediata o temprana para
salvar la vida. Aunque se prefiere un diagnóstico definitivo, muchas de estas terapias se
administran en base a un diagnóstico presunto con o sin resultados de paraclínicos.
Los pacientes con formas más leves de choque / hipotensión o pacientes que han sido
estabilizados deben someterse a una evaluación diagnóstica completa, mientras continúa la
reanimación. Normalmente hay suficiente tiempo disponible en estos pacientes para obtener
los estudios de laboratorio e imagen definitiva, de modo que el diagnóstico y el tratamiento se
puede hacer de manera simultánea. Sin embargo, la evaluación sigue siendo sensible al tiempo,
ya que los pacientes de esta categoría tienen riesgo de inestabilidad hemodinámica
nuevamente, de tal manera que una rápida reorientación de la estrategia diagnóstica y
terapéutica puede ser necesario.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 49
A continuación se describen identifica intervenciones inmediatas a realizar ante sospecha de
las diferentes situaciones de inestabilidad hemodinámica:
Choque anafiláctico: Los pacientes con alta sospecha de shock anafiláctico (por ejemplo,
hipotensión, estridor inspiratorio, edema oral y facial, urticaria, antecedentes de exposición
reciente a alergenos comunes [ej. las picaduras de abeja]) deben recibir epinefrina
intramuscular. Los pacientes con ventilación mecánica también pueden tener una elevación
repentina de la presión inspiratoria de pico. La dosis normal de un adulto es de 0,3 mg de
1:1000 epinefrina inyectados región media externa del muslo y repetir cada 5 a 15 minutos,
según sea necesario. Otros agentes administrados después de la epinefrina incluyen
antihistamínicos (por ejemplo, difenhidramina 25 a 50 mg y ranitidina 50 mg por vía
intravenosa), Salbutamol nebulizado (1 mg en 3 ml de solución salina), y metilprednisolona (1
a 2 mg / kg por vía intravenosa). La triptasa, total o histamina debe evaluarse antes o poco
después del tratamiento.
Neumotórax a tensión: Debe sospecharse en aquellos con taquipnea, dolor torácico pleurítico
unilateral y ruidos respiratorios abolidos, distensión de las venas del cuello, desviación traqueal
del lado contrario afectado, y factores de riesgo de neumotórax a tensión (por ejemplo,
traumatismo, procedimiento reciente, ventilación mecánica, enfermedad pulmonar quística
subyacente). Los pacientes con ventilación mecánica también pueden tener una elevación
repentina de la presión de meseta. Los pacientes que tienen fuerte sospecha de neumotórax a
tensión no requieren una radiografía de tórax y se debe colocar un tubo de toracostomía de
emergencia (24 o 28 Fr, 36 Fr en trauma; en quinto espacio intercostal, línea axilar media) o
descompresión con aguja usando un catéter intravenoso de calibre 14 al 16 (segundo o tercer
espacio intercostal, línea media clavicular) seguido de tubo de toracostomía inmediata; el tubo
de toracostomía está indicada cuando la descompresión falla.
La guía ecográfica es preferible tanto para el diagnóstico como la colocación del tubo. Además,
preferimos que el drenaje de un neumotórax a tensión se lleva a cabo antes de la intubación
endotraqueal a menos que el paciente ya está intubado o está en paro cardíaco. Para aquellos
con ventilación mecánica, la ventilación con presión positiva debe ser reducida. La confirmación
radiográfica de reexpansión debe realizarse después de drenaje (por ejemplo, ecografía,
radiografía de tórax).
Taponamiento pericárdico: Se debe sospechar en pacientes con disnea, taquicardia,
hipotensión, presión venosa yugular elevada, ruidos cardíacos disminuidos, pulso paradójico, y
los factores de riesgo conocidos (por ejemplo, traumatismo, diátesis hemorrágica, derrame
pericárdico conocido, procedimiento torácico o pericárdico reciente). La demostración de
taponamiento por ecografía (derrame pericárdico, colapso de cavidades cardiacas derechas y
vena cava inferior dilatada) se debe realizar antes de la pericardiocentesis. La ecografía
también guía colocación de la aguja o catéter y examina la respuesta al drenaje de líquido del
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 50
saco pericárdico. En casos raros, una toracotomía de emergencia puede realizarse en aquellos
que no responden al drenaje del catéter o en aquellos que desarrollan paro cardiaco durante
la reanimación.
Es importante destacar que la pericardiocentesis no debe intentarse en pacientes con derrame
pericárdico debido a la disección aórtica o rotura miocárdica, como el alivio del taponamiento
cardíaco puede empeorar el sangrado. Tales pacientes requieren intervención quirúrgica
emergente. En los casos en que el taponamiento es dudoso, se requieren datos adicionales
como mediciones hemodinámicas a través de cateterización de la arteria pulmonar por un
experto.
Hemorragia significativa: Los pacientes con sospecha de choque hemorrágico deben ser
identificados como traumático o no traumático:
• Traumáticas: Los pacientes con antecedentes de traumatismo cerrado o penetrante
requiere ecografía a la cabecera para localizar la fuente de la hemorragia, así como para
la evaluación de otras lesiones corporales (FAST, E-FAST). Esta población también puede
beneficiarse de drenaje (por ejemplo, hemotórax) o intervención quirúrgica (por ejemplo,
ruptura de bazo).
• No traumáticas: Los pacientes con sospecha de tener un aneurisma aórtico abdominal
(AAA) roto (por ejemplo, hipotensión, dolor abdominal o de espalda, masa abdominal
pulsátil, historia conocida de aneurisma abdominal) deben ser evaluados preferentemente
mediante tomografía computarizada con contraste (TC) antes de la intervención
quirúrgica; sin embargo, los pacientes a menudo son demasiado inestables para obtener
de forma segura una tomografía computarizada, y el manejo deben producirse de forma
empírica. La ecografía que demuestra la hemorragia peritoneal y aneurisma se puede
realizar cuando la TC no es seguro o no está disponible. Para los pacientes con las
manifestaciones de hemorragia gastrointestinal superior o inferior (por ejemplo,
hematemesis, hematoquecia, la anemia, la diátesis hemorrágica), la intervención
endoscópica, la embolización o cirugía puede estar indicada.
Esta población general requiere grandes volúmenes de hemoderivados, y se deben evitar
vasopresores de manera inicial. Se debe realizar tipo de sangre y pruebas de cruce de paquetes
globulares, un recuento sanguíneo completo y estudios de coagulación deben ser obtenidos
en todos los pacientes con sospecha de hemorragia.
Arritmias potencialmente mortales: Manejo acorde a guias de soporte vital cardiovascular
avanzada (SVCA) 2015.
Choque séptico: Los pacientes con sospecha de infección (por ejemplo, fiebre, hipotensión, y
un foco séptico sospechado) se benefician de la administración precoz de antibióticos por vía
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 51
intravenosa, la elección de los cuales se determina por la fuente de sospecha, y reposición de
líquidos intravenosas. Si la fuente es desconocida y Pseudomonas (poco probable), estamos a
favor de la combinación de vancomicina con cefalosporina de cuarta o tercera generación (por
ejemplo, ceftriaxona o cefotaxima , cefepima) o una beta-lactamico (por ejemplo, piperacilina-
tazobactam) o un carbapenemico (por ejemplo, imipenem o meropenem ). La leucocitosis y,
en particular bandemia, así como los datos de laboratorio y de imagen indicativos de una fuente
de infección, hace muy posible a la sepsis como causa del choque. Cultivos y hemocultivos
deben obtenerse, preferiblemente antes de la administración de antibióticos, sin que esto
retrase su administración. Los signos vitales continuos y la medición de lactato sérico, se
pueden usar para estratificar el riesgo de que el paciente séptico.
Choque cardiogénico por infarto de miocardio: Los pacientes que presentan hipotensión
asociada con isquemia miocárdica y cambios en el ECG compatibles con infarto de miocardio
con elevación del ST (IAMCESST) se benefician de reperfusión coronaria temprana. Elevación
de Troponina o CK MB elevados (posterior a 4 horas de inicio de síntomas) y edema pulmonar
en la radiografía de tórax apoyan el diagnóstico. Las intervenciones incluyen la administración
de agentes farmacológicos (por ejemplo, agentes antiplaquetarios, heparina), procedimientos
de revascularización coronaria (por ejemplo, angioplastia con balón), y/o una bomba de balón
de contrapulsación aortica).
Choque cardiogénico por insuficiencia de válvula aórtica o mitral aguda: Los pacientes con dolor
torácico, hipotensión, y nuevo soplo diastólico temprano de tono bajo es compatible con
insuficiencia de válvula aórtica y deben someterse a ecocardiografía antes de la intervención
quirúrgica. Los estudios adicionales de laboratorio o de imagen que apuntan a descubrir la
etiología de la ruptura (por ejemplo, la TC de tórax para la disección aórtica, hemocultivos y
ecocardiografía transesofágica para absceso de raíz aórtica) pueden ser necesarios en esta
población. Los pacientes con insuficiencia respiratoria aguda y nuevo soplo sistólico después
de un infarto agudo de miocardio (IAM) deben ser sometidos a ecocardiografía
preferentemente para búsqueda de insuficiencia de válvula mitral o defecto del tabique
ventricular, lo que también es posible que requiera intervención quirúrgica urgente.
Disección de aorta ascendente: Los pacientes con disección aórtica típicamente se presentan
con la hipertensión y dolor torácico o de espalda. Sin embargo, hipotensión y choque se
producen por disección retrógrada que resulta en insuficiencia aórtica aguda, taponamiento
pericárdico, o infarto de miocardio. Los pacientes con sospecha de disección deben someterse
a la TC con contraste de diagnóstico, la ecocardiografía transesofágica, o imágenes por
resonancia magnética (IRM), según su disponibilidad. Cuando tales imágenes no son seguras,
la ecocardiografía transtorácica o ecografía a la cabecera del paciente que demuestra la
dilatación de la raíz aórtica y un colgajo de la íntima puede ser de apoyo para el diagnóstico.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 52
Tromboembolia pulmonar hemodinámicamente inestable (TEP masiva): Los pacientes con
hipotensión, disnea aguda e hipoxemia tienen alta sospecha de Tromboembolia pulmonar (TEP)
puede beneficiarse de terapia trombolítica sistémica. La Rx de tórax “normal” y elevación del
dímero D, troponina, y niveles de péptido natriurético (BNP o proBNP) son apoyo al
diagnóstico. Angiotomografía pulmonar es el método de diagnóstico preferido en esta
población. Sin embargo, para aquellos en los que la TC no es seguro, un diagnóstico presuntivo
se puede obtener mediante ecocardiografía (por ejemplo, dilatación del ventrículo derecho,
presencia de trombo) justifican la administración de un agente trombolítico, cuando no existan
contraindicaciones.
Insuficiencia suprarrenal: Los pacientes con sospecha de insuficiencia suprarrenal (por ejemplo,
hipotensión, depleción de volumen, la historia de deficiencia de glucocorticoides o suspensión
abrupta) deben recibir la reposición de líquidos y juiciosamente dexametasona 4 mg por vía
intravenosa. La selección de la dexametasona se basa en la capacidad de interpretar las
mediciones de cortisol en suero como parte de la evaluación. Cortisol sérico, corticotropina
(ACTH), la aldosterona, la renina, y la bioquímica sérica debe elaborarse para confirmar el
diagnóstico.
EVALUACIÓN DIAGNÓSTICA INICIAL
Por lo general, se realiza lo siguiente:
• Evaluación general: La evaluación debe incluir una historia clínica y evaluación del estado
de alerta, mucosas y lengua, venas del cuello, pulmones, corazón y abdomen, así como la
piel y articulaciones. Hipotensión, oliguria, alteraciones del estado mental y piel fría y
húmeda son hallazgos clínicos centinela que deben hacer sospechar de un tratamiento
directo con fluidos intravenosos y posterior evaluación con estudios de laboratorio y de
imagen correspondiente.
• Electrocardiograma: Monitorización cardiaca y/o electrocardiograma (ECG) se debe realizar
en pacientes con hipotensión y estado de choque. ECG puede revelar una arritmia o
segmento ST cambios compatibles con isquemia o pericarditis. Un ECG de bajo voltaje puede
ser sugestiva de un derrame pericárdico. Los signos clásicos de la embolia pulmonar (S1,
Q3, T3) o isquemia miocárdica, también pueden ser evidentes
• Evaluación de la etiología: Una evaluación exhaustiva de la etiología subyacente del choque
se debe realizar después de la estabilización.
Evaluación de laboratorio: Las pruebas de laboratorio deben realizarse temprano en la
evaluación de pacientes con estado del choque para identificar la causa del mismo y/o falla
orgánica temprana. Un lactato elevado (> 2 mmol / L) es un indicador temprano de
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 53
hipoperfusión y es particularmente útil en aquellos que son normotensos o hipertensos (es
decir, aquellos en los que es menos probable que se sospeche de choque).
Sugerimos las siguientes pruebas básicas de laboratorio pueden obtener en la mayoría de los
pacientes con estado de choque indiferenciado, recordando que la prueba debe ajustarse de
acuerdo con la sospecha de etiología:
LABORATORIOS BASICOS PARA ESTADO DE CHOQUE INDIFERENCIADO
Lactato sérico Biometría hemática completa
Pruebas de función renal y hepática Estudios de coagulación y D-dímero
Enzimas cardiacas y péptidos natriuréticos Gasometría arterial y/o venosa.
Tabla 6.2 Laboratorios en choque indiferenciado
Evaluación de imagen: Una diversidad de estudios de imagen se requieren para realizar
diagnostico etiológico del estado de choque, radiografías, tomografías, resonancia magnética;
pero sin dudas el advenimiento de la ecografía a la cabecera del paciente aporta datos de
diagnóstico pero también de monitorización, se requiere adiestramiento para realización e
interpretación de las imágenes realizadas.
CARDIOGENICO HIPOVOLEMICO/
DISTRIBUTIVO DISTRIBUTIVO
TARDIO TEMPRANO OBSTRUCTIVO
Evaluación Falla cardiaca Hipovolemia o Tamponamiento Embolia Neumotorax a tensión
vasodilatación cardiaco pulmonar
Cardiaca VI severamente VD pequeño, VI VD pequeño, VI VD dilatado, VI VD pequeño, VI
hipokinético y/o hiperkinético hiperkinetico, derrame hipokinético hiperkinético.
disfunción valvular pericardico.
Vena Cava Fija y distendida Flexible y colapsable. Fija y distendida Fija y distendida Fija y distendida
inferior
Pulmón Perfil B Perfil A Perfil A Perfil A Perfil A NO
Deslizamiento pleural Deslizamiento pleural Deslizamiento Deslizamiento DESLIZAMIENTO,
± derrame pleural ± derrame pleural ± Consolidados Punto pulmonar
Otros ± Foco séptico, ± Colección de Venas hepáticas y Trombosis ± Desplazamiento
Venas hepáticas líquidos (FAST) yugulares distendidas venosa traqueal, Venas
distendidas ± Aneurisma A. Abd. Venas hepáticas hepaticas distendidas.
± Foco séptico distendidas
Tratamiento y Inotropicos, Fluidoterapia, Pericardiocentésis Trombólisis Drenaje torácico,
monitoreo diureticos, ICP o Vasoconstrictores, Cirugía cirugía.
cirugía Cirugía
Tabla 6.3 Principales características encontradas en la ecografía a la cabecera del paciente.
SOPORTE HEMODINÁMICO:
En general, aquellos pacientes con sospecha de choque deberían recibir apoyo hemodinámico
con líquidos intravenosos, seguido por vasopresores cuando los liquidos intravenosos no
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 54
logran restaurar la perfusión tisular adecuada (ver algoritmo en capitulo 3). Mientras que la
presión óptima de perfusión de los órganos se recomienda mantener la presión arterial media
mayor de 60 a 65 mmHg (>80 mmHg en Hipertensos crónicos mal controlados). Cabe
mencionar que en el choque hipovolémico se prefiere evitar vasopresores y el choque
cardiogénico donde se prefiere inicio pronto de vasopresores.
Líquidos intravenosos: Son agentes de primera línea en el tratamiento de pacientes con estado
de choque. Nosotros preferimos administrar Hartman en bolo, que se puede repetir de manera
juiciosa hasta que la presión arterial y la perfusión de tejidos mejore; se debe tener evaluación
continua para evitar edema pulmonar y/o hipertensión intraabdominal, este último se presenta
a mayor tiempo y cantidad de líquidos.
El volumen total infundido se determina por la etiología de choque. A modo de ejemplo, los
pacientes con choque obstructivo en embolia pulmonar o choque cardiogénico por infarto de
miocardio de ventrículo izquierdo por lo general requieren pequeños volúmenes de líquidos
intravenosos, mientras que aquellos con infarto del VD o sepsis a menudo necesitan 2 L, y
aquellos con shock hemorrágico frecuentemente requieren volúmenes > 3 a 5 L (a menudo
incluyen hemoderivados). La administración de la terapia diurética debe evitarse en pacientes
hipotensos con edema pulmonar hasta que la necesidad de apoyo hemodinámico haya sido
retirado.
La elección óptima de líquido es debatible. Sin embargo, la solución más aceptada es el Ringer
Lactato (Hartman) y aquellos con choque hemorrágico deben ser tratados preferentemente
con hemoderivados cuando estén disponibles. Se recomienda evitar la administración
de cristaloides tipo pentastarch o hidroxietilalmidón por aumentar las posibilidades de lesión
renal aguda y mortalidad. La albumina se administrará en casos especiales y por expertos en
pacientes graves.
Vasopresores: Los vasopresores se requieren con frecuencia en el tratamiento de pacientes
con sospecha de choque para restaurar la perfusión tisular adecuada. Es importante destacar
que el uso de vasopresores en pacientes con choque hemorrágico o hipovolémico puede ser
perjudicial, de tal manera que vasopresores sólo deben utilizarse como una forma adicional de
soporte hemodinámico cuando la volemia intravascular se haya restablecido.
Los vasopresores se debe ajustar de acuerdo a la respuesta (es decir, los índices de perfusión
de los tejidos incluyendo la presión arterial, la diuresis, el estado mental y el color de la piel) y
la limitación de los efectos secundarios (por ejemplo, taquicardia).
Diuréticos: No son de uso de manera inicial en paciente inestable en el área de urgencias, sin
embargo en el caso que exista edema agudo pulmonar en contexto de emergencia hipertensiva
debe ser administrado. El diurético de ASA tipo Furosemida 0.5- 1mg/kg en bolo inicial se utiliza
además de vasodilatadores.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 55
DOSIS INICIAL MANTENIMIENTO DOSIS MAXIMA CARACTERISTICAS
NOREPINEFRINA(Receptores α1 y β1)
8-12 mcg/min 2-4 mcg/min 35-100 Elección en Choque séptico, cardiogenico
(0.1-0.15 mcg/Kg/min) (0.025-0.05 mcg/min e hipovolémico*
mcg/Kg/min) (0.5-0.75
mcg/Kg/min)
ADRENALINA(β1 y α1, dosis muy bajas β2)
1 mcg/min 1-10 mcg/min 10-35 mcg/min Elección en Choque anafiláctico
(0.014 mcg/Kg/min) (0.014-0.14 (0.14-0.5 Aumenta FC, puede inducir
mcg/Kg/min) mcg/Kg/min) taquiarritmias, isquemia miocárdica e
hipoperfusión mesentérica.
FENILEFRINA(α-1)
100-180 mcg/min 20-80 mcg/min 80-360 Vasoconstrictor α-1 puro.
(2 mcg/Kg/min) (0.25-1.1 mcg/min Indicado:
mcg/Kg/min) (1.1-6 1. Norepinefrina induce
mcg/Kg/min) taquiarritmias.
2. Choque séptico refractario
(Norepinefrina-Vasopresina)
3. Alto Q con hipotensión
Tabla 6.4. Principales Vasopresores utilizados en paciente con estado de choque con hipotensión
DOSIS INICIAL MANTENIMIENTO DOSIS MAXIMA CARACTERISTICAS
DOPAMINA (Receptores β1, Dosis elevadas α1)
2-5 mcg/Kg/min 5-10 20- >50 mcg/Kg/min Segunda línea después de NE en
mcg/Kg/min pacientes seleccionados (es
arritmogenica)
Elección en bradicardia inestable
VASOPRESINA(Receptores V1, vasoconstricción: activación de fosfolipasa C. V2 efecto antidiurético)
0.01- 0-03 u/ min 0.03- 0.04 u/ > 0.04 u/ min puede Adición a Norepinefrina
min causar isquemia No de primera línea
miocárdica, debe
reservarse como rescate
Tabla 6.4.1. Principales Vasopresores utilizados en paciente con estado de choque con hipotensión
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 56
DOSIS INICIAL MANTENIMIENTO DOSIS MAXIMA CARACTERISTICAS
DOBUTAMINA(Receptoresβ1)
0.5-1 2-20 mcg/Kg/min 20- 40 mcg/Kg/min, Elección en Choque
mcg/Kg/min TERAPIA DE cardiogenico con bajo Q y TAS
RESCATE mayor 90 mmHg.
Disfunción miocárdica en
sepsis.
Puede inducir Hipotensión y
taquicardia
LEVOSIMENDAN(Sensibilizador de canales Ca++, Apertura canales K+ periférico)
0.05 0.05- 0.2 0.2 mcg/kg/min Insuficiencia cardiaca grave
mcg/kg/min mcg/kg/min
Tabla 6.5. Principales inotrópicos utilizados en paciente con estado de choque con hipocontractilidad cardiaca
Choque combinado: Es importante destacar que muchas formas de choque coexisten. Como un
ejemplo, hipovolemia con shock cardiogénico y puede resultar en comportamiento
hemodinámico confuso (por ejemplo, fracción de eyección baja con mucosas secas y una VCI
colapsable). En tales casos, después de la respuesta a los tratamientos empíricos dirigidos a
las posibles causas de shock el médico debe determinar qué tipo de choque es el
predominante.
Por ultimo deberíamos hacerse todo lo posible para tratar la causa desencadenante del estado
de choque. En algunos casos la etiología es clara (por ejemplo, choque hemorrágico de una
herida de bala en el abdomen), pero en otros casos la etiología es menos evidente (por
ejemplo, choque obstructivo por TEP masiva). Una vez conocido el diagnóstico, las terapias
específicas deben ser dirigidas, y la respuesta a la terapia monitoreados (por ejemplo, presión
arterial media, uresis, estado mental, nivel de lactato sérico).
Conclusiones:
El monitoreo hemodinámico debe ser individualizado, dinámico, integral y siguiendo las
tendencias del enfermo, debiendo pensar:
1. En la patología mas grave que pueda provocar la muerte del paciente.
2. La patología mas común que pueda presentar el paciente.
3. Patologías menos frecuentes.
4. Formas atípicas o poco comunes de patologías comunes.
5. No olvide situaciones mixtas (Ej. Choque séptico y cardiogénico).
6. Realizar mediciones y evaluaciones frecuentes pre, tras y pos intervención.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 57
Esquema 6. Forrester Swan modificado por Zamora, Zamarrón y Pérez Nieto
PAM= Presión arterial media, IQ= Índice cardiaco, POAP= Presión de oclusión de la arteria pulmonar, * Preserva
contractilidad perse.
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 58
Monitoreo Hemodinámico y Gasométrico (MHEGAS) 59
También podría gustarte
- AVENTHO Manual para Curso de Ventilación MecánicaDocumento58 páginasAVENTHO Manual para Curso de Ventilación MecánicaNoemi Campos92% (48)
- Manual Alteraciones Del Equilibrio Acido Base 2020pdfpdfDocumento42 páginasManual Alteraciones Del Equilibrio Acido Base 2020pdfpdfsonia isanami50% (2)
- Ventilacion Mecanica SATI 2da EdicionDocumento518 páginasVentilacion Mecanica SATI 2da EdicionDavid Andres91% (33)
- Chatburn Taxonomia TraduccionDocumento17 páginasChatburn Taxonomia TraduccionEsau Garcia100% (16)
- Ventilacion Mecania Manual BasicoDocumento53 páginasVentilacion Mecania Manual BasicoCarlos Castillo Barragan100% (5)
- Taller de Gases y HemodinámicoDocumento20 páginasTaller de Gases y HemodinámicoCarlos RosasAún no hay calificaciones
- Tratado de Medicina CriticaDocumento2 páginasTratado de Medicina CriticaMelisaMontenegroHidalgo100% (2)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones
- Ventilación mecánica pediatríaDocumento46 páginasVentilación mecánica pediatríaJessyMomo100% (3)
- Topicos Selectos en Anestesiologia Carrillo PDFDocumento363 páginasTopicos Selectos en Anestesiologia Carrillo PDFMartin Villarroel100% (3)
- Libro de Ventilacion Mecanica DR DueñasDocumento473 páginasLibro de Ventilacion Mecanica DR Dueñasjaimillo68100% (8)
- Manual Sovec VentilaciónDocumento53 páginasManual Sovec VentilaciónPaola Monterrosa100% (5)
- Tarjetas MHEGAS 20 12final PDFDocumento10 páginasTarjetas MHEGAS 20 12final PDFHoracio Sosa100% (4)
- Taller GasometricoDocumento12 páginasTaller GasometricoLuis Arzola88% (16)
- Tamagnone 2019 LIBRO POCUS Manual Práctico Ultrasonografía CríticaDocumento376 páginasTamagnone 2019 LIBRO POCUS Manual Práctico Ultrasonografía Críticajesus hernadez100% (2)
- El Libro de La UciDocumento1 páginaEl Libro de La Ucinicolas100% (1)
- Reanimación NeonatalDocumento362 páginasReanimación NeonatalAngel Iván Martínez Guadalupe100% (4)
- Escala de riesgo quirúrgico ASA e índices de riesgo perioperatorioDocumento4 páginasEscala de riesgo quirúrgico ASA e índices de riesgo perioperatorioZeykid100% (5)
- SNC - Soporte neurocrítico: De la urgencia a la terapia intensivaDe EverandSNC - Soporte neurocrítico: De la urgencia a la terapia intensivaAún no hay calificaciones
- Ultrasonido en emergencias y cuidados críticosDe EverandUltrasonido en emergencias y cuidados críticosCalificación: 5 de 5 estrellas5/5 (2)
- Guía de decisión en urgencias medicina del adulto (GUMA)De EverandGuía de decisión en urgencias medicina del adulto (GUMA)Calificación: 5 de 5 estrellas5/5 (1)
- Aventho Ventilacion MecanicaDocumento66 páginasAventho Ventilacion MecanicaMilca Ramirez100% (1)
- Tarjetas IcarusDocumento16 páginasTarjetas IcarusFernando Mendieta100% (1)
- Algoritmos y Tarjetas Digitales UrcaDocumento19 páginasAlgoritmos y Tarjetas Digitales UrcaErnesto Alonso Zamora Anguiano100% (1)
- Taller Hemodinamico GasometricoDocumento31 páginasTaller Hemodinamico GasometricoJorge Barrios Flores100% (2)
- Tarjetas Avento Nueva SDocumento18 páginasTarjetas Avento Nueva SJULIO ADÁN HUERTA UGARTE100% (4)
- Aventho Neurocrítico PDFDocumento9 páginasAventho Neurocrítico PDFAlex Rodrigo100% (1)
- Taller GasometricoDocumento65 páginasTaller GasometricoAlonso Diaz0% (1)
- Ventilacion Mecanica en El Paciente NeurocriticoDocumento28 páginasVentilacion Mecanica en El Paciente Neurocriticorepre64100% (1)
- Dubin Interpretacion de ECGDocumento383 páginasDubin Interpretacion de ECGFrancisco100% (4)
- Chiappero - Ventilación MecánicaDocumento268 páginasChiappero - Ventilación MecánicaSamuel Acosta57% (7)
- Fisiologia Respiratoria Aplicada A Ventilacion MecanicaDocumento47 páginasFisiologia Respiratoria Aplicada A Ventilacion MecanicaGere ChumpitazAún no hay calificaciones
- Gases ArterialesDocumento8 páginasGases ArterialesJohan Meyer100% (1)
- Manual de cuidado intensivo cardiovascular pediátrico (segunda edición)De EverandManual de cuidado intensivo cardiovascular pediátrico (segunda edición)Calificación: 5 de 5 estrellas5/5 (2)
- Carpeta Gerencial - Punto 11 BorradorDocumento104 páginasCarpeta Gerencial - Punto 11 BorradorZURISADDAY SANCHEZ RAMIREZ100% (3)
- Introducción HipoglucemiaDocumento8 páginasIntroducción Hipoglucemiavanessa100% (1)
- Manual de Anestesia en OdontopediatriaDocumento16 páginasManual de Anestesia en OdontopediatriaDelia G. ReyesAún no hay calificaciones
- Interpretación Rápida De La Gasometría Arterial: Gasometría Arterial En 4 PasosDe EverandInterpretación Rápida De La Gasometría Arterial: Gasometría Arterial En 4 PasosAún no hay calificaciones
- Principios de anestesiología y algología para médicos en formaciónDe EverandPrincipios de anestesiología y algología para médicos en formaciónAún no hay calificaciones
- Ultrasonido pulmonar focalizado: Serie Ultrasonido focalizado en urgencias y cuidado críticoDe EverandUltrasonido pulmonar focalizado: Serie Ultrasonido focalizado en urgencias y cuidado críticoAún no hay calificaciones
- Anestesiología: Apúntes para el médico generalDe EverandAnestesiología: Apúntes para el médico generalCalificación: 3.5 de 5 estrellas3.5/5 (4)
- Tarjeta SM He Gas FinalDocumento9 páginasTarjeta SM He Gas FinalHm JoseAún no hay calificaciones
- Atlas de Curvas AVENTHO 3ra EdiciónDocumento16 páginasAtlas de Curvas AVENTHO 3ra EdiciónJuan R Hernandez Lozano100% (2)
- Ventilación Mecánica 2Documento62 páginasVentilación Mecánica 2souls0693100% (1)
- Poblano PDFDocumento11 páginasPoblano PDFJesus Ernesto Salazar GarciaAún no hay calificaciones
- Tarjetas SIR AVENTHO PDFDocumento7 páginasTarjetas SIR AVENTHO PDFIsabel Enríquez100% (1)
- Programación en VMIDocumento13 páginasProgramación en VMIMaría Alejandra García Q100% (1)
- Bienvenido A La Ventilación Mecánica AVENTHODocumento3 páginasBienvenido A La Ventilación Mecánica AVENTHOLucy Quispe MedranoAún no hay calificaciones
- Taller HemodinamicoDocumento1 páginaTaller Hemodinamicommoraes0709100% (4)
- Monitoreo Del Paciente Bajo Ventilación MecánicaDocumento28 páginasMonitoreo Del Paciente Bajo Ventilación MecánicaIvan PalaciosAún no hay calificaciones
- Tarjetas de Trabajo AVENTHO CDocumento17 páginasTarjetas de Trabajo AVENTHO CJose Gerardo Espinoza VeraAún no hay calificaciones
- Tarjeta SM He GasDocumento5 páginasTarjeta SM He GasLaura CR0% (1)
- SDRAAVENTHO2Documento16 páginasSDRAAVENTHO2Jairo Sosa100% (2)
- Curso ONLINE Ventilación Mecánica AVENTHO EVALUACIÓN FINALDocumento3 páginasCurso ONLINE Ventilación Mecánica AVENTHO EVALUACIÓN FINALcarlos parada100% (1)
- Cuidado Intensivo Trauma PDFDocumento1272 páginasCuidado Intensivo Trauma PDFAiled Hernandez100% (6)
- Manual Washington de Medicina de UrgenciasDocumento987 páginasManual Washington de Medicina de UrgenciasOmar Soto95% (21)
- Repaso Puemr2Documento206 páginasRepaso Puemr2Alex Vargas100% (1)
- Ventilacion Mecanica Controlada y Asistida ControladaDocumento12 páginasVentilacion Mecanica Controlada y Asistida ControladaYina Marcela Quintero Ortega100% (1)
- 11-Terapia IntensivaDocumento366 páginas11-Terapia IntensivaE Castillo Ortega100% (1)
- Sesion 8 - ItsDocumento33 páginasSesion 8 - Itsozkar socualaya mantariAún no hay calificaciones
- Caso Clinico PsicosomaticaDocumento12 páginasCaso Clinico PsicosomaticaAriana N. Castillo H.Aún no hay calificaciones
- 207 411 1 SMDocumento2 páginas207 411 1 SMKaren NiikOleAún no hay calificaciones
- Evaluación de La Exposición y Efectos en La Salud Pública Cuando Hay Deficiencias en El Manejo de Residuos PeligrososDocumento4 páginasEvaluación de La Exposición y Efectos en La Salud Pública Cuando Hay Deficiencias en El Manejo de Residuos PeligrososLizAún no hay calificaciones
- Anexo 6 RDocumento2 páginasAnexo 6 RGCanisAún no hay calificaciones
- Padron Actualizado300511Documento9 páginasPadron Actualizado300511Instituto Canzion AntofagastaAún no hay calificaciones
- Capítulo 18 - AbortoDocumento50 páginasCapítulo 18 - AbortoAndrAún no hay calificaciones
- Hiperfosfatasemia en La Infancia: Interpretación y Actitud DiagnósticaDocumento5 páginasHiperfosfatasemia en La Infancia: Interpretación y Actitud DiagnósticaMarianaAún no hay calificaciones
- LinfadenectomiaDocumento10 páginasLinfadenectomiaTania RodriguezAún no hay calificaciones
- Materia CardioDocumento39 páginasMateria CardioMilenka yvone Rubina castilloAún no hay calificaciones
- Fármacos Que Afectana Al Sistema Nervioso CentralDocumento30 páginasFármacos Que Afectana Al Sistema Nervioso CentralJose RamosAún no hay calificaciones
- Ganglios BasalesDocumento46 páginasGanglios BasalesAndres DangondAún no hay calificaciones
- Trastorno humor orgánicoDocumento29 páginasTrastorno humor orgánicomarilyn100% (1)
- Quistes Odontogenicos MexicoDocumento8 páginasQuistes Odontogenicos MexicoDanae ElorrietaAún no hay calificaciones
- Informe de vigilancia de salud ocupacionalDocumento10 páginasInforme de vigilancia de salud ocupacionalRuben Dario BravoAún no hay calificaciones
- Cuarto de Moldes y AccesoriosDocumento41 páginasCuarto de Moldes y AccesoriosCarolay ParedesAún no hay calificaciones
- MONOGRAFIA Cancer de MamaDocumento24 páginasMONOGRAFIA Cancer de MamaLuisiñho Coba0% (1)
- Cuentos para El LíbanoDocumento10 páginasCuentos para El LíbanoFabio MoralesAún no hay calificaciones
- Módulo-VIII. Heridas y Piediabético Ecos de Cirugia 2018Documento29 páginasMódulo-VIII. Heridas y Piediabético Ecos de Cirugia 2018Yolis MirandaAún no hay calificaciones
- Neoplasia Ii Anaplasia y Diferenciacion 3Documento24 páginasNeoplasia Ii Anaplasia y Diferenciacion 3Ruth FernandezAún no hay calificaciones
- Vitamina B1 PDFDocumento6 páginasVitamina B1 PDFmanuelaAún no hay calificaciones
- EnalaprilDocumento2 páginasEnalaprilJacqueline DomínguezAún no hay calificaciones
- Trebol Salud 01.04.19 PDFDocumento21 páginasTrebol Salud 01.04.19 PDFYoni NorabuenaAún no hay calificaciones
- Eficacia Del OLEOZON® Oral Como MedicamentoDocumento10 páginasEficacia Del OLEOZON® Oral Como Medicamentodavid peña100% (1)
- Sinave MspasDocumento42 páginasSinave MspasAntonioGregorio100% (1)
- Clase 1 Enfermería BásicaDocumento50 páginasClase 1 Enfermería BásicaJustino SantistevanAún no hay calificaciones
- Vacuna Contra La VaricelaDocumento10 páginasVacuna Contra La Varicelajuan gustavo gamarra cascpAún no hay calificaciones