Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Experimento #2
Cargado por
cvcvcccccrvcf0 calificaciones0% encontró este documento útil (0 votos)
9 vistas2 páginasTítulo original
Experimento Nº 2
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
9 vistas2 páginasExperimento #2
Cargado por
cvcvcccccrvcfCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
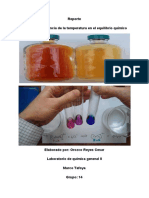
Experimento Nº 2: Efecto de la variación de la temperatura, Complejo de
Cobalto
a) Al agregar agua al [Co (H2O)4]Cl2(s) ¿Qué complejo se ha formado?
Se ha formado [Co(H2O)6]2+(ac) , que es un ion hexa- hidratado.
b) Cuándo se lleva a baño maría (90 °C):
¿Qué sucede?
La disolucion se vuelve de color azul porque se formo mas cantidad de cloruro de colbato.
¿En qué sentido se ha desplazado el equilibrio?
Se desplaza en dirección endotérmica , es decir, hacia la izquierda.
¿Cuál ha sido la causa?
Al ser una reacción exotérmica , el aumento de la temperatura causa que el equilibrio de la reacción se
desplaza hacia la derecha hacia el ion [CoCl4]-.
c. Cuando se lleva a baño de hielo:
¿Qué sucede?
La solución se torna color rosada.
¿En qué sentido se ha desplazado el equilibrio?
Se desplaza en dirección derecha.
¿Cuál ha sido la causa?
Al exponer la solucion a bajas temperturas podemos observar un cambio de color , ya que segun la ley
de Chatelier el equilibrio se desplazara hacia la derecha para formar mas ion Colbato hexahidratado
porque la finalidad es restablecer el equilibrio.
d. Escriba las ecuaciones químicas correspondientes.
e. Indique si la reacción es exotérmica o endotérmica.
Endotérmica ya que nos muestra el efecto del cambio de la temperatura sobre el desplazamiento del
equilibrio.
También podría gustarte
- Hidrolisis 2Documento4 páginasHidrolisis 2eduardohk18Aún no hay calificaciones
- QGII Equilibrio QuímicoDocumento4 páginasQGII Equilibrio Químicofrancisco guamanAún no hay calificaciones
- LABORATORIO - CAMBIOS DE COLOR DEL CobaltoDocumento2 páginasLABORATORIO - CAMBIOS DE COLOR DEL CobaltoSasaAún no hay calificaciones
- Reporte - Práctica 8Documento6 páginasReporte - Práctica 8jimenaAún no hay calificaciones
- Laboratorio Reacciones QuimicasDocumento5 páginasLaboratorio Reacciones QuimicasingridamorAún no hay calificaciones
- Practica 8 Quimica General IIDocumento11 páginasPractica 8 Quimica General IIusuarin9575% (4)
- Informe IiDocumento8 páginasInforme IiAlba CanoAún no hay calificaciones
- Equilibrio QuimicoDocumento3 páginasEquilibrio QuimicoTeresa Cifuentes⃝⃤0% (2)
- Principio de Le ChatelierDocumento6 páginasPrincipio de Le ChatelierGatica17Aún no hay calificaciones
- Practica 8 PDFDocumento7 páginasPractica 8 PDFCesar OrozcoAún no hay calificaciones
- Reacciones QuimicasDocumento5 páginasReacciones QuimicasFrank Aaron Nacarino VillegasAún no hay calificaciones
- Practica 7 QuimicaDocumento3 páginasPractica 7 Quimicagabrielrs0505Aún no hay calificaciones
- Práctica 08 REPORTE.Documento7 páginasPráctica 08 REPORTE.Wendy JoselineAún no hay calificaciones
- AnalisisDocumento2 páginasAnalisisAlejandra Lopez RuizAún no hay calificaciones
- Informe 2 QG2Documento10 páginasInforme 2 QG2Carlos Cesar Lopez SuarezAún no hay calificaciones
- Analisis Ion Cobalto QuimikkkkkkkkDocumento1 páginaAnalisis Ion Cobalto Quimikkkkkkkkpaula andrea araujoAún no hay calificaciones
- Práctica 8 QG2Documento4 páginasPráctica 8 QG2Dianne VanAún no hay calificaciones
- ENTREGABLEDocumento4 páginasENTREGABLEGabriela RodriguezAún no hay calificaciones
- Informe 3 Quimica LabDocumento7 páginasInforme 3 Quimica LabJuanAún no hay calificaciones
- 4.-Reacciones QímicasDocumento7 páginas4.-Reacciones QímicasgigigelpAún no hay calificaciones
- QG Equilibrio SolubilidadDocumento5 páginasQG Equilibrio SolubilidadMichele Tsuyoi RGAún no hay calificaciones
- Propiedades QuimicasDocumento6 páginasPropiedades QuimicasDANIELA GARCIA POSADAAún no hay calificaciones
- QGII Equilibrio Químico Richard MartínezDocumento5 páginasQGII Equilibrio Químico Richard Martínezfrancisco guamanAún no hay calificaciones
- Influencia de La Temperatura en El Equilibrio Químico: Experimento 1 ProblemaDocumento4 páginasInfluencia de La Temperatura en El Equilibrio Químico: Experimento 1 Problemaelias2222Aún no hay calificaciones
- Reacciones QuimicasDocumento14 páginasReacciones QuimicasAldoAún no hay calificaciones
- Práctica QuimicaDocumento5 páginasPráctica QuimicagonzalezrodriguezivannAún no hay calificaciones
- ACTIVIDAD #9 Reacciones QuímicasDocumento1 páginaACTIVIDAD #9 Reacciones QuímicasMatias MolleckerAún no hay calificaciones
- Equilibrio Químico InformeDocumento5 páginasEquilibrio Químico InformeIsa BerronesAún no hay calificaciones
- Repor Práctica 8 Influencia de La TemDocumento3 páginasRepor Práctica 8 Influencia de La TemAlexia LunaAún no hay calificaciones
- Quimica Del CobreDocumento11 páginasQuimica Del CobreRutth Apolinario RicoAún no hay calificaciones
- Efervescencia: ENERGIA (Luz y Calor) QUÍMICADocumento2 páginasEfervescencia: ENERGIA (Luz y Calor) QUÍMICAIsela LemusAún no hay calificaciones
- Método de Condensación Química para La Obtención de Sistemas ColoidalesDocumento8 páginasMétodo de Condensación Química para La Obtención de Sistemas ColoidalesRonal Vásquez BautistaAún no hay calificaciones
- Informe 7 Equilibrio QuimicoDocumento9 páginasInforme 7 Equilibrio QuimicoCamila SanchezAún no hay calificaciones
- Equilibrio Químico Iones y Ley de Acción de Masas.Documento7 páginasEquilibrio Químico Iones y Ley de Acción de Masas.Dayito PerezAún no hay calificaciones
- Informe Quimica 2Documento9 páginasInforme Quimica 2Evelin HidalgoAún no hay calificaciones
- Cambios Energeticos y Fuerzas IntermolecularesDocumento9 páginasCambios Energeticos y Fuerzas IntermolecularesMauricio Leguizamon Arredondo100% (1)
- Formacion de Complejos de CobaltoDocumento4 páginasFormacion de Complejos de CobaltoJulián IdárragaAún no hay calificaciones
- Formación de Complejos de CobaltoDocumento4 páginasFormación de Complejos de CobaltoMontserrat CartagenaAún no hay calificaciones
- Practica 8Documento4 páginasPractica 8Fernando PilónAún no hay calificaciones
- 3esofq SV Es Ud06 SolDocumento10 páginas3esofq SV Es Ud06 Solrosa100% (3)
- Tipos de Reacciones QuimicasDocumento8 páginasTipos de Reacciones QuimicasLeydi BautistaAún no hay calificaciones
- Copia de Práctica - Factores Que Afectan Al Equilibrio - Documentos de GoogleDocumento5 páginasCopia de Práctica - Factores Que Afectan Al Equilibrio - Documentos de GooglecristhianAún no hay calificaciones
- Reporte Practica 8Documento6 páginasReporte Practica 8ANDREA MARTINEZ BECERRILAún no hay calificaciones
- InformeDocumento4 páginasInformeDavid Alexander CastroAún no hay calificaciones
- QuímicaDocumento5 páginasQuímicaricardo ruedaAún no hay calificaciones
- Reacciones ReversiblesDocumento6 páginasReacciones ReversiblesALBERTO_GALVEZ0% (1)
- Laboratorio QuimicaDocumento3 páginasLaboratorio QuimicaFernando NavarreteAún no hay calificaciones
- REPORTE 5 QG UsacDocumento13 páginasREPORTE 5 QG UsacJnnrshAún no hay calificaciones
- Laboratorio #6 de Inorganica IDocumento10 páginasLaboratorio #6 de Inorganica IJuan Diego TrujilloAún no hay calificaciones
- Laboratorioa 5-Experimento 3'''Documento1 páginaLaboratorioa 5-Experimento 3'''Aldair Mejia CanoAún no hay calificaciones
- Informe de Lab Oratorio 6 Des Quc3admicasDocumento6 páginasInforme de Lab Oratorio 6 Des Quc3admicasAndaleitor RapSoulAún no hay calificaciones
- Exercicios de Aula UD4 - SOLUCIÓNSDocumento4 páginasExercicios de Aula UD4 - SOLUCIÓNSPaula Ramos VilarAún no hay calificaciones
- Sem07 - Práctica #6 - Guía Reacciones Químicas PDFDocumento12 páginasSem07 - Práctica #6 - Guía Reacciones Químicas PDFJhon F.Aún no hay calificaciones
- Equilibrio KC KP y KsDocumento42 páginasEquilibrio KC KP y KsJuan Pedro Ateneo FormacionAún no hay calificaciones
- Cuestiones y Problemas Del Tema 6: Equilibrio QuímicoDocumento21 páginasCuestiones y Problemas Del Tema 6: Equilibrio QuímicoBlueStorsAún no hay calificaciones
- Comprobación de Las Leyes de WernerDocumento9 páginasComprobación de Las Leyes de WernerBelén TapiaAún no hay calificaciones
- Informe 7-8Documento4 páginasInforme 7-8Mariana Rosiles GarcíaAún no hay calificaciones
- Explicación de La Práctica 8, Influencia de La Temp en El EQ - 2022-2Documento5 páginasExplicación de La Práctica 8, Influencia de La Temp en El EQ - 2022-2Luis Mario 607 Vasquez RomeroAún no hay calificaciones
- Balance de materia orientado a procesosDe EverandBalance de materia orientado a procesosAún no hay calificaciones
- Conocimiento Humano y Conocimiento AnimalDocumento19 páginasConocimiento Humano y Conocimiento AnimalcvcvcccccrvcfAún no hay calificaciones
- Guardini - Quien Es El HombreDocumento3 páginasGuardini - Quien Es El HombrecvcvcccccrvcfAún no hay calificaciones
- Jorge EdgarDocumento5 páginasJorge EdgarcvcvcccccrvcfAún no hay calificaciones
- Guardini - Quien Es El HombreDocumento3 páginasGuardini - Quien Es El HombrecvcvcccccrvcfAún no hay calificaciones
- La VidaDocumento11 páginasLa VidacvcvcccccrvcfAún no hay calificaciones
- Antropología Filosófica - Vida Vegetativa, Sensitiva, Intelectiva, VolitivaDocumento42 páginasAntropología Filosófica - Vida Vegetativa, Sensitiva, Intelectiva, VolitivacvcvcccccrvcfAún no hay calificaciones
- Medicina RomanaDocumento5 páginasMedicina RomanacvcvcccccrvcfAún no hay calificaciones
- Licceo de Costa RicaDocumento4 páginasLicceo de Costa RicacvcvcccccrvcfAún no hay calificaciones
- Pascual DoradoDocumento1 páginaPascual DoradocvcvcccccrvcfAún no hay calificaciones
- Cuestionario 2Documento5 páginasCuestionario 2cvcvcccccrvcfAún no hay calificaciones
- MexicoDocumento74 páginasMexicocvcvcccccrvcfAún no hay calificaciones
- Grupos Quimica InvestigaciónDocumento4 páginasGrupos Quimica InvestigacióncvcvcccccrvcfAún no hay calificaciones
- Práctica 3 - Secuenciales Variables y OperadoresDocumento2 páginasPráctica 3 - Secuenciales Variables y OperadorescvcvcccccrvcfAún no hay calificaciones
- Historia de La Filosofía AntiguaDocumento8 páginasHistoria de La Filosofía AntiguaJose Miguel Gallegos HuamanAún no hay calificaciones
- Sesion 3Documento13 páginasSesion 3cvcvcccccrvcfAún no hay calificaciones
- Dubai NuevoDocumento39 páginasDubai NuevocvcvcccccrvcfAún no hay calificaciones
- Ind - Manual de QuimicaDocumento5 páginasInd - Manual de QuimicacvcvcccccrvcfAún no hay calificaciones