Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Reaccion Homogenea Hidrolisis Anhidrido Acetico
Cargado por
Diana RubiTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Reaccion Homogenea Hidrolisis Anhidrido Acetico
Cargado por
Diana RubiCopyright:
Formatos disponibles
lOMoARcPSD|807865
Reacción Homogénea ( Hidrólisis Anhídrido Acético)
Laboratorio de Análisis Instrumental (Universidad Autónoma Metropolitana)
StuDocu no está patrocinado ni avalado por ningún colegio o universidad.
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
HIDRÓLISIS (FORMACIÓN DE ANHÍDRIDO ACÉTICO)
Laboratorio de Ciencias II, Universidad Autónoma Metropolitana
Unidad Cuajimalpa. Licenciatura en Ingeniería Biológica.
Email:
Equipo #1 Fecha: 14-Enero-2020 Rev:1
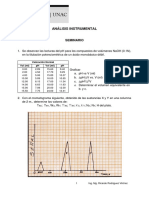
RESUMEN:
Se llevó a cabo la hidrólisis de Ácido Acético. Para ello, los equipos a utilizar, se calibraron y
prepararon para su utilización. Para el Potenciómetro marca conductronic modelo p45. Así
mismo, se calibró el equipo para poder obtener el valor de pH en las sustancias a trabajar.
Posteriormente, se preparó la solución de 9.63 mL de Ácido Acético en un matraz aforado de
500 mL, el cual se llevó al aforo con agua destilada. Se inició el cronómetro para recolectar
los datos del pH y la conductividad que emite. Tomando nota durante 40 minutos. De esta
misma solución, se prepararon concentraciones desde 0.1 M hasta 0.4 M. De los cuales se
midió la conductividad y su pH usando el mismo procedimiento anterior.
ABSTRACT:
An acetic acid hydrolysis was carried out. For this, the equipment to be used was calibrated
and prepared for its use. For the potentiometer brand conductronic model p45. Likewise, the
equipment was calibrated to obtain the pH value in the substances to be worked.
Subsequently, the 9.63 mL solution of Acetic Acid was prepared in a 500 mL volumetric
flask, which was brought to the capacity with distilled water. The stopwatch was started to
collect the pH and conductivity data it emits. Taking note for 40 minutes.
From this same solution, concentrations from 0.1 M to 0.4 M. were prepared, of which the
conductivity and its pH were measured using the same procedure above.
INTRODUCCIÓN
El anhídrido acético, es uno de los anhídridos carboxílicos más simples. Con fórmula química
(CH3CO)2O. Es un líquido incoloro que huele fuertemente a vinagre (ácido acético) debido a
su reacción con la humedad del aire. El anhídrido acético fue sintetizado por primera vez por
C. F. Gerhardt a partir de cloruro de benzoilo y acetato de potasio. Hoy en día es uno de los
.
intermedios orgánicos más importantes en la industria petroquímica [1]
El anhídrido acético se disuelve en agua hasta aproximadamente un 2,6% (m/m). Sin
embargo, una solución acuosa de anhídrido acético no es estable porque éste descompone en
unos pocos minutos (el tiempo exacto depende de la temperatura) en una solución de ácido
acético [2] .
La hidrólisis del anhídrido acético produce ácido acético,mejor conocido como ácido
metilencarboxílico, se puede encontrar en forma de ion acetato. Es una reacción química
donde los anhídridos reaccionan con agua para dar ácidos carboxílicos. Al ser disueltas en
agua, sus iones constituyentes se combinan con los iones hidronio u oxonio, H3O+ o bien con
los iones hidroxilo, OH-, o ambos (puede decirse que el agua reacciona "rompiendo el
compuesto").
Por lo tanto se debe de obtener el porcentaje de conversión de anhídrido acético a ácido
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
acético mediante una hidrólisis, en la que se debe de obtener un registro de la conductividad,
la temperatura y el pH en periodos de tiempo.
EXPERIMENTACIÓN
Materiales:
● 6 Vasos de precipitados de 250 ml ● 3 Matraces aforados de 100 ml
● 2 Vasos de precipitados de 500 ml ● 2 Vasos de precipitado de 10 ml
● 1 Matraz aforado de 500 ml ● 5 Vaso de precipitado de 100 ml
● 2 Matraz aforado de 250 ml ● 2 Charola
● 3 Pipetas graduadas de 10 ml ● 2 Espátula
● 1 Potenciómetro conductronic ● Maskintape
modelo p45 ● 1 probeta de 50 ml
● 1 Agitador magnético, Termómetro ● 2 pipetas de 20 ml.
● Parrilla, Propipetas
METODOLOGÍA
Curva de calibración
En los matraces aforados se prepararon soluciones de anhídrido acético en las siguientes
concentraciones 0.4 M, 0.3 M 0.2 M 0.1 M. como se muestra en la tabla 1.
Se calibró el conductímetro con una solución buffer de Cloruro de potasio KCL al 0.01 para
medir la conductividad de las soluciones.
Reacción homogénea
Prepara 500 mL de una solución al 0.2 M de Anhídrido Acético en H2O: En un matraz
aforado de 500ml agregar 9.63 mL AA y aforar con H2O a temperatura y presión ambiente e
iniciar el cronómetro.
Vertir la solución en un vaso de precipitado de 600 mL y agitar Se encendió el equipo, se
reguló la agitación de R1 y R2 así como los flujos de entrada a R1 (Ver Tabla 1). Se colocó el
conductímetro portátil dentro de R1, y se usó para R2 el conductímetro integrado en el
equipo.
Los valores de conductividad se registraron en intervalos de tiempo de 1 minuto hasta que la
reacción alcanzó el estado estacionario mientras temperatura y pH por 40 min en intervalos
de acuerdo con la tabla 2.
RESULTADOS Y DISCUSIÓN DE RESULTADOS:
Durante la realización de esta práctica, se logró obtener con éxito la conversión de anhídrido
acético a ácido acético mediante una hidrólisis y llevar los registros de: conductividad pH y
temperatura. Para llevar a cabo nuestra hidrólisis se hicieron los siguientes cálculos.
Cálculos:
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
Datos
● 0.2 M de A,A à 0.2 (mol/L) de A,A.
● ρ(A,A): 1.08x10-3 (g/L).
● PM(A,A): 102.1 (g/mol).
● 0.5 L de Solución.
Moles: (0.2 mol/L) * (0.5 L
)= 0.1 mol de A,A.
Masa: (0.1 m
ol A,A)(102.1 g/mol A,A)= 10.21 g A,A.
Volumen: (10.21 g A,A/1.08 g/mol A,A)= 9.45 mL de A,A 500 mL de H2O.
[(9.45 mL de A,A)(100%)/(98%)]= 9.64 mL de A,A
PH: Podemos ver en la Tabla 2, que nuestro PH cambió drásticamente en el intervalo de
14 minutos a 16 minutos, esto se debe a que el Potenciómetro no daba las cantidades
correctas por lo que después de los 14 minutos de registro el equipo prefirió cambiar el
método de medición de usar el Potenciómetro a usar Tiras Reactivas al PH para así
tener una medición correcta.
Curva de Calibración:
Al haber logrado nuestra hidrólisis, con ayuda de una solución b uffer de Cloruro de
potasio KCL al 0.01 teniendo así los resultados de nuestra Tabla 1 que será expresada
en la siguiente gráfica.
Concentración de Ácido y Anhídrido
Para sacar nuestra concentración de
AcAc usamos los datos de nuestra
Tabla 1
Con la ayuda del Software Excel
obtuvimos la siguiente ecuación de la
recta, como se puede observar en la
gráfica 2.
En el siguiente caso que es la
concentración del A,A se obtuvo su
concentración gracias a la reacción la
cual nos dice que por cada 2
moléculas de AcAc hay 1 molécula de
A,A.
Así como en la siguiente gráfica se muestra la generación de ácido acético y la
disminución de anhídrido acético
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
Caso 1: Donde la conductividad es
igual a 429(mS/cm)
Concentración de AcAc =
[(0.0006)*(429)]-(0.201)
Concentración de AcAc = 0.0564
0.06
Concentración de A,A en el caso 1=
[0.201-(0.06/2)]
Concentración de A,A en el caso 1=
0.171
Para la hidrólisis del anhídrido
acético se midió la conductividad, ph
y temperatura utilizando un potenciómetro en la solución dándole prioridad a la primera, esta
se midió en intervalos de tiempo (0,5,6,8,10,12….) en minutos hasta que el valor no
presentará un cambio significativo, de igual modo usamos escalas de concentración
molar(0.1, 0.2, 0.4,) .
Como se muestra en resultados la conductividad aumenta de manera exponencial, en los
intervalos de 2 minutos el incremento era considerablemente alto, cuando aumentamos el
tiempo a 5 minutos su incremento había disminuido. La temperatura no tuvo cambios
significativos en cada intervalo, llegando a aumentar un grado durante todo el tiempo que se
elaboró la práctica.
En la medición de pH en un comienzo usamos un pHmetro este nos daba valores de pH muy
altos en donde no concordaba por que los resultados indicaba que era una solución básica; al
notar esto utilizamos papel pH y nuestros resultados eran más coherentes ya que era una
ácido.
BIBLIOGRAFÍA:
[1]
Held, H., Rengstl, A. and Mayer, D. 2000. Acetic Anhydride and Mixed Fatty Acid Anhydrides.
Ullmann's Encyclopedia of Industrial Chemistry.
2 Celanese acetyl intermediates. (2011). Page 1 Product Description and Handling GuideAcetic
Anhydride. 10 de enero del 2020, de celanese acetyl intermediates Sitio web:
https://www.celanese.com/sitecore%20modules/web/-/media/Intermediate%20Chemistry/Files/Produ
ct%20Descriptions/Product_Description_and_Handling_Guide-Acetic_Anhydride.pdf .
ANEXO A: tablas generadas
Concentración de AcAc (mol/L) Conductividad (mS/cm) pH
0.1 463 4
0.2 654 4
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
0.3 776 4
0.4 943 4
agua 20 7
Tabla 3: Concentraciones totales de AA y
AcAc
Concentración Concentración de
Tiemp Conductivida Temperatura pH
AA (M) AcAc (M)
o d (mS/cm) (°C)
0.17 0.06
(min)
0 34 16 9 0.145 0.11
5 429 16 9.2 0.125 0.15
6 510 16 9.5 0.105 0.19
0.09 0.22
8 580 16 9.7
0.075 0.25
10 654 16 9.7
0.065 0.27
12 708 16 9.5
0.055 0.29
14 754 16 9.7
0.045 0.31
16 790 17 3
0.04 0.32
18 823 17 4
0.035 0.33
20 848 17 4
0.035 0.33
22 868 17 4
0.025 0.35
24 884 17 4
0.02 0.36
25 893 17 4
0.015 0.37
30 920 17 4
35 938 17 4
40 948 17 4
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
ANEXO B: hojas de seguridad
ANHÍDRIDO ACÉTICO
Formula química: C4H6O3
● Propiedades físicas y químicas
Estado físico: Líquido similar al agua
Apariencia y olor: Incoloro, con fuerte olor a vinagre
Concentración: 99% y 90%
PH:1
Punto de inflamación: 49°C
Temperatura de autoignición: 330°C
Peligros de fuego o explosión: Necesita ser calentado para que sus vapores enciendan. Puede
reaccionar violentamente con materiales oxidantes, por ejemplo con ácido acético.
Presión de vapor a 20°C: 11.4mmHg
Densidad de vapor: 3.52
Densidad a 20°C: 1.08
Solubilidad en agua y otros solventes: Completamente miscible en agua. Miscible en alcohol,
glicerina, éter.
● Control de exposición/ protección ambiental
Medidas para reducir la posibilidad de exposición: En los lugares de trabajo debe haber buena
ventilación, ya sea natural o forzada.
Protección respiratoria: Proteja las vías respiratorias con filtros para gases ácidos y vapores orgánicos.
Guantes de protección: Use guantes de puño largo, de neopreno u otro material plástico o de goma.
Protección de la vista: Proteja la vista con anteojos de protección química
Otros equipos de protección: Si se anticipa un posible contacto con el producto, proteja todo el cuerpo
y use botas de neopreno.
Métodos de limpieza: Neutralice el material derramado con cenizas de soda, o carbonato de calcio
molido. El líquido puede ser absorbido con arena o con polvo de cemento. La mezcla resultante puede
ser recogida y llevada a un horno para su incineración.
Condiciones de almacenamiento: Mantenga la temperatura de almacenamiento sobre el punto de
congelamiento (16.7°C) ya que el material se expande al cristalizar.
ÁCIDO ACÉTICO
Fórmula química: C2H4O2
● Propiedades físicas y químicas
Estado físico: Líquido higroscópico
Apariencia y olor: Incoloro
Inodoro, olor punzante (a vinagre)
Concentración: 99% y 90%
Punto de inflamación: 39°C
Temperatura de autoignición: 485°C
Presión de vapor a 20°C: 1.5 kPa
Densidad de vapor: 2.1
Densidad a 20°C: 1.02
Descargado por abi mon (cerezarubi92@gmail.com)
lOMoARcPSD|807865
● Control de exposición/ protección ambiental
Medidas para reducir la posibilidad de exposición: En los lugares de trabajo debe haber buena
ventilación, ya sea natural o forzada.
Protección respiratoria: Proteja las vías respiratorias con filtros para gases ácidos y vapores orgánicos.
Guantes de protección: Use guantes de puño largo, de neopreno u otro material plástico o de goma.
Protección de la vista: Proteja la vista con anteojos de protección química.
Otros equipos de protección: Si se anticipa un posible contacto con el producto, proteja todo el cuerpo
y use botas de neopreno.
Condiciones de almacenamiento: Almacenar en un área sin acceso a desagües o alcantarillas.
Descargado por abi mon (cerezarubi92@gmail.com)
También podría gustarte
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Cuadernillo MatematicasDocumento86 páginasCuadernillo MatematicasVictor Alberto Tezoco0% (3)
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- TITULACIÓN POTENCIOMÉTRICA ACIDO Oxalico Final FinalDocumento12 páginasTITULACIÓN POTENCIOMÉTRICA ACIDO Oxalico Final Finalalejandro0% (1)
- Informe 6Documento13 páginasInforme 6ivan1989104Aún no hay calificaciones
- LitografiaDocumento8 páginasLitografiaJavier Arancibia MartinezAún no hay calificaciones
- Valoraciones Potenciométricas de Muestras de Carbonato de SodioDocumento11 páginasValoraciones Potenciométricas de Muestras de Carbonato de SodioingrossAún no hay calificaciones
- Cinetica Química EjerciciosDocumento8 páginasCinetica Química EjerciciosJose LozanoAún no hay calificaciones
- DETERMINACIÓN DE Na Y K EN UNA BEBIDA HIDRATANTE POR ESPECTROSCOPIA DE ABSORCIÓN ATÓMICADocumento4 páginasDETERMINACIÓN DE Na Y K EN UNA BEBIDA HIDRATANTE POR ESPECTROSCOPIA DE ABSORCIÓN ATÓMICAAndrew Serra100% (1)
- Caso Douglas S.ADocumento4 páginasCaso Douglas S.AMerly Celeste Ramos PardaveAún no hay calificaciones
- Higham Tom - El Mundo Antes de NosotrosDocumento278 páginasHigham Tom - El Mundo Antes de NosotrosGerardo Ernesto Lugo Olivas100% (1)
- Titulacion Acido-Base Usando Un Electrodo de PHDocumento7 páginasTitulacion Acido-Base Usando Un Electrodo de PHAlejandro CastellanosAún no hay calificaciones
- Titulacion ConducDocumento11 páginasTitulacion ConducRick RodriguezAún no hay calificaciones
- Actividades de Respeto y ToleranciaDocumento10 páginasActividades de Respeto y ToleranciaJuanAntonioAún no hay calificaciones
- Echo-Actividad de Puntos Evaluables - Escenario 6 - Primer Bloque-Ciencias Basicas - Virtual - Herramientas para La ProductividadDocumento5 páginasEcho-Actividad de Puntos Evaluables - Escenario 6 - Primer Bloque-Ciencias Basicas - Virtual - Herramientas para La ProductividadDanielaAún no hay calificaciones
- Ciencias 4Documento227 páginasCiencias 4Paola Sepúlveda Vargas100% (5)
- Conductimetria RobinsonDocumento9 páginasConductimetria RobinsonKervin A. Pérez M.Aún no hay calificaciones
- Laboratorio de Ingenieria Quimica 1Documento4 páginasLaboratorio de Ingenieria Quimica 1Xavier CrAlAún no hay calificaciones
- Practica FQ #10 y 11Documento11 páginasPractica FQ #10 y 11Fabiola100% (1)
- Titulaciones CoulombimetricasDocumento6 páginasTitulaciones CoulombimetricasNatalia ValenciaAún no hay calificaciones
- Practica#2 Oxidacion Del Ioduro Con Persulfato Grupo 1Documento10 páginasPractica#2 Oxidacion Del Ioduro Con Persulfato Grupo 1Priscila SaavedraAún no hay calificaciones
- Practica 5-Tanque Agitado ContinuoDocumento8 páginasPractica 5-Tanque Agitado ContinuoLeinaAlexandraLópezAún no hay calificaciones
- Practica 5-Tanque Agitado ContinuoDocumento7 páginasPractica 5-Tanque Agitado ContinuoClaudia GonzalesAún no hay calificaciones
- Informe 1 Ingenieria de ReaccionesDocumento19 páginasInforme 1 Ingenieria de ReaccionesAdeleyda Tineo YucraAún no hay calificaciones
- Informe5 FQDocumento14 páginasInforme5 FQAngela Pinedo FAún no hay calificaciones
- Informe 5 TAC 1Documento9 páginasInforme 5 TAC 1Ana Belen Zurita100% (1)
- GL6 2012Documento3 páginasGL6 2012Mariangel GüilAún no hay calificaciones
- Ejercicios 2. Acidez, Alcalinidad y DurezaDocumento6 páginasEjercicios 2. Acidez, Alcalinidad y DurezaJeanPierreAún no hay calificaciones
- Aplicación de Medidas Conductimétricas en La Determinación de Variables Fisicoquímicas para Diferentes ElectrolitosDocumento8 páginasAplicación de Medidas Conductimétricas en La Determinación de Variables Fisicoquímicas para Diferentes ElectrolitosNahomi CordobaAún no hay calificaciones
- 1QUI01-Química 1 (1) - 26Documento1 página1QUI01-Química 1 (1) - 26lomade2224Aún no hay calificaciones
- Practica 1 EstandarizaconDocumento5 páginasPractica 1 EstandarizaconALEX STIVEN VALENCIA FERNANDEZAún no hay calificaciones
- Informe 2 Lab. FisicoquimicaDocumento5 páginasInforme 2 Lab. FisicoquimicaAmanda ArizaAún no hay calificaciones
- S1501072 LaboratorioReactoresQuimicosDocumento42 páginasS1501072 LaboratorioReactoresQuimicosJhon DiazAún no hay calificaciones
- Guia de Ejercicios de Cinetica Química (Ceing 2021)Documento8 páginasGuia de Ejercicios de Cinetica Química (Ceing 2021)jose jimenezAún no hay calificaciones
- Lab 7Documento23 páginasLab 7delacruztifanny2Aún no hay calificaciones
- GUIA de LAB #7 EQUILIB QUÍM BQU01Documento12 páginasGUIA de LAB #7 EQUILIB QUÍM BQU01Sebastian MQAún no hay calificaciones
- Titulación Potenciométrica de Una Mezcla de Na CO Y Nahco Fecha: Martes 20 de Octubre Del 2020 Incógnita: Fundamento TeóricoDocumento4 páginasTitulación Potenciométrica de Una Mezcla de Na CO Y Nahco Fecha: Martes 20 de Octubre Del 2020 Incógnita: Fundamento TeóricoDaniela CamposAún no hay calificaciones
- Bqu01 Lab #7 (Equilib Químico)Documento11 páginasBqu01 Lab #7 (Equilib Químico)Brayan Rivera ArgumedoAún no hay calificaciones
- Laboratorio de ReactoresDocumento2 páginasLaboratorio de Reactoresingrid_brigithAún no hay calificaciones
- QM-2512 Tarea 1Documento2 páginasQM-2512 Tarea 1Johan RojasAún no hay calificaciones
- Practica 4Documento4 páginasPractica 4abiAún no hay calificaciones
- Reporte Q.A 2Documento8 páginasReporte Q.A 2MisaelAún no hay calificaciones
- CÁLCULOS Coeficiente de RepartoDocumento8 páginasCÁLCULOS Coeficiente de RepartoLeandroFuentesMedina0% (1)
- Seminario de Problemas para Examen Final PDFDocumento4 páginasSeminario de Problemas para Examen Final PDFCarlos Baca SanchezAún no hay calificaciones
- Titulación ConductimétricaDocumento14 páginasTitulación ConductimétricachinozkarAún no hay calificaciones
- Pre-Informe AdsorcionDocumento18 páginasPre-Informe AdsorcionLuisa MedinaAún no hay calificaciones
- Practica Segundo, Parcial Grupo CDocumento6 páginasPractica Segundo, Parcial Grupo CMarvin Ceballos0% (1)
- P3 Liq 1703Documento10 páginasP3 Liq 1703Jose Armando JimenezAún no hay calificaciones
- Guia 7 3ESTEQUIOMETRIADocumento4 páginasGuia 7 3ESTEQUIOMETRIAbernardo hurozAún no hay calificaciones
- Guia LFQ 4 2021Documento5 páginasGuia LFQ 4 2021HIUSTON REYMUNDO FLORESAún no hay calificaciones
- Oxidacion Del Yoduro Con Peroxido de Hidrogeno PDFDocumento8 páginasOxidacion Del Yoduro Con Peroxido de Hidrogeno PDFAndrew SilvaAún no hay calificaciones
- Practica Reacción de Saponificación Del Acetato-De EtiloDocumento2 páginasPractica Reacción de Saponificación Del Acetato-De EtiloyaneliAún no hay calificaciones
- P3 LiqDocumento8 páginasP3 LiqCarlos MeunierAún no hay calificaciones
- Guia LFQ 3 20172Documento5 páginasGuia LFQ 3 20172Danny OnallAún no hay calificaciones
- Practica#5.RTAC. Grupo 3Documento8 páginasPractica#5.RTAC. Grupo 3LeinaAlexandraLópezAún no hay calificaciones
- Informe 2 - Absorción AtómicaDocumento9 páginasInforme 2 - Absorción AtómicaIveth Patricia Betacourth OrobioAún no hay calificaciones
- Cinética de La Reacción de Oxidación Del Alcohol Bencílico Por PermanganatoDocumento4 páginasCinética de La Reacción de Oxidación Del Alcohol Bencílico Por PermanganatoJuan Carlos GAún no hay calificaciones
- Guia Eq 2019 CorregidaDocumento29 páginasGuia Eq 2019 CorregidaAaron B. Quispe RomeroAún no hay calificaciones
- Informe 13-Conductividad-LfqaiiDocumento10 páginasInforme 13-Conductividad-LfqaiiÁlvaro Olórtegui IglesiasAún no hay calificaciones
- Practica-6 Reactor TubularDocumento9 páginasPractica-6 Reactor TubularPriscila Saavedra100% (1)
- Mec - SapoDocumento11 páginasMec - SapoAndres PerezAún no hay calificaciones
- Ejemplo SaponificacionDocumento15 páginasEjemplo SaponificacionHugo CastorenaAún no hay calificaciones
- Boletin Tema 3-1920Documento3 páginasBoletin Tema 3-1920manu regueiroAún no hay calificaciones
- Problemas de Aplicación Reactores IdealesDocumento4 páginasProblemas de Aplicación Reactores IdealesjorgeAún no hay calificaciones
- Quimica OrganicaDocumento38 páginasQuimica OrganicaDiana RubiAún no hay calificaciones
- Quimica OrganicaDocumento77 páginasQuimica OrganicaDiana RubiAún no hay calificaciones
- Compuestos NitrogenadosDocumento80 páginasCompuestos NitrogenadosDiana RubiAún no hay calificaciones
- Quimica OrganicaDocumento39 páginasQuimica OrganicaDiana RubiAún no hay calificaciones
- SaludDocumento3 páginasSaludDiana RubiAún no hay calificaciones
- Proteccion Social en SaludDocumento3 páginasProteccion Social en SaludDiana RubiAún no hay calificaciones
- Quimica OrganicaDocumento26 páginasQuimica OrganicaDiana RubiAún no hay calificaciones
- FQ Exposición 2 RevisonDocumento17 páginasFQ Exposición 2 RevisonDiana RubiAún no hay calificaciones
- Teorias EnfermeriaDocumento18 páginasTeorias EnfermeriaDiana RubiAún no hay calificaciones
- Teorias EnfermeriaDocumento4 páginasTeorias EnfermeriaDiana RubiAún no hay calificaciones
- Familias y Protagonistas)Documento2 páginasFamilias y Protagonistas)Diana RubiAún no hay calificaciones
- Teorias de EnfermeriaDocumento24 páginasTeorias de EnfermeriaDiana RubiAún no hay calificaciones
- Determinación Del Contenido de Azúcares ReductoresalumnosDocumento5 páginasDeterminación Del Contenido de Azúcares ReductoresalumnosDiana RubiAún no hay calificaciones
- AZUCARESDocumento8 páginasAZUCARESDiana RubiAún no hay calificaciones
- Unidad Ii Disoluciones Quimicas-1Documento55 páginasUnidad Ii Disoluciones Quimicas-1Angelli Veronica Arias HerreraAún no hay calificaciones
- Tarea 1 Franco Garcia Alejandra, Inclan Rubi DianaDocumento1 páginaTarea 1 Franco Garcia Alejandra, Inclan Rubi DianaDiana RubiAún no hay calificaciones
- Problemas de Procesos TermodinámicosDocumento10 páginasProblemas de Procesos TermodinámicosDiana RubiAún no hay calificaciones
- Clase1 2 Repaso de Termodinámica 29y31mar21alumnosDocumento24 páginasClase1 2 Repaso de Termodinámica 29y31mar21alumnosDiana RubiAún no hay calificaciones
- Unidad Ii Disoluciones Quimicas-1Documento55 páginasUnidad Ii Disoluciones Quimicas-1Angelli Veronica Arias HerreraAún no hay calificaciones
- Clase1 - Repaso de Termodinámica - 29mar21Documento17 páginasClase1 - Repaso de Termodinámica - 29mar21Diana RubiAún no hay calificaciones
- Clase 021Documento22 páginasClase 021Diana RubiAún no hay calificaciones
- Clase 3-Probabilidad (1) KKKDocumento16 páginasClase 3-Probabilidad (1) KKKDiana RubiAún no hay calificaciones
- Guia de Estudio Problemas 1parcialDocumento6 páginasGuia de Estudio Problemas 1parcialDiana RubiAún no hay calificaciones
- Procesos RestringidosDocumento9 páginasProcesos RestringidosDiana RubiAún no hay calificaciones
- Procesos RestringidosDocumento9 páginasProcesos RestringidosDiana RubiAún no hay calificaciones
- Equivalente Quimico Resumen PDFDocumento2 páginasEquivalente Quimico Resumen PDFAngel Vicente Sanchez PilcoAún no hay calificaciones
- Cap 1 V 2Documento29 páginasCap 1 V 2Neda Machicado TitoAún no hay calificaciones
- Prueba Diagnóstica Del Área de Matemática - 5Documento11 páginasPrueba Diagnóstica Del Área de Matemática - 5Jose Manuel MatematicAún no hay calificaciones
- LEISHMANIASISDocumento93 páginasLEISHMANIASISJOHANNA SANTANA100% (1)
- 8 Sin Marca de AguaDocumento194 páginas8 Sin Marca de Aguaalexanderlopez504teletrabajoAún no hay calificaciones
- Syllabus Fundamentos de Mercadeo 100504A-224Documento15 páginasSyllabus Fundamentos de Mercadeo 100504A-224DIANA ANGELICA CARRANZA GUAYARAAún no hay calificaciones
- El Rosario (Florence L. Barclay)Documento222 páginasEl Rosario (Florence L. Barclay)Jesús AmadoAún no hay calificaciones
- Indicador de Presión y Vacio Transformadores Mayores A 2500 kVA o NBAI Mayor A 2000kV PDFDocumento1 páginaIndicador de Presión y Vacio Transformadores Mayores A 2500 kVA o NBAI Mayor A 2000kV PDFromoAún no hay calificaciones
- Tema: Redes Virtuales A La Actualidad, Reconociendo Sus RiesgosDocumento3 páginasTema: Redes Virtuales A La Actualidad, Reconociendo Sus RiesgosVane VelaAún no hay calificaciones
- INVENTARIO Laptop LENOVO TIC 01Documento4 páginasINVENTARIO Laptop LENOVO TIC 01Antonio Barrios JorgeAún no hay calificaciones
- Semana 9 - Co CreaciónDocumento52 páginasSemana 9 - Co CreaciónOSCAR ADRIAN MARCAÑAUPA RICAPAAún no hay calificaciones
- Análisis de Vibraciones ISO Categoría I: Certificación IMMP Según ISO 18436-2Documento1 páginaAnálisis de Vibraciones ISO Categoría I: Certificación IMMP Según ISO 18436-2Jercy SanchezAún no hay calificaciones
- Diseño Textil y Moda 0.3Documento2 páginasDiseño Textil y Moda 0.3Jose Manuel Rosario TejadaAún no hay calificaciones
- ENCOFRADODocumento26 páginasENCOFRADORoberth ChombopAún no hay calificaciones
- Diferentes Tipos de Pastillas de FrenoDocumento2 páginasDiferentes Tipos de Pastillas de FrenoEvelyn EspirituAún no hay calificaciones
- Parcial GERENCIA ESTRATEGICA #1Documento7 páginasParcial GERENCIA ESTRATEGICA #1Angel MiguelAún no hay calificaciones
- Exposicion TH 040Documento18 páginasExposicion TH 040Sebastian Pedraza RamirezAún no hay calificaciones
- Axiomas de Los Números RealesDocumento9 páginasAxiomas de Los Números RealesAMYNNXXXXAún no hay calificaciones
- CUNICULTURADocumento15 páginasCUNICULTURAKatly Cartolin BarronAún no hay calificaciones
- Programacion de Obra ActualizadoDocumento1 páginaProgramacion de Obra ActualizadoDaniel SánchezAún no hay calificaciones
- Modelo Examen - Estructura Economica Territorial UNSAMDocumento2 páginasModelo Examen - Estructura Economica Territorial UNSAMMarlene StemkeAún no hay calificaciones
- Informe #05 CalicatasDocumento11 páginasInforme #05 CalicatasJulio Cesar Ambrosio CamposAún no hay calificaciones
- UntitledDocumento226 páginasUntitledKim MAún no hay calificaciones
- Precursores de TGSDocumento6 páginasPrecursores de TGSPablo ArciniegaAún no hay calificaciones
- Sistema RespiratorioDocumento2 páginasSistema Respiratoriopaolufjfkfkjfjfjfjrja reyes saldañaAún no hay calificaciones
- El Transporte Argentino - Pág.19-42,51-66Documento41 páginasEl Transporte Argentino - Pág.19-42,51-66chinopatAún no hay calificaciones