Documentos de Académico
Documentos de Profesional
Documentos de Cultura
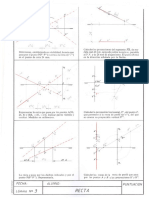
Solución Ejercicios Diedrico
Cargado por
Joel 10Descripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Solución Ejercicios Diedrico
Cargado por
Joel 10Copyright:
Formatos disponibles
DISTRIBUCIÓN ELECTRÓNICA 2ºBACH
TABLA PERIÓDICA
SOLUCIONES DE LOS EJERCICIOS DEL LIBRO
Página 72:
20. Orden creciente el tamaño de: Cu, Br, Ca, Cs y O
El radio atómico aumenta a medida que aumenta el periodo, ya que crece el número de
niveles y por tanto su tamaño. El O está en el periodo 2, el Ca, Cu, y Br en el periodo 4 y el Cs
en el 6. Por tanto el átomo más pequeños es el del O y el mayor el del Cs.
Los otros tres están en el mismo periodo, y el tamaño disminuye a medida que aumenta Z, ya
que para un mismo nivel, al aumentar Z, l aumenta tanto la carga nuclear como los electrones
de la periferia y esto hace que la fuerza sea mayor provocando una disminución del tamaño y
por lo tanto del radio. Luego
Cs > Ca > Cu > Br > 0
21. Ordenar, por orden creciente, el tamaño de los iones isoelectrónicos:
F-, Ne, Mg2+, Na+ y O2-
El tamaño de los aniones es mayor que el de los cationes. En el caso de los cationes al perder
electrones y mantener la carga nuclear aumenta la fuerza de atracción por lo que disminuye el
tamaño respecto al átomo neutro y en el caso de los aniones al ganar electrones en el mismo
nivel se producen fuerzas de repulsión y aumenta el tamaño.
ranión>rcation
Dentro de los cationes isoelectrónicos, en un mismo periodo, el tamaño disminuye al
aumentar Z, ya que se mantiene el mismo número de electrones y aumenta la carga
nuclear , aumenta la fuerza de atracción y el tamaño disminuye
Na+> Mg2+
En el caso de los aniones isoelectrónicos, en un mismo periodo, el tamaño disminuye con Z,
pues aumenta la carga nuclear y mantiene, en un mismo nivel, igual número de electrones.
O2- > F-
Luego el orden será:
Mg2+ < Na+ < Ne < F- < O2-
Página 74. EJERCICIO 25.
IES “ANTONIO CALVÍN” 1
DISTRIBUCIÓN ELECTRÓNICA 2ºBACH
TABLA PERIÓDICA
Ei1= 6,11 eV/partícula
Ei2= 11,87 eV/partícula
La suma de las dos energías de ionización es la que se necesita para que el Ca se convierta en
Ca2+
Ca → Ca2+ + 2e-
6,11 + 11,87 = 17,98 eV
19
1,6 · 10 J
17,98 eV · =2,88 · 10-18 J/átomo
eV
6,022·10 23 átomos J
20 g Ca · · 2,88 · 10 18
= 867,2 · 103 J
40 g Ca átomo
IES “ANTONIO CALVÍN” 2
También podría gustarte
- Ejercicio Resuelto 12 - AtomoDocumento1 páginaEjercicio Resuelto 12 - AtomovitoAún no hay calificaciones
- Actividad Propiedades Periodicas de Los ElementosDocumento6 páginasActividad Propiedades Periodicas de Los ElementosBRIAN JULIO SOLANOAún no hay calificaciones
- Sesion-06 EstructuraDocumento8 páginasSesion-06 EstructuraasdAún no hay calificaciones
- Propiedades químicas de la tabla periódica y tipos de enlaceDocumento12 páginasPropiedades químicas de la tabla periódica y tipos de enlaceMARCOS HUMBERTO GONZALES YUYASAún no hay calificaciones
- Guía Electroquímica (Conceptos Generales) PDFDocumento17 páginasGuía Electroquímica (Conceptos Generales) PDFKristofer BonillaAún no hay calificaciones
- ELECTROQUÍMICA - Chimborazo RosaDocumento19 páginasELECTROQUÍMICA - Chimborazo RosaMärïbël Č JërëzAún no hay calificaciones
- 01 - Propiedades PeriódicasDocumento40 páginas01 - Propiedades PeriódicasLuciaAngrigianiAún no hay calificaciones
- Celdas GalvanicasDocumento6 páginasCeldas GalvanicasJuan FranciaAún no hay calificaciones
- Pila VoltaicaDocumento12 páginasPila VoltaicaChava Martín GrimaldiAún no hay calificaciones
- Tema 3 Enlace QuimicoDocumento19 páginasTema 3 Enlace Quimicopaulagarcia343Aún no hay calificaciones
- 2.2.-A. - Enlaces IonicosDocumento13 páginas2.2.-A. - Enlaces IonicosIvonne De la RosaAún no hay calificaciones
- Enlace Ionico, CovalenteDocumento9 páginasEnlace Ionico, CovalenteFatima VillarAún no hay calificaciones
- 2 PAU EstructuraAtómicaClasificacionPeriódicaElementos Soluc - 211123 - 180129Documento24 páginas2 PAU EstructuraAtómicaClasificacionPeriódicaElementos Soluc - 211123 - 180129Anny SnyAún no hay calificaciones
- Pilas GalvanicasDocumento9 páginasPilas GalvanicasJuly Nym NeylaAún no hay calificaciones
- The HackerDocumento3 páginasThe Hackermaria eugeniaAún no hay calificaciones
- OxidaciónDocumento9 páginasOxidaciónRequeza WalterAún no hay calificaciones
- Celda Galvanik Clase MagistralDocumento6 páginasCelda Galvanik Clase MagistralAurienyerlis ZambranoAún no hay calificaciones
- Tema Enlace QuimicoDocumento26 páginasTema Enlace QuimicoliceomariaAún no hay calificaciones
- S14.s1 - Material - ElectroquímicaDocumento24 páginasS14.s1 - Material - ElectroquímicaJuanka RosalesAún no hay calificaciones
- Ejercicios Resueltos Del LibroDocumento7 páginasEjercicios Resueltos Del LibroDaniel Sopla CubasAún no hay calificaciones
- Laboratorio de Electroquimica N°2Documento11 páginasLaboratorio de Electroquimica N°2Alexander QuirozAún no hay calificaciones
- Notación de CeldaDocumento5 páginasNotación de CeldaAldo Benjamin Becerra GaytanAún no hay calificaciones
- Celdas Galvanicas de MetalesDocumento4 páginasCeldas Galvanicas de MetalesMarisabel Guanipa100% (1)
- Propiedades físicas y químicas de los elementosDocumento2 páginasPropiedades físicas y químicas de los elementosAldair MercadoAún no hay calificaciones
- Celda GalvánicaDocumento5 páginasCelda GalvánicaJosé Antonio García-Olveros GonzálezAún no hay calificaciones
- Tema 3 EnlaceDocumento34 páginasTema 3 Enlacejrb759Aún no hay calificaciones
- Enlace IonicoDocumento4 páginasEnlace Ionicomariliag730Aún no hay calificaciones
- Inf 8Documento8 páginasInf 8Yess Flores DelgadoAún no hay calificaciones
- Semana15 - ElectroquímicaDocumento56 páginasSemana15 - ElectroquímicaCALETF PIERO RODRIGUEZ CARRASCOAún no hay calificaciones
- 7.1 Semana 4 ElectroquimicaDocumento20 páginas7.1 Semana 4 ElectroquimicaFelix Lopez MurgaAún no hay calificaciones
- 4 - Propiedades Periódicas - PPSDocumento13 páginas4 - Propiedades Periódicas - PPSMajoAún no hay calificaciones
- Celda GalvánicaDocumento10 páginasCelda GalvánicaLilianaEstifaneChoqueAún no hay calificaciones
- Tabla Periódica - Propiedades PeriódicasDocumento28 páginasTabla Periódica - Propiedades PeriódicasCRISTIAN MARTINEZ OREAún no hay calificaciones
- Abbaschian R. Physical Metallurgy Principles 4ed., Capitulo 3 Español - (081-100)Documento20 páginasAbbaschian R. Physical Metallurgy Principles 4ed., Capitulo 3 Español - (081-100)Moisés Morera AlfaroAún no hay calificaciones
- Estructura Basica Del Atomo y Sus InteraccionesDocumento32 páginasEstructura Basica Del Atomo y Sus InteraccionesJUAN CAMILO RUIZ LINARESAún no hay calificaciones
- Tema 2 Enlace QuímicoDocumento24 páginasTema 2 Enlace QuímicoGuillermo Martínez RamónAún no hay calificaciones
- Modulo 8Documento12 páginasModulo 8RafaelAún no hay calificaciones
- Compuestos Ionicos Relación de RadiosDocumento6 páginasCompuestos Ionicos Relación de RadiosDario DoriaAún no hay calificaciones
- Asm-Semana 07 (Propiedades Periódicas)Documento20 páginasAsm-Semana 07 (Propiedades Periódicas)Jazmin Parí quispeAún no hay calificaciones
- UD1 - ABAU - Ejercicio 20 - SoluciónDocumento3 páginasUD1 - ABAU - Ejercicio 20 - SoluciónIago ArsequellAún no hay calificaciones
- Radio Atómico, Ionico y CovalenteDocumento10 páginasRadio Atómico, Ionico y CovalenteYahir BetancurAún no hay calificaciones
- Electroquimiica - ElectrolisisDocumento19 páginasElectroquimiica - ElectrolisisEncarnación Vicenta Sánche CuriAún no hay calificaciones
- Informe 6 FinalDocumento4 páginasInforme 6 Finalkaren giraldoAún no hay calificaciones
- Propiedades PeriodicasDocumento3 páginasPropiedades PeriodicasMatias BassoAún no hay calificaciones
- Presentacion Propiedades Periodica de Los ElementosDocumento26 páginasPresentacion Propiedades Periodica de Los ElementosEstefany PinedaAún no hay calificaciones
- Celda GalvánicaDocumento5 páginasCelda GalvánicaMcGyverAún no hay calificaciones
- 9 Demuestre Que El Tamaño de Los Átomos Decrece de Izquierda A Derecha Usando El Segundo Periodo de La Tabla PeriódicaDocumento4 páginas9 Demuestre Que El Tamaño de Los Átomos Decrece de Izquierda A Derecha Usando El Segundo Periodo de La Tabla PeriódicaYessid Páez NúñezAún no hay calificaciones
- Propiedades periódicasDocumento25 páginasPropiedades periódicasFidel GonzalezAún no hay calificaciones
- Celdas Electroquimicas DefinitivaDocumento4 páginasCeldas Electroquimicas DefinitivaANDERSON RUBIO CLEVESAún no hay calificaciones
- Ej SELECTIVIDAD Quimica TEMA 1Documento13 páginasEj SELECTIVIDAD Quimica TEMA 1Rodeo CrabAún no hay calificaciones
- Solucionario Taller QuímicaDocumento7 páginasSolucionario Taller QuímicaOwell Negrete BotoneroAún no hay calificaciones
- Ejercicios sobre radios atómicos, potenciales de ionización, electroafinidad y electronegatividadDocumento10 páginasEjercicios sobre radios atómicos, potenciales de ionización, electroafinidad y electronegatividadRogerAún no hay calificaciones
- Apuntes Enlace Quimico 2ºDocumento25 páginasApuntes Enlace Quimico 2ºbenedictAún no hay calificaciones
- 7reacciones Redox y 5 de NeutralizaciónDocumento25 páginas7reacciones Redox y 5 de NeutralizaciónJorgeMoralesAún no hay calificaciones
- 7 ReaccionesredoxDocumento15 páginas7 ReaccionesredoxMariana SofíaAún no hay calificaciones
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaDe EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaAún no hay calificaciones
- Diferencias TiemposDocumento2 páginasDiferencias TiemposJoel 10Aún no hay calificaciones
- Números ComplejosDocumento38 páginasNúmeros ComplejosJoel 10Aún no hay calificaciones
- Solución Ejercicios DiedricoDocumento2 páginasSolución Ejercicios DiedricoJoel 10Aún no hay calificaciones
- Ejercicio ACLDocumento4 páginasEjercicio ACLJoel 10Aún no hay calificaciones
- UbuntuDocumento18 páginasUbuntuJoel 10Aún no hay calificaciones
- El Desastre Perfecto, Noticias FilosofíaDocumento3 páginasEl Desastre Perfecto, Noticias FilosofíaJoel 10Aún no hay calificaciones
- Dibujo Técnico Sistema Diédrico Intersecciones PrácticaDocumento11 páginasDibujo Técnico Sistema Diédrico Intersecciones PrácticaAniSRodriguezAún no hay calificaciones
- Lamina 3 10 Diedrico Inicial ResueltasDocumento8 páginasLamina 3 10 Diedrico Inicial Resueltasisabel100% (2)
- Fuerzas gravitatorias y sus efectosDocumento2 páginasFuerzas gravitatorias y sus efectosJoel 10Aún no hay calificaciones
- Evolución para ModdleDocumento20 páginasEvolución para ModdleJoel 10Aún no hay calificaciones
- Fuerzas gravitatorias y sus efectosDocumento2 páginasFuerzas gravitatorias y sus efectosJoel 10Aún no hay calificaciones
- Pautas para Redactar Una DisertaciónDocumento2 páginasPautas para Redactar Una DisertaciónEduardo Salgado EnríquezAún no hay calificaciones
- La Caída Del Imperio Colonial y La Crisis Del 98Documento3 páginasLa Caída Del Imperio Colonial y La Crisis Del 98Mario Axel Becerra HerreraAún no hay calificaciones
- Ejercios Resueltos VariosDocumento60 páginasEjercios Resueltos VariosMacu DC DiazAún no hay calificaciones
- Biología 1 BachillerDocumento1 páginaBiología 1 BachillerJoel 10Aún no hay calificaciones
- Ecuaciones de DimensionDocumento7 páginasEcuaciones de DimensionDiego JaramilloAún no hay calificaciones
- La Caída Del Imperio Colonial y La Crisis Del 98Documento3 páginasLa Caída Del Imperio Colonial y La Crisis Del 98Mario Axel Becerra HerreraAún no hay calificaciones
- Intersecciones LaminasDocumento5 páginasIntersecciones LaminasAlex Vibora PeinadoAún no hay calificaciones
- Ecuaciones de DimensionDocumento7 páginasEcuaciones de DimensionDiego JaramilloAún no hay calificaciones
- Calculo de ErroresDocumento4 páginasCalculo de ErroresCCLA88Aún no hay calificaciones
- Lamina 3 10 Diedrico Inicial ResueltasDocumento8 páginasLamina 3 10 Diedrico Inicial Resueltasisabel100% (2)
- LENGUADocumento19 páginasLENGUAJoel 100% (1)
- Evolución para ModdleDocumento20 páginasEvolución para ModdleJoel 10Aún no hay calificaciones
- R 2 Ejercicios Formulacion Organica Con SolucionDocumento6 páginasR 2 Ejercicios Formulacion Organica Con SolucionLuzvid Roxana Alejo OchoaAún no hay calificaciones
- Evolucion Del Género HomoDocumento9 páginasEvolucion Del Género HomoJoel 10Aún no hay calificaciones
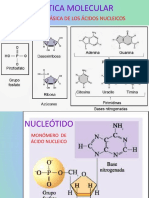
- Genética Molecular 1Documento18 páginasGenética Molecular 1Joel 10Aún no hay calificaciones
- Diedrico8 PDFDocumento4 páginasDiedrico8 PDFJoel 10Aún no hay calificaciones
- Capitulo5 Sistemas 10Documento55 páginasCapitulo5 Sistemas 10Yajairita Uzcategui ParraAún no hay calificaciones
- MorfologiaDocumento4 páginasMorfologiaJoel 10Aún no hay calificaciones
- Tarea 3.2Documento9 páginasTarea 3.2Vrapzytt RamosAún no hay calificaciones
- Balance Iónico AguasDocumento4 páginasBalance Iónico AguasjmattaAún no hay calificaciones
- Taller Carga El Ctrica y Campo El Ctrico PDFDocumento2 páginasTaller Carga El Ctrica y Campo El Ctrico PDFValentina SanchezAún no hay calificaciones
- Evaluación Bimestral. I PERIODO. GRADO 10°. ASIGNATURA. CIENCIAS QUÍMICASDocumento2 páginasEvaluación Bimestral. I PERIODO. GRADO 10°. ASIGNATURA. CIENCIAS QUÍMICASDIANA CATALINA CRUZ GONZALEZAún no hay calificaciones
- Anión y Catión para Primer Grado de SecundariaDocumento2 páginasAnión y Catión para Primer Grado de SecundariaAndy LilaAún no hay calificaciones
- QUIMICA 1ro BGU . - Semana 2. P3Documento9 páginasQUIMICA 1ro BGU . - Semana 2. P3Josue gallardoAún no hay calificaciones
- Tabla Periodica Ii (08-08-20)Documento2 páginasTabla Periodica Ii (08-08-20)JEFFERSON MAGUIÑA TOLENTINOAún no hay calificaciones
- Tabla de IonesDocumento2 páginasTabla de IonesDon Venedic DormanAún no hay calificaciones
- Brown Cap.2 Átomos Moléculas e IonesDocumento59 páginasBrown Cap.2 Átomos Moléculas e IonesErick JiménezAún no hay calificaciones
- Relaciones Periódicas Entre Los Elementos. Raymond ChangDocumento24 páginasRelaciones Periódicas Entre Los Elementos. Raymond ChangBrayan ChopraAún no hay calificaciones
- Actividad de QuimicaDocumento4 páginasActividad de QuimicaAlexander BedoyaAún no hay calificaciones
- Caih - 2º Nivel - Guia de Estudio Quimica - Tabla PeriodicaDocumento6 páginasCaih - 2º Nivel - Guia de Estudio Quimica - Tabla Periodicawendy avila guerreroAún no hay calificaciones
- Ejercicios Resueltos de BalanceoDocumento11 páginasEjercicios Resueltos de BalanceoPeralta Ramirez Frank80% (5)
- Evaluación Propiedades Químicas 10Documento2 páginasEvaluación Propiedades Químicas 10wilsonAún no hay calificaciones
- Configuracion Electronica de Los Elementos de TranscisionDocumento8 páginasConfiguracion Electronica de Los Elementos de TranscisionleidyAún no hay calificaciones
- LAB. de QG II - Reporte Práctica 12 - Solubilidad de Sales en AguaDocumento5 páginasLAB. de QG II - Reporte Práctica 12 - Solubilidad de Sales en AguaALEJANDRA ESPARZA SANCHEZAún no hay calificaciones
- Afinidad Electronica1 PDFDocumento3 páginasAfinidad Electronica1 PDFAnonymous vd5JxNCAún no hay calificaciones
- Lista de iones aniónicos y catiónicosDocumento1 páginaLista de iones aniónicos y catiónicoscuatatapaAún no hay calificaciones
- 17-Iones II EjerciciosDocumento4 páginas17-Iones II Ejerciciosmarina morales100% (1)
- SALESDocumento5 páginasSALESALAIN SOTOAún no hay calificaciones
- Matrícula vehículos checklistDocumento2 páginasMatrícula vehículos checklistColegio San Luis GonzagaAún no hay calificaciones
- Regla de Los RadiosDocumento17 páginasRegla de Los RadiosEdgar De la OAún no hay calificaciones
- Reyes E. El Balance Ionico en Ecuador Su Verdadera ImportanciaDocumento75 páginasReyes E. El Balance Ionico en Ecuador Su Verdadera ImportanciaAngeloAún no hay calificaciones
- Iones PoliatómicosDocumento1 páginaIones PoliatómicosDosazelaAún no hay calificaciones
- Tabla de Iones PoliatomicosDocumento1 páginaTabla de Iones PoliatomicosChristian SolisAún no hay calificaciones
- Ejercicios de Ley CoulombDocumento8 páginasEjercicios de Ley CoulombJuanita BarreroAún no hay calificaciones
- Enlace IónicoDocumento5 páginasEnlace IónicoAICHAAún no hay calificaciones
- Análisis de aniones: tipos y clasificaciónDocumento9 páginasAnálisis de aniones: tipos y clasificaciónJimenaCorderoSotoAún no hay calificaciones
- Tabla de Aniones 2Documento3 páginasTabla de Aniones 2Hector VillarroelAún no hay calificaciones
- Diagramas de PiperDocumento10 páginasDiagramas de PiperAndre RosalesAún no hay calificaciones