Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Potenciales Termodinamicos
Potenciales Termodinamicos
Cargado por
FranciaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Potenciales Termodinamicos
Potenciales Termodinamicos
Cargado por
FranciaCopyright:
Formatos disponibles
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
Facultad de Qumica, U.N.A.M.
Departamento de Fisicoqumica
Termodinmica (E.P.) 1212
POTENCIALES TERMODINMICOS
Objetivo
Que el alumno conozca la importancia de los potenciales termodinmicos, su interpretacin fsica
y su aplicacin en una reaccin de xido-reduccin en una pila comercial.
Cuestionario Previo
1. Qu es una reaccin de xido-reduccin?
2. Qu es una pila y cul es el principio de su funcionamiento?
3. Investigar qu es una pila de xido de plata-zinc, cul es la reaccin de xido-reduccin que
se lleva a cabo en ella y las aplicaciones de este tipo de pilas.
4. Qu es el potencial elctrico?
5. Qu es el trabajo elctrico?
6. Escribir la ecuacin que relaciona al trabajo elctrico con el potencial elctrico para una
reaccin de xido-reduccin.
7. Explicar la interpretacin fsica de G cuando un proceso se lleva a cabo a presin
y temperatura constantes.
8. Investigar la interpretacin fsica de H y S cuando un proceso se lleva a cabo a
presin constante.
9. Cul es la ecuacin que relaciona a G con H y S a temperatura constante?
G a temperatura y presin
10. Explicar el criterio de espontaneidad y equilibrio asociado con
constantes.
11. Mencionar cules son los factores que afectan el signo de G en la ecuacin que
relaciona a G con H y S a temperatura y presin constantes.
Problema
Determinar experimentalmente los potenciales termodinmicos (Hr, Gr y Sr) a 298.15 K
de una reaccin de xido-reduccin que se efecta en una pila comercial de xido de plata-zinc
(Ag2O-Zn) y explicar su interpretacin fsica.
Manejo de residuos
Investigar el manejo y tratamiento de las pilas de Ag2O-Zn cuando estas terminan su vida til.
Se recomienda el uso de un depsito con el propsito de colectar el agua usada durante el trabajo
experimental y reutilizarla.
Guardar el aceite de nujol en un frasco para reutilizarlo en prcticas posteriores.
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 1
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
Material y reactivos
1 termmetro digitala
1 multmetro digitalb
1 controlador de inmersin de temperaturac
1 hielera de unicel
1 vaso de precipitados de 100 mL
2 soportes universales
1 pinza de tres dedos
1 elevador
1 pila comercial de Ag2O-Zn de 1.55 V
1 portapilas
2 cables con conexin de banana (rojo y negro)
aceite de nujol
agua
hielo
NOTA:
a
Termmetro digital con resolucin de 0.1C.
b
Multmetro digital con resolucin de 1 x 10-4 V.
c
Controlador de inmersin de temperatura con estabilidad trmica de 0.2C.
Desarrollo experimental
Figura 1. Esquema general del dispositivo experimental para la medicin de potenciales termodinmicos en una pila
comercial de Ag2O-Zn.
Montar el dispositivo experimental de acuerdo al esquema de la figura 1.
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 2
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
1. Unir los cables con conexin de banana al portapilas, empleando soldadura de estao,
respetando el cdigo de colores (cable rojo: polo positivo y cable negro: polo negativo), para
asegurar que la polaridad es la correcta.
2. Sujetar la pila de Ag2O-Zn en el portapilas. Revisar que la polaridad y el contacto elctrico
sean correctos.
3. Colocar aceite de nujol en el vaso de precipitados de 100 mL, y sumergir el portapilas que
contiene la pila.
4. Introducir el elevador dentro de la hielera de unicel y colocar sobre ste el vaso de
precipitados con el aceite de nujol y el portapilas con la pila.
5. Introducir y encender el termmetro digital dentro del aceite de nujol, sujetndolo al soporte
universal con una pinza de tres dedos.
6. Conectar las terminales de los cables del portapilas con el multmetro. Verificar que la
polaridad sea correcta.
7. Introducir el controlador de temperatura al bao, ajustndolo con el soporte universal.
8. Colocar en la hielera una mezcla de hielo y agua, y llenar hasta una altura de 20 cm.
9. Encender el multmetro, elegir la escala de voltaje (corriente continua, V ) con el selector
giratorio y presionar durante un segundo el botn de alta resolucin (Hi Res) para
visualizar en el multmetro la cuarta cifra en la medicin del potencial elctrico (voltaje) (Vase
figura 2).
Figura 2. Esquema general del multmetro y su conexin con el portapilas que contiene la pila de Ag2O-Zn.
10. Encender el controlador de inmersin de temperatura (vase la figura 3) con el interruptor
diferencial (11), y el botn de encendido (4). Emplear la velocidad de circulacin alta (high)
(8) y ajustar con la perilla indicadora (1) la temperatura en aproximadamente 10C y esperar
hasta que la luz de calentamiento (6) se apague totalmente y as asegurar que se alcance el
equilibrio trmico dentro del bao, y que la temperatura se encuentre alrededor de 10C.
NOTA: en caso de contar con un modelo diferente, consultar el manual del equipo.
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 3
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
11. Registrar el potencial elctrico a esa temperatura (10C), en la tabla 1.
12. Mover la perilla indicadora (1) para incrementar la temperatura del bao y cada 5C
aproximadamente anotar el valor del potencial elctrico y la temperatura a la que se efectu la
medicin. Repetir este procedimiento hasta alcanzar una temperatura de aproximadamente 40C y
tener siete determinaciones registradas en la tabla 1.
Figura 3. Esquema que muestra las vistas frontal y trasera del controlador de inmersin de temperatura: (1) perilla
indicadora de temperatura; (2) botn de reinicio; (3) indicador del punto de seguridad; (4) botn de encendido;
(5) botn para refrigeracin; (6) luz de calentamiento; (7) luz de enfriamiento; (8) botn para la velocidad de la
bomba de circulacin; (9) etiqueta de identificacin; (10) entrada elctrica y (11) interruptor diferencial.
Manejo de datos
Completar la tabla efectuando los clculos requeridos en las columnas.
Tabla 1.
t / (C) T / (K) E / (V) Welec / (J) Gr / (J)
Anlisis y discusin de resultados
1. Cules son las propiedades que cambian durante el experimento?
2. Cules son las propiedades que no cambian durante el experimento?
3. Escribir la ecuacin qumica que se lleva a cabo en la pila.
4. Cmo se calcula el trabajo elctrico de la reaccin?
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 4
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
5. Cmo se calcula el Gr de la reaccin?
6. Hacer una grfica de Gr / (J) vs T / (K).
7. Con base en los resultados experimentales, cmo es la relacin entre el Gr y T?
8. Determinar la pendiente y la ordenada al origen de la lnea recta obtenida.
9. Cul es la interpretacin fsica de la pendiente y de la ordenada al origen obtenidas y qu
unidades tienen respectivamente?
10. Calcular el valor de Gr a 298.15 K a partir de los datos de la pendiente y ordenada al
origen.
11. Empleando la tabla 2 y considerando los datos reportados en la literatura de Hm,f, Gm,f, y
Sm, calcular Hr, Gr y Sr para esta reaccin y compararlos con los datos obtenidos
experimentalmente. Determinar el % error en cada caso.
Tabla 2.
Datos Datos
Propiedad: % Error:
experimentales: tericos:
Hr / (J)
Gr / (J)
TSr / (J)
Reflexionar y responder
1. Por qu se utiliza aceite de nujol en lugar de agua para calentar la pila?
2. Cul es la finalidad de utilizar una hielera de unicel para colocar el bao trmico?
3. Cules son los cambios energticos que se llevan a cabo en la pila?
4. De acuerdo con los resultados experimentales, explicar:
a) las condiciones de temperatura en las que la reaccin es ms favorable y por qu.
b) si la reaccin es exotrmica o endotrmica y por qu.
c) si aumenta o disminuye el desorden al transformarse los reactivos en productos y por qu.
5. Determinar Hr, Sr y Gr a 298.15 K para las siguientes reacciones, explicando en cada
caso si la reaccin es o no espontnea, si es exotrmica o endotrmica y si aumenta o disminuye
el desorden al transformarse los reactivos en productos, en esas condiciones. Buscar los datos de
de Hm,f, Gm,f, y Sm que se requieran de la literatura.
a) 2 NH3 (g) N2 (g) + 3 H2 (g) d) SnCl4 (l) + 4 H2O (l) Sn(OH)4 (s) + 4 HCl (g)
b) CaCO3 (s) CaO (s) + CO2 (g) e) H2 (g) + O2 (g) H2O (l)
c) CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (l) f) TiO2 (s) + 2 C (s) + 2 Cl2 (g) TiCl4 (l) + 2 CO (g)
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 5
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
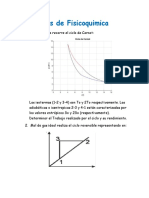
6. En un experimento, se determin la variacin del potencial elctrico como funcin de la
temperatura para una celda de Daniell, obtenindose los siguientes datos:
T / (K) 283.15 288.85 293.05 298.35 303.25 307.95
E / (V) 1.1051 1.1041 1.1034 1.1025 1.1017 1.1008
La reaccin global que se lleva a cabo en la celda es: Cu2+(ac) + Zn (s) Cu (s) + Zn2+(ac).
Con esta informacin, determinar Hr, Sr y Gr a 298.15 K, explicando la interpretacin
fsica de la variacin de cada una de las propiedades termodinmicas en esas condiciones.
7. El dixido de nitrgeno (NO2) es un gas txico que se produce en los motores de combustin
interna, el cual tiende a dimerizarse, de acuerdo con la siguiente reaccin: 2 NO2 (g) N2O4 (g).
Los datos de Hf y S a 298.15 K se presentan a continuacin en la siguiente tabla:
Compuesto: Hf / (kJ/mol) S / (J/mol K)
NO2 (g) 33.18 240.06
N2O4 (g) 9.16 304.29
a) Calcular Hr, Sr y Gr a 298.15 K
b) Asumiendo que Hr y Sr son independientes de la temperatura En qu condiciones se
favorecer la formacin del dmero N2O4, a bajas o altas temperaturas y por qu?
Aplicacin de lenguaje termodinmico
1. Definir cul es el sistema termodinmico.
2. Cuntos componentes tiene el sistema y cules son?
3. Clasificar este sistema de acuerdo: a) al nmero de fases; b) con su interaccin con el entorno.
4. Cules son las paredes del sistema y cmo se clasifican: a) por la interaccin mecnica
sistema-entorno; b) por la interaccin trmica sistema-entorno; c) por el paso de materia
sistema-entorno?
Cuestionario final
Qu aprend?
Cmo lo aprend?
Qu es lo que se me dificult entender?
Sugerencias para mejorar esta prctica.
Conclusiones
(Propuestas por el alumno).
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 6
DEPARTAMENTO DE FISICOQUMICA PROYECTO PAPIME 100110
Referencias Bibliogrficas
R. Chang, Qumica, McGraw Hill, 9 ed., Mxico, 2007, p. 131-140, 796-800, 823-832.
C. Arredondo-Snchez, Recuperacin de metales contenidos en pilas y bateras domsticas,
Tesis de Licenciatura, Facultad de Qumica, U.N.A.M., (2001) p. 3-13.
M. J. Smith and C. A. Vincent, J. Chem. Educ. 66, 8, (1989) 683-687.
M. J. Smith and C. A. Vincent, J. Chem. Educ. 66, 2, (1989) 529-531.
P. Atkins and L. Jones, Chemical Principles, Freeman, 3rd ed., New York, 2005, p. 472-473,
A11-A16.
R. A. Serway and J. E. Faughn, College Physics, 6th ed., Thompson, Canada, 2006, p. 498-501.
D. Halliday, R. Resnick and K. S. Krane, Fsica, Vol 2, CECSA, 4 ed., Mxico, 1992, p. 67-75.
P. W. Atkins, Fisicoqumica, Addison Wesley Iberoamericana, Mxico, 1987, p. 55.
R. Chang, Fisicoqumica, 3 ed., McGraw Hill, Mxico, 2008, p. 165-171, 356-357.
K. J. Leidler y J. F. Meiser, Fisicoqumica, CECSA, 1 ed., Mxico, 2006, p. 102.
T. Engel and P. Reid, Qumica Fsica, Pearson Addison Wesley, Espaa, 2006, p. 113-119,
239-242.
D. W. Ball, Physical Chemistry, Thompson, Pacific Grove, U.S.A., 2003, p. 72, 93-94.
SEMARNAT (2005), Norma Oficial Mexicana NOM-052-SEMARNAT-2005, Caractersticas,
procedimiento de identificacin, clasificacin y los listados de los residuos peligrosos, publicada
en el Diario Oficial de la Federacin el 23 de junio de 2006.
Cmara de Dip. del H. Congreso de la Unin (2007), Ley General para la Prevencin y Gestin
Integral de los Residuos, ltima reforma publicada en el Diario Oficial de la Federacin el 19 de
junio de 2007.
SCFI (2006), Proyecto de Norma Mexicana PROY-NMX-AA-104-SCFI-2006, Especificaciones
para la clasificacin e identificacin de pilas y bateras para el manejo ambientalmente
adecuado de stas, cuando sean desechadas.
Manual de Operacin del Controldador de Inmersin de Temperatura: Modelos con Control
Analgico, Polyscience, Niles, IL, U.S.A., 2004, p. 18-31.
Manual de Uso del Multmetro, Fluke Serie 80, Everett, WA, U.S.A., 2004, p. 9-14.
J. A. Dean, Langes Handbook of Chemistry, Vol IV, 13th ed., McGraw Hill, New York, 1996,
p. 9-45, 9-46, 9-70.
G. Rayner-Canham, Qumica Inorgnica Descriptiva, 2 ed., Prentice Hall, Mxico, 2000,
p. 541-544.
A. E. Saieed and K. M. Davies, J. Chem. Educ. 73, 10, (1996) 959-962.
LABORATORIO DE TERMODINMICA ELABOR: M. EN C. GERARDO OMAR HERNNDEZ SEGURA 7
También podría gustarte
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Manual de Operacion de Filtro PrensaDocumento31 páginasManual de Operacion de Filtro PrensaCarlos Alcantara Santana100% (13)
- Técnicas de Impresión en OdontologíaDocumento8 páginasTécnicas de Impresión en OdontologíaDiana García EscorciaAún no hay calificaciones
- S15.s1 - CAF3-2021 - 3HDocumento41 páginasS15.s1 - CAF3-2021 - 3HSh4Dow FoX0% (1)
- Laboratorio de Transferencia de CalorDocumento36 páginasLaboratorio de Transferencia de CalorrinconrriAún no hay calificaciones
- Práctica 9 - Termoquímica - Entalpia de Una DisoluciónDocumento4 páginasPráctica 9 - Termoquímica - Entalpia de Una DisoluciónKarla Andrea JonasAún no hay calificaciones
- Taller FisicoquimicaDocumento5 páginasTaller FisicoquimicadavidAún no hay calificaciones
- Ejercicio AdsorciónDocumento4 páginasEjercicio AdsorciónjoseAún no hay calificaciones
- ProtocoloDocumento7 páginasProtocolomartinoly19mAún no hay calificaciones
- Potenciales TermodinamicosDocumento12 páginasPotenciales TermodinamicosAngel Lopez0% (1)
- Reporte Práctica 1. Potenciales Termodinámicos.Documento9 páginasReporte Práctica 1. Potenciales Termodinámicos.Wendy JoselineAún no hay calificaciones
- 1 Potenciales TermodinámicosDocumento7 páginas1 Potenciales TermodinámicosDylan Ruiz AguilarAún no hay calificaciones
- Practica 1 - Potenciales TermodinamicosDocumento9 páginasPractica 1 - Potenciales Termodinamicosbrandon moralesAún no hay calificaciones
- Practica 1 Potenciales TermodonamicosDocumento9 páginasPractica 1 Potenciales TermodonamicosLANA100% (1)
- Reporte P1 EyCDocumento6 páginasReporte P1 EyCJEAN RENE RAMIREZ NAVAAún no hay calificaciones
- Practica 1 EquilibrioDocumento9 páginasPractica 1 EquilibrioAlejandro García LópezAún no hay calificaciones
- Potenciales Termodinamicos ReporteDocumento14 páginasPotenciales Termodinamicos ReporteBerenice Vázquez100% (1)
- EyC Práctica 1Documento11 páginasEyC Práctica 1KiiKi DeeAún no hay calificaciones
- Calor de Neutralización REVDocumento6 páginasCalor de Neutralización REVRafael Arce FernándezAún no hay calificaciones
- PB ZNDocumento5 páginasPB ZNmarzinusAún no hay calificaciones
- Practica1. Potenciales TermodinamicosDocumento8 páginasPractica1. Potenciales TermodinamicosOscar RSAún no hay calificaciones
- Informe Calor de SolucionDocumento23 páginasInforme Calor de SolucionpattylopezlunaAún no hay calificaciones
- Reporte Práctica #7-1 PDFDocumento8 páginasReporte Práctica #7-1 PDFSebastian CarrilesAún no hay calificaciones
- Termodinamica ENUNCIADOSDocumento4 páginasTermodinamica ENUNCIADOSMåiirå SDj K. ZYtAún no hay calificaciones
- Termo Practica 4Documento7 páginasTermo Practica 4Erika LMAún no hay calificaciones
- Reporte 1 EyCDocumento7 páginasReporte 1 EyCGabriela AltamiranoAún no hay calificaciones
- Taller Balance de Energia Balance de Energia.Documento5 páginasTaller Balance de Energia Balance de Energia.Sharyl CondiaAún no hay calificaciones
- Práctica 1 PREVIO.Documento5 páginasPráctica 1 PREVIO.Wendy JoselineAún no hay calificaciones
- Laboratorios Transferencia de CalorDocumento28 páginasLaboratorios Transferencia de CalorJair Andres Arevalo Banoy100% (1)
- Manual Practica Laboratorio IiiDocumento7 páginasManual Practica Laboratorio IiiManuel CortesAún no hay calificaciones
- Taller - SEGUNDA LEYDocumento5 páginasTaller - SEGUNDA LEYPascual Jose HerreraAún no hay calificaciones
- Practica 2 Balance de Energia en Estado Inestable Mezclado No Ideal Intermitente de SolucionDocumento6 páginasPractica 2 Balance de Energia en Estado Inestable Mezclado No Ideal Intermitente de SolucionSusette Diaz0% (1)
- TermoDocumento3 páginasTermoRodrigo Garcia0% (1)
- Informe de TermoquimicaDocumento18 páginasInforme de TermoquimicaClaudia Aroste Ceron100% (1)
- Laboratorio de Quimica N7Documento14 páginasLaboratorio de Quimica N7LINDER ANTONIO LOPEZ DOMINGUEZAún no hay calificaciones
- Practica 11. ElectroquímicaDocumento14 páginasPractica 11. ElectroquímicaNadia BarriosAún no hay calificaciones
- LEyC Practica9 FormatoDocumento4 páginasLEyC Practica9 FormatoAlejandro Guerrero NenteAún no hay calificaciones
- Práctica #1Documento4 páginasPráctica #1Karen MoralesAún no hay calificaciones
- Informe Calor Específico FÍSICO-QUÍMICADocumento17 páginasInforme Calor Específico FÍSICO-QUÍMICAeric7lopezAún no hay calificaciones
- Potenciales TermodinámicosDocumento6 páginasPotenciales TermodinámicosMariana HopeAún no hay calificaciones
- Guia de Calor de NautralizacionDocumento6 páginasGuia de Calor de NautralizacionCarla FloresAún no hay calificaciones
- Practica 1 Eq y CDocumento10 páginasPractica 1 Eq y CFredy Akenaton ArroyoAún no hay calificaciones
- Reporte de Laboratorio N°3-2022-1Documento17 páginasReporte de Laboratorio N°3-2022-1Angel MarellaAún no hay calificaciones
- Lab 6-Motor TérmicoDocumento3 páginasLab 6-Motor TérmicoJuan David MoyanoAún no hay calificaciones
- Guia QMC 100-1Documento5 páginasGuia QMC 100-1EnsoAún no hay calificaciones
- Asignación IDocumento7 páginasAsignación ISara AguirreAún no hay calificaciones
- Práctica N8 - TERMODINÁMICADocumento2 páginasPráctica N8 - TERMODINÁMICAJose Chavez VargasAún no hay calificaciones
- Práctica 8-Cambio de Entalpía de Fusión Del HieloDocumento8 páginasPráctica 8-Cambio de Entalpía de Fusión Del HieloAxelAún no hay calificaciones
- Practicas Quimica Fisica Licenciatura QuimicaDocumento26 páginasPracticas Quimica Fisica Licenciatura QuimicapapucicuAún no hay calificaciones
- Articulo Unidad II Fenomenos de TransporteDocumento8 páginasArticulo Unidad II Fenomenos de TransporteMaria HerreraAún no hay calificaciones
- Lista Termodinámica 2019 05 20 JMA PDFDocumento5 páginasLista Termodinámica 2019 05 20 JMA PDFRegina MogrovejoAún no hay calificaciones
- AttachmentDocumento7 páginasAttachmentmiguel EncarnacionAún no hay calificaciones
- Practica Domiciliaria 6Documento6 páginasPractica Domiciliaria 6Julio Soto LovonAún no hay calificaciones
- 1572065183taller Termodinamica 2008 Fisica 10Documento3 páginas1572065183taller Termodinamica 2008 Fisica 10lorena quintero guerreroAún no hay calificaciones
- 5.2 Síntesis Del AmoníacoDocumento10 páginas5.2 Síntesis Del AmoníacoMoztazaMerloAún no hay calificaciones
- Calor de CombustionDocumento9 páginasCalor de CombustionSe BasAún no hay calificaciones
- Potenciales TermodinamicosDocumento6 páginasPotenciales TermodinamicosOmar MonteroAún no hay calificaciones
- Termodinámica QuímicaDocumento20 páginasTermodinámica QuímicaLuciaAún no hay calificaciones
- Clase 04 - y - 05 - Unidad II DIM 404Documento47 páginasClase 04 - y - 05 - Unidad II DIM 404SAIR MORALES ARAVENAAún no hay calificaciones
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Flujo de fluidos e intercambio de calorDe EverandFlujo de fluidos e intercambio de calorCalificación: 1 de 5 estrellas1/5 (1)
- Termodinámica clásica. Protocolos experimentales sobre primera y segunda leyes, y sobre potenciales selectosDe EverandTermodinámica clásica. Protocolos experimentales sobre primera y segunda leyes, y sobre potenciales selectosAún no hay calificaciones
- TDS - XM7 42-15 - EsDocumento1 páginaTDS - XM7 42-15 - EsFrancisca FuentesAún no hay calificaciones
- Que Es HibridaciónDocumento3 páginasQue Es HibridaciónAlciraAún no hay calificaciones
- Obtencion de Acetato de Isoamilo - CompressDocumento12 páginasObtencion de Acetato de Isoamilo - CompressMIRNA SANTOSAún no hay calificaciones
- Guia de Aprendizaje Función PH y Poh Quimica OnceDocumento6 páginasGuia de Aprendizaje Función PH y Poh Quimica OncekarlacastrillonAún no hay calificaciones
- Tinciones Diferenciales - ZSPDocumento34 páginasTinciones Diferenciales - ZSPVega Martínez ValeriaAún no hay calificaciones
- Qgii Obtencion y Propiedades Del Hidrogeno 2 SubiDocumento7 páginasQgii Obtencion y Propiedades Del Hidrogeno 2 SubiStiven PalomoAún no hay calificaciones
- A Enzimas Herramienta Util en Sintesis Organicos 17 GotorDocumento9 páginasA Enzimas Herramienta Util en Sintesis Organicos 17 GotorRALPH STEIN RIVERA BOTONARESAún no hay calificaciones
- Cont. Físico y MecDocumento20 páginasCont. Físico y MecCorina Lucero IGAún no hay calificaciones
- Bebidas Lacteas FermentadasDocumento34 páginasBebidas Lacteas FermentadasKike S RangelAún no hay calificaciones
- Clase 5 - Diapositiva - Números CuánticosDocumento31 páginasClase 5 - Diapositiva - Números CuánticoscristianAún no hay calificaciones
- Taller 2..generalidades BioquimicaDocumento4 páginasTaller 2..generalidades BioquimicaLILY OCHOAAún no hay calificaciones
- El Intercambiador de Calor de Placas 1ALFA LAVAL PDFDocumento6 páginasEl Intercambiador de Calor de Placas 1ALFA LAVAL PDFOscar Yoan Chipana RamosAún no hay calificaciones
- Harinas, Levaduras y Otros Agentes LeudantesDocumento12 páginasHarinas, Levaduras y Otros Agentes LeudantesRabichinChocolateríaArtesanalAún no hay calificaciones
- Preinforme 1. Extracción de Aceites EsencialesDocumento9 páginasPreinforme 1. Extracción de Aceites EsencialesDalíAsesoríasAún no hay calificaciones
- Quimica CR 2023-1Documento3 páginasQuimica CR 2023-1dragon ball superAún no hay calificaciones
- Grupo 5 Operaciones Unitarias Exposición Extraccion.Documento9 páginasGrupo 5 Operaciones Unitarias Exposición Extraccion.Daya AtienciaAún no hay calificaciones
- Discusion IDocumento3 páginasDiscusion ITATIANAAún no hay calificaciones
- TP Hormigón ArmadoDocumento3 páginasTP Hormigón ArmadoJavier VerónAún no hay calificaciones
- Taller de ÓxidosDocumento2 páginasTaller de ÓxidosAlejo LondoñoAún no hay calificaciones
- Determinación de Cloruros y Carbonatos en El SueloDocumento5 páginasDeterminación de Cloruros y Carbonatos en El SueloalexaAún no hay calificaciones
- PonenciaFECONS AlejandroFernndezDomnguezDocumento18 páginasPonenciaFECONS AlejandroFernndezDomnguezJorge Luis Oré CubaAún no hay calificaciones
- Ejercicios Propuestos - Estequiometría - TAREA 5Documento4 páginasEjercicios Propuestos - Estequiometría - TAREA 5nicolasreisanchoAún no hay calificaciones
- Problemario de Filtración - Procesos de Separación I - 20 PDFDocumento3 páginasProblemario de Filtración - Procesos de Separación I - 20 PDFIsaac RamirezAún no hay calificaciones
- Resolucion de La Practica de QuimicaDocumento1 páginaResolucion de La Practica de QuimicacorredorAún no hay calificaciones
- Protocolo SO2Documento20 páginasProtocolo SO2Anggie BeltránAún no hay calificaciones
- Power Alcanos 2020Documento50 páginasPower Alcanos 2020noelia25455Aún no hay calificaciones
- Sistemas de Un Solo Componente (Sustancia Pura)Documento9 páginasSistemas de Un Solo Componente (Sustancia Pura)MiguelAún no hay calificaciones