Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Compuestos Aromaticos
Cargado por
Matias DamiánDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Compuestos Aromaticos
Cargado por
Matias DamiánCopyright:
Formatos disponibles
130
6.-HIDROCARBUROS AROMTICOS.
INTRODUCCIN
Los compuestos aromticos abarcan una amplia gama de sustancias
qumicas de uno dos o ms anillos altamente insaturados de frmula C nHn que
poseen propiedades qumicas singulares.
La aromaticidad no es un atributo de los compuestos de C e H solamente,
sino que tambin en su estructura pueden encontrarse otros tomos como oxgeno y
nitrgeno constituyendo la gran familia de los compuestos heterocclicos aromticos.
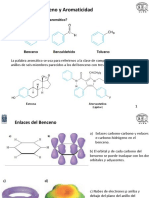
En el siglo XVII, Kekul propuso una estructura para el hidrocarburo ms
representativo de los aromticos: el benceno C 6H6.
H
H
(A)
H
Estructura N1
Hay una gran estabilidad qumica asociada a la estructura del benceno y en
general a todos los compuestos aromticos. Esto es debido a que son estructuras
qumicas cclicas, planas que poseen un nmero mximo de dobles enlaces
conjugados permitiendo as una amplia deslocalizacin electrnica en su sistema .
Su estudio ha demostrado que los enlaces entre los tomos de carbono sucesivos
son semejantes, es decir, no se puede distinguir entre enlace simple y enlace doble
como en la estructura (A) De esta manera, la estructura del benceno, es un hbrido
de resonancia entre las estructuras contribuyentes (C) y (D) La estructura (E) no es
una mezcla de (C) y (D), sino que es una estructura que tiene caractersticas fsicas
y qumicas ponderadas tanto de (C) como de (D):
H
Estructura N2
(C)
(E)
(D)
131
Si la longitud del enlace simple C-C es de 1,54 x 10 -8 cm y la del doble C=C
es 1,34 x 10-8 cm, la longitud del enlace C-C aromtico tiene un valor intermedio
entre simple y doble de 1,39 x 10 -8 cm.
REPRESENTACIN DEL BENCENO.
Estructura N3
Estas representaciones se encuentran a menudo en los textos de qumica
orgnica. A la izquierda, una representacin resonante de sus estructuras
contribuyentes. La figura de la derecha, es la representacin de un hbrido de
resonancia que pone de manifiesto que la extensin de la deslocalizacin
electrnica abarca el anillo completo. Se ver ms adelante que una u otra de las
formas (estructura N3) es til para dar cuenta de las propiedades qumicas de estos
compuestos.
OTRAS ESTRUCTURAS AROMTICAS:
La estructura de la molcula de benceno es una de las ms sencillas y
recurrente entre los compuestos aromticos, aunque tenemos tambin algunas otras
(Estructura N4) que son un tanto ms complejas con varios anillos insaturados:
naftaleno
fenantreno
antraceno
Estructura N4
Estas molculas complejas suelen encontrarse a menudo en nuestro mbito
cotidiano de vida, por ejemplo, en el holln de las chimeneas, en el alquitrn de los
pavimentos urbanos, en el humo del tabaco, etc y son conocidas desde hace mucho
tiempo como molculas inductoras de algn tipo de cncer. Ciertos policiclos
aromticos como el Benzo [ a ] pireno cuya estructura se muestra ms abajo
(Estructura N5), son capaces de producir alteraciones genticas en sistemas
biolgicos, an a muy bajas concentraciones.
132
benzo [ a ] pireno
Estructura N5
Se supone que estas sustancias pro-carcingenas, son transformadas por
algn proceso enzimtico en un carcingeno activo, capaz de interaccionar con el
ADN celular, alterando en ese momento el mensaje gentico indispensable para la
reproduccin celular normal.
ALGUNOS COMPUESTOS AROMTICOS HETEROCCLICOS.
Todas estas molculas cclicas, contienen al menos un tomo diferente al
carbono formando parte del anillo, el que puede ser de cinco o ms tomos. Por
ejemplo:
H
pirrol
furano
tiofeno
N
piridina
Estructura N6
Algunas bases heterocclicas aromticas como la citosina, uracilo, adenina y
guanina (Estructura N7) son componentes esenciales de los cidos nucleicos.
NH2
NH
O
N
H
citosina
O
N
H
uracilo
NH2
O
N
N
H
adenina
N
Estructura N7
HN
H2N
N
guanina
N
H
133
REPRESENTACIN DE LA AROMATICIDAD CON ORBITALES
MOLECULARES Y LA REGLA DE H CKEL (4N+2)
Como se dijo previamente, un compuesto aromtico es un anillo con mltiples
dobles enlaces conjugados. Los clculos de Erich Hckel, (qumico alemn del
Instituto de Fsica Terica de Stuttgard en la dcada de 1930) permitieron deducir
que, al igual que aquellos tomos de los gases nobles, cuando sus orbitales
atmicos estaban completos con sus respectivos pares de electrones, se obtenan
estructuras de gran estabilidad, encontr que lo mismo sucede con las molculas
con sistemas electrnicos conjugados y formando sistemas cclicos o anillos .
Estas estructuras tambin adquiran una estabilidad extraordinaria si sus orbitales
moleculares se llenaban cada uno con un par de electrones con espn opuesto. Sin
embargo haba otra condicin que deba cumplirse, estos sistemas
sern estables
si el nmero de electrones en la estructura cclica cumple con la relacin 4n + 2,
donde n debe ser entero incluyendo adems el valor cero. Es decir, n puede tomar
valores 0, 1, 2, 3, 4, etc.
El valor de n=0 implica segn Hckel un nivel bsico y nico susceptible de
ser llenado con solo un par de electrones, el resto de los orbitales con energa
creciente aparecen de a pares de niveles. Este nivel nico y bsico est presente en
todos los sistemas aromticos.
Por ejemplo: si los seis orbitales atmicos p del benceno, se combinan entre
s, tiene lugar la formacin de seis orbitales moleculares; tres enlazantes y tres
antienlazantes. Sus seis electrones ocuparn completamente y en parejas de
espines opuestos, los tres orbitales inferiores enlazantes (Diagrama N1)
Otra de las condiciones que debe cumplirse en los aromticos, es su
coplanaridad. Los diferentes orbitales atmicos p deben ser paralelos entre s y de
esta manera, obtener su mxima superposicin para poder deslocalizar con mxima
efectividad los electrones sobre el total del sistema cclico de dobles enlaces
conjugados (Figura N1). Esta condicin obliga a que todos los tomos que forman
parte del sistema aromtico estn en un mismo plano.
Al aplicar aquella regla que dice que: La mezcla de igual nmero de orbitales
atmicos generan igual nmero de orbitales moleculares, a los seis orbitales 2p del
benceno, entonces, cuando estos seis orbitales atmicos 2p perfectamente
paralelos, se mezclan entre s, generarn seis orbitales moleculares,
134
orbitales
p
benceno
Figura N1
Segn Hckel entonces, se debera obtener la siguiente distribucin de
orbitales moleculares, niveles de energa y electrones para obtener el diagrama.
orbitales
antienlazantes
E
energa de un
orbital 2p
orbitales
enlazantes
seis electrones pi de un compuesto aromtico
como el benceno.
Diagrama N1
Las estructuras aromticas no deben ser consideradas solamente como molculas
neutras, y tambin pueden ser especies con carga elctrica, y presentarse como,
aniones o cationes. Por ejemplo:
C sp3
H
C sp2
H
+
ciclopropeno
no aromtico
(4n+2) = 2
n = 0 pero
no es plano
catin aromtico
ciclopropenilo
(4n+2) = 2
n = 0 plana
135
El ciclopropeno muestra una inusual tendencia a ceder un hidruro para as
formar un carbocatin aromtico ciclopropenilo mucho ms estable que la molcula
neutra.
Otro ejemplo:
H
-H
ciclopentadieno
no aromtico
(4n+2) = 4
n = 1/2 no plano
anin aromtico
ciclopentadienilo
(4n+2) = 6
n = 1 plano
Esquema N1
Por lo mismo, se ha encontrado que este hidrocarburo presenta tambin un
inusual carcter cido pKa = 16, semejante a los alcoholes, valor que contrasta con
la acidez que muestran los alcanos pK a alrededor de 40 a 50. Esto se debera a la
gran estabilidad que logra el anin al adquirir una estructura aromtica.
Cuando no se cumple la regla del (4n + 2), se dice que estos compuestos
cclicos son anti aromticos a pesar de tener dobles enlaces conjugados.
Por Ejemplo:
ciclopentadienilo
catin
(B)
ciclobutadieno
neutro
(A)
ciclopropenilo
anin
(C)
Estructura N8
Y ninguna de ellas es aromtica, puesto que no cumplen con la condicin de
tener un valor de n entero. Son estructuras poco estables.
Para (A) que tiene cuatro electrones localizados en cuatro orbitales p se
puede ver el siguiente diagrama de energa de orbitales moleculares:
ciclobutadieno
Diagrama N2
136
De los cuatro orbitales moleculares hay dos entre ellos de igual energa
(Diagrama N2). A esos orbitales isoenergticos se les llama degenerados, en la
jerga de los qumicos terico cunticos. Los cuatro electrones deben ser colocados
entonces, llenando los orbitales moleculares desde aquel de menor energa hacia
arriba y aquellos orbitales degenerados o isoenergticos deben ser llenados con un
electrn cada vez. De esta manera hay dos electrones que quedan desapareados y
la molcula no es aromtica.
Una situacin semejante se presenta en las otras dos molculas que
acompaan al ciclobutadieno. Demuestre usted ahora esa condicin de no
aromaticidad que presentan esas estructuras inicas.
Otra estructura interesante es la que presenta el cicloheptatrieno:
-H
anin
-H
cicloheptatrieno
catin
Esquema N2
Los diagramas de energa de los orbitales involucrados con estas estructuras
se muestran a continuacin:
anin
(A)
neutra
(B)
catin
(C)
Diagrama N3
La estructura (B) que es la molcula neutra, no es aromtica a pesar de
cumplir la regla de Hckel, ya que, por no ser plana, (posee un carbono CH 2 - con
hibridacin sp3) no puede deslocalizar los electrones alrededor del anillo.
137
La estructura (A) es una estructura plana, pero no cumple con la regla de (4n
+ 2), y posee electrones desapareados (ver diagrama N3) por lo tanto es antiaromtica.
La estructura (C) es una estructura plana, ya que, al perder un hidruro (protn
con dos electrones) en el carbono sp3, este cambia a hibridacin sp2 quedando
entonces un orbital vaco p paralelo al resto de los orbitales p del anillo conjugado.
Cumple adems con la regla de Hckel y por lo tanto es aromtico.
Problema:
Si los pares de electrones no compartidos del nitrgeno que estn en el pirrol y
tambin en piridina, en un orbital atmico sp 2. Implica este hecho que ambas
molculas son aromticas?. Puede dar usted una explicacin razonable en caso de
que su respuesta sea afirmativa o negativa?
Pirrol
Piridina
N
NOMENCLATURA DE LOS COMPUESTOS AROMTICOS.
Los compuestos se conocen desde hace mucho tiempo, incluso, antes que
aparecieran las reglas de la nomenclatura IUPAC, por esa razn, hay en la literatura
actual numerosos ejemplos de nombres triviales en la qumica de esta familia. Por
ejemplo:
CH3
benceno
tolueno
CHO
benzaldehido
NH2
COOH
anilina
cido benzoico
Estructura N9
NO2
OH
CH
CH2
COOH
CH3
OH
HO
nitrobenceno
Estructura N10
fenol
estireno
CH3
para-xileno
OH
cido glico
138
IUPAC, acepta estos nombres no sistemticos. Pero nombre sistemtico de
estos compuestos, lo define IUPAC como la combinacin del nombre del sustituyente
como prefijo del nombre benceno. As por ejemplo (Vea la Tabla N1):
Sustituyente
Grupo funcional.
Hidroxi
Amino
Etenil
-OH
-NH2
-CH=CH2
Nombre del
compuesto.
Hidroxibenceno
Aminobenceno
Etenilbenceno
Nombre comn
Fenol
Anilina
Estireno
Tabla N1
Cuando el anillo benceno est como sustituyente, su nombre es fenil, y el
carbono de la valencia libre es el N1
fenil
Estructura N11
Otros sustituyentes aromticos bencenoides son:
CH2
CH
bencil
benciliden
CH
difenilmetil
bencilidin
trifenilmetil
Estructura N12
Benceno disustituido:
Cuando sobre el anillo hay ms de un sustituyente, aparecen diferentes
estructuras isomricas:
139
ISMERO
G
S
ORTO
MONO
META
S
G
PARA
Diagrama N4
En general estos ismeros se abrevian con una letra como sigue:
o- de orto, m- de meta y p-de para.
En esta nomenclatura, lo importante es la posicin relativa de los
sustituyentes. El grupo sustituyente G puede estar sobre cualquier tomo de
carbono del anillo.
Hay veces en que se combina esta regla de la disustitucin o, m, p con
nombres comunes no sistemticos. Por ejemplo:
OH
NO 2
ISMERO
SUSTITUCIN
o-nitrofenol
(1-2) ORTO
NH2
m-cloroanilina
Cl
(1-3)
META
140
CO2H
(1-4)
cido p-hidroxibenzoico
PARA
OH
Figura N2
Cuando hay ms de dos sustituyentes en el benceno, se numera el ncleo
aromtico siguiendo el sentido que d a los sustituyentes la menor numeracin
posible. Adems, hay que respetar la precedencia de los grupos funcionales. Vea la
tabla N1, Captulo N1.
OH
1
NH2
NO2
NH2
4-amino-2-nitrofenol
y no 4-hidroxi-3-nitroanilina
Cl
H3C
3-cloro-5-metilanilina
y no 3-amino-5-clorotolueno
Estructura N13
OH
CO2H
1
NH2
O 2N
Br
CHO
OH
cido 2-bromo-4-hidroxi-5-nitrobenzoico 2-amino-3-hidroxibenzaldehido
Estructura N14
Observe que se ha dado la numeracin 1, al carbono perteneciente al anillo
que tiene unida la funcin qumica ms importante entre los sustituyentes, es decir,
la funcin que tiene la mayor precedencia en qumica orgnica. (Captulo 1) Esta
funcin prioritaria, nos informa, a qu familia qumica pertenece la molcula que
tenemos delante. El sentido de la numeracin, sigue el mismo criterio citado ya, es
141
decir, darle al resto de los sustituyentes, la menor numeracin posible. En el nombre
final, estos se ordenan segn orden alfabtico.
REACCIONES QUMICAS DEL BENCENO
Desde aqu en adelante, tomaremos la molcula de benceno como modelo
representativo de la familia de los aromticos, estudiando en l, las diferentes
propiedades qumicas de estos compuestos.
La sustitucin electroflica es la reaccin ms comn de estos compuestos
Esta consiste en el reemplazo en el anillo de un hidrgeno por otro tomo o grupo
de tomos. El mecanismo general describe el ataque de un electrfilo lo
suficientemente fuerte como para producir un intermediario no aromtico en la etapa
lenta:
H
+
Esquema N3
Aqu, E+ es el electrfilo. Las tres estructuras contribuyentes de la derecha
(Pueden ser reemplazadas por un hbrido de resonancia que se muestra ms abajo)
ponen de manifiesto, que el carbono al cual se une el electrfilo, cambia su
hibridacin de sp2 a sp3, es decir, hay ruptura de la aromaticidad, y por consiguiente
hay un aumento de la energa de este catin intermediario con relacin a la molcula
aromtica. A esta estructura de alta energa se le llama complejo sigma.
estructuras contribuyentes
hbrido de resonancia
Estructura del complejo sigma representado como un hbrido de resonancia.
Figura N3
142
La formacin del complejo sigma, va precedida del paso por el complejo
activado o de transicin de mxima energa de activacin (vea el grfico N2)
Ntese adems, que en las estructuras contribuyentes, la carga positiva se dispersa
en el interior del anillo afectando especficamente a los carbonos orto y para con
relacin al carbono del electrfilo. Como se mencion anteriormente, este hecho
ocurre lentamente, constituyndose en la etapa determinante de la reaccin.
Luego viene una segunda etapa rpida, en la cual, el sistema se estabiliza
por prdida del protn (Ver grfico N2), recuperando as su aromaticidad al quedar
nuevamente todos los carbonos del anillo aromtico con hibridacin sp2:
E
+
rpido
BH
Esquema N4
El protn es sacado por B- que es la base de Lewis en el sistema. Note que
esta base podra actuar como un nuclefilo tambin y adicionarse al anillo formando
un ciclohexadieno, sin embargo, no sucede porque se pierde la aromaticidad y el
producto sera uno de mucha ms energa.
E
B
E
H
coordenada de reaccin
Grfico N1
143
Muchas de estas reacciones pueden ser llevadas a cabo a temperaturas
relativamente moderadas, menores a 100C.
El diagrama de reaccin (Grfico N2), representa la curva tpica de la
sustitucin electroflica en un anillo aromtico. La formacin de T1, tiene la energa
de activacin ms alta y representa la etapa lenta de la reaccin, aquella en la cual,
el sistema comienza a perder su aromaticidad hasta llegar al intermediario o
complejo sigma con el carbono tetradrico.
El complejo de transicin T2, que se forma cuando el intermediario comienza
a perder el protn para recuperar su aromaticidad, tiene una energa de activacin
menor, lo que significa que es una etapa ms rpida que la anterior. La salida del
protn lleva a la formacin del producto.
T1
T2
E
Ea
reac.
prod.
coordenada de reaccin
Grfico N2
MECANISMO DE LAS REACCIONES DE SUSTITUCIN AROMTICA Y LA
MONOSUSTITUCIN EN EL ANILLO AROMTICO.
Las reacciones de sustitucin en un anillo aromtico, abren una puerta
enorme al campo de la sntesis orgnica. Esta se proyecta hacia diversos campos
del diario vivir. Por ejemplo, en muchos de los plsticos, detergentes, combustibles,
frmacos y drogas, etc. que estamos utilizando diariamente
A continuacin se presenta un listado de las reacciones de sustitucin ms
comunes que tienen lugar entre un compuesto aromtico y un reactivo electrfilo.
Estas son:
1.- Nitracin
2.- Halogenacin
3.- Sulfonacin
4.- Alquilacin
5.- Acilacin.
144
1.- NITRACIN.
En esta reaccin el electrfilo es el in nitronio (NO2+). Este catin se genera
in situ por la accin del cido sulfrico (pKa = -5,2) sobre el cido ntrico (pKa =-1,4).
De acuerdo con los valores relativos de pKa, el cido sulfrico acta como un cido
protonando al cido ntrico segn el equilibrio:
H2SO4
H2NO3
HNO 3
HSO4
Esquema N5
Luego el cido conjugado del cido ntrico se desproporciona formando as la
especie nitrante NO2+ ( in nitronio ):
H2O
H2NO3
NO2
Esquema N6
Este electrfilo fuerte, ataca al anillo aromtico en una primera etapa lenta,
rompiendo su aromaticidad:
NO2
lento
+ NO 2
Esquema N7
Lo que sigue es el ataque de la base conjugada del cido sulfrico,
extrayendo el protn del complejo y restaurando as el sistema aromtico. Esta etapa
va acompaada de emisin de energa al alcanzar el sistema un estado estable que
es el producto de la reaccin:
NO2
NO2
+
HSO4
rpido
H2SO4
nitrobenceno
Esquema N8
El producto final de esta reaccin es el nitrobenceno. Como usted pudo ver, el
cido sulfrico actu como generador de la especie nitrante y tambin como
catalizador de la reaccin ya que se recupera al final en la ltima etapa.
145
2.- HALOGENACIN.
La fluoracin y la iodacin son reacciones poco frecuentes en un laboratorio
qumico y requieren de reactivos especiales. Por esa razn no sern tratadas aqu.
En cambio, la cloracin y la bromacin del benceno, se efectan en presencia
de un catalizador cido como el trihalogenuro frrico respectivo. Por ejemplo, para
clorar el benceno utilizaremos el tricloruro frrico y para bromar ser necesario el
tribromuro frrico. El mecanismo de estas halogenaciones se desarrolla al igual que
la nitracin, en dos etapas: Primero, el ataque del electrfilo sobre el anillo para
formar un intermediario con la prdida momentnea de la aromaticidad del benceno
en una etapa lenta:
H
+
Cl
Cl
FeCl3
lento
Cl + FeCl4
Esquema N9
Aqu hay que recordar que el catin intermediario es un hbrido de resonancia
en el cual intervienen tres estructuras contribuyentes que deslocalizan la carga
positiva alrededor del anillo.
En una segunda etapa rpida, la base conjugada FeCl 4- extrae el protn
desde el carbono sp3 del anillo, para as recuperar el carcter aromtico en el
producto.
H
Cl + FeCl4
rpido
Cl
+
HCl
FeCl3
Esquema N10
La forma de la curva o diagrama de reaccin es cualitativamente semejante a
la de la nitracin y en este aspecto, la bromacin tiene tambin las mismas
caractersticas o requerimientos energticos.
3.- SULFONACIN.
Es una reaccin de gran importancia industrial, sobretodo en el campo de los
detergentes. En el laboratorio el benceno es sulfonado con cido sulfrico fumante,
o sea, una mezcla de cido sulfrico y anhdrido sulfrico SO 3.
146
Al parecer, el agente electroflico se generara por autoprotolisis del cido
sulfrico y posterior descomposicin de esta especie protonada:
2 H2SO4
H3SO4
H3O
H3SO4
HSO4
SO3
Esquema N11
El electrfilo SO3 tiene el tomo de azufre altamente deficiente en electrones
debido a la mayor electronegatividad de los oxgenos unidos a l, y por lo tanto, es
el tomo de azufre el que atacar y se unir con el carbono del anillo aromtico:
O
S
azufre altamente electronegativo
Figura N4
La sulfonacin se distingue de la nitracin y de la halogenacin, porque la
etapa lenta de la reaccin no es la formacin del enlace C-electrfilo, ni la salida del
protn en la segunda etapa:
H
+
SO3
SO3
lenta
lenta
Esquema N12
La remocin del protn en la siguiente etapa desde el carbono sp3 es una
etapa semejante en cuanto a energa a la etapa anterior en la reaccin. Este hecho
es importante en la reversibilidad del equilibrio(esquema N12 y 13):
147
SO 3
SO 3
+
lento
HSO 4
lento
H2SO4
Esquema N13
Finalmente, el medio cido de la reaccin proporciona el protn.
SO3H
SO3
+
rpido
H3O
rpido
H2O
cido benceno sulfnico
Esquema N14
La sulfonacin, es entonces una reaccin reversible. Como se ver
posteriormente, tiene numerosas ventajas en sntesis, ya que este grupo (sulfn)
puede ser desplazado del anillo por simple calentamiento a reflujo del compuesto
aromtico sulfonado en una solucin diluida de cido sulfrico.
T1
T2
H
SO 3
Product.
React.
coordenada de reaccin
Grfico N3
En el diagrama puede verse que T2 es semejante a T1. En T2 la energa de
activacin corresponde a la ruptura del enlace C(sp3))-H del intermediario.
4.- ALQUILACION DE FRIEDEL Y CRAFTS.
148
Esta es una reaccin en la cual, con ayuda de un acatalizador cido, es
posible introducir una cadena lateral en el anillo aromtico.
El esquema general para esta reaccin puede escribirse de la siguiente
manera: donde R-X es un halogenuro de alquilo.
R
+
Esquema N15
La alquilacin electroflica aromtica, solo puede llevarse a cabo en presencia
de un cartalizador, porque el halogenuro de alquilo no es un electrfilo lo
suficientemente fuerte como para romper la aromaticidad del sistema. El tricloruro de
aluminio, que se usa como catalizador en esta reaccin, aumenta la electroflia del
agente alquilante por el siguiente mecanismo:
Sea RX el halogenuro de alquilo, donde X puede ser cloro o bromo:
R
AlCl3
AlCl3
catalizador
R
X AlCl3
producto coordinado
+
R
carbocatin
XAlCl3
Esquema N16
Como todas aquellas reacciones en las que se forman carbocationes, hay que
tener presente un posible reordenamiento o trasposicin del carbocatin a uno ms
estable, y as el producto de la reaccin ser diferente al esperado.
Por ejemplo: Si R es n-propilo:
CH3CH2CH2
Br
AlCl3
catalizador
CH3CH2CH2 Br
AlCl3
compuesto coordinado
Br AlCl3
CH3CH2CH2
producto coordinado
CH3CH2CH2
carbocatin 1
muy inestable
H
CH3 CH
CH2
migra un hidruro
Esquema N17
CH3 CH
CH3
carbocatin 2
mas estable
BrAlCl3
149
En este caso, puede notarse que el agente alquilante ha cambiado de
carbocatin primario, n-propilo, a isopropilo secundario que es ms estable.
Prosiguiendo con el esquema del mecanismo:
H
R XAlCl3
lento
XAlCl3
R
XAlCl3
rpido
AlCl3
+ HX
Esquema N18
Siempre en una reaccin de alquilacin, deber tenerse el cuidado de utilizar
un halogenuro de alquilo terciario o secundario estable, para inducir productos con
poca o nada de contaminacin debido a reacciones laterales y con alto rendimiento
del compuesto esperado.
Ejemplo 1:
CH3
CH3
CH3
X
AlCl3
CH3
XAlCl3
CH3
CH3
Esquema N19
El carbocatin electroflico no puede reordenarse a una especie ms estable y
este ser el agente alquilante que proporcionar un producto nico, el
terbutilbenceno.
Ejemplo 2:
CH3CHCH2CH3
X
AlCl3
CH3CHCH2CH3
XAlCl3
150
CH3CHCH2CH3
CH3CHCH2CH3
AlCl3X
+ AlCl3 + HX
Esquema N20
En este caso, el agente alquilante es el ms estable y no hay posibilidades de
que se reordene. Produce un nico producto.
La etapa lenta de la reaccin , es decir, aquella asociada a la energa de
activacin mayor al de todas las etapas, es el ataque de la especie electroflica al
anillo aromtico. El resto de las etapas son rpidas y no determinantes para la
velocidad de la reaccin.
Limitaciones para la reaccin de Friedel y Crafts.
1. Al ser los grupos alquilo, dadores de electrones, estos aumentan la densidad
de aquellos en el anillo aromtico, y por consecuencia, facilitan la entrada de
ms de un grupo alquilo. El resultado entonces, es un producto polialquilado.
Esta dificultad experimental puede minimizarse si se tiene la precaucin de
usar un grn exceso del compuesto aromtico para que de esta manera,
disminuya la probabilidad de que un nuevo grupo alquilo presente en la
solucin se encuentre con un anillo que ya ha sido alquilado.
2. La reaccin de Friedel Crafts no se produce si se quiere alquilar un anillo
aromtico en el que se encuentre un grupo aceptor fuerte de electrones,
como por ejemplo, el grupo nitro o ciano y en general grupos sustituyentes
con efecto elctrico (-M), ya que esta reaccin es muy sensible a la
disminucin de la densidad electrnica del anillo
3. Tampoco es posible alquilar un compuesto aromtico que tenga ya algn
sustituyente de carcter bsico o con electrones no compartidos, como el
grupo amino, alquil amino o dialquilamino. Estos derivados interaccionan con
el (cido de Lewis) tricloruro de aluminio consumindolo y al mismo tiempo
formando un grupo amino cuaternario fuertemente aceptor. Vea esquema
N21, ms abajo.
151
aceptor fuerte
dador fuerte
H2N
H2N AlCl3
+
AlCl3
Esquema N21
4. Otra restricin se encuentra, al tratar de hacer reaccionar haluros de arilo o
vinilo. Estos enlaces C-halgeno son demasiado fuertes para romperlos o si
es que llegaran a romperse, lo haran tan lentamente que la reaccin sera de
poco inters prctico.
X
C
haluro de vinilo
haluro de arilo
Estructura N15
PROBLEMA
Es la siguiente proposicin verdadera o falsa?
El nitrobenceno se alquila por Friedel y Craft en la posicin meta.
Exponga al menos un argumento importante que avale su respuesta.
5.- ACILACIN DE FRIEDEL Y CRAFTS .
En esta reaccin no es posible el reordenamiento, como sucede en la
reaccin de alquilacin que acabamos de ver. Solo agrega una etapa ms al
esquema que es la reduccin del grupo carbonilo siempre que sea necesaria.
El mismo catalizador utilizado en la alquilacin de Friedel y Crafts, es decir, el
tricloruro de aluminio, colocado frente a un halogenuro de cido o anhidrido de
cido, generar una especie electroflica (Catin acilo) Ver esquema N22, capaz de
atacar un sistema aromtico y provocar la sustitucin de uno de sus hidrgenos.
152
Luego se dan ejemplos de reaciones de coordinacin halgeno aluminio y
oxgeno aluminio respectivamente:
O
R
C O
catin acilo
R
C
X AlCl3
halogenuro de
cido
O
R
C
O
XAlCl3
R
C O
catin acilo
AlCl3
OAlCl3
O
anhidrido de cido
Esquema N22
El catin acilo atacar al anillo aromtico, sin posibilidad de reordenamiento,
no como ocurre en algunos casos de la reaccin de alquilacin.
El ataque transcurre lentamente.
O
H
O
+
XAlCl3
lenta
R
XAlCl3
R
Esquema N23
Luego en una segunda etapa rpida, ocurre el ataque de la base conjugada
XAlCl3- o RCOOAlX3- , segn sea el caso, para restablecer la aromaticidad en el
sistema. Por ejemplo:
O
O
H
R
+
XAlCl3
rpida
+ AlCl3
HX
acilbenceno
Esquema N24
Las acilaciones de Friedel y Crafts, adolecen de los mismos problemas
mencionados en 2 y 3 anteriormente, para la alquilacin.
153
SNTESIS DE ALQUILBENCENOS COMO PRODUCTO DE LA REACCIN DE
REDUCCIN DE ACILBENCENOS.
Como se sabe, el grupo carbonilo C=O puede ser reducido entre otros, por el
mtodo de Clemmensen , es decir, por tratamiento del compuesto carbonlico con
amalgama de cinc y cido clorhdrico.
CH2
Zn(Hg),HCl
+ ZnCl2
+ etc.
metileno
grupocarbonilo
Esquema N25
Puede utilizarse tambin, el mtodo de Wolff-Kischner o Tioacetales como
mtodo alternativo especfico para reducir los carbonilos.
As, la secuencia completa para obtener n-propilbenceno a partir de benceno
es:
O
C CH2CH3
O
+ CH3CH2 C
AlCl3
X
HX
Esquema N26
Luego hay que reducir el grupo carbonilo usando por ejemplo, el mtodo de
Clemmensen:
O
C CH2CH3
CH2CH2 CH3
Zn(Hg),HCl
propilbenceno
Esquema N27
La alquilacin directa con ,por ejermplo, el halogenuro de alquilo
CH3CH2CH2X, no puede hacerse simplemente, porque hay un reordenamiento del
catin primario CH3CH2CH2+ a otro secundario mucho ms estable: CH 3CH+CH3,
inhibiendo al producto esperado n-propilbenceno que es muy diferente al
isopropilbenceno que es el producto principal de esta mal planificada reaccin.
154
CH2CH2CH3
CH3 CHCH3
Dos de los posibles productos de la
reaccin con ms de tres tomos de
carbono.
REACCIONES DE TRANSFORMACIN PARA LOS SUSTITUYENTES
1 COMO INTRODUCIR UNA CADENA LATERAL AL ANILLO AROMTICO.
Como lo vimos en la primera parte, (Recacin de Friedel y Crafts), hay dos
formas de llevar a cabo esta transformacin:
1.a) Por sustitucin electroflica con un halogenuro de alquilo, usando como
catalizador el tricloruro de aluminio (AlCl 3). Hay que recordar las limitaciones de esta
reaccin, que es la posibilidad de reordenamiento y la otra es la polisustitucin del
anillo debido al incremento de reactividad que se produce por el efecto elctrico
dador de la primera sustitucin alqulica en el anillo, que lo hace ms reactivo a una
segunda, tercera, etc, sustitucin.
Por ejemplo:
1.a1 Cuando hay tres o ms carbonos en una cadena a introducir, esta se
reordenar irremediablemente para llegar a un producto diferente al esperado:
H3C CH
CH3
+ CH3CH2CH2X
HX
AlCl3
Cuando solo hay dos tomos de carbono en la cadena de sustitucin no
habr reordenamiento.
1.b) La otra forma, es por sustitucin electroflica con un anhidrido o halogenuro (Cl,
o Br) de cido de dos, tres, o ms tomos de carbono, en presencia de (AlCl 3).
1.b1 Una de ellas es:
155
O
O
RCH2C
+
C
AlCl3
CH2R
+
RCH2C
RCH2C
OH
O
1.b2 La otra es:
O
O
+ RCH2C
C
AlCl3
CH2R
+ HX
X
Ambas reacciones 1.b1 y 1.b2, tienen la ventaja sobre las anteriores en que no se
produce reordenamiento.
Aqu es importante considerar que el grupo alquilo R, de la reaccin 1.a, tiene
la capacidad de orientacin para una segunda sustitucin electroflica en el anillo a
la posicin relativa orto-para.
De la misma manera, la reaccin 1.b1 y 1. b2, introducen en el anillo un grupo
acilo (RCO-), los que son orientadores meta tpicos en sntesis orgnica.
Si se reduce el grupo carbonilo por el mtodo de Clemmensen, Zn(Hg),HCl o
con Hidrazina en medio bsico (Wolff - Kischner), este grupo funcional acilo, se
transforma en un radical alquilo RCH 2-, (el grupo carbonilo CO se ha transformado
en CH2) cambiando la orientacin en una segunda sustitucin, a orto-para.
En otras palabras, la transformacin qumica del CO a CH 2, implica un cambio
elctrico fundamental del grupo sustituyente y consecuentemente en la orientacin si
se hace una segunda sustitucin en el anillo:
156
O
C
Reduccin
CH2R
CH2CH2R
orientador
orto-para
orientador
meta
El cambio de la estructura qumica del grupo funcional
implica en este caso un acambio de orientacin en una segunda
la sustitucin
2.- ALGUNAS TRANSFORMACIONES EN LA CADENA LATERAL.
Una vez introducida la cadena lateral, es posible efectuar algunas
transformaciones simples tales como:
2.a BROMACIN BENCLICA SOBRE LA CADENA
Aprovechndo la posibilidad de halogenar el carbono vecino a un doble
enlace, allico o benclico, condicin que se cumple justamente en el carboco unido
al anillo, llamado benclico, por el mecanismo de radicales libres (Ver tambin el
captulo de alquenos), utilizando la N-bromosuccinimida como inductor, con lo que
es relativamente fcil obtener un producto halogenado como el que se muestra a
continuacin:
Br
CH2
CH
NBS
2.b FORMACIN DEL DOBLE ENLACE EN LA CADENA
2.b1 El tratamiento de un halogenuro de alquilo o arilo con una base fuerte como
el hidrxido alcalino (KOH), da lugar a la formacin de un doble enlace en la cadena
lateral por una simple eliminacin de HBr.
CHBr
CH2R
CH
CHR
OH
H2O
La amida sdica, tambin es una buena base para obtener el doble enlace en
un halogenuro de alquilo o arilo:
157
CHBr
CH2R
CH
CHR
NaNH2/NH3
NaBr
He aqu otro ejemplo de como introducir un doble enlace en una cadena
lateral:
Br
CH2CH2CH3
CH
CHCH2CH3
NBS
CHCH3
KOH/EtOH
Esquema N33
Esta secuencia muestra la manera ms comn de introducir un halgeno en
una cadena lateral, y crear posteriormente por eliminacin un doble enlace al tratar
el compuesto con una base fuerte como el hidrxido.o amida sdica Ahora bin,
sobre este doble enlace, pueden aplicarse todas las reacciones de alquenos que ya
se han visto anteriormente. (Ver captulo 3)
2.c-TRANSFORMACIONES QUE PUEDEN HACERSE SOBRE UN DOBLE
ENLACE EN UNA CADENA LATERAL.
2.c.1-Tambin, a partir de un doble enlace, es posible crear un grupo
funcional aldehido -CHO como sustituyente en el anillo aromtico. Para esto, solo
basta con la ozonolisis del compuesto en cuestin:
CH
CHR
CHO
O 3/Zn (H2O)
Zn(OH)2
RCHO
2.c.2- Si se utiliza un oxidante ms enrgico, como por ejemplo el KMNO4 en
medio cido, se logra la formacin de cido benzoico:
158
CH
CHR
COOH
KMnO4/H2SO4
+ RCOOH
MnO2,H2O
2.c.3 Pero si el compuesto aromtico no posee hidrgenos alfa, obtendremos
una cetona (Recuerde que la oxidacin a cido carboxlico de una cadena lateral de
un anillo aromtico se produce solamente si en el carbono alfa hay por lo menos un
tomo de hidrgeno).
CH3
CH3
C
CHR
KMnO4/H2SO4
MnO2,H2O
O
+ RCOOH
La oxidacin de un anillo aromtico con permanganato de potasio en medio
cido no lo afecta; solo afecta las cadenas laterales sin importar su estructura
aliftica, y lo ms importante es que tengan al menos un hidrgeno benclico. La
oxidacin conduce a la formacin de un grupo carboxilo en el carbono benclico,
perdindose el resto de la cadena. Ntese que aqu hay un cambio de orientacin
del sustituyente al ir desde alquilo orientador o-p (activador) a carboxilo orientador m
(desactivador)
hidrgeno benclico
COOH
CHR2
KMnO4/H
Esquema N39
Otro ejemplo:
159
hidrgenos benclicos
COOH
KMnO4/H
COOH
Esquema N40
3.-OBTENCIN DE UN DIHALOGENURO VECINAL
3.a Dentro de estas reacciones de alquenos est la adicin de bromo en
tetracloruro , obtenindose asi un dihalogenuro vecinal.
CH
CHBr
CHCH3
CHBrCH3
Br2/CCl4
Esta reaccin es importante para la obtencin de un triple enlace. Ya que al
ser tratado con una base fuerte como el amiduro de sodio en amonaco, se produce
un alquino.
CHBr
CHBrCH3
NaNH2/NH3 (lquido)
CH3 + NaBr
La presencia de un triple enlace en la cadena lateral, habre la posibilidad de
aplicar sobre l, las transformaciones qumicas ya vistas en el captulo de los
alquinos, como por ejemplo Hidratacin con disiamilborano (DSMB)
O
C
DSMB/ H2O
H2O2,OH
O
CH2R
CH2
Obteniendo una mezcla compleja de cetonas aromticas isomricas.
4.-COMO OBTENER UNA AMINA A PARTIR DE NITROBENCENO:
160
Por simple reduccin con cinc y cido clorhdrico, se puede reducir el grupo
nitro a amino.
NO2
NH2
Zn/HCl
Esquema N34
NO2
NH2
Zn/HCl
NO2
NH2
Esquema N35
Si hay dos grupos nitro, puede reducirse solo uno de ellos por reaccin con
polislfuro de amonio:
NO2
NH2
(NH4)2Sx
NO2
NO2
Esquema N36
5.- OBTENCIN Y UTILIZACIN DE LAS SALES DE DIAZONIO EN SNTESIS
El tratamiento de la amina aromtica con nitrito de sodio en medio cido
clorhdrico y a baja temperatura, produce un compuesto qumico llamado cloruro de
161
bencenodiazonio o comunmente una sal de diazonio. Estas sales son muy
inestables a temperatura ambiente y por lo tanto deben ser mantenidos a una
temperatura inferior a los 5C para poder utilizarlas posteriormente. Como se podr
ver, es un intermediario muy importante en los procesos sintticos de la qumica
orgnica:
NH2
N 2 Cl
NaNO2/HCl
5C
sal de diazonio
Esquema N37
La utilidad de las sales de diazonio queda demostrada en el esquema de ms
abajo:
OH
Cl
CN
H2O,H
N 2 Cl
CuCN
HCl,Cu2Cl2
I
HBr,Cu2Br2
KI
Br
H3PO2
Diagrama N7
Las sales de diazonio pueden ser fcilmente transformadas en los respectivos
halogenuros de arilo por tratamiento de la sal con el respectivo halogenuro cuproso.
Esta transformacin se llama reaccin de Sandmeyer. Por otro lado, los ioduros de
arilo se obtienen al tratar la sal de diazonio con ioduro de potasio. Ver el diagrama
N7 ms arriba.
162
Con cianuro cuproso se puede introducir un grupo nitrilo al anillo,
obteniendose el benzonitrilo que es un valioso intermediario para obtener cidos
benzoicos y otros compuestos:
COOH
CN
H3O
Esquema N38
Si la sal de diazonio se calienta en agua, se obtiene fenol. No hay otro
mtodo tan simple y directo para introducir un grupo OH en un anillo aromtico.
Finalmente, el tratamiento de la sal de diazonio con cido hipofosforoso, nos
permite remover el grupo N2+ (diazonio) y as poder aprovechar el efecto orientador
de un grupo nitro o amino para introducir otro grupo sustituyente antes de su
eliminacin.
DISUSTITUCIN ELECTROFLICA AROMTICA EN EL BENCENO.
Designemos como G al grupo sustituyente en el benceno.
La pregunta importante que es necesario hacerse al querer hacer una segunda
sustitucin sobre el anillo es: Cmo influye elctricamente este grupo ya
sustituido en la reactividad del sistema aromtico?.
Para responderla, lo que debemos hacer es simplemente: clasificar los diferentes
tomos y/o grupos de tomos que configuran el sustituyente G, segn los efectos
elctricos inductivo (I) y mesomrico (M). (Ver tambin el captulo 2) Intuitivamente
es vlido suponer que, la suma y magnitud relativa de estos dos efectos en el
sustituyente debera darnos una idea general del comportamiento elctrico del grupo
en el sistema aromtico.
Examinemos cuidadosamente los diferentes tipos de sustituyentes.
Se conocen tres tipos de sustituyentes, segn las magnitudes relativas de los
efectos elctricos inductivo (I) y mesomrico (M). Estos son:
1) Grupos con efecto (+I, +M) que son:
1a.- Aquellos que estn unidos al resto de la molcula por un tomo de
carbono sp3 (Vea que el valor de la electronegatividad del C= 2,5 y del
hidrgeno H= 2,2) y este a su vez, a hidrgenos o a otro carbono con carga
formal = 0. Ejemplo de estos grupos es: -CH3, -CH2R, -CHRR, -CRRR.
163
1b.- Aquellos grupos inicos como: O -, o el carboxilato COO -, los cuales
poseen una gran densidad electrnica. Son en general bases conjugadas de
cidos fuertes.
Todos ellos son dadores netos de electrones. Son incapaces de recibir o
acomodar cualquier incremento de carga electrnica extra.
2) Grupos con efecto (-I, +M)
En esta categora de sustituyentes hay que diferenciar dos subgrupos:
2a.- Aquellos grupos en los cuales el efecto inductivo (-I), parece ser muy
pequeo en valor absoluto, comparado con el efecto mesomrico (+M), lo que
estara implicando un efecto elctrico neto dador.
Estos tomos o grupos de tomos que conforman el sustituyente, se
caracterizan por estar unidos al resto de la molcula por un tomo ms
electronegativo que el carbono, (O, N) de ah su efecto (-I) y por otro lado,
tener pares de electrones no compartidos, los que pueden ser cedidos al
sistema pi, a travs de una efectiva superposicin de orbitales del tipo p. Este
ltimo efecto es ptimo si el tamao de aquellos orbitales atmicos son de un
tamao similar. Vea la figura de ms abajo. Esto se da entre el Carbono y el
Oxgeno o el Nitrgeno.
C N
C O
Son tomos que estn ubicados en la misma fila o perodo de la tabla
peridica, es decir, usan orbitales 2p de igual tamao para una efectiva
deslocalizacin.
Ejemplo de este tipo de sustituyentes es:
OH
OCH3
NH2
NHR
OR
NRR
2b.- Aquellos grupos en los cuales el efecto inductivo (I) predomina sobre el
efecto mesomrico (+M)
En este caso, el efecto elctrico neto es aceptor.
Entre estos grupos de sustituyentes estn aquellos en los que el tomo
directamente unido al resto de la molcula pertenece al tercer, cuarto o quinto
perodo o fila de la tabla peridica. (S, Cl, Br, I)
Estos tomos, son todos ms electronegativos que el carbono, por eso,
presentan un efecto inductivo negativo o (-I)
Como poseen pares de electrones desapareados, deberan presentar
un comportamiento dador o efecto mesomrico positivo (+M), sin embargo,
debido a que los orbitales atmicos p del carbono comparado en tamao con
164
los del azufre y halgenos tales como cloro, bromo y yodo, son tan diferentes
que la efectividad de la deslocalizacin electrnica de esos pares es mnima.
Vea la figura de ms abajo.
Esto pone de manifiesto el hecho de que prevalezca el efecto inductivo
negativo (-I) por sobre el mesomrico (+M) y entonces el efecto elctrico neto
del sustituyente es de aceptor.
Ejemplo de estos grupos sustituyentes es:
Cl
SCH3
Br
3) Grupos con efecto elctrico (-I, -M)
El tercer tipo de sustituyente es aquel que presenta un efecto elctrico inductivo
(-I) y un efecto mesomrico (-M). Estos son grupos aceptores netos.
El tomo del grupo unido al resto de la molcula es el carbono. Sin embargo,
este carbono siempre est unido a otro ms electronegativo, por lo que presenta un
efecto elctrico inductivo negativo (-I).
La electronegatividad de un tomo como el nitrgeno o el oxgeno, producen
asimetra en la densidad electrnica del enlace sigma entre ambos tomos,
aumentando as la electronegatividad del carbono, creando de esta manera un
fuerte efecto elctrico inductivo (-I) sobre el resto de la molcula.
enlace sigma
165
En este tipo de sustituyente, el enlace entre estos tomos es adems de tipo
mltiple, doble o triple. Por lo tanto tambin intervienen enlaces de tipo pi. Por
ejemplo:
O
C
Q
Donde Q puede ser:
OR
OH
NH2
NHR
NRR'
Como todos los tomos involucrados pertenecen al mismo perodo en la tabla
peridica (filas), los orbtales 2p son similares y el efecto elctrico mesomrico (-M)
de estos grupos se manifiesta fuertemente sobre todo el sistema pi de la molcula.
Un enlace mltiple entre carbono, nitrgeno y oxgeno, con diferente
electronegatividad da lugar a enlaces polarizados, con la densidad de carga
negativa sobre el tomo ms electronegativo. As se puede observar en los grupos
de esta categora:
O
O
C
Hay otro sustituyente que ha sido dejado aparte porque no interviene el tomo
de carbono en su estructura como tomo directamente unido al resto de la molcula,
este es el grupo nitro
Aqu el tomo del grupo que est unido al resto de la molcula, es el
nitrgeno, que pertenece al mismo perodo que el carbono en la tabla peridica. El
tamao de los orbitales atmicos es semejante y por lo tanto, el efecto mesomrico
se manifiesta fuertemente. Por otro lado, el nitrgeno (3,0) que es ms
electronegativo que el carbono (2,5), hace que este grupo presente un pronunciado
efecto atractor (-I) sobre el resto de la molcula.
166
O
N
O
En este grupo, tambin hay enlaces de tipo pi entre tomos de diferente
electronegatividad, ( O= 3,4; N= 3,0) de ah la aparicin de un fuerte efecto elctrico
mesomrico (-M), semejante al resto de los grupos de este tipo.
En resumen, el resultado de esta doble accin, es hacer que el tomo de
nitrgeno del grupo que est unido directamente al resto de la molcula, sea
deficiente electrnicamente en su entorno, a travs de su enlace sigma (-I) y
deficiente tambin a travs de su enlace pi (-M). Sus dos efectos elctricos
negativos apuntan en el mismo sentido y por tanto es un grupos netamente atractor
de electrones.
En general, entonces, gracias a la combinacin de estos mecanismos
elctricos, los sustituyentes, son capaces de hacer variar la reactividad de las
molculas, donde y cuando ellos estn presentes.
Como lo veremos ahora y a grandes rasgos, los grupos sustituyentes se
manifiestan de dos maneras: cediendo electrones o captando electrones hacia s. Es
decir, hay solo dos alternativas considerando a G como el grupo sustituyente:
(a): Si G es un grupo dador de electrones (+I,+M) y (-I,+M), las diferentes
densidades de carga elctrica en el anillo se distribuirn, como puede observarse
claramente en las estructuras contribuyentes (B), (C) y (D):
167
el grupo G es un
dador de electrones
G
(A)
(B)
(C)
(D)
Diagrama N5
Ntese que el grupo dador, aumenta la densidad electrnica en el anillo en
las posiciones 2-4 y 6, es decir, en orto y para con respecto al sustituyente G.
Un grupo electroflico, evidentemente atacar aquellas posiciones que
muestren una mayor densidad electrnica. Por esa razn a este grupo dador G, se
le llama orientador orto-para y su velocidad de reaccin ser mayor mientras mayor
sea la densidad de carga inducida, en comparacin con la densidad electrnica en
el anillo del benceno. En otras palabras, un grupo activador aumentar la densidad
electrnica en las posiciones orto y para relativa al sustituyente G, y la velocidad de
reaccin frente al ataque de un electrfilo, ser con relacin al benceno, mayor
mientras mayor sea el aumento de densidad electrnica inducida.
Por ejemplo:
op
op
op
E
+
E
Mezcla de productos
168
Debe agregarse que dentro del conjunto de grupos activadores (Ver en el
recuadro la tabla N2), los ltimos, es decir los alquilos son activadores dbiles, y
del resto, las dos primeras filas corresponden a los grupos activadores ms fuertes.
NH2 ,
OH ,
NR2
NHR ,
OCH3 ,
OR
NHCOCH3 ,
NHCOR
CHR2
CH3,
CH2R,
grupos activadores y orientadores orto-para
Tabla N2
b): Cuando el grupo sustituyente G en el benceno es un aceptor, la distribucin de la
densidad electrnica en el anillo cambia radicalmente en comparacin al caso del
grupo dador.
Diagrama N6
Observando las estructuras contribuyentes, se encuentra que la posicin
meta es la que presenta una mayor densidad de carga relativa, dentro del anillo
sustituido, pero, si se la compara con el benceno, esta ser menor.
Por ejemplo:
169
m
E
E
Todos aquellos grupos que tienen un comportamiento similar al descrito, se
les llama grupos desactivadores y son orientadores meta en una segunda
sustitucin electroflica aromtica. Pertenecen a aquellos grupos caracterizados
elctricamente por sus efectos (-I,-M).
COR,
CONH2,
CN,
COOH,
COOR,
CONR2
CONHR,
NO2 ,
CHO
NR3
grupos desactivadores y orientadores meta
Tabla N3
Un caso especial lo presentan los halgenos. El efecto elctrico neto de estos
grupos hace que ellos sean atractores de electrones por lo que desactivan al anillo
aromtico, sin embargo, como poseen electones no compartidos en su capa
electrnica externa, su efecto produce orientacin orto- para. Estos grupos orientan
la sustitucin electroflica a las posiciones orto y para, pero como son
desactivantes, su velocidad de reaccin ser menor a la velocidad de reaccin
del benceno.
F ,
Cl ,
Br ,
grupos desactivadores, pero orientadores orto para.
Tabla N4
170
PROBLEMA:
Dibuje las estructuras de los productos principales de la reaccin de
mono nitracin para cada uno de ellos usando una mezcla de HNO 3/H2SO4.
NO2
OH
CH3
(2)
(3)
Br
NHCH3
NH3
(1)
(4)
(5)
Haga un esquema de sntesis para obtener (Y) a partir de benceno y
cualquier otro reactivo orgnico o inorgnico necesario:
(Y)
Br
CHO
CRITERIOS PARA DEFINIR LA ORIENTACIN EN UN BENCENO YA
DISUSTITUIDO
Que sucede con la orientacin hacia la sustitucin, cuando se desea
predecir el producto que resulta de hacer una nueva reaccin de sustitucin en un
anillo bencnico donde ya hay de antemano dos sustituyentes?
Experimentalmente se ha encontrado que segn el tipo de sustituyentes
presentes previamente en el anillo, es posible notar ciertas tendencias que permiten
hacer buenas estimaciones con relacin al producto que se espera al hacer
experimentalmente la reaccin.
Estas tendencias pueden ser agrupadas en forma gruesa, en tres grupos,
segn la combinacin de los efectos elctricos de los sustituyentes:
Caso (A): Donde ambos grupos son (+I,+M) o (-I,+M) y cualquier combinacin entre
ellos. Sus condiciones experimentales (Por ejemplo: temperatura y presin) son
generalmente suaves. Estos grupos son orientadores orto-para (op). De manera
que si op1=op2, entonces tendremos que:
a1.- Ambos sustituyentes iguales en posicin orto uno con respecto al otro:
171
op1
op 1
op 2
op1
op2
op2
+
E
E
Mezcla de productos
Si op1op2, entonces se obtendr una mezcla compleja de productos. Por
ejemplo:
OH
OH
CH3
CH3
+
OH
OH
CH3 E
+
E
OH
CH3
CH3
+
E
E
Mezcla compleja de productos
a2.- Los sustituyentes iguales op1 y op2 estn en posicin meta uno con respecto
al otro:
op 1
op1
E
op2
op1
E
+
op2
op2
E
Producto principal
En el ejemplo que sigue ahora, op1 y op2 son diferentes y ambos
sustituyentes tienen aproximadamente la misma capacidad orientadora, sin
embargo, es de esperar que por la disposicin de los grupos, por ejemplo, CH 3 y Cl,
aquella sustitucin que se producira entre ambos sustituyentes debera tener un
menor rendimiento.
Es lo que se conoce como impedimento estrico, y los dos productos
restantes sern los productos posibles o ms probables.
172
Cl
Cl
E
E
H3C
Cl
Cl
E
+
H3C
+
H3C
H3C
E
productos principales de la reaccin
a3.- Ahora, si los sustituyentes estn en posicin para uno respecto al otro y si
op1=op2, entonces deberamos esperar que el producto de esta reaccin sea:
op1
op 1
E
op2
op 2
Si op1 op2, el sustituyente ms fuerte dirigir la sustitucin. Sin embargo, el
producto final de la reaccin estar fuertemente contaminado. Estas son reacciones
rpidas en condiciones ptimas de temperatura. Por ejemplo:
OH
OH
OH
E
+
E
CH3
CH3
CH3
Mezcla compleja de productos
contaminados
Caso B: Uno de los sustituyentes es director orto-para, es decir, pertenece a los
grupos (+I, +M) o (-I, +M). El otro pertenece al grupo (-I,-M), es decir, orientador a la
posicin meta.
Aqu se pueden presentar los siguientes casos:
b1.- Sus posiciones relativas son orto, y de acuerdo con nuestros conocimientos
previos, producirn:
173
op
op
m
op
m
m
+
E
Mezcla de productos
El siguiente ejemplo muestra que la direccin de la sustitucin esta dirigida
por el sustituyente activador. En este caso el grupo -CH 3:
NO2
NO 2
CH3
NO2
CH3
CH3
+
Mezcla de productos
b2.-En el siguiente caso, se obtendr una mezcla de productos, aun cuando ser el
grupo op quin dirija la sustitucin. Sin embargo es de esperar tambin la
contaminacin con el compuesto producido por la accin directora del grupo m.
op
op
E
m
op
op
E
y
+
m
E
Mezcla de productos
Prod. secundario
El producto secundario, debido al impedimento estrico provocado por los
grupos originales en posicin relativa meta, no sobrepasa generalmente el 5% del
total de los productos.
Por ejemplo:
174
CH3
CH3
CH3
CH3
y
CN
+
CN
CN
CN
E
Prod. secundario
Mezcla de productos
b3.- Aqu los sustituyentes estn en posicin relativa para, y hay que esperar otra
vez que aquel sustituyente orientador op sea el que mande en la orientacin por
sobre m. La posicin de ambos sustituyentes hace que entre ellos se refuercen para
dar solo un nico producto. Ntese que en este caso hay un reforzamiento en el
efecto orientador de ambos grupos.
op
op
E
m
nico producto
Debera esperarse una reaccin relativamente lenta en condiciones ptimas,
debido a la presencia en el anillo aromtico, de un grupo desactivador.
CH3
CH3
E
NH4
NH4
nico producto
Otro caso simple como el anterior en que los grupos presentes en el anillo
refuerzan sus efectos orientadores es:
175
E
NH2
NH2
E
NO2
NO2
aqu hay refuerzo en la orientacin
El grupo NH2 orienta a orto y para, siempre que el medio no sea fuertemente
cido. El NO2 es orientador meta y sus efectos coinciden en la posicin orto con
relacin al grupo amino.
NH2
Orienta op
Orienta m
NH3
medio cido
La orientacin del grupo amino cambia de op a m por
protonacin en un medio cido.
Si el medio fuera fuertemente cido se hace necesario proteger el grupo
amino evitando as su protonacin.
Su proteccin se logra haciendo reaccionar la fenilamina con anhidrido
actico para formar la acetanilida, mucho menos bsica que el grupo amino -NH 2 ,
conservando la orientacin op.
NHCOCH3
NH2
(CH3CO)2O
+ CH3COOH
(CH3CO)2O es el anhidrido actico
La recuperacin posterior del grupo amino se realiza facilmente mediante un
calentamiento suave de la acetanilida en medio cido.
176
NHCOCH3
NH3 O2CCH3
cido diluido
Caso C: Cuando ambos grupos sustituyentes son (-I,-M), es decir, son ambos
desactivadores u orientadores meta, (mi), aparecen estas tres posibilidades segn
las posiciones relativas de los sustituyentes:
c1.- En este caso, ambos sustituyentes son iguales, lo que hace que el producto
sea nico:
m1
m1
m2
m2
E
nico producto
Sin embargo, si los sustituyentes son diferentes, entonces aparecern las
complicaciones. El producto esperado estar altamente contaminado:
NO2
NO 2
NO 2
CN
CN
CN
+
E
E
Mezcla de productos
c2.- Ambos grupos sustituyentes son iguales y son orientadores meta, Por su
posicin relativa, ellos se refuerzan entre si dando entonces solo un producto.
177
m1
m1
E
m2
m2
nico producto
De la misma manera, si ellos son diferentes darn por su orientacin relativa
en el anillo, un solo producto. Por ejemplo:
NO2
NO 2
E
CHO
CHO
c3.- La posicin relativa para entre los sustituyentes se refuerza siempre que ambos
sean iguales.
m1
m1
E
m2
m2
nico producto
Si m1 m2, entonces esta vez habr mezclas complicadas en todos los
casos,
178
NO2
NO2
NO2
+
E
COOR
COOR
COOR
Todas las reacciones del tipo C sern por supuesto, ms lentas con respecto
a las mismas reacciones con el benceno, debido a que en este caso, ambos grupos
sustituyentes son desactivadores
PROBLEMA:
De al menos dos argumentos que permitan decidir si el p-dimetilbenceno
(p-Xileno) es ms reactivo en una reaccin de sustitucin electroflica que el pclorotolueno.
ALGUNAS SNTESIS DE COMPUESTOS AROMTICOS
POLISUSTITUIDOS:
Sera imposible abarcar la enorme variedad de compuestos que se pueden
obtener, aplicando a su sntesis, las reacciones generales que hemos visto hasta
este momento. Sin embargo resulta til hacer algunos comentarios generales.
Cuando se planea una sntesis de un compuesto aromtico, uno de los
hechos importantes que hay que tener en cuenta es, la correcta secuencia de
introduccin de los sustituyentes. Este orden est basado en la aplicacin del
conocimiento de lo que es, la activacin o desactivacin y la orientacin de los
diferentes grupos qumicos involucrados.
Por ejemplo
Si se quiere sintetizar la molcula aromtica trisustituida que se muestra ms
abajo, se ver que es importante el orden en que se vayan introduciendo cada
sustituyente:
Haga un esquema de sntesis pra obtener(A), a partir de benceno.
179
NO 2
CH3
Cl
O
(A)
Primero: Si usted nitra el benceno, no podr acilar por Friedel y Crafts en una etapa
posterior, puesto que este es un gropo desactivador.
Segundo: Si usted clora primero, este grupo que es orientador o,p no le permitir
introducir los otros grupos que estn en posiciones relativas meta.
Por lo tanto, queda la nica posibilidad que es primero acilar. Luego, nitrar, no clorar
porque este orientara la nitracin a posiciones o,p con relaci a l. Finalmente
clorar.
NO2
NO2
Cl2/FeCl3
NO2
CH3COCl
AlCl3
CH3
CH3
CH3
Cl
O
(A)
Otro ejemplo:
Se quiere sintetizar el p-nitrotolueno y el m-nitroclorobenceno a partir de
benceno y cualquier otro reativo orgnico e inorgnico necesario. Proponga un
esquema de sntesis:
CH3
Cl
NO2
NO2
Estructura N16
En el primer caso, debemos tener en cuenta que el nitro es un orientador
meta y el metilo es un orientador orto-para. Como la posicin relativa de ambos
sustituyentes es para del uno con respecto al otro, resulta lgico proceder a
introducir primero el grupo metilo en el benceno. En el segundo caso se debe
introducir primero el grupo nitro (orientador meta) y este orientar posteriormente la
introduccin del cloro (que es orientador para) a la posicin meta.
180
Otro ejemplo:
Si se desea obtener 1-nitro-2,4-dibromobenceno a
nitrobenceno. Esta es una de las posibles secuencias de sntesis:
NO2
de
NO2
NO2
(NH4)xS
HNO3/H2SO4
NH2
NO2
NO2
NO2
NO2
Br2/FeBr3
partir
Br
1 NaNO2/HCl
Br
2 H3PO2
NH2
NH2
Br
Br
Esquema N41
En este caso se ha aprovechado la activacin y orientacin del grupo amino
para dirigir la introduccin de los dos tomos de bromo. Posteriormente el grupo
amino se lleva a sal de diazonio y se elimina con cido hipofosforoso.
De otra manera, si reducimos primero el grupo nitro a amino, entonces, a
partir de anilina podemos llegar al mismo producto. El elegir uno u otro camino de
sntesis depender entre otras cosas del nmero de pasos necesarios, mientras
menos pasos sean necesarios, ms simple ser la secuencia sinttica, o bin la
disponibilidad de reactivos lo ms simples y baratos posibles etc.
NH2
NH2
N2 Cl
Br
Br2/FeBr3
Br
Br
HNO2/HCl
Br
181
NO2
N2 Cl
Br
Br
H3PO2
Br
Br
HNO3/H2SO4
Br
Br
Esquema N42
En este caso, tambin se aprovecha la orientacin del grupo amino para
introducir los bromos y luego se elimina. Por ltimo se nitra, aprovechando ahora la
orientacin reforzada de los dos bromos.
Ejemplo:
Se desea sintetizar el p-nitrobenzoico a partir de benceno:
Las orientaciones de ambos grupos son meta y por lo tanto si quiero llegar a
un compuesto con los sustituyentes en posicin relativa para, ninguno de ellos me
sirve. Sin embargo, se sabe que el metilo es un orientador para y me ser til para
introducir el grupo nitro en esa posicin relativa. Entonces se metila primero el
benceno mediante la reaccin de Friedel y Crafts con un halogenuro de metilo como
reactivo:
CH3
CH3Br
AlCl3
Esquema N43
La nitracin del tolueno produce una mezcla de ismeros los que pueden ser
separados por algn mtodo fsico adecuado:
182
CH3
CH3
CH3
NO2
HNO3/H2SO4
NO2
el p-nitrotolueno es el producto principal
y puede ser separado por recristalizacin
Esquema N44
Ahora se puede oxidar el grupo metilo para obtener el producto deseado.
CH3
COOH
KMnO4/H
NO2
NO2
Esquema N45
Que habra sucedido si se oxida primero el metilo y luego se nitra?
orientador
orientador meta
orto-para
CH3
COOH
KMnO4/H
COOH
HNO 3/H2SO4
NO2
Esquema N46
Otro ejemplo:
Se quiere sintetizar el cido o-bromobenzoico:
183
Sabemos que el bromo es un orientador o-p y el COOH es un orientador
meta, pero sabemos adems que el metilo que es un orientador o-p y que puede ser
transformado posteriormente en carboxilo por oxidacin del metilo con
permanganato de potasio en medio cido, por lo tanto se puede optar por introducir
cualquiera de ellos primero el metilo o el bromo. Sin embargo, el bromo es un
desactivante en cambio el metilo es un activante y aunque dbil ser ms rpida la
reaccin con este ltimo.
CH3
CH3Br/AlCl3
CH3
CH3
CH3
Br
Br2/FeBr3
Br
Esquema N47
Ntese que se produce una mezcla de productos en esta etapa, sin embargo,
uno puede forzar la reaccin ahora, para que se produzca principalmente el
producto orto, con la ayuda de un grupo que pueda ser posteriormente removido:
CH 3
CH 3
SO 3 H
SO3 /H2SO4
+
SO3 H
Esquema N48
CH3
184
La eficiente separacin del ismero para y la halogenacin de este
compuesto sulfonado para su posterior hidrlisis, permite obtener un producto con
muy bun rendimiento.
CH3
CH3
CH3
Br
Br2/FeBr3
SO3H
Br
H2SO4 dil.
SO3H
Esquema N49
Solo resta oxidar el metilo con KmnO4 en medio cido.
COOH
CH3
Br
Br
KMnO4 / H
Esquema N50
Que es el producto esperado.
Otro ejemplo:
Hacer un esquema de sntesis para obtener con buen rendimiento, el 1bromo-2-clorobenceno a partir de clorobenceno y cualquier otro reactivo orgnico e
inorgnico necesario:
Cl
Cl
Cl
NaNO2/H2SO4
NO2
+
NO2
185
Hay que separar ambos ismeros por algn mtodo fsico, como por ejemplo
la recristalizacin, y proseguir la sntesis con el ismero adecuado.
Cl
Cl
Br
Br2/FeBr3
NO2
NO2
Aprovechando la orientacin reforzada inducida por el cloro y el grupo nitro, y
luego la eliminacin del grupo clorurodiazonio (N2+Cl-) con cido H3PO2:
Cl
Br
1) Zn/HCl
Cl
Br
2) H3PO2
NO2
Hay otro grupo como el sulfnico (SO3H), que es fcilmente eliminado
produciendo el mismo efecto del grupo nitro en la orientacin y sustitucin (Ver el
ejemplo anterior).
Cl
Cl
Cl
SO3/H2SO4
SO 3H
+
SO3H
Deben ser separados por algn metodo fsico
antes de proseguir con la sntesis.
186
Cl
Cl
Br
Br2/FeBr3
SO 3H
SO 3H
Este grupo es eliminado por simple calentamiento a reflujo del compuesto en
una solucin de cido sulfrico diluido.
Cl
Cl
Br
H2SO4/H2O
Br
Reflujo
SO3H
Estos mtodos de sntesis son adecuados para obtener buen rendimiento y
pureza, siempre que esa posible obtener una buena separacin de los ismeros
orto-para de los nitrados o de los sufonados.
PROBLEMA:
Examine, cada una de las siguientes estructuras y ordnelas de mayor a
menor segn su reactividad, frente a un halogenuro de alquilo y en presencia
de AlCl3. Justifique su eleccin brevemente.
187
NO2
OH
CH3
(2)
(3)
Br
NHCH3
NH3
(1)
(5)
(4)
Trate de hacer un esquema de sntesis para los dos siguientes
compuestos aromticos (A) y (B) a partir de benceno y cualquier otro reactivo
orgnico e inorgnico necesario.
O
CH2CCH3
CH2CHO
(B)
(A)
NO2
Br
PROBLEMA:
Haga un esquema de sntesis para obtener a partir de benceno y
cualquier otro reactivo orgnico o inorgnico SOLO UNA de las siguientes
estructuras:
CH3
CH2CH2
HO
CHCH2OH
Br
(A)
(B)
PROBLEMA:
Proponer y hacer un anlisis de un esquema de sntesis para el 3,5dibromofeniletileno a partir de benceno y cualquier otro reactivo orgnico e
inorgnico:
188
CH
CH2
Br
Br
En primer lugar, por las posiciones relativas de los sustituyentes, la
introduccin del primer halgeno debe venir solo si hay previamente un sustituyente
con orientacin meta. Por esta razn, el primer sustituyente en el anillo debe ser
orientador meta y de dos tomos de carbono.
En segundo lugar, los dos halgenos no pueden provenir de una
halogenacin directa sobre el anillo con bromo en presencia de tribromurofrrico.
Solo uno de ellos puede venir de aquel orientador meta. Cul es la razn de esta
afirmacin?. La razn es que si hay uno de los halgenos ya introducido en el
compuesto, este grupo es orientador o-p, y asumir la direccin de la siguiente
halogenacin.
COCH3
O
CH3C
Cl
AlCl3
Este grupo orientador meta puede adicionar un tomo de bromo en posicin
meta. Posteriormente, hay que tener presente una regla general sobre orientacin,
que dice que un grupo orientador orto-para como es el bromo este el caso, mandar
sobre el orientador meta en una subsiguiente sustitucin.
COCH3
COCH3
Br2/FeBr3
Br
As, en la siguiente sustitucin, donde manda el halgeno bromo como
orientador o-p, resultar en una mezcla como la siguiente:
189
COCH3
COCH3
COCH3
COCH3
Br Br
Br2/FeBr3
+
Br
Br
Br
Br
Br
La reduccin del grupo carbonilo con Clemmensen previamente a la
halogenacin, redundar en la obtencin de una mezcla ms compleja que la ya
descrita.
Queda entonces la posibilidad de introducir el segundo bromo por
transformacin de un grupo nitro que es orientador meta. As, se tiene la siguiente
secuencia:
COCH3
COCH3
HNO2/H2SO4
NO 2
Ambos sustituyentes son orientadores meta y forzarn la halogenacin
fuertemente a la posicin meta relativa a aquellos dos.
COCH3
COCH3
Br2/FeBr3
NO2
Br
NO2
Luego, se reduce el grupo carbonilo con Clemmensen y el nitro con Zn/HCl,
obteniendo:
CH2CH3
CH2CH3
1.- Zn/HCl
2.- Zn(Hg),HCl
Br
NO2
Br
NH2
Cmo se puede ahora introducir el otro tomo de bromo a partir de esta
estructura?
190
Recuerde que el grupo nitro puede ser transformado en amino o sal de
diazonio. La sal de diazonio puede ser a su vez transformada en (Ver el esquema)
en Cl, Br, I, CN, OH, H.
CH2CH3
CH2CH3
NaNO2/HCl
Br
NH2
Br
N2 Cl
El tratamiento de la sal cloruro de diazonio con bromuro cuproso (Reaccin
de Sandmeyer), resulta en:
CH2CH3
CH2CH3
Br2Cu2
Br
Br
Br
N2 Cl
Por ltimo, el doble enlace en la cadena lateral se obtiene con una
halogenacin benclica (bromacin) con NBS y posterior tratamiento del producto de
reaccin con una base fuerte como el hidrxido de potasio en etanol como solvente.
CH2CH3
CH
CH2
1) NBS
2)KOH/CH3CH2OH
Br
Br
Br
Br
LA RETROSNTESIS
Cuando se dominan los pasos de transformacin, como los que se han visto
previamente en varios captulos, es posible analizar y proponer un esquema de
sntesis comenzando desde el producto y en diversas etapas coherentes, llegar
hasta los reactivos dados. No hay duda de que esta forma de ver una sntesis
requiere, entre otras actitudes, tener mucha experiencia en la forma en que se hacen
las modificaciones estructurales de las molculas, como as tambin ser capaz de
visualizar a partir de la estructura del producto, las posibles estructuras precursoras.
Por ejemplo, se plantea el siguiente ejercicio.
191
Proponga usted una va retrosinttica para obtener el compuesto qumico (A),
a partir de benceno, utilizando para ello cualquier mtodo, reactivo orgnico e
inorgnico y la condicin experimental necesario.
CH
CH2
(A)
A simple vista, este compuesto invita a pensar que:
a) Hay un doble enlace en una cadena lateral, el cual puede ser obtenido a
travs de dos mtodos simples.
Una de ellas es mediante una reaccin de deshidrohalogenacin como la que se
muestra a continuacin (Ver captulo de alquenos)
CHBr
CH
CH3
CH2
KOH/EtOH
(X)
Si la sntesis tiene su punto de partida en el benceno, entonces, debe
recurrirse a Friedel y Crafts para obtener el precursor (X) a partir del benceno
ramificado.
Si la cadena lateral es ms larga, debe usarse la acilacin para evitar los
reordenamientos. Por supuesto que la cadena hidrocarbonada en el anillo, se tiene
cuando se reduce el grupo carbonilo (CO) con un mtodo apropiado como por
ejemplo el de Clemmensen.
O
O
RCX
AlCl3
Cuando el nmero de tomos de carbono de la cadena lateral es menor a
tres, es vlido el uso del bromuro de alquilo directamente puesto que no hay
posibilidad de reordenamiento en la cadena.
192
En este caso particular el grupo alquilo es etilo.
CH2CH3
CH3CH2X
AlX3
Etilbenceno
Y finalmente, la relacin que hay entre etilbenceno y el 1-etilbenceno
bromado es claramente la halogenacin (bromacin) de esta molcula. Esto se logra
con NBS.
CHBrCH3
CH2CH3
NBS
Etilbenceno
La otra opcin es utilizando la reaccin de Wittig (Ver captulo de los
alquenos)
CHBr
CH
1) Ph3P, RLi
(Y)
2) HCHO
CH2
193
PROBLEMAS DEL CAPTULO COMPUESTOS AROMTICOS:
1.-Haga un esquema retrospectivo de sntesis para los siguientes compuestos (A) y
(B), hasta llegar a benceno como el reactivo principal disponible. Usted puede usar
cualquier otro reactivo orgnico e inorgnico y condicin experimental.
CH(OH)CH3
CH2CH2OH
(B)
(A)
Cl
Br
2.-Haga un esquema de sntesis del compuesto (A) a partir del benceno y cualquier
otro reactivo orgnico e inorgnico necesario:
(A)
Br
3.- Escriba un esquema de sntesis para obtener 2-(p-nitrofenil)etanol (A) a partir de
benceno y cualquier otro reactivo orgnico e inorgnico necesario.
NO2
(A)
CH2CH2OH
4.- Escriba un esquema de sntesis para obtener el compuesto (A) a partir de
benceno y cualquier otro reactivo orgnico e inorgnico necesario.
194
O
CH2CCH3
(A)
OH
5.- Escriba un esquema de sntesis para obtener el compuesto (A) a partir de
benceno, y cualquier otro reactivo orgnico e inorgnico necesario.
NH2
(A)
CH2CHO
6.- Haga un esquema de sntesis para la transformacin:
HOCHCH2CH2CH3
?
Cl
Utilizando cualquier reactivo orgnico e inorgnico necesario.
7.- Haga un esquema de sntesis para la transformacin:
CH2CHO
?
Br
Utilizando cualquier reactivo orgnico e inorgnico necesario.
8.- A partir de benceno y cualquier reactivo orgnico de no ms de tres tomos de
carbono y cualquier reactivo inorgnico necesario, haga un esquema de sntesis
para (A):
195
CH2
CH3
(A)
9.- Al tratar de hacer una nitracin del 2-fenil-2-butanol con una mezcla nitrante
(HNO3/H2SO4), se produjo inesperadamente 2-metanitrofenil-2-buteno:
a) Escriba un mecanismo de reaccin que d cuenta de la formacin del
producto inesperado.
b) Proponga entonces usted, un esquema de sntesis para la obtencin del 2para-nitrofenil-2-butanol
OH
CH3
CH3CH2
2-fenil-2-butanol
10.- Haga un esquema de sntesis para la siguiente molcula (A), a partir de
benceno o tolueno. Usted dispone adems de cualquier otro reactivo orgnico e
inorgnico necesario.
H
H3C
(A)
OH
11.- La conocida aspirina es un derivado acetilado del cido 2-hidroxibenzoico.
Sobre la base de las reacciones que usted conoce:
a) Proponga un esquema de sntesis del cido 2-hidroxibenzoico, a partir de
benceno y cualquier otro reactivo orgnico e inorgnico necesario.
b) Nombre segn IUPAC cada intermediario que aparezca en el esquema de
sntesis propuesta por usted.
12.- Para los siguientes compuestos aromticos:
196
a)
b)
c)
Cl
NO2
NH2
CH3
(A)
(B)
(C)
(D)
Prediga y ordene, de mayor a menor, su reactividad relativa frente a la
mononitracin, en un medio fuertemente cido.
Indique la posicin de la mononitracin.
Dibuje en base a su respuesta en los puntos a) y b). Cul y donde
estar sustituido el producto principal frente a una segunda nitracin?.
13.- Obtener (Y) a partir de benceno y cualquier otro reactivo orgnico o inorgnico
necesario:
(Y)
Br
CHO
14.- Haga un esquema de sntesis para los tres compuestos (A) (B) y (C) a partir de
benceno. Usted dispone adems de cualquier otro reactivo orgnico e inorgnico
necesario.
CO2H
NH2
Br
CCH 2CH 3
NO2
(A)
(B)
(C)
Cl
NO2
Br
15.- (a) A partir de benceno y cualquier otro reactivo orgnico e inorgnico
necesarios, sintetice los cidos (A) y (B).
197
CO 2H
CO2H
(B)
(A)
NH2
NO2
(b) Como podra, utilizando (A) o (B) como punto de partida, obtener los cidos (C),
(D),(E) y (F). Haga un esquema simple de sntesis para cada caso (sin indicar el
mecanismo):
CO 2H
CO2H
(D)
(C)
CO 2H
(E)
CO2H
(F)
CN
Cl
OH
16.- Haga un esquema de sntesis para SOLO UNO de los dos siguientes
compuestos aromticos a partir de benceno y cualquier otro reactivo orgnico e
inorgnico necesario.
O
CH2CCH3
CH2CHO
(B)
(A)
NO2
Br
17.- Disee, a partir de benceno y cualquier otro reactivo orgnico e inorgnico
necesario, los esquemas de sntesis para dos de las cuatro molculas cuyas
estructuras se muestran mas abajo:
198
CH
CH
CH
COOH
Br
(A)
(B)
como nico producto
en la ltima etapa de la sntesis
NH2
CH
CH
CH2
Cis
(C)
(D)
NO2
También podría gustarte
- Introducción a la química de los metales de transiciónDe EverandIntroducción a la química de los metales de transiciónAún no hay calificaciones
- Compuestos AromaticosDocumento26 páginasCompuestos AromaticosCharly Jose Carlos100% (1)
- Hidrocarburos AromaticosDocumento69 páginasHidrocarburos AromaticosElvis Rogers PakitaAún no hay calificaciones
- Hidrocarburos AromaticosDocumento54 páginasHidrocarburos AromaticosTatiana jazmin Neyra vergaraAún no hay calificaciones
- Benceno y DerivadosDocumento58 páginasBenceno y DerivadosEduardo DegiorgioAún no hay calificaciones
- CH 21 AromaticosDocumento70 páginasCH 21 AromaticosRobert Velázquez LucianoAún no hay calificaciones
- Separata Aromáticos 1Documento12 páginasSeparata Aromáticos 1Elver TuestaAún no hay calificaciones
- Tema 9 QODocumento66 páginasTema 9 QOmaritzasotitoAún no hay calificaciones
- BencenoDocumento65 páginasBencenoEsme PilcoAún no hay calificaciones
- AromaticidadDocumento6 páginasAromaticidadMilagros Valinotti GaunaAún no hay calificaciones
- Quimica Organica 2 Unidad 3Documento30 páginasQuimica Organica 2 Unidad 3AharónVázquez0% (1)
- Tema 1.1Documento11 páginasTema 1.1Yhoselyn MareñoAún no hay calificaciones
- 12 QuimicaDocumento26 páginas12 QuimicaRAY NIKKY DAMIAN GRONERTHAún no hay calificaciones
- AlquenosDocumento41 páginasAlquenosMosh Torres100% (1)
- Planta de de Hidrocarburos AromaticosDocumento3 páginasPlanta de de Hidrocarburos Aromaticosnoelia cossioAún no hay calificaciones
- Guía Del Curso QUÍMICA ORGÁNICA I (1311)Documento30 páginasGuía Del Curso QUÍMICA ORGÁNICA I (1311)Celso MéndezAún no hay calificaciones
- Guia AromaticosDocumento10 páginasGuia AromaticosYolehidis Franchesca Sena VasquezAún no hay calificaciones
- Hidrocarburos CiclicosDocumento5 páginasHidrocarburos CiclicosMario Tenorio PerezAún no hay calificaciones
- Clase Alquenos, Alquinos, AromaticosDocumento21 páginasClase Alquenos, Alquinos, Aromaticosnobody :bAún no hay calificaciones
- Hidrocarburos Alifáticos y Aromáticos TrabajoDocumento6 páginasHidrocarburos Alifáticos y Aromáticos TrabajoRossanaMarquezDiazAún no hay calificaciones
- Benceno EstructuraDocumento51 páginasBenceno Estructuraeuduardo100% (1)
- Aromaticidad PDFDocumento68 páginasAromaticidad PDFMARIAAún no hay calificaciones
- Benceno 2 - 6 Por HojaDocumento3 páginasBenceno 2 - 6 Por HojaMario MartinAún no hay calificaciones
- Compuestos AromáticosDocumento53 páginasCompuestos AromáticosJEAN CAMILO PORRAS RICOAún no hay calificaciones
- Quimica Del PetroleoDocumento40 páginasQuimica Del PetroleoCarlos Alejandro100% (1)
- Tema IV. Compuestos AromáticosDocumento27 páginasTema IV. Compuestos AromáticosVenusAún no hay calificaciones
- Resúmenes de Los TemasDocumento50 páginasResúmenes de Los TemasMiguel Dominguez EugenioAún no hay calificaciones
- Material de Aromaticos-ClaseDocumento25 páginasMaterial de Aromaticos-ClaseMaritza HernandezAún no hay calificaciones
- Tema2 AlquenosDocumento34 páginasTema2 AlquenosMiranda DanielAún no hay calificaciones
- Hidrocarburos Aromaticos III 2020Documento11 páginasHidrocarburos Aromaticos III 2020Jessenia Ponce VillatoroAún no hay calificaciones
- Compuestos AromaticosDocumento11 páginasCompuestos AromaticosLuis MiguelAún no hay calificaciones
- Resonancia y AromaticidadDocumento30 páginasResonancia y AromaticidadRicardo Alfonso Trujillo SantillanaAún no hay calificaciones
- Prácticas Resueltas. Química OrgánicaDocumento20 páginasPrácticas Resueltas. Química OrgánicaFabiola BallesteroAún no hay calificaciones
- Química Del CarbonoDocumento12 páginasQuímica Del CarbonoJesus DiazAún no hay calificaciones
- Clase 17 Tema VI LG. Clase 14 Tema V BUDocumento45 páginasClase 17 Tema VI LG. Clase 14 Tema V BURolleros unidosAún no hay calificaciones
- Compuestos Aromáticos Equipo 1Documento55 páginasCompuestos Aromáticos Equipo 1Dalia SantosAún no hay calificaciones
- Taller de Química Orgánica PDFDocumento16 páginasTaller de Química Orgánica PDFMaría José Lopez RuizAún no hay calificaciones
- Hidrocarburos AromaticosDocumento12 páginasHidrocarburos AromaticosEstefy Patiño OrellanaAún no hay calificaciones
- Tema 6 QODocumento48 páginasTema 6 QODANY HERNANDEZ HERNANDEZAún no hay calificaciones
- Guia AromaticosDocumento8 páginasGuia AromaticosReyna RomanoAún no hay calificaciones
- AR-I Presentación Aromáticos MonosustituidosDocumento50 páginasAR-I Presentación Aromáticos MonosustituidosConstantino AquilesAún no hay calificaciones
- Expo Quimica 5Documento43 páginasExpo Quimica 5Victor RodriguezAún no hay calificaciones
- Compuestos-Aromaticos y Alcvoholes ExposicionDocumento13 páginasCompuestos-Aromaticos y Alcvoholes ExposicionSidalia Mercedes Taveras0% (1)
- Taller de Bioquimica.Documento19 páginasTaller de Bioquimica.Ángel MestraAún no hay calificaciones
- Química Intermedio Pre 9Documento12 páginasQuímica Intermedio Pre 9Mai 37Aún no hay calificaciones
- Benceno y DerivadosDocumento65 páginasBenceno y DerivadosGustavo Lagos100% (1)
- Hidrocarburos AromaticosDocumento46 páginasHidrocarburos AromaticosSandra OzAún no hay calificaciones
- Hidrocarburos AromaticosDocumento14 páginasHidrocarburos AromaticosSidalia Mercedes TaverasAún no hay calificaciones
- Tema 9 QODocumento66 páginasTema 9 QOAlexander Rojas TorresAún no hay calificaciones
- Compuestos AromaticosDocumento50 páginasCompuestos Aromaticoseuaa_9201100% (6)
- Informe Hidrocarburos Aromaticos Chamaco Mamani Leslie LisbethDocumento15 páginasInforme Hidrocarburos Aromaticos Chamaco Mamani Leslie LisbethJhoselyn Isabel Usmayo QuispeAún no hay calificaciones
- Aromaticidad TautomeriaDocumento11 páginasAromaticidad TautomeriaceabymmbtAún no hay calificaciones
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaDe EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaCalificación: 5 de 5 estrellas5/5 (1)
- La tabla periódica de los elementos químicosDe EverandLa tabla periódica de los elementos químicosCalificación: 1 de 5 estrellas1/5 (1)
- Escuela Preparatoria Oficial Anexa A La Normal de AtlacomulcoDocumento10 páginasEscuela Preparatoria Oficial Anexa A La Normal de AtlacomulcoLulu CruzAún no hay calificaciones
- Guía de Ejercicios N°1 Parte BDocumento1 páginaGuía de Ejercicios N°1 Parte BTriz MaruAún no hay calificaciones
- Ácidos y BasesDocumento7 páginasÁcidos y BasesibethAún no hay calificaciones
- 7-Equilibrios Acido Base IIDocumento33 páginas7-Equilibrios Acido Base IIGabriela Margarita Loza CasaAún no hay calificaciones
- Lab. 03 - Análisis Del Grupo Ii de CationesDocumento21 páginasLab. 03 - Análisis Del Grupo Ii de CationesJhonatan EGAún no hay calificaciones
- Test Diagnóstico para Hidrocarburos Aromáticos - Test de Le Rosen y Test de Friedel y CraftsDocumento13 páginasTest Diagnóstico para Hidrocarburos Aromáticos - Test de Le Rosen y Test de Friedel y Craftslemuel avilaAún no hay calificaciones
- Apuntes de Formulacion InorganicaDocumento11 páginasApuntes de Formulacion Inorganicacaumente14Aún no hay calificaciones
- 4 To QUIMDocumento38 páginas4 To QUIMVillegas F. EdsonAún no hay calificaciones
- Nomenclatura IDocumento3 páginasNomenclatura IMaría GutiérrezAún no hay calificaciones
- Aldehídos y CetonasDocumento4 páginasAldehídos y CetonasCatherine JaimeAún no hay calificaciones
- Quimica ElvaDocumento10 páginasQuimica ElvaJefferson Loor RamirezAún no hay calificaciones
- 2° Informe de Analitica CDocumento9 páginas2° Informe de Analitica CGERSON MARTIN CUCHO FERNANDEZAún no hay calificaciones
- Guia de Aprendizaje Quimica 11Documento17 páginasGuia de Aprendizaje Quimica 11Yisely Carolaen Criollo CabezasAún no hay calificaciones
- Agentes QuelantesDocumento7 páginasAgentes QuelantesLuis DiazAún no hay calificaciones
- Apunte 1 quimica-IIIDocumento24 páginasApunte 1 quimica-IIILeire León LeónAún no hay calificaciones
- Practica 5 OBTENCIÓN Y PROPIEDADES DE LOS HIDRÓXIDOSDocumento6 páginasPractica 5 OBTENCIÓN Y PROPIEDADES DE LOS HIDRÓXIDOSjuliette beilzaAún no hay calificaciones
- Sintesis de Esteres Beta NerolinaDocumento7 páginasSintesis de Esteres Beta NerolinadanielAún no hay calificaciones
- EJERCICIOS TEMA 2.leyes y Conceptos Básicos en QuímicaDocumento5 páginasEJERCICIOS TEMA 2.leyes y Conceptos Básicos en Químicavictor.b.i.villadeaspeAún no hay calificaciones
- Grupo CarboniloDocumento4 páginasGrupo CarboniloRuben Villamizar FlorezAún no hay calificaciones
- 6to QuimicaDocumento5 páginas6to Quimicaroberto lazoAún no hay calificaciones
- Laboratorio VirtualDocumento2 páginasLaboratorio VirtualLuz Sierra CondorchoaAún no hay calificaciones
- Cuestionario de Organica2.0Documento13 páginasCuestionario de Organica2.0Viviana lisseth Arce GuzmanAún no hay calificaciones
- Estequiometria I - EjerciciosDocumento3 páginasEstequiometria I - EjerciciosAna Maria Hernandez Farfan100% (1)
- Exposicion Quimica HIDROXIDOSDocumento13 páginasExposicion Quimica HIDROXIDOSPerlita Del Mar AntonioAún no hay calificaciones
- HIDROCARBUROSDocumento31 páginasHIDROCARBUROSCRISTOPHER ANDERSON CASTRO GAMARRAAún no hay calificaciones
- DeshidratacionDocumento6 páginasDeshidratacionFiorella MiglioAún no hay calificaciones
- Taller Equilibrio Acido - Base - KpsDocumento1 páginaTaller Equilibrio Acido - Base - KpsYundra MoralesAún no hay calificaciones
- Actividad 15-ACIDO-BASEDocumento3 páginasActividad 15-ACIDO-BASEJoseph Diaz QAún no hay calificaciones
- Informe #1 - Solubilidad y Clasificación Por SolventesDocumento5 páginasInforme #1 - Solubilidad y Clasificación Por SolventesIlario MinnarAún no hay calificaciones
- Complejos MetalicosDocumento12 páginasComplejos MetalicosshimatzuAún no hay calificaciones