Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cloruro de Sodio Uziel
Cargado por
Uziel Cosme Ojeda0 calificaciones0% encontró este documento útil (0 votos)
7 vistas8 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas8 páginasCloruro de Sodio Uziel
Cargado por
Uziel Cosme OjedaCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 8
CLORURO DE SODIO
El cloruro de sodio, sal común o sal de
mesa, denominada en su forma mineral
como halita, es un compuesto químico con
la fórmula NaCl. El cloruro de sodio es una
de las sales responsables de la salinidad
del océano y del fluido extracelular de
muchos organismos.
HISTORIA
En la antigüedad, el cloruro de sodio era
muy apetecido como un bien transable y
como condimento, y se remuneraba en la
época preclásica romana a los soldados
que construían la Vía Salaria, que
empezaba en las canteras de Ostia hasta
Roma, con un generoso salarium
argentum. También era el salario de un
esclavo, ya que se entregaba una pequeña
bolsa con sal; por lo que la palabra
asalariado tiene un significado
etimológicamente peyorativo.
PROPIEDADES QUIMICAS
Propiedades químicas
Es un compuesto iónico formado por un catión sodio (Na+) y un anión cloruro (Cl-),
y ,puede sufrir las reacciones características de cualquiera de estos dos iones. Como
cualquier otro cloruro iónico soluble, precipita cloruros insolubles cuando es agregado a
una disolución de una sal metálica apropiada, como nitrato de plata:
NaCl(aq) + AgNO3(aq) → AgCl(s) + NaNO3(aq)
Otro método para separar ambos componentes es mediante la electrólisis.
Si se aplica una corriente eléctrica continua con un elevado potencial a una salmuera
alcalina, el producto anódico es gas dicloro (Cl2) y los catódicos son hidróxido de sodio
(NaOH) y dihidrógeno (H2).
electrólisis: 2 NaCl(aq) → 2 NaOH(aq) + Cl2(gas) + H2(gas)
Como la mayoría de las sales iónicas confiere propiedades coligativas a sus
disoluciones, es decir, es capaz de variar la presión de vapor de la disolución, elevar el
punto de ebullición y descender el punto de congelación según su concentración molal
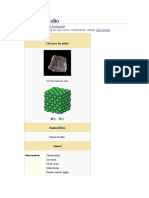
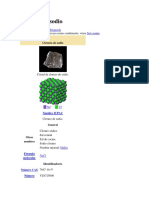
ESTRUCTURA
La estructura del cloruro de sodio (NaCl) se describe como
un empaquetamiento cúbico centrado en las caras (c.c.c.)
de aniones cloruro (Cl-) en el que todos los huecos
octaédricos se encuentran ocupados por los cationes sodio
(Na+), según se deduce de la aplicación de la regla de
relación de radios , aunque su celdilla unidad puede
describirse utilizando tanto (a) cationes en los vértices y
centros de las caras de un cubo como (b) aniones en los
vértices y centros de las caras de un cubo. No obstante, es
de destacar que, atendiendo a la regla de la relación de
radios, la descripción de la celdilla unidad con cationes en
los vértices y centros de las caras NO SIGNIFICA que la
estructura pueda describirse como un empaquetamiento de
cationes sodio cuyos huecos octahédricos estan todos
ocupados por los aniones cloruro.
PROPIEDADES
Punto de ebullición 1465ºC
Punto de fusión 801ºC
Fácil disolución en el agua 35.9g/100 ml a 25ºC
Solubilidad en amoniaco 2.15 g/100 ml solubilidad en
metanol 1.49 g/100 ml (Soluble en etilenglicol, glicerol,
glicol y ácido fórmico)
insoluble solo en ácido clorhídrico
PH neutro
Masa moral de 58.443 g/mol
No es inflamable y su densidad es de 2.165 g/cm3.
No se obtiene ningún tipo de reacción ante otros
compuestos químicos, de normal se requiere la adición
de energía para alcanzar una reacción química
(electrólisis de NaCI en agua y forma gas de cloro).
PRODUCCION
El cloruro de sodio es producido en masa
por la evaporación de agua de mar o
salmuera de otros recursos, como lagos
salados, y minando la roca de sal, llamada
halita.
En 2002, la producción mundial de sal se
estimó en 210 millones de toneladas
métricas, y los principales países
productores fueron Estados Unidos (40.3
millones de toneladas), China (32.9),
Alemania (17.7), India (14.5) y Canadá
(12.3)
APLICACIONES
El cloruro de sodio es usado universalmente como aditivo alimentario.
También se usa en la producción de papel y celulosa, en los productos de
baño y en detergentes.
Antiséptico local y preservante de alimentos
La sal, gracias a su elevado poder osmótico, es capaz de deshidratar un
amplio espectro de virus y bacterias en estado no esporulado, por lo que se
usa como un doloroso antiséptico para desinfectar heridas.
Muy pocos microorganismos, como los halófilos y organismos superiores
como los crustáceo braquiópodos conocidos como las Artemias, pueden
resistirse al poder osmótico de la sal. Entre los microorganismos resistentes a
la salinidad está el caso de la bacteria B. marismortui, encontrada en el mar
Muerto.
La salazón de la carne es una forma de preservar ésta de la acción
bacteriana, ya que la sal retrasa la descomposición proteínica. Para preservar
alimentos, el cloruro de sodio extrae el agua de estos, impidiendo el
PRODUCTOS
También podría gustarte
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAAún no hay calificaciones
- Cloruro de SodioDocumento10 páginasCloruro de SodioJohn Rafael Carrillo DolugarAún no hay calificaciones
- Cloro y Sosa CausticaDocumento15 páginasCloro y Sosa CausticaLuxainne Tremont EchegarayAún no hay calificaciones
- Tema de TesisDocumento18 páginasTema de TesisJose Carlos Huamani QuicañoAún no hay calificaciones
- Cloruro de SodioDocumento10 páginasCloruro de SodiobetshabeAún no hay calificaciones
- Cloruro de SodioDocumento12 páginasCloruro de Sodiovict1992Aún no hay calificaciones
- Cloruro de SodioDocumento7 páginasCloruro de SodioJuan Carlos MosqueraAún no hay calificaciones
- Trabajo de ProcesoDocumento11 páginasTrabajo de ProcesoAlexander A TorresAún no hay calificaciones
- Trabajo sobre las propiedades y usos del cloruro de sodioDocumento8 páginasTrabajo sobre las propiedades y usos del cloruro de sodioshiAún no hay calificaciones
- Cloruro de Sodio (NaCl) - Estructura, Propiedades, UsosDocumento10 páginasCloruro de Sodio (NaCl) - Estructura, Propiedades, UsosCarlosAún no hay calificaciones
- Estudio de Los Principales Grupos y Elementos de La Tabla PeriodicaDocumento23 páginasEstudio de Los Principales Grupos y Elementos de La Tabla PeriodicaAntonio Palacios BautistaAún no hay calificaciones
- Obtencion de NAOHDocumento18 páginasObtencion de NAOHClaudia Madeleyne Espinoza ReynosoAún no hay calificaciones
- Proceso Cloro-Soda: Producción de Cloro, Soda Cáustica e Hidrógeno a Partir de NaClDocumento22 páginasProceso Cloro-Soda: Producción de Cloro, Soda Cáustica e Hidrógeno a Partir de NaClAsdrúbalDanielPerezAún no hay calificaciones
- Acido Clorhídrico: ObjetivoDocumento9 páginasAcido Clorhídrico: ObjetivoLuis Ignacio AstroñaAún no hay calificaciones
- MoleculaDocumento16 páginasMoleculaAlexsoulAún no hay calificaciones
- Estudio de CasoDocumento6 páginasEstudio de CasoErik BlancoAún no hay calificaciones
- Solidificacion de MetalesDocumento5 páginasSolidificacion de MetalesJuan Carlos Angles BetancurtAún no hay calificaciones
- Agua RegiaDocumento10 páginasAgua RegiaSheyla Rios CalzadillaAún no hay calificaciones
- Justificacion Teorica e ExperimentalDocumento6 páginasJustificacion Teorica e ExperimentalAnonymous 8QDfPXmaAAún no hay calificaciones
- Proceso Cloro SodaDocumento18 páginasProceso Cloro SodaMarcelo Alegria100% (1)
- Familia IA - 011 SodioDocumento5 páginasFamilia IA - 011 SodioTiffani Estrella EstrellaAún no hay calificaciones
- Fabricacion Industrial de La Potasa IDocumento16 páginasFabricacion Industrial de La Potasa IEdgar Alexander DBAún no hay calificaciones
- Obtencion Del Hidroxido de Sodio NaOH Trabajo TerminadoDocumento16 páginasObtencion Del Hidroxido de Sodio NaOH Trabajo TerminadoAngel Calderon Eche100% (1)
- QUIMICA INORGANICA .-Clase IIDocumento41 páginasQUIMICA INORGANICA .-Clase IINieve PerezAún no hay calificaciones
- Sal común: propiedades y usosDocumento4 páginasSal común: propiedades y usosivanjcm85Aún no hay calificaciones
- Purificacion de Cloruro de SodioDocumento7 páginasPurificacion de Cloruro de SodiocelimarAún no hay calificaciones
- Purificacion de Cloruro de SodioDocumento7 páginasPurificacion de Cloruro de SodiocelimarAún no hay calificaciones
- Diagrama de Flujo Proceso SolvayDocumento15 páginasDiagrama de Flujo Proceso Solvayjerc1324Aún no hay calificaciones
- Obtencion de Naoh Por ElectrolisisDocumento2 páginasObtencion de Naoh Por ElectrolisisIsrael Grover Condorcet MancillaAún no hay calificaciones
- Cloruro de Sodio (NaCl)Documento15 páginasCloruro de Sodio (NaCl)KAROLINA FLORES DUARTEAún no hay calificaciones
- Cloruros Formula de La Sal 10K de Sal Por 200 Litros de Agua - 07 - 07Documento9 páginasCloruros Formula de La Sal 10K de Sal Por 200 Litros de Agua - 07 - 07Martin IbarraAún no hay calificaciones
- Industria de La Sosa CausticaDocumento26 páginasIndustria de La Sosa CausticaHéctor Faya SánchezAún no hay calificaciones
- Obtencion de NAOH Por Metodos ElectroquímicosDocumento8 páginasObtencion de NAOH Por Metodos ElectroquímicosDiego Javier100% (3)
- Acfrogabwiu7nq3bwfwrr4 Yymsqxhsuuptomdbqenl8ba7xwbzxvnzgr6ah Sfcp5pjl9gyttxoqctpujbt90fzc27sdsybk2fqqfwlp5l7tdnnwzbfdcfi ZWRT Dpsiludelkgo45vukj8i60Documento43 páginasAcfrogabwiu7nq3bwfwrr4 Yymsqxhsuuptomdbqenl8ba7xwbzxvnzgr6ah Sfcp5pjl9gyttxoqctpujbt90fzc27sdsybk2fqqfwlp5l7tdnnwzbfdcfi ZWRT Dpsiludelkgo45vukj8i60Jesus C. BuenoAún no hay calificaciones
- El OxalatooooDocumento10 páginasEl OxalatooooCesar RamirezAún no hay calificaciones
- Preparación de Cloro e Hidróxido de Sodio Por ElectrólisisDocumento18 páginasPreparación de Cloro e Hidróxido de Sodio Por Electrólisisricardo100% (1)
- AlcaliDocumento12 páginasAlcaliQf Jhon DonadoAún no hay calificaciones
- Sodio Metalico PERFILDocumento8 páginasSodio Metalico PERFILANGIE STYLES100% (1)
- Ácido ClorhídricoDocumento9 páginasÁcido ClorhídricoEdgar A. GeroldAún no hay calificaciones
- Industria Del Cloro-AlcaliDocumento50 páginasIndustria Del Cloro-AlcaliJorge BautistaAún no hay calificaciones
- ClorosodaDocumento16 páginasClorosodawinderAún no hay calificaciones
- Agua RegiaDocumento4 páginasAgua RegiaKaren Eliana Gutierrez Huahuasonco100% (1)
- Sales alcalinas: carbonato de sodioDocumento49 páginasSales alcalinas: carbonato de sodioEdgar Jose Paez VicuñaAún no hay calificaciones
- Dureza de AguaDocumento31 páginasDureza de AguaWilliam SmithAún no hay calificaciones
- ÁCIDO SULFÚRICO.. TrabajoDocumento38 páginasÁCIDO SULFÚRICO.. Trabajoadrianaemilys0% (2)
- Informe Transformaciones de La Materia DesarrolloDocumento4 páginasInforme Transformaciones de La Materia Desarrolloabrahamurbina88Aún no hay calificaciones
- Tipos de Yacimiento de Sales en MexicoDocumento12 páginasTipos de Yacimiento de Sales en MexicoIrvin Ca OsAún no hay calificaciones
- Solucion Base 0,02NDocumento10 páginasSolucion Base 0,02NQuiqueRiosaSanchezAún no hay calificaciones
- Agua RegiaDocumento4 páginasAgua RegiaEccler Huashuayllo Castillo100% (1)
- 03 NaCl IPP2Documento43 páginas03 NaCl IPP2alvaroAún no hay calificaciones
- Diapos de La Soda CaústicaDocumento12 páginasDiapos de La Soda CaústicaJaqueline Vilcapuma0% (1)
- CLORHIDRICODocumento9 páginasCLORHIDRICOMARIO LINO CABRERAAún no hay calificaciones
- Curso TRATAMIENTO DE AGUA PARA CALDERASDocumento49 páginasCurso TRATAMIENTO DE AGUA PARA CALDERASJorge Daniel Moreno IralaAún no hay calificaciones
- AguaDocumento7 páginasAguaMarlis RodriguezAún no hay calificaciones
- Reacciones Endotérmicas y ExotérmicasDocumento12 páginasReacciones Endotérmicas y ExotérmicasJenni armstrongAún no hay calificaciones
- NaCl PropiedadesDocumento4 páginasNaCl PropiedadesHector MolinaAún no hay calificaciones
- Propiedades físicas y químicas de la sal y la anhidritaDocumento23 páginasPropiedades físicas y químicas de la sal y la anhidritaCarlosAún no hay calificaciones
- Propiedades químicas del agua y su importanciaDocumento198 páginasPropiedades químicas del agua y su importanciaHenry Bajaña Guevara100% (1)
- Hipoclorito TareaDocumento31 páginasHipoclorito TareaCristhianMontañoAún no hay calificaciones
- 05-12-16 Oficio Multiple 146-2022 Control en La Puerta de Ingreso (R) (R)Documento1 página05-12-16 Oficio Multiple 146-2022 Control en La Puerta de Ingreso (R) (R)Eddy Peralta GuzmanAún no hay calificaciones
- FINAL MergedDocumento97 páginasFINAL MergedREDES SALUDAún no hay calificaciones
- InfografíaDocumento1 páginaInfografíaRaquel Aznar GarciaAún no hay calificaciones
- Oscilaciones amortiguadas masa-resorteDocumento21 páginasOscilaciones amortiguadas masa-resorteJoseph Silva OrdonezAún no hay calificaciones
- MENOGUIAPATOLOGIAVULVARDocumento60 páginasMENOGUIAPATOLOGIAVULVARLilly MejiaAún no hay calificaciones
- 2.actividad Domiciliaria.2018Documento7 páginas2.actividad Domiciliaria.2018Angel Huaman AclariAún no hay calificaciones
- Convertidores BuckDocumento9 páginasConvertidores BuckEduard Vega AyalaAún no hay calificaciones
- Reseña Critica Gerencia Estrategica de Costos Jose PadillaDocumento2 páginasReseña Critica Gerencia Estrategica de Costos Jose PadillaJose Padilla SenhaAún no hay calificaciones
- Desarrollando Mis Capacidades - 1Documento1 páginaDesarrollando Mis Capacidades - 1Abigail RuizAún no hay calificaciones
- Actividades TISGDocumento2 páginasActividades TISGNicolás MincraftianoAún no hay calificaciones
- Introducción A Las Técnicas VolumétricasDocumento10 páginasIntroducción A Las Técnicas VolumétricasYaritza VerdugaAún no hay calificaciones
- 4 Sumatoria de Fuerzas y TorquesDocumento4 páginas4 Sumatoria de Fuerzas y TorquesEduardo BalbucaAún no hay calificaciones
- Cálculo de Las Fuerzas, Tiempo y Aceleración Que Actúan Sobre Un Auto en Movimiento Por Un Plano InclinadoDocumento25 páginasCálculo de Las Fuerzas, Tiempo y Aceleración Que Actúan Sobre Un Auto en Movimiento Por Un Plano InclinadoLuis Peralta MartinAún no hay calificaciones
- ARSI U1AA2 Metodología Uveg OkDocumento9 páginasARSI U1AA2 Metodología Uveg OkJuan Manuel Rodriguez Mendez0% (1)
- Aglutinantes y AglomeradosDocumento20 páginasAglutinantes y AglomeradosAngie Julieth Montaña BarretoAún no hay calificaciones
- requisitosRETCC ConDocumento3 páginasrequisitosRETCC ConHender Samuel Teran EspinozaAún no hay calificaciones
- Sobre El Concepto y Medida Del Tecnoestrés-Una RevisiónDocumento9 páginasSobre El Concepto y Medida Del Tecnoestrés-Una RevisiónLuzmi RosasAún no hay calificaciones
- Dureza materiales ensayos Brinell Rockwell VickersDocumento32 páginasDureza materiales ensayos Brinell Rockwell VickersPaula Sanchez RegueraAún no hay calificaciones
- Impactos Ambientales Generados Por Avances TecnológicosDocumento15 páginasImpactos Ambientales Generados Por Avances TecnológicosYOINER EDWARDO TORRES ANGULOAún no hay calificaciones
- 05 - TIRISTORES - e - DISPOSITIVOS DE DISPARO - IGBT - 2021Documento25 páginas05 - TIRISTORES - e - DISPOSITIVOS DE DISPARO - IGBT - 2021Damarys A. Ulloa S.Aún no hay calificaciones
- Factura educación crédito cobroDocumento3 páginasFactura educación crédito cobroVerito BasalduaAún no hay calificaciones
- Boletín 4140 - Información ProyectadaDocumento4 páginasBoletín 4140 - Información ProyectadaArantxa GarcíaAún no hay calificaciones
- Borrador Proyecto Feria de CienciasDocumento9 páginasBorrador Proyecto Feria de CienciasToxic FherAún no hay calificaciones
- Trabajo Sociedad de Gananciales D.F.SDocumento19 páginasTrabajo Sociedad de Gananciales D.F.SLuis Miguel Sillocca CarranzaAún no hay calificaciones
- Prospecto 2020Documento65 páginasProspecto 2020Luis BarbozaAún no hay calificaciones
- 2-Probabilidad CondicionalDocumento13 páginas2-Probabilidad CondicionalPablo Bourlot0% (1)
- 10 Proyectos Sencillos y Explicados para Empezar Con Arduino 4Documento89 páginas10 Proyectos Sencillos y Explicados para Empezar Con Arduino 4Gonzalez GinoAún no hay calificaciones
- Aparato Locomotor - Anatomìa HumanaDocumento33 páginasAparato Locomotor - Anatomìa HumanaEdizon QRAún no hay calificaciones
- Calor, cambios de estado y entropíaDocumento14 páginasCalor, cambios de estado y entropíaOmar CarrascoAún no hay calificaciones
- Anamnesis-Ecológica Editable2Documento6 páginasAnamnesis-Ecológica Editable2Paloma Valdés100% (1)