0% encontró este documento útil (0 votos)
11 vistas8 páginasTema 8. Ciclo Celular
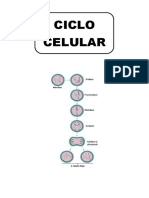
El ciclo celular es un proceso que incluye la duplicación y división celular, dividido en fases G1, S, G2 y M en eucariotas, con mecanismos de control que aseguran su correcta ejecución. Los complejos ciclina-Cdk regulan las transiciones entre fases y son activados e inactivados mediante fosforilación y degradación. Factores de crecimiento y señales externas influyen en la proliferación celular, mientras que la senescencia y apoptosis son procesos que limitan la división celular.
Cargado por
Noelia Lázaro RodriguezDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
11 vistas8 páginasTema 8. Ciclo Celular
El ciclo celular es un proceso que incluye la duplicación y división celular, dividido en fases G1, S, G2 y M en eucariotas, con mecanismos de control que aseguran su correcta ejecución. Los complejos ciclina-Cdk regulan las transiciones entre fases y son activados e inactivados mediante fosforilación y degradación. Factores de crecimiento y señales externas influyen en la proliferación celular, mientras que la senescencia y apoptosis son procesos que limitan la división celular.
Cargado por
Noelia Lázaro RodriguezDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd