Documentos de Académico
Documentos de Profesional
Documentos de Cultura
V de Cow Practica 3 Control
V de Cow Practica 3 Control
Cargado por
CAROL SANABRIA SIÑANIZ0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaTítulo original
V de cow practica 3 control
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaV de Cow Practica 3 Control
V de Cow Practica 3 Control
Cargado por
CAROL SANABRIA SIÑANIZCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
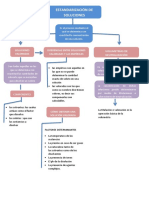
PREPARACIÓN Y
ESTANDARIZACIÓN DE REACTIVOS
DOMINIO PREGUN DOMINIO
CONCEP TA DE METODO
Fundamento: El control en un proceso que sirve para Procedimiento:
demostrar que los procedimientos realizados son adecuados ¿Cómo se puede describir la forma
para el fin propuesto. Se estandariza el sistema analítico y el correcta para preparar una Preparar la solución de hidróxido de sodio a
método. Intervalo de concentración de analito sobre el cual el
solución estandarizada y cómo se partir del q.p y ácido sulfúrico a partir del
método produce resultados proporcionales a la misma.
identifican las características de las concentrado realizando los cálculos para
Una solución es la mezcla homogénea de dos o más soluciones en función a su preparar 250 ml de solución
componentes. El componente que se encuentra en menor
expresión química? Estandarizar la solución con el reactivo
proporción se llama SOLUTO, y es aquella que se disuelve en
el solvente y el que está en mayor proporción se llama
correspondiente utilizando el indicador
SOLVENTE y es aquella que disuelve al soluto. adecuado
Determinar su Fc
Las expresiones químicas para expresar la concentración con Vira la fenolftaleína de incoloro a rosado
mayor exactitud y que se las considerar científicas, son
Molaridad (M), Normalidad (N), molalidad (m).
Vira el naranja de metilo de amarillo a
rosado
Durante la preparación de soluciones se cometen una serie de Para acido:
errores, puede ser: de pesada, durante el aforo, el reactivo no
sea puro y está húmedo, etc. Por lo tanto para usar estas - Preparar 100ml de ácido sulfúrico al
soluciones en un análisis cuantitativo, es necesario corregir o 0,1N
hallar la concentración real de esta solución, por ello se - Colocar 50ml de agua destilada en el
estandarizan o se halla el FACTOR DE CORRECCION (Fc) de
matraz aforado
una solución. Fc = volumenteórico/Volumen practico.
- Pipetear el cálculo para H2SO4 y vaciar
Análisis volumétrico: procedimiento basado en la medida del al matraz aforado
volumen de reactivo necesario. Valoración: a una disolución - Aforar con agua destilada, tapamos y
que contiene al analito se le añaden incrementos de volumen
agitamos
de una disolución del reactivo. Reactivo valorante: Reactivo
Para bases:
que reacciona estequiométricamente con el analito. Punto
deequivalencia. Punto final: Es en realidad el punto que se - En un matraz Erlenmeyer pesar el
mide en una volumetría. Error de valoración: Es la diferencia cáculo correspondiente de bicarbonato
entre el punto final y el punto de equivalencia. Valoración del de sodio
blanco: Disolución que no presenta analito, sobre la cual se - Añadir 20ml de agua destilada
realiza el mismo proceso de valoración. - Añadir de 2-3 gotas de rojo de metilo
También podría gustarte
- Reporte 1. Preparacion de Soluciones Estandar HCL y NaOHDocumento4 páginasReporte 1. Preparacion de Soluciones Estandar HCL y NaOHaylin rodriguez100% (1)
- Preparacion de SolucionesDocumento10 páginasPreparacion de SolucionesLeyner SalgadoAún no hay calificaciones
- Informe Ácido Cítrico TERMINADODocumento9 páginasInforme Ácido Cítrico TERMINADOAna BellAún no hay calificaciones
- Estandarización de SolucionesDocumento7 páginasEstandarización de SolucionesFrank Huamani SullaAún no hay calificaciones
- PREPARACIÓN DE UNA SOLUCIÓN DE NaOH Y ESTANDARIZACIÓN CON FTALATO ÁCIDO DE POTASIODocumento4 páginasPREPARACIÓN DE UNA SOLUCIÓN DE NaOH Y ESTANDARIZACIÓN CON FTALATO ÁCIDO DE POTASIOEliana picoAún no hay calificaciones
- Informe #4. Reacciones Ácido Base 1Documento24 páginasInforme #4. Reacciones Ácido Base 1Eliana picoAún no hay calificaciones
- ADITIVOS y ADICIONES PDFDocumento29 páginasADITIVOS y ADICIONES PDFJuan Carlos WonkaAún no hay calificaciones
- Manual Tecnico Tuberia Alcantarillado Corrugado PDFDocumento24 páginasManual Tecnico Tuberia Alcantarillado Corrugado PDFSeider DcAún no hay calificaciones
- Titulación Potenciometrica Ka y Masa Molar de Un Ácido DébilDocumento9 páginasTitulación Potenciometrica Ka y Masa Molar de Un Ácido DébilAndres Ardila MartinezAún no hay calificaciones
- V de Cow CONTROL IbuprofenoDocumento1 páginaV de Cow CONTROL IbuprofenoCAROL SANABRIA SIÑANIZAún no hay calificaciones
- Informe Sobre Determinacio de Acido Citrico de Jugo de Frutas ComercialDocumento7 páginasInforme Sobre Determinacio de Acido Citrico de Jugo de Frutas ComercialRocioAún no hay calificaciones
- Preparacion de Soluciones Comp.3Documento9 páginasPreparacion de Soluciones Comp.3Paola MolanoAún no hay calificaciones
- Informe de Analitica 1Documento7 páginasInforme de Analitica 1Juan PalmaAún no hay calificaciones
- Laboratorio Número 10 Ale RuizDocumento12 páginasLaboratorio Número 10 Ale RuizJoel Pablo MamaniAún no hay calificaciones
- SOLUCIONESDocumento11 páginasSOLUCIONESGIANCARLO MAMANI RAMIREZAún no hay calificaciones
- Practica N ° 08Documento11 páginasPractica N ° 08Michael Legalize StoneAún no hay calificaciones
- Informe de Laboratorio - SolucionesDocumento3 páginasInforme de Laboratorio - SolucionesJesus BenitezAún no hay calificaciones
- P7 LQS Riverón Reyes AndreaDocumento34 páginasP7 LQS Riverón Reyes AndreaReyesAún no hay calificaciones
- Practica 8Documento9 páginasPractica 8Juan Miguel VelezAún no hay calificaciones
- Practica Completa-Sesión 7Documento22 páginasPractica Completa-Sesión 7Paulina100% (1)
- Práctica 3Documento6 páginasPráctica 3jhordanogomezAún no hay calificaciones
- Informe Preparacion y Estandarizacion de SolucionesDocumento7 páginasInforme Preparacion y Estandarizacion de SolucionesCristian Andres Cordoba CarvajalAún no hay calificaciones
- Reporte3 QuímicaAnalíticaDocumento5 páginasReporte3 QuímicaAnalíticaStarbuck 1994Aún no hay calificaciones
- Introduccion Al Analisis VolumetricoDocumento20 páginasIntroduccion Al Analisis VolumetricoCecy ToaquizaAún no hay calificaciones
- Estandarización de Ácido Clorhídrico e Hidróxido de Sodio PDFDocumento3 páginasEstandarización de Ácido Clorhídrico e Hidróxido de Sodio PDFLuis SalcedoAún no hay calificaciones
- Practica 2 PetroDocumento5 páginasPractica 2 PetroWilliams de Jesus Coronel AlvarezAún no hay calificaciones
- Experimento de Titulación de Vinagre A Partir de NaOHDocumento3 páginasExperimento de Titulación de Vinagre A Partir de NaOHDiego GalánAún no hay calificaciones
- Articulo Volumetria Quimica LLDocumento20 páginasArticulo Volumetria Quimica LLJuliana FigueroaAún no hay calificaciones
- Informe 8Documento7 páginasInforme 8Eumarielys EspinozaAún no hay calificaciones
- Informe 6 - Analisis VolumetricoDocumento13 páginasInforme 6 - Analisis Volumetricojean100% (1)
- Practica 12Documento7 páginasPractica 12MAYLEN VALENTINA GARCIA SANTIAGOAún no hay calificaciones
- Practica Soluciones Normalizadas 1Documento8 páginasPractica Soluciones Normalizadas 1Gianmarco Mamani LaricoAún no hay calificaciones
- Estandarizacion KOHDocumento5 páginasEstandarizacion KOHheberth simancasAún no hay calificaciones
- Informe Lab9Documento13 páginasInforme Lab9Camilo Andres Castro AguilarAún no hay calificaciones
- Acido BaseDocumento6 páginasAcido BaseMarly Callejas PerezAún no hay calificaciones
- Informe Triple Lab QuimicaDocumento5 páginasInforme Triple Lab QuimicaKaryn Zuleny CaballeroAún no hay calificaciones
- Informe 5. Acidemetría y Alcalimetría.Documento6 páginasInforme 5. Acidemetría y Alcalimetría.Stephanie AlvaradoAún no hay calificaciones
- Titulacion Acido Base Del Vinagre Comercial Con NaOHDocumento6 páginasTitulacion Acido Base Del Vinagre Comercial Con NaOHAndreaAún no hay calificaciones
- Lab II de Quimica Informe 1 PreparacionDocumento3 páginasLab II de Quimica Informe 1 Preparacionsofia luna hanssenAún no hay calificaciones
- LauraDocumento9 páginasLauraLaura PerezAún no hay calificaciones
- "Actividad 1 - Ordenador Gráfico, Soluciones Empíricas y Las Soluciones Valoradas".Documento7 páginas"Actividad 1 - Ordenador Gráfico, Soluciones Empíricas y Las Soluciones Valoradas".Jes HernandezAún no hay calificaciones
- Guía de Laboratorio 3 - Estandarización de Reactivos y Soluciones.Documento6 páginasGuía de Laboratorio 3 - Estandarización de Reactivos y Soluciones.Erika Mary Yolanda PARRA ALVAREZAún no hay calificaciones
- Articulo Cientifico Titulación y Determinación de Una Solución de Ácido Clorhídrico 0,1NDocumento8 páginasArticulo Cientifico Titulación y Determinación de Una Solución de Ácido Clorhídrico 0,1NANGIE KARINA SEPULVEDA RODRIGUEZAún no hay calificaciones
- Practica 13 (Titulacion)Documento6 páginasPractica 13 (Titulacion)Melanny RejasAún no hay calificaciones
- Practica 7. Valoracion Acido BaseDocumento3 páginasPractica 7. Valoracion Acido BaseDaniel FerminAún no hay calificaciones
- Preparacion de Patrones AcidoDocumento4 páginasPreparacion de Patrones AcidoAndres Felipe Reyes OrtegaAún no hay calificaciones
- Volumetría Acido BaseDocumento49 páginasVolumetría Acido BaseSol PolitanoAún no hay calificaciones
- Quimica Practica 7Documento11 páginasQuimica Practica 7karinasegurapulidoAún no hay calificaciones
- Informe de Laboratorio 2Documento10 páginasInforme de Laboratorio 2Kathe SanchezAún no hay calificaciones
- Lab Practica 08Documento8 páginasLab Practica 08eder50% (2)
- Titulacion Acido BaseDocumento6 páginasTitulacion Acido BaseJhoan Alexander LambrañoAún no hay calificaciones
- Practica 1Documento17 páginasPractica 1jhordanleoAún no hay calificaciones
- INFORME 6-7 LAB Quimica IIDocumento10 páginasINFORME 6-7 LAB Quimica IIKATLYN MARCELA BARRIOS TROUTTAún no hay calificaciones
- Laboratorio 5Documento9 páginasLaboratorio 5Edgar EspinozaAún no hay calificaciones
- claseTP3 ValoradasDocumento17 páginasclaseTP3 ValoradasSoyBambi xdAún no hay calificaciones
- 10.guia de SolucionesDocumento6 páginas10.guia de SolucionesMaria RoaAún no hay calificaciones
- Informe 1 Analitica FinalDocumento12 páginasInforme 1 Analitica FinalDiegoAún no hay calificaciones
- Práctica 7 Determianción de Acidez de Vinagre ComercialDocumento3 páginasPráctica 7 Determianción de Acidez de Vinagre ComercialAmy MaldonadoAún no hay calificaciones
- Clase 2 Introducción A Las Titulaciones y Tit Acido BaseDocumento29 páginasClase 2 Introducción A Las Titulaciones y Tit Acido BaseyoriAún no hay calificaciones
- Preparacion NAOHDocumento8 páginasPreparacion NAOHOsmin RiveraAún no hay calificaciones
- Practica 5 - Volumetria - Tiutluaciones de Neutralizacion Acido-BaseDocumento6 páginasPractica 5 - Volumetria - Tiutluaciones de Neutralizacion Acido-Basekarla ruizAún no hay calificaciones
- V de Cow Practica 10 ControlDocumento1 páginaV de Cow Practica 10 ControlCAROL SANABRIA SIÑANIZAún no hay calificaciones
- GLOSARIODocumento3 páginasGLOSARIOCAROL SANABRIA SIÑANIZAún no hay calificaciones
- Practica 5 PreguntasDocumento1 páginaPractica 5 PreguntasCAROL SANABRIA SIÑANIZAún no hay calificaciones
- V de Cow CONTROLDocumento1 páginaV de Cow CONTROLCAROL SANABRIA SIÑANIZAún no hay calificaciones
- SedimentoDocumento10 páginasSedimentoCAROL SANABRIA SIÑANIZAún no hay calificaciones
- CuestionarioDocumento1 páginaCuestionarioCAROL SANABRIA SIÑANIZAún no hay calificaciones
- El Plomo....Documento6 páginasEl Plomo....CAROL SANABRIA SIÑANIZAún no hay calificaciones
- Calculos y Resultados ControlDocumento2 páginasCalculos y Resultados ControlCAROL SANABRIA SIÑANIZAún no hay calificaciones
- Practica 5. Ob, Cris, Urin.Documento9 páginasPractica 5. Ob, Cris, Urin.CAROL SANABRIA SIÑANIZAún no hay calificaciones
- Tereftalato de Polietileno (Pet) 1Documento15 páginasTereftalato de Polietileno (Pet) 1John VincentAún no hay calificaciones
- 4 Cap4 QG1 2021-IIDocumento155 páginas4 Cap4 QG1 2021-IIARMIN GARCIA CHOQUEHUANCAAún no hay calificaciones
- Trabajo Práctico de Laboratorio 2023 - Tsga .Docx (2)Documento6 páginasTrabajo Práctico de Laboratorio 2023 - Tsga .Docx (2)Camila ZamudioAún no hay calificaciones
- Amidas ExposicionDocumento20 páginasAmidas ExposicionlauraAún no hay calificaciones
- QuímicaDocumento24 páginasQuímicaLuis MiliánAún no hay calificaciones
- EjerciciosDocumento6 páginasEjerciciosJuan sebastian Segovia gordilloAún no hay calificaciones
- AnvaDocumento4 páginasAnvaIsidoro Neyra Campos0% (1)
- HIDROCARBUROSDocumento3 páginasHIDROCARBUROSrubens babolinAún no hay calificaciones
- Investigacion Previa Alquenos y AlquinosDocumento7 páginasInvestigacion Previa Alquenos y AlquinosSalvador ZúñigaAún no hay calificaciones
- "Optimización Optimización y Formulación de Una Pasta Lava Trastes" de Una PastaDocumento99 páginas"Optimización Optimización y Formulación de Una Pasta Lava Trastes" de Una Pastaedwin castanedaAún no hay calificaciones
- Qumica Actividad 2 Unidad 3Documento3 páginasQumica Actividad 2 Unidad 3Edwin VelezAún no hay calificaciones
- Documento Completo Trabajo Quimica Jasmina 2018Documento38 páginasDocumento Completo Trabajo Quimica Jasmina 2018Jose Angel Calero Herrera100% (1)
- Estandarización de La Solución de NaOHDocumento7 páginasEstandarización de La Solución de NaOHHenry ArenasAún no hay calificaciones
- Ficha 1 Entalpias Reacción SolDocumento9 páginasFicha 1 Entalpias Reacción SolCruz SAÚLAún no hay calificaciones
- Estructura Lewis Ácido ClóricoDocumento4 páginasEstructura Lewis Ácido ClóricoOptiman BuyandsellAún no hay calificaciones
- Síntesis y Descomposición Del AguaDocumento8 páginasSíntesis y Descomposición Del AguaPérez Martínez Luz MaríaAún no hay calificaciones
- MG (OH) 2Documento1 páginaMG (OH) 2Jose Jara AlekejosAún no hay calificaciones
- Dime Til AminaDocumento11 páginasDime Til AminaDiego GuayacanAún no hay calificaciones
- Ejercicio 1Documento5 páginasEjercicio 1margareth castillaAún no hay calificaciones
- Prácticas Entrenamiento ONQDocumento5 páginasPrácticas Entrenamiento ONQMonserrat GonzalezAún no hay calificaciones
- Analisis de Cadmio, Boro y Arsenico en El Rio OsmoreDocumento25 páginasAnalisis de Cadmio, Boro y Arsenico en El Rio OsmoreYossi Chino BlancosAún no hay calificaciones
- SEMANA 8 - EstequimetriaDocumento2 páginasSEMANA 8 - EstequimetriaMarco Alarcon0% (1)
- Práctica No. 5. Identificación de Grupos Funcionales Inorgánicos y NomenclaturaDocumento10 páginasPráctica No. 5. Identificación de Grupos Funcionales Inorgánicos y Nomenclaturajulian alfonsoAún no hay calificaciones
- Temario QU-0114 - I-2021Documento17 páginasTemario QU-0114 - I-2021Fabricio Piñar SibajaAún no hay calificaciones
- Práctico de Carbohidratos 2010Documento7 páginasPráctico de Carbohidratos 2010Oscar G. Marambio100% (1)
- Freddy Guerrero Control5Documento5 páginasFreddy Guerrero Control5Freddy GuerreroAún no hay calificaciones
- Componentes Biótico y AbióticosDocumento35 páginasComponentes Biótico y AbióticosDomingo Mestra RossoAún no hay calificaciones
- Bioquímica 2 Ciclo de PentosaDocumento2 páginasBioquímica 2 Ciclo de PentosaItzel rosario Aguilar mendozaAún no hay calificaciones