Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Atomo REGLAOCTETOYTABLA
Cargado por
FABIANA MUÑOZTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Atomo REGLAOCTETOYTABLA
Cargado por
FABIANA MUÑOZCopyright:
Formatos disponibles
Física y Química 4º ESO Atomo y Sistema Periódico página 1 de 7
Átomo, sistema periódico y propiedades
Las partículas elementales
Descubrimiento del electrón
Tiene lugar en 1897 (J.J. Thomson) en el tubo de rayos catódicos.
F = q·E = m·a ; a = q·E/m
h = ½ a·t2 = ½ q·E·t2/m
La distancia d es recorrida en un
tiempo t a velocidad constante v:
luego t = v/d sustituyendo:
h = ½ q·E·v2/(m·d2)
La relación carga masa del electrón
1. En el tubo se 2. Al hacerla pasar 3. La viene dada por:
emite desde el cátodo una por el campo eléctrico se trayectoria indica que 2
radiación que se propaga en desvía de forma que indica tiene masa puesto que
línea recta que su signo es negativo. presenta inercia.
4. Manteniendo el campo E se añade un campo
magnético que desvía la radiación en sentido contrario:
q·E =q·v·B de donde v = E/B
sustituyendo:
2 2
Thomson logra determinar la relación carga masa de estos rayos y resulta ser igual para cualquier gas
que llene el tubo. Como consecuencia se llegó a la conclusión de que forman parte de toda la materia.
Estas partículas tienen carga negativa y masa muy pequeña. Reciben el nombre de electrones.
El protón
Haciendo el estudio de descargas en un tubo similar al de rayos catódicos con la diferencia de que se
cambia la posición relativa del ánodo y el cátodo se observa la aparición de los rayos canales.
Se llaman así porque aparecen en este caso cuando el ánodo está perforado. Se trata de partículas con
las siguientes propiedades:
1 Los rayos canales tienen carga positiva puesto que son 2 Tienen masa (se observa 3 La relación carga masa en
atraídos por el electrodo negativo. inercia) y ésta es mucho los mismos depende del gas
mayor que la del electrón. que llena el tubo.
Cuando el tubo está lleno de hidrógeno estas partículas son protones.
El neutrón
El neutrón fue descubierto en 1932 por Chadwick (alumno de Rutherford). Poco después del
establecimiento del modelo nuclear del átomo el mismo Rutherford planteó la necesidad de su
existencia. Sin embargo, debido a que es una partícula sin carga fue mucho más difícil detectarla.
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
Física y Química 4º ESO Atomo y Sistema Periódico página 2 de 7
Número atómico y másico
El modelo atómico nuclear de Rutherford plantea un átomo
prácticamente vacío, el núcleo contendrá protones y neutrones
cuya masa es la práctica totalidad de la masa del átomo y,
circulando alrededor de él, los electrones tienen la carga
negativa que compensa a la positiva del núcleo. La relación
de tamaño núcleo átomo se compara con la relación de
tamaño entre una bola de golf y un campo de fútbol. Por
todo el espacio correspondiente a las gradas y el resto del campo se
moverían unos mosquitos pequeños (los electrones).
Los átomos del mismo elemento tienen el mismo número atómico
aunque puede haber átomos del mismo elemento que tengan
diferente número másico, difieren en el número de neutrones, se
llaman isótopos de ese elemento. La mayor parte de los elementos presentan varios isótopos, unos son
estables y otros son radiactivos y alcanzan la estabilidad por emisión de radiaciones.
Las teorías atómicas
A continuación se muestra un resumen de las distintas teorías atómicas a lo largo de los años:
1808 John Dalton deduce, en 1801 la ley de las proporciones múltiples y la ley de las presiones
parciales. Basándose en las leyes de conservación de la masa (Lavoisier) y de las
proporciones definidas (Proust) deduce su teoría atómica:
1. La materia está formada por átomos indivisibles e indestructibles.
2. Los átomos del mismo elemento tienen iguales la masa y el resto de las propiedades.
3. Los átomos de distintos elementos tienen distintas estas propiedades.
4. Cuando dos o mas átomos de distintos elementos se unen forman otro átomo de un
compuesto químico (habla de átomos y no de moléculas, concepto que será introducido
posteriormente por Avogadro)
Teoría atómica de Thomson
J.J. Thomson Premio Nobel de Física (1906) “En reconocimiento a sus estudios teóricos y
experimentales de la conducción de la electricidad en gases”
Como se vio anteriormente, el descubrimiento del electrón y
su caracterización cálculo de carga y masa por parte de J.J.
Thomson, lleva a replantear el modelo atómico de Dalton. Thomson
considera que los electrones estarán imbuidos dentro del átomo. Este
tendría carga positiva en cantidad suficiente para neutralizar la carga
negativa de los electrones que contiene. Cuando un átomo neutro capta uno
o más electrones queda cargado negativamente mientras que adquiere carga
positiva cuando pierde uno o más electrones.
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
Física y Química 4º ESO Atomo y Sistema Periódico página 3 de 7
Modelo nuclear de Rutherford
En 1908 Ernst Rutherford recibe el premio Nobel de Química “por sus investigaciones sobre
la desintegración de los elementos y la química de sustancias radiactivas”.
A partir de los resultados experimentales de dos alumnos suyos, Geiger y Marsden, en
1909, llegó al modelo nuclear del átomo.
¿En qué consistía el experimento? En principio hay que decir que lo que se intentaba estudiar era otra
cosa, concretamente la difracción de la radiación α (alfa) por una lámina muy fina de oro. Hay que decir
que los experimentadores Geiger y Marsden, pasaban muchas horas en un cuarto a oscuras observando
el centelleo de las partículas α cuando impactaban sobre una superficie fosforescente.
Rutherford interpretó los resultados. En primer lugar considera que las partículas chocan con los átomos
que forman la lámina de oro. Estos átomos no pueden ser los que plantea el modelo de Thomson puesto
que las partículas pasarían a través de ellos sin sufrir desviaciones.
La mayoría de las partículas pasan sin Aproximadamente el 10% de ellas se
Solamente una de cada 10000 se refleja
desviarse desvían ligeramente
La única explicación plausible sería considerar que la materia está mayoritariamente vacía, que los
átomos tienen un núcleo central que concentra casi toda la masa del átomo y la carga positiva y una
corteza de diez a cien mil veces mayor por la que circulan los electrones.
Modelo de Bohr
El modelo atómico de Rutherford tiene el problema de su estabilidad. Es decir, los electrones son
partículas cargadas que giran en torno al núcleo. Los cuerpos que giran están sometidos a una
aceleración (aceleración normal o centrípeta). Las partículas cargadas sometidas a una aceleración
emiten energía. En este caso el electrón emitiría energía que la adquiere de él mismo y que hace que su
contenido energético sea cada vez menor. Como consecuencia de ello el electrón describiría una órbita
cada vez de menor radio hasta llegar a caer sobre el núcleo.
Esto ocurriría en un periodo muy corto de tiempo con lo que el átomo descrito por Rutherford no sería
-7
estable. Duraría alrededor de una diezmillonésima de segundo (10 s).
Además está el problema de los espectros atómicos. Interpretando cada raya espectral como una
transición de un nivel energético a otro, podemos ver que no todas las órbitas son posibles.
Para salvar todos estos problemas Bohr establece su modelo atómico que se basa en tres postulados:
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
Física y Química 4º ESO Atomo y Sistema Periódico página 4 de 7
• Los electrones giran en torno al núcleo en órbitas circulares estacionarias, sin emitir ni absorber
energía.
La primera de las discordancias del modelo de Rutherford queda superada. Si el electrón no puede emitir
ni absorber energía el átomo es estable.
• Las órbitas no pueden ser cualesquiera, están cuantizadas. Solamente aquellas en las que el
momento angular del electrón es un múltiplo entero de ħ (h/2π) siendo h la constante de
Planck
mvr = n h/(2 π)
n es el número cuántico principal que toma valores enteros positivos 1, 2, 3…
• Cuando un electrón cambia de órbita emite o absorbe una cantidad de energía que es igual a la
diferencia entre las energías de la posición final e inicial e igual a hν (siendo ν la frecuencia de la
onda emitida).
Ef - E0 = h ν
La combinación del segundo y tercer postulados explicarán perfectamente la formación de espectros
discontinuos del hidrógeno y coinciden asombrosamente los valores de las frecuencias de los mismos con
las predichas por los postulados. Precisamente esta fué la comprobación que dió validez al modelo de
Bohr.
Modelo atómico actual
El modelo atómico de Bohr también presentaba algunas dificultades a la hora de interpretar algunos
resultados experimentales. Por esta razón se le fueron añadiendo correcciones a medida que éstas iban
surgiendo.
La primera corrección la realizó Sommerfeld que añadió la posibilidad de existencia de órbitas elípticas.
Para cada nivel energético n las elipses no podían tener cualquier excentricidad sino que solo valían
algunas. Nuevamente estamos ante una cuantización. En este caso era el valor de un número cuántico k
(azimutal) cuyos valores eran enteros desde 0 hasta n - 1.
Una segunda corrección tuvo en cuenta la distinta orientación espacial de las órbitas para lo cual se
introdujo otro número cuántico (no podían tener cualquier orientación) y por último hubo la necesidad
de introducir el número cuántico magnético de spin (±½) (una forma de cuantizar la rotación
electrónica sobre si mismo)
Fue E. Schrödinger quien, basándose en la hipótesis de la dualidad onda corpúsculo de Louis de Broglie y
el principio de incertidumbre de W. Heisenberg, estableció una teoría en la que explicaba que el
comportamiento de las partículas podría definirse mediante una ecuación de la onda que las
acompañaba. La función de onda que describe el comportamiento de una partícula es Ψ. De esta forma,
aplicando operadores matemáticos a esa función de onda, podría conocerse la información relativa a las
distintas magnitudes físicas asociadas a la citada partícula.
Lo bueno, MUY BUENO, de esta nueva teoría es que los números cuánticos que ahora son:
• n - número cuántico principal (n = 1, 2, 3, 4...)
• l - número cuántico secundario (l = 0, 1, 2,..., n - 1)
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
Física y Química 4º ESO Atomo y Sistema Periódico página 5 de 7
• ml - número cuántico magnético (ml = - l, -(l -1),....., 0, ....., l - 1, l )
• ms - número cuántico magnético de spin (±½)
no surgen ahora a remolque de resultados experimentales que obligan a hacer modificaciones en el
modelo, sino que son condicionantes matemáticos para que los operadores al aplicarse a la función de
onda tengan una solución real. (Igual que para que el operador logaritmo o raiz cuadrada obliga a que
para tener solución real el número al que se aplica sea positivo.
2
Por otra parte se establece una relación entre el cuadrado de esta función de onda (Ψ ) y la
probabilidad de encontrar la partícula en una zona del espacio. Esa zona de máxima probabilidad se
llama orbital. Esa zona se corresponde con los valores de tres números cuánticos (n, l y ml) el cuarto
número cuántico es el destinado a definir ya la partícula (el electrón).
Como dentro del mismo átomo no puede haber dos partículas con los cuatro números cuánticos iguales
(Principio de exclusión de Pauli) podemos deducir que en cada orbital caben solamente dos electrones.
Ordenación periódica de los elementos
Los elementos químicos (unos 118) se tratan de ordenar. Esto se hace
atendiendo a las propiedades de los mismos. Desde un principio se
hicieron agrupaciones buscando coincidencias en las propiedades. La
primera vez que se ordenaron con éxito se debe a Mendeleiev (1969)
que los ordena atendiendo a las masas atómicas. Además hace otra
cosa, aquellos elementos que tienen propiedades químicas similares
los coloca en el mismo grupo y cuando tenía que dejar algún hueco lo
hacía. Por otra parte tuvo que alterar la colocación de algunos elementos para que las propiedades
coincidieran. Sorprendentemente, los huecos hacían predecir la existencia de elementos químicos que
mas tarde se descubrieron y cuyas propiedades coinciden con las predichas antes de su descubrimiento.
Lothar Meyer hace una ordenación similar a la de Mendeleiev con un año de retraso. Puesto que se
supone que la hizo sin conocimiento del trabajo del primero se suele atribuir la tabla periódica a ambos
químicos.
En el sistema periódico actual los elementos se ordenan por su número atómico.
Desaparecen las alteraciones de orden en elementos que tenían que producirse en la tabla
de Mendeleiev. Esta ordenación se debe a un químico inglés, Henry Moseley, que
estableció la forma de conocer el número atómico de los elementos midiendo la frecuencia
de los rayos X que éstos producían. Tuvo una vida muy corta pues, a los 27 años, resultó
muerto por un disparo en la frente durante la I Guerra Mundial. Si hubiese vivido más
posiblemente habría hecho muchas mas aportaciones a la Ciencia. Se especula con la idea de que esa es
la razón por la que el Gobierno Inglés, desde entonces, no permite que ningún científico se aliste en
tiempo de guerra.
La tabla periódica actual está ordenada en grupos (columnas de
elementos con propiedades químicas similares) y periodos (filas de
elementos en las que se produce una variación gradual de las
propiedades). Hay dieciocho grupos y siete periodos.
Los periodos son siete:
• Primero muy corto (solamente contiene dos elementos)
• Segundo y el tercero cortos con ocho elementos cada uno
• Cuarto y el quinto largos (contienen dieciocho elementos cada uno)
• Sexto y séptimo muy largos con treinta y dos elementos (hay que sumar a los 18 que se
contarían los 14 que corresponden a los lantánidos o los actínidos)
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
Física y Química 4º ESO Atomo y Sistema Periódico página 6 de 7
Como se puede ver los orbitales s y p se van llenando en los En la tabla superior se ven los nombres que se dan a los
grupos 1, 2, 13, 14, 15, 16, 17 y 18 que corresponden a los elementos de los distintos grupos o bloques en el Sistema
elementos representativos. Periódico.
Configuración electrónica
Los átomos están constituidos por protones y neutrones en el núcleo y por electrones en la corteza.
Como hemos visto éstos se van colocando en los distintos niveles y subniveles en orden de energías
crecientes. La regla de llenado es la siguiente: "la suma de n + l debe ser mínima y en caso de
coincidencia se llena primero el orbital de n menor".
Esta es la regla de llenado o Aufbau. En los
1s
orbitales s caben hasta 2 electrones, en los p
2s 2p hasta 6, en los d hasta 10 y en los f hasta 14.
3s 3p 3d Como se puede observar más arriba, los
4s 4p 4d 4f elementos de cada grupo tienen igual la
configuración electrónica de la última capa con lo
5s 5p 5d 5f que presentarán el mismo comportamiento
químico ya que éste viene determinado
6s 6p 6d 6f
exclusivamente por esta estructura electrónica
7s 7p 7d 7f más externa.
Regla del octeto
Al hacer la configuración electrónica de los elementos químicos observamos que hay una periodicidad
en la misma y que los elementos del mismo grupo en la Tabla Periódica presentan igual configuración
electrónica en la capa mas externa.
Por otra parte se observa que los elementos más estables son los gases nobles que poseen en su última
capa ocho electrones. Parece lógico pensar que los átomos pueden alcanzar su máxima estabilidad
logrando ocho electrones en esa última capa.
Periodicidad de las propiedades
Potencial de ionización se define como la energía necesaria por mol para formar un ión positivo cuando
los átomos se encuentran en estado gaseoso.
+
Y + PI → Y
Según la configuración electrónica y la regla del octeto
mencionada anteriormente parece lógico pensar que
será más fácil arrancar el electrón más externo en el caso
1
de los átomos que tienen en la última capans y a medida
que avanzamos en un periodo este potencial de
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
Física y Química 4º ESO Atomo y Sistema Periódico página 7 de 7
ionización irá creciendo, es decir, de izquierda a derecha.
Por otra parte se produce un efecto de pantalla cada vez mayor en los electrones más externos por la
presencia de otros electrones en niveles inferiores entre
ellos y el núcleo. Será por tanto más fácil, dentro del
mismo grupo, arrancar los electrones más externos
cuanto más abajo estemos. Se deduce que el potencial de
ionización crece de abajo hacia arriba en el mismo grupo.
Crecimiento del potencial de ionización, afinidad
electrónica y electronegatividad
Afinidad electrónica se define como la energía que se
desprende por mol al formarse un ión negativo:
–
X → X + AE
La afinidad electrónica será máxima en los elementos cuya configuración electrónica esté próxima a la
de los gases nobles y mínima en los alcalinos. También será mayor cuanto menor sea el efecto de
pantalla de los electrones de las capas inferiores. Es decir, como en el caso del potencial de
ionización crece de izquierda a derecha y de abajo hacia arriba.
Electronegatividad se define como la capacidad que tiene un átomo para atraer el par electrónico
compartido frente a otro átomo. Se deduce de la propia definición que se trata de una magnitud
relativa. Varía en la forma que lo hace la afinidad
electrónica y el potencial de ionización.
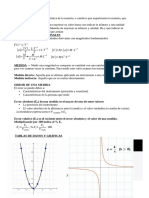
Volumen atómico es función del radio atómico. Los
máximos corresponden a los elementos del grupo 1 y los
mínimos a los del grupo 17.También se ve que aumenta
según aumenta el número atómico dentro del mismo
grupo mientras en cada periodo aumenta de derecha a
izquierda.
Para ver las animaciones y descargar apuntes en pdf visita http://fisicayquimicaenflash.es
También podría gustarte
- Cómo funciona el sistema TBIDocumento52 páginasCómo funciona el sistema TBIaldo jesus100% (1)
- Trabajo Exposicion Grupo 3Documento5 páginasTrabajo Exposicion Grupo 3Jesus David PerezAún no hay calificaciones
- Guia Teoria Atomica 8° BASICODocumento7 páginasGuia Teoria Atomica 8° BASICOAnonymous PShSARDzgYAún no hay calificaciones
- 04 AtomoDocumento36 páginas04 AtomoEdward Oblitas ZevallosAún no hay calificaciones
- Quimica Semana 03 - 2021 IiiDocumento5 páginasQuimica Semana 03 - 2021 IiiDavid LlontopAún no hay calificaciones
- estructura atómicaDocumento21 páginasestructura atómicaJose CalaniAún no hay calificaciones
- COEVALUACIÓNDocumento4 páginasCOEVALUACIÓNMicaa FariasAún no hay calificaciones
- ATOMODocumento6 páginasATOMOLola locaAún no hay calificaciones
- ESTRUCTURA DE LA MATERIA. Modelos Atómicos.Documento34 páginasESTRUCTURA DE LA MATERIA. Modelos Atómicos.dabe-quimico100% (4)
- Átomo Es La Porción Más Pequeña de La MateriaDocumento55 páginasÁtomo Es La Porción Más Pequeña de La MateriaSofia GonzalezAún no hay calificaciones
- El At0m0 y Su Estructura IDocumento7 páginasEl At0m0 y Su Estructura IMichaeljoel MoqueteAún no hay calificaciones
- Teorias AtómicasDocumento10 páginasTeorias AtómicasLeonilde Coromoto Vejar100% (1)
- Clase 1 Modelo Atómico 1Documento30 páginasClase 1 Modelo Atómico 1Cabarcas CelenaAún no hay calificaciones
- Tema 3Documento33 páginasTema 3Anahi MilagrosAún no hay calificaciones
- Ciencia e Ingenieria en Diseño de Los MaterialesDocumento171 páginasCiencia e Ingenieria en Diseño de Los MaterialesJesús FloresAún no hay calificaciones
- Sem03 - Teoría Atómica de La MateriaDocumento8 páginasSem03 - Teoría Atómica de La MateriaWalter Torres QuiñonesAún no hay calificaciones
- AtomosDocumento9 páginasAtomosseleneavila.licAún no hay calificaciones
- 02 - Teoria Atomica - CepreDocumento6 páginas02 - Teoria Atomica - Ceprerenejusto13Aún no hay calificaciones
- Fisica T1-2Documento6 páginasFisica T1-2alex alexAún no hay calificaciones
- Estructura AtomicaDocumento130 páginasEstructura AtomicaElizabeth Nina VillcaAún no hay calificaciones
- 2 AtomosDocumento69 páginas2 AtomosErick MegoAún no hay calificaciones
- Quimica 2Documento27 páginasQuimica 2sheryl summerAún no hay calificaciones
- Teorías y Modelos AtómicosDocumento40 páginasTeorías y Modelos AtómicosFRANAún no hay calificaciones
- NIVELACIÓN FORMATIVA 2 - 2do. CURSODocumento4 páginasNIVELACIÓN FORMATIVA 2 - 2do. CURSOVanessa CBAún no hay calificaciones
- Tema 2Documento28 páginasTema 2elcapiteniarazonAún no hay calificaciones
- Tema 6 - Estructura AtómicaDocumento24 páginasTema 6 - Estructura AtómicaM.P-DestruAún no hay calificaciones
- Tema 34Documento24 páginasTema 34olahuertaAún no hay calificaciones
- Taller Final Modelos Del Átomo de HidrógenoDocumento26 páginasTaller Final Modelos Del Átomo de HidrógenoSAMANTA GILAún no hay calificaciones
- Teorias Atomicas 2023 1Documento27 páginasTeorias Atomicas 2023 1Rodrigo JeagerAún no hay calificaciones
- InvestigacionDocumento28 páginasInvestigacionDenisse CeballosAún no hay calificaciones
- Quimica TeoremasDocumento8 páginasQuimica TeoremasCarlos Sanchez Hernandez100% (1)
- Modelos atómicos desde Dalton hasta SchrödingerDocumento3 páginasModelos atómicos desde Dalton hasta SchrödingerEuAún no hay calificaciones
- Modelos atómicos desde Demócrito a BohrDocumento13 páginasModelos atómicos desde Demócrito a BohrJorge CrbAún no hay calificaciones
- Modelo AtómicoDocumento25 páginasModelo AtómicoDAnielAún no hay calificaciones
- ATOMÍSTICADocumento20 páginasATOMÍSTICAhotmuysoyAún no hay calificaciones
- Modelos Atómicos y Estructura Atómica 5to Sec.Documento3 páginasModelos Atómicos y Estructura Atómica 5to Sec.Junior Collantes BacilioAún no hay calificaciones
- Química 2 Guia 1Documento16 páginasQuímica 2 Guia 1Alexander GustavoAún no hay calificaciones
- Antecedentes Del Modelo Atomico ActualDocumento7 páginasAntecedentes Del Modelo Atomico Actualroberto ferneliAún no hay calificaciones
- Cuadernillo Quimica I ISADocumento74 páginasCuadernillo Quimica I ISAKarim Zgaib100% (1)
- UD1. Estructura Atómica - Clasificacion.periodica-4Documento28 páginasUD1. Estructura Atómica - Clasificacion.periodica-4Luigi GalenoAún no hay calificaciones
- La Evolucion de Los Modelos AtomicosDocumento13 páginasLa Evolucion de Los Modelos AtomicosFELIX RAUL ECHEVERRIA CUBASAún no hay calificaciones
- Estructura de La Materia 2018Documento82 páginasEstructura de La Materia 2018samioAún no hay calificaciones
- qca 1Clase Estructura atómicaDocumento74 páginasqca 1Clase Estructura atómicaDANY HTAún no hay calificaciones
- TEMA 11Documento16 páginasTEMA 11Paula LabataAún no hay calificaciones
- Luis RauseoDocumento16 páginasLuis RauseoCarmen HernandezAún no hay calificaciones
- QG1 Átomo IDocumento33 páginasQG1 Átomo IJokasta Thaily Cedeno ValleAún no hay calificaciones
- 3 Modelos AtómicosDocumento37 páginas3 Modelos AtómicosFreddy Muñoz RiffoAún no hay calificaciones
- Modelo Atómico de Bohr y RutherfordDocumento9 páginasModelo Atómico de Bohr y RutherfordLeslie VazquezAún no hay calificaciones
- Modelo de ThonsonDocumento22 páginasModelo de ThonsonGladys Makkoukdji KassarAún no hay calificaciones
- QuimicaDocumento8 páginasQuimicaAriel IgnacioAún no hay calificaciones
- Tema 3 FyQDocumento38 páginasTema 3 FyQadansancheznietoAún no hay calificaciones
- Tema 3 Parte 1Documento14 páginasTema 3 Parte 1adansancheznietoAún no hay calificaciones
- Tema IDocumento32 páginasTema IExequiel RomeoAún no hay calificaciones
- Bohr SommerfeldDocumento10 páginasBohr SommerfeldXimenaAún no hay calificaciones
- Experimento de Rayos Catódicos de JJ Thomson. Equipo 2Documento20 páginasExperimento de Rayos Catódicos de JJ Thomson. Equipo 2Mhara WinzigAún no hay calificaciones
- Modelos AtomicosDocumento7 páginasModelos AtomicosLalo EspinoAún no hay calificaciones
- HTTPSWWW - Edu.xunta - Galcentrosiesvalminoraulavirtualpluginfile.php38450mod Resourcecontent1ESTRUCTURA20ATÓMICA20Y2Documento18 páginasHTTPSWWW - Edu.xunta - Galcentrosiesvalminoraulavirtualpluginfile.php38450mod Resourcecontent1ESTRUCTURA20ATÓMICA20Y2ANTIA FERNÁNDEZ PEREIRAAún no hay calificaciones
- Teoría AtómicaDocumento7 páginasTeoría Atómicadanlou117Aún no hay calificaciones
- El ÁtomoDocumento16 páginasEl ÁtomoAndrea MolinaAún no hay calificaciones
- Estructura Del Átomo ModernoDocumento8 páginasEstructura Del Átomo Modernoarnaldo simon sirpa laricoAún no hay calificaciones
- Breve Encuesta Sobre La Actualidad de Producción Ovina y PorcinaDocumento1 páginaBreve Encuesta Sobre La Actualidad de Producción Ovina y PorcinaFABIANA MUÑOZAún no hay calificaciones
- Cortes Porcinos y Sus BondadesDocumento10 páginasCortes Porcinos y Sus BondadesFABIANA MUÑOZAún no hay calificaciones
- Anatomia y Fisiologia de CerdosDocumento18 páginasAnatomia y Fisiologia de CerdosFABIANA MUÑOZAún no hay calificaciones
- CP 1 - DOMESTICACION Del CerdoDocumento2 páginasCP 1 - DOMESTICACION Del CerdoFABIANA MUÑOZAún no hay calificaciones
- Configuración Electrónic1Documento2 páginasConfiguración Electrónic1FABIANA MUÑOZAún no hay calificaciones
- Configuración Electrónica o Configuración PeriódicaDocumento7 páginasConfiguración Electrónica o Configuración PeriódicaFABIANA MUÑOZAún no hay calificaciones
- 1 Problemas EjerciciosDocumento2 páginas1 Problemas EjerciciosFABIANA MUÑOZAún no hay calificaciones
- TP 1-CebadaDocumento2 páginasTP 1-CebadaFABIANA MUÑOZAún no hay calificaciones
- TP 3 - Ejercicios Densidad de Siembra y RendimientoDocumento1 páginaTP 3 - Ejercicios Densidad de Siembra y RendimientoFABIANA MUÑOZAún no hay calificaciones
- La Mujer y El Trabajo RuralDocumento22 páginasLa Mujer y El Trabajo RuralFABIANA MUÑOZAún no hay calificaciones
- Impacto Ambiental Grupo3Documento18 páginasImpacto Ambiental Grupo3axel saldarriagaAún no hay calificaciones
- Corriente Alterna 2Documento4 páginasCorriente Alterna 2Matías AlarcónAún no hay calificaciones
- Copia de Copia de Reporte05 - CBA - 2020 - 1Documento10 páginasCopia de Copia de Reporte05 - CBA - 2020 - 1Jhon Josue Ccari SupoAún no hay calificaciones
- Peimar - ES - OFFGRID - OS10 20 30 50 80 100 150PDocumento2 páginasPeimar - ES - OFFGRID - OS10 20 30 50 80 100 150PJesus SantosAún no hay calificaciones
- Taller Tecnología (Desechos Tecnológicos)Documento2 páginasTaller Tecnología (Desechos Tecnológicos)gabimedina0411Aún no hay calificaciones
- Trabajo Colaborativo Semana 4 Culltura Amiental Calentamiento GlobalDocumento10 páginasTrabajo Colaborativo Semana 4 Culltura Amiental Calentamiento Globaldeiby johan valencia muñozAún no hay calificaciones
- Rebobinado de Un TransformadorDocumento8 páginasRebobinado de Un TransformadorDavid MamaniAún no hay calificaciones
- Puesta A TierraDocumento54 páginasPuesta A TierraArnel HernandezAún no hay calificaciones
- Experiencia #7 Transferencia de Calor Por Radiación (1420)Documento9 páginasExperiencia #7 Transferencia de Calor Por Radiación (1420)Alexsander Becerra PinzónAún no hay calificaciones
- Matriz de Aspectos e Impactos SABIDocumento8 páginasMatriz de Aspectos e Impactos SABINataly Su GarciaAún no hay calificaciones
- Reglas generales sobre dispositivos y medios de salvamentoDocumento44 páginasReglas generales sobre dispositivos y medios de salvamentoJulieta SilveiraAún no hay calificaciones
- HellDocumento19 páginasHellEduardo García OrtegaAún no hay calificaciones
- MPd: Mantenimiento predictivo y sus técnicasDocumento39 páginasMPd: Mantenimiento predictivo y sus técnicasAlvaro Santa Cruz DiazAún no hay calificaciones
- PROYECTO Construcción de Lámparas Con Luz Led y Sensor de MovimientoDocumento31 páginasPROYECTO Construcción de Lámparas Con Luz Led y Sensor de Movimientolovato.jj014Aún no hay calificaciones
- Convertidores Electrã Nicos Energã A Solar Fotovoltaica, AplicacDocumento342 páginasConvertidores Electrã Nicos Energã A Solar Fotovoltaica, AplicacefowenAún no hay calificaciones
- P-Sst-03-Procedimiento de Trabajo en CalienteDocumento12 páginasP-Sst-03-Procedimiento de Trabajo en CalienteLlCesarll LlPerez CerazollAún no hay calificaciones
- Trabajo de Investigación Grupo 8Documento20 páginasTrabajo de Investigación Grupo 8Angel Ramírez chujutalliAún no hay calificaciones
- Motor DieselDocumento22 páginasMotor DieselIgnacio LopezAún no hay calificaciones
- Acondicionador de Aire SolarDocumento31 páginasAcondicionador de Aire SolarAlicia Cristina Villalobos MonteroAún no hay calificaciones
- Preparatario Mecanica 2023-3Documento2 páginasPreparatario Mecanica 2023-3Diego RodriguezAún no hay calificaciones
- Libro de Control de Clases: #Orden de CompraDocumento8 páginasLibro de Control de Clases: #Orden de CompraSussy Ortiz MercadoAún no hay calificaciones
- Espuma 17 CBSDocumento19 páginasEspuma 17 CBSRonal Honores CastilloAún no hay calificaciones
- Informe 2Documento11 páginasInforme 2Wilmer QuispeAún no hay calificaciones
- Intervencion MinminasDocumento21 páginasIntervencion Minminassergio balcazarAún no hay calificaciones
- Semana 3Documento20 páginasSemana 3Cesar pariAún no hay calificaciones
- Pro-Wedge SpanishDocumento22 páginasPro-Wedge Spanishjuan carlos arcani huantoAún no hay calificaciones
- RutherfordDocumento4 páginasRutherfordPobyAún no hay calificaciones
- Mining Catálogo ESDocumento7 páginasMining Catálogo ESJohann Alexander Caballero BohorquezAún no hay calificaciones
- Hoja de Proceso Semestre 3Documento5 páginasHoja de Proceso Semestre 3Aldair Emerson Paredes BlasAún no hay calificaciones