Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Linea Del Tiempo Ma - Quimica
Cargado por
Franco Rincón GiselleDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Linea Del Tiempo Ma - Quimica
Cargado por
Franco Rincón GiselleCopyright:
Formatos disponibles
INSTITUTO POLITÉCNICO NACIONAL
CENTRO DE ESTUDIOS CIENTÍFICOS Y
TECNOLÓGICOS 7 “CUAUHTÉMOC”
LINEA DEL TIEMPO DE
MODELOS ATÓMICO
FRANCO RINCÓN GISELLE
3IMI
LABASTIDA LEMUS ANA LUISA
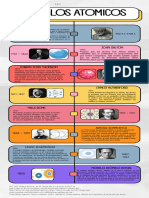
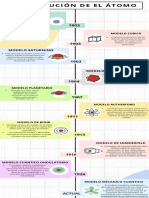
MODELOS
ATÓMICOS
DALTON
“Postulados Atómicos”. Sostenía que
todo estaba hecho de átomos, indivisibles
e indestructibles, incluso mediante 450 AC
reacciones químicas. Dalton proponía
que los átomos de un mismo elemento
químico eran iguales entre sí y tenían la
misma masa e iguales propiedades
DEMOCRITO
Propuso que el mundo estaba formado
por partículas muy pequeñas e indivisibles,
1803 de existencia eterna, homogéneas e
incompresibles, cuyas únicas diferencias
eran de forma y tamaño, nunca de
funcionamiento interno. Estas partículas se
bautizaron como “átomos”,
THOMSON
Descubridor del electrón en 1897,
este modelo es previo al descubrimiento
de los protones y neutrones, por lo que 1902
asumía que los átomos estaban
compuestos por una esfera de carga
positiva y los electrones de carga
negativa estaban incrustados en ella,
LEWIS
“Modelo del Átomo Cúbico”, en
este modelo Lewis proponía la
1904 estructura de los átomos
distribuida en forma de cubo, en
cuyos ocho vértices se hallaban los
electrones.
BOHR
Propuso el modelo de Bohr para
explicar cómo podían los electrones
tener órbitas estables (o niveles
1911
energéticos estables) rodeando el
núcleo. Además explica por qué los
átomos tienen espectros de emisión
característicos.
RUTHERFORD
Determinó que el átomo está
compuesto por un núcleo atómico de
1913 carga positiva (donde se concentra la
mayor parte de su masa) y los
electrones, que giran libremente
alrededor de este
núcleo.
SCHRODINGER
A partir de los estudios de Bohr y
Sommerfeld, concebía los electrones 1916
como ondulaciones de la materia, lo
cual permitió la formulación posterior
de una interpretación probabilística de
la función de onda
SOMMERFELD
Entre sus modificaciones del
modelo está la afirmación de que las
órbitas de los electrones fueran circulares
1926 o elípticas, que los electrones tuvieran
corrientes eléctricas minúsculas y que a
partir del segundo nivel de energía
existieran dos o más subniveles.
2023
MODELO ATÓMICO ACTUAL
Se basa en la teoría cuántica y
la mecánica cuántica. En este modelo,
los electrones se encuentran en
orbitales atómicos definidos, que son
regiones de alta probabilidad de
encontrar un electrón.
También podría gustarte
- Linea de Tiempo Aportaciones en El Modelo AtomicoDocumento5 páginasLinea de Tiempo Aportaciones en El Modelo AtomicoJuan PabloAún no hay calificaciones
- Linea de Tiempo Modelos Atomicos QuimicaDocumento2 páginasLinea de Tiempo Modelos Atomicos QuimicaLeidy Yohana Bayona Florez86% (7)
- Línea de Tiempo Modelos AtomicosDocumento1 páginaLínea de Tiempo Modelos Atomicosandres felipe galindo duquinoAún no hay calificaciones
- Cuadro Comparativo - Modelos AtomicosDocumento3 páginasCuadro Comparativo - Modelos AtomicosEuan Sánchez Gabriel EduardoAún no hay calificaciones
- Linea de Tiempo Modelos AtomicosDocumento1 páginaLinea de Tiempo Modelos AtomicosMARCO ANTONIO RAMIREZ REYESAún no hay calificaciones
- Modelos AtomicosDocumento15 páginasModelos AtomicosLópez García Axel UrielAún no hay calificaciones
- Modelos AnatomicosDocumento12 páginasModelos AnatomicosSayory Castillo CastilloAún no hay calificaciones
- Modelos AtómicosDocumento16 páginasModelos AtómicosNMA1283% (6)
- Linea Del Tiempo PDFDocumento1 páginaLinea Del Tiempo PDFFranklin Enmanuel Cordero BobadillaAún no hay calificaciones
- Línea de Tiempo Modelos Atomicos - Velasco SantiagoDocumento3 páginasLínea de Tiempo Modelos Atomicos - Velasco SantiagoSantiago Vs100% (1)
- Modelos AtomicosDocumento4 páginasModelos Atomicosalansalas34erAún no hay calificaciones
- Línea de Tiempo: Modelos AtómicosDocumento1 páginaLínea de Tiempo: Modelos AtómicosMisael Ruiz Gutiérrez100% (2)
- Modelos AtómicosDocumento2 páginasModelos AtómicosAlejandro RusinqueAún no hay calificaciones
- Hernández Cruz Frida Pamela - Modelos Átomicos - 551Documento3 páginasHernández Cruz Frida Pamela - Modelos Átomicos - 551ho liAún no hay calificaciones
- Modelos AtomicosDocumento3 páginasModelos AtomicosSamanta Trejo SalcedoAún no hay calificaciones
- Modelos AtómicosDocumento1 páginaModelos AtómicosSolano Torres SaraAún no hay calificaciones
- Guia Modelo AtomicoDocumento2 páginasGuia Modelo AtomicoSamuel PinzonAún no hay calificaciones
- Los Modelos Atomicos y Su HistoriaDocumento5 páginasLos Modelos Atomicos y Su HistoriaKennia Rivera GuapulemaAún no hay calificaciones
- Atividad - Modelos AtómicosDocumento2 páginasAtividad - Modelos AtómicosGab BrielAún no hay calificaciones
- Exposicion Los Modelos AtomicosDocumento9 páginasExposicion Los Modelos Atomicoslarasaranatalia51Aún no hay calificaciones
- Linea de Tiempo Teoria AtomistaDocumento4 páginasLinea de Tiempo Teoria AtomistaEsperanza López MosquedaAún no hay calificaciones
- Libro Química - Biología Primero 21-22Documento95 páginasLibro Química - Biología Primero 21-22CYV ASESORESAún no hay calificaciones
- QUÍMICA - MODELOS ATÓMICOS - : Cad Logr Comie Co L Decisió D IntentarlDocumento3 páginasQUÍMICA - MODELOS ATÓMICOS - : Cad Logr Comie Co L Decisió D IntentarlLa Kpoper ShippeadoraAún no hay calificaciones
- Linea de TiempoDocumento6 páginasLinea de TiempoYamilet ReyesAún no hay calificaciones
- Infografía de Línea de Tiempo Timeline Con Años Fechas Multicolor ModernoDocumento1 páginaInfografía de Línea de Tiempo Timeline Con Años Fechas Multicolor Modernocamilo velezAún no hay calificaciones
- Fusión NuclearDocumento30 páginasFusión NuclearTrapGameAún no hay calificaciones
- Modelos AtómicosDocumento5 páginasModelos AtómicosTrapGameAún no hay calificaciones
- Modelos AtómicosDocumento4 páginasModelos AtómicosRaulZorrillaAún no hay calificaciones
- Modelos AtómicosDocumento6 páginasModelos AtómicosNathalia HerreraAún no hay calificaciones
- Actividad 1. Investigación de Modelos AtómicosDocumento3 páginasActividad 1. Investigación de Modelos Atómicos2Jose Alberto Meza VelázquezAún no hay calificaciones
- Teoría AtómicaDocumento5 páginasTeoría AtómicaPercy PérezAún no hay calificaciones
- Modelos Del AtomoDocumento2 páginasModelos Del Atomocamiv14ygAún no hay calificaciones
- Qui MicaDocumento235 páginasQui MicaJupiter GonzalezAún no hay calificaciones
- Modelo AtomicoDocumento4 páginasModelo AtomicoRoberto Lopez HernándezAún no hay calificaciones
- Alcances y Limitaciones de Los Modelos AtomicosDocumento4 páginasAlcances y Limitaciones de Los Modelos Atomicosmariafernanda herreramartinezAún no hay calificaciones
- Historia de Los Modelos Atómicosy Modelo Mecanico CuanticoDocumento20 páginasHistoria de Los Modelos Atómicosy Modelo Mecanico CuanticoDELMY ISABEL ÁLVAREZ VILLAFRANCOAún no hay calificaciones
- Teoría AtómicaDocumento23 páginasTeoría AtómicaCupul Cauich Diego RobertoAún no hay calificaciones
- Conceptos Atomicos AnterioresDocumento7 páginasConceptos Atomicos Anterioresdenis leonAún no hay calificaciones
- InfografíaDocumento1 páginaInfografíaLorena CastroAún no hay calificaciones
- Infografía Línea Del Tiempo Timeline Historia Moderno Creativo MulticolorDocumento3 páginasInfografía Línea Del Tiempo Timeline Historia Moderno Creativo MulticolorRosannksAún no hay calificaciones
- Linea de Tiempo - Biologia - 20230918 - 082145 - 0000Documento1 páginaLinea de Tiempo - Biologia - 20230918 - 082145 - 0000Brell DiazAún no hay calificaciones
- Tarea Evidencias de Estructura AtómicaDocumento5 páginasTarea Evidencias de Estructura Atómicaalanntorres09ctrlAún no hay calificaciones
- Modelos AtomicosDocumento10 páginasModelos AtomicosErnesto RamosAún no hay calificaciones
- Modelo AtomicoDocumento8 páginasModelo AtomicoOctavio Felipe Mendez MorenoAún no hay calificaciones
- Modelos AtómicosDocumento19 páginasModelos AtómicosGrenorich Steven Ruiz ReyesAún no hay calificaciones
- Teoría Atómica y Estructura de La Materia Equipo 3Documento23 páginasTeoría Atómica y Estructura de La Materia Equipo 3lesliemartinezAún no hay calificaciones
- Linea Del Tiempo Modelos AtómicosDocumento1 páginaLinea Del Tiempo Modelos AtómicosBEIDA ISABEL PEREZ MIRANDAAún no hay calificaciones
- Modelo AtómicDocumento5 páginasModelo AtómicElver Ramirez LopezAún no hay calificaciones
- Infografia de La Evolución Del Atomo - Lesly PDFDocumento1 páginaInfografia de La Evolución Del Atomo - Lesly PDFLesly MuñetonezAún no hay calificaciones
- Teoria AtomicaDocumento3 páginasTeoria AtomicaNeheyler MecatrónicoAún no hay calificaciones
- Linea Del Tiempo de La Teoria AtomicaDocumento2 páginasLinea Del Tiempo de La Teoria AtomicaMadrid Silva Victor Joshua 1IM11Aún no hay calificaciones
- LMy TDocumento6 páginasLMy Tlu pnAún no hay calificaciones
- Actividades de QuimicaDocumento7 páginasActividades de Quimicairvingfeel0409swAún no hay calificaciones
- Modelos Atómicos EspDocumento2 páginasModelos Atómicos Espmartasantosegea2Aún no hay calificaciones
- Taipe Chachayma Edith Sesión 5Documento14 páginasTaipe Chachayma Edith Sesión 5Edith Rosmery Taipe ChachaymaAún no hay calificaciones
- Actividad 1. Investigación de Modelos AtómicosDocumento1 páginaActividad 1. Investigación de Modelos AtómicosTonantzin Ireri Castro Zavala100% (2)
- Modulo 4 QT 2021Documento7 páginasModulo 4 QT 2021Carina BogadoAún no hay calificaciones
- Teoria AtomicaDocumento6 páginasTeoria AtomicaAnthonyAún no hay calificaciones
- Química PREDocumento4 páginasQuímica PREVictor Huerta RojasAún no hay calificaciones
- Fórmula Púrpura ReseñaDocumento2 páginasFórmula Púrpura ReseñaMarian AyalaAún no hay calificaciones
- Manual de Trabajos Espacios Confinados 2020Documento14 páginasManual de Trabajos Espacios Confinados 2020Kuky ParisiAún no hay calificaciones
- 22.1. Mobilgrease 28Documento4 páginas22.1. Mobilgrease 28JeefAún no hay calificaciones
- Concentración de Menas AuríferasDocumento4 páginasConcentración de Menas AuríferasG77Aún no hay calificaciones
- Clase 07 Estructura y Función Del HematíeDocumento117 páginasClase 07 Estructura y Función Del HematíeWilliam Apaza Mamani100% (1)
- Taller de Fluidos 1Documento16 páginasTaller de Fluidos 1Mariel Yance Orozco50% (2)
- Clasificación de Agitadores o ImpulsoresDocumento14 páginasClasificación de Agitadores o ImpulsoresIsrael Esparza AngelesAún no hay calificaciones
- Guía de Ejercicios 2bDocumento9 páginasGuía de Ejercicios 2bEdgardo TabiloAún no hay calificaciones
- Justificacion Del MartilloDocumento4 páginasJustificacion Del MartilloSerGyux Zepol EpsiuqAún no hay calificaciones
- LibroDocumento8 páginasLibroPhil MoralesAún no hay calificaciones
- Fenomeno de La Lluvia Acida en El MundoDocumento8 páginasFenomeno de La Lluvia Acida en El Mundowilliam apazaAún no hay calificaciones
- Clasificación de Los Métodos de EsterilizaciónDocumento5 páginasClasificación de Los Métodos de EsterilizaciónSam NuñezAún no hay calificaciones
- Expo Demostracion de Grasas Neutras en Un Corte Histologico MaribelDocumento18 páginasExpo Demostracion de Grasas Neutras en Un Corte Histologico MaribelWilliam Gaston Herrera SolanoAún no hay calificaciones
- Ficha Tecnica de Barras. 2021Documento7 páginasFicha Tecnica de Barras. 2021jherryAún no hay calificaciones
- Práctica Calor Específico SólidoDocumento6 páginasPráctica Calor Específico SólidoAna CorsiniAún no hay calificaciones
- Simulacro Primer Parcial Con Respuestas PDFDocumento7 páginasSimulacro Primer Parcial Con Respuestas PDFBryanCoelloAún no hay calificaciones
- Analisis de La Formacion de Una Sal Co Mpleja - Complejos de Werner - 1Documento3 páginasAnalisis de La Formacion de Una Sal Co Mpleja - Complejos de Werner - 1milagrosAún no hay calificaciones
- Ácidos y BasesDocumento17 páginasÁcidos y BasesHugo Danilo Santos Borbor100% (2)
- Matriz Iper Tanque Ahulado.Documento14 páginasMatriz Iper Tanque Ahulado.Victor aaron DuranAún no hay calificaciones
- Hidrostal UcvDocumento19 páginasHidrostal UcvHector23-56nAún no hay calificaciones
- HS - Roe Mat Bloque (Zapi)Documento5 páginasHS - Roe Mat Bloque (Zapi)Luis Sánchez RoblesAún no hay calificaciones
- Informe MetalografíaDocumento10 páginasInforme MetalografíaNicolas MontoyaAún no hay calificaciones
- Guia Bioquimica IiDocumento85 páginasGuia Bioquimica IiARIEL TAIPEAún no hay calificaciones
- Matrices, Refuerzos y Adhesivos 2023 ADocumento8 páginasMatrices, Refuerzos y Adhesivos 2023 AHugo MoralesAún no hay calificaciones
- Características Principales Aplicaciones Típicas: Acero Dulce, Celulósico - AWS E6011Documento2 páginasCaracterísticas Principales Aplicaciones Típicas: Acero Dulce, Celulósico - AWS E6011jhosser andres jojoa calderonAún no hay calificaciones
- Perovskita PDFDocumento5 páginasPerovskita PDFDavid DazirAún no hay calificaciones
- Nec2011-Cap.14-Energías Renovables-021412Documento110 páginasNec2011-Cap.14-Energías Renovables-021412Mercedez BenzAún no hay calificaciones
- Tarea 3, Roque Mendoza, FundicionDocumento8 páginasTarea 3, Roque Mendoza, FundicionRoque Luis Mendoza SanchezAún no hay calificaciones
- Pirámides EnergéticasDocumento6 páginasPirámides EnergéticasERIKA VIVIANA TOBÓN HENAOAún no hay calificaciones
- Ácidos CarboxílicosDocumento16 páginasÁcidos CarboxílicosbsjxujdnAún no hay calificaciones