Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y Adolescentes
Cargado por
yurubiTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y Adolescentes
Cargado por
yurubiCopyright:
Formatos disponibles
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
GUÍA DE PRÁCTICA CLÍNICA DE DIAGNÓSTICO
Y TRATAMIENTO DE LEUCEMIA MIELOIDE
CRÓNICA EN NIÑOS Y ADOLESCENTES
SUB UNIDAD DE ATENCIÓN INTEGRAL ESPECIALIZADA DEL
PACIENTE DE TRASPLANTE DE PROGENITORES
HEMATOPOYÉTICOS – HEMATOLOGÍA CLINICA
Firmado digitalmente por BROGGI
ANGULO Oscar Alfredo FAU
20552196725 soft
Motivo: Doy V° B°
Fecha: 18.11.2022 17:23:36 -05:00
Firmado digitalmente por MURILLO
Firmado digitalmente por GODOY Firmado digitalmente por VELIZ
VIZCARRA Sergio Antonio FAU
VILA Victoria Angelica FAU SILVA Emma Victoria FAU
20552196725 soft
20552196725 soft 20552196725 soft
Motivo: Soy el autor del documento
Motivo: Soy el autor del documento Motivo: Doy V° B°
Fecha: 25.11.2022 16:04:27 -05:00
Fecha: 04.11.2022 11:37:35 -05:00 Fecha: 19.12.2022 10:49:26 -05:00
Elaborado por: Revisado por: Aprobado por:
Unidad de Atención Integral
Sub Unidad de Atención Especializada. Dra. Elizabeth Zulema
Integral Especializada del Tomás Gonzáles de
Paciente de Trasplante de Sub Unidad de Atención Integral Palomino
Progenitores Especializada del Paciente de
Trasplante de Progenitores Directora General del
Hematopoyéticos – Instituto Nacional de Salud
Hematopoyéticos
Hematología Clínica del Niño San Borja
Unidad de Gestión de la Calidad
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 1 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia
Mieloide Crónica en Niños y Adolescentes
Índice
I Finalidad ........................................................................................................................................................ 4
II Objetivo ........................................................................................................................................................... 4
III Ámbito de Aplicación ................................................................................................................................. 4
IV Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y Adolescentes. ... 4
4.1 Nombre y código CIE 10: C 92.1………………………………………………………………..………..4
V Consideraciones Generales ..................................................................................................................... 4
5.1 Definición………………………………………………………………………………………………..………..4
5.2 Etiología…………………………………………………………………….……………………………………..5
5.3 Fisiopatología………………………………………………………………….………………………..………5
5.4 Aspectos Epidemiológicos…….…………………………………………….……………………..………7
5.5 Factores de Riesgo asociados………………………………………………..………………….………..7
5.5.1 Medio ambiente …………………………………………………...…………………………………7
5.5.2 Estilo de vida …………………………………………………………………………………….……7
5.5.3 Factores hereditarios……………………………………………………..…………………….….8
VI Consideraciones Específicas ................................................................................................................... 8
6.1 Cuadro clínico………………………………………………………………………………...………………....8
6.1.1 Signos y síntomas……………………………………………………………….……………….…. 8
6.1.2 Interacción cronológica……………………………………………………………………………8
6.1.3 Gráficos, diagramas o fotografías……………………………………..……………………….9
6.2 Diagnóstico…………………………………………………………………………….……………………….. 9
6.2.1 Criterios de diagnóstico…………………………………………………..…………………….…9
6.2.2 Diagnóstico diferencial………………….…………………………….…………………………11
6.3 Exámenes auxiliares……………………………………………..…………………………………………11
6.3.1 De patología clínica…………………..……………………………………………………………11
6.3.2 De imágenes…………………………………………………..…………………………………...…12
6.3.3 de exámenes especiales complementarios…………………………………………….. 12
6.4 Manejo según complejidad y capacidad resolutiva…………………………………………....13
6.4.1 Medidas generales y preventivas ………………………………………………………..… 14
6.4.2 Terapéutica………………………………………………………………………………………...…14
6.4.3 Efectos adversos o colaterales del tratamiento………………….…………………….19
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 2 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
6.4.4 Signos de alarma …………………………………………………….…………………………….20
6.4.5 Criterios de alta……………………………………………………………………………………..20
6.4.6 Pronóstico……………………………………………………………………………………………..21
6.5 Complicaciones……………………………………………………………………..………………………...21
6.6 Criterios de referencia y contra referencia……………………………………..……………….. 22
6.7 Flujograma………………………………………………………..…………………………………………... 23
VII Autores .......................................................................................................................................................... 27
VIII Anexos…………………………………………………………………………………………………………...…….28
IX Referencias Bibliográficas o Bibliografía………………………………………………………………..29
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 3 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Guía de Práctica Clínica de Diagnóstico y Tratamiento Leucemia
Mieloide Crónica en Niños y Adolescentes
I.-Finalidad
La finalidad de esta guía es contribuir con un instrumento técnico de referencia
institucional y nacional para apoyar la toma de decisiones clínicas basado en
recomendaciones sustentadas con la mejor evidencia científica disponible, que les
permita a los profesionales de la salud, un abordaje integral de la Leucemia Mieloide
Crónica en pacientes pediátricos que acuden al Instituto Nacional de Salud del Niño San
Borja.
II.-Objetivo
● Unificar criterios de diagnóstico y tratamiento entre los profesionales de salud
especialistas en el manejo de la Leucemia Mieloide Crónica en niños y adolescentes
● Realizar recomendaciones basadas en evidencia para una adecuada detección y
diagnóstico temprano, así como un tratamiento oportuno.
● Identificar efectos adversos que pueden presentar los pacientes pediátricos
durante el tratamiento para prevenir y reducir el número de complicaciones.
III.-Ámbito de Aplicación
La presente Guía de Práctica Clínica es de aplicación en la Sub Unidad de Atención Integral
Especializada del Paciente de Trasplante de Progenitores Hematopoyéticos (TPH)-
Hematología, específicamente para ser usada por los profesionales médicos de la
Especialidad de Hematología del Instituto Nacional de Salud del Niño San Borja.
Adicionalmente puede ser usada por las demás instituciones públicas de salud a nivel
nacional que cuenten con la especialidad y sean del nivel de complejidad.
La Guía será usada en los pacientes pediátricos, niños y adolescentes que presentan el
diagnóstico y reciben tratamiento de Leucemia Mieloide Crónica.
IV.-Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
4.1. NOMBRE Y CODIGO
LEUCEMIA MIELOIDE CRONICA CIE10: C92.1
V.-Consideraciones Generales
5.1. DEFINICIÓN
La leucemia mieloide crónica (LMC) es una neoplasia mieloproliferativa de
naturaleza clonal con origen en una célula madre pluripotencial común a las 3 series
hematopoyéticas.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 4 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
5.2. ETIOLOGÍA
La causa es desconocida. No hay evidencia de que tenga relación con fármacos o
infecciones; los estudios de los efectos de las bombas atómicas y de los
supervivientes del accidente nuclear de Chernóbil demuestran que solo grandes
dosis de radiación pueden inducir la aparición de una LMC.
Lo que sí se conoce es que aparece una traslocación genética de tipo t (9; 22) que
produce un reordenamiento de los genes BCR/ABL, produciendo el
denominado cromosoma Philadelphia (Ph).
La proteína resultante es una tirosina quinasa cuya alteración transforma
el ATP en ADP, fosforilando un sustrato que altera la médula ósea y su
funcionamiento.
5.3. FISIOPATOLOGÍA
Está asociada a la translocación recíproca entre los brazos largos de los cromosomas
9 y 22, t(9;22) (q34.1;q11.2), que da como resultado el cromosoma Philadelphia (Ph)
Los puntos de ruptura involucran al gen ABL1 , ubicado en el brazo largo del
cromosoma 9, y el gen BCR, en el brazo largo del cromosoma 22. La translocación
origina el oncogén de fusión BCR-ABL1, cuya transducción resulta la proteína de
fusión quimérica BCR-ABL1. Esta proteína tiene actividad de tirosina quinasa
constitutiva y causa la activación anormal de varias vías de señalización intracelular,
resultando en inestabilidad genómica, proliferación celular patológica y persistencia
de clones de LMC.
El gen ABL1 normal, codifica una proteína p145 con actividad de tirosina quinasa. El
gen BCR codifica una proteína p160, con actividad de serina-treonina quinasa que
actúa en la regulación del crecimiento celular. Para cumplir con su actividad
quinasa, la proteína ABL1 debe primero ser fosforilada, lo que se logra por medio de
la autofosforilación, dicha proteína tiene tres dominios principales denominados
SH1, SH2 y SH3 (Figura 1) que juntos expresan y regulan la actividad de quinasa.
SH1 es el sitio de unión del ATP; SH2 es el punto de anclaje de las proteínas
receptoras de fosfato y SH3 es el dominio que controla la actividad de fosforilación.
Cuando el ATP se une a su sitio de unión, el fosfato se transfiere a la región SH2 de la
proteína ABL1, que cambia su conformación alterando la estructura terciaria de la
proteína y expone el sitio activo de la enzima. Cuando un segundo ATP se une a su
sitio de unión y una proteína receptora se fija en el dominio SH2, el grupo fosfato es
transferido a la proteína receptora. Esta fosforilación inicia una cascada de señales
intracelulares que culminan en la activación de múltiples factores de transcripción.
Estas vías de transducción de señales están diseñadas para activar los genes
necesarios para controlar la proliferación celular, la diferenciación y la apoptosis. En
la LMC, al producirse la translocación, se pierden los dominios SH2 y SH3 y, con
ellos, la capacidad de autorregulación, llevando a la célula a una actividad
constitutiva de tirosina quinasa, agregando de modo continúo fosfatos a los residuos
de tirosina en las proteínas citoplasmáticas, y la activación de varias vías de
transducción de señales. El resultado es el aumento de la proliferación clonal de
células mieloides secundario a la reducción o la pérdida de la sensibilidad a los
reguladores proteicos, el incremento de la proliferación celular independiente del
factor de crecimiento por la activación del gen RAS, y una disminución de la
apoptosis o resistencia a ella.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 5 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Evaluación de BCR-ABL1
El gen ABL1 normal contiene 11 exones, el punto de corte se produce en forma
constante en el extremo 5´ del exón 2, mientras que el gen BCR normal con 20
exones presenta cuatro posibles puntos de corte que dan lugar a las distintas
isoformas. Las rupturas en el gen BCR se presentan: entre los exones 13 a 15; dando
lugar a la isoforma BCR mayor (BCR-M): transcripto p210 (b2-a2 y b3-a2), presente
en la mayoría de los casos de LMC. Otro punto de corte es en el exón 2; isoforma BCR
menor (BCR-m): transcripto p190 (e1-a2), presente en alrededor del 80% de las
leucemias linfoblásticas agudas Ph+ de los niños y en el 50% de los adultos, siendo
infrecuente en los pacientes con LMC. Y por último, el punto de corte en el exón 19;
isoforma BCR-micro (BCR-μ): transcripto p230 (e3-a2) presente en muchos
pacientes con LMC neutrofílica (LMC-n). Por consiguiente, los cuatro puntos de corte
posibles del BCR producen cuatro genes quiméricos diferentes, lo que resulta en un
total de tres productos proteicos distintos (Figura 2) Por ello es fundamental la
detección del transcripto involucrado al diagnóstico para realizar un correcto
seguimiento de la enfermedad a lo largo del tratamiento.
Figura 1. Regulación fisiológica de la proteína ABL normal y desregulación de
BCR-ABL1 en procesos celulares claves como la proliferación, adherencia y
apoptosis.
Adaptado de: Leucemia Mieloide Crónica-Avances en biología y nuevos enfoques de
tratamiento. New England of Medicine October 9, 2003
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 6 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Figura 2. Translocación t (9; 22) (q34.1; q11.2) en leucemia mieloide crónica
Adaptado de: La Biología de la Leucemia Mieloide Crónica. New England of Medicine July 15,
1999
5.4. ASPECTOS EPIDEMIOLÓGICOS
Es una enfermedad rara en niños y adolescentes, representa el 2-3% de todas las
leucemias en niños menores de 15 años y el 9% en adolescentes entre 15 y 19 años.
La incidencia anual promedio de CML en niños más pequeños de 15 años es 0.6-1.0
casos por millón y de 15-19 años es 2.1 por millón. Es más frecuente en hombres y el
riesgo aumenta con la edad.
Es diferente de la LMC en adultos: Tienden a presentar características mucho más
agresivas (mayor recuento de glóbulos blancos con una mediana de 242 × 10 9 / l,
mayor tamaño del bazo en proporción al tamaño del cuerpo, mayor frecuencia de
fases avanzadas en el momento del diagnóstico)
5.5. FACTORES DE RIESGO ASOCIADO
5.5.1. Medio ambiente
El único factor etiológico definitivo es la radiación ionizante
5.5.2. Estilos de vida
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 7 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
El riesgo no parece verse afectado por el hábito de fumar, la alimentación o
infecciones.
Personas expuestas a pesticidas o bencenos parecen presentar un aumento
moderado del riesgo de aparición de LMC.
5.5.3. Factores hereditarios
No existe una clara predisposición familiar o vínculo con la supresión inmune,
aunque se han publicado informes de casos aislados de LMC infantil en gemelos,
Síndrome de Down, después del trasplante renal.
VI.-Consideraciones Específicas
6.1. CUADRO CLINICO
Es una enfermedad de progresión lenta y no interfiere totalmente con el desarrollo
de los glóbulos rojos, glóbulos blancos y plaquetas, por lo tanto, algunos pacientes
pueden no tener ningún signo o síntoma.
6.1.1. Signos y síntomas
✔ Debilidad
✔ Fatiga
✔ Cansancio durante las actividades cotidianas básicas
✔ Fiebre
✔ Dolor en los huesos
✔ Pérdida de peso sin explicación
✔ Dolor o sensación de saciedad debajo de las costillas, en el lado izquierdo,
debido al agrandamiento del bazo
✔ Sudores nocturnos
6.1.2. Interacción cronológica
No existe interacción cronológica preestablecida por presentar diferentes formas
de afectación.
La historia natural de la LMC está dada por una continua progresión desde una
fase crónica donde el recuento de leucocitos es alto pero la maduración es
normal, hasta una fase blástica caracterizada por el aumento de blastos en
médula ósea (MO) y sangre periférica (SP) superior al 20% acompañada de
defectos en la maduración en un periodo no superior a 5 años cuando no se
recibe tratamiento oportuno. La fase blástica generalmente es precedida por una
fase de aceleración que se evidencia por una neutrofilia marcada y otros signos,
que se describen más adelante.
Sin tratar, la LMC en fase crónica progresará hasta la fase acelerada en 3 a 5 años.
La Fase acelerada sin tratamiento, tiene una mediana de supervivencia entre 4 y
6 meses. La supervivencia es aún menor si se produce una fase blástica, con una
mediana de supervivencia en pacientes sin tratar de 2 a 4 meses.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 8 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
El 92% de los niños son diagnosticados en fase crónica, mientras que un 6% lo son
en fase acelerada y el 2% restante en fase blástica.
6.1.3. Gráficos diagramas o fotografías
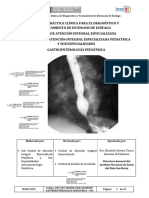
Figura 3. Lamina periferia en leucemia mieloide crónica
Adaptado de: Image Bank. American Society of Hematology October 24, 2018
El Frotis de sangre periférica muestra leucocitosis marcada con la presencia de un
espectro completo de células mieloides que incluyen muchos neutrófilos maduros,
algunos metamielocitos, mielocito y basofilia.
6.2. DIAGNÓSTICO
6.2.1. Criterios de diagnóstico
La identificación de la fase de la LMC en el momento del diagnóstico constituye la
base para la planificación del tratamiento.
No existe una definición o consenso universalmente aceptado sobre la LMC en
fase acelerada (FA) y fase blástica (FB).
La European LeukemiaNet (ELN) utiliza criterios diferentes para definir FA y FB
en comparación con los criterios de la OMS.
La clasificación de la OMS define la FB como ≥ 20% de blastos en la sangre
periférica o medula ósea o la proliferación de blastos extramedulares (puede
ocurrir en cualquier lugar) pero con mayor frecuencia se observa en la piel,
ganglios linfáticos, bazo, huesos o el sistema nervioso central y en niños es
predominantemente linfoblastos.
Recomendamos seguir los criterios de la OMS como se describe a continuación.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 9 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Tabla 1. Criterios diagnósticos para las fases de la enfermedad en la LMC
según la OMS.
FASE CRONICA (FC) FASE ACELERADA (FA) FASE BLASTICA (FB)
Debe cumplir con Debe cumplir con 1 o más de los Debe cumplir con 1 o
todos los siguientes siguientes criterios más de los siguientes
criterios: criterios
Documentación de t (9; Blastos 10% -19% en SP o MO Blastos >20% en SP o
22) o el gen de fusión MO
Bcr-Abl
Blastos en MO < 10% Basófilos en SP al menos 20% Proliferación de
blastos
extramedulares
No cumple ningún Trombocitopenia persistente (100 × Grandes focos o grupos
criterio para la FA o FB 10 9 / L) no relacionada con la terapia, de blastos en la biopsia
o trombocitosis persistente (1000 × de médula ósea
10 9 / L) que no responde a la terapia
El aumento del tamaño del bazo y el
aumento del recuento de glóbulos
blancos que no responden a la terapia
Evidencia citogenética de evolución
clonal (aparición de una anormalidad
genética adicional que no estaba
presente en la muestra inicial en el
momento del diagnóstico de la LMC en
fase crónica)
La proliferación megacariocítica en
láminas y grupos considerables,
asociada con marcada reticulina o
fibrosis de colágeno, y / o displasia
granulocítica severa, debe
considerarse como sugestiva de CML-
FA; aunque estos hallazgos aún no se
han analizado en grandes estudios
clínicos; sin embargo, no está claro si
son criterios independientes para la
fase acelerada; a menudo ocurren
simultáneamente con una o más de las
otras características enumeradas
Adaptado de: La Clasificación de la Organización Mundial de la Salud (OMS) de las Neoplasias
Mieloides. Blood April 4,2002
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 10 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
6.2.2. Diagnóstico diferencial
Para diagnosticar la LMC es suficiente cuando el paciente cursa con importante
leucocitosis y significativa esplenomegalia, pero cuando el paciente tiene una
leucocitosis moderada es importante hacer el diagnóstico diferencial con:
✔ Otros síndromes mieloproliferativos crónicos
✔ Síndromes mieloproliferativos /mielodisplásicos
✔ Leucemia mielomonocitica juvenil
✔ Leucocitosis reactiva
✔ Infecciones
✔ Corticoterapia,
✔ Mieloptisis
✔ Estados de shock
✔ Hemolisis o
✔ Hemorragias agudas
✔ Reacción medular de agranulocitosis.
6.3. Exámenes Auxiliares
6.3.1. De Patología clínica (Ver Tabla 2)
Análisis de sangre
Hemograma, frotis de sangre periférica
Estudio básico de coagulación: Tiempo de protrombina, Tiempo de
Trombina, Tiempo de tromboplastina parcial actividad, fibrinógeno.
Bioquímica: perfil hepático y renal, electrolitos, calcio, fosforo, ácido úrico,
perfil tiroideo (TSH, T4), perfil lipídico, glucosa, Hb glicosilada, PTH, 25-
hidroxi vitamina D, DHL, cortisol, gonadotropina y esteroides sexuales.
Grupo sanguíneo
Serologías de: VHA, VHB, VHC, CMV, VEB, VIH, parvovirus B19.
Test de embarazo (en adolescentes)
Estudios Específicos:
Mielograma: Evaluación de la morfología, % de blastos y % promielocitos
Biopsia ósea: Evaluación de la fibrosis, celularidad, transformación, pero no
obligatoria
Cariotipo: Evaluación de Cromosoma Ph + y / u otras anormalidades
clonales
Hibridación fluorescente in situ (FISH) si falla la citogenética de la médula
Identificación y posterior cuantificación de gen de fusión BCR-ABL p210
por RT-PCR
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 11 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Citometría de flujo: En fase blástica.
6.3.2. De imágenes
Radiografía de tórax
Ecografía abdominal completa
Ecocardiograma, electrocardiograma
Densitometría ósea
6.3.3. De exámenes especiales complementarios
Mutación del dominio de tirosina quinasa en el momento al diagnóstico solo
está indicado para Fase Acelerada / Fase Blástica
Evaluación de la mutación T315I en casos de falta de respuesta inicial al
tratamiento.
Estudio de histocompatibilidad del paciente, hermanos consanguíneos
Desarrollo puberal según la etapa de Tanner
Talla, peso, IMC
Edad Ósea
TABLA 2: Evaluación inicial y seguimiento de LMC
Evaluación En el momento Seguimiento
del diagnostico
Historia clínica y
examen físico con
Cada visita
documentación del X
tamaño del bazo
por palpación (Cm
debajo del margen
costal)
Estatura / peso / X Cada visita
IMC
Escala de Tanner X Cada 6 meses
Hemograma con X Cada visita
formula diferencial
% Blastos X
PCR cuantitativa en X Cada 3 meses
sangre periférica
para BCR-ABL
Aspiración de Morfología X A los 3, 6, 12 meses
médula ósea
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 12 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
% Blastos X
% basófilos X
Cariotipo de X A los 3, 6, 12 meses
medula ósea
PCR cuantitativa X
medula ósea para
BCR-ABL
Biopsia de hueso X
Grupo sanguíneo X
Perfil de INR / APTT X
coagulación
Evaluación cardiaca Ecocardiograma X Anualmente
ECG con X Anualmente
intervalo QT
Química Química X Cada 3 meses
ampliada con
funciones
renales y
hepáticas.
Lipasa X Cada 3 meses
Glucosa X Cada 3 meses
Ácido úrico X Cada 3 meses
Colesterol X Cada 3 meses
Hb A1C X Cada 3 meses
Perfil lipídico X Cada 3 meses
Función de la X 4-6 semanas después de
tiroides inicio de terapia con TKI y
luego anualmente
Virología CMV, panel de X
hepatitis,
varicela zoster
Prueba de HLA X Puede solicitarse más tarde
Adaptado de: Guía de NCCN para la Práctica Clínica en Oncología LMC versión 2.2020 y
Recomendaciones para el manejo de la LMC en niños y jóvenes hasta los 18 años. Brit J
Haematol Junio, 2014; 167: 33–47
6.4. Manejo según nivel de Complejidad y Capacidad Resolutiva
Se recomienda que todo paciente con sospecha de Leucemia Mieloide Crónica sea
derivado inmediatamente a un establecimiento de salud categoría III-1 o III-2 para
ampliar estudios diagnósticos confirmatorios, categorizar el estadio de la
enfermedad (LMC-FC, LMC-FA, LMC-FB), identificar factores de riesgo adicionales
(p. Ej., Aberraciones cromosómicas adicionales) e iniciar tratamiento inmediato.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 13 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
6.4.1. Medidas generales y preventivas
Garantizar una buena hidratación.
Tratar el sangrado o infección, si está presente.
Leucoaferesis si hay evidencia de leucostasis (inusual en LMC con recuentos de
leucocitos <200 × 10 9 / l): infiltrados pulmonares, priapismo, retinopatía
severa/papiledema.
Alopurinol (10 mg / kg; máximo 300 mg). Solo es necesario si el recuento de
glóbulos blancos es> 20 × 10 9 / l.
Iniciar Hidroxiurea 25- 50mg / m2/ día; dividido en 3 dosis (jarabe si está
disponible) hasta que se confirme el diagnóstico de LMC.
6.4.2. Terapéutica
Los Inhibidores de tirosina quinasa (ITK) es la terapia de elección en LMC.
Imatinib (ITK-1G) era el único aprobado pot la FDA para la terapia de primera
línea en pacientes pediátricos. Dasatinib (ITK-2G) fue aprobado como terapia de
primera y segunda línea en 2017. Nilotinib (ITK-2G) también fue aprobado en
2018 como terapia de primera y segunda línea para pacientes pediátricos con
LMC.
LMC FASE CRÓNICA
Primera Línea de tratamiento:
Iniciar Inhibidor de Tirosina Quinasa (ITK) tan pronto como sea posible; una
vez confirmado el diagnóstico, elección de acuerdo con la disponibilidad,
facilidad de administración, costo, toxicidad y comorbilidad asociada. (Ver
fluxograma N° 1)
✔ Imatinib: 340 mg / m2 / una vez al día, (dosis máxima 600 mg) se puede
administrar con alimentos.
✔ Dasatinib: 60 mg / m2/ una vez al día (dosis máxima de 100 mg) se puede
administrar con alimentos.
✔ Nilotinib: 230 mg / m2 /cada 12 horas (dosis máxima 400 mg), evitar
alimentos 2 horas antes y 1 hora después.
Asegurar una adecuada adherencia al tratamiento (Anexo1)
Monitoreo del estado de la enfermedad mediante BCR-ABL cuantitativa cada 3
meses y según (Tabla 3).
Cambiar a un ITK -2G diferente en caso de intolerancia, toxicidad, resistencia o
falla terapeutica es decir no cumple con criterios de respuesta al
tratamiento según (Tabla 4, Tabla 5 y Tabla 6)
TABLA 3: Monitoreo de LMC basado en las recomendaciones de NCCN
RECOMENDACIONES
- Cada visita
Historia clínica y examen físico con
- Semanalmente hasta clínicamente estable
documentación del tamaño del bazo - Quincenal hasta respuesta hematológica
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 14 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
completa
por palpación (centímetros debajo
del margen costal) - Luego mensualmente hasta 3 meses a partir
de diagnóstico y luego cada 3 meses
- Cada visita
Hemograma con formula diferencial
y perfil metabólico completo
- Cada 3 meses hasta respuesta citogenética
Cariotipo de medula ósea
completa (CCyR)
- Falta de respuesta
- Ante cualquier signo de pérdida de respuesta
- En el momento del diagnóstico
PCR cuantitativa en sangre periférica
para BCR-ABL - Cada 3 meses hasta remisión molecular
mayor(RMM) y luego
- cada 3 meses durante 2 años y
- luego cada 3-6 meses.
- Si aumento de 1 log en RMM, repita en 1-3
meses
Análisis de mutaciones Dominio de En fase crónica si
quinasa BCR-ABL - Respuesta inicial inadecuada
- Cualquier signo de pérdida de respuesta o
- Aumento de 1 log en la transcripción o
pérdida de RMM
- Progresión de la enfermedad a AP o BP
Adaptado de: Guía de NCCN para la Práctica Clínica en Oncología Leucemia Mieloide Crónica versión
2.2020
TABLA 4: Criterios para definir la respuesta al tratamiento con TKI en niños y
adolescentes con CML-FC
TIPO DE RESPUESTA DURACION ANTICIPADA DE LA RESPUESTA
Respuesta No signos y síntomas de enfermedad con
Hematológica bazo no palpable
Completa (RHC)
completa (RH)
WBC <10 × 10 3 / L, plaquetas <450 ×
10 9 / L, y <5% de basófilos (todo dentro
de los valores normales apropiados para la
edad)
Ausencia de células inmaduras: mielocitos,
promielocitos o blastos en sangre
periférica.
Respuesta Completa CCyR) Sin metafases con Ph (+)
citogenética (RC)
Parcial (CCyP) 1% a 35% de metafases de Ph (+)
(analizado mínimo en
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 15 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
20 metafases PH +)
Menor 36 a 65% de metafases de Ph (+)
Mínima 66%-95% de metafases de Ph (+)
Respuesta Molecular Respuesta Transcripciones no detectables, o
(RM) molecular reducción de > 3 log en la transcripción
completa (RMC) desde el diagnóstico
transcripciones Bcr-
Abl
Respuesta Transcripciones < 0.1%
Molecular mayor
(RMM)
Recaída Cualquier signo de pérdida de respuesta
(recaída hematológica o citogenética)
Incremento en 1 log en los niveles de
transcripción BCR-ABL1 con pérdida de
MMR debería provocar
estudio de médula ósea para evaluar la
pérdida de CCyR y análisis mutacional
Adaptado de: Guía de NCCN para la Práctica Clínica en Oncología Leucemia Mieloide Crónica versión
2.2020
TABLA 5: Tiempo aceptable para la respuesta terapéutica de ITK de primera
línea.
Tiempo en meses Señales de advertencia Falta de Consideraciones
Respuesta optima respuesta clínicas para pacientes
con signos de
Hematológica advertencia o falta de
y citogenética BCR- respuesta
ABL1
Diagnóstico NA FB o FA; del Nivel NA Evaluar TPH
(9q-); basal
Anormalidades
citogenéticas
adicional
en las células
Ph +
3 meses RHC, Ph+ 36-95% >10% Sin RHC; Evaluar cumplimiento
enfermedad del paciente
BCR-ABL1
estable
≤10% and/or Evaluar las
Ph+ ≤35% o progresión de interacciones
la enfermedad farmacológicas.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 16 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Ph +> 95 Análisis mutacional
Cambiar a ITK
alternativo y evaluar
TPH
6 meses BCR-ABL1 Ph+ 1-35% 1-10% Ph+ >35%
<1% BCR-ABL1
>10%
CCyR (Ph+
0%)
12 meses CCyR , >0.1-1% Ph+ ≥1% BCR-
ABL1 >1%
BCR-ABL1
≤0.1%
Adaptado de: Guía de NCCN para la Práctica Clínica en Oncología Leucemia Mieloide Crónica versión
2.2020
TABLA 6: Definición de respuesta molecular basada en el IS; adoptada de las
pautas de ELN y de NCCN, que se pueden usar en niños
Respuesta
Tiempo en mes óptima Advertencia Fracaso
3 BCR-ABL1 <10% IS BCR-ABL1 ≥10% IS
6 BCR-ABL1 <1% * IS BCR-ABL1 1-10% IS BCR-ABL1 ≥10% IS
12 BCR-ABL1 <0.1% IS BCR-ABL1 0.1-1% IS BCR-ABL1 ≥1% IS
Adaptado de: Guía de NCCN para la Práctica Clínica en Oncología Leucemia Mieloide
Crónica versión 2.2020
Segunda Línea de Tratamiento:
● Antes de iniciar: verificar mutaciones de dominio tirosina quinasa Bcr-Abl y
adherencia al tratamiento.
● Cambiar a ITK-2G: Dasatinib 60 mg / m 2/ día o Nilotinib 230mg/m2/cada 12
horas (de acuerdo con disponibilidad, toxicidad, costo, fácil administración)
● Iniciar búsqueda de hermanos HLA compatibles o donantes no relacionados
● Si el paciente desarrolla progresión o recaída a segunda línea de tratamiento
pasara a TPH alogénica mieloablativa.
LMC Fase Acelerada
● Iniciar con dasatinib a 80 mg / m 2 /d.
● Iniciar búsqueda de hermanos HLA compatibles o donantes no relacionados y
proceder a TPH alogénico mieloablativo una vez en remisión (CCyR).
● Si el paciente falla o tiene una respuesta subóptima en cualquier momento (Tabla
5), proceder inmediatamente a TPH alogénico mieloablativa (ver fluxograma 3)
LMC Fase Blástica
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 17 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
● Iniciar con dasatinib a 80 mg / m 2 /d.
● Iniciar esquema de quimioterapia para Leucemia Aguda de acuerdo a tipificación
por citometria de flujo.
● Iniciar búsqueda de hermanos HLA compatibles o donantes no relacionados
● Una vez en remisión (segunda fase crónica), pasar a TPH alogénico mieloablativo
(ver fluxograma 4)
Tercera Línea de tratamiento:
● Trasplante de Progenitores hematopoyéticos alogénico: (Tabla 7)
● Fase Blástica o Fase Acelerada en el momento del diagnostico
● Progresión a Fase blástica o fase acelerada
● Falla a múltiples ITKs (no cumple con criterios de respuesta)
● Toxicidad o intolerancia inaceptable a ITKs
● En caso de falta de adherencia; el TPH es discutible ya que es necesario también
para los medicamentos de TPH (p. ej., profilaxis de GVHD)
TABLA 7: Consideraciones acerca de la Indicación de TPH Alogénico en niños
con CML en la era de ITK
Indicación de TPH Comentario
Los datos sobre resultados a largo plazo en niños
Sin consenso siguen siendo escasos.
Se recomienda ITK-2G primero. Si no se dispone
Fase avanzada (CML-FA o CML- de un donante adecuado y se logran hitos de
FB) en el momento del respuesta, se puede continuar con ITK bajo
diagnóstico estrecha supervisión.
Realice el intento de lograr un segundo FC con
Progresión a CML-FA o CML-FB ITK-2G primero.
Resistencia a 2 ITKs; intolerancia
inaceptable a todos los ITK Primero dar ponatinib, si está disponible y en
aprobados en niños; Mutación pacientes con peso de adulto solo como terapia
T315I puente a TPH. *
* Ponatinib no está aprobado para su uso en niños. No se han realizado estudios
pediátricos y no se puede recomendar una dosis pediátrica segura.
Adaptado de: Como trato Leucemia Mieloide crónica en Niños y Adolescentes. Blood May
30, 2019
Análisis de la Mutación del dominio quinasa BCR-ABL1
La resistencia primaria a ITK en pacientes con LMC- FC sin complicaciones es raro. Por lo
tanto, no se requiere solicitar de rutina al diagnóstico o en aquellos con una respuesta
óptima a ITK.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 18 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Se recomienda solicitar el análisis mutacional si no se cumple con los criterios de
respuesta al tratamiento (respuesta suboptima), pérdida de respuesta, o se observa
progresión de la enfermedad a Fase Acelerada o Fase Blastica.
6.4.3. Efectos adversos o colaterales del tratamiento
Efectos secundarios frecuentes:
Anemia Moderada a Severa: Se debe recurrir a transfusión o
administración de eritropoyetina en lugar de reducir la dosis.
Neutropenia: si RAN<1 · 0 × 10 9 / l: detener hasta 2 semanas; reiniciar
cuando RAN > 1 · 0 × 10 9 / l. Agregar factor estimulante de colonias de
granulocitos (G-CSF) si la neutropenia persistente y está en Fase
Crónica. Reiniciar dosis completa si la neutropenia dura <2 semanas, de lo
contrario, reduzca la dosis en un 20%.
Plaquetopenia: Si recuentos de plaquetas <50 × 10 9 / l:
suspender; reiniciar cuando las plaquetas estén > 100 × 10 9 / l. Reduzca la
dosis en un 20% si es recurrente.
Síntomas gastrointestinales: son comunes náuseas durante las primeras
semanas de tratamiento. Se recomienda agregar un antiemético, como
ondansetrón, y tomar imatinib antes de acostarse.
Pruebas de función hepática alterada: Observación
Efectos secundarios menos frecuentes
Edema / retención de líquidos: diurético oral, si hay derrame pleural
severo (ocurrencia rara con dasatinib) toracocentesis y curso breve de
esteroides.
Calambres musculares: reposición de calcio / magnesio.
Dolor óseo: afecta al 10% de los niños y disminuye con una terapia más
prolongada, indicar agentes antiinflamatorios no esteroideos.
Erupción cutánea (pruriginoso / maculopapular): observación y agregar
esteroides tópicos.
Diarrea
Letargo
Cefalea
Aumento de peso
Toxicidad cardiaca: Con Imatinib y dasatinib posible pero no probado, con
nilotinib se ha informado prolongación del intervalo QT y muerte súbita;
No usar nilotinib en antecedentes de problemas cardíacos o electrolíticos
(Solicitar EKG, ecocardiograma, electrolitos si hay preocupación clínica).
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 19 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Efectos secundarios endocrinológicos:
Alteración en la densidad ósea: Los ITK tienen un efecto sobre el
metabolismo óseo; se ha descrito hiperparatiroidismo secundario,
hipofosfatemia con fosfaturia, alteración en el metabolismo del calcio, Se
recomienda verificar niveles de calcio, fósforo, hormona paratiroidea
(PTH) y 25-hidroxi vitamina D al inicio y luego seguimiento cada 6 meses,
ingesta adecuada de calcio en la dieta, suplementos de vitamina D con
ergocalciferol o colecalciferol, radiografía simple y densitometría ósea
anualmente.
Alteración en el crecimiento: Se ha reportado alteración del crecimiento
de manera significativa sobre todo en prepúberes, se recomienda medir
peso, talla IMC basal y luego cada 3 meses.
Retraso puberal: Se recomienda evaluación de la pubertad a la edad de 8
años al inicio del tratamiento y luego cada 6 meses hasta la finalizar de la
pubertad. Gonadotropina y esteroides sexuales se deben solicitar al inicio y
más tarde durante el tratamiento si la pubertad o desarrollo sexual se
retrasa (adolescente postpuberal).
Híper o hipoglucemia: Solicitar Hb glicosilada, cortisol sérico anualmente.
Alteración de función tiroidea: Solicitar perfil tiroideo anualmente.
Fertilidad y salud reproductiva: Son teratogénicos y se excretan en la
leche humana, se recomienda para los varones pospuberes banco de
esperma antes de TPH y para las adolescentes evitar la gestación.
Otras consideraciones: No se recomienda vacunas vivas atenuadas, estas
se pueden administrar después de varias semanas de haber suspendido el
tratamiento si está en RM profunda, las vacunas muertas son seguras.
6.4.4. Signos de alarma
✔ Al diagnóstico: Fase Blástica o Fase Acelerada; del (9q-); Anormalidades
citogenética adicional en las células Ph+.
✔ A los 3 meses de tratamiento no respuesta hematológica completa y un
BCR-ABL1> 10%.
✔ A los 6 meses de tratamiento no CCyR (Ph+ 0%) y BCR-ABL >1%
✔ A los 12 meses de tratamiento un BCR-ABL1 > 0.1%
Si hay evidencia de estos signos de alarma seguir consideraciones clínicas según
Tabla 4.
6.4.5. Criterios de Alta
Hasta el momento no hay datos que muestren la viabilidad de suspender el ITK
en la población pediátrica con LMC. Queda pendiente ensayos clínicos
prospectivos adecuados.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 20 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
6.4.6. Pronóstico
Los sistemas de puntuación pronostica para predecir el resultado del tratamiento
en los pacientes con LMC bien establecidos en adultos (p. ej., SOKAL, EUTOS,
HASFORD) no se aplican en niños.
✔ La Fase de la enfermedad al diagnóstico es lo que determina el pronóstico
LMC en fase acelerada o blástica tienen un pronóstico menos favorable que
aquellos con la enfermedad en fase crónica.
Otros factores de mal pronósticos al diagnóstico son:
✔ La edad: En niños y adolescentes tiende ser más agresiva.
✔ Esplenomegalia gigante
✔ Trombocitosis o trombocitopenia
✔ Proporción de blastos elevados en SP
✔ Basófilos y eosinófilos elevados en SP
✔ Marcada leucocitosis
✔ Alteraciones citogenéticas añadidas.
6.5. COMPLICACIONES
✔ Leucostasis: Es poco común en la LMC con recuento de leucocitos < 200 ×
10 9 / l. El riesgo es menor debido a la preponderancia de glóbulos blancos
maduros a diferencia de las leucemias agudas donde la leucocitosis es por la
presencia de blastos. El inicio temprano de Hidroxiurea ayuda a disminuir la
leucocitosis y reducir el riesgo de leucostasis sin necesidad de aféresis.
La evidencia clínica de leucostasis, más que el recuento de leucocitos,
debería ser el indicador de leucoaferesis terapéutica.
Debe realizarse de forma urgente si hay signos de leucostasis y lesión de
órganos terminales como: dificultad respiratoria (infiltrados pulmonares),
priapismo, retinopatía / papiledema grave o síntomas del sistema nervioso
central, relacionados con un accidente cerebrovascular isquémico o
hemorrágico; también es útil en el manejo de la LMC en el embarazo.
Si se usa; con hidratación alcalinizada (3 L/m2/día) para un PH urinario de
7-7.5, Hidroxiurea 25- 50mg / m2/ día; dividido en 3 dosis (jarabe si está
disponible) e iniciar terapia con TKI lo antes posible.
✔ Hiperuricemia: Alopurinol (10 mg / kg/día, 300 mg/m2/día, dosis máxima
300 mg) más hidratación alcalinizada (3 L/m2/día) para un PH urinario de
7-7.5. El alopurinol solo debe ser necesario si el recuento de leucocitos es>
20 × 10 9 / l.
✔ Trombocitosis: En contraste con las leucemias agudas, el recuento de
plaquetas es normal en la LMC-FC o se eleva por encima de 500 × 10 9 / L en
la mitad de los pacientes pediátricos. No requiere antiagregación
plaquetaria, se resuelve al iniciar tratamiento con ITK.
✔ Hemorragias mucocutáneas: Se observa en más del 10% de los niños con
recuentos plaquetarios elevados al momento del diagnóstico. El sangrado es
causado por una concentración plasmática reducida de multímeros grandes
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 21 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
del factor Von Willebrand (Sindrome de VW adquirido) y por anomalías en
la función plaquetaria (trombastenia de Glanzmann). Se resuelve luego de
iniciar el tratamiento con ITK.
✔ Infecciones: Ante fiebre superior a 38ºC o febrícula mantenida, realizar
cultivos e iniciar de inmediato un tratamiento antibiótico empírico dirigido
en primer lugar a la cobertura frente a Bacilos Gram negativos, en segundo
lugar, frente a Cocos Gram positivos y también según la clínica, frente a
anaerobios. Ante la persistencia de fiebre durante 5- 7 días tras el inicio de la
antibioticoterapia y en ausencia de cultivos positivos, valorar la posibilidad
de iniciar tratamiento antifúngico empírico. La profilaxis de la neumonía por
Pneumocystis jiroveci (PJP) no es necesaria con la terapia con TKI.
✔ Citopenias: Soporte Transfusional: Para mantener cifra de Hemoglobina
superior a 7-8 g/dl y mantener plaquetas > a 20 x109/l en situación de
riesgo hemorrágico, e inclusive superior a 50 x109/l, en caso de hemorragia
o procedimiento invasivo como colocación de catéter. Administración de
Filgrastim en caso de neutropenia secundaria a tratamiento con ITK en LMC-
FC: dosis de 5 mcg/kg/día por vía subcutánea o endovenosa. Por vía
endovenosa se administra en 30 minutos y diluyendo el vial de 30 millones
UI en 20 ml de Suero Glucosado 5% (incompatible en suero fisiológico).
✔ Infarto esplénico: Pueden aparecer si hay esplenomegalia masiva. Son una
causa rara de dolor abdominal, realizándose el diagnóstico por tomografía.
El término de trombosis del eje esplenoportal (TEEP) se utiliza cuando la
trombosis se extiende a la vena esplénica, vena mesentérica superior o a
vena mesentérica inferior Ante el diagnóstico de TEEP, la heparinización
precoz influye en el pronóstico y la repermeabilización, que puede lograrse
hasta después de 4-6 meses tras el inicio de la anticoagulación. Por lo que
recomienda mantener anticoagulación al menos durante 6 meses a un año.
La administración de trombolíticos es controvertida, debido a la alta tasa de
complicaciones graves, reservándose para los que no responden a la
anticoagulación.
✔ Rotura esplénica: Rara vez se han notificado casos de rotura esplénica en
adultos y hasta ahora no en niños.
6.6. CRITERIOS DE REFERENCIA Y CONTRARREFERENCIA
REFERENCIA: Todo paciente pediátrico con sospecha clínica de Leucemia Mieloide
Crónica (hiperleucocitosis, leucocitosis, visceromegalia) debe ser referido para
evaluación a un establecimiento de salud del tercer nivel de atención (III-1, III-2),
para un adecuado diagnóstico, clasificación y terapia.
CONTRAREFERENCIA: Los pacientes en tratamientos específicos de acuerdo al
estadio de la enfermedad (LMC-FC o LMC-FA) serán evaluados cada 1 a 3 meses, de
acuerdo a la respuesta según el tiempo de tratamiento en consultorio externo. Los
pacientes estabilizados serán contrareferidos y reevaluados cada 6 meses de
acuerdo con evolución.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 22 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
6.7. FLUXOGRAMAS
Fluxograma N °1: Imatinib primera línea en LMC- Fase Crónica
Adaptado de: Como trato Leucemia Mieloide crónica en Niños y Adolescentes. Blood May 30, 2019
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 23 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Fluxograma N° 2: ITK - 2G (Dasatinib, Nilotinib) primera línea en LMC- Fase Crónica
Adaptado de: Como trato Leucemia Mieloide crónica en Niños y Adolescentes. Blood May 30, 2019
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 24 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Fluxograma N° 3: Manejo LMC- Fase Acelerada
LMC FASE ACELERADA
- Buscar el mejor donante para TPH
- Mutación dominio quinasa
ITK – 2G
Si donante consanguíneo: Donante alterno
TPH en CCyR
Respuesta optima Respuesta subóptima
Continuar ITK - 2G TPH con el mejor
donante o terapia
Indefinidamente experimental
Recomendaciones para el manejo de la LMC en niños y jóvenes hasta los 18 años. Brit J Haematol Junio,
2014; 167: 33–47
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 25 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
Fluxograma N° 4: Manejo LMC-Fase Blástica
LMC FASE BLASTICA
- Buscar el mejor donante para TPH
- Mutación dominio quinasa
Quimioterapia
+
ITK – 2G
2da. Fase crónica: TPH con el mejor No 2da. Fase crónica: Terapia
donante dentro de los 3 meses experimental
ITK - 2G TPK con mejor donante
en segunda Fase crónica
Terapia experimental
Recomendaciones para el manejo de la LMC en niños y jóvenes hasta los 18 años. Brit J Haematol Junio,
2014; 167: 33–47
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 26 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
VII.- AUTORES
Responsable de Implementar la Guía de Práctica Clínica:
Jefe de la Sub Unidad de Atención Integral Especializada del Paciente de
Trasplante de Progenitores Hematopoyéticos.
Dr. Sergio Antonio Murillo Vizcarra.
Jefa del Servicio de Hematología Clínica de la Sub Unidad de Atención Integral
Especializada del Paciente de Trasplante de Progenitores Hematopoyéticos.
Dra. Victoria Angélica Godoy Vila.
Fecha de elaboración:
03/11/2022.
Instituto Nacional de Salud del Niño-San Borja.
Vigencia de la Guía:
Vigencia: 03 años a partir de su aprobación mediante Resolución Directoral.
Equipo responsable de la Elaboración de la Guía de Práctica Clínica:
Médico Hematóloga Victoria Angélica Godoy Vila.
Jefa del Servicio de Hematología Clínica SUAIEP TPH
vgodoy@insnsb.gob.pe
Médico Hematóloga Kelly Margot Monteza Izquierdo.
Médico Asistente de Hematología Clínica SUAIEP TPH
kmonteza@insnsb.gob.pe
Médico Hematóloga Karen Priscilla Valdez Saldaña.
Médico Asistente de Hematología Clínica SUAIEP TPH
kvaldez@insnsb.gob.pe
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 27 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
VIII.-Anexos
ANEXO N° 1: Recomendaciones para mejorar la adherencia a los ITK en
adolescentes con LMC
MEDICO PACIENTE
Informar el horario recomendado para la Incorporar la toma de medicamentos en las
terapia con TKI (Ej., 1 o 2 veces al día, con o rutinas diarias y tomar a la misma hora
sin alimentos, con el estómago vacío). todos los días (Ej. Antes de cepillarse los
dientes por la noche).
Hacer que otros profesionales como Tener un pastillero, un diario de las dosis
Farmacéuticos o, personal de enfermería tomadas u olvidadas y marcar en un
refuercen la información. calendario.
Proporcionar folletos de información para el Usar recordatorios visuales (Ej., Notas en el
paciente. refrigerador, en el espejo).
Mantener documentación clara en el historial Decir a un familiar o amigo cercano que se lo
del paciente (Ej. Citas de reevaluación). recuerde.
Discutir problemas de seguridad de los Configurar una alarma (en un reloj o
medicamentos con el paciente y los padres. teléfono móvil).
Renovar la receta a un horario fijo (Ej., Hacer un contrato con los padres, con
mensualmente, cada 3 meses). recompensas por no olvidarse de tomar el
medicamento.
Comuníquese con su médico acerca de las
dosis que no tomó y las razones por las que
no las tomó.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 28 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
IX.-Referencias Bibliográficas o Bibliografía
1. Hijiya N, Schultz KR, Metzler M, Millot F, Suttorp M. Pediatric chronic myeloid
leukemia is a unique disease that requires a different approach. Blood. 2016;
127(4):392-399.
2. Hijiya N, Millot F, Suttorp M. Chronic myeloid leukemia in children: clinical
findings, management, and unanswered questions. Pediatr Clin North Am. 2015;
62(1):107-119.
3. Castagnetti F, Gugliotta G, Baccarani M, et al; GIMEMA CML Working Party.
Differences among young adults, adults and elderly chronic myeloid leukemia
patients. Ann Oncol. 2015; 26(1):185-192.
4. Millot F, Guilhot J, Suttorp m, et al. advanced phases at diagnosis of childhood
chronic myeloid leukemia: the experience of the International Registry for Chronic
Myeloid Leukemia (CML) in Children and Adolescents (I-CML-Ped Study)
[abstract]. Blood. 2017; 130(suppl 1). Abstract 316.
5. Krumbholz M, Karl M, Tauer JT, et al. Genomic BCR-ABL1 breakpoints in pediatric
chronic myeloid leukemia. Genes Chromosomes Cancer. 2012; 51(11):1045-1053.
6. Ernst T, Busch M, Rinke J, et al. Frequent ASXL1 mutations in children and young
adults with chronic myeloid leukemia. Leukemia. 2018; 32(9):2046-2049.
7. Chae HD, Murphy LC, Donato M, et al. Comparison of the transcriptomic signature
of pediatric vs. adult CML and normal bone marrow stem cells [abstract]. Blood.
2018; 132(suppl 1). Abstract 4246.
8. Chae HD, Murphy LC, Donato M, et al. Comparison of the transcriptomic signature
of pediatric vs. adult CML and normal bone marrow stem cells [abstract]. Blood.
2018; 132(suppl 1). Abstract 4246.
9. Sokal JE, Gomez GA, Baccarani M, et al. Prognostic significance of additional
cytogenetic abnormalities at diagnosis of Philadelphia chromosome-positive
chronic granulocytic leukemia. Blood. 1988; 72(1):294-298.
10. Hasford J, Baccarani M, Hoffmann V, et alPredicting complete cytogenetic response
and subsequent progression-free survival in 2060 patients with CML on imatinib
treatment: the EUTOS score. Blood. 2011; 118(3):686-692.
11. Hasford J, Pfirrmann M, Hehlmann R, et alWriting Committee for the Collaborative
CML Prognostic Factors Project Group. A new prognostic score for survival of
patients with chronic myeloid leukemia treated with interferon alfa. J Natl Cancer
Inst. 1998; 90(11):850-858.
12. Gurrea Salas D, Glauche I, Tauer JT, Thiede C, Suttorp M. Can prognostic scoring
systems for chronic myeloid leukemia as established in adults be applied to
pediatric patients? Ann Hematol. 2015; 94(8):1363-1371.
13. Millot F, Guilhot J, Suttorp M, et al. Prognostic discrimination based on the EUTOS
long-term survival score within the International Registry for Chronic Myeloid
Leukemia in children and adolescents. Haematologica. 2017; 102(10):1704-1708.
14. Bower H, Björkholm M, Dickman PW, Höglund M, Lambert PC, Andersson TM. Life
expectancy of patients with chronic myeloid leukemia approaches the life
expectancy of the general population. J Clin Oncol. 2016; 34(24):2851-2857.
15. Suttorp M, Schulze P, Glauche I, et al. Front-line imatinib treatment in children and
adolescents with chronic myeloid leukemia: results from a phase III trial.
Leukemia. 2018; 32(7):1657-1669.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 29 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
16. Millot F, Baruchel A, Guilhot J, et al. Imatinib is effective in children with previously
untreated chronic myelogenous leukemia in early chronic phase: results of the
French national phase IV trial. J Clin Oncol. 2011; 29(20):2827-2832.
17. Champagne MA, Fu CH, Chang M, et al. Higher dose imatinib for children with de
novo chronic phase chronic myelogenous leukemia: a report from the Children’s
Oncology Group. Pediatr Blood Cancer. 2011; 57(1):56-62.
18. Gore L, Kearns PR, de Martino ML, et alDasatinib in pediatric patients with chronic
myeloid leukemia in chronic phase: results from a phase II trial. J Clin Oncol. 2018;
36(13):1330-1338.
19. Hijiya N, Maschan A, Rizzari C, et al Efficacy and safety of nilotinib in pediatric
patients with Philadelphia chromosome–positive (PH+) chronic myeloid leukemia
(CML): results from a phase 2 trial [abstract]. Pediatr Blood Cancer. 2017; 64(S3).
Abstract S22.
20. Shima H, Tokuyama M, Tanizawa A, et alDistinct impact of imatinib on growth at
prepubertal and pubertal ages of children with chronic myeloid leukemia. J
Pediatr. 2011; 159(4):676-681.
21. Bansal D, Shava U, Varma N, Trehan A, Marwaha RK. Imatinib has adverse effect on
growth in children with chronic myeloid leukemia. Pediatr Blood Cancer. 2012;
59(3):481-484.
22. Samis J, Lee P, Zimmerman D, Arceci RJ, Suttorp M, Hijiya N. Recognizing
endocrinopathies associated with tyrosine kinase inhibitor therapy in children
with chronic myelogenous leukemia. Pediatr Blood Cancer. 2016; 63(8):1332-
1338.
23. Samis J, Lee P, Zimmerman D, Suttorp M, Hijiya N. The complexity of growth failure
in children receiving tyrosine kinase inhibitor therapy for chronic myelogenous
leukemia. Pediatr Blood Cancer. 2017; 64(12): e26703.
24. Millot F, Guilhot J, Baruchel A, et alGrowth deceleration in children treated with
imatinib for chronic myeloid leukaemia. Eur J Cancer. 2014; 50(18):3206-3211.
25. Saussele S, Richter J, Guilhot J, et alEURO-SKI investigators. Discontinuation of
tyrosine kinase inhibitor therapy in chronic myeloid leukaemia (EURO-SKI): a
prespecified interim analysis of a prospective, multicentre, non-randomised, trial.
Lancet Oncol. 2018; 19(6):747-757.
26. Mahon FX. Treatment-free remission in CML: who, how, and why? Hematology Am
Soc Hematol Educ Program. 2017; 2017:102-109.
27. Saußele S, Richter J, Hochhaus A, Mahon FX. The concept of treatment-free
remission in chronic myeloid leukemia. Leukemia. 2016; 30(8):1638-1647.
28. Giona F, Saglio G, Moleti ML, et al. Treatment-free remission after imatinib
discontinuation is possible in paediatric patients with chronic myeloid leukaemia.
Br J Haematol. 2015; 168(2):305-308.
29. de la Fuente J, Baruchel A, Biondi A, et al; International BFM Group (iBFM) Study
Group Chronic Myeloid Leukaemia Committee. Managing children with chronic
myeloid leukaemia (CML): recommendations for the management of CML in
children and young people up to the age of 18 years. Br J Haematol. 2014;
167(1):33-47.
30. Suttorp M, Eckardt L, Tauer JT, Millot F. Management of chronic myeloid leukemia
in childhood. Curr Hematol Malig Rep. 2012;7(2):116-124.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 30 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
31. Hijiya N, Zwaan CM, Rizzari C, et al. Nilotinib in pediatric patients with philadelphia
chromosome-positive (PH+) chronic myeloid leukemia (CML) or PH+ acute
lymphoblastic leukemia (ALL): a pharmacokinetic study [abstract]. Pediatr Blood
Cancer. 2017; 64(S1). Abstract S34.
32. Zwaan CM, Rizzari C, Mechinaud F, et al. Dasatinib in children and adolescents with
relapsed or refractory leukemia: results of the CA180-018 phase I dose-escalation
study of the Innovative Therapies for Children with Cancer Consortium. J Clin
Oncol. 2013; 31(19):2460-2468.
33. Suttorp M, Metzler M, Millot F, et al. Generic formulations of imatinib for treatment
of Philadelphia chromosome-positive leukemia in pediatric patients. Pediatr Blood
Cancer. 2018; 65(12):e27431.
34. Padula WV, Larson RA, Dusetzina SB, et al. Cost-effectiveness of tyrosine kinase
inhibitor treatment strategies for chronic myeloid leukemia in chronic phase after
generic entry of imatinib in the United States. J Natl Cancer Inst. 2016; 108(7):108-
117.
35. Hochhaus A, Saglio G, Hughes TP, et alLong-term benefits and risks of frontline
nilotinib vs imatinib for chronic myeloid leukemia in chronic phase: 5-year update
of the randomized ENESTnd trial. Leukemia. 2016; 30(5):1044-1054.
36. Cortes JE, Saglio G, Kantarjian HM, et alFinal 5-year study results of DASISION: the
Dasatinib Versus Imatinib Study in Treatment-Naïve Chronic Myeloid Leukemia
Patients Trial. J Clin Oncol. 2016; 34(20):2333-2340.
37. Cortes JE, Gambacorti-Passerini C, Deininger MW, et alBosutinib versus imatinib
for newly diagnosed chronic myeloid leukemia: results from the randomized
BFORE Trial. J Clin Oncol. 2018; 36(3):231-237.
38. Giles FJ, Mauro MJ, Hong F, et al. Rates of peripheral arterial occlusive disease in
patients with chronic myeloid leukemia in the chronic phase treated with imatinib,
nilotinib, or non-tyrosine kinase therapy: a retrospective cohort analysis.
Leukemia. 2013; 27(6):1310-1315.
39. Douxfils J, Haguet H, Mullier F, Chatelain C, Graux C, Dogné JM. Association between
BCR-ABL tyrosine kinase inhibitors for chronic myeloid leukemia and
cardiovascular events, major molecular response, and overall survival: a
systematic review and meta-analysis. JAMA Oncol. 2016; 2(5):625-632.
40. Larson RA, Hochhaus A, Hughes TP, et al. Nilotinib vs imatinib in patients with
newly diagnosed Philadelphia chromosome-positive chronic myeloid leukemia in
chronic phase: ENESTnd 3-year follow-up [published correction appears in
Leukemia. 2012;26:2302]. Leukemia. 2012; 26(10):2197-2203.
41. Hantel A, Larson RA. Imatinib is still recommended for frontline therapy for CML.
Blood Adv. 2018; 2(24):3648-3652.
42. Cortes JE. A second-generation TKI should always be used as initial therapy for
CML. Blood Adv. 2018; 2(24):3653-3655.
43. NCCN Clinical Practice Guidelines in Oncology. Chronic myelogenous leukemia,
version 1.2019. National Comprehensive Cancer Network.
44. Radich JP, Deininger M, Abboud CN, et al. Chronic MYELOID LEUKEMIA, VERSion
1.2019, NCCN clinical practice guidelines in oncology. J Natl Compr Canc Netw.
2018; 16(9):1108-1135.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 31 de 32
Instituto Nacional de Salud
del Niño – San Borja
Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Mieloide Crónica en Niños y
Adolescentes
45. NCCN Clinical Practice Guidelines in Oncology. Chronic myelogenous leukemia,
version 2.2020. National Comprehensive Cancer Network.
46. Baccarani M, Castagnetti F, Gugliotta G, Rosti G. A review of the European
LeukemiaNet recommendations for the management of CML. Ann Hematol. 2015;
94(suppl 2):S141-S147.
47. Patel AB, O’Hare T, Deininger MW. Mechanisms of resistance to ABL kinase
inhibition in chronic myeloid leukemia and the development of next generation
ABL kinase inhibitors. Hematol Oncol Clin North Am. 2017; 31(4):589-612.
48. Soverini S, Hochhaus A, Nicolini FE, et al. BCR-ABL kinase domain mutation
analysis in chronic myeloid leukemia patients treated with tyrosine kinase
inhibitors: recommendations from an expert panel on behalf of European
LeukemiaNet. Blood. 2011; 118(5):1208-1215.
49. Millot F, Claviez A, Leverger G, Corbaciglu S, Groll AH, Suttorp M. Imatinib cessation
in children and adolescents with chronic myeloid leukemia in chronic phase.
Pediatr Blood Cancer. 2014; 61(2):355-357.
50. Branford S, Melo JV, Hughes TP. Selecting optimal second-line tyrosine kinase
inhibitor therapy for chronic myeloid leukemia patients after imatinib failure: does
the BCR-ABL mutation status really matter? Blood. 2009; 114(27):5426-5435.
51. Yamamoto M, Hori T, Igarashi K, Shimada H, Tsutsumi H. Response to ponatinib
before hematopoietic stem cell transplantation in a child with relapsed
Philadelphia chromosome-positive acute lymphoblastic leukemia. Pediatr Int
(Roma). 2018; 60(1):85-87.
52. Nickel RS, Daves M, Keller F. Treatment of an adolescent with chronic myeloid
leukemia and the T315I mutation with ponatinib. Pediatr Blood Cancer. 2015;
62(11):2050-2051.
53. Gardiner P, Dvorkin L. Promoting medication adherence in children. Am Fam
Physician. 2006; 74(5):793-798.
54. Mancini J, Simeoni MC, Parola N, et alAdherence to leukemia maintenance therapy:
a comparative study among children, adolescents, and adults. Pediatr Hematol
Oncol. 2012; 29(5):428-439.
Noviembre, 2022 Código: GPC-003/INSN-SB/UAIE/SUAIEPTPH-HC-V.01 Página 32 de 32
También podría gustarte
- Insnsb Manual de HemovigilanciaDocumento16 páginasInsnsb Manual de HemovigilanciaJenny BenitesAún no hay calificaciones
- RD Nâ° 000244-2020-Dg-Insnsb Gpc-009-Insnsb-Usdt-Susd-Ge DT SD Noonan V1 2Documento24 páginasRD Nâ° 000244-2020-Dg-Insnsb Gpc-009-Insnsb-Usdt-Susd-Ge DT SD Noonan V1 2Adri VillegasAún no hay calificaciones
- RD #000160-2021-Dg-Insnsb Guia de Resonancia MagneticaDocumento78 páginasRD #000160-2021-Dg-Insnsb Guia de Resonancia MagneticaErnesto García100% (1)
- Guia Aspirado de Medula Osea Gp-001-Insnsb-Uaiesuaieptph-Hc-V.01Documento17 páginasGuia Aspirado de Medula Osea Gp-001-Insnsb-Uaiesuaieptph-Hc-V.01Javier EspinosaAún no hay calificaciones
- GPC Gran Quemado en PediatríaFDocumento49 páginasGPC Gran Quemado en PediatríaFAngel Bartra FloresAún no hay calificaciones
- RD #000251-2020-Dg-Insnsb Gpc-001-Insnsb-De Enfermedades Oncohematologicas - VF 17.11Documento28 páginasRD #000251-2020-Dg-Insnsb Gpc-001-Insnsb-De Enfermedades Oncohematologicas - VF 17.11Karen BarcenasAún no hay calificaciones
- RD #000079-2022-Dg-Insnsb GPC de Diagnostico y Tratamiento de Linfoma de HodgkinDocumento36 páginasRD #000079-2022-Dg-Insnsb GPC de Diagnostico y Tratamiento de Linfoma de HodgkinSusy RamosAún no hay calificaciones
- RD #000092-2021-Dg-Insnsb GPC Hipotiroidismo CongenitoDocumento33 páginasRD #000092-2021-Dg-Insnsb GPC Hipotiroidismo CongenitoSergio Flores GuarderasAún no hay calificaciones
- GPC Miastenia Gravis 2Documento36 páginasGPC Miastenia Gravis 2Gustavo GutierrezAún no hay calificaciones
- RD #000056-2021-Dg-Insnsb 13-Gpc-013-Insnsb-Usdt-Susd-Ge DG de Las CC V1Documento22 páginasRD #000056-2021-Dg-Insnsb 13-Gpc-013-Insnsb-Usdt-Susd-Ge DG de Las CC V1Danito2588Aún no hay calificaciones
- Guia de Practica Clinica Quiste de Coledoco 2da Rev CRHN Ugc 07.11.22ffDocumento33 páginasGuia de Practica Clinica Quiste de Coledoco 2da Rev CRHN Ugc 07.11.22ffGeronimo Zenteno FelixAún no hay calificaciones
- Guía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Linfoblástica AgudaDocumento132 páginasGuía de Práctica Clínica de Diagnóstico y Tratamiento de Leucemia Linfoblástica Agudavero solAún no hay calificaciones
- RD #000155-2020-Dg-Insnsb Oftalmo - 5 - GPC de Retinopatia Del Prematuro - VFDocumento42 páginasRD #000155-2020-Dg-Insnsb Oftalmo - 5 - GPC de Retinopatia Del Prematuro - VFSusana GuillenAún no hay calificaciones
- Guia de Procedimientos Crossmatch FC-XM V.02-2022Documento15 páginasGuia de Procedimientos Crossmatch FC-XM V.02-2022Nicole Lia Hernandez RojasAún no hay calificaciones
- GPC BronquiolitisFDocumento22 páginasGPC BronquiolitisFAntonio González BenítezAún no hay calificaciones
- GPC FiebreDocumento21 páginasGPC FiebreJosé Francisco Huerta SandovalAún no hay calificaciones
- Guía de Práctica Clínica para El Diagnóstico Y Tratamiento de Los Errores Innatos Del MetabolismoDocumento52 páginasGuía de Práctica Clínica para El Diagnóstico Y Tratamiento de Los Errores Innatos Del MetabolismoClaudia Evelyn Calcina MuchicaAún no hay calificaciones
- RD #000164-2020-Dg-Insnsb Gineco - GPC Transtorno Del Ciclo Menstrual - VFDocumento22 páginasRD #000164-2020-Dg-Insnsb Gineco - GPC Transtorno Del Ciclo Menstrual - VFgreysiAún no hay calificaciones
- RD #000264-2021-DG-INSNSB GUIA DE HEPATOBLASTOMA FINAL Dic 2021 CON CODIGOFDocumento36 páginasRD #000264-2021-DG-INSNSB GUIA DE HEPATOBLASTOMA FINAL Dic 2021 CON CODIGOFDamaris MondacaAún no hay calificaciones
- RD #000248-2019-Dg-Insnsb GPC Via LagrimalDocumento23 páginasRD #000248-2019-Dg-Insnsb GPC Via Lagrimal1309Aún no hay calificaciones
- RD #000143-2021-Dg-Insnsb Guia de Practica ClinicaDocumento27 páginasRD #000143-2021-Dg-Insnsb Guia de Practica ClinicaNicole VeintimillaAún no hay calificaciones
- Diarea Aguda - INSN 2022Documento36 páginasDiarea Aguda - INSN 2022Erick TelloAún no hay calificaciones
- RD #000047-2021-Dg-Insnsb Otorrino - 5 - GPC de Papilomatosis Laringea - VFDocumento57 páginasRD #000047-2021-Dg-Insnsb Otorrino - 5 - GPC de Papilomatosis Laringea - VFGuillermo MoranteAún no hay calificaciones
- RD #000050-2021-Dg-Insnsb GPC Linfangioma Quistico FinalDocumento16 páginasRD #000050-2021-Dg-Insnsb GPC Linfangioma Quistico FinalDalia Emely Carrasco RamosAún no hay calificaciones
- RD #000004-2021-Dg-Insnsb GPC Obesidad Endocrinologia Octubre 2020FDocumento30 páginasRD #000004-2021-Dg-Insnsb GPC Obesidad Endocrinologia Octubre 2020FJulio David Vilca PizarroAún no hay calificaciones
- Politraumatizado Pediátrico - InSN 2020Documento35 páginasPolitraumatizado Pediátrico - InSN 2020Erick TelloAún no hay calificaciones
- Guia de Practica Clinica Tumores SupratentorialesDocumento26 páginasGuia de Practica Clinica Tumores SupratentorialesSusana AreliAún no hay calificaciones
- RD #000234-2020-DG-INSNSB EPILEPSIA EN PEDIATRIA v02Documento45 páginasRD #000234-2020-DG-INSNSB EPILEPSIA EN PEDIATRIA v02Daphne Millene Abregú CarboneroAún no hay calificaciones
- GPC TEC aprobFFDocumento16 páginasGPC TEC aprobFFPamela DíazAún no hay calificaciones
- RD #000185-2020-Dg-Insnsb Gineco - 5 - GPC Hipertrofia de Labios Menores - VFFDocumento19 páginasRD #000185-2020-Dg-Insnsb Gineco - 5 - GPC Hipertrofia de Labios Menores - VFFWonder AllenAún no hay calificaciones
- Guia Practica Quiste Aracnoideo MINISTERIO DE SALUD PERUDocumento15 páginasGuia Practica Quiste Aracnoideo MINISTERIO DE SALUD PERUAlejandroAún no hay calificaciones
- GP Apertura Esternon de Emg y Cierre Esternal DiferidoDocumento31 páginasGP Apertura Esternon de Emg y Cierre Esternal DiferidoYadira GiraldoAún no hay calificaciones
- RD #000138-2021-Dg-Insnsb GP Colecta de Celulas Progenitores FinalDocumento34 páginasRD #000138-2021-Dg-Insnsb GP Colecta de Celulas Progenitores FinalHarold Hendrik Mallaupoma MiguelAún no hay calificaciones
- RD N° 000091-2021-DG-INSNSB Guia de Procedimiento Craniectomia Descompresiva ActualizadoDocumento35 páginasRD N° 000091-2021-DG-INSNSB Guia de Procedimiento Craniectomia Descompresiva ActualizadoNestor PalmaAún no hay calificaciones
- RD #000098-2021-DG-INSNSB GPC 02 Enfermedad Por Reflujo Gastroesofagico 2Documento27 páginasRD #000098-2021-DG-INSNSB GPC 02 Enfermedad Por Reflujo Gastroesofagico 2Yarely De la RosaAún no hay calificaciones
- GP 039-Medicion de Osmolaridad Serica y Urinaria.v2Documento20 páginasGP 039-Medicion de Osmolaridad Serica y Urinaria.v2Luis GonzalezAún no hay calificaciones
- RD #000226-2020-DG-INSNSB Guía Proced Electromiografía - 2020 3REV UGC CHN 19.06.2020Documento39 páginasRD #000226-2020-DG-INSNSB Guía Proced Electromiografía - 2020 3REV UGC CHN 19.06.2020Mt MtAún no hay calificaciones
- RD #000240-2021-DG-INSNSB GP Drenaje Percutáneo de Abscesos y Colecciones LíquidasF-5Documento25 páginasRD #000240-2021-DG-INSNSB GP Drenaje Percutáneo de Abscesos y Colecciones LíquidasF-5Residencia Cirugia GeneralAún no hay calificaciones
- RD #000053-2021-Dg-Insnsb Guia de Practica Clinica Aneurismas Intracraneales PediatricosDocumento33 páginasRD #000053-2021-Dg-Insnsb Guia de Practica Clinica Aneurismas Intracraneales PediatricosJoaquin HIdalgo GarayAún no hay calificaciones
- RD #000269-2021-Dg-Insnsb Guia de Procedimientos Toxoplasma GondiiDocumento16 páginasRD #000269-2021-Dg-Insnsb Guia de Procedimientos Toxoplasma GondiiFrankVillalobosAún no hay calificaciones
- RD #000227-2020-Dg-Insnsb Guia de Procedimiento de Estudio Lectrofisiológico y Ablación en PediatríaDocumento20 páginasRD #000227-2020-Dg-Insnsb Guia de Procedimiento de Estudio Lectrofisiológico y Ablación en PediatríaAnn DéctorAún no hay calificaciones
- RD #000008-2021-Dg-Insnsb 3-Gpc-003-Insnsb-Usdt-Susd-Ge DT SD Klinefelter V1 PDFDocumento20 páginasRD #000008-2021-Dg-Insnsb 3-Gpc-003-Insnsb-Usdt-Susd-Ge DT SD Klinefelter V1 PDFjoanaahmAún no hay calificaciones
- RD #000199-2021-DG-INSNSB GP 3er VENTRICULOSTOMÍA ENDOSCÓPICADocumento22 páginasRD #000199-2021-DG-INSNSB GP 3er VENTRICULOSTOMÍA ENDOSCÓPICAEffy Marcy Tripp Trikix MilAún no hay calificaciones
- RD #000201-2020-DG-INSNSB CYC - 16 - GP Osteomielitis - VFDocumento13 páginasRD #000201-2020-DG-INSNSB CYC - 16 - GP Osteomielitis - VFLuz Verónica Hernández NoriegaAún no hay calificaciones
- Instituto Nacional de Salud Del Niño San Borja: Fecha: Octubre 2020 Página 1 de 24Documento24 páginasInstituto Nacional de Salud Del Niño San Borja: Fecha: Octubre 2020 Página 1 de 24Cristina Elizabeth Salguero CevallosAún no hay calificaciones
- RD #000252-2019-Dg-Insnsb Guía de Práctica Clínica para El Diagnóstico y Tratamiento Del Craneofaringioma en PediatríaDocumento33 páginasRD #000252-2019-Dg-Insnsb Guía de Práctica Clínica para El Diagnóstico y Tratamiento Del Craneofaringioma en PediatríaJorge MontenegroAún no hay calificaciones
- GPC PARA DX Y TX DE LA DISTROFIA MUSCULAR DE DUCHENNE-BECKER-NEUROLOGÍA PED. Revi 02 JulioDocumento26 páginasGPC PARA DX Y TX DE LA DISTROFIA MUSCULAR DE DUCHENNE-BECKER-NEUROLOGÍA PED. Revi 02 JuliorenovacionmedicamentosAún no hay calificaciones
- Talla Baja - InSN 2021Documento48 páginasTalla Baja - InSN 2021Erick TelloAún no hay calificaciones
- Guía de Procedimiento Detección Molecular de La Mutación Tipo A en El Gen Npm1Documento14 páginasGuía de Procedimiento Detección Molecular de La Mutación Tipo A en El Gen Npm1estefanyluzAún no hay calificaciones
- RD #000151-2020-Dg-Insnsb Uro - 3 - GPC Hidronefrosis - VFDocumento20 páginasRD #000151-2020-Dg-Insnsb Uro - 3 - GPC Hidronefrosis - VFAndrea AyalaAún no hay calificaciones
- RD #000175-2020-DG-INSNSB CyC - 1 - GP TRAQUEOSTOMIA - V02Documento11 páginasRD #000175-2020-DG-INSNSB CyC - 1 - GP TRAQUEOSTOMIA - V02Santiago VilatuñaAún no hay calificaciones
- RD #000238-2020-Dg-Insnsb Guia de Procedimientos Recuperacion Post Anestesica Rev UgcDocumento19 páginasRD #000238-2020-Dg-Insnsb Guia de Procedimientos Recuperacion Post Anestesica Rev UgcKATHERINE OLGA SANCHEZ YANAYACOAún no hay calificaciones
- RD #000128-2021-Dg-Insnsb Guia de Drenaje Ok 19FDocumento23 páginasRD #000128-2021-Dg-Insnsb Guia de Drenaje Ok 19FKATTY LUCIA POVES VARGASAún no hay calificaciones
- GPC SD Down AprobDocumento31 páginasGPC SD Down AprobDaniel Ramirez100% (1)
- Kawasaki - InSN 2021Documento25 páginasKawasaki - InSN 2021Erick TelloAún no hay calificaciones
- RD #000194-2020-Dg-Insnsb GPC 003 Diarrea CronicaDocumento19 páginasRD #000194-2020-Dg-Insnsb GPC 003 Diarrea CronicaLilian Serrano TorresAún no hay calificaciones
- RD #000225-2020-DG-INSNSB GP Toxina Botulínica en PX Parálisis CerebralDocumento37 páginasRD #000225-2020-DG-INSNSB GP Toxina Botulínica en PX Parálisis CerebralMayriAún no hay calificaciones
- GPC DE ESTENOSIS DE ESÓFAGO Mayo 2023FFDocumento21 páginasGPC DE ESTENOSIS DE ESÓFAGO Mayo 2023FFSandro ChirioAún no hay calificaciones
- RD #000016-2022-DG-INSNSB GP 064 - Guía Procedimiento FILMARRAYDocumento20 páginasRD #000016-2022-DG-INSNSB GP 064 - Guía Procedimiento FILMARRAYWenSarmientoBAún no hay calificaciones