Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Equipartición de Energía
Cargado por
Jhon Fuentes Gallego0 calificaciones0% encontró este documento útil (0 votos)
22 vistas5 páginasEl documento explica el teorema de la equipartición de la energía en la física estadística clásica y cómo predice la distribución igual de la energía entre los diferentes grados de libertad de un sistema. Sin embargo, experimentos mostraron discrepancias con esta predicción a bajas temperaturas, lo que llevó al desarrollo de la mecánica cuántica para explicar los efectos cuánticos observados.
Descripción original:
quimica
Título original
Equipartición de energía
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEl documento explica el teorema de la equipartición de la energía en la física estadística clásica y cómo predice la distribución igual de la energía entre los diferentes grados de libertad de un sistema. Sin embargo, experimentos mostraron discrepancias con esta predicción a bajas temperaturas, lo que llevó al desarrollo de la mecánica cuántica para explicar los efectos cuánticos observados.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
22 vistas5 páginasEquipartición de Energía
Cargado por
Jhon Fuentes GallegoEl documento explica el teorema de la equipartición de la energía en la física estadística clásica y cómo predice la distribución igual de la energía entre los diferentes grados de libertad de un sistema. Sin embargo, experimentos mostraron discrepancias con esta predicción a bajas temperaturas, lo que llevó al desarrollo de la mecánica cuántica para explicar los efectos cuánticos observados.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 5
Equipartición de energía
Agitación térmica de un péptido con estructura de hélice alfa . Los
movimientos son aleatorios y complejos, la energía de un átomo
puede fluctuar enormemente. Sin embargo, el teorema de
equipartición permite calcular la energía cinética promedio de cada
átomo, así como la energía potencial promedio de muchos modos
de vibración. Las esferas grises, rojas y azules
representan átomos de carbono , oxígeno y nitrógeno respectivame
nte. Las esferas blancas más pequeñas representan átomos
de hidrógeno .
En la física estadística clásica, la equipartición de energía es un
resultado notable según el cual la energía total de un sistema
en equilibrio termodinámico se distribuye en partes iguales en
promedio entre sus diferentes componentes. Este resultado se
sigue muy directamente del postulado fundamental de la física
estadística ; a menudo hablamos del principio de equipartición de
energía.
Más precisamente, el teorema de equipartición da una ecuación
que permite relacionar la temperatura de un sistema macroscópico
con las energías medias de las partículas microscópicas que lo
componen, permitiendo así realizar predicciones cuantitativas. A
menudo se resume con la fórmula: " por término cuadrático en la
expresión de la energía", donde es la constante de Boltzmann y
la temperatura expresada en kelvin . El teorema permite calcular la
energía total de un sistema a una temperatura determinada, a
partir de la cual se puede calcular su capacidad calorífica específica,
antes llamada calor específico o calor específico. Pero también da
los valores promedio de los componentes de la energía, como la
energía cinética de una partícula o la energía potencial asociada
con un modo particular de vibración.
Aunque el teorema de equipartición hace predicciones precisas en
determinadas condiciones, es inexacto cuando los efectos cuánticos son
significativos, como a bajas temperaturas. Cuando la energía térmica k B T es
menor que el espaciado de energía cuántica en un grado particular de
libertad , la energía promedio y la capacidad calorífica de este grado de
libertad son menores que los valores predichos por equipartición. Se dice que
tal grado de libertad está "congelado" cuando la energía térmica es mucho
menor que este espaciamiento. Por ejemplo, la capacidad calorífica de un
sólido disminuye a bajas temperaturas a medida que varios tipos de
movimiento se congelan, en lugar de permanecer constante como predice la
equipartición. Tales disminuciones en la capacidad calorífica fueron uno de
los primeros signos para los físicos del siglo XIX de que la física clásica era
incorrecta y de que se necesitaba un modelo científico nuevo y más sutil.
Junto con otra evidencia, el fracaso de la equipartición para modelar la
radiación de cuerpo negro, también conocida como la catástrofe
ultravioleta, llevó a Max Planck a sugerir que la energía en los osciladores de
un objeto, que emiten luz, estaba cuantificada, una hipótesis revolucionaria
que estimuló el desarrollo de mecánica cuántica y teoría cuántica de
campos .
Las observaciones experimentales de las capacidades
caloríficas específicas de los gases también plantearon
preocupaciones sobre la validez del teorema de
equipartición. El teorema predice que la capacidad
calorífica molar de los gases monoatómicos simples
debe ser aproximadamente 3 cal / (mol · K), mientras
que la de los gases diatómicos debe ser
aproximadamente 7 cal / (mol · K). Los experimentos
confirmaron la predicción anterior, [3] pero
encontraron que las capacidades de calor molar de los
gases diatómicos eran típicamente alrededor de 5
cal / (mol · K), [23] y caían a alrededor de 3 cal / (mol ·
K) a temperaturas muy bajas. [24] Maxwell notó en
1875 que el desacuerdo entre el experimento y el
teorema de equipartición era mucho peor de lo que
incluso estos números sugieren; [25] dado que los
átomos tienen partes internas, la energía térmica
debe entrar en el movimiento de estas partes
internas, haciendo que los calores específicos
predichos de los gases monoatómicos y diatómicos
sean mucho más altos que 3 cal / (mol · K) y 7 cal /
(mol · K ), respectivamente.
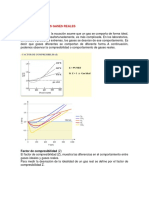
Gráfico idealizado del calor específico molar de un gas diatómico frente a la
temperatura. Concuerda con el valor (7/2) R predicho por equipartición a
altas temperaturas (donde R es la constante del gas ), pero disminuye a
(5/2) R y luego (3/2) R a temperaturas más bajas, como el vibracional y los
modos de movimiento rotacional están "congelados". El fracaso del teorema
de equipartición condujo a una paradoja que solo fue resuelta por la
mecánica cuántica. Para la mayoría de las moléculas, la temperatura de
transición T rot es mucho menor que la temperatura ambiente, mientras
que T vib puede ser diez veces mayor o más. Un ejemplo típico es el monóxido
de carbono, CO, para los que T rot ≈ 2,8 K y T vib ≈ 3.103 K . Para moléculas
con átomos muy grandes o débilmente unidos, T vib puede estar cerca de la
temperatura ambiente (alrededor de 300 K); por ejemplo, T vib ≈ 308 K para
el gas de yodo , I 2 .
Una tercera discrepancia se refería al calor específico de los
metales. [26] Según el modelo clásico de Drude , los electrones metálicos
actúan como un gas casi ideal, por lo que deberían contribuir (3/2) N e k B a
la capacidad calorífica según el teorema de equipartición, donde N e es el
número de electrones . Experimentalmente, sin embargo, los electrones
contribuyen poco a la capacidad calorífica: las capacidades caloríficas
molares de muchos conductores y aislantes son casi las mismas. [26]
Se propusieron varias explicaciones del fracaso de la equipartición para tener
en cuenta las capacidades caloríficas molares. Boltzmann defendió la
derivación de su teorema de equipartición como correcta, pero sugirió que
los gases podrían no estar en equilibrio térmico debido a sus interacciones
con el éter . Lord Kelvin sugirió que la derivación del teorema de
equipartición debe ser incorrecta, ya que no estaba de acuerdo con el
experimento, pero no pudo mostrar cómo. En 1900 Lord Rayleigh en lugar
presentar una visión más radical que el teorema de equipartición y la
asunción experimental de equilibrio térmico eran tanto correcta; para
reconciliarlos, señaló la necesidad de un nuevo principio que proporcione un
"escape de la destructiva simplicidad" del teorema de equipartición. Albert
Einstein proporcionó ese escape, al demostrar en 1906 que estas anomalías
en el calor específico se debían a efectos cuánticos, específicamente la
cuantificación de la energía en los modos elásticos del sólido. Einstein utilizó
el fracaso de la equipartición para defender la necesidad de una nueva teoría
cuántica de la materia. Las medidas de Nernst de 1910 de calores específicos
a bajas temperaturas apoyaron la teoría de Einstein y llevaron a la aceptación
generalizada de la teoría cuántica entre los físicos.
También podría gustarte
- Equiparticion de La EnergiaDocumento2 páginasEquiparticion de La Energiajljo0% (1)
- Teorema de EquiparticiónDocumento34 páginasTeorema de EquiparticiónC DiazAún no hay calificaciones
- Teorema de EquiparticiónDocumento53 páginasTeorema de EquiparticiónMarck R. Quispe AtamariAún no hay calificaciones
- Teorema de EquiparticiónDocumento26 páginasTeorema de EquiparticiónChristian Adolfo Bravo MartínezAún no hay calificaciones
- Mecanismos de Transferencia - CalorDocumento5 páginasMecanismos de Transferencia - CaloralexanderAún no hay calificaciones
- Transición Lambda (Transformaciones de Fases)Documento5 páginasTransición Lambda (Transformaciones de Fases)Dulce Job BenitezAún no hay calificaciones
- Termo TemperaturaDocumento36 páginasTermo TemperaturaValentina Aburto57% (7)
- FFFFDocumento9 páginasFFFFCesar CardonaAún no hay calificaciones
- Seminario Gases Ideales y Reales 2016-2 ListoDocumento18 páginasSeminario Gases Ideales y Reales 2016-2 ListoAraceli Fernandez MendozaAún no hay calificaciones
- Separata Nº15 - Fisica - Transferencia de CalorDocumento5 páginasSeparata Nº15 - Fisica - Transferencia de CalorCarlos Eduardo Joo GarcíaAún no hay calificaciones
- Calor Termo PDFDocumento112 páginasCalor Termo PDFAngelica RojasAún no hay calificaciones
- Cero AbsolutoDocumento7 páginasCero AbsolutoyonnsalAún no hay calificaciones
- Uriel TTDocumento21 páginasUriel TTUriel AlvarezAún no hay calificaciones
- .. Word Energia CineticaDocumento8 páginas.. Word Energia CineticaGilberto MendozaAún no hay calificaciones
- Problemas Res. Cap 23Documento6 páginasProblemas Res. Cap 23Tomás HerzogAún no hay calificaciones
- Actividad 4Documento9 páginasActividad 4Amparo DelatorreAún no hay calificaciones
- TermodinamicaDocumento16 páginasTermodinamicaronnyAún no hay calificaciones
- Apunte I TermodinamicaDocumento74 páginasApunte I TermodinamicaValdebenito Muñoz ClaudioAún no hay calificaciones
- Resumen Capítulo 2 ChangDocumento2 páginasResumen Capítulo 2 ChangJesús HernándezAún no hay calificaciones
- Calor y Energía Térmica PDFDocumento14 páginasCalor y Energía Térmica PDFHellen RozoAún no hay calificaciones
- La Transferencia de Calor Está Relacionada Con Los Cuerpos Calientes y Fríos LlamadosDocumento2 páginasLa Transferencia de Calor Está Relacionada Con Los Cuerpos Calientes y Fríos LlamadosManuel Aguilar MartinezAún no hay calificaciones
- Manual de Termodinamica InacapDocumento96 páginasManual de Termodinamica InacapAlbenis160Aún no hay calificaciones
- Ecuación de Estado para Gases RealesDocumento13 páginasEcuación de Estado para Gases RealesCristian Ccaso MamaniAún no hay calificaciones
- Capacidad CaloríficaDocumento9 páginasCapacidad CaloríficaFernando SánchezAún no hay calificaciones
- Clement DesormesDocumento14 páginasClement DesormesRodrigo RodryAún no hay calificaciones
- El Experimento de FranckDocumento4 páginasEl Experimento de FranckJunior DiazAún no hay calificaciones
- Taller Historia de La Termodinámica, 23 SepDocumento5 páginasTaller Historia de La Termodinámica, 23 SepK-rlosGarciaGarciaAún no hay calificaciones
- Einstein Albert - Annus MirabilisDocumento86 páginasEinstein Albert - Annus MirabilisAdrian RuizAún no hay calificaciones
- 3.5 Termodinamica.Documento11 páginas3.5 Termodinamica.MaxDrucker100% (1)
- El Experimento de La Gota de AceiteDocumento24 páginasEl Experimento de La Gota de AceiteFatimaBermudezAún no hay calificaciones
- CALOR Final 08Documento35 páginasCALOR Final 08pablo.mendeluk100% (11)
- Resumen Capítulo 5 A 8Documento9 páginasResumen Capítulo 5 A 8EVER EUGENIO TRISTAN YEPIZAún no hay calificaciones
- Mecánica Clásica Átomo de Hidrógeno Problema de Los Dos CuerposDocumento1 páginaMecánica Clásica Átomo de Hidrógeno Problema de Los Dos CuerposMiguel Le GrandAún no hay calificaciones
- Colectividad CanónicaDocumento4 páginasColectividad CanónicaJoseAún no hay calificaciones
- Ley de CharlesDocumento15 páginasLey de CharlesOmar PerezAún no hay calificaciones
- Copia de DocumentoDocumento4 páginasCopia de Documentosofia.f.duran.aAún no hay calificaciones
- Biologia NovenoDocumento5 páginasBiologia NovenoINSTITUTO TECNICO NUEVO MILENIO IDETECAún no hay calificaciones
- Informe #5 Peso EquivalenteDocumento19 páginasInforme #5 Peso EquivalenteGiancarlo Sanchez33% (3)
- Introduccion A La Fisica ModernaDocumento12 páginasIntroduccion A La Fisica ModernaLeslie MartínezAún no hay calificaciones
- Quimica General IDocumento18 páginasQuimica General ISofía Alvarez HernandezAún no hay calificaciones
- Nicolas Léonard Sadi Carnot, Considerado Como El "Padre de La Termodinámica", Fue El Primero en Establecer Las Bases Sobre Las Que Se Formularon Después Las Leyes de La TermodinámicaDocumento7 páginasNicolas Léonard Sadi Carnot, Considerado Como El "Padre de La Termodinámica", Fue El Primero en Establecer Las Bases Sobre Las Que Se Formularon Después Las Leyes de La TermodinámicaCANDELARIO VELA LARAAún no hay calificaciones
- Tema 57 en WordDocumento16 páginasTema 57 en WordfaniAún no hay calificaciones
- Fisca 4Documento6 páginasFisca 4Jhan Carlos Alania AldanaAún no hay calificaciones
- Leyes Fundamentales de La Quà - Mica y Teorã - A Atã MicaDocumento19 páginasLeyes Fundamentales de La Quà - Mica y Teorã - A Atã MicaAmeth PittiAún no hay calificaciones
- Conductividad Termica de Los Materiales y Ley de FourierDocumento122 páginasConductividad Termica de Los Materiales y Ley de FourierCynthia NegreteAún no hay calificaciones
- Marcelino Muñoz Trejo - Ensayo (Entalpía y Entropía) BMEDocumento5 páginasMarcelino Muñoz Trejo - Ensayo (Entalpía y Entropía) BMEMarc MuñozAún no hay calificaciones
- La Termodinámica 1Documento12 páginasLa Termodinámica 1sachaa8hotmail.comAún no hay calificaciones
- El Atomo A1Documento17 páginasEl Atomo A1Julian Camilo Tilano DurangoAún no hay calificaciones
- Capacidad CaloríficaDocumento6 páginasCapacidad CaloríficaYubelgx100% (1)
- QUÍMICADocumento9 páginasQUÍMICAraul tapra velardeAún no hay calificaciones
- Operaciones Unitarias en Ingenieria AmbientalDocumento16 páginasOperaciones Unitarias en Ingenieria Ambientaljorge curo panccaAún no hay calificaciones
- Transferencia de CalorDocumento3 páginasTransferencia de CalorMartyn Enoc Rioja OrtegaAún no hay calificaciones
- Ley de Dilución de OstwaldDocumento33 páginasLey de Dilución de Ostwalduriel140580% (5)
- Sistemas de Capacidad Térmica GlobalDocumento15 páginasSistemas de Capacidad Térmica GlobalJesus CordovaAún no hay calificaciones
- Segunda Ley de La TermodinamicaDocumento10 páginasSegunda Ley de La TermodinamicaJOSE ESCOBAR HERRERAAún no hay calificaciones
- Calor Específico, Capacidad Calorifica y Expasión TermicaDocumento17 páginasCalor Específico, Capacidad Calorifica y Expasión TermicaRitchie DanielAún no hay calificaciones
- Ley de Enfriamiento de NewtonDocumento3 páginasLey de Enfriamiento de NewtonShirley CernaAún no hay calificaciones
- Resumen Las 4 Leyesdel UniversoDocumento6 páginasResumen Las 4 Leyesdel UniversoEFRAIN EDGARDO CORNEJO MARQUEZAún no hay calificaciones
- Mecánica Cuántica Relativista y No Relativista: las dos a la vez: Parte I: Estados estacionariosDe EverandMecánica Cuántica Relativista y No Relativista: las dos a la vez: Parte I: Estados estacionariosAún no hay calificaciones
- Determinación de La Conductancia Molar y Análisis Gravimétrico Del Contraión y de Los Metales de Los ComplejosDocumento2 páginasDeterminación de La Conductancia Molar y Análisis Gravimétrico Del Contraión y de Los Metales de Los ComplejosJhon Fuentes GallegoAún no hay calificaciones
- Carlos Paredes Diaz-FqDocumento1 páginaCarlos Paredes Diaz-FqJhon Fuentes GallegoAún no hay calificaciones
- Informe SUSTITUCIÓN NUCLEOFÍLICA SN1Documento11 páginasInforme SUSTITUCIÓN NUCLEOFÍLICA SN1Jhon Fuentes GallegoAún no hay calificaciones
- Oscilaciones Amortiguadas 123Documento4 páginasOscilaciones Amortiguadas 123Jhon Fuentes GallegoAún no hay calificaciones
- UntitledDocumento16 páginasUntitledJhon Fuentes GallegoAún no hay calificaciones
- UntitledDocumento3 páginasUntitledJhon Fuentes GallegoAún no hay calificaciones
- Ley de HessDocumento4 páginasLey de HessJhon Fuentes GallegoAún no hay calificaciones
- FORO Fenomenos de TransporteDocumento3 páginasFORO Fenomenos de TransporteJhon Fuentes GallegoAún no hay calificaciones
- Qué Son Las Ondas ElectromagnéticasDocumento7 páginasQué Son Las Ondas ElectromagnéticasJhon Fuentes GallegoAún no hay calificaciones
- FORO Fenomenos de TransporteDocumento3 páginasFORO Fenomenos de TransporteJhon Fuentes GallegoAún no hay calificaciones
- Informe #2 OrganicaDocumento5 páginasInforme #2 OrganicaJhon Fuentes GallegoAún no hay calificaciones
- Resumen: P Co/CwDocumento1 páginaResumen: P Co/CwJhon Fuentes GallegoAún no hay calificaciones
- ENSAYO Q. ComputacionalDocumento5 páginasENSAYO Q. ComputacionalJhon Fuentes GallegoAún no hay calificaciones
- Taller ResuentoDocumento8 páginasTaller ResuentoJhon Fuentes GallegoAún no hay calificaciones
- Mezcla Urea Alcohol Etilico (G) Alcohol Etilico (KG) T (°C) T (K)Documento5 páginasMezcla Urea Alcohol Etilico (G) Alcohol Etilico (KG) T (°C) T (K)Jhon Fuentes GallegoAún no hay calificaciones
- Propiedades ColigativasDocumento8 páginasPropiedades ColigativasJhon Fuentes GallegoAún no hay calificaciones
- Informe Lab - Determinación de Pesos Moleculares - Método de Dumas de GasesDocumento23 páginasInforme Lab - Determinación de Pesos Moleculares - Método de Dumas de GasesJhon Fuentes GallegoAún no hay calificaciones
- Taller 2 - GasesDocumento16 páginasTaller 2 - GasesJhon Fuentes GallegoAún no hay calificaciones
- Informe #2 Masa Molecular de Una Sustancia VolátilDocumento25 páginasInforme #2 Masa Molecular de Una Sustancia VolátilJhon Fuentes GallegoAún no hay calificaciones
- Taller N°1 - Teoria Cinetico-Molecular de Los GasesDocumento6 páginasTaller N°1 - Teoria Cinetico-Molecular de Los GasesJhon Fuentes GallegoAún no hay calificaciones
- Clase 4. 21-04Documento8 páginasClase 4. 21-04Karen CisternasAún no hay calificaciones
- Control de Plagas y Enfermedades. Orellana 4Documento2 páginasControl de Plagas y Enfermedades. Orellana 4Kristian Giovanny Palencia BlancoAún no hay calificaciones
- 16JB, JH: Enfriadoras de Agua de AbsorciónDocumento2 páginas16JB, JH: Enfriadoras de Agua de AbsorciónJose CuevasAún no hay calificaciones
- Tema 9Documento49 páginasTema 9sorayazeyyafAún no hay calificaciones
- Diseño, Operación y Optimizacion de Sist. Trat. CrudoDocumento116 páginasDiseño, Operación y Optimizacion de Sist. Trat. CrudoLuis Enrique Leyva OvalleAún no hay calificaciones
- Calibracion Del CalorimetroDocumento7 páginasCalibracion Del CalorimetroLaura StylesAún no hay calificaciones
- ACT9Documento3 páginasACT9Luis Ernesto Valdez GalavizAún no hay calificaciones
- P11.2 y 11.3 - VelazquezDocumento11 páginasP11.2 y 11.3 - VelazquezAngel VelazquezAún no hay calificaciones
- Tesis Asfalto Con CauchoDocumento0 páginasTesis Asfalto Con CauchoC.m. WilAún no hay calificaciones
- Primer Taller de Transferencia de Calor I 2024Documento5 páginasPrimer Taller de Transferencia de Calor I 2024Ruben Dario Agredo NovaAún no hay calificaciones
- 16 Calor y FrioDocumento2 páginas16 Calor y FrioRosario NuñezAún no hay calificaciones
- 1-Calor y Transferencia de EnergíaDocumento9 páginas1-Calor y Transferencia de EnergíaAlfonso SegarraAún no hay calificaciones
- Teoría Cuántica, El Principio de Church-Turing y La Computadora Cuántica UniversalDocumento18 páginasTeoría Cuántica, El Principio de Church-Turing y La Computadora Cuántica UniversalLaura Milena RBAún no hay calificaciones
- Guia Termodinamica Aplicada IDocumento5 páginasGuia Termodinamica Aplicada IJose MuñozAún no hay calificaciones
- CalorimetriaDocumento7 páginasCalorimetriaFrancisca MontalvoAún no hay calificaciones
- Práctica 7-1 Capacidad Calorífica de Un Calorímetro.Documento3 páginasPráctica 7-1 Capacidad Calorífica de Un Calorímetro.ulises rhoadsAún no hay calificaciones
- Definición Del Mantenimiento PredictivoDocumento6 páginasDefinición Del Mantenimiento PredictivoJose BriceñoAún no hay calificaciones
- Fundamentos de SecadoDocumento2 páginasFundamentos de SecadoAndrea SifuentesAún no hay calificaciones
- Sustancias RefrigerantesDocumento19 páginasSustancias RefrigerantesAlonsoZarzosaAún no hay calificaciones
- Protocolo de Investigacion Princiio de Los Sistemas de Rrefrigeracion para QuesosDocumento7 páginasProtocolo de Investigacion Princiio de Los Sistemas de Rrefrigeracion para QuesosAntonio FloresAún no hay calificaciones
- Rep. 1H. Estación Meteorológica AutomáticaDocumento2 páginasRep. 1H. Estación Meteorológica AutomáticaVicky MorenoAún no hay calificaciones
- TAREA-CICLO DE REFRIGERACIÓN - Ángel SantamaríaDocumento18 páginasTAREA-CICLO DE REFRIGERACIÓN - Ángel Santamaríaangelfsv040102Aún no hay calificaciones
- Ciclo de CarnotDocumento6 páginasCiclo de CarnotJorge FabiánAún no hay calificaciones
- Aire Humedo1 PDFDocumento37 páginasAire Humedo1 PDFunsa 2020Aún no hay calificaciones
- Practica 3Documento3 páginasPractica 3JUAN JOEL RUIZ HUALIAún no hay calificaciones
- Problemas ResueltosDocumento10 páginasProblemas ResueltosDavid Fontecha60% (5)
- Codigo Asme Seccion V Articulo 6 2015Documento17 páginasCodigo Asme Seccion V Articulo 6 2015Juan Yunior Cano CervantesAún no hay calificaciones
- Talleres 1 y 2Documento9 páginasTalleres 1 y 2MariapAún no hay calificaciones
- Diseno 2k FactorialDocumento16 páginasDiseno 2k Factorialcrisglez60Aún no hay calificaciones
- Informe Doble TuboDocumento5 páginasInforme Doble TuboPAULA ALEJANDRA MALDONADO PULIDOAún no hay calificaciones