Documentos de Académico
Documentos de Profesional
Documentos de Cultura
APF 1.5.3 Protocolo Notificacion Sospecha de RAM en HRLBO V0 2021
Cargado por
karinaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
APF 1.5.3 Protocolo Notificacion Sospecha de RAM en HRLBO V0 2021
Cargado por
karinaCopyright:
Formatos disponibles
PROTOCOLO DE NOTIFICACIÓN DE SOSPECHA DE
REACCIONES ADVERSAS A MEDICAMENTOS (RAM) EN
HOSPITAL LIBERTADOR BERNARDO O´HIGGINS
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 1 de 9
1. OBJETIVOS
Definir el proceso de Farmacovigilancia pasiva, mediante la estandarización de las
notificaciones de sospecha de RAM, sensibilizando además sobre la relevancia del
reporte oportuno de la misma. De este modo se espera, contribuir a mejorar la
seguridad de nuestros pacientes, en el uso racional de medicamentos.
2. ALCANCE
Aplica a todos los profesionales de los equipos clínicos que participan tanto en la
prescripción como en la administración de medicamentos en pacientes del HRLBO.
Población objetivo, pacientes que reciben administración de medicamentos en
HRLBO.
3. DEFINICIONES
• Farmacovigilancia (FV): Es el conjunto de actividades relacionadas con la
detección, evaluación, comprensión y prevención de los efectos adversos asociados al
uso de los medicamentos o cualquier otro problema relacionado con medicamentos.
• Reacción Adversa a Medicamento (RAM): Es una respuesta a un medicamento
que es nociva, no intencionada y que ocurre a dosis normalmente utilizadas en el ser
humano.
• Reacción Adversa Grave: Cualquier RAM que cumpla una de las siguientes
condiciones:
o Ponga en peligro la vida o sea mortal.
o Implique incapacidad o invalidez grave.
o Cause o prolongue la hospitalización.
• Reacción Adversa Inesperada: Es una reacción adversa que no se menciona en la
monografía del producto, o en los folletos de información al paciente o al profesional
autorizados en el respectivo registro sanitario.
• Abuso: Uso excesivo intencionado, permanente, o esporádico, de un medicamento,
que se ve acompañado de efectos nocivos físicos o psicológicos.
• Falta de eficacia: Falla inesperada de un medicamento para producir el efecto
deseado, según lo determinado por la investigación científica previa.
• Causalidad: Es la relación de asociación entre el medicamento administrado y el
evento adverso observado.
• Formulario de notificación: Formulario para el reporte de sospechas de reacciones
adversas, tanto en soporte papel como electrónico.
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 2 de 9
• FV Pasiva: Sistema de notificaciones espontáneas basada en la identificación y
detección de las reacciones adversas sospechosas.
• FV Activa: Procedimientos de Farmacovigilancia intensiva, basados en la recolección
sistemática y detallada de datos sobre todos los efectos perjudiciales que pueden
suponerse inducidos por medicamentos en determinados grupos de población.
Estudios epidemiológicos.
• Centro Nacional de Farmacovigilancia: Corresponde a la sección del Instituto de
Salud Pública de Chile responsable de coordinar el Programa Nacional de
Farmacovigilancia.
• QF: Químico Farmacéutico
• Signos: En medicina, un signo es algo que se identifica durante un examen físico o
en una prueba de laboratorio que indica la posibilidad de que una persona tenga una
afección o enfermedad
• Síntomas: Problema físico o mental que presenta una persona, el cual puede indicar
una enfermedad o afección. Los síntomas no se pueden observar y no se manifiestan
en exámenes médicos
4. RESPONSABLES
• Profesionales de los Equipos de Servicios Clínicos:
Conocer y cumplir el presente protocolo.
Responsables de notificar todas las sospechas de reacciones adversas a
medicamentos de la que tenga conocimiento, mediante el formulario de notificación.
• Químico Farmacéutico Encargado de Farmacovigilancia:
Elaborar, difundir, supervisar el cumplimiento del presente protocolo.
Es el encargado de recepcionar, revisar, analizar y validar todos los reportes e
informarlos en la plataforma RED-RAM perteneciente al Dpto. de Farmacovigilancia
del ISP.
• Químico Farmacéutico Jefe de Farmacia:
Conocer y colaborar en temas relacionados a la supervisión e implementación del
presente protocolo.
5. DESARROLLO
5.1 Proceso de Notificación:
Los profesionales deben completar el formulario de “Notificación de Sospecha de
RAM” con la información requerida, a través de:
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 3 de 9
✓ Formulario en formato Excel disponible en el computador del Servicio Clínico
(Anexo N°1).
Posteriormente, debe ser enviada al correo electrónico:
farmacovigilancia.hrlbo@gmail.com, las notificaciones se pueden realizar las 24 horas
del día, los 7 días de la semana.
El profesional notificador debe priorizar la notificación de RAM graves o inesperadas.
Son de importancia aquellas RAM de medicamentos de reciente incorporación en el
arsenal farmacológico del Hospital. También se pueden notificar RAM de productos
biológicos, biotecnológicos, radiofármacos, y/o fitofármacos. Además, se pueden
realizar reportes relacionados con el mal uso de los medicamentos, es decir, en
situaciones de abuso o dependencia y falta de eficacia. Es importante que cada caso
antes señalado, se notifique sólo una vez para no producir duplicidad de la
información.
En HRLBO y en cumplimiento a recomendación ISP, el Departamento de Calidad e
IAAS, envía notificaciones recibidas de Eventos Adversos, correspondientes a Errores
de Medicación (asociados a la administración) a Encargado de Farmacovigilancia,
para la revisión, ante una eventual asociación a sospecha de RAM.
Esta actividad tiene como objetivo, realizar una mayor pesquisa a nivel institucional
de este tipo de eventos, contribuyendo así, a la generación de acciones preventivas o
a la elaboración de normativas de manejo de RAM.
5.2 Procedimiento de Registro en Formulario de Notificación RAM.
a) Reporte:
Señale en el casillero correspondiente si este reporte es inicial o es un seguimiento
de un reporte anterior. Esta información será de gran utilidad para obtener
información adicional en el caso que sea necesario.
b) Seleccione Tipo de Reporte:
• Espontáneo: Corresponde al caso que es identificado en forma espontánea,
es decir, se produce sin haber una búsqueda sistemática de casos y, una vez
identificado, se decide notificar.
• De Estudio: Corresponde a un caso que se identifica a través de una
búsqueda activa o sistemática de casos, es decir, es detectado con una
metodología aplicada, la cual está destinada a detectar y recolectar la
información de todos los casos que se produzcan en la muestra o población
seleccionada. Puede tratarse de estudios clínicos, estudios de utilización de
medicamentos, estudios farmacoepidemiológicos, estudios
farmacoeconómicos, monitoreo intensivo, entre otros.
• Otro: Esta clasificación está destinada a clasificar los reportes que no
corresponden a un caso espontáneo ni provienen de un estudio (ejemplo: un
programa de seguimiento de pacientes).
• Desconocido: Corresponde a la clasificación de los reportes obtenidos de
literatura, en los que no se puede determinar el origen de la detección o bien
existe la duda de si provienen de una detección espontánea o de estudio.
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 4 de 9
c) Datos Del Paciente:
• Iniciales del paciente: Corresponde a un identificador del paciente,
destinado a distinguirlo de otros pacientes, resguardando su identidad. Se
recomienda usar las iniciales del o la paciente.
• RUN/Número de Ficha Clínica: Proporcionar un identificador interno,
destinado a la trazabilidad de los datos. Es útil para investigar datos
adicionales o hacer un seguimiento.
• Sexo: Consignar el género masculino, femenino o intersex del paciente
afectada (o) por la RAM.
• Unidad/Servicio Clínico: Señalar la unidad o servicio donde se encontraba
el paciente al momento de presentar la RAM (es útil para efectos de
seguimiento y para entender el contexto del paciente).
• Grupo etario: Se debe consignar tanto si se conoce como si se desconoce la
edad exacta del paciente. En este último caso, se constituye en un campo
validador de la información.
• Edad: Expresar de preferencia en años (A). Utilizar meses (M) solo si el
paciente es menor de 1 año (Ej. 04 M) y días (D), si es menor de un mes (Ej.
15 D). No olvidar consignar la unidad.
• Peso: Expresar en Kg. Esta información es particularmente importante en
ancianos, niños y pacientes desnutridos u obesos. Si desconoce el peso
exacto, por favor coloque el peso aproximado y entre paréntesis indique
"aprox."
• Talla: Usar cm. Este dato es de gran importancia en niños y en el reporte de
sospecha de RAM de fármacos oncológicos.
• Pueblo indígena declarado: Se debe consultar al paciente o al familiar
responsable de la siguiente forma: ¿Pertenece usted (el paciente) a alguno de
los siguientes pueblos indígenas: Alacalufe o Kawashkar, Atacameño o Lickan
Antay, Aimara, Colla, Diaguita, Mapuche, Quechua, Rapa Nui, Yámana o
Yagán. Luego de esto, debe registrarse la respuesta en el formulario,
utilizando el código de 2 dígitos correspondiente, según el siguiente esquema:
o 00: El paciente no pertenece a ningún pueblo originario.
o 01 a 09: El paciente pertenece a alguno de los pueblos originarios
listados. El código específico se elige de acuerdo a la tabla de
codificación que se encuentra en el formulario de notificación.
o 10: El paciente no sabe si pertenece o no a algún pueblo originario, o a
qué pueblo originario pertenece.
o 11: El paciente pertenece a un pueblo originario que no está incluido
en la lista de codificaciones. En este caso debe registrarse en el
formulario el pueblo originario al que pertenece, a continuación de la
frase “Otro pueblo originario declarado:”
o 12: El paciente no responde.
o 13: No es posible preguntar el dato. Esto puede ocurrir tanto porque el
paciente no está presente al momento de efectuar el reporte como por
otras circunstancias.
d) Descripción de la Reacción Adversa
• Fecha de Inicio de RAM: Es muy importante para la evaluación de
causalidad. Si no tiene la fecha exacta, es útil informar mes y año, o una
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 5 de 9
referencia cronológica que permita claridad entre la toma del medicamento y
la aparición de la RAM.
• Duración de la RAM: Señalar el tiempo de duración del efecto observado,
seleccionado la unidad de tiempo respectivo (minutos, horas, etc). En caso no
entregar información de la fecha exacta de ocurrencia, responder la pregunta
¿La RAM ocurrió después de la administración del medicamento sospechoso?
Esto, con la finalidad de conocer la temporalidad asociada.
• Descripción de la reacción adversa: Indique el evento que sospecha
provocado por el medicamento, usando el término que describa de mejor
forma el conjunto de síntomas del paciente. Luego, detalle los signos y
síntomas (definir en el punto 3 cada uno). que considere forman parte de
ese evento. Entregue de forma resumida toda la información clínica relevante.
Si piensa que hay más de un evento, descríbalos separadamente, en la misma
notificación.
e) Fármaco(s)
• Rol del medicamento: Señale si, además del o los medicamentos
sospechosos, el paciente recibió medicamentos concomitantes, seleccionado la
casilla correspondiente (sí, no, desconocido). Luego, en las primeras dos
columnas de la tabla, marque la casilla bajo la S si el medicamento a ingresar
es un Fármaco Sospechoso o bajo la C si es un Fármaco Concomitante. Todo
reporte debe llevar al menos un fármaco marcado como sospechoso. Todo
fármaco debe llevar marcada una, y solo una, de las dos columnas.
• Informe el fármaco sospechoso: Informe el nombre del fármaco
sospechoso con su nombre genérico, luego identifique el nombre comercial®
o, si es genérico, el laboratorio; señalar el número de serie o lote si es
posible. Si el fármaco sospechoso es un producto biológico, el número de serie
o lote es esencial.
• Dosis, vía de administración y frecuencia: Señale la dosis administrada, la
unidad de medida, vía de administración y la frecuencia de uso. Ejemplos: 500
mg 3 veces al día, vía oral; 10 mg diarios en infusión IV; 1 aplicación cada 12
horas, vía tópica.
• Fechas de inicio y término de fármaco: Señalar en qué fecha comenzó la
administración del fármaco sospechoso y la fecha en que éste se suspendió. Si
el fármaco continúa siendo administrado, se debe especificar en el apartado
correspondiente a Fecha de Término con el término CONT.
• Motivo de prescripción: Señale la enfermedad o molestia del paciente por la
cual fue prescrito el medicamento. Entre los medicamentos concomitantes, se
debe considerar todos los otros fármacos (incluyendo analgésicos, vitaminas,
"productos naturales" y hierbas) recetados o automedicados que el paciente
esté consumiendo, con sus respectivas dosis, vía de administración, razón de
uso y fecha de inicio y término del tratamiento. Si desconoce alguno de estos
datos, indíquelo.
f) Tratamiento de la RAM
Señale las medidas adoptadas frente al evento adverso (por ej. suspensión del
tratamiento, ajuste de dosis, administración de un medicamento o un antídoto
específico, etc.)
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 6 de 9
g) Resultado de la RAM
Señale cuál fue el resultado final conocido de la RAM al momento de la notificación,
en el casillero correspondiente. Se debe marcar “recuperado” si está total o
parcialmente recuperado. Marque “no recuperado” si no hay indicios de mejoría. En
caso que el paciente haya fallecido, señale, si se ha determinado, la causa de
muerte, y la fecha, si se dispone de ella.
h) Suspensión/Re administración
Indique si el fármaco fue suspendido después de la aparición de la RAM, haya sido a
causa de ella o no. Luego, señale si la RAM desapareció o disminuyó en intensidad
luego de suspender o reducir la dosis del fármaco sospechoso. En caso que el
fármaco se haya suspendido, indicar si éste fue readministrado o no y, en tal caso, si
hubo reaparición de la RAM posterior a la readministración del medicamento. Procure
que exista coherencia entre las respuestas a las preguntas.
i) Consecuencia
Indique, en el casillero correspondiente, qué consecuencia hubo para el paciente, a
causa de la reacción adversa. Informe si a causa de la RAM el paciente fue
hospitalizado, o si ésta prolongó su estadía hospitalaria, o si puso en peligro
inminente su vida (hubo que intervenir para salvarle la vida) o si le produjo una
secuela incapacitante, la cual se debe describir. Esta información permite evaluar la
seriedad del evento.
j) Comentarios
Señale cualquier antecedente clínico relevante que no le haya sido preguntado, como
la patología de base u otras enfermedades, alergias previas, exposición previa a los
medicamentos, datos de análisis de laboratorio, exposición a otros elementos como
cosméticos, contaminantes, alimentos, etc. En este apartado puede complementar el
caso y detallar el resultado de la suspensión y/o readministración del fármaco. Si
necesita más espacio, puede agregar hoja anexa. Es importante que entregue
cualquier información que a su juicio ayude al evaluador a entender mejor el caso.
k) Datos del Informante
El notificador se debe identificar, informando su profesión, el establecimiento en el
que tuvo lugar la RAM o su toma de conocimiento, teléfono, FAX y correo electrónico
de contacto. Registre la fecha de reporte.
Nota: Se debe tener presente que la identidad del informante se considera
confidencial.
5.3 Recolección de Información y Notificación al ISP por QF. Encargado de
FV HRLBO
El Farmacéutico encargado una vez cuente con las notificaciones en el correo
electrónico, debe revisar que el formulario este correctamente llenado, de lo
contrario, se comunicará con el profesional notificador para completar el dato
faltante.
Una vez validada toda la información, notificará al Centro Nacional de FV mediante la
plataforma online RED-RAM http://sistemared-
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 7 de 9
ram.ispch.gob.cl/farmacovigilancia/Login.aspx en el plazo que dicta la norma
vigente; 72 horas para las graves y 30 días para las no graves, desde que se toma
conocimiento del RAM. Posteriormente el Centro Nacional de FV evaluará causalidad
de la reacción.
Toda la información recibida mediante correo electrónico se ingresa a una base de
datos con el objetivo de consolidar y tener trazabilidad de la información.
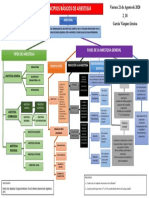
Flujograma de Notificación de Sospecha de RAM
6. REGISTROS
Identificación Almacenamiento Protección Recuperación Retención Disposición
Notificación Unidad de QF Encargado FV Por fecha 5 años Después
de Sospecha Farmacia de 5 años
de RAM se elimina
Base de Unidad de QF Encargado FV Por fecha 5 años Después
Datos FV Farmacia de 5 años
7. INDICADORES
Revisar Ficha Indicador Clínico “Porcentaje de Notificaciones de Sospecha de RAM
enviadas oportunamente a ISP según protocolo”.
8. REFERENCIAS.
• Norma General Técnica N°140 sobre Sistema Nacional de Farmacovigilancia de
Productos Farmacéuticos de Uso Humano, aprobada por Resolución Nº381 del 20 de
junio de 2012.
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 8 de 9
• D.S. Nº 3/2010 que aprueba Reglamento del Sistema Nacional de Control de los
Productos Farmacéuticos de Uso Humano.
• Instructivo para la notificación de Sospechas de reacciones adversas A medicamentos.
5ta Edición. ANAMED. Santiago de Chile, febrero 2015.
• https://www.cancer.gov/espanol/publicaciones/diccionarios/diccionario-cancer/
9. REVISIÓN Y CONTROL DE CAMBIOS.
Fecha Tipo Aprobación
06 de septiembre 2021 Se libera para su uso Director (S) HRLBO
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
Código: SGC-PR-NRAM/APF 1.5.3
Fecha: 06 septiembre 2021
PROTOCOLO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIONES ADVERSAS A Versión: 0
MEDICAMENTOS (RAM) EN HRLBO
Vigencia: 06 septiembre 2026
Página: 9 de 9
10. ANEXOS
ANEXO N° 1: Formulario Notificación de Sospecha de RAM en HRLBO.
FORMULARIO DE NOTIFICACIÓN DE
SOSPECHA DE REACCIÓN ADVERSA A MEDICAMENTOS (RAM)
REGLAS DE NOTIFICACIÓN
▪ El presente archivo es una adaptación de formulario de Farmacovigilancia-ISP y es propiedad del Departamento de Calidad e IAAS HRLBO
▪ La identidad del paciente y del informante es información confidencial
▪ Incorporar fechas en formato dd/mm/aaaa
▪ El formulario será enviado por la unidad afectada a la siguiente dirección de correo electrónica: farmacovigilancia.hrlbo@gmail.com
¡POR FAVOR LLENE TODAS LAS CASILLAS EN AMARILLO QUE CONTIENEN # (Código)!
REPORTE (#) TIPO REPORTE (#) FECHA REPORTE
UNIDAD O SERVICIO CLINICO (#)
DATOS DEL PACIENTE
Nombres y Apellidos (Texto Libre) Ficha Clínica (Número) RUN (Número)
Sexo (#) Peso/Kg. (Número) Talla/cm. (Número)
Edad (Número) Grupo etario (#)
Declara Pueblo Originario (#)
En caso de otro pueblo originario ¿Cuál?
DESCRIPCIÓN DE LA REACCIÓN ADVERSA
Fecha inicio RAM (dd/mm/aaaa) Duración (N°) Tiempo (#)
La RAM ocurrió después de la admnistración del Farmaco Sospechoso (#)
Descripción de la Reacción Adversa (Texto Libre)
DATOS DEL FARMACO
Recibió Fármaco Concomitante (#) S: Fármaco Sospechoso C:Fármaco Concomitante
Fármaco (S) Texto Libre
SoC Fármaco Marca Lote Dosis Frecuencia Vía de Fecha Fecha Motivo de la Prescripción
adm. Inicio Término
TRATAMIENTO DE LA RAM
Paciente recibio tratamiento especifico para la RAM (incluyendo suspensión de farmacos o ajustes de dosis) (#)
Describa (Texto Libre)
Resultado de la RAM (#) En caso de muerte Fecha
Causa de muerte (Texto Libre)
¿Se suspendió el fármaco sospechoso luego de la aparición de la RAM? (#)
¿Tras disminuir o suspender el fármaco sospechoso disminuyó o desapareció la RAM? (#)
¿Se readministró el fármaco sospechoso luego de suspenderlo? (#)
¿Reapareció o se intensificó la RAM luego de la readministración del fármaco sospechoso? (#)
CONSECUENCIA DE LA RAM EN EL PACIENTE
Debido a la RAM el paciente:
¿Requirio hospitalización? ¿Prolongo hospitalización? Señale días (N°)
¿Puso en peligro su vida? Secuela (#) Describa secuela
COMENTARIOS (Ej. Antecedentes Clínicos Relevantes, Patología de Base, Alergias, Exposición Previa al Fármaco y Evolución )
Describa (Texto Libre)
DATOS INFORMANTE
Nombre profesional Profesión
¡MUCHAS GRACIAS POR SU COMPROMISO!
Protocolo de Notificación de Sospecha de Reacciones Adversas a Medicamentos (RAM) en HRLBO
Departamento de Calidad e IAAS - HRLBO
También podría gustarte
- Ciencia regulatoria: Medicamentos bio y su relevancia para la saludDe EverandCiencia regulatoria: Medicamentos bio y su relevancia para la saludAún no hay calificaciones
- Farmacovigilancia Programas ESNDocumento30 páginasFarmacovigilancia Programas ESNLizzyta AyastaAún no hay calificaciones
- Sistemas de Notificacion en FarmacovigilanciaDocumento45 páginasSistemas de Notificacion en FarmacovigilanciaKamy Blas0% (1)
- Programa de Farmaco VigilanciaDocumento10 páginasPrograma de Farmaco VigilanciaYese MosqueraAún no hay calificaciones
- Tarea 2 (19-01-24)Documento5 páginasTarea 2 (19-01-24)Norma LuzAún no hay calificaciones
- Farmacovigilancia Eq.9Documento20 páginasFarmacovigilancia Eq.9Daniela Miranda0% (1)
- Presentacion Definiciones Generales de FarmacovigilanciaDocumento11 páginasPresentacion Definiciones Generales de FarmacovigilanciaPaul Sandoval OlayaAún no hay calificaciones
- Generalidades de FarmacovigilanciaDocumento61 páginasGeneralidades de FarmacovigilanciaKarolina OñateAún no hay calificaciones
- Farmacovigilancia Programas ESNDocumento48 páginasFarmacovigilancia Programas ESNIsamar DiazAún no hay calificaciones
- 9.1 Gestión de Riesgos - FV y RAMDocumento20 páginas9.1 Gestión de Riesgos - FV y RAMFernando Villalba100% (2)
- Proyecto FarmacovigilanciaDocumento15 páginasProyecto FarmacovigilanciaCarlos A BarandaAún no hay calificaciones
- SF-PFT-01 Elaboración Del Reporte de FarmacovigilanciaDocumento6 páginasSF-PFT-01 Elaboración Del Reporte de FarmacovigilanciaSixto VIVERO CASSIANIAún no hay calificaciones
- Manual de Farmacovigilancia Ese Santa Gertrudis Modificado (Reparado)Documento10 páginasManual de Farmacovigilancia Ese Santa Gertrudis Modificado (Reparado)Sebiitas Lpz Porras LiveAún no hay calificaciones
- FARMACOVIGILANCIADocumento5 páginasFARMACOVIGILANCIAAida Oshin Jihuallanca MamaniAún no hay calificaciones
- Alerta SanitariaDocumento5 páginasAlerta SanitariaMauricio RodriguezAún no hay calificaciones
- Farmacovigilancia Programas ESNDocumento43 páginasFarmacovigilancia Programas ESNDiego Licetti ValenciaAún no hay calificaciones
- Guia de Causalidad UPSALA - INVIMADocumento1 páginaGuia de Causalidad UPSALA - INVIMASharon RinconAún no hay calificaciones
- Far Mac I Vigi LanciaDocumento6 páginasFar Mac I Vigi LanciaJuan Diego Uribe MuñozAún no hay calificaciones
- DGFDDocumento7 páginasDGFDherbert14Aún no hay calificaciones
- 4 Farmacia Hospitalaria Modulo Iv Farmacovigilancia G1Documento28 páginas4 Farmacia Hospitalaria Modulo Iv Farmacovigilancia G1Alejandra Cadenas0% (1)
- Programa FarmacovigilanciaDocumento16 páginasPrograma FarmacovigilanciaVicky SalazarAún no hay calificaciones
- Farmacovigilancia CorregidoDocumento48 páginasFarmacovigilancia CorregidoLaura Daniela Medina Reyes0% (1)
- Microsoft PowerPoint - FARMACOVIGILANCIA SEMANA 2Documento26 páginasMicrosoft PowerPoint - FARMACOVIGILANCIA SEMANA 2JLuis GarciaAún no hay calificaciones
- Actividad 2 Farmacovigilancia LinaDocumento12 páginasActividad 2 Farmacovigilancia Linaluis carlos agudelo alzateAún no hay calificaciones
- Ivc-Vig-In009 Instructivo Gestin de Reportes de Eventos Asociados Al Uso de MedicamentosDocumento5 páginasIvc-Vig-In009 Instructivo Gestin de Reportes de Eventos Asociados Al Uso de MedicamentosQ.F. Rocio Velàsquez MAún no hay calificaciones
- Protocolo Reacción Adversa A MedicamentosDocumento3 páginasProtocolo Reacción Adversa A MedicamentosTomas ToledoAún no hay calificaciones
- Buenas Prácticas de FarmacovigilanciaDocumento133 páginasBuenas Prácticas de Farmacovigilanciakajedafe100% (1)
- PNO 001 Notificación de RAMDocumento6 páginasPNO 001 Notificación de RAMJean AntoineAún no hay calificaciones
- Encuesta FV 2021Documento5 páginasEncuesta FV 2021Alfredo TrejoAún no hay calificaciones
- Practico N 2 de Farmacovigilancia DefinitDocumento6 páginasPractico N 2 de Farmacovigilancia Definitbelen3roenfermeriaAún no hay calificaciones
- Grupo2 Subgrupo3 Seminario 7Documento31 páginasGrupo2 Subgrupo3 Seminario 7RUTH GABRIELA BENAVIDEZ CARBAJALAún no hay calificaciones
- Formación: ContinuadaDocumento5 páginasFormación: Continuadanicoll diazAún no hay calificaciones
- FARMACOVIGILANCIA - Clase 23 NovDocumento9 páginasFARMACOVIGILANCIA - Clase 23 NovNurii TacoAún no hay calificaciones
- Norma InvimaDocumento9 páginasNorma InvimaJuan LoperaAún no hay calificaciones
- Manual de Buenas Prácticas de FarmacovigilanciaDocumento43 páginasManual de Buenas Prácticas de FarmacovigilanciaMiracoli BaViAún no hay calificaciones
- Programa de FarmacovigilanciaDocumento9 páginasPrograma de FarmacovigilanciaLuis Carlos Buena VidalAún no hay calificaciones
- Estudios y FarmacovigilanciaDocumento75 páginasEstudios y FarmacovigilanciaJean Pierre Cano MolinaAún no hay calificaciones
- Pno NotificacionDocumento7 páginasPno NotificacionSajimars SajimarAún no hay calificaciones
- Guía N°6 FarmacologíaDocumento6 páginasGuía N°6 FarmacologíaFranco SotoAún no hay calificaciones
- Analisis BD RAMDocumento31 páginasAnalisis BD RAMDiego Licetti ValenciaAún no hay calificaciones
- FarmacovigilanciaDocumento7 páginasFarmacovigilanciastephanieAún no hay calificaciones
- Documento de Apoyo - Clasificación de RamsDocumento10 páginasDocumento de Apoyo - Clasificación de RamsBeatriz OsAún no hay calificaciones
- 1 Farmacovigilancia en Establecimientos de Atención MédicaDocumento51 páginas1 Farmacovigilancia en Establecimientos de Atención MédicaKHANDI IBARRA0% (1)
- Farmacovigilancia NoviembreDocumento6 páginasFarmacovigilancia NoviembreJulieth BarahonaAún no hay calificaciones
- SF-PFT-02 Elaboración Del Reporte de TecnovigilanciaDocumento6 páginasSF-PFT-02 Elaboración Del Reporte de TecnovigilanciaSixto VIVERO CASSIANIAún no hay calificaciones
- Protocolo Lasa-2 - VFDocumento13 páginasProtocolo Lasa-2 - VFDianita Patricia Bohorquez RoseroAún no hay calificaciones
- DianaCarrilloUnidad 1 Tarea 2 Contextualizacion - PreguntasDocumento8 páginasDianaCarrilloUnidad 1 Tarea 2 Contextualizacion - PreguntasJorge RibonAún no hay calificaciones
- Tarea 2 Contextualización IndividualDocumento7 páginasTarea 2 Contextualización IndividualJuan Diego Uribe MuñozAún no hay calificaciones
- Unidad 1 Tarea 2 Contextualización ResumenDocumento13 páginasUnidad 1 Tarea 2 Contextualización ResumeneduinsonAún no hay calificaciones
- Ass Rsa Gu042Documento13 páginasAss Rsa Gu042Edinson Javier Cuello CastroAún no hay calificaciones
- Sistema - Peruano - de - Farmacovigilancia (Modo de Compatibilidad) (Reparado)Documento39 páginasSistema - Peruano - de - Farmacovigilancia (Modo de Compatibilidad) (Reparado)Eve TaypeAún no hay calificaciones
- 4 Metodos de FarmacovigilanciaDocumento51 páginas4 Metodos de FarmacovigilanciaDavis MeraAún no hay calificaciones
- ContextualizaciònDocumento12 páginasContextualizaciònadolfo diazAún no hay calificaciones
- Taller de Farmacovigilancia 2015Documento4 páginasTaller de Farmacovigilancia 2015Edith Ramírez menAún no hay calificaciones
- Norma Oficial FarmacovigilanciaDocumento57 páginasNorma Oficial FarmacovigilanciatiavmexAún no hay calificaciones
- Sistema Peruano de FarmacovigilanciaDocumento39 páginasSistema Peruano de FarmacovigilanciapylytlAún no hay calificaciones
- 2021 Preguntas Frecuentes FarmacovigilanciaDocumento3 páginas2021 Preguntas Frecuentes Farmacovigilanciaacpomier-esAún no hay calificaciones
- 08 1058875pjzczfsnqaDocumento22 páginas08 1058875pjzczfsnqaJavier Alexander Ito ApazaAún no hay calificaciones
- Far Maco Vigi LanciaDocumento13 páginasFar Maco Vigi LanciaJonathan Ricardo Serrano GaleanoAún no hay calificaciones
- Señales en Farmacovigilancia RedPARFDocumento56 páginasSeñales en Farmacovigilancia RedPARFNicolas Mateo Gonzalez LopezAún no hay calificaciones
- APF Proc. Manejo Med. Controlados en HRLBO V1-2018Documento22 páginasAPF Proc. Manejo Med. Controlados en HRLBO V1-2018karinaAún no hay calificaciones
- APF 1.4.1 Procedimientos de Farmacia HRLBO V1-2018Documento21 páginasAPF 1.4.1 Procedimientos de Farmacia HRLBO V1-2018karinaAún no hay calificaciones
- APDs 1.1.3 Reacciones Adv e Incidentes V3 2022Documento16 páginasAPDs 1.1.3 Reacciones Adv e Incidentes V3 2022karinaAún no hay calificaciones
- APA 1.4 Manual de Bioseguridad V3 2019Documento10 páginasAPA 1.4 Manual de Bioseguridad V3 2019karinaAún no hay calificaciones
- 2022 EducadiccionesDocumento136 páginas2022 EducadiccioneskarinaAún no hay calificaciones
- Administracion de Medicamentos - 2Documento17 páginasAdministracion de Medicamentos - 2karinaAún no hay calificaciones
- Exposicion Ansioliticos e HipnoticosDocumento33 páginasExposicion Ansioliticos e HipnoticosDANIELA BARRIOS CAMARGO ESTUDIANTEAún no hay calificaciones
- Actividades Farmacología PDFDocumento3 páginasActividades Farmacología PDFJoshua le GodinieAún no hay calificaciones
- Farmacos DosisDocumento12 páginasFarmacos DosisEnzo Claudio Leandro Soto RojasAún no hay calificaciones
- Kardex Enfermeria SamuDocumento31 páginasKardex Enfermeria SamuAnonymous x0P332K5uuAún no hay calificaciones
- Fibrilacion AuricularDocumento23 páginasFibrilacion AuricularDavid Santiago Jaramillo ZapataAún no hay calificaciones
- "Ensayo" Legalización de La MarihuanaDocumento9 páginas"Ensayo" Legalización de La MarihuanaGabriel Martínez100% (1)
- Farmacología Antimicotica - Modulos de FarmaciaDocumento15 páginasFarmacología Antimicotica - Modulos de FarmaciaMiguel Machaca Flores (QuimioFarma)Aún no hay calificaciones
- Vías de Administración y FF 2020Documento48 páginasVías de Administración y FF 2020Katerine RiquelmeAún no hay calificaciones
- Indica Brevemente La Utilidad Clínica de Los Barbitúricos EmpleadosDocumento2 páginasIndica Brevemente La Utilidad Clínica de Los Barbitúricos EmpleadosQuique De La LuzAún no hay calificaciones
- Captura de Pantalla 2023-07-15 A La(s) 10.41.21 P.M.Documento1 páginaCaptura de Pantalla 2023-07-15 A La(s) 10.41.21 P.M.diegolazarochinoAún no hay calificaciones
- ToziDocumento1 páginaToziLetty LuAún no hay calificaciones
- Tarea5 Propuesta de Modelo de TablaDocumento3 páginasTarea5 Propuesta de Modelo de Tablakendy paola soto gilAún no hay calificaciones
- Lista de Precio Drogueria Vitalclinic 02-08-2023Documento45 páginasLista de Precio Drogueria Vitalclinic 02-08-2023farmacia puertoordazAún no hay calificaciones
- Clasificación de FármacosDocumento8 páginasClasificación de FármacosKaaren NooveloAún no hay calificaciones
- NeurotransmisoresDocumento11 páginasNeurotransmisoresAnonymous BLioPV5fSuAún no hay calificaciones
- Passurta FolletoDocumento25 páginasPassurta FolletoJosefinaHerrerosAún no hay calificaciones
- Farmacos Antiparasitarios 2018Documento7 páginasFarmacos Antiparasitarios 2018Luz Guevara CastilloAún no hay calificaciones
- Anestesicos Auxiliares Expo FiiDocumento16 páginasAnestesicos Auxiliares Expo FiiMijaelCaceresAún no hay calificaciones
- Aripiprazol FichaDocumento4 páginasAripiprazol FichaallhasreadAún no hay calificaciones
- Ivc Vig FM026Documento2 páginasIvc Vig FM026Leidy Alexandra Castillo HolguínAún no hay calificaciones
- VancomicinaDocumento23 páginasVancomicinaMaria Jose Gonzalez OsmaAún no hay calificaciones
- MelatoninaDocumento6 páginasMelatoninaMoisesAún no hay calificaciones
- Catálogo General de Medicamentos 2017Documento26 páginasCatálogo General de Medicamentos 2017Abdiel ValenciaAún no hay calificaciones
- Las Drogas en La SociedadDocumento2 páginasLas Drogas en La SociedadEver Eliú Ruíz ArchilaAún no hay calificaciones
- EpleronaDocumento6 páginasEpleronaRoberto Lugo GuadarramaAún no hay calificaciones
- Preguntas para El ExamenDocumento12 páginasPreguntas para El ExamenVera Nevarez Alejandro XavierAún no hay calificaciones
- AMORDocumento9 páginasAMORLaura OrosteguiAún no hay calificaciones
- Farmacocinetica PDFDocumento9 páginasFarmacocinetica PDFJcflow FlowAún no hay calificaciones
- Principios Basicos de AnestesiaDocumento1 páginaPrincipios Basicos de AnestesiaJessica DowneyAún no hay calificaciones
- Nociones Fundamentales Sobre Sutancias NocivasDocumento7 páginasNociones Fundamentales Sobre Sutancias NocivasCarlos HenriquezAún no hay calificaciones