Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Taller 2 Cinética Química
Cargado por
Vicky RuDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Taller 2 Cinética Química
Cargado por
Vicky RuCopyright:
Formatos disponibles
FACULTAD DE INGENIERÍA QUÍMICA Y
AGROINDUSTRIAL TALLER II – CINÉTICA
QUÍMICA
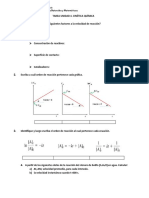
1.
El NO2 (g) se descompone en NO y O2 a 383°C, obteniéndose los datos presentados en la tabla 1. Determinar el orden de la
reacción respecto a la concentración del NO2 y calcule la constante de rapidez.
Concentración vs tiempo ln vs tiempo
[NO2] (M) ln(NO2)
0.15 0
0 5 10 15 20 25
0.1 -1
NO2
0.05 -2
-3
0
0 5 10 15 20 25 -4
Tiempo -5
-6
1/[NO2]
1/NO2
250
200
150
1/NO2
100
50
0
0 5 10 15 20 25
Tiempo
Por tanto, la reacción es de segundo orden.
M= 0,0170-0,1000/5-0 = -0.0166
Por la ecuación de segundo orden K= -0.0166
2.
Se conocen las constantes de velocidad a distintas temperaturas para la reacción de primer orden A → B (tabla 2).
Determinar gráficamente la energía de activación para la reacción anterior.
Tabla 1: Tabla 2:
Tiempo (s) [NO2] (M)
0 0,1000 K (s-1) T (°C)
5 0,0170 10,6 10
10 0,0090 47,4 20
15 0,0062 162 30
20 0,0047 577 40
Ea
m=−( )
R
-0.0166 k=-(Ea/8,314x10^-3 kj/k mol)
Ea = 1.38 kj/mol
T (K)
283,15
293,15
303,15
313,15
Ln k
7
6
5
4
Ln (k)
3
2
1
0
0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.1 0.11
1/T
3.
a) Calcular el tiempo de vida media para la descomposición del pentóxido de dinitrógeno a 70°C (Rx de primer orden), si la
constante de velocidad a dicha temperatura es 6,8x10-3 s-1, y si en el inicio de la reacción se tenían 0,3 moles de N 2O5 en
un recipiente de 0,5 lts. b) Calcular cuántas moles de N2O5 quedarán después de 3 minutos? c) Qué tiempo se necesita
para que la cantidad del reactivo se reduzca a 0,03 moles de N2O5.
a) K= 6,8x10-3 s-1
0,3 moles de N2O5 en un recipiente de 0,5 lts.
T1/2= ln 2/k
= ln 2 /6,8x10-3s^-1
= 0.0001 s
b)
ln [A]= -K t + ln [A]
In [A] = - 6,8x10-3 s-1 180 s + ln [A]
[A]=
4.
La constante de velocidad para la descomposición de la molécula XY a 30°C es 6x10 -2s-1. Calcular la constante de velocidad
a 120°C si la energía de activación es 50 KJ/mol.
Ea = 50 KJ/mol
K= 0.06 s^-1
También podría gustarte
- Cinética Yodinación de La AcetonaDocumento2 páginasCinética Yodinación de La AcetonaJosé Alejandro Valencia Alcalde100% (1)
- Ejercicios Guia 4Documento13 páginasEjercicios Guia 4DORIELYS DAYANA LOPEZ CASTRILLOAún no hay calificaciones
- Oxidación Del Ion IoduroDocumento12 páginasOxidación Del Ion IoduroIsita AlvarezAún no hay calificaciones
- Tarea 4, Cinetica QG FinalDocumento14 páginasTarea 4, Cinetica QG FinalDaisy FuentesAún no hay calificaciones
- Cuestionario 7Documento4 páginasCuestionario 7Eduardo SalinasAún no hay calificaciones
- Cinética de Reducción Del Ion PermanganatoDocumento6 páginasCinética de Reducción Del Ion PermanganatoCarlos MadridAún no hay calificaciones
- Fisicoquimica GustavoDocumento5 páginasFisicoquimica GustavoDiego MuñozAún no hay calificaciones
- Laboratorio #1 - CineticaDocumento16 páginasLaboratorio #1 - CineticaPaul Vicente Candia TorresAún no hay calificaciones
- Efecto de La Temperatura Sobre La Rapidez de La Reacción.....Documento9 páginasEfecto de La Temperatura Sobre La Rapidez de La Reacción.....saul corona100% (1)
- Grupo 6Documento39 páginasGrupo 6Marcos SamaniegoAún no hay calificaciones
- Pauta Solemne 2 Quim200 201620Documento5 páginasPauta Solemne 2 Quim200 201620daniela estefiAún no hay calificaciones
- Cinética de Oxidación de Etanol Con Cromo.....Documento2 páginasCinética de Oxidación de Etanol Con Cromo.....Valentina SaenzAún no hay calificaciones
- Práctica CalificadacineticaDocumento2 páginasPráctica CalificadacineticaLuis APAún no hay calificaciones
- Tercer Tutorial - Grupo 5Documento12 páginasTercer Tutorial - Grupo 5Amed Enrique Ortega MonteroAún no hay calificaciones
- Quiz 3 - 2023-1Documento3 páginasQuiz 3 - 2023-1Angela Lorena DíazAún no hay calificaciones
- Coef Vol. GlobalDocumento11 páginasCoef Vol. Globalpaul vasquezAún no hay calificaciones
- S02.s1 - Ejercicios Resueltos PDFDocumento11 páginasS02.s1 - Ejercicios Resueltos PDFAngel100% (1)
- Cinetica Practica 2Documento12 páginasCinetica Practica 2Kristel ThomasAún no hay calificaciones
- Tarea Previa Al Examen DepartamentalDocumento8 páginasTarea Previa Al Examen DepartamentalGameplays Of Games PcAún no hay calificaciones
- Resolución Ej. 3 CinéticaDocumento3 páginasResolución Ej. 3 CinéticaSimon AbadovskyAún no hay calificaciones
- Informe Ley de VelocidadDocumento3 páginasInforme Ley de VelocidadJossi JmAún no hay calificaciones
- Informe de Determinacion de Ley de VelocDocumento11 páginasInforme de Determinacion de Ley de VelocAntonio Zapata SolisAún no hay calificaciones
- Problemas Resueltos-1Documento14 páginasProblemas Resueltos-1lucas juanAún no hay calificaciones
- Cinética de La Descomponían Del Tiosulfato de SodioDocumento8 páginasCinética de La Descomponían Del Tiosulfato de Sodiodaniel pardo100% (2)
- PeroxodisulfatoDocumento9 páginasPeroxodisulfatoplazadelizana100% (2)
- Cinética de Reducción Del Ion PermanganatoDocumento7 páginasCinética de Reducción Del Ion PermanganatoJulieth BarriosAún no hay calificaciones
- Practica CinèticaDocumento4 páginasPractica CinèticaNicolás GómezAún no hay calificaciones
- Practica de Laboratorio Efecto Iónico Velocidad de ReaccionDocumento10 páginasPractica de Laboratorio Efecto Iónico Velocidad de Reaccionivan estevesAún no hay calificaciones
- Discusion 10Documento4 páginasDiscusion 10Elmer CardonaAún no hay calificaciones
- Reporte 13 CineticaDocumento18 páginasReporte 13 CineticaAlejandro MartínezAún no hay calificaciones
- Wa0000Documento6 páginasWa0000diani perez perezAún no hay calificaciones
- T4-10 Avalo O n1 FINALDocumento7 páginasT4-10 Avalo O n1 FINALChicha's HomeAún no hay calificaciones
- Tarea Cinética Química AaDocumento4 páginasTarea Cinética Química Aagustavo valdiviesoAún no hay calificaciones
- Parciales CineticaDocumento19 páginasParciales CineticaJocelyn BernabeAún no hay calificaciones
- Ope III Teoria 343-352Documento4 páginasOpe III Teoria 343-352Alex PereiraAún no hay calificaciones
- 2019-I Taller Cinética QuímicaDocumento4 páginas2019-I Taller Cinética Químicacarlos cuervoAún no hay calificaciones
- Informe Practica N°2 Fisico QuimicaDocumento12 páginasInforme Practica N°2 Fisico QuimicaChristian RodríguezAún no hay calificaciones
- Laboratorio 02 - Simulador de Cinetica QuimicaDocumento5 páginasLaboratorio 02 - Simulador de Cinetica QuimicaOlger Aragon BerlangaAún no hay calificaciones
- Informe 5 de CinéticaDocumento5 páginasInforme 5 de CinéticaBrenda MichelAún no hay calificaciones
- Reporte 2. CInética de Saponificación Del Acetato de EtiloDocumento14 páginasReporte 2. CInética de Saponificación Del Acetato de EtiloLuis Ocampo ElizaldeAún no hay calificaciones
- Seminario IIIDocumento4 páginasSeminario IIIFrank Huarhua CarrascoAún no hay calificaciones
- Seminario IIIDocumento4 páginasSeminario IIIFrank Huarhua CarrascoAún no hay calificaciones
- Cálculos y Resultados (Cinetica Quimica)Documento6 páginasCálculos y Resultados (Cinetica Quimica)Daniel Marcelo VelasquezAún no hay calificaciones
- Examen Final de Fisico QumicaDocumento4 páginasExamen Final de Fisico QumicaFERNANDO ESCAJADILLO CHARCAAún no hay calificaciones
- Examen Final-Fq-2004-IDocumento4 páginasExamen Final-Fq-2004-IwefweFWEfAún no hay calificaciones
- Informe Lab 3 Cinética Química Reloj de IodoDocumento9 páginasInforme Lab 3 Cinética Química Reloj de IodoValesska SánchezAún no hay calificaciones
- Informe Práctica N°7Documento10 páginasInforme Práctica N°7Darian PintoAún no hay calificaciones
- Examen ResueltoDocumento3 páginasExamen ResueltoYordy QuecañoAún no hay calificaciones
- Q5 PAU Equilibrio SolucDocumento62 páginasQ5 PAU Equilibrio SolucPablo LedesmaAún no hay calificaciones
- Tarea ReaccionesDocumento6 páginasTarea ReaccionesNaysha LicuonaAún no hay calificaciones
- Ejercicios 9.1-9.2-9.4Documento5 páginasEjercicios 9.1-9.2-9.4Pedro Luis ManchayAún no hay calificaciones
- Repaso PC3Documento4 páginasRepaso PC3BC NandoAún no hay calificaciones
- Cinetica Quimica 2Documento6 páginasCinetica Quimica 2jaionelibAún no hay calificaciones
- Informe Guion 2, LIQ IVDocumento7 páginasInforme Guion 2, LIQ IVbernardo beneitez benetAún no hay calificaciones
- 01 Primera Evaluación Tuni Huanca FernandoDocumento5 páginas01 Primera Evaluación Tuni Huanca Fernandofrancisco rodriguezAún no hay calificaciones
- Informe - Lab - Practica #3Documento6 páginasInforme - Lab - Practica #3jkmikaAún no hay calificaciones
- Ejercicios Reactores (2 Parcial)Documento5 páginasEjercicios Reactores (2 Parcial)Rolando Torrez locoAún no hay calificaciones
- Reporte Práctica 1. Equilibrio QuímicoDocumento8 páginasReporte Práctica 1. Equilibrio QuímicoAmérica González SaucedoAún no hay calificaciones
- Ejercicios de Química General - Cinética Química SIN RESOLUCIÓNDocumento7 páginasEjercicios de Química General - Cinética Química SIN RESOLUCIÓNAleAún no hay calificaciones
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Anexo 1 Especificaciones Tecnicas Im30-1239 Sellos y Bombas FlowserveDocumento24 páginasAnexo 1 Especificaciones Tecnicas Im30-1239 Sellos y Bombas FlowserveCristian Jhair PerezAún no hay calificaciones
- Losa Maciza 1Documento15 páginasLosa Maciza 1Alvaro MalcaAún no hay calificaciones
- Calculo Radiacion TermicaDocumento7 páginasCalculo Radiacion TermicaAngel CuyaAún no hay calificaciones
- Curso JavascriptDocumento28 páginasCurso JavascriptDavid CrAún no hay calificaciones
- Ser Omni 4Documento8 páginasSer Omni 4roblestolentino100% (2)
- Trabajo MateDocumento8 páginasTrabajo MatemariaAún no hay calificaciones
- Memoria Descriptiva Puente UrasquiDocumento29 páginasMemoria Descriptiva Puente UrasquiJohan Erick Quiñones Hospina100% (1)
- MathcadDocumento13 páginasMathcadcarlosAún no hay calificaciones
- Ejemplo 4 Bus de Sensores Basado en RS485Documento9 páginasEjemplo 4 Bus de Sensores Basado en RS485José ÁlvarezAún no hay calificaciones
- Apuntes Propiedades Químicas Corrosión y OxidaciónDocumento23 páginasApuntes Propiedades Químicas Corrosión y OxidaciónSARAH VASQUEZ SHANKSAún no hay calificaciones
- El Teorema de PitágorasDocumento9 páginasEl Teorema de PitágorasNathaly LlanosAún no hay calificaciones
- 5ºct. Semana 29 Aprendo en Casa .2021Documento6 páginas5ºct. Semana 29 Aprendo en Casa .2021Adrian Del P. Palacios PercaAún no hay calificaciones
- Unidades HunterDocumento12 páginasUnidades HunterGalhy Vigo MEndezAún no hay calificaciones
- 03 Juegos Estáticos 1Documento28 páginas03 Juegos Estáticos 1Juan GarciaAún no hay calificaciones
- Hacer Facturas en VFP - CopquinDocumento15 páginasHacer Facturas en VFP - CopquinArmando LazarteAún no hay calificaciones
- Sesión 1, Introducción A RDocumento23 páginasSesión 1, Introducción A RJose Carlos Torres LopezAún no hay calificaciones
- Resolucion Problemas Calculo DiferencialDocumento17 páginasResolucion Problemas Calculo DiferencialAntonioGutiérrez100% (2)
- Examen de Entrada de Fisica IIDocumento3 páginasExamen de Entrada de Fisica IICristian Alarcón PolucoAún no hay calificaciones
- Actividad 1 Módulo 3-2Documento3 páginasActividad 1 Módulo 3-2Ricardo RamosAún no hay calificaciones
- 1239683662.matematica Abba - RomeroDocumento20 páginas1239683662.matematica Abba - RomeroMercedes Corpus MechatoAún no hay calificaciones
- Villanueva Pruneda PDFDocumento247 páginasVillanueva Pruneda PDFdamguirre64Aún no hay calificaciones
- Constantes NumericasDocumento1 páginaConstantes Numericasmarcuadrado5342Aún no hay calificaciones
- Experiencia de Aprendizaje NDocumento27 páginasExperiencia de Aprendizaje NPredrojesus BecerraAún no hay calificaciones
- Ficha Tecnica WV JettaDocumento4 páginasFicha Tecnica WV JettaFernando Londono100% (1)
- L14 Estructuras CondicionalesDocumento4 páginasL14 Estructuras CondicionalesLeslie Gabriela García FernándezAún no hay calificaciones
- Ejercicios Preparatorios Segundo Parcial - Parte 1 (Lewis, Geometria, Hibridacion y Polaridad)Documento3 páginasEjercicios Preparatorios Segundo Parcial - Parte 1 (Lewis, Geometria, Hibridacion y Polaridad)Emilio BlancoAún no hay calificaciones
- Tarea 8 Semana 8Documento14 páginasTarea 8 Semana 8Ingris IngrisitaAún no hay calificaciones
- Investigacion OperativaDocumento39 páginasInvestigacion Operativajeque66160% (5)
- Plantilla para Sustentar TesisDocumento11 páginasPlantilla para Sustentar TesisPablo HuarayaAún no hay calificaciones