Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Modelos Atómicos
Cargado por
EMMA MARGARITA TORRESTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Modelos Atómicos
Cargado por
EMMA MARGARITA TORRESCopyright:
Formatos disponibles
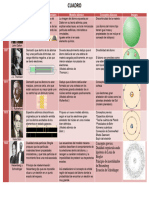
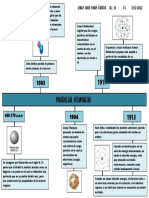
Evolución histórica de los modelos atómicos
Año que se Nombre del Nombre del Postulados sobre el modelo Representación del
propuso el modelo filósofo o modelo
modelo científico
500 años A.C. Atomista Demócrito y Todo lo que se percibe a
Leucipo través de los sentidos está
(filósofos formado por pequeñas
griegos partículas, macizas, con
diferentes formas y texturas
llamadas átomos.
1803/Se publica Teoría atómica John Dalton Materia formada por átomos
en 1908. de Dalton iguales entre sí, si son del
mismo elemento y diferentes
entre sí, si son de
diferentes elementos. No se
crean ni se destruyen, se
conservan. Las proporciones
de átomos se mantienen cuando
se forma un compuesto.
1891/1897 Existencia del George Se propone la existencia de
electrón Stoney/Joseph otras partículas con carga
Thomson elemental, el electrón,
posteriormente se comprueba
experimentalmente su
existencia (rayos catódicos).
1904 Modelo atómico Joseph Thomson El átomo está constituido por
budín de pasas una masa positiva y en ella
se encuentran incrustados los
electrones negativos, como
pasas en un budín, de manera
que resulta eléctricamente
neutro
1911 Modelo atómico Ernest El átomo tiene una zona
nuclear (modelo Rutherford central, llamada núcleo, con
planetario) carga positiva, muy pequeña y
maciza donde se concentra la
masa del átomo y una zona
mucho mayor y prácticamente
vacía que rodea al núcleo
llamada periferia en donde se
encuentran los electrones que
giran en órbitas alrededor
del núcleo.
1913 Modelo atómico Niels Bohr El átomo de hidrógeno está
de Bohr (para formado por un núcleo central
el átomo de constituido por un protón;
Hidrógeno) alrededor de él gira el
electrón en órbitas
circulares permitidas. El
electrón tiene valores
definidos de energía. A cada
órbita le corresponde un
número que se relaciona con
el valor de energía.
1924 Modelo de Erwin Los electrones se comportan
Schrödinger Schrödinger y su como ondas o partículas
grupo de dispuestos en orbitales de
investigadores energía en donde existe
cierta probabilidad de
encontrarlos. La energía de
estos está cuantizada y
aumenta a medida que se
incrementa el valor de n
siendo n=1 el nivel de menor
energía.
También podría gustarte
- Dinamicas JovenesDocumento60 páginasDinamicas JovenesAlejandro Palacios86% (7)
- Modelos AtomicosDocumento2 páginasModelos AtomicosDuyujoju Gor Agu86% (29)
- Requerimiento de AceroDocumento5 páginasRequerimiento de AceroEtnan Adbiel Huamani CondoriAún no hay calificaciones
- Evolución del microscopio en 40 pasosDocumento2 páginasEvolución del microscopio en 40 pasosIvett Ponce88% (8)
- Manual Basico Uso Del ExplosimetroDocumento2 páginasManual Basico Uso Del ExplosimetroMelissa Rivera Quispe40% (5)
- Modelacion de Un Tanque de CalentamientoDocumento12 páginasModelacion de Un Tanque de CalentamientoMauricio100% (1)
- Teoria AtomicaDocumento3 páginasTeoria AtomicaNeheyler MecatrónicoAún no hay calificaciones
- Modelos AtomicosDocumento1 páginaModelos AtomicosMonica Rodriguez Gonzalez100% (1)
- Manual de Mecanica Del Suelo Y CimentacionesDocumento119 páginasManual de Mecanica Del Suelo Y CimentacionesNaylaSb100% (5)
- Anexo No 2 Modelos AtómicosDocumento4 páginasAnexo No 2 Modelos AtómicosLuz Nelly Maya OrtizAún no hay calificaciones
- Evolución de los modelos atómicos desde Demócrito hasta SchrödingerDocumento2 páginasEvolución de los modelos atómicos desde Demócrito hasta SchrödingerWilfredo José VallejosAún no hay calificaciones
- Cuadro Comparativo de Los Modelos AtomicosDocumento1 páginaCuadro Comparativo de Los Modelos Atomicoslautarobre10Aún no hay calificaciones
- Tarea Evidencias de Estructura AtómicaDocumento5 páginasTarea Evidencias de Estructura Atómicaalanntorres09ctrlAún no hay calificaciones
- evolucion de los modelos atomicosDocumento8 páginasevolucion de los modelos atomicosIsrael GarAún no hay calificaciones
- Aporte Estructura MolecularDocumento3 páginasAporte Estructura MolecularMartha Echeverri TrochezAún no hay calificaciones
- Modelos AtómicosDocumento10 páginasModelos AtómicosCristian BravoAún no hay calificaciones
- Estructura Atomica II - QuimicaDocumento4 páginasEstructura Atomica II - QuimicaBrinny VelazcoAún no hay calificaciones
- El Átomo_ su historia y estructuraDocumento8 páginasEl Átomo_ su historia y estructuraEmilio RaschiaAún no hay calificaciones
- LMy TDocumento6 páginasLMy Tlu pnAún no hay calificaciones
- Modelos Atomicos2Documento1 páginaModelos Atomicos2hector sahil hernandez hernandezAún no hay calificaciones
- Modelos atómicos comparativosDocumento2 páginasModelos atómicos comparativosAndrea GonzalezAún no hay calificaciones
- Química PREDocumento4 páginasQuímica PREVictor Huerta RojasAún no hay calificaciones
- Modelos Atomicos 2Documento3 páginasModelos Atomicos 2Jhoe Henrriquez0% (1)
- Actividades Componente Químico. (Autoguardado)Documento14 páginasActividades Componente Químico. (Autoguardado)Maria Fernanda Prasca Ruiz0% (1)
- Presentacion Power Point Episodio 4 IIDocumento24 páginasPresentacion Power Point Episodio 4 IIMaría Eugenia García CarralAún no hay calificaciones
- Componentes Modelo BohrDocumento4 páginasComponentes Modelo Bohrjesus gomezAún no hay calificaciones
- Modelos atómicos clave en la historia de la físicaDocumento2 páginasModelos atómicos clave en la historia de la físicaRichard Qvispe CAún no hay calificaciones
- Modelo AtómicoDocumento4 páginasModelo AtómicoMarvin BatresAún no hay calificaciones
- Línea Del Tiempo de Los Modelos Atómicos - Propuso Hipótesis Sobre La Naturaleza de La Materia Con - StudocuDocumento1 páginaLínea Del Tiempo de Los Modelos Atómicos - Propuso Hipótesis Sobre La Naturaleza de La Materia Con - StudocuJavier Duran AguilarAún no hay calificaciones
- Quimica - 4 ToDocumento5 páginasQuimica - 4 ToVictor Huerta RojasAún no hay calificaciones
- Cuadro Modelos Atómicos - Roldán Marianela 6°EDocumento2 páginasCuadro Modelos Atómicos - Roldán Marianela 6°EAgusAún no hay calificaciones
- Modelos atómicos línea tiempoDocumento2 páginasModelos atómicos línea tiempoLeidy Yohana Bayona Florez86% (7)
- Línea de Tiempo: Modelos AtómicosDocumento1 páginaLínea de Tiempo: Modelos AtómicosMisael Ruiz Gutiérrez100% (2)
- Semana 5, Teoria AtomicaDocumento3 páginasSemana 5, Teoria Atomicajulian David PatiñoAún no hay calificaciones
- Apuntes de QuimcaDocumento4 páginasApuntes de QuimcaLuis Angel Lopez CuautleAún no hay calificaciones
- Tarea BioquímicaDocumento6 páginasTarea BioquímicaIvanna Salazar SosaAún no hay calificaciones
- Historia Del AtomoDocumento15 páginasHistoria Del Atomoisaac luna cañete100% (1)
- Modelos AtómicosDocumento5 páginasModelos AtómicosTrapGameAún no hay calificaciones
- Fusión NuclearDocumento30 páginasFusión NuclearTrapGameAún no hay calificaciones
- Activida3 OlveraRenata Grupo103Documento6 páginasActivida3 OlveraRenata Grupo103Renata Olvera ChávezAún no hay calificaciones
- Modelos Del AtomoDocumento2 páginasModelos Del Atomocamiv14ygAún no hay calificaciones
- Modelos Atómicos y ÁtomoDocumento11 páginasModelos Atómicos y ÁtomoAna Masís SanabriaAún no hay calificaciones
- Resumen Química Común - Diferenciado PDFDocumento112 páginasResumen Química Común - Diferenciado PDFIsaac Sepulveda100% (1)
- Modelos atómicos: evolución histórica de las teorías sobre la estructura del átomoDocumento112 páginasModelos atómicos: evolución histórica de las teorías sobre la estructura del átomoJENNIFER POBLETE CONTRERAS100% (1)
- El ÁtomoDocumento4 páginasEl ÁtomoDamely Olivo AvilesAún no hay calificaciones
- Atomos y Modelos AtomicosDocumento4 páginasAtomos y Modelos AtomicosIgnacio Nuñez FuentesAún no hay calificaciones
- Modulo 4 QT 2021Documento7 páginasModulo 4 QT 2021Carina BogadoAún no hay calificaciones
- Modelos atómicos evoluciónDocumento4 páginasModelos atómicos evoluciónMelissa CalzadaAún no hay calificaciones
- Química San Agustin - 2023 - 4to SecDocumento128 páginasQuímica San Agustin - 2023 - 4to SecPROFESOR ADOLFO RAMÓNAún no hay calificaciones
- Sesión 03 Modelos-AtómicosDocumento10 páginasSesión 03 Modelos-AtómicosEdwar J CordovaAún no hay calificaciones
- Introducción A La Química 1. - Modelos AtómicosDocumento5 páginasIntroducción A La Química 1. - Modelos AtómicosholaAún no hay calificaciones
- GUIA # 5 Estructura AtomicaDocumento6 páginasGUIA # 5 Estructura AtomicaEukarys SáenzAún no hay calificaciones
- 711 Guia 1 Modelos AtómicosDocumento2 páginas711 Guia 1 Modelos AtómicosMaria CarrilloAún no hay calificaciones
- Modelos Atomicos TripticoDocumento4 páginasModelos Atomicos Tripticomiguel100% (2)
- Modelo AtomicosDocumento2 páginasModelo AtomicosRomell CardenasAún no hay calificaciones
- Estructura Atomica El Etomo - TeoriaDocumento3 páginasEstructura Atomica El Etomo - TeoriaSilvia Esmeralda Atoche MirandaAún no hay calificaciones
- Linea de Tiempo-Yurisell Nieto-LicFísica-QuímicaGeneralADocumento2 páginasLinea de Tiempo-Yurisell Nieto-LicFísica-QuímicaGeneralAYurisell NietoAún no hay calificaciones
- Cuadro ComparativoDocumento3 páginasCuadro ComparativoMARIA ALEJANDRA CAMPO MENDOZAAún no hay calificaciones
- Modelo atómico de DemócritoDocumento8 páginasModelo atómico de DemócritoWilliam castilloAún no hay calificaciones
- 95223735-Tabla-modelos-atomicosDocumento1 página95223735-Tabla-modelos-atomicosJosstin ValenciaAún no hay calificaciones
- Captura de Pantalla 2023-09-05 A La(s) 11.11.17 A.M.Documento1 páginaCaptura de Pantalla 2023-09-05 A La(s) 11.11.17 A.M.Javier Duran AguilarAún no hay calificaciones
- MÓDULO 2 - Fundamentos de QuímicaDocumento52 páginasMÓDULO 2 - Fundamentos de Químicajose.torres1Aún no hay calificaciones
- Modelos atómicos: evolución históricaDocumento1 páginaModelos atómicos: evolución históricaPerez AlhanAún no hay calificaciones
- Modelos AtómicosDocumento1 páginaModelos AtómicosSimon34Aún no hay calificaciones
- COSTOSDocumento5 páginasCOSTOSEMMA MARGARITA TORRESAún no hay calificaciones
- Fisica20200527 ESTEBANDocumento4 páginasFisica20200527 ESTEBANEMMA MARGARITA TORRESAún no hay calificaciones
- Cuadernillo Alumno CIENCIAS 2 Semana 4 Al 8 MayoDocumento10 páginasCuadernillo Alumno CIENCIAS 2 Semana 4 Al 8 MayoEMMA MARGARITA TORRESAún no hay calificaciones
- Tipos de Galaxias: Espirales, Elípticas e IrregularesDocumento7 páginasTipos de Galaxias: Espirales, Elípticas e IrregularesEMMA MARGARITA TORRESAún no hay calificaciones
- Tablero Con Dado MatyapoyoDocumento1 páginaTablero Con Dado MatyapoyoEMMA MARGARITA TORRESAún no hay calificaciones
- AMISTADDocumento7 páginasAMISTADEMMA MARGARITA TORRESAún no hay calificaciones
- Tabaco y salud: causas y consecuencias del tabaquismoDocumento9 páginasTabaco y salud: causas y consecuencias del tabaquismoEMMA MARGARITA TORRESAún no hay calificaciones
- La FamiliaDocumento7 páginasLa FamiliaEMMA MARGARITA TORRESAún no hay calificaciones
- Plantilla Genograma FamiliarDocumento1 páginaPlantilla Genograma FamiliarEMMA MARGARITA TORRESAún no hay calificaciones
- Ciencias La Biodiversidad en México Primero Semana Del 25 de Mayo Al 5 de JunioDocumento33 páginasCiencias La Biodiversidad en México Primero Semana Del 25 de Mayo Al 5 de JunioOrtiz CamachoAún no hay calificaciones
- Resolucion de Problemas Colineales y ConcurrentesDocumento54 páginasResolucion de Problemas Colineales y ConcurrentesVeronica Montezuma AguilarAún no hay calificaciones
- AdivinanzasDocumento39 páginasAdivinanzasEMMA MARGARITA TORRESAún no hay calificaciones
- Preguntas de Opción Múltiple - Versión 1Documento42 páginasPreguntas de Opción Múltiple - Versión 1EMMA MARGARITA TORRESAún no hay calificaciones
- Ruleta RETOSDocumento2 páginasRuleta RETOSEMMA MARGARITA TORRESAún no hay calificaciones
- Ciencia DivertidaDocumento4 páginasCiencia DivertidaEMMA MARGARITA TORRESAún no hay calificaciones
- Fenómenos Físicos y QuímicosDocumento2 páginasFenómenos Físicos y QuímicosEMMA MARGARITA TORRESAún no hay calificaciones
- Construyo Mi Circuito ElectricoDocumento7 páginasConstruyo Mi Circuito ElectricoEMMA MARGARITA TORRESAún no hay calificaciones
- Unidades MedicionesDocumento68 páginasUnidades MedicionesWelder Welder CobosAún no hay calificaciones
- Resuleto de Cambio UnidadesDocumento2 páginasResuleto de Cambio UnidadesFrancisco Javier Vera TorresAún no hay calificaciones
- Cadenaalimenticias-Repaso 1Documento13 páginasCadenaalimenticias-Repaso 1EMMA MARGARITA TORRESAún no hay calificaciones
- BiomoleculasDocumento19 páginasBiomoleculasEMMA MARGARITA TORRESAún no hay calificaciones
- Resolucion de Problemas Colineales y ConcurrentesDocumento54 páginasResolucion de Problemas Colineales y ConcurrentesVeronica Montezuma AguilarAún no hay calificaciones
- ADICCIONES ResumenDocumento7 páginasADICCIONES Resumenrosa26101982Aún no hay calificaciones
- Proyectodarwincc 161021090301Documento9 páginasProyectodarwincc 161021090301EMMA MARGARITA TORRESAún no hay calificaciones
- Fichas de RecetaDocumento5 páginasFichas de Recetadoraimon10Aún no hay calificaciones
- Relaciones EcologicasDocumento26 páginasRelaciones EcologicasEMMA MARGARITA TORRESAún no hay calificaciones
- Resumen Vectores Tippens Fisica 1 (Shrunk)Documento24 páginasResumen Vectores Tippens Fisica 1 (Shrunk)EMMA MARGARITA TORRESAún no hay calificaciones
- Perfil de Proyecto de Tesis 2016Documento22 páginasPerfil de Proyecto de Tesis 2016José Moreto CamposAún no hay calificaciones
- Taller Cantidad - de - Movimiento FinalDocumento11 páginasTaller Cantidad - de - Movimiento FinalSantiago OoAún no hay calificaciones
- Semiología Del Ego y ComplejidadDocumento21 páginasSemiología Del Ego y ComplejidadLourdes TebéAún no hay calificaciones
- Evaluación de La Biodegradación Aerobia de Poliuretano Residual Generado en La Industria de Fabricación de RefrigeradoresDocumento12 páginasEvaluación de La Biodegradación Aerobia de Poliuretano Residual Generado en La Industria de Fabricación de RefrigeradoresClara CastellanosAún no hay calificaciones
- Trabajo de Procesamiento Gas RealDocumento5 páginasTrabajo de Procesamiento Gas RealsolodarwinAún no hay calificaciones
- Bousinesq y Coriolis FinalDocumento9 páginasBousinesq y Coriolis FinalGallardo Diaz PatriciaAún no hay calificaciones
- Manejo y Conservacion de SueloDocumento41 páginasManejo y Conservacion de Suelolualj100% (3)
- Equipo de CristalizacionDocumento3 páginasEquipo de CristalizacionJulia MorejonAún no hay calificaciones
- Prueba Planea 5to GradoDocumento36 páginasPrueba Planea 5to GradoAngel Hernandez LorenzoAún no hay calificaciones
- JossimarlabDocumento24 páginasJossimarlabJOSSIMAR JORDANO BACA CONDORI100% (1)
- Didactica Sesion IDocumento6 páginasDidactica Sesion IMilagros Llave NietoAún no hay calificaciones
- Examen Parcial de Mineralogía UNAMDocumento1 páginaExamen Parcial de Mineralogía UNAMMarlene NeriAún no hay calificaciones
- Diagramas de fase y difusión en aleaciones y materialesDocumento3 páginasDiagramas de fase y difusión en aleaciones y materialesDQAún no hay calificaciones
- Sistemas GeotérmicosDocumento17 páginasSistemas GeotérmicosFabrizioAún no hay calificaciones
- Introduccion A La Contaminacion de Los Suelos 11Documento8 páginasIntroduccion A La Contaminacion de Los Suelos 11GONSALITO YTAún no hay calificaciones
- Plan de Tesis de Concreto Puzolánico222Documento38 páginasPlan de Tesis de Concreto Puzolánico222David HaytaAún no hay calificaciones
- Requena EIB SDDocumento176 páginasRequena EIB SDSharon alvarado mescuaAún no hay calificaciones
- Genesis Del SueloDocumento16 páginasGenesis Del SueloAidaCupulBalamAún no hay calificaciones
- D 2210 Manejo Material RadiactivoDocumento34 páginasD 2210 Manejo Material RadiactivoAndres AracenaAún no hay calificaciones
- Modelos Atomicos JDocumento6 páginasModelos Atomicos JIveth IzquierdoAún no hay calificaciones
- Destilación de pentano-heptanoDocumento15 páginasDestilación de pentano-heptanoLuciane Espinoza VillarroelAún no hay calificaciones
- Comunidades Bioticas y EcosistemasDocumento40 páginasComunidades Bioticas y EcosistemasUsias Isau Paz GarciaAún no hay calificaciones
- Unidad 4 Cuerpos IgneosDocumento25 páginasUnidad 4 Cuerpos Igneosagu.echave97Aún no hay calificaciones
- Practica de Laboratorio - Cinetica QuimicaDocumento3 páginasPractica de Laboratorio - Cinetica Quimicali100% (1)
- Dinámica de fluidos: Ecuaciones de continuidad y BernoulliDocumento15 páginasDinámica de fluidos: Ecuaciones de continuidad y BernoulliCarmen Henriquez de ReyesAún no hay calificaciones
- Informe Ambiental Del Estado de Guatemala 2016Documento138 páginasInforme Ambiental Del Estado de Guatemala 2016Allan FernandoAún no hay calificaciones