Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ejercicio 3
Cargado por
Daniel LautaroDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ejercicio 3
Cargado por
Daniel LautaroCopyright:
Formatos disponibles
Viveros Lautaro Daniel 313244
Ejercicio Nº3:
Prepare una tabla estequiométrica para cada una de las siguientes reacciones y exprese la concentracion de
cada especie en la reaccion como una funcion de la conversion, evaluando todas las constantes (por ej., ε y Θ).
despues asuma que la reaccion sigue una ley de velocida elemental y escriba la velocidad de reaccion
unicamente en funcion de la conversion, es decir:
-rA = f ( X)
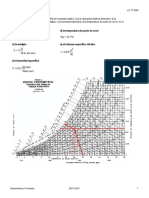
a) Para la reaccion en fase líquida:
las concentraciones iniciales de oxido de etileno y agua son 1 lbmol/pie3 y 3.47lbmol/pie3, respectivamente.
lbmol := 453.5924mol
Reactivo limite OXIDO DE ETILENO
Especie Simbolo Inicial Cambio Final
Ox. de etileno A n A0 -n A0 X n A = n A0 ( 1 - X)
-b
n B = n A0 ΘB - X
b
Agua B n B0 = n A0 ΘB n A0 X
a a
n C = n A0 ΘC + X
c c
1,2 etanodiol C n C0 = n A0 ΘC n A0 X
a a
lbmol lbmol
CA0 := 1 CB0 := 3.47
3 3
ft ft
CA0 C B0
yA0 := = 0.224 yB0 := = 0.776
CA0 + CB0 C A0 + CB0
Coeficientes estequimetricos
a := 1 c := 1
b := 1
c b a
δ := - - = -1 ε := δ yA0 = -0.224
a a a
Operaciones y Procesos 8/11/2021 1
Viveros Lautaro Daniel 313244
Valores de Θ
yA0
ΘA := =1 ΘC := 0
yA0
yB0
ΘB := = 3.47
yA0
Ley de Velocidad
-rA = k CA CB
CONCENTRACIONES
nA (
n A0 1 - X )
CA = = = CA0 ( 1 - X) Fase liquida υ = υ0
υ υo
nB
= CA0 ΘB - X
b
CB =
υ a
Ley de Velocidad
-rA = k CA CB = k CA0 ( 1 - X) CA0 ΘB - X
b
a
-rA = k CA0 ( 1 - X) ΘB - X
2 b
a
b) Para la pirolisis isotermica, isobárica en fase gaseosa
Entra etano puro al reactor de flujo a 6 atm y 1100 K, como cambiaria su ecuación para la concentracion y la
velocidad de reaccion si esto se llevara a cabo en un reactor intermitente de volumen constante.
P0 := 6atm
T0 := 1100K
Operaciones y Procesos 8/11/2021 2
Viveros Lautaro Daniel 313244
Especie Simbolo Inicial Cambio Final
Etano A FA0 -FA0 X FA = FA0 ( 1 - X)
FB = FA0 ΘB + X
b b
Etileno B FB0 = FA0 ΘB FA0 X
a a
FC = FA0 ΘC + X
c c
Hidrogeno C FC0 = FA0 ΘC FA0 X
a a
yA0 := 1
Coeficientes estequimetricos
a := 1 c := 1
b := 1
c b a
δ := + - =1 ε := δ yA0 = 1
a a a
Valores de Θ
yA0
ΘA := =1 ΘC := 0
yA0
ΘB := 0
Ley de Velocidad
-rA = k CA
CONCENTRACIONES
FA (
FA0 1 - X ) CA0 ( 1 - X)
Reactor isotermico e isobarico
CA = = =
υ υo ( 1 + ε X) ( 1 + ε X)
FA0 FA0 yA0 P P
CA0 = = = =
V Rg T Rg T Rg T
FT
P
Operaciones y Procesos 8/11/2021 3
Viveros Lautaro Daniel 313244
Ley de Velocidad
( 1 - X) P0
-rA = k
( 1 + ε X) Rg T0
Si fuese un reactor Intermitente de volumen constante
P0
-rA = k( 1 - X)
Rg T0
c) Para la oxidacion catalitica, isobarica, isotermica en fase gaseosa
la alimentacion entra a un reactor de lecho empacado (PBR) a 6 atm y 260 °C, y es una mezcla estequiométrica
unicamente de oxigeno y etileno
Especie Simbolo Inicial Cambio Final
Etileno A FA0 -FA0 X FA = FA0 ( 1 - X)
-b
FB = FA0 ΘB - X
b
Oxigeno B FB0 = FA0 ΘB FA0 X
a a
FC = FA0 ΘC + X
c c
Oxido de etileno C FC0 = FA0 ΘC FA0 X
a a
P0 := 6atm
T0 := 260 °C
1 0.5
yA0 := = 0.667 yB0 := = 0.333
1 1.5
1+
2
Operaciones y Procesos 8/11/2021 4
Viveros Lautaro Daniel 313244
Coeficientes estequimetricos
a := 1 c := 1
1
b :=
2
c b a
δ := - - = -0.5 ε := δ yA0 = -0.333
a a a
Valores de Θ
yA0
ΘA := =1 ΘC := 0
yA0
yB0
ΘB := = 0.5
yA0
Ley de Velocidad
dX
FA0 = -rA
dW
0.5
-rA = k CA CB
FA FA0 ( 1 - X) ( 1 - X) P T0
CA = = = CA0
V P0 T ( 1 + ε X) P0 T
V0
( 1 + ε X)
0
P T
Θ - b X
B
FB
a P T0
CB = = CA0
V ( 1 + ε X) P0 T
0.5
Θ - b X
B
dX 1 a P T0 ( 1 - X) P T0
= C A0 CA0
dW FA0 ( 1 + ε X) P0 T ( 1 + ε X) P0 T
Operaciones y Procesos 8/11/2021 5
Viveros Lautaro Daniel 313244
1.5 T 0.5 1.5
( 1 - X)
ΘB - X
dX 1 1.5 P 0 b
= CA0
dW FA0
( 1 + ε X)
1.5 P0
T a
dP -α T P0
= ( 1 + ε X)
dW 2 T0 P
P0
( 1 - ϕ) 150 ( 1 - ϕ) μ
β0 = G + 1.75 G
ρ0 Dp ϕ
3 Dp
2 β0
α=
Ac ρc ( 1 - ϕ) P0
Si la reaccion es isobarica, isotermica
0.5
( 1 - X)
ΘB - X
dX 1 1.5 b
= CA0
dW FA0
( 1 + ε X)
1.5 a
dP -α
= P0 ( 1 + ε X) Si es isobarica la reaccion, este ecuacion diferencial es nula
dW 2
Operaciones y Procesos 8/11/2021 6
También podría gustarte
- Ingenieria de Reacciones Quimicas I: Interpretación de Datos Cinéticos ExperimentalesDocumento90 páginasIngenieria de Reacciones Quimicas I: Interpretación de Datos Cinéticos ExperimentalesmiriamAún no hay calificaciones
- Ejemplo 6.3 TreybalDocumento7 páginasEjemplo 6.3 TreybalJuan Carlos Montes CalaAún no hay calificaciones
- Anexo - Curriculum Montajes EmeltaDocumento38 páginasAnexo - Curriculum Montajes EmeltaOscar Bravo100% (1)
- Problema de BalanceDocumento2 páginasProblema de BalanceRoger Fiel Vega ToscanoAún no hay calificaciones
- FISICOQUIMICA2Documento14 páginasFISICOQUIMICA2Jesus Alexis Cervantes RamirezAún no hay calificaciones
- Diapositiva 4 CSTR SeguridadDocumento56 páginasDiapositiva 4 CSTR SeguridadDENIS LEYVAAún no hay calificaciones
- اسبانية 7Documento34 páginasاسبانية 7Aljebre MohmedAún no hay calificaciones
- Ejercicio 4Documento8 páginasEjercicio 4Daniel LautaroAún no hay calificaciones
- Grupo 3 Ejercicio 8,2 Ocon TojoDocumento13 páginasGrupo 3 Ejercicio 8,2 Ocon TojoEvelyn PinedaAún no hay calificaciones
- Ejemplo7.23 Caso Sistemas InmisciblesDocumento3 páginasEjemplo7.23 Caso Sistemas InmisciblesAlvaro Gustavo50% (2)
- Calcular El Factor de Frecuencia y La Energía de Activación para La Reacción de Descomposición Del Cloruro Diazonico de Benceno en Cloro Benceno y NitrógenoDocumento1 páginaCalcular El Factor de Frecuencia y La Energía de Activación para La Reacción de Descomposición Del Cloruro Diazonico de Benceno en Cloro Benceno y NitrógenoAlexisGalloAún no hay calificaciones
- Actividad 2. Del Angel Montes Rudy JovannyDocumento5 páginasActividad 2. Del Angel Montes Rudy Jovannyjavi RodriguezAún no hay calificaciones
- Ejercicios MC Cabe Enthile. Poncho SavaritDocumento15 páginasEjercicios MC Cabe Enthile. Poncho SavaritStefano Gomez LlimpeAún no hay calificaciones
- Ejercicio 1Documento5 páginasEjercicio 1Daniel LautaroAún no hay calificaciones
- TF2126 Tema V y VI Problemas ResueltosDocumento70 páginasTF2126 Tema V y VI Problemas ResueltosMiguel GalvizAún no hay calificaciones
- Universidad de Guayaquil Facultad de Ingeniería Química Ingeniería de Las Reacciones Ing. Stefanie Bonilla Bermeo, MSCDocumento9 páginasUniversidad de Guayaquil Facultad de Ingeniería Química Ingeniería de Las Reacciones Ing. Stefanie Bonilla Bermeo, MSCJose LozanoAún no hay calificaciones
- Problema de FiltraciónDocumento5 páginasProblema de FiltraciónCecy CarbajalAún no hay calificaciones
- Pre 1 OU - Reyes CastilloDocumento3 páginasPre 1 OU - Reyes CastillonercAún no hay calificaciones
- Problema AmoniaDocumento9 páginasProblema AmoniaValentinaAún no hay calificaciones
- DR Tema2 3raedDocumento33 páginasDR Tema2 3raedLucy Isabel Carpio Ramírez50% (2)
- MasaDocumento2 páginasMasaCatalina3009Aún no hay calificaciones
- Trabajo de Opu de Grupo de 3 IntegrantesDocumento23 páginasTrabajo de Opu de Grupo de 3 IntegrantesRodrigo BaluarteAún no hay calificaciones
- Ejemplo7.23 Caso Sistemas InmisciblesDocumento4 páginasEjemplo7.23 Caso Sistemas InmisciblesAlvaro GustavoAún no hay calificaciones
- Problemas LeyRaoult 4oct2019Documento15 páginasProblemas LeyRaoult 4oct2019DavidMejiaAún no hay calificaciones
- Segundo AvanceDocumento27 páginasSegundo AvanceKEVIN DANILO ACEVEDO PEREZ ESTUDIANTE ACTIVOAún no hay calificaciones
- Cuestionario 3Documento3 páginasCuestionario 3Silver NicaraguaAún no hay calificaciones
- C.. - '.. - 13 FEB 20b: Instituto de Investigación de Ingeniería QuímicaDocumento124 páginasC.. - '.. - 13 FEB 20b: Instituto de Investigación de Ingeniería QuímicaKatherin Massiel Codoceo UlloaAún no hay calificaciones
- Prob 9 15 Treybal 2021Documento6 páginasProb 9 15 Treybal 2021Sergio VargasAún no hay calificaciones
- Parcial de Opus ResueltoDocumento18 páginasParcial de Opus ResueltoIngrid Natalia RamirezAún no hay calificaciones
- Tarea 2. Torres MendozaDocumento4 páginasTarea 2. Torres MendozaLisensiado LlovisAún no hay calificaciones
- Práctica 1 Calor Diferencial de SoluciónDocumento7 páginasPráctica 1 Calor Diferencial de SoluciónDaniel Ortiz LealAún no hay calificaciones
- 3 Equiipo 5 Problemario PDFDocumento11 páginas3 Equiipo 5 Problemario PDFSalvador SantosAún no hay calificaciones
- Primer Grupo-ProblemasDocumento15 páginasPrimer Grupo-ProblemasZayda MireyAún no hay calificaciones
- Problemas Resueltos - Ingeniería de Las Reaccciones Químicas IIDocumento82 páginasProblemas Resueltos - Ingeniería de Las Reaccciones Químicas IIAlejandra VelascoAún no hay calificaciones
- Ejercicios Semana 16Documento4 páginasEjercicios Semana 16Gabriel AgripinoAún no hay calificaciones
- Problema 7.10 KERNDocumento6 páginasProblema 7.10 KERNJurgen Corpi Gómez100% (1)
- Cer Vera AndreaDocumento21 páginasCer Vera AndreaAndrea CerveraAún no hay calificaciones
- Problema 1Documento12 páginasProblema 1Kartel KalientitoxAún no hay calificaciones
- Trey Bal EjerciciosDocumento7 páginasTrey Bal EjerciciosFabio Eitnar MelgarejoAún no hay calificaciones
- Universidad Autónoma de San Luis Potosí: Facultad de Ciencias QuímicasDocumento85 páginasUniversidad Autónoma de San Luis Potosí: Facultad de Ciencias QuímicasAlejandro RomoAún no hay calificaciones
- Ejercicios Ocon Tojo Cap 3docx PDF FreeDocumento12 páginasEjercicios Ocon Tojo Cap 3docx PDF FreeJorge Nolasco CruzAún no hay calificaciones
- Ejercicio Ec. ArrheniusDocumento10 páginasEjercicio Ec. ArrheniusAndrés DelaRosa MartínezAún no hay calificaciones
- KC KP Ky: Atm Atm - L. SDocumento4 páginasKC KP Ky: Atm Atm - L. SMei CelisAún no hay calificaciones
- Ejerciio. 7. 10 (Operaciones Unitarias 2)Documento13 páginasEjerciio. 7. 10 (Operaciones Unitarias 2)Lester Halsey GutierrezAún no hay calificaciones
- E MonografiaDocumento18 páginasE MonografiaGrover Raul Bazan AriasAún no hay calificaciones
- IQ.09.01 - Actividad Asincrónica 6Documento4 páginasIQ.09.01 - Actividad Asincrónica 6Adolfo LazoAún no hay calificaciones
- Tarea XI TermoDocumento42 páginasTarea XI TermoGabriel Arturo Castillo CcorimayyaAún no hay calificaciones
- Asignación Destilación FINALDocumento34 páginasAsignación Destilación FINALJAMIT GUZMAN MARTINEZAún no hay calificaciones
- SINTESISDocumento48 páginasSINTESISYamimoon DtnAún no hay calificaciones
- Serie 1 Cinetica Quimica2021-2Documento6 páginasSerie 1 Cinetica Quimica2021-2Josue Hernandez MrkzAún no hay calificaciones
- Asignación Isomerizacion de Nbutano A IsobutanoDocumento14 páginasAsignación Isomerizacion de Nbutano A IsobutanoDesiree MarinAún no hay calificaciones
- Problema 9.1treybalDocumento18 páginasProblema 9.1treybalTobiI SempaiAún no hay calificaciones
- DIFUSIVIDADDocumento9 páginasDIFUSIVIDADAdrian Hernandez OmañaAún no hay calificaciones
- Ej Balance de Masa CombustionDocumento1 páginaEj Balance de Masa CombustionLizbeth AbrilAún no hay calificaciones
- 1er Examen Parcial de Ingeniería de Reactores Químicos II 26Documento2 páginas1er Examen Parcial de Ingeniería de Reactores Químicos II 26TobiI SempaiAún no hay calificaciones
- Extraccion SL 1Documento38 páginasExtraccion SL 1Álvaro YisusAún no hay calificaciones
- Elaboracion de Simil Jugo3Documento4 páginasElaboracion de Simil Jugo3Alvaro GustavoAún no hay calificaciones
- Práctica 4Documento6 páginasPráctica 4DztAún no hay calificaciones
- Ejercicios de CalorDocumento6 páginasEjercicios de CalorFrancis Meza BaldeonAún no hay calificaciones
- Ejercicio 2Documento3 páginasEjercicio 2Daniel LautaroAún no hay calificaciones
- Ejercicio 1Documento8 páginasEjercicio 1Daniel LautaroAún no hay calificaciones
- Ejercicio 4Documento4 páginasEjercicio 4Daniel LautaroAún no hay calificaciones
- Ejercicio 4Documento7 páginasEjercicio 4Daniel LautaroAún no hay calificaciones
- Tarea 7-Rodriguez Lopez Pedro ArturoDocumento9 páginasTarea 7-Rodriguez Lopez Pedro ArturoMafer Mabel GalarzaAún no hay calificaciones
- InformeDocumento7 páginasInformeDaniel LautaroAún no hay calificaciones
- Anexo I-PFDDocumento1 páginaAnexo I-PFDDaniel LautaroAún no hay calificaciones
- Trabajo Práctico N°1Documento20 páginasTrabajo Práctico N°1Daniel LautaroAún no hay calificaciones
- Libro 2Documento2 páginasLibro 2Daniel LautaroAún no hay calificaciones
- Anexo VIIA-NFENDS4167-00-A4-HiResDocumento8 páginasAnexo VIIA-NFENDS4167-00-A4-HiResDaniel LautaroAún no hay calificaciones
- Informe Trabajo 6CDocumento3 páginasInforme Trabajo 6CDaniel LautaroAún no hay calificaciones
- Anexo V-DS - TE6101 - Es - Es - 111563Documento15 páginasAnexo V-DS - TE6101 - Es - Es - 111563Daniel LautaroAún no hay calificaciones
- Anexo IV-FI01 Us Kap02Documento156 páginasAnexo IV-FI01 Us Kap02Daniel LautaroAún no hay calificaciones
- Informe Trabajo 6BDocumento3 páginasInforme Trabajo 6BDaniel LautaroAún no hay calificaciones
- Transporte de Gas A Media PresiónDocumento8 páginasTransporte de Gas A Media PresiónDaniel LautaroAún no hay calificaciones
- Informe Trabajo 6BDocumento3 páginasInforme Trabajo 6BDaniel LautaroAún no hay calificaciones
- Trabajo Practico #6C: Transporte de Gas Natural A Alta Presion-GasoductosDocumento26 páginasTrabajo Practico #6C: Transporte de Gas Natural A Alta Presion-GasoductosDaniel LautaroAún no hay calificaciones
- Informe Trabajo 6ADocumento3 páginasInforme Trabajo 6ADaniel LautaroAún no hay calificaciones
- Informe Trabajo 6ADocumento3 páginasInforme Trabajo 6ADaniel LautaroAún no hay calificaciones
- Ejercicio 2Documento3 páginasEjercicio 2Daniel LautaroAún no hay calificaciones
- InformeDocumento5 páginasInformeDaniel LautaroAún no hay calificaciones
- Libro 1Documento9 páginasLibro 1Daniel LautaroAún no hay calificaciones
- InformeDocumento5 páginasInformeDaniel LautaroAún no hay calificaciones
- Libro 1Documento26 páginasLibro 1Daniel LautaroAún no hay calificaciones
- Ejercicio 5Documento3 páginasEjercicio 5Daniel LautaroAún no hay calificaciones
- Ejercicio 5Documento6 páginasEjercicio 5Daniel LautaroAún no hay calificaciones
- Ejercicio 4Documento3 páginasEjercicio 4Daniel LautaroAún no hay calificaciones
- Ejercicio1 2Documento3 páginasEjercicio1 2Daniel LautaroAún no hay calificaciones
- Ejercicio 3Documento4 páginasEjercicio 3Daniel LautaroAún no hay calificaciones
- Ejercicio 3Documento3 páginasEjercicio 3Daniel LautaroAún no hay calificaciones
- Ejercicio1 2Documento3 páginasEjercicio1 2Daniel LautaroAún no hay calificaciones
- Ejercicio 3Documento3 páginasEjercicio 3Daniel LautaroAún no hay calificaciones
- Ejercicio 3Documento12 páginasEjercicio 3Daniel LautaroAún no hay calificaciones
- Evaporacion WordDocumento12 páginasEvaporacion WordAriana JuradoAún no hay calificaciones
- Examen TerceroDocumento13 páginasExamen TerceroleyAún no hay calificaciones
- Tema Tesis UdchDocumento16 páginasTema Tesis UdchJoseSilvaAún no hay calificaciones
- Actividad Eje 2 Estrategias GerencialesDocumento21 páginasActividad Eje 2 Estrategias GerencialesDaniel BarajasAún no hay calificaciones
- AguadesarrollosostenibleDocumento8 páginasAguadesarrollosostenibleeverAún no hay calificaciones
- Cuarto. Guía 5. Unidad 2 Análisis de Textos Narrativos PDFDocumento3 páginasCuarto. Guía 5. Unidad 2 Análisis de Textos Narrativos PDFAnge EspinozaAún no hay calificaciones
- 5 19may Evaluación Diagnostica Comunicación PrimariaDocumento57 páginas5 19may Evaluación Diagnostica Comunicación PrimariamarchanthuanAún no hay calificaciones
- Banco de PreguntasDocumento4 páginasBanco de PreguntasAlfonso RomoAún no hay calificaciones
- MONOGRAFIAToxina Botulinica Tipo A - C.D. 1 PDFDocumento55 páginasMONOGRAFIAToxina Botulinica Tipo A - C.D. 1 PDFEdumar EspinozaAún no hay calificaciones
- Exposicion Muerte AbsolutaDocumento3 páginasExposicion Muerte AbsolutaKoinoyokan KintsukuroiAún no hay calificaciones
- GW Instek Sfg-2007Documento3 páginasGW Instek Sfg-2007Logan RodriguezAún no hay calificaciones
- Dibujos OrtogonalesDocumento9 páginasDibujos OrtogonalesLeticia Reyes FlorentinoAún no hay calificaciones
- Concepto Del Espacio de DisseDocumento3 páginasConcepto Del Espacio de DisseWcaro TutiendaAún no hay calificaciones
- Alfonso - Hernandez - Actividad2 AgostoDocumento14 páginasAlfonso - Hernandez - Actividad2 AgostopacoxD :vAún no hay calificaciones
- Ficha 8 MatemáticaDocumento12 páginasFicha 8 MatemáticaJuan Carlos MadaAún no hay calificaciones
- Tabla de Convalidacion - Ing - Ind - Pensum 2016Documento1 páginaTabla de Convalidacion - Ing - Ind - Pensum 2016Sobeida JimenezAún no hay calificaciones
- I. - 1. El Poblamiento de America.Documento13 páginasI. - 1. El Poblamiento de America.Eduardo Cardenas CamposAún no hay calificaciones
- Las Actividades Económicas de OceaníaDocumento8 páginasLas Actividades Económicas de OceaníaLuis RomeroAún no hay calificaciones
- Criterio Financieros para Seleccion de InversionesDocumento49 páginasCriterio Financieros para Seleccion de InversionesAsdfAún no hay calificaciones
- Chevrolet-Spark 2013 ES-MX MX 7d2421337eDocumento202 páginasChevrolet-Spark 2013 ES-MX MX 7d2421337eIsmael Elias Rondan MamaniAún no hay calificaciones
- Terrier 2006Documento6 páginasTerrier 2006ita79Aún no hay calificaciones
- Sena 2Documento7 páginasSena 2Javier AndresAún no hay calificaciones
- Amenorrea SecundariaDocumento17 páginasAmenorrea SecundariaJuan Diego Condori SaavedraAún no hay calificaciones
- Guía Seminario #2 - Farmacología Sistema Nervioso Autónomo - 2019 2Documento1 páginaGuía Seminario #2 - Farmacología Sistema Nervioso Autónomo - 2019 2yaritzaAún no hay calificaciones
- Taller de Gasto No OperacionalesDocumento212 páginasTaller de Gasto No OperacionalesMerlys Milena Manjarres HuertoAún no hay calificaciones
- Metrados de CargasDocumento11 páginasMetrados de CargasShirley VasquezAún no hay calificaciones
- CerealesDocumento35 páginasCerealesCESIA RAQUEL AVITIA CANOAún no hay calificaciones
- BH User ManualDocumento104 páginasBH User Manualhapizeguet8128Aún no hay calificaciones