Mayo 18 de 2021
El Comportamiento Transitorio de un RCTA
La operación en estado estacionario de cualquier reactor es precedida por
el inicio de la misma, también llamada “el arranque del reactor”. Esto es, la
puesta en marcha de una operación que requiere conocer la naturaleza de la
reacción (su cinética, exotermicidad, equilibrio químico, etc) así como de los
procesos de transferencia de materia y calor en el reactor asociados con la
reacción. Por esto, es importante que, conjuntamente con el trabajo
experimental en un reactor a nivel laboratorio o de escala de banco, se lleve a
cabo la simulación matemática del comportamiento dinámico (transitorio) del
reactor, con el proposito de diseñar y construir la unidad de reacción a nivel
industrial. De lo anterior deriva nuestra ecuación (de acuerdo con JJ Carberry):
Reactor = Reacción (1)
Donde el primer término incluye a:
Reactor=Comportamiento transitorio + Transporte (masa y calor) (2)
En esta parte consideramos el comportamiento transitorio de un RCTA para una
reacción exotérmica que ocurre en paralelo y en serie (ver problema 21),
derivando sus balances de materia y calor, y resolviendo numéricamente el
modelo dinámico resultante, utilizando un método de Runge-Kutta de 4O orden
(ver Conte y de Boor, Elementary Numrical Analysis, MC Graw Hill, 1980).
La reacción es la siguiente, y queremos encontrar las condiciones de operación
donde se logre una mayor producción del componente B.
1 B
2
A
3 C
Con los siguientes datos:
1
�Volumen del reactor: V=1500 cm3.
Flujo volumétrico: F0= 100 cm3.
Capacidad térmica: ρCp= 750 cal/(cm3-K).
Coeficiente de transferencia de calor. U= 0.15 (cal/cm2-min-K).
Área de enfriamiento: Ae= 350 cm2.
Concentraciones de alimentación: CA0=5.0 x 10-3 (gmol/ cm3).
Temperatura de alimentación: T0= 425 K y 450 K.
Temperatura del medio de enfriamiento: Te= 440 K y 450 K.
Datos de la cinética triangular
Reacción ko (1/seg) EA (cal/gmol) (−ΔH ) (cal/gmol)
1 5.50x107 19,500 25,000
2 3.50x106 20,800 20,000
3 1.30x106 24,700 45,000
Los balances de materia y energía en el caso transitorio son:
dC A ( C AO − C A )
= − (k1 + k3 )C A (3)
dt θ
dC B −C B
= + (k1C A − k2C B ) (4)
dt θ
dCC −CC
= + (k3C A + k2C B ) (5)
dt θ
dT (To − T ) ⎛α⎞
= + [ (k1 J1 + k3 J 3 )C A + k2 J 2C B ] − ⎜ ⎟ (T − TE ) (6)
dt θ ⎝θ⎠
α ⎛ UA ⎞ ⎛ Fo ⎞ ⎛ UA ⎞ ⎛ Fo ⎞ ⎛ (−ΔH i ) ⎞
donde = ⎜ ⎟= ⎜ ⎟ y Ji = ⎜ (i=1,2,3)
θ ⎜⎝ V ρ Cp ⎟⎠ ⎝ Fo ⎠ ⎜⎝ Foρ Cp ⎟⎠ ⎝ V ⎠ ⎝ ρ Cp ⎟⎠
La solución numéricamente del sistema de ecuaciones (3) a (6) puede ahora ser
utilizada como una herramienta valiosa para encontrar las condiciones de
operación de un RCTA, e investigar el papel de cada uno de los parámetros de
operación (To, Te, V, Fo etc) involucrados.
2
�La simulación de este proceso tiene como objetivo mostrar este procedimiento
complementario para el diseño de un RCTA, y para esto consideramos tres casos
en los cuales las temperaturas de alimentación (To) y del medio de enfriamiento
(Te) son diferentes. Las figuras 1 a 3 muestra el efecto que tiene utilizar
diferentes valores de To (o de Te) en la distribución de productos dentro del
RCTA, cuando se alcanza el estado estacionario, y especialmente en su
comportamiento dinámico. Tomemos como base la figura 1, y comparemos la
producción del componente B que se obtiene cuando Te cambia de 425 a 450 K
(figura 2), y que nos muestra que si bien CB tiene una magnitud similar, la
concentración CA es mayor para el primer caso, lo que obligaría a emplear un
mayor gasto de energía en la separación y purificación de B. Por otro lado, la
máxima temperatura alcanzada en el caso 2 es mayor, lo cual podría ser no
muy conveniente.
T T
To=425 K y Te=440 K To=425 K y Te=450 K
580 0.005 580 0.005
560 560
Concentración Cn (gmol/cm )
Temperatura en el RCTA (K)
Concentración Cn (gmol/cm )
0.004
Temperatura en el RCTA (K)
0.004
540 540
520 520
0.003 0.003
500 CA
CA 500
CB
CB 0.002
480 CC 0.002
CC 480
460 460
0.001 0.001
3
440 440
420 0 420 0
0 50 100 150 200 250 300 350 0 50 100 150 200 250 300 350
tiempo (min) tiempo (min)
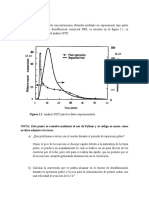
Figura 1. Comportamiento dinámico en Figura 2. Comportamiento dinámico en
el RCTA caso (a) el RCTA caso (b)
También observamos que el estado estacionario del caso 2 se alcanza en un
menor tiempo de operación, ya que a mayor valor de Te la reacción procede más
rápidamente. Comparemos ahora el caso 1 con el 3 (figura 3, pag. 5), el cual
3
�tiene el mismo valor de Te pero To se ha incrementado de 425 a 450 K. Aquí
podemos observar que la temperatur amáxima que se alcanza en el RCTA es
casi 90 K mayor que en el caso 1, lo cual no es deseable (por motivos de
seguridad y control del RCTA), y tambien podemos ver que hay una menor
producción del componente B y mayor producción del componente C (que no es lo
deseable), ya que esto se debe a que EA3>EA2, lo cual favorece la producción de
C sobre la de B.
La figura 4 muestra que a las condiciones del caso 3 solo hay un estado
estacionario, y corresponde al de mayor conversión (o encendido). Las figuras 5
y 6 muestran lo que se conoce como el plano de fase del RCTA, (ver algún libro
sobre ecuaciones diferenciales ordinarias, como por ej. Arrowsmith & Place:
Dynamical Systems. Chapman & Hall, 1992). Esto es, cómo varian la temperatura
y las concentraciones dentro del reactor a diferentes temperaturas de
alimentación, cuando Te= 440 K(Fig. 5) y Te= 450 K(Fig. 6). En estas figuras se
muetra la región donde puede operar el reactor con una alta conversión, como
función de la temperatura de alimentación To. Algo que es importante destacar
es que la evolución de la temparatura y concentraciones en el RCTA a lo largo
del tiempo, es la respuesta transitoria (dinámica) del reactor durante la cual la
generación y eliminación de calor no son iguales, sino hasta que se alcanza el
estado estacionario.
Este ejercicio no termina aquí, ya que sería importante saber cómo sería la
operación utilizando un volumen diferente del RCTA, o incluso qué pasa si
cambiamos el tipo de reactor a uno de fluto tapon (RFT) con condiciones de
operación similares, lo cual veremos en la siguiente clase, de cómo son los
balances de materia y calor en un RFT, para el caso de una operación
transitoria.
4
� T Multiplicidad
To=450 K y Te=440 K 500
650 0.005
QE
400 QG
(cal/seg)
Concentración Cn (gmol/cm )
Temperatura en el RCTA (K)
600 0.004
300
550 0.003
G
CA
y Q
200
CB
500 0.002
E
CC
Q
100 T = 530 (K)
(1 solo EE)
450 0.001
0
3
400 450 500 550 600 650 700
400 0 Temperatura (K)
0 50 100 150 200 250 300 350
tiempo (min)
Figura 3. Comportamiento dinámico en Figura 4. La multiciplidad de estados
el RCTA caso (c) estacionarios se reduce a solamente
un estado estacionario (encendido) en
el RCTA
Region de Operacion para Te= 440 (K) Region de Operacion para Te= 450 (K)
540 0.005 600 1
XA
Concentración Cn (gmol/cm )
Temperatura en el RCTA (K)
520
Temperatura en el RCTA (K)
T 0.004 0.8
550
Conversión (X )
500
0.003 0.6
480 T
500
CA
460 0.002 0.4
CB
CC
440
A
450
0.001 0.2
420
3
400 0 400 0
360 380 400 420 440 460
370 380 390 400 410 420 430
Temperatura de Alimentacion To (K) Temperatura de Alimentacion To (K)
Figura 5. Región de operación del RCTA Figura 6. Región de operación del
(Plano de Fases) RCTA (Plano de Fases)