Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Dispensar Medicamentos - Material de Estudio
Dispensar Medicamentos - Material de Estudio
Cargado por
Norlan Gonzalez CastroTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Dispensar Medicamentos - Material de Estudio
Dispensar Medicamentos - Material de Estudio
Cargado por
Norlan Gonzalez CastroCopyright:
Formatos disponibles
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
MATERIAL DE ESTUDIO EN PLATAFORMA VIRTUAL
CONTENIDO
TEMA 1. HISTORIA DE LA FARMACIA
1. La farmacia en el mundo
2. La farmacia en América
3. Símbolos de la farmacia
4. La Farmacia en Colombia
TEMA 2. NORMATIVIDAD GENERAL PARA EL SERVICIO FARMACÉUTICO
1. El ejercicio de la farmacia
2. Los Establecimientos Farmacéuticos
3. Control de los Establecimientos Farmacéuticos
4. Los medicamentos y los dispositivos médicos
5. Procesos del Servicio Farmacéutico
6. Turnos de las Farmacias y Droguerías
7. Preparaciones magistrales y droga blanca
8. Servicio de inyectología y glucometría
9. Publicidad y promoción de los medicamentos
10. Decreto único reglamentario del sector salud y protección social
TEMA 3. PRINCIPIOS DE FARMACOLOGÍA
1. Farmacología
2. El medicamento
3. Clasificación de los medicamentos
TEMA 4. LA DISPENSACIÓN
1. Definición
2. La comunicación como base de la dispensación
3. Características del dispensador
4. Como dispensar
5. Dispensación de medicamentos, Decreto 780 de 2016
TEMA 5. AUTOMEDICACIÓN RESPONSABLE
1. Uso incorrecto de los medicamentos
2. Consecuencias del uso inadecuado de los medicamentos
3. Factores que contribuyen al uso incorrecto de los medicamentos
TEMA 6. MEDICAMENTOS DE CONTROL ESPECIAL Y MONOPOLIO DEL ESTADO
1. Definiciones
2. Manejo de sustancias sometidas a fiscalización
3. Requisitos para la inscripción
4. Recurso humano idóneo
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
5. Distribución, venta y usos de medicamentos monopolio del Estado
6. Pérdida y destrucción de sustancias, medicamentos y/o productos sometidos a
fiscalización
7. Prescripción de medicamentos de control especial
8. Recetario Oficial
9. Infracciones y sanciones
Tema 7. Farmacovigilancia
1. Definiciones
2. Elementos
3. Atención Farmacéutica
4. Programa Nacional de Farmacovigilancia.
Tema 8. Dispositivos Médicos – Tecnovigilancia
1. Definiciones
2. Clasificación de los dispositivos médicos
3. Tecnovigilancia
Guías de aprendizaje
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tema 1. HISTORIA DE LA FARMACIA.
1. La Farmacia en el mundo
La enfermedad ha acompañado a los seres vivos, forma parte del proceso natural de la
vida, por esta razón desde el inicio el ser humano ha buscado métodos que le permitan
manejar la enfermedad y procurarse un mejor bienestar.
En este propósito el hombre ha escudriñado sobre productos en los diferentes reinos
(animal, vegetal y mineral) que le provean de sustancias que le permitan afrontar y
mejorar sus dolencias e incluso que le den bienestar o belleza.
Las personas que se dedicaban al arte de curar eran indispensables para las
comunidades, eran los curanderos, brujos o chamanes. Una de las culturas que más
aportaron investigaciones sobre el concepto de salud y bienestar fue la egipcia quienes
dejaron información detallada sobre los procesos farmacológicos, tenían entre sus
deidades a Anubis.
La característica de estos curanderos consistía, además de las mezclas de sustancias, en
la realización de conjuros y ritos que les daban a los remedios un valor místico, lo que
además en muchas culturas convertían al curandero en un líder espiritual.
En Grecia tomaron los principios sobre la farmacia de las culturas egipcias y babilónicas,
la salud era tan importante para ellos que varios de sus dioses tenían relación con el
bienestar: Pharmakis era la diosa de la magia experta en plantas medicinales, Apolo y
Artemis tenían poderes curativos, Esculapio era el dios médico que transmitió sus
conocimientos a sus hijas Higea y Panacea.
Hipócrates consideraba que la enfermedad es causada por un desequilibrio entre los
cuatro humores del cuerpo (bilis, bilis negra, sangre y flema), para preparar
medicamentos estaban los pharmacópolas, esto sería el primer modelo de farmacia
occidental.
En Roma Dioscórides escribe “Materia Médica”, Andrómaco hace famosa la “Triaca
Magna” y Galeno prepara sus propios medicamentos que producían un efecto contrario al
síntoma de la enfermedad.
Fue en las naciones islámicas donde retomaron los escritos griegos de Galeno y
Dioscórides, hicieron medicamentos con sabores agradables, introdujeron el uso de
jarabes además de la coloración de los productos para darle una presentación más
llamativo, dejaron textos sobre medicamentos y su forma de prepararlos, por ejemplo,
“Colección de medicamentos y elementos simples” de Ebn-Beitar. Al parecer las primeras
farmacias se abrieron como establecimiento independiente en Bagdad.
En 1240 Federico II de Alemania ordenó la regulación de la preparación de medicamentos
y sus precios, esto se reconoce como la separación oficial entre la medicina y farmacia.
Para la Edad Media las ciencias médicas estaban influenciadas por la religión y se
desarrolló en su gran mayoría en monasterios y conventos, ya en el Renacimiento el suizo
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Paracelso implanta el concepto de “yatroquímia” que tiene en cuenta la química como
parte de la terapia, lo que permite pasar a otras sustancias además de las plantas
utilizadas.
En 1498 aparece la primera farmacopea: “El recetario Florentino”, las farmacias se
enriquecen con la variedad que le provee la química y las plantas descubiertas en
América, aparecen grandes botánicos y químicos en Europa: Besler, Tabernaemontanus
y Coudenberg.
En el siglo XVII son varios los avances de las ciencias farmacéuticas, se introduce la
farmacia en el ámbito institucional, se reconoce al Boticario Mayor del Rey y al Boticario
Mayor del Ejército, en la oficina de farmacia se separa el laboratorio de la zona de
atención al público, se introduce la quina, la ipecacuana y el bálsamo del Perú, como
novedad aparecen los enemas como parte del tratamiento.
Los boticarios franceses avanzan con el descubrimiento de la acetona, el tartrato sódico
potásico, el nitrato y sulfato potásico, el acetato mercúrico, el cloruro de etilo.
Para el siglo XVIII, Proust enuncia la “Ley de proporciones definidas”, Scheele descubre el
oxígeno, el nitrógeno y la glicerina, Hoeffer el ácido bórico, Böttger el caolín.
En el Siglo XIX la tecnología permite la fabricación de nuevos equipos de laboratorio y la
preparación de nuevas formas farmacéuticas como cápsulas, la farmacia se industrializa y
aparecen la farmacia como carrera independiente en muchas universidades.
Aparecen nuevos fármacos como la morfina (Serturner), la cafeína (Pelietir y Caventou,
que también aislaron la quinina y la estricnina entre otros), otros avances fueron:
Parmentier difunde con éxito la patata en Francia para combatir la hambruna, Buchner
descubre la parafina, Courtois el yodo, Soubeiran el cloroformo, Serulias el yodoformo,
Balard el bromo, Stromeyer el cadmio, Oersted el aluminio, Döbereiner el acetaldeído,
Walker las cerilias de fricción, Guibourt la cumarina, Ambrosioni el azúcar en la sangre de
los diabéticos, Bussy el magnesio y el berilio, Klaus el rutenio etc.
En el Siglo XX la farmacia es parte fundamental de los tratamientos, se incluye en los
estudios universitarios, hay un gran avance de la producción farmacéutica industrial,
Fleming con la penicilina y Pasteur con el proceso de pasteurización impulsan las ciencias
farmacéuticas, se reglamenta la Farmacia para la salud pública, se establecen las
políticas farmacéuticas en cada nación, la investigación permite nuevos medicamentos, ya
para finales del siglo e inicio del Siglo XXI la Farmacia se enfoca en el paciente y en la
comunidad.
Vídeos de apoyo
Historia de la Farmacia, Parte 1. Rony Condeña, EVILAF, 2017
https://www.youtube.com/watch?v=H6PLv9wZGTc&t=6s
2. La Farmacia en América
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Las investigaciones antropológicas y arqueológicas evidencian prácticas de medicina
hace más de 3.500 años en la América precolombina, una mezcla de medicina y ritos
sagrados que en muchas regiones superaron la conquista y colonización,
Son varios los aportes que las culturas Olmeca, Teotihuacana, Maya, Zapoteca, Inca y
Chibcha dieron a la medicina de la Europa conquistadora, muchas de las comisiones para
registrar los descubrimientos en América incluyen datos sobre técnica y plantas
medicinales, como la Historia general de las cosas de la Nueva España de Fray
Bernardino de Sahagún (1557), el códice escrito en latín Libelius de Medicinalibus
Indorum Herbis que recopila los métodos curativos del indígena Martin de la Cruz (1552),
la Historia natural y moral de los Incas de José Acosta (1600) y los estudios de la
Expedición botánica en la Nueva Granada por José Celestino Mutis.
Luego de las guerras de la independencia Latinoamericana a principios del siglo XX la
farmacia es básicamente magistral con principios activos que llegaban de Europa
principalmente y hacia 1930 se inicia la industrialización en varios países de la región con
inversión de empresas farmacéuticas europeas y norteamericanas, lo que genera
opciones para el crecimiento de la visita médica y la apertura de farmacias en varios
lugares donde incluso no existía la prestación de servicios médicos.
Luego de los años 50 del siglo XX los gobiernos incluyen a las farmacias como parte de la
asistencia social a través de los denominados seguros sociales, a partir de 1980 se inician
la inclusión de los medicamentos en las políticas de Estado, garantizando inicialmente la
disponibilidad, la eficacia y la calidad.
Bajo las directrices de la Organización Mundial de la Salud (OMS) y el apoyo de la
Organización Panamericana de la Salud (OPS) se inicia en el continente la construcción
de la Política Farmacéutica Nacional por país, que además del tema de la
farmacoeconomía incluye el uso racional y adecuado de los medicamentos, lo que
contempla la fijación y regulación de los precios.
A principios del siglo XXI la globalización llevó a una restructuración de la mayoría de las
industrias farmacéuticas en la región, se pasó de producción nacional a producción para
otras regiones, esto sumado a la fusión de varias empresas multinacionales y la
producción de medicamentos en la región asiática lo que influye en los precios de los
productos.
En la actualidad la farmacia en Latinoamérica va más allá de la producción y
comercialización de medicamentos, el ingreso de medicamentos genéricos ha llevado a
establecer mecanismos que permitan al usuario acceder a varias opciones de precio, lo
que ha requerido un rol activo del farmacéutico hacia la asistencia, donde la información y
la educación al paciente permitan lograr:
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
1. Promoción de la salud y estilos de vida saludables.
2. Información veraz sobre la calidad de los productos a partir de conceptos de
biodisponibilidad y bioequivalencia
3. Información al médico y al paciente sobre la disponibilidad de los medicamentos
4. Educación al paciente para el uso adecuado de medicamentos, especialmente en
grupos de pacientes y de moléculas de estrecho margen terapéutico.
5. Retroalimentación permanente a las redes locales y nacionales de
farmacovigilancia.
6. Acompañamiento al paciente para lograr una efectiva adherencia a la terapia.
7. Prevenir, detectar y corregir Problemas Relacionados con el Medicamento
8. Oferta de asistencia y atención farmacéutica.
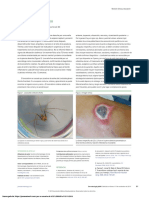
3. Símbolos de la Farmacia
La Copa de Higia y es el más utilizado por los Farmacéuticos en el mundo, posiblemente
desde 1796 cuando se acuñó por la Sociedad Parisina de Farmacia.
Desde el punto de vista comercial es común que la Farmacia se identifique en sus avisos
por una cruz griega verde, aunque también se observa el mortero y el pistilo acompañado
del carácter de receta R/, en Alemania se puede observar la A roja gótica, la “A” proviene
del término Apotheke.
La farmacia en nuestra región celebra su día el 1 de diciembre en conmemoración del 1er
Congreso Panamericano de la Farmacia realizado en la Habana Cuba en 1948 y donde
se crea la Federación Panamericana de la Farmacia.
La Federación Internacional Farmacéutica (FIP) acordó en el año 2009 establecer el 25
de septiembre como el DÍA INTERNACIONAL DEL FARMACÉUTICO, es importante
indicar que la denominación de Farmacéutico varía según el país, además del Químico
Farmacéutico existe también el título de Farmacéutico, Químico Farmacéutico Bioquímico
y Regente de Farmacia.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
En cada país se celebra adicionalmente el día del Farmacéutico y del personal auxiliar.
4. La Farmacia en Colombia
Colombia ya tenía algunas farmacias en la Colonia que las manejaban principalmente los
médicos y así continuó hasta inicios del siglo XX, era una farmacia de preparaciones
magistrales con principios activos importados principalmente de Europa.
Con la explotación de la quina se crearon algunos laboratorios farmacéuticos
principalmente en los Santanderes, entre ellos Laboratorios Román (1835) y Botica
Alemana (1863), los demás establecimientos producían magistrales para sus usuarios y
algunos comenzaron a vender a otras farmacias.
En 1913 con la Ley 33 se crea el Consejo Superior de Sanidad que luego se denomina
DIRECCIÓN NACIONAL DE HIGIENE Y ASISTENCIA PÚBLICA (ley 15 de 1925), que
tenía entre sus funciones la inspección de sustancias alimenticias, drogas y bebidas
alcohólicas.
En 1935 los farmacéuticos graduados lograron exclusividad del ejercicio con la Ley 44, a
los empíricos se les reconoció su labor a través de los “Diplomas de Licenciados”, la
mayoría de los farmacéuticos graduados estudiaban en Europa ya que solo hasta ese año
inició la Escuela de Farmacia de la Universidad Nacional que se denominó Facultad de
Farmacología y Farmacia.
En 1941 se crea la Escuela de Farmacia de la Universidad de Cartagena, en 1942 se creó
la Facultad de Química y Farmacia en el Instituto de Tecnología que existía en ese
entonces en Barranquilla que fue incorporado a la Universidad del Atlántico y en 1943
nace en la Universidad de Antioquia
Los “Diplomas de Licenciados” son reemplazados por una autorización con la Ley 84 de
1946, estos licenciados seguían siendo empíricos, la mayoría eran aprendices de las
farmacias.
La segunda guerra mundial hizo que se promoviera la industria farmacéutica nacional
ante la dificultad de importar productos europeos, Los Farmacéuticos universitarios se
dedican a la producción de medicamentos por lo que se permite a las personas que
demostraran práctica en la venta de medicamentos, no se requiere formación académica.
(Decreto 124 de 1954)
En 1967 el Dr. Antonio Mesa propone en la Universidad de Antioquia el programa de
REGENCIA DE FARMACIA, entre sus reflexiones indica:
“Todos los días más comercializada, más "tienda" y más viciada. Grandes escándalos
como falsificaciones, cambios de etiquetas, venta de muestras gratis, comercio de
estupefacientes, etc., era comidilia diaria".
Se requería de un profesional que se formara exclusivamente para la Farmacia con una
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
duración menor en sus estudios y con una consigna: Recuperar la Farmacia, por la salud
del pueblo".
Ese año inicia la carrera intermedia de Regencia de Farmacia en la Universidad de
Antioquia, reconocida por la Ley 47 de 1967 que la establece como profesión auxiIIar de
la Química Farmacéutica.
Para inicio de la década de 1970 los Químicos Farmacéuticos ejercían principalmente en
la industria farmacéutica y los nuevos Regentes de Farmacia comenzaron a ejercer en las
farmacias hospitalarias y entrega de medicamentos de Instituto de Seguros Sociales, la
ausencia de farmacéuticos en las farmacias comunitarias motivó en 1971 la Ley 8,
autoriza a los empíricos para manejar establecimientos farmacéuticos y se denominan
Directores de Droguería. En 1974 la ley 17, autoriza a los Expendedores de Drogas
Para finales del siglo XX hay dos grandes sucesos que serían el inicio de la nueva
farmacia en Colombia, para 1993 se emite la Ley 100 del Sistema de Seguridad Social,
que conlieva a la creación del Instituto Nacional de Vigilancia de Medicamentos y
Alimentos INVIMA y se da apertura económica lo que permite la importación de
medicamentos, principalmente moléculas en presentación de genéricos y copias.
Ante la necesidad de contar con personal idóneo varias universidades inician el programa
de Regencia de Farmacia en varias regiones del país, entre ellos la Escuela de Química
Industrial hoy Corporación Tecnológica de Bogotá (1977), Universidad Industrial de
Santander (1986), Universidad Nacional Abierta y a Distancia (1994), Universidad de
Córdoba (1995), Universidad Pedagógica y Tecnológica de Tunja (1998), Universidad
Mariana (1999), Universidad de Caldas (2000)
Para 1998 se separa la Regencia de Farmacia de la Química Farmacéutica y se
especializa la investigación, producción, distribución, dispensación de productos
farmacéuticos.
En el 2003 se emite la Política Farmacéutica Nacional, para el 2012 se emite el Conpes
155 con la nueva Política Farmacéutica Nacional
En el 2005 se reglamenta el Servicio Farmacéutico a través del Decreto 2200 y se define
como:
“Es el servicio de atención en salud responsable de las actividades, procedimientos e
intervenciones de carácter técnico, científico y administrativo, relacionados con los
medicamentos y los dispositivos médicos utilizados en la promoción de la salud y la
prevención, diagnóstico, tratamiento y rehabilitación de la enfermedad, con el fin de
contribuir en forma armónica e integral al mejoramiento de la calidad de vida individual y
colectiva”.
En ese decreto se establece el Modelo de Gestión del Servicio Farmacéutico que se
implementa en la Resolución 1403 de 2007.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
En el año 2005 a través del Decreto 3616 se establecen se establecen las
denominaciones de los auxiliares en las áreas de la salud, se adoptan sus perfiles
ocupacionales y de formación, los requisitos básicos de calidad de sus programas, es en
esta norma donde se crea el AUXIIIAR EN SERVICIOS FARMACÉUTICOS.
La farmacia en Colombia tiene varios campos de acción según el tipo de servicio o de
establecimiento donde se realicen las actividades, desde el 2018 se inició la
implementación del SISTEMA DE GESTIÓN DE LA CALIDAD PARA
ESTABLECIMIENTOS FARMACÉUTICOS en la cual se busca que la farmacia en nuestro
país sea asistencial en cumplimiento de su definición y acorde a las sugerencias de la
Organización Mundial de la Salud.
Vídeo de apoyo
Historia de la Farmacia, Parte 2. Rony Condeña, EVILAF, 2017
https://www.youtube.com/watch?v=1M6KBQ51YXw&t=2s
Documentos de apoyo para consulta del estudiante
- DESARROLIO DE LOS SERVICIOS FARMACÉUTICOS EN COLOMBIA. Serie
Buscando Remedio, Equipo Fundación IFARMA. 2013
- UN VIAJE HISTÓRICO POR LA FARMACIA. María Teresa Narváez Eraso, Revista
UNIMAR. Universidad de Nariño.
- Caracterización Ocupacional del Sector Farmacéutico en Colombia, enfoque por
entornos. Mesa Sectorial de Salud. Servicio Nacional de Aprendizaje SENA. 2008
Bibliografía del tema
Redactado a partir del libro “Epopeya Farmacéutica, la Farmacia en el mundo antiguo”,
Luis Marcos Nogales, Ediciones Universidad Salamanca, febrero de 2012.
Información tomada de la página de la Universidad Central de Venezuela, disponible en
http://www.ucv.ve/estructura/facultades/facultad-de-farmacia/detalie-noticias-
farmacia/article/1o-de-diciembre-dia-panamericano-de-la-
farmacia.html?tx_ttnews%5BbackPid%5D=715&cHash=2bbea259f1 consultado el 17-01-
2018
Cortez-Galiardo, V., Macedo-Ceja, J. P., Hernández-Arroyo, M., Arteaga-Aureoles, G.,
Espinosa-Galván, D., & Rodríguez-Landa, J. F. (2004). Farmacognosia: breve historia de
sus orígenes y su relación con las ciencias médicas. Revista Biomédica, 15(2), 123-136.
Iñesta, A., & Oteo, L. A. (2011). La industria farmacéutica y la sostenibilidad de los
sistemas de salud en países desarrollados y América Latina. Ciência & saúde coletiva, 16,
2713-2724.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Debesa García, F. (2006). El farmacéutico y la salud pública. Revista Cubana de
Farmacia, 40(1), 0-0.
Federación Internacional Farmacéutica. https://www.fip.org/
- Ley 485 de 4998
- Ley 47 de 1967
- Decreto 780 de 2016
- Resolución 1403 de 2007
- Introducción a la Regencia de Farmacia, Augusto Ortega, UNAD 2006
- Proyecto educativo del Programa de Regencia de Farmacia. Omar Correa y otros.
UdeA
- Caracterización laboral del sector farmacéutico en Colombia, enfoque por entornos.
Mesa sectorial de salud, SENA, 2008
- Documentos plan de acreditación UFPS, UT y RED DE REGENTES DE
FARMACIA
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tema 2. NORMATIVIDAD GENERAL PARA EL SERVICIO FARMACÉUTICO
En este módulo revisaremos las Leyes, Decretos, Resoluciones y Acuerdos de mayor uso
en la Droguería, existen varias que son transversales a la actividad del servicio
farmacéutico y que el técnico en farmacia reforzará en el ejercicio de su profesión:
Constitución Política de Colombia, esta norma del año 1991 es la Ley Suprema ya que
ella se plasma todo lo referente a la organización de nuestro país, en el artículo 49 se
consagra el servicio a la salud, pero en la Ley 1751 de 2015 garantiza el derecho
fundamental a la salud, la regulariza y establece los mecanismos de protección.
El Decreto 2200 de 2005, hoy Decreto 780 de 2016 DECRETO ÚNICO
REGLAMENTARIO DEL SECTOR SALUD Y PROTECCIÓN SOCIAL del Ministerio de
Salud y Protección Social, reglamenta el Servicio Farmacéutico al considerarlo un Servicio
de Atención en Salud y tiene en cuenta elementos como: los procesos del servicio
farmacéutico, la prescripción de medicamentos, la distribución y dispensación de
medicamentos, el Comité de Farmacia y Terapéutica, la información de los
medicamentos, la inspección, vigilancia y control.
Ahora observemos las normas según el campo de aplicación:
1. El ejercicio de la Farmacia
En Colombia pueden trabajar en Farmacia personal con formación académica y personas
que acreditan su experiencia:
- Químico Farmacéutico, es un profesional universitario reglamentado por la ley 212
de 1995, ejerce como Director Técnico en todos los servicios farmacéuticos.
- Regente de Farmacia, es un tecnólogo universitario reconocido por la Ley 485 de
1998, ejerce como Director Técnico en servicio farmacéutico de baja complejidad,
establecimientos farmacéuticos mayoristas siempre que no haya reempaque o
reenvase, en Farmacia Droguería siempre que no haya preparación de magistrales
estériles, Droguería y Farmacia Homeopática nivel I, también ejerce en servicios
farmacéuticos de mediana y alta complejidad como responsable de áreas.
- Expendedor de Drogas, es una persona a la que se le reconoce 10 años mínimo de
experiencia a través de la Ley 17 de 1974, puede ser Director Técnico en
Droguerías.
- Auxiliar en Servicios Farmacéuticos, es un técnico laboral por competencias
reconocido por el Decreto 3616 de 2005, no puede ser Director Técnico.
Hay casos excepcionales que le permiten al médico ser Director Técnico temporal en
casos de no encontrarse recurso humano, Decreto 1970 de 1990, para las Tiendas
Naturistas se puede trabajar en ellas con un entrenamiento en el manejo de estas según
lo establece la Resolución 0126 de 2009.
2. Los Establecimientos Farmacéuticos
El Decreto 780 de 2016 establece los siguientes establecimientos Farmacéuticos:
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
- Dependientes de una IPS: Farmacias Hospitalarias según la complejidad de la
institución y Ambulatorios, estos últimos pueden ser prestados por Farmacias
Droguerías y Droguerías.
- Independientes o Establecimientos Farmacéuticos, que a su vez se dividen en
mayoristas (laboratorios que distribuyen, agencias de especialidades y depósitos
de drogas) y minoristas (Farmacia Droguería y Droguería).
El Decreto 1737 de 2005 establece desde la preparación hasta la comercialización de
medicamentos homeopáticos a través de Farmacias Homeopáticos (nivel I y II, estas
últimas pueden realizar preparaciones homeopáticas magistrales y oficinales)
La Resolución 0126 de 2009 establece las condiciones para la venta de medicamentos
fitoterapéuticos y homeopáticos de venta libre a través de las Tiendas Naturistas.
La Resolución 2003 de 2014 establece las condiciones para la habilitación de servicios
farmacéuticos en Instituciones Prestadoras de Servicios de Salud.
El Decreto 4664 de 2006 permite a los médicos que ejercen terapias alternativas a
realizar preparaciones magistrales en su establecimiento.
En el Decreto 3050 de 2005 se permite la comercialización de medicamentos de venta
libre en establecimientos de gran superficie.
3. Control de los Establecimientos Farmacéuticos
La máxima autoridad en la vigilancia de productos farmacéuticos y establecimientos es el
INSTITUTO NACIONAL DE VIGILANCIA DE MEDICAMENTOS Y ALIMENTOS, INVIMA,
creado por el artículo 245 de la Ley 100 de 1993, posteriormente el Decreto 1290 de 1994
establece las funciones y organización, en el 2004 a través del Decreto 211 se restructuró
la entidad y en la Ley 1122 de 2007 se respalda su función como ente superior. El INVIMA
es el responsable de la emisión de Registros Sanitarios.
Para el manejo de los Medicamentos de Control Especial y Monopolio del Estado se
establece la UNIDAD ADMINISTRATIVA ESPECIAL DEL FONDO NACIONAL DE
MEDICAMENTOS, reglamentado por el Decreto 1478 de 2006.
Las Secretarías e Institutos de Salud Departamentales pueden realizar visitas de
Inspección, Vigilancia y Control, así como las dependencias municipales que se
establezcan para tal fin.
4. Los medicamentos y los dispositivos médicos
El Decreto 677 de 1995 reglamenta el régimen de registros y licencias, así como el control
de calidad de los medicamentos.
El Decreto 1737 de 2005 establece las condiciones para el manejo de los medicamentos
homeopáticos magistrales y oficinales.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
El Decreto 2266 de 2004 establece las condiciones de los productos fitoterapéuticos.
El Decreto 4725 de 2005 establece las condiciones de los dispositivos médicos
La Resolución 1478 de 2006 establece las condiciones de los Medicamentos de Control
Especial y Monopolio del Estado y el Decreto 0315 de 2020 que actualiza el listado de
medicamentos de control especial y monopolio del Estado.
El Decreto 3050 de 2005 establece las condiciones para el expendio de los
medicamentos.
5. Procesos del Servicio Farmacéutico
El Decreto 780 de 2016 establece los procesos del servicio farmacéutico, posteriormente
se establece el modelo de gestión del servicio farmacéutico a través de la Resolución
1403 de 2007.
Para los servicios farmacéuticos dependientes de una Institución Prestadora de Servicios
de Salud se aplican los estándares de habilitación contemplados en la Resolución 3100
de 2019.
6. Turnos de Farmacias y Droguerías
Aunque no se aplica en las ciudades que cuentan con servicio de farmacias
independientes que tienen horario 24 horas, en los sitios donde no las hay, la autoridad
local debe establecer turnos de atención al público y que está contemplado en el Decreto
2169 de 1949.
7. Preparaciones Magistrales y Droga Blanca
Las preparaciones magistrales están contempladas en la Resolución 1403 de 2007, los
productos denominados DROGA BLANCA que son aquellos utilizados como materia
prima en la elaboración de preparaciones magistrales se encuentran contemplados en la
Resolución 243630 de 1999.
Las preparaciones magistrales, los medicamentos homeopáticos magistrales y oficinales y
la droga blanca no requiere registro sanitario para su comercialización, se debe realizar su
mercadeo en lugares autorizados para esa condición.
8. Servicio de inyectología y glucometría en droguerías
El Decreto 780 de 2016 establece las condiciones para la prestación del servicio de
inyectología por vía intramuscular y la glucometría por punción con equipo portátil en
droguerías.
9. Publicidad y promoción de medicamentos
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
La información que puede estar contenida en las cajas y etiquetas de los productos
farmacéuticos está contemplado en las siguientes normas
- Código sanitario Ley 9 de 1979
- Medicamentos Decreto 677 de 1995
- Productos fitoterapéuticos y homeopáticos de venta libre, Resolución 4320 de 2004.
- Productos Fitoterapéuticos de venta bajo formula, Decreto 2266 de 2004
- Medicamentos homeopáticos, Decreto 3554 de 2004
- Dispositivos Médicos: Decreto 4725 de 2006
- Suplementos Dietarios, Decreto 3249 de 2006
10. Decreto único reglamentario del Sector Salud y Protección Social
Ante la cantidad de normas que se aplican a los diferentes ámbitos de la salud, se hizo
necesario unificarlas a través del Decreto 780 de 2016 que es un decreto compilatorio y
toma como referencia las normas expuestas anteriormente.
Vídeo de apoyo
Introducción al Servicio Farmacéutico. Fabio Alberto González Salgado. 2016
https://www.youtube.com/watch?v=U6_xe5SE5bY
Prestación del Servicio Farmacéutico. Fabio Alberto González Salgado. 2013
https://www.youtube.com/watch?v=ydyFdeX7l0U&t=4s
Resolución 3100 de 2019. Johan Tapiero. 2020
https://www.youtube.com/watch?v=Qf7exy6R0r0
Documentos de apoyo para consulta del estudiante
- Decreto 780 de 2016. Capítulo 10, Droguerías y Servicio Farmacéutico.
- Resolución 10911 del 1992, Requisitos para Droguerías
- Decreto 1950 de 1964. Dirección Técnica.
Bibliografía del tema
- Constitución Política de Colombia, 1991
- Decreto 1290 de 1994
- Decreto 1478 de 2006
- Decreto 1737 de 2005
- Decreto 1970 de 1990
- Decreto 2169 de 1949
- Decreto 2266 de 2004
- Decreto 2330 de 2006
- Decreto 3050 de 2005
- Decreto 3249 de 2006
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
- Decreto 3554 de 2004
- Decreto 3616 de 2005
- Decreto 4664 de 2006
- Decreto 4725 de 2005
- Decreto 677 de 1995
- Ley 1122 de 2007
- Ley 17 de 1974
- Ley 1751 de 2015
- Ley 212 de 1995
- Ley 485 de 1998
- Ley 9 de 1979
- Resolución 0126 de 2009
- Resolución 1403 de 2007
- Resolución 3100 de 2019
- Resolución 4320 de 2004
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tema 3. PRINCIPIOS DE FARMACOLOGÍA
1. Farmacología
La Farmacología es la ciencia que estudia el origen, las acciones, los efectos bioquímicos
y fisiológicos, las propiedades y el uso terapéutico de las sustancias que interactúan sobre
los organismos vivos.
La Farmacocinética en términos generales podemos decir que es lo que el organismo le
hace al medicamento, esos pasos se conocen como LADME (Liberación, Absorción,
Distribución, Metabolismo y Excreción).
La Farmacodinamia es el estudio de los efectos bioquímicos y fisiológicos de los fármacos
y de sus mecanismos de acción en relación entre la concentración del fármaco y el efecto
de este sobre un organismo, en otras palabras, es lo que el medicamento le hace al
organismo.
En Farmacología debemos tener algunos conceptos básicos como:
Absorción: Una vez liberado de la forma farmacéutica el fármaco debe absorberse para
ser utilizado por el organismo.
Biodisponibilidad: es la cantidad y la velocidad a la que un principio activo se absorbe a
partir de una forma farmacéutica.
Bioequivalencia: es un término de farmacocinética para evaluar comparativamente la
equivalencia terapéutica entre dos medicamentos con el mismo principio activo en el
mismo organismo.
Distribución: El medicamento una vez se absorbe debe distribuirse para hasta liegar el
lugar de acción, o sea el sitio donde debe funcionar.
Dosis: Es la calidad de un medicamento que se administra para lograr eficazmente un
efecto determinado.
Efecto colateral: son efectos indeseados consecuencia directa de la acción principal del
medicamento.
Efecto indeseado: cuando el medicamento produce otros efectos que pueden resultar
indeseados con las mismas dosis que se produce el efecto terapéutico;
Efecto placebo: son manifestaciones que no tienen relación con alguna acción realmente
farmacológica.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Efecto primario: es el efecto fundamental terapéutico deseado del fármaco.
Efecto secundario: son efectos independientes de la acción principal del fármaco.
Excreción: La eliminación de los fármacos o de sus metabolitos se realiza por las vías de
excreción del organismo siendo el más común la orina.
Farmacoepidemiología: El estudio del uso de los medicamentos y sus efectos en grandes
poblaciones.
Farmacognosia: Es el estudio del estudio de las drogas y principios activos de origen
natural, vegetal, microbiano y animal.
Farmacotecnia: también conocida como tecnología farmacéutica y consiste en
comprender los medios y procesos que se llevan a cabo en la fabricación de
medicamentos y productos farmacéuticos.
Farmacovigilancia: En el 2002 la OMS la define como la ciencia que trata de recoger,
vigilar, investigar y evaluar la información de los efectos de los medicamentos, productos
biológicos, plantas medicinales, y medicinas tradicionales, con el objetivo de identificar
información sobre nuevas reacciones adversas y prevenir los daños en los pacientes.
Indicación y contraindicación: La indicación es para lo que se puede emplear un
medicamento, las indicaciones de los medicamentos los establecen las autoridades
sanitarias. Una contraindicación es una situación específica en la cual no se debe utilizar
un fármaco.
Interacción: Es una reacción entre dos o más medicamentos o entre un medicamento y un
alimento o bebida, también puede ocurrir entre la interacción entre un medicamento y el
estado de salud del paciente.
Liberación: Los medicamentos se presentan en una forma farmacéutica que es aquella
que utilizamos para administrarlos, una vez administrados los principios activos se deben
liberar de la forma farmacéutica para ser absorbidos por el organismo. Algunos productos
no requieren liberación.
Metabolismo: Se conoce como metabolismo el conjunto de procesos físicos y químicos
que suceden en un organismo, el hígado es uno de los principales órganos del
metabolismo de los fármacos, el paso por el hígado también se conoce como
metabolismo de primer paso.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Receptores: Los medicamentos ejercen su acción sobre una célula debido a receptores
sobre la superficie celular, estos receptores se clasifican en dos grupos:
1. Agonistas: El fármaco produce un efecto combinándose y estimulando al
receptor. Estos agonistas pueden ser completos, parciales o inversos.
2. Antagonistas: Acá el fármaco produce un efecto bloqueando al receptor y siendo
capaz de reducir los efectos de los agonistas. Pueden ser reversibles o
irreversibles.
2. El Medicamento.
Se puede definir medicamento como aquél preparado farmacéutico obtenido a partir de
principios activos, con o sin sustancias auxiliares, presentado bajo forma farmacéutica
que se utiliza para la prevención, alivio, diagnóstico, tratamiento, curación o rehabilitación
de la enfermedad.
Hay otras definiciones según el tipo de medicamentos como: medicamento esencial,
medicamento nuevo, medicamento homeopático, preparaciones farmacéuticas con base
en plantas medicinales, producto fitoterapéutico, medicamento genérico y medicamento
bioequivalente.
Otros elementos que forman parte esencial de un medicamento son: el envase para
garantizar la calidad, la presentación comercial, la etiqueta con la información, el registro
sanitario, el lote de producción, la fecha de caducidad y los datos del laboratorio
fabricante; si el producto de es de venta libre tiene información adicional de uso en la
etiqueta.
Los medicamentos tienen varios orígenes, pueden extraerse de plantas, otros vienen de
los animales y algunos son minerales, la industria farmacéutica aplica la biotecnología
para elaborar nuevos fármacos.
3. Clasificación de los medicamentos
Hay varias maneras de clasificar los medicamentos y se aplican según la necesidad,
observemos la más utilizadas:
1. Según su condición de dispensación: Se clasifican en: medicamentos de venta bajo
prescripción u orden médica, medicamentos de venta libre, medicamentos de uso
institucional, medicamentos de control especial y/o monopolio del Estado.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
2. Según el uso en el sistema de salud: Se presentan los medicamentos de forma práctica
para ser consultados por los profesionales de la salud, incluidos en los listados
institucionales y se organizan así:
- Programas Especiales, que cubren enfermedades que afectan la salud pública, allí se
encuentran los esquemas de vacunación, por ejemplo.
- Uso Ambulatorio, que hace referencia a los medicamentos que el paciente utiliza en su
casa de forma autónoma y bajo su responsabilidad.
- Principios activos de uso hospitalario, productos farmacéuticos utilizados durante la
estancia del paciente en las instituciones de salud y que son administrados por un
profesional.
- Principios activos para uso especializado, entre los que encuentran los medicamentos
para el cáncer, VIH – SIDA, hemodiálisis y trasplante de órganos, entre otros.
Cada grupo se encuentra según la clasificación ATC (Anatomical, therapeutic, chemical
classification system) o Anatómico, Terapéutico, Químico, que organiza según los grupos
terapéuticos en 14 grupos básicos así:
Sistema digestivo y metabólico;
Sangre y órganos hematopoyéticos;
Sistema cardiovascular;
Medicamentos dermatológicos;
Aparato genitourinario y hormonas sexuales;
Preparados hormonales sistémicos;
Antiinfecciosos en general para uso sistémico;
Agentes antineoplásicos e inmunomoduladores;
Sistema musculo esquelético;
Sistema nervioso;
Productos antiparasitarios;
Sistema respiratorio;
Órganos de los sentidos.
3. Según su condición de almacenamiento: son medicamentos con una condición especial
de almacenamiento, entre ellos están: temperatura ambiente, cadena de frío,
medicamentos higroscópicos, medicamentos fotosensibles, medicamentos barbitúricos.
4. Según la terapia: Además de la alopatía existe otras medicinas denominadas
alternativas, como la homeopatía, acupuntura, fitoterapia, ayurveda, medicina tradicional
china y algunos tratamientos indígenas.
5. Según su forma de producción: Se encuentran los medicamentos elaborados en
producción masiva en laboratorios farmacéuticos y los medicamentos extemporáneos
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
preparados para un paciente específico, también conocidos como preparaciones
magistrales, este último concepto aplica también para la preparación de nutriciones
enterales y parenterales.
6. Clasificación VEN: En este grupo se clasifican los medicamentos en: Vitales,
Esenciales, No esenciales.
Vídeos de apoyo
Introducción a la farmacología. Enfermera.com
https://www.youtube.com/watch?v=MpOPIJ-ENHI
Farmacocinética. Absorción. Enfermera.com
https://www.youtube.com/watch?v=toeSvvO3kTU
Farmacocinética. Distribución. Enfermera.com
https://www.youtube.com/watch?v=lO68EqrDs9o
Farmacocinética. Metabolismo. Enfermera.com
https://www.youtube.com/watch?v=TD1t8LjMC3Q
Farmacocinética. Excreción. Enfermera.com
https://www.youtube.com/watch?v=KwoaHqVkHrM
Vías de administración de fármacos. Enfermera.com
https://www.youtube.com/watch?v=G6yM39mZCBw
Mecanismos generales de acción de los fármacos. Enfermera.com
https://www.youtube.com/watch?v=tiUaECK_IPM
Reacciones adversas. Enfermera.com
https://www.youtube.com/watch?v=NbyZMle9oN0
Seguridad en el uso de los medicamentos. Enfermera.com
https://www.youtube.com/watch?v=is2zgyY0_CE
Documentos de apoyo para el estudiante
- Manual de Conocimientos Básicos de Farmacología. Sergio Alberto Viruete.
Universidad de Guadalajara, 2015
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tema 4. LA DISPENSACIÓN
1. Definición
Es la entrega de uno o más medicamentos y dispositivos médicos a un paciente o su
cuidador, con la información sobre su uso adecuado, realizada por el Farmacéutico o
persona legalmente autorizada.
La dispensación de medicamentos es la acción asistencial más importante en las
actividades de la farmacia ya que refuerzan la información impartida por el médico, debe
servir para despejar dudas del paciente, apoya la adherencia a la terapia y previene,
detecta y corrige problemas relacionados con los medicamentos.
A continuación, conoceremos los elementos claves para una buena dispensación.
2. La comunicación como base de la dispensación
La comunicación es la principal herramienta de la dispensación ya que es allí donde se
logra la atención del paciente y por ende se inicia la actividad educativa.
La comunicación debe ser eficaz, sencilia y resolutiva, sin embargo, no todo lo que se
dice es todo lo que se percibe, existe un embudo en donde la comunicación se decanta y
puede causar distorsiones:
Se parte de una idea la cual ser quiere comunicar, o sea lo que quiero decir
Según el medio que utilice, incluso el lenguaje o los gestos, puede existir una
manera como lo digo
Según ese medio o el estado de atención pueden existir cambios en lo que se oye
Según la forma como se capta el mensaje puede existir cambios en lo que
comprende quien recibe la información
En igual proporción puede existir variaciones en lo que la persona que escucha
logra retener.
Quien contesta, según su interpretación puede asumir una posición y se genera de
nuevo el ciclo.
La comunicación no es solo palabras, hay una comunicación con una influencia mayor y
que el dispensador debe tener en cuenta al momento de entablar relación con el paciente,
es la comunicación No Verbal.
En la dispensación la persona que la realiza debe tener en cuenta que lo importante es la
comprensión del paciente sobre la terapia, el medicamento y sobre todo sobre la
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
importancia del concepto de bienestar en su calidad de vida, para ello la comunicación
debe ser la base de su labor.
El dispensador debe estar atento y disponible, comprender que más importante que las
actividades administrativas y técnicas de la farmacia su atención se debe orientar
permanentemente hacia el paciente, su cuidador y la comunidad.
3. Características del Dispensador
La persona que realiza la dispensación debe comprender la importancia de esta actividad,
debe ir más allá del proceso mecánico y ubicarse en el rol de agente sanitario, por esto su
principal característica debe ser la imagen que proyecta, su pulcritud, su atención, su
interpretación de las necesidades del paciente y, ante todo, despejar dudas. Entre esas
características se encuentra hacerse corresponsable del tratamiento farmacoterapéutico.
Tenga en cuenta las siguientes recomendaciones:
1. Ser amable, no regañar al paciente ni hacerle gestos de mal gusto.
2. Conocer bien el área de almacenamiento.
3. Conocer perfectamente el listado de los productos que maneja la institución
o establecimiento para evitarle demoras al paciente.
4. Conocer las normas establecidas para prescripción y dispensación de los
medicamentos de control especial, al igual que el manejo y almacenamiento.
5. Estar capacitado para interpretar correctamente la fórmula médica.
6. Conocer y aplicar los elementos éticos de la dispensación de
medicamentos.
7. Ser completamente imparcial.
8. Tener vocación de servicio, no de vendedor.
9. Orientar al paciente y aconsejarlo para que no se automedique.
10. Ser discreto, no hacer comentarios de mal gusto sobre su posible
enfermedad.
4. Como Dispensar
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
En muchas farmacias el farmacéutico no logra atender a todas las personas, por esa
razón delega en el personal auxiliar parte de las actividades de dispensación.
A continuación, observaremos algunas generalidades al momento de dispensar.
1. Recepción del Usuario
La dispensación comienza por una comunicación efectiva, en ella la recepción del usuario
es importante, hay varios factores para tener en cuenta:
a. Imagen del establecimiento: La farmacia se debe considerar una extensión del
servicio de salud, su facilidad de acceso, la comodidad del área, la distribución de
los espacios, la publicidad, la exhibición y los servicios que se presten en ella
influyen en la recepción.
Es conveniente que al ingreso del establecimiento se ubique una placa con la
identificación del Director Técnico o Regente de la Farmacia, eso facilita la
interacción con los pacientes, en el interior debe destinarse un espacio para colocar
los títulos del personal que labora en el área.
b. Imagen del personal de farmacia: No hay una segunda oportunidad para dar
causar una primera impresión.
La imagen del personal de farmacia debe estar acorde a su labor como agente
sanitario.
El aspecto del personal sanitario debe proyectar salud, el cabello ordenado y
limpio, el maquillaje en las mujeres y el cuidado de la barba en los hombres son
también importantes; el uso de accesorios debe ser discreto para evitar molestias;
las uñas y manos limpias son también factores importantes; la utilización de
uniforme o bata es importante para proyectar la imagen personal, lo mismo que el
vestuario, de igual manera la identificación del personal que atiende.
c. El saludo: Saludar es el primer paso para lograr la atención del usuario y lograr que
exista una comunicación efectiva, se saluda desde el contacto visual, la sonrisa de
bienvenida y demostrar que estamos atentos a las inquietudes.
d. La atención. En la farmacia la atención a las necesidades del usuario es importante
para conocer sus expectativas. Evite distraerse con el uso de dispositivos como
teléfonos móviles o equipos de cómputo.
2. Evaluar la solicitud
Debemos recordar que dispensar no es solo entregar, por eso al momento de dispensar
se debe evaluar la solicitud, comenzando por determinar el tipo de medicamento, si es
venta libre o de prescripción médica.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
En las solicitudes de medicamentos de venta libre tenga en cuenta:
a. El usuario: Hay que determinar quién es el usuario, especialmente pacientes
pediátricos, madres gestantes o que estén lactando y adultos mayores, ya que
ellos pueden presentar mayores riesgos con el uso de los productos farmacéuticos
incluso siendo de venta libre.
b. Sintomatología: En la automedicación responsable es importante tener en cuenta
los síntomas, ya que en muchas ocasiones el paciente suele confundirlos y generar
otros problemas de salud.
c. Tiempo de la sintomatología: Hay que reconocer el tiempo que tienen dichos
síntomas, si superan los 3 días es necesaria la atención médica.
d. Medidas anteriores: Se debe considerar si el paciente ha recurrido a otras
alternativas.
e. Medicamentos para otras patologías: Con esto se evitan interacciones y posibles
reacciones adversas.
f. Tiempo de consumo del medicamento: Se debe constatar si el paciente ha
consumido el producto con anterioridad y durante cuando tiempo.
Recuerde que los medicamentos de venta libre están diseñados para el manejo de signos
y síntomas, no son tratamientos curativos, esto es importante comunicárselo al paciente.
En la solicitud de medicamentos de venta bajo prescripción médica, se debe cumplir la
normativa legal.
Tenga en cuenta que muchos usuarios buscan medicamentos que no son venta libre y
que no cuentan con la fórmula médica, es importante indicar al paciente la importancia de
presentar la orden médica para evitar equivocaciones.
3. Selección del Medicamento.
La selección del medicamento tendrá dos enfoques: venta libre o venta bajo prescripción.
En los medicamentos de venta libre, la selección que realice el paciente debe estar
acompañada por la orientación del farmacéutico, en todos los casos se debe indicar al
paciente los riesgos y los cuidados que deben tenerse.
En los medicamentos de venta bajo prescripción, hay que ofrecerle al paciente varias
opciones del mercado, considerando siempre que la forma farmacéutica puede incidir en
la absorción y en el efecto.
Se debe tener en cuenta aquellos medicamentos de estrecho margen terapéutico o que
tienen como condición los estudios de biodisponibilidad y bioequivalencia.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
4. Información al dispensar.
Dispensar debe considerarse como un acto profesional, la información es importante, por
eso al momento de dispensar se debe indicar:
a. Nombre genérico y comercial si lo tiene.
b. Concentración y forma farmacéutica.
c. Vía de administración.
d. Dosis y frecuencia.
e. Efectos secundarios, precauciones, interacciones.
f. Almacenamiento y conservación.
g. Duración del tratamiento y adherencia a la terapia.
h. El consejo de farmacia.
5. Acondicionamiento y entrega
Dispensar no solo es información, es también servicio, el momento de acondicionar la
entrega del producto tenga en cuenta:
a. Método para la preparación del producto, si lo requiere.
b. Fecha de vencimiento y tiempo de estabilidad una vez abierto.
c. Fraccionamiento si se requiere.
d. Embalaje y transporte.
6. Despedida
Despedirse además de ser un acto de cortesía, reforzará en el paciente la imagen de la
farmacia y nos permitirá retroalimentar la información.
En la despedida es importante hacer énfasis en la siguiente información:
a. Es un medicamento, consérvelo en un lugar fresco y seco
b. Manténgalo en un lugar lejos del alcance de los niños y pacientes con problemas
cognitivos
c. Una vez se suspenda o finalice el tratamiento hay que dar manejo adecuado a los
residuos, la farmacia debe orientar sobre dicho manejo.
d. Ante cualquier duda o si los síntomas persisten consulte con el farmacéutico o su
médico, no se automedique.
7. Documentación
La documentación que se maneja en la dispensación depende de actividades de tipo
administrativo, en los medicamentos de control especial como los psicotrópicos se debe
realizar registros de seguimiento, en todos los casos se debe cumplir con la normativa
legal.
5. Dispensación de medicamentos. Decreto 780 de 2016
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Artículo 2.5.3.10.2 DISPENSACIÓN. - Es la entrega de uno o más medicamentos y
dispositivos médicos a un paciente y la información sobre su uso adecuado realizada por
el Químico Farmacéutico y el Tecnólogo en Regencia de Farmacia. Cuando la dirección
técnica de la Droguería, o del establecimiento autorizado para la comercialización al detal
de medicamentos, esté a cargo de personas que no ostenten título de Químico
Farmacéutico o Tecnólogo en Regencia de Farmacia la información que debe ofrecer al
paciente versará únicamente sobre los aspectos siguientes: condiciones de
almacenamiento; forma de reconstitución de medicamentos cuya administración sea la vía
oral; medición de la dosis; cuidados que se deben tener en la administración del
medicamento; y, la importancia de la adherencia a la terapia.
Artículo 2.5.3.10.15. CARACTERÍSTICAS DE LA PRESCRIPCIÓN.
- Toda prescripción de medicamentos deberá hacerse por escrito, previa evaluación del
paciente y registro de sus condiciones y diagnóstico en la historia clínica, utilizando para
ello la Denominación Común Internacional (nombre genérico) y cumpliendo los siguientes
requisitos:
1. Solo podrá hacerse por personal de salud debidamente autorizado de acuerdo con su
competencia.
2. La prescripción debe ser en letra clara y legible, con las indicaciones necesarias para
su administración.
3. Se hará en idioma español, en forma escrita ya sea por copia mecanográfica, medio
electromagnético y/o computarizado.
4. No podrá contener enmendaduras o tachaduras, siglas, claves, signos secretos,
abreviaturas o símbolos químicos, con la excepción de las abreviaturas aprobadas por el
Comité de Farmacia y Terapéutica de la Institución.
5. La prescripción debe permitir la confrontación entre el medicamento prescrito y el
medicamento dispensado (en el caso ambulatorio) y administrado (en el caso hospitalario)
por parte del profesional a cargo del servicio farmacéutico y del Departamento de
Enfermería o la dependencia que haga sus veces.
6. La prescripción debe permitir la correlación de los medicamentos prescritos con el
diagnóstico.
7. La dosis de cada medicamento debe expresarse en el sistema métrico decimal y en
casos especiales en unidades internacionales cuando se requiera.
8. Cuando se trate de preparaciones magistrales, además de los requisitos de
prescripción, se debe especificar claramente cada uno de los componentes con su
respectiva cantidad.
ARTÍCULO 2.5.3.10.16. CONTENIDO DE LA PRESCRIPCIÓN.
- La prescripción del medicamento deberá realizarse en un formato el cual debe contener,
como mínimo, los siguientes datos cuando éstos apliquen:
1. Nombre del Prestador de Servicios de Salud o Profesional de la Salud que prescribe,
dirección y número telefónico o dirección electrónica.
2. Lugar y fecha de la prescripción.
3. Nombre del paciente y documento de identificación.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
4. Número de la historia clínica
5. Tipo de usuario (contributivo, subsidiado, particular, otro).
6. Nombre del medicamento expresado en la Denominación Común Internacional (nombre
genérico).
7. Concentración y forma farmacéutica.
8. Vía de administración.
9. Dosis y frecuencia de administración.
10. Período de duración del tratamiento.
11. Cantidad total de unidades farmacéuticas requeridas para el tratamiento, en números
y letras.
12. Indicaciones que a su juicio considere el prescriptor.
13. Vigencia de la prescripción.
14. Nombre y firma del prescriptor con su respectivo número de registro profesional.
Artículo 2.5.3.10.18. OBLIGACIONES DEL DISPENSADOR.
- Son obligaciones del dispensador:
1. Verificar que la prescripción esté elaborada por el personal de salud competente y
autorizado y que cumpla con las características y contenido de la prescripción,
establecidos en el presente decreto.
2. Verificar que las preparaciones: magistrales, extemporáneas, estériles; nutrición
parenteral; y, mezclas de medicamentos oncológicos, contengan en el rótulo o etiquetas
la información sobre el paciente hospitalizado o ambulatorio, según el caso; de la
preparación o de la mezcla; y, la firma del responsable.
3. Exigir la prescripción para aquellos medicamentos en los que aparezca en la etiqueta la
leyenda "Venta Bajo Fórmula Médica".
4. No dispensar y consultar al prescriptor cuando identifique en una prescripción posibles
errores, con el fin de no incurrir en falta contra la ética profesional.
5. Verificar y controlar que los medicamentos dispensados correspondan a los prescritos.
6. Informar al usuario sobre los aspectos indispensables que garanticen el efecto
terapéutico y promuevan el uso adecuado de los medicamentos, tales como: condiciones
de almacenamiento, cómo reconstituirlos, cómo medir la dosis, que cuidados debe tener
en la administración, interacciones con alimentos y otros medicamentos, advertencias
sobre efectos adversos, contraindicaciones y la importancia de la adherencia a la terapia.
Cuando la dirección técnica de la Droguería esté a cargo de persona que no ostente título
de Químico Farmacéutico o Tecnólogo en Regencia de Farmacia la información que debe
ofrecer al paciente está señalada en el artículo 2.5.3.10.3. del presente decreto.
7. Brindar a los usuarios pautas sobre el uso adecuado de los medicamentos de venta sin
prescripción facultativa o de venta libre.
8. Recibir la capacitación ofrecida por las entidades oficiales o de otros actores del Sector
Salud y/o capacitarse continuamente en los conocimientos teóricos y destrezas
necesarias en el ejercicio del cargo u oficio, a fin de ir aumentando progresivamente las
competencias laborales.
Artículo 2.5.3.10.19. PROHIBICIONES DEL DISPENSADOR.
- El dispensador no podrá:
1. Adulterar o modificar en cualquier forma la prescripción.
2. Cambiar el principio activo, concentración, forma farmacéutica, vía de administración,
frecuencia, cantidad y la dosis prescrita.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
3. Dispensar medicamentos alterados o fraudulentos.
4. Violar la reserva a que está obligado por razón de la función que desempeña.
5. Recomendar a los usuarios la utilización de medicamentos.
6. Tener muestras médicas de medicamentos.
7. Tener envases y empaques vacíos, en el servicio farmacéutico, o en aquellos
establecimientos farmacéuticos que no estén autorizados para realizarlos
8. Inducir al paciente o consumidor a la compra de un medicamento que reemplace o
sustituya al prescrito o al solicitado.
Vídeos de apoyo
- Red+ | Mueren dos menores en Bogotá por error en la dispensación de un
medicamento. 2020 https://www.youtube.com/watch?v=vjQERxmxUNU
- ¿Qué es la Dispensación de medicamentos? 2020
https://www.youtube.com/watch?v=SIDP6XI-EMc
- Alcanza frascos, un riesgo para la dispensación de medicamentos
https://www.youtube.com/watch?v=dUEtAjKCZr0
Documentos de apoyo para el estudiante
- ABC en el uso de los medicamentos. INVIMA 2014
- Acuerdo 228 de 2002. Listado básico de medicamentos.
- Listado de Medicamentos de Venta Libre – INVIMA
- Listado de Medicamentos de Estrecho Margen Terapéutico
- Listado de Medicamentos de Control Especial y Monopolio del Estado.
Bibliografía del módulo
Asistencia y Consejo Farmacéutico. González S, Fabio A. Asociación de Regentes de
Farmacia de Norte de Santander, ASORFANORS. Cúcuta (Colombia), 2007
Atención Farmacéutica: Principios y experiencias. Curso a distancia. Armando, Pedro;
Correa Saide, Viviana y colaboradores. Colegio de Farmacéuticos de la Provincia de
Córdoba. Córdoba (Argentina), 2001.
Buenas Prácticas de Dispensación. Asociación de Química y Farmacia de Uruguay.
Montevideo (Uruguay), 2006
El papel del farmacéutico en el sistema de atención de la salud: Atención Farmacéutica.
Informe d de la reunión de la Organización Mundial de la Salud. Tokio (Japón), 1993
Farmacia Nuevo Milenio, Cuadernos de Farmacia. Aguilar, María y colaboradores. SENA
y Grupo Editorial Mundo Médico. Bogotá (Colombia), 1999
Guía de Pautas Básicas en Atención Farmacéutica. Paura Andrea. Colegio de
Farmacéuticos de la Provincia de Buenos Aires. Buenos Aires (Argentina), 2001.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Identificación de problemas relacionados con la prescripción, dispensación y utilización de
medicamentos antigripales y analgésicos, AINE’s, en establecimientos farmacéuticos
(Cafam) de la ciudad de Bogotá, D. C. Sanchez B. José M; Cruz, Ana E; Leon, Luis F.
Universidad Nacional Abierta y a Distancia. Bogotá (Colombia) 2010.
Manual de la Nueva Farmacia. Rubio Gálvez, José. Editorial Diaz de Santos. Madrid
(España) 1999
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tema 5. LA AUTOMEDICACIÓN RESPONSABLE
La Organización Mundial de la Salud (OMS) definió el concepto de automedicación
responsable como aquel que comprende el uso de medicamentos por el consumidor para
prevenir y manejar desórdenes o síntomas autorreconocibles.
Por uso racional de los medicamentos se entiende su uso correcto y apropiado; para que
haya un uso racional, el paciente tiene que recibir el medicamento adecuado y la dosis
debida durante un periodo de tiempo suficiente, al menor costo para él y para la
comunidad.
Cuando se habla de automedicación hay dos términos que debemos tener en cuenta,
automedicación irresponsable y automedicación responsable.
La automedicación irresponsable es el acto por el cual los pacientes consiguen y utilizan
los medicamentos sin ninguna intervención por parte del médico (diagnóstico de la
enfermedad, prescripción o seguimiento del tratamiento). Constituye una decisión del
propio paciente, muchas veces aconsejados por amigos o familiares u otro tipo de
informaciones.
La automedicación responsable es la participación del farmacéutico ante la decisión
propia de un paciente de tratar sus síntomas con medicamentos de venta libre,
aconsejándolo en forma oportuna y orientándolo a que vaya al médico que corresponda.
Esta automedicación está ligada a síntomas, no a un diagnóstico médico.
1. Uso incorrecto de los medicamentos
La OMS calcula que más de la mitad de los medicamentos se prescriben, dispensan o
venden de forma inapropiada, y que la mitad de los pacientes no los toman
correctamente. Este uso incorrecto puede adoptar la forma de un uso excesivo,
insuficiente o indebido de medicamentos de venta con o sin receta.
Entre los problemas frecuentes se encuentran:
la polifarmacia (consumo de demasiados medicamentos);
el uso excesivo de antibióticos e inyecciones;
la prescripción no ajustada a directrices clínicas;
la automedicación inapropiada.
Sin embargo, la automedicación parece ser una alternativa adecuada para solucionar los
problemas del usuario, ya que permitiría el uso racional, informado y seguro de los
medicamentos de venta libre.
La institución ve en la automedicación responsable una fórmula válida de atención a la
salud en las sociedades desarrolladas, destacando que no se debe dejar a un lado el
estratégico papel del médico.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Los objetivos de la OMS, al proponer la automedicación responsable, son prevenir y tratar
síntomas y problemas menores de salud que no requieran consulta médica; reducir la
continua presión que tienen los servicios médicos para el alivio de esos problemas,
especialmente cuando los recursos son limitados; aumentar la disponibilidad de recursos
destinados a la atención de poblaciones rurales o distantes, donde el acceso a los
servicios médicos es difícil y ayudar a que los pacientes crónicos controlen su patología.
En la automedicación es importante considerar que el papel del profesional farmacéutico
a nivel internacional ha estado cambiando en las dos últimas décadas, siendo
orientadores responsables sobre el cuidado diario de la salud y una figura clave en la
cadena de provisión de medicamentos. Su educación y capacitación los prepara para
proporcionar información sólida acerca de estos productos.
También los desarrollos recientes de medicamentos nuevos más efectivos y considerados
adecuados para libre acceso por vía oral o tópica, y la reconsideración de los viejos por
seguridad reconocida, ponen al alcance de la población una gama interesante de
alternativas automanejables.
La industria farmacéutica tiene un trabajo preponderante, por eso debe proporcionar
medicamentos con altos estándares de seguridad, calidad y eficacia, que cumplen con
todos los requisitos legales de empaque y etiquetado, empleando en los prospectos
advertencias claras y toda la información necesaria para orientar al paciente y al
farmacéutico.
El peligro real de esta actitud son los efectos secundarios, incluso reacciones adversas,
que pueden causar en el paciente molestias adicionales como somnolencia, mareos, dolor
de cabeza, entre otros. En la mayoría de los casos, estas dolencias no son graves, pero
en otros, el daño puede ser fatal.
El efecto secundario funciona diferente en cada persona, de ahí que sea importante que
un médico que sepa detectar las debilidades y el historial clínico sea quien indique el
medicamento adecuado.
En la automedicación el usuario adquiere medicamentos sin necesidad de recurrir al
médico, para tratar molestias menores, estos medicamentos denominados de venta libre
(OTC por sus siglas en inglés o Especialidades Farmacéuticas Publicitarias EFP, para el
servicio de salud español), tienen un amplio margen de seguridad y han demostrado su
eficacia para algunas dolencias comunes tales como dolor, fiebre, resfriado, alergias
leves, entre otros.
Sin embargo, asalta la duda sobre si el usuario es la persona indicada para auto
medicarse o si es necesario que un profesional cercano lo asesore.
La primera pregunta al respecto debe ser: ¿sabe el usuario cuales son los síntomas de la
enfermedad para la cual adquiere los productos?
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
La segunda sería: ¿Es consciente el usuario del uso que debe darle al producto, el tiempo
del tratamiento, las condiciones del almacenamiento y sobre todo los consejos
adicionales?
Las respuestas son subjetivas y varían dependiendo de varios factores, entre ellos el
cultural, por eso sigue siendo tema de discusión sobre si estos productos deben
permanecer monopolizados por las farmacias o pueden comercializarse en otros
establecimientos como los supermercados y los almacenes de grandes superficies sin la
presencia de un farmacéutico.
La mayoría de los casos de automedicación ocurren debido a la recomendación que un
amigo o familiar hace de alguna medicina que a él le resultó. Sin embargo, no
necesariamente va a actuar de la misma manera en otro organismo, aunque los síntomas
parezcan los mismos.
La automedicación responsable está orientada a evitar una serie de riesgos potenciales y
obtener un beneficio en término de curación o alivio de síntomas. Para ello la labor del
farmacéutico es indispensable ya que ayuda al paciente a reconocer adecuadamente los
síntomas, reconduciéndolo al médico de ser necesario, además de educar al paciente en
el manejo de aspectos importantes en la dispensación tales como dosificación,
interacciones, efectos secundarios y adversos, alimentación, almacenamiento y, sobre
todo, le informará como valorar el resultado del tratamiento y qué hacer en caso de que
no sea el esperado.
Para el sistema sanitario la automedicación responsable es un mecanismo útil en la
búsqueda de la utilización óptima de los recursos médicos aminorando la sobrecarga de
los servicios de salud como consecuencia de tratamiento de enfermedades menores,
ayudando a prevenir y tratar afecciones que no requieren de consulta médica y a
satisfacer el deseo natural de la población a tener mayor control individual sobre las
decisiones que afecten su salud personal, pero así mismo un exceso del uso puede
provocar un retraso en la búsqueda de atención médica oportuna, un uso irracional y
hasta una resistencia bacteriana, en eso cumple una función importante el farmacéutico.
Esta labor debe ser práctica permanente en la farmacia, no solo por su impacto
económico y social sino por la ventaja que puede significarle a la salud pública, ya que
orienta debidamente al usuario hacia el sistema sanitario ahorrándole esfuerzos y costos
que pueden evitarse.
El apoyo del personal de farmacia de tener varias consideraciones que deben ser también
del paciente:
Primero que nada, es fundamental que se tenga bien clara la enfermedad que se padece
para no solicitar un medicamento equivocado. Luego, en la farmacia siempre se puede
consultar acerca de los efectos secundarios y del rendimiento que éste pueda tener.
Por otra parte, es necesario que se indague sobre la interacción que ese medicamento
pueda tener con otros medicamentos, plantas o alimentos; asimismo, leer
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
cuidadosamente las instrucciones puede significar la prevención de una reacción
negativa.
Con respecto a la dosis, no debe excederse de la recomendada por el farmacéutico o por
lo que dice en el instructivo, en él, también se explicita el tiempo que se puede tomar el
medicamento continuamente; este lapso no debe ser superado sin antes la
recomendación del médico. Si los síntomas persisten o surgen nuevos es mejor recurrir
donde un especialista.
Cuando se compre el medicamento es importante que se especifique en la farmacia
condiciones especiales, tales como presión arterial alta o baja, estado de embarazo,
deficiencias cardiacas, padecimientos crónicos como diabetes, hemofilia, y cualquier otra
circunstancia particular, pues éstas pueden afectar la reacción que se tenga a la
medicina.
Para evitarse mayores problemas de salud es importante que en cualquier caso fuera de
lo común, o ante la menor muestra de síntomas con los que no se esté familiarizado, se
recurra inmediatamente al doctor.
La automedicación puede causar daños irreversibles en la salud, por lo que es mejor no
practicarla ni tampoco inducir a otros a su práctica.
2. Consecuencia del uso inadecuado de medicamentos
El uso incorrecto de los medicamentos ocurre en todos los países, es nocivo para los
pacientes y constituye un desperdicio de recursos. Entre sus consecuencias se
encuentran:
La resistencia a los antimicrobianos. El uso excesivo de antibióticos aumenta la
resistencia a los antimicrobianos y el número de medicamentos que dejan de ser
eficaces para combatir las enfermedades infecciosas.
Las reacciones adversas a los medicamentos y los errores de medicación. Las
reacciones adversas a los medicamentos originadas por su uso erróneo o por
reacciones alérgicas pueden ser causa de enfermedad, sufrimiento y muerte.
El desperdicio de recursos. Un 10 a 40% de los presupuestos sanitarios nacionales
se gasta en medicamentos. La compra de medicamentos directamente por el
usuario puede causar graves dificultades económicas a los pacientes y a sus
familias. Si los medicamentos no se prescriben y usan adecuadamente, se
desperdician miles de millones de dólares de fondos públicos y personales.
La pérdida de confianza del paciente. El uso excesivo de medicamentos escasos
contribuye a menudo al agotamiento de existencias y al aumento de los precios
hasta niveles inasequibles, lo cual merma la confianza del paciente. Los malos
resultados sanitarios debidos al uso inadecuado de los medicamentos también
pueden reducir la confianza.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
3. Factores que contribuyen al uso incorrecto de los medicamentos
Falta de conocimientos teóricos y prácticos. Las dudas sobre el diagnóstico, la falta
de conocimientos de los prescriptores sobre los enfoques diagnósticos óptimos, la
inexistencia de información independiente, como pueden ser las directrices clínicas
y de oportunidades para efectuar un seguimiento de los pacientes o el temor a
posibles pleitos, son factores que contribuyen a la prescripción y dispensación
inadecuadas de los medicamentos.
Promoción de los medicamentos inapropiada y contraria a la ética por parte de las
empresas farmacéuticas. La mayoría de los prescriptores obtienen la información
sobre los medicamentos de las empresas farmacéuticas y no de fuentes
independientes, como las directrices clínicas, esto puede conducir a menudo al uso
excesivo. En algunos países está permitida la publicidad de medicamentos que
necesitan receta dirigida directamente al consumidor, lo cual puede llevar a los
pacientes a presionar a los médicos pidiéndoles medicamentos innecesarios.
Beneficios de la venta de medicamentos. En muchos países los minoristas
prescriben y venden medicamentos sin necesidad de receta. Cuanto más vendan
mayores serán sus ingresos, lo cual conduce al consumo excesivo de
medicamentos, y en particular de los más caros.
Disponibilidad de medicamentos sin restricciones. En muchos países la
prescripción de medicamentos como los antibióticos se hace libremente, sin
necesidad de receta, esto conduce al consumo excesivo, a la automedicación
inapropiada y a la inobservancia de los regímenes posológicos.
Sobrecarga de trabajo del personal sanitario. Muchos prescriptores apenas tienen
tiempo para dedicar a cada paciente, lo cual puede estar en el origen de
diagnósticos y tratamientos deficientes, en esas circunstancias, se basan en
hábitos de prescripción porque no tienen tiempo para actualizar sus conocimientos
sobre los medicamentos.
Medicamentos inasequibles. En lugares donde los medicamentos son inasequibles,
los pacientes pueden no comprar las cantidades necesarias para un tratamiento
completo o no comprar ningún medicamento en absoluto, en lugar de ello pueden
buscar alternativas como los medicamentos de calidad no garantizada adquiridos a
través de Internet u otras fuentes, o los medicamentos que han sido prescritos a
sus familiares o amigos.
Inexistencia de políticas farmacéuticas nacionales coordinadas. Las políticas
básicas recomendadas por la OMS para garantizar el uso apropiado de los
medicamentos solo se aplican en menos de la mitad de los países, dichas políticas
incluyen medidas e infraestructuras apropiadas para monitorizar y reglamentar el
uso de los medicamentos, y para capacitar y supervisar a los profesionales
sanitarios que realizan las prescripciones.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Vídeos de apoyo
- Automedicación responsable. Colegio de Farmacéuticos de Costa Rica
https://www.youtube.com/watch?v=2xYNbfXMQgU
- Peligros de la automedicación con antibióticos
https://www.youtube.com/watch?v=o7E2Xj5oBls
Documentos de apoyo para el estudiante
- LA AUTOMEDICACIÓN: UNA COSTUMBRE SIN CONTROL ADECUADO, QUE
ATENTA CONTRA LA SALUD Y LA CALIDAD DE VIDA DE LOS CIUDADANOS.
UNAD 2009
Bibliografía del tema
Ramírez Puerta, D., Larrubia Muñoz, O., Escorteli Mayor, E., & Martínez Martínez, R.
(2006). La automedicación responsable, la publicidad farmacéutica y su marco en la
Atención Primaria. Medicina de FamiIIa-SEMERGEN, 32(3), 117-124.
Marulanda, F. Á. T. (2002). Estudio sobre automedicación en la Universidad de Antioquia,
Medeliín, Colombia. Iatreia, 15(4), 242-247.
Kregar, G., & Filinger, E. (2005). ¿Qué se entiende por automedicación? Acta Farm.
Bonaerense, 24(1), 130-133.
Wirtz, V. J., Dreser, A., & Leyva, R. (2009). El debate sobre la automedicación. salud
pública de México, 51, 179-180.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
TEMA 6. MEDICAMENTOS DE CONTROL ESPECIAL Y MONOPOLIO DEL
ESTADO
La siguiente información corresponde a lo indicado en la Resolución 1478 de 2006 del
Ministerio de Protección Social
1. Definiciones
ABUSO: Es el uso indebido de drogas o medicamentos con fines no médicos.
ADICCIÓN O DROGADICCIÓN: Es la dependencia a una droga.
ATENCIÓN FARMACÉUTICA: Es la asistencia a un paciente o grupo de pacientes, por
parte del profesional Químico Farmacéutico, en el seguimiento del tratamiento
farmacoterapéutico, dirigida a contribuir con el médico tratante y otros profesionales del
área de la salud en la consecución de los resultados previstos para mejorar su calidad de
vida.
ESTABLECIMIENTO FARMACÉUTICO: Es el establecimiento dedicado a la producción,
almacenamiento, distribución, comercialización, dispensación, control o aseguramiento de
la calidad de los medicamentos, dispositivos médicos o de las materias primas necesarias
para su elaboración y demás productos autorizados por Ley para su comercialización en
dicho establecimiento.
ESTÁNDAR DE REFERENCIA: Son las sustancias utilizadas como patrones de
comparación en los test y ensayos oficiales de las farmacopeas.
ESTUPEFACIENTE: Es la sustancia con alto potencial de dependencia y abuso.
FONDO ROTATORIO DE ESTUPEFACIENTES: Es la Oficina encargada dentro de la
Secretaría, Instituto o Dirección de Salud a nivel departamental, que ejerce la vigilancia,
seguimiento y control a las entidades públicas, privadas y personas naturales que
procesen, manipulen, sinteticen, fabriquen, distribuyan, vendan, consuman, dispensen
sustancias sometidas a fiscalización y medicamentos que las contengan; así como
garantizar la disponibilidad de medicamentos Monopolio del Estado a través de la
dispensación y distribución en su jurisdicción y las demás funciones que le sean
asignadas por el Ministerio de la Protección Social, o la institución competente.
FRANJA VIOLETA: Es la característica que identifica a los medicamentos de control
especial.
MATERIA PRIMA DE CONTROL ESPECIAL O SUSTANCIA SOMETIDA A
FISCALIZACIÓN: Es toda sustancia cualquiera que sea su origen, que produce efectos
mediatos e inmediatos de dependencia psíquica o física en el ser humano; aquella que,
por su posibilidad de abuso, pueda tener algún grado de peligrosidad en su uso, o aquella
que haya sido catalogada como tal, en los convenios internacionales, por el Ministerio de
la Protección Social, o la Comisión Revisora del INVIMA. Dentro de éstas se incluyen los
estándares de referencia, patrones y reactivos.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
MEDICAMENTO SOMETIDO A FISCALIZACIÓN DE USO HUMANO O VETERINARIO:
Es el preparado farmacéutico obtenido a partir de uno o más principios activos de control
especial, catalogados como tal en las convenciones de estupefacientes (1961),
precursores (1988) y psicotrópicos (1971), o por el Gobierno Nacional, con o sin
sustancias auxiliares presentado bajo forma farmacéutica definida, que se utiliza para la
prevención, diagnóstico, tratamiento, curación o rehabilitación de las enfermedades de los
seres vivos.
MONOPOLIO DEL ESTADO: Derecho poseído de exclusividad por el Estado.
PRECURSOR QUÍMICO: Es la sustancia o mezcla de sustancias a partir de las cuales se
producen, sintetizan u obtienen drogas que crean dependencia.
PREVENCIÓN: Conjunto de actividades encaminadas a reducir y evitar el mal uso de
sustancias y medicamentos que puedan causar dependencia.
PREVISIÓN: Cupo asignado de sustancias o productos sometidos a fiscalización que
podrán importar las entidades públicas o privadas o personas naturales previa
autorización de la U.A.E. Fondo Nacional de Estupefacientes.
PRINCIPIO ACTIVO: Compuesto o mezcla de compuestos que tienen acción
farmacológica.
RECETARIO OFICIAL: Documento oficial autorizado por la entidad competente, de
carácter personal e intransferible que utilizan los prescriptores de salud para la
formulación de los medicamentos de control especial y de Monopolio del Estado.
SERVICIO FARMACÉUTICO: Es el servicio de atención en salud responsable de las
actividades, procedimientos e intervenciones de carácter técnico, científico y
administrativo, relacionado con los medicamentos y los dispositivos médicos utilizados en
la promoción de la salud y la prevención, diagnóstico, tratamiento y rehabilitación de la
enfermedad, con el fin de contribuir en forma armónica e integral al mejoramiento de la
calidad de vida individual y colectiva.
SINTETIZAR: Formación artificial de un cuerpo compuesto mediante la combinación de
sus elementos.
SUSTANCIA PSICOTRÓPICA: Es la droga que actúa sobre el sistema nervioso central
produciendo efectos neuro - psicofisiológicos.
2. Manejo de sustancias sometidas a fiscalización
Para el manejo de las sustancias sometidas a fiscalización, medicamentos o cualquier
otro producto que las contengan, existen las siguientes modalidades de inscripción:
importación, exportación, compra y venta local, distribución mayorista nacional,
fabricación y acondicionamiento de sustancias sometidas a fiscalización y/o productos
que las contengan, éstas se tramitarán únicamente ante la U.A.E. Fondo Nacional de
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Estupefacientes del Ministerio de la Protección Social. La U.A.E. Fondo Nacional de
Estupefacientes informará a los Fondos Rotatorios de Estupefacientes sobre las
inscripciones realizadas de competencia de su jurisdicción.
Para las modalidades de dispensación, distribución minorista o mayorista de
medicamentos de control especial dentro de un mismo departamento, la inscripción se
realizará en cada uno de los Fondos Rotatorios de Estupefacientes de las Direcciones
Institutos o Secretarias Departamentales de Salud.
Las farmacias–droguerías, droguerías, depósitos de drogas, agencias de especialidades
farmacéuticas: Deben allegar la siguiente documentación:
1. Solicitud firmada por el representante legal o su apoderado debidamente facultado,
adjuntando el respectivo poder.
2. Listado de medicamentos sometidos a fiscalización indicando: nombre del
medicamento expresado en la Denominación Común Internacional, concentración y forma
farmacéutica.
3. Las entidades públicas presentarán copia del acto administrativo mediante el cual se
creó, copia del acto administrativo de nombramiento y acta de posesión del
Representante Legal.
4. Acta de la visita efectuada por las Direcciones Institutos o Secretarias Departamentales
de Salud, con fecha no mayor a un (1) año, con evaluación de condiciones mínimas para
el manejo de medicamentos sometidos a fiscalización, de acuerdo con la normatividad
vigente.
5. Fotocopia de la tarjeta profesional y contrato del Químico Farmacéutico para Farmacias
- Droguerías, Droguerías, Depósitos de Drogas, Agencias de Especialidades
Farmacéuticas o el Certificado de Inscripción ante la Autoridad Sanitaria competente y
contrato en el caso del Tecnólogo en Regencia de Farmacia para Droguerías y Depósitos
de Drogas.
Los establecimientos veterinarios que realicen distribución y comercialización de
medicamentos sometidos a fiscalización se ceñirán a lo establecido en la presente
Resolución y deberán allegar copia del Acto Administrativo emitido por el ICA
La inscripción de que trata este capítulo tendrá una vigencia de cinco (5) años, siendo
renovables por periodos iguales previo estudio y concepto técnico de la U.A.E. Fondo
Nacional de Estupefacientes. La Renovación deberá solicitarse con tres (3) meses de
anticipación a la fecha de su vencimiento. Si en dicho término no se llegara a solicitar se
cancelará la inscripción de manera automática.
3. Requisitos para la inscripción
Todos los solicitantes de inscripción ante la UAE Fondo Nacional de Estupefacientes y/o
Fondos Rotatorios de Estupefacientes deberán cumplir con los siguientes requisitos:
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
1. Disponer de una infraestructura física debidamente adecuada que cuente con:
Área de almacenamiento. - Estará ubicada en un área debidamente adecuada y de
dimensiones determinadas por el volumen de las actividades y/o procesos que realicen.
Será independiente, diferenciada y señalada, debe permanecer limpia y ordenada.
Pisos. - Los pisos deben ser de material impermeable, resistente y contar con un
sistema de drenaje que permita su fácil lavado y limpieza.
Paredes. - Las paredes y muros deben ser impermeables, sólidos, de fácil limpieza y
resistentes a factores ambientales como humedad y temperatura.
Techos. - Los techos y cielo-rasos deben ser resistentes y de fácil lavado y limpieza.
Iluminación. - Debe poseer un sistema de iluminación natural o artificial que permita la
conservación adecuada e identificación de los medicamentos y un buen manejo de la
documentación.
Ventilación. - Debe tener un sistema de ventilación natural y/o artificial que garantice la
conservación adecuada de los medicamentos sometidos a fiscalización.
Condiciones de temperatura y humedad. - Debe contar con mecanismos que garanticen
las condiciones de temperatura y humedad relativa recomendadas por el fabricante
conforme con lo establecido en el proceso de recepción técnica y almacenamiento. Así
mismo debe llevar los registros permanentes de estas variables y utilizando para ello
termómetros, higrómetros o instrumentos que cumplan con dichas funciones,
respectivamente.
Criterios de almacenamiento. - Las sustancias y/o medicamentos sujetos a fiscalización
se almacenarán de acuerdo con la clasificación farmacológica y orden alfabético. El
almacenamiento de las sustancias sometidas a fiscalización y medicamentos de control
especial debe mantenerse bajo estrictas condiciones de seguridad.
Comunicaciones. - Contarán básicamente con los medios de comunicación siguientes:
servicio de teléfono, servicio de fax o trasmisión electrónica de datos e Internet.
2. Contar con una dotación constituida por equipos, instrumentos, bibliografía y materiales
necesarios para el cumplimiento de los objetivos de las actividades y/o procesos que se
realicen.
3. Teniendo en cuenta lo establecido en el artículo 21 del Decreto 2200 de 2005, el
recurso humano idóneo para el manejo de medicamentos de control especial se sujetará
a lo establecido en la presente norma.
4. En el evento en que la entidad no mantenga las condiciones mínimas exigidas en la
presente capitulo, de manera automática se procederá a la cancelación de la inscripción.
4. Recurso humano idóneo
Las Farmacias–droguerías, droguerías, depósitos de drogas, agencias de especialidades
farmacéuticas: La dirección técnica estará a cargo del Químico Farmacéutico o del
Tecnólogo en Regencia de Farmacia.
En los establecimientos farmacéuticos distribuidores de medicamentos sometidos a
fiscalización para uso veterinario la dirección técnica estará determinada según la
regulación del ICA.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
La dirección de las droguerías donde se manejen medicamentos de control especial
carentes de facilidades de acceso al recurso humano idóneo podrá ser ejercida por
Directores de Droguería, Farmacéuticos Licenciados o Expendedores de Drogas. Para lo
cual se deberá presentar Certificación expedida por la Secretaría, Instituto o Dirección
Departamental de Salud acerca de la no disponibilidad del recurso humano en su
jurisdicción.
Instituciones Prestadoras de Servicios de Salud: El Servicio Farmacéutico Dependiente
estará bajo la dirección del Químico Farmacéutico o Tecnólogo en Regencia de Farmacia,
teniendo en cuenta el grado de complejidad del servicio, así: Alta y Mediana complejidad:
Exclusivamente el Químico Farmacéutico. Baja complejidad: Químico Farmacéutico o
Tecnólogo en Regencia de Farmacia.
Establecimientos farmacéuticos que se encarguen de realizar una o más actividades y/o
procesos propios del servicio farmacéutico por cuenta de otra persona: Estarán bajo la
dirección de un Químico Farmacéutico o Tecnólogo en Regencia de Farmacia teniendo en
cuenta el grado de complejidad del Servicio prestado y la normatividad vigente.
Establecimientos dedicados a la importación, exportación, fabricación, compra y venta
local de sustancias sometidas a fiscalización y productos que las contengan la dirección
estará a cargo exclusivamente de un Químico Farmacéutico.
Los directores técnicos funcionarán diariamente en un horario suficiente para satisfacer la
demanda de servicios de los usuarios. El tiempo mínimo de permanencia sin excepción
será de ocho (8) horas diarias. Sin embargo, las entidades podrán prestar servicio
nocturno, debiendo contar con la presencia permanente de su director técnico o de un
trabajador de esta, debidamente capacitado y entrenado, encargado por dicho director y
bajo su responsabilidad.
Los directores técnicos deberán estar en la capacidad de ofrecer la información oportuna,
completa, veraz, independiente y de calidad sustentada en evidencia científica y/o técnica
sobre sustancias sometidas a fiscalización y de productos que las contengan
5. Distribución, venta y usos de medicamentos monopolio del Estado
La distribución y venta de los medicamentos Monopolio del Estado, se hará a través de la
U.A.E. Fondo Nacional de Estupefacientes del Ministerio de la Protección Social o por los
Fondos Rotatorios de Estupefacientes a nivel departamental, en caso excepcional se
realizará por los establecimientos que sean facultados por la U.A.E. Fondo Nacional de
Estupefacientes mediante acto administrativo.
En los departamentos si amerita el caso, se podrá autorizar la dispensación de los
medicamentos monopolio del Estado, previo el envío a la U.A.E. Fondo Nacional de
Estupefacientes para su aprobación de un oficio suscrito por el señor Gobernador
justificando y solicitando la autorización para suscribir un convenio con un tercero, con el
fin de que se tenga disponibilidad de los medicamentos monopolio del Estado.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Para el uso ambulatorio e intrahospitalario de medicamentos monopolio del Estado, las
EPS, ARS, Instituciones Prestadoras de Servicios de Salud, Establecimientos
Farmacéuticos, deben inscribirse en la U.A.E. Fondo Nacional de Estupefacientes o en los
Fondos Rotatorios de Estupefacientes a nivel departamental quien expedirá el
correspondiente acto administrativo.
En caso de que la Institución Prestadora de Salud no dispense los medicamentos
Monopolio del Estado, deberá solicitar permiso a la UAE Fondo Nacional de
Estupefacientes y/o Fondos Rotarios de Estupefacientes para suscribir un convenio con
un tercero con el fin de garantizar la disponibilidad de estos a sus usuarios.
La Institución Prestadora de Servicios de Salud, deberá allegar de inmediato copia del
convenio suscrito entre las partes a la UAE Fondo Nacional de Estupefacientes y/o
Fondos Rotarios de Estupefacientes con el objeto de legalizar la prestación del servicio
por parte del contratista, quien deberá ser inscrito por el contratante.
En el evento que un particular requiera de dichos medicamentos serán vendidos
directamente por la entidad facultada por la U.A.E. Fondo Nacional de Estupefacientes o
por los Fondos Rotatorios de Estupefacientes, de acuerdo con los requisitos y las
cantidades autorizadas en la presente Resolución. La dispensación, venta y entrega de
medicamentos Monopolio del Estado, se hará previa presentación de la prescripción
médica, quedando prohibido el despacho por correo.
En los casos de cambio de terapia o fallecimiento del paciente, si existen sobrantes de los
medicamentos Monopolio del Estado, el familiar del paciente deberá hacer la devolución
de estos al respectivo lugar donde fue adquirido.
6. Pérdida y destrucción de sustancias, medicamentos y/o productos sometidos
a fiscalización
En caso de pérdida de sustancias, medicamentos y/o productos sometidos a fiscalización,
se deberá informar inmediatamente a la U.A.E. Fondo Nacional de Estupefacientes del
Ministerio de la Protección Social o al Fondo Rotatorio de Estupefacientes, anexando la
copia de la denuncia ante el órgano competente, así como los avances que presente
dicha investigación.
Cuando se requiera dar de baja sustancias sometidas a fiscalización, medicamentos y/o
Productos que las contengan, se pedirá autorización a la U.A.E. Fondo Nacional de
Estupefacientes del Ministerio de la Protección Social o al Fondo Rotatorio de
Estupefacientes,
La destrucción de sustancias sometidas a fiscalización, medicamentos y/o productos que
las contengan por vencimiento, deterioro u otra razón, se hará con la intervención del
Delegado de la sociedad o entidad solicitante y un delegado de la U.A.E. Fondo Nacional
de Estupefacientes del Ministerio de la Protección Social, o del Fondo Rotatorio de
Estupefacientes, la cual debe ser solicitada mínimo con diez (10) días calendario de
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
antelación, informando la fecha, hora y lugar en que se llevará a cabo dicho
procedimiento.
En caso de no efectuarse la destrucción en la fecha estipulada, el solicitante deberá
informar a la U.A.E. Fondo Nacional de Estupefacientes o al Fondo Rotatorio de
Estupefacientes, con el fin de reprogramarla.
La destrucción deberá efectuarse de acuerdo con las normas técnicas establecidas por el
Ministerio del Medio Ambiente, Vivienda y Desarrollo Territorial.
7. Prescripción de medicamentos de control especial
La cantidad total prescrita de medicamentos sometidas a fiscalización se hará, teniendo
en cuenta los siguientes parámetros:
a.- Medicamentos correspondientes a: "Analgésicos Narcóticos", "Analgésicos
Moderadamente Narcóticos", a "Barbitúricos o Medicamentos, que contienen Barbitúricos,
con excepción de Fenobarbital; a "Anfetaminas y Estimulantes Centrales"; a
"Tranquilizantes e Hipnóticos no Barbitúricos" y demás medicamentos de control especial,
hasta la dosis requerida para treinta (30) días calendario.
b.- Medicamentos correspondientes a "Oxitócicos y Antihemorrágicos Uterinos", la dosis
ordenada bajo la responsabilidad del médico tratante.
c.- Fenobarbital, hasta la dosis requerida para noventa (90) días calendario.
Los médicos, médicos veterinarios y médicos veterinarios zootecnistas graduados y en
ejercicio legal de su profesión son los únicos profesionales que podrán prescribir
Medicamentos de control especial, franja violeta, en la fórmula del Recetario Oficial.
Los médicos veterinarios, médicos veterinarios zootecnistas, para prescribir
Medicamentos sometidos a fiscalización, deberán estar inscritos en el Consejo
Profesional de Medicina Veterinaria y de Zootecnia de Colombia – COMVEZCOL, donde
obtienen el Registro y Matrícula Profesional, de acuerdo con la Ley 073 de 1985 y la Ley
576 de 2000, sobre los profesionales autorizados para prescribir medicamentos de
sometidos a fiscalización.
Para los pacientes que requieran salir o entrar al país que estén sometidos a tratamiento
con medicamentos que contengan estupefacientes incluidos en las Listas I y II de la
Convención de 1961 enmendada por el Protocolo de 1972, o que contengan sustancias
sicotrópicas en las Listas II, III y IV del Convenio de 1971, deberán cumplir con lo
siguiente:
1. Las cantidades máximas autorizadas de medicamentos que se podrán transportar para
uso personal corresponderán a un tratamiento estándar de 30 días, cualquiera sea la
sustancia de que trate.
2. Cuando los pacientes bajo tratamiento de estas sustancias viajen hacia Colombia se
les exigirá copia de la fórmula médica en la cual se ha recetado el medicamento. Cuando
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
se supere el tiempo de estadía en más de un (1) mes, si el paciente necesita continuar
con el tratamiento, debe consultar a un Médico en ejercicio legal de su profesión en el
país para que expida dicha fórmula y podrá adquirir los medicamentos siguiendo las
normas internas.
3. Cuando el paciente requiera salir del país debe tener en cuenta las restricciones y
prohibiciones que pueden tener los países de destino. Así mismo, al salir del país el
paciente bajo tratamiento debe tener consigo copia de la fórmula médica en la cual esté
prescrito el uso del medicamento. Cuando algún país solicite un requisito adicional a la
fórmula médica, o certificación del uso para tratamiento de alguno de estos
medicamentos, ésta podrá ser expedida por la U.A.E. Fondo Nacional de Estupefacientes
del Ministerio de la Protección Social, con base en el resumen de la historia clínica
expedida por la IPS o el médico tratante.
8. Recetario Oficial
La prescripción de medicamentos de control especial para uso humano o veterinario solo
se podrá efectuar en los recetarios oficiales suministrados por los Fondos Rotatorios de
Estupefacientes, para médicos en ejercicio legal de su profesión y/o por COMVEZCOL
para médicos veterinarios y médicos veterinarios zootecnistas.
El Recetario debe ajustarse al formato indicado por el Fondo Nacional de Estupefacientes.
Los profesionales que laboren en las instituciones podrán hacer uso del Recetario Oficial
adquirido por la entidad. Los Fondos Rotatorios de Estupefacientes de las Secretarías,
instituciones o Direcciones Departamentales de Salud, y/o COMVEZCOL para médicos
veterinarios, son los únicos autorizados para emitir, distribuir y vender el Recetario Oficial
para la prescripción.
Las instituciones que compren Recetarios Oficiales para su distribución a los médicos de
su institución serán solidariamente responsables del manejo y buen uso que se les dé a
los mismos.
Los Fondos Rotatorios de Estupefacientes y COMVEZCOL para la elaboración de los
respectivos Recetarios Oficiales, tendrán en cuenta los lineamientos que para el efecto
señale la U.A.E. Fondo Nacional de Estupefacientes del Ministerio de la Protección Social.
ARTÍCULO 86.- Los recetarios oficiales para la formulación de medicamentos de control
especial tendrán un original, que quedará en el Establecimiento o Entidad que dispense, y
dos copias, en las cuales se anotará que fue dispensado; una para el paciente y otra para
el trámite administrativo pertinente.
Ninguna entidad podrá exigir la presentación de una fórmula médica en dos (2) originales
para soportar tramites internos administrativos.
Cuando a un profesional se le extravíe el Recetario Oficial, deberá formular la denuncia
correspondiente e informar inmediatamente por escrito al Fondo Rotatorio de
Estupefacientes de la respectiva Dirección Departamental de Salud, allegando copia de la
denuncia.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Para el caso de que un medicamento sea formulado en un Departamento diferente al de
adquisición o compra, se podrá autorizar la fórmula por parte de la U.A.E. Fondo Nacional
de Estupefacientes o del Fondo Rotatorio de Estupefacientes Departamental.
El Recetario Oficial debe contener como mínimo los siguientes datos:
1. Codificación.
2. Nombre del prescriptor, dirección y teléfono.
3. Fecha de expedición de la prescripción.
4. Nombre del paciente, dirección y número del documento de identidad si es el caso.
5. Denominación Común Internacional del medicamento, concentración y forma
farmacéutica, cantidad total en números y letras y dosis diaria (frecuencia de
administración), vía de administración y tiempo de tratamiento.
6. Firma del prescriptor con su respectivo número de registro profesional.
La fórmula médica debe ser única para los medicamentos de control especial. En ella no
deben prescribirse otros medicamentes diferentes a los sometidos a control especial. Una
vez dispensado el medicamento se deberá colocar sello de dispensado en la prescripción
correspondiente.
9. Infracciones y sanciones
Las infracciones se calificarán como leves, graves y muy graves atendiendo a los criterios
de riesgos para la salud, cuantía del eventual beneficio obtenido, grado de
intencionalidad, gravedad de la alteración sanitaria y social producida, generalización de
la infracción y reincidencia.
Constituirán faltas administrativas y serán sancionadas en los términos previstos en el
artículo anterior, las infracciones que a continuación se tipifican:
INFRACCIONES LEVES:
a. No informar a la U.A.E. Fondo Nacional de Estupefacientes o Fondos Rotatorios de
Estupefacientes los cambios de Representante Legal, director técnico, razón social, No.
NIT, dirección y teléfonos.
b. No aportar, las entidades o personas responsables, los informes que estén obligados a
suministrar por razones sanitarias, técnicas, económicas, administrativas, financieras y
legales.
c. No contar los Fondos Rotatorios de Estupefacientes con las existencias necesarias de
Medicamentos de Control Especial Monopolio del Estado.
d. No disponer de existencias mínimas de Medicamentos de Control Especial para
supuestos de emergencia o catástrofe, en los casos que resulte obligado.
e. Dificultar la labor inspectora mediante cualquier acción u omisión que perturbe o retrase
la misma.
f. Dispensar medicamentos de Control Especial transcurrido el plazo de validez de la
prescripción o sin el cumplimiento de los requisitos del Recetario Oficial.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
g. No cumplir correctamente con los datos y advertencias que debe contener la
prescripción de medicamentos de Control Especial.
h. Ofrecer directa o indirectamente cualquier tipo de incentivo, primas u obsequios, por
quien tenga intereses directos o indirectos en la producción, fabricación y
comercialización de sustancias sometidas a fiscalización o productos que las contengan a
los profesionales sanitarios implicados en el ciclo de prescripción, dispensación y
administración.
i. No registrar los movimientos de sustancias sometidas a fiscalización y/o medicamentos
que las contengan en los respectivos registros.
j. Vender al detal medicamentos de Control Especial siendo mayorista o al por mayor
siendo minorista.
k. No conservar los medicamentos bajo las condiciones de almacenamiento exigidas por
la U.A.E. Fondo Nacional de Estupefacientes del Ministerio de la Protección Social. La
auto formulación de medicamentos de control especial por parte de médicos.
m. Dispensar medicamentos de Control Especial con más de quince días de haber sido
expedida la prescripción médica.
n. Entregar al cuerpo médico, Entidades Aseguradoras de Planes de Beneficio e IPS
muestras médicas o comerciales de medicamentos de control especial como estrategia de
mercadeo.
INFRACCIONES GRAVES:
a. Reincidir en la misma falta.
b. Cometer la falta para ocultar otra.
c. Tener excedentes y/o faltantes de materias primas o medicamentos de Control Especial
sin la debida justificación.
d. Elaborar, fabricar, importar, exportar, comprar localmente o distribuir sustancias
sometidas a fiscalización, medicamentos o productos que las contengan por personas no
autorizadas.
e. Funcionamiento del Servicios Farmacéuticos sin la presencia y actuación del Director
Técnico responsable.
f. Impedir la actuación de los inspectores, debidamente acreditados, en los centros en los
que se elaboren, fabriquen, distribuyan y dispensen sustancias sometidas a fiscalización,
medicamentos o productos que las contengan
g. Preparar fórmulas magistrales que contengan sustancias sometidas a fiscalización y/o
medicamentos sin los requisitos legales establecidos.
h. Dispensar medicamentos en establecimientos no autorizados.
i. Dispensar sin Recetario Oficial medicamentos sometidos a control especial.
j. Realizar promoción o publicidad, a través de los medios de comunicación masiva a los
medicamentos FRANJA VIOLETA.
k. La reincidencia en la comisión de infracciones leves, así como la comisión de alguna de
las infracciones calificadas como leves cuando concurran de forma grave.
INFRACCIONES MUY GRAVES:
a. Poner en el mercado medicamentos de Control Especial sin haber obtenido el Registro
Sanitario o la autorización de fabricación.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
b. Incumplimiento de las medidas cautelares y definitivas sobre medicamentos que las
autoridades sanitarias competentes acuerden por causa grave de salud pública.
c. Desviar sustancias sometidas a fiscalización, medicamentos o productos que las
contengan, hacia canales ilícitos.
d. Fabricación de medicamentos de Control Especial sin el lleno de los requisitos
establecidos.
e. Vender, dispensar, distribuir o usar medicamentos de control especial para fines no
médicos.
f. El ofrecimiento de primas, obsequios, premios, concursos o similares como métodos
vinculados a la promoción o venta al público de los medicamentos de Control Especial.
g. La reincidencia en la comisión de faltas graves en los últimos cinco años.
h. La reincidencia en la comisión de infracciones graves, así como la comisión de algunas
de las infracciones calificadas como graves cuando ocurran de forma grave.
i. El uso de sustancias sometidas a fiscalización o medicamentos que las contengan para
cometer actos delictivos, generará además el procedimiento a que haya lugar ante la
autoridad competente según lo establecido en el código penal, ya que pueden poner a las
personas en estado de indefensión.
Conocido el hecho o recibida la denuncia o el aviso, la autoridad competente ordenará la
correspondiente investigación para verificar los hechos u omisiones constitutivas de
infracción prevista en la presente Resolución.
Para efectos de la verificación de los hechos u omisiones podrán realizarse todas aquellas
diligencias que se consideren conducentes, tales como visitas, inspecciones, toma de
muestras, exámenes de laboratorio, pruebas de campo, químicas, prácticas de
dictámenes periciales y en general todas aquellas que se consideren conducentes. El
término para la práctica de esta diligencia no podrá exceder de tres (3) meses contados a
partir de la fecha de iniciación de la correspondiente investigación.
Cuando la autoridad competente encuentre con base en las diligencias practicadas que
aparece plenamente comprobado, que el hecho investigado no ha existido, que el
presunto infractor no lo cometió, que las normas no lo consideran como sanción o que el
procedimiento sancionatorio no podía iniciarse o proseguirse, procederá a dictar un acto
administrativo que así lo declare y ordenará cesar el procedimiento contra el presunto
infractor. Este acto deberá notificarse personalmente al investigado o en su defecto, por
edicto conforme a lo dispuesto por el Código Contencioso Administrativo. Si la falta no se
tipifica en ninguna de las anteriores se calificará como levísima y se sancionará mediante
la amonestación.
Si de las diligencias practicadas se concluye que existe mérito para adelantar la
investigación, se procederá a notificar personalmente al presunto infractor de los cargos
que se formulan y se pondrá a su disposición el expediente con el propósito de que
solicite a su costa copia de este.
Las infracciones señaladas serán sancionadas aplicando una graduación de mínimo,
medio y máximo a cada nivel de infracción, en función de la negligencia e intencionalidad
del sujeto infractor, fraude o connivencia, incumplimiento de las advertencias previas, cifra
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
de negocios de la empresa, número de personas afectadas, perjuicio causado, beneficios
obtenidos a causa de la infracción y permanencia y transitoriedad de los riesgos así:
a) Infracciones leves: Grado mínimo: hasta dos salarios mínimos mensuales vigentes.
Grado medio: desde dos a seis salarios mínimos mensuales legales vigentes. Grado
máximo: desde seis a diez salarios mínimos mensuales legales vigentes.
b) Infracciones graves: Grado mínimo: desde doce a veinte salarios mínimos mensuales
legales vigentes. Grado medio: desde veinte a cuarenta salarios mínimos mensuales
legales vigentes. Grado máximo: desde cuarenta a ochenta salarios mínimos legales
vigentes, pudiendo rebasar dicha cantidad hasta alcanzar el quíntuplo del valor de los
medicamentos o servicios objeto de la infracción.
c) Infracciones muy graves: Grado mínimo: desde cien a doscientos salarios mínimos
mensuales legales vigentes. Grado medio: desde doscientos a trescientos salarios
mínimos mensuales legales vigentes. Grado máximo: desde trescientos a quinientos
salarios mínimos mensuales legales vigentes, pudiendo rebasar dicha cantidad hasta
alcanzar el quíntuplo del valor de los medicamentos o servicios objeto de la infracción.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
TEMA 7. FARMACOVIGILANCIA
La Farmacovigilancia surge como resultado de situaciones relacionadas con respuestas
no deseadas al uso de medicamentos, a finales del siglo XIX fueron descritas y
analizadas las muertes que se produjeron con la introducción del cloroformo como
anestésico general y la aparición de ictericia con la administración de arsenicales para el
tratamiento de la sífilis.
En la década de 1930 en los Estados Unidos de América ocurrieron más de 100 muertes
en niños debido a la administración de un jarabe de sulfanilamida que contenía
dietilenglicol como disolvente.
El suceso, que puede ser considerado como definitorio, es conocido como "desastre de la
talidomida", ocurrido a comienzos de los años 1960, con posterioridad a la introducción en
el mercado de este medicamento se apreció un marcado incremento de malformaciones
congénitas como la focomelia y se identificó a la talidomida como la responsable, lo que
decidió su retirada del mercado. Mas de 4000 nacimientos de malformados ya habían
ocurrido en Europa en el momento de retirarla.
El programa de Farmacovigilancia tiene como objetivo principal realizar vigilancia a los
medicamentos luego que estos están siendo comercializados para determinar la
seguridad de estos.
Los principales objetivos de la Farmacovigilancia son:
1. Detección temprana de las reacciones adversas e interacciones desconocidas hasta
ese momento
2. Detección de aumentos de la frecuencia de reacciones adversas (conocidas).
3. Identificación de factores de riesgo y de los posibles mecanismos subyacentes de las
reacciones adversas.
4. Estimación de los aspectos cuantitativos de la relación beneficio/riesgo y difusión de la
información necesaria para mejorar la regulación y prescripción de medicamentos.
Los objetivos finales de la Farmacovigilancia son:
1. El uso racional y seguro de los medicamentos.
2. La evaluación y comunicación de los riesgos y beneficios de los medicamentos
comercializados Identificación de factores de riesgo y de los posibles mecanismos
subyacentes de las reacciones adversas.
3. La educación y la información a los pacientes.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
1. Definiciones
ACCIONES INSEGURAS: Son acciones u omisiones que tiene el potencial de generar
daño o evento adverso. Es una conducta que ocurre durante el proceso de atención en
salud por miembros del equipo misional de salud.
BARRERA DE SEGURIDAD: Una acción o circunstancia que reduce la probabilidad de
presentación del incidente o evento adverso.
ERROR DE MEDICACION: Suceso que puede evitarse y que es causado por una
utilización inadecuada de un medicamento produciendo lesión a un paciente mientras la
medicación está bajo control del personal
EVENTO ADVERSO: Resultado de una atención en salud que de manera no intencional
produjo daño. Los eventos adversos pueden ser prevenibles y no prevenibles.
EVENTO ADVERSO PREVENIBLE: Resultado no deseado, no intencional que se habría
evitado mediante el cumplimiento de los estándares del cuidado asistencial disponibles en
un momento determinado.
EVENTO ADVERSO NO PREVENIBLE: Resultado no deseado, no intencional que se
presenta a pesar del cumplimiento de los estándares del cuidado asistencial.
EVENTO ADVERSO SERIO: El evento adverso serio constituye un daño no intencionado
que pudo haber llevado a la muerte o al deterioro serio de la salud del paciente, con
hospitalización, discapacidad o incapacidad parcial o permanente, o evento clínico
importante.
FACTOR CONTRIBUTIVO: Condiciones que predisponen una acción insegura (falla
activa).
FARMACOVIGILANCIA: Es la ciencia y actividades relacionadas con la detección,
evaluación, entendimiento y prevención de los eventos adversos o cualquier otro
problema relacionado con medicamentos También es la actividad específica que
monitorea el uso de medicamentos en los pacientes.
INCIDENTE: Evento o circunstancia que sucede en la atención clínica de un paciente y
que no le genera daño, pero que en su ocurrencia se incorporan fallas en los procesos de
atención.
REACCIÓN ADVERSA A MEDICAMENTOS (RAM): Alteración y/o lesión producida
cuando los medicamentos se utilizan de manera apropiada (son difícilmente evitables),
también definida como reacción nociva y no deseada que se presenta tras la
administración de un fármaco, a dosis utilizadas habitualmente en la especie humana.
2. Elementos
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Los programas de farmacovigilancia cuentan con unos elementos básicos como:
Elemento 1 - procedimiento
Con relación a este elemento, las actividades mínimas a documentar son:
1. Notificación (Identificación/captación del evento adverso o incidente a través de formato
físico o magnético): Se sugiere que los prestadores de servicios de salud implementen un
formato único general de reporte de eventos e incidentes que sirva para los diferentes
programas de vigilancia como: seguridad del paciente, tecnovigilancia, reactivo vigilancia,
hemo vigilancia, entre otros.
El Ministerio de Salud cuenta con documentos guías que son herramientas para promover
la estrategia de la seguridad del paciente en el sistema obligatorio de garantía de calidad
de la atención en salud, el cual incluye un formato para la notificación de eventos
adversos que puede ser adoptado o adaptado por la Institución.
2. Registro y procesamiento: Una vez se cuente con la notificación de los eventos
adversos estos deben ser consolidados en medio físico o magnético, se sugiere a los
prestadores de servicios de salud, utilizar la base de datos de eventos adversos que
tengan implementada para el programa de seguridad del paciente para evitar replicar
registros o duplicidad en la información.
Esto facilita el correcto análisis y seguimiento a los eventos notificados, lo cual permite un
adecuado monitoreo a través de indicadores relacionados.
Se sugiere a los profesionales independientes implementar un formato de registro de
fallas en la atención en salud para las buenas prácticas de seguridad del paciente.
3. Análisis: Una vez notificado, registrado y procesado el evento adverso, este debe ser
clasificado como: evento adverso prevenible o evento adverso no prevenible, esto con el
fin de identificar las causas que ocasionaron la aparición del evento adverso y a su vez
generar acciones correctivas y/o preventivas.
• Acción Correctiva: Acción encaminada a identificar, analizar y eliminar las causas
de los eventos adversos detectados con el fin de prevenir que estas situaciones
puedan presentarse de nuevo.
• Acción Preventiva: Acción encaminada a identificar, analizar y eliminar las causas
de los posibles eventos adversos, a fin de prevenir que estas situaciones se
materialicen.
Para el caso de eventos adversos no prevenibles como las reacciones adversas a
medicamentos, se recomienda se evalúen bajo la herramienta Algoritmo de
Naranjo que permite establecer el grado de asociación entre el medicamento y el
daño ocasionado para así identificar los medicamentos cuyos efectos colaterales o
secundarios sean peligrosos o severos para el paciente permitiendo por parte del
prestador la identificación de medicamentos de alto riesgo.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Las instituciones de salud deben formular planes de mejoramiento de acuerdo con el
análisis realizado.
4. Reporte Extrainstitucional: Dentro de las obligaciones establecidas los prestadores de
servicios de salud deberán enviar los reportes de eventos adversos que generaron daño
leve o moderado periódicamente a la autoridad competente. Se sugiere a los prestadores
de servicios de salud adoptar los formatos de reporte utilizados por la entidad estatal líder
de la Red de Farmacovigilancia.
Elemento 2: programa de divulgación y capacitación
Las capacitaciones en Farmacovigilancia son uno de los mecanismos que contribuyen al
uso seguro de medicamentos en la prestación de servicios de salud, se recomienda que
estén incluidas en el plan de capacitaciones del programa institucional de seguridad del
paciente, con el objeto de socializar y unificar criterios para la adecuada gestión de los
eventos adversos.
Elemento 3 comité de análisis de eventos adversos
Este grupo podrá ser el comité de farmacia y terapéutica u otros comités clínicos de la
entidad. Se sugiere que el análisis de los eventos adversos relacionados con
medicamentos sea realizado por el grupo de seguridad del paciente.
Los profesionales y servicios farmacéuticos independientes de los sistemas hospitalarios
no deben contar con un comité de análisis de eventos adversos, pero si deben demostrar
el análisis de los eventos presentados en su prestación de servicios.
Elemento 4 monitoreo de eventos adversos
Contar con un adecuado sistema de monitoreo de eventos adversos permite la
minimización y prevención de estos.
3. Atención Farmacéutica
Definición: es la provisión responsable de la farmacoterapia con el propósito de alcanzar
unos resultados concretos que mejoren la calidad de vida del paciente
(Hepler y Strand, 1990).
La ATENCIÓN FARMACÉUTICA consiste en la realización del seguimiento farmacológico
en el paciente, con dos objetivos:
1. Responsabilizarse con el paciente de que el medicamento le va a hacer el efecto
deseado por el medico que lo prescribió o por el farmacéutico que lo indicó.
2. Estar atento para que a lo largo del tratamiento no aparezcan o aparezcan los mínimos
problemas no deseados, y si aparecen, resolverlos entre los dos o con la ayuda de su
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
medico.
(Faus y Martinez, 1999)
«Es un concepto de práctica profesional en el que el paciente es el principal beneficiario
de las acciones del farmacéutico. Es el compendio de actitudes, comportamientos,
compromisos, inquietudes, valores éticos, funciones, conocimientos, responsabilidades y
destrezas del farmacéutico en la prestación de la farmacoterapia, con objeto de lograr
resultados terapéuticos definidos en la salud y calidad de vida del paciente»
Reunión Organización Mundial de la Salud, Tokio 1.993
Este compromiso parte de la actitud que tiene el farmacéutico por el ejercicio en la
farmacia, y la dispensación es una actividad que más que complementar es el puente que
permite detectar, prevenir y corregir problemas con los medicamentos.
Estos problemas se contemplan en dos grupos importantes, los Problemas Relacionados
con la Utilización de los Medicamentos y los Problemas Relacionados con los
Medicamentos.
Problemas relacionados con el uso de los medicamentos (PRUM)
Corresponden a causas prevenibles de Problemas Relacionados con Medicamentos,
asociados a errores de medicación (prescripción, dispensación, administración o uso por
parte del paciente o cuidador), incluyendo los fallos en el Sistema de Suministro de
Medicamentos, relacionados principalmente con la ausencia en los servicios de procesos
administrativos y técnicos que garanticen la existencia de medicamentos que realmente
se necesiten, acompañados de las características de efectividad, seguridad, calidad de la
información y educación necesaria para su uso correcto.
Estos problemas se pueden clasificar de la manera siguiente:
a) Relativos a la disponibilidad.
b) Relativos a la calidad.
c) Relativos a la prescripción.
d) Relativos a la dispensación.
e) Relativos a la administración.
f) Relativos al uso.
Esta clasificación está sujeta a los avances de las ciencias farmacéuticas, especialmente,
en el área de la prestación de servicios.
Los PRUM (Problemas Relacionados con la Utilización de Medicamentos), se entienden
como desviaciones en la forma correcta como se deben emplear terapéuticamente un
medicamento.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
En los sistemas de salud, el seguimiento fármaco terapéutico se convierte en una forma
efectiva para minimizar los PRM los PRUM y los costos asociados a la morbimortabilidad
por medicamentos, la cual en los estudios realizados se encuentra que es alta y relevante
para la salud individual y colectiva.
Observemos en detalie cada uno de estos problemas:
1. PRUM derivados de la disponibilidad.
- Disponibilidad de medicamentos menos efectivos, seguros o económicos en el
Servicio Farmacéutico lo que conduce a que el personal médico tenga que prescribirlos
debido a la ausencia de medicamentos más adecuados
- Ausencia de medicamentos (pendientes o faltantes) en la farmacia, lo que
conduce a una dispensación incompleta.
- Medicamentos no disponibles en el Servicio Farmacéutico por políticas
institucionales.
2. PRUM derivados de la calidad.
Este concepto de calidad debe ir más aliá de la producción, debe tenerse en cuenta la
forma farmacéutica, así como el origen de los productos, la trazabilidad en un
componente indispensable.
La falta de control en los proveedores puede generar presencia en medicamentos
adulterados o falsificados con concentraciones de principio activo inferior a la especificada
o que presentan alteraciones fisicoquímicas.
3. PRUM relativos a la prescripción.
En la prescripción racional, la elección del mejor medicamento requiere la ponderación
juiciosa de los conceptos psicosociales de la enfermedad, del conocimiento de la
terapéutica y del costo de los medicamentos.
- Ilegibilidad y omisión en la información en la prescripción médica.
- Prescripción de un medicamento a una dosis, frecuencia, pauta, vía y forma
farmacéutica inadecuada.
- Elección incorrecta del medicamento, existe una terapia farmacológica más
efectiva y ajustada a las características del paciente (balance efectividad – seguridad)
- Interacciones farmacocinéticas o farmacodinámicas entre medicamento-
medicamento, medicamento–alimento, medicamento–enfermedad, medicamento–
fitoterapéuticos, medicamento–pruebas de laboratorio, que generan antagonismo o
disminución de la concentración plasmática o toxicidad por efectos sinérgicos.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
- Información e instrucciones incorrectas al paciente.
- Ausencia de prescripción para un medicamento necesario para el paciente.
- Prescripción de un medicamento contraindicado.
- Monitorización incorrecta
4. PRUM relativos a la dispensación
Estos se pueden presentar por los siguientes aspectos:
- Suministro del medicamento equivocado, es decir tiene un principio activo,
concentración o forma farmacéutica diferente a la indicada por el médico.
Este es un error frecuente por falta de concentración del personal o exceso de carga
laboral.
- Suministro de un medicamento en una cantidad diferente a la indicada por el
médico.
Las dificultades económicas en muchas ocasiones hacen que el paciente reciba
cantidades inferiores de medicamento, en esto también se involucra las presentaciones
de los productos.
- Suministro incompleto de la totalidad de los medicamentos indicados por el
médico.
En muchos casos y debido a problemas sociales y económicos, el paciente suele realizar
parte de la terapia ya que asume que algunos productos pueden suplir la acción de otros.
- Creencia de poder prescribir medicamentos irresponsablemente a los usuarios sin
conocer en profundidad la patología presente, interacciones medicamentosas, o
condiciones fisiológicas del paciente
La confusión entre automedicación (utilización de medicamentos de venta libre) y
autoprescripción (utilización de medicamentos de venta bajo fórmula), hacen que algunas
personas diferentes al médico sugieran el uso de medicamentos.
- Despacho de medicamentos sin la entrega de la información sobre su uso,
manipulación y conservación correcta.
Ésta es una práctica común en las farmacias institucionales donde se realiza entregas de
productos, en gran medida por falta de sensibilización en el personal del área.
- Cambio de un medicamento por otro, generalmente por intereses económicos y de
forma irresponsable
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
- Tardanza en el despacho de medicamentos a los servicios intrahospitalarios.
- Medicamento deteriorado, almacenamiento inadecuado que se afecta por
condiciones ambientales
- Monitorización incorrecta, falta de seguimiento farmacoterapéutico al paciente.
- Información incorrecta para la administración o para la utilización.
5. PRUM relativos a la administración
Entre ellos encontramos:
- Medicamento no administrado o administración de medicamento incorrecto
- Medicamento no autorizado por el prescriptor.
- Administración de medicamento a una dosis, frecuencia, pauta, forma
farmacéutica o vía de administración inadecuada
- Asociaciones o mezclas incompatibles física o químicamente
- Manipulación inadecuada del medicamento (dilución, exposiciones a temperatura,
humedad y luz desfavorables)
- Monitorización incorrecta.
6. PRUM relativos al uso
Es importante considerar que el paciente debe recibir toda la información desde el
prescriptor hasta el dispensador para darle uso adecuado al medicamento. En este grupo
encontramos:
- Automedicación o autoprescripción que puede lievar al consumo de un
medicamento inseguro para el paciente por sus características clínicas.
- Rechazo del medicamento por parte del paciente
- Intoxicación por uso de medicamento inadecuado o aumento de dosis y pauta de
dosificación
- Incumplimiento, no adherencia terapéutica, que puede ser: parcial (dosis omitida),
dosificación (dosis mayor o menor, adicional), o incumplimiento total.
- Cambio de dosificación, vía de administración incorrecta, técnica incorrecta,
tiempo incorrecto, o intervalos errados.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
- Cambios en los estilos de vida y hábitos alimenticios que producen interacciones
con el medicamento, o modifican la absorción.
Problemas Relacionados con los Medicamentos (PRM)
Un problema relacionado con la medicación es cualquier evento indeseable que presenta
el paciente, y en el que está involucrado o se sospecha que lo está el tratamiento
farmacológico y que interfiere de manera real o puede interferir en una evolución deseada
del paciente
Todos los pacientes necesitan que la medicación:
1. Esté adecuadamente indicada
2. Sea efectiva
3. Sea segura
4. Sea cómodo
Si el tratamiento se aparta de estas cuatro condiciones los objetivos planteados y los
resultados obtenidos no serán los esperados.
Los PRM se clasifican en:
Problemas de indicación
El paciente necesita indicación de tratamiento por:
Posible problema de salud no tratado
Tratamiento asociado o preventivo
El paciente tiene indicación de un tratamiento farmacológico que no necesita por:
Automedicación irresponsable
Adicción / consumo de drogas
Tratamiento innecesario.
Problemas de Eficacia
El paciente recibe un fármaco que es inadecuado para el trastorno por:
Fármaco mal indicado por el problema de salud.
Trastorno resistente a la medicación
El paciente recibe una posología demasiado baja del medicamento por:
Dosis inadecuada, dosis menores a las terapéuticas de acuerdo a edad, peso,
estado fisiológico, etc.
Periodo de toma inadecuado
Duración insuficiente del tratamiento
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Administración incorrecta
Interacción farmacológica
Calidad del medicamento
Problema de Seguridad
Cuando el paciente presenta una reacción adversa al medicamento por:
Fármaco peligroso para el paciente
Reacción alérgica al medicamento
Administración incorrecta
Interacción farmacológica
Efecto indeseable
Cuando el paciente recibe una posología demasiada alta por:
Dosis inadecuada
Período de toma inadecuada
Duración exagerada del tratamiento
Interacción farmacológica
Calidad del medicamento
Problemas de Cumplimiento
El paciente no cumple el tratamiento, problemas de adherencia al tratamiento por:
Producto no disponible
Recursos insuficientes para adquirir el producto
Imposibilidad o incomodidad de realizar el tratamiento
Falta de comprensión del tratamiento
Negativa al tratamiento
Olvidos
Problemas Relacionados con el Estilo de Vida
El farmacéutico en su condición de agente sanitario debe estar atento a los problemas
que surjan de los hábitos higiénico – sanitario, y debe colaborar con el paciente
fomentando un buen estilo de vida.
Muchas veces los tratamientos farmacológicos no son exitosos, porque influyen en el
paciente otros factores que no dependen de la medicación: la falta de indicación de una
dieta o ejercicio físico en caso de ser necesario, problemas en el cumplimiento de esa
indicación o la adecuación de la misma, son situaciones en las que el farmacéutico puede
colaborar para corregirlas. Evitar excesos o hábitos perjudiciales para la salud también
contribuyen a una mejor calidad de vida del paciente.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Estamos en una sociedad que relaciona medicamento con salud sin tener en cuenta en
muchas ocasiones el cambio de hábitos alimenticios o higiénicos pueden corregir un
problema de salud.
Observemos el enfoque hace corregir estos problemas
Problemas de indicación
Necesita indicación de dieta
Necesita indicación de ejercicio
Necesita indicación de suspender el hábito de consumir alcohol
Necesita indicación de reducir o suspender las infusiones
Necesita suspender el habito de fumar.
Problemas de cumplimiento
Todas las situaciones anteriores fueron indicadas, pero el paciente no cumple las
premisas
Problemas de adecuación
La dieta no es adecuada, tiene una indicación de dieta, el paciente la cumple pero
no es la adecuada para el mismo
El ejercicio no adecuado, tiene una indicación de ejercicio, lo cumple, pero no es el
adecuado para el paciente.
4. Programa Nacional de Farmacovigilancia
El Instituto Nacional de Vigilancia de Medicamentos y Alimentos-INVIMA a través del
Programa Nacional de Farmacovigilancia, trabaja en pro del uso seguro de los
medicamentos, en el marco de los sistemas institucionales y regionales de
farmacovigilancia.
El Programa tiene como objetivo principal realizar vigilancia a los medicamentos luego
que estos se comercializan para determinar la seguridad de los mismos. Las siguientes
son las líneas de acción del Programa:
1.Acopio y análisis de reacciones adversas y otros fenómenos relacionados con
medicamentos y productos biológicos.
2.Socialización de información sobre seguridad de medicamentos.
3.Coordinar la Red Nacional de Farmacovigilancia
Esta red cuenta con dos grupos de actores: Personas (Pacientes, cuidadores y
profesionales de la salud -médicos tratantes, odontólogos, enfermeros, químicos
farmacéuticos, etc.-) e Instituciones (Hospitales, clínicas, autoridades seccionales de
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
salud, laboratorios farmacéuticos, importadores y comercializadores de medicamentos,
Invima).
La Red cuenta con el Grupo de Farmacovigilancia del Invima como nodo central.
El Programa Nacional permite al Invima conocer los eventos adversos o problemas
relacionados con el uso de los medicamentos y de esta forma conocer o ampliar la
información de seguridad y promover el uso seguro y adecuado de los mismos en
Colombia a través de una serie de contactos institucionales y personales.
Vídeos de apoyo
- La herencia de la Talidomida
https://www.youtube.com/watch?v=d2FGbUKyhSw
https://www.youtube.com/watch?v=sYaByx-hC80
- Farmacovigilancia y errores de medicación. Asociación Colombiana de
Farmacovigilancia
https://www.youtube.com/watch?v=7cgJ6AnW_nU
- Farmacovigilancia y seguridad del paciente.
https://www.youtube.com/watch?v=NHCVLykPtIM
https://www.youtube.com/watch?v=JHVvr88k994
Material de apoyo para el estudiante
ELABORACIÓN DE UNA GUÍA PARA LA IMPLEMENTACIÓN DE PROGRAMAS
INSTITUCIONALES DE FARMACOVIGILANCIA PARA PR ESTADORES DE SERVICIO
DE SALUD EN COLOMBIA. MARLEN SILVA REYES, PABLO CÉSAR RIVERA
ZUMAQUÉ. Trabajo de grado UDCA, 2016
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tema 8. DISPOSITIVOS MÉDICOS – TECNOVIGILANCIA
1. Definiciones (Decreto 4725 de 2005)
Accesorio: El destinado especialmente por el fabricante para ser utilizado en forma
conjunta con un dispositivo médico, para que este último, pueda emplearse de
conformidad con la finalidad prevista para el producto por el fabricante del mismo.
Acondicionamiento: Son todas las operaciones por las cuales un dispositivo médico se
empaca y rotula para su distribución.
Advertencia: Llamado de atención, generalmente incluido en los textos de las etiquetas
y/o empaques, sobre algún riesgo particular asociado con la utilización de los dispositivos
médicos.
Buenas Prácticas de Manufactura de Dispositivos Médicos BPM-: Son los procedimientos
y métodos utilizados para asegurar la calidad durante la manufactura, el empaque,
almacenamiento y la instalación de los dispositivos médicos para uso humano. Estos
procedimientos se refieren a la estructura organizacional, responsabilidades, procesos y
recursos para implementar los requisitos de calidad asociados con el dispositivo médico.
Certificado de Capacidad de Almacenamiento y Acondicionamiento - CCAA-: Es el acto
administrativo que expide el Instituto Nacional de Vigilancia de Medicamentos y Alimentos
- INVIMA - a los importadores de dispositivos médicos, en el que consta el cumplimiento
de las condiciones sanitarias para el almacenamiento y/o acondicionamiento, control de
calidad, de dotación y recurso humano, que garantizan su buen funcionamiento, así como
la capacidad técnica y la calidad de los mismos.
Certificado de Cumplimiento de Buenas Prácticas de Manufactura - CCBPM: Es el acto
administrativo que expide el Instituto Nacional de Vigilancia de Medicamentos y Alimentos
- INVIMA - para los fabricantes de dispositivos médicos, en el cual se hace constar que el
establecimiento fabricante cumple con las Buenas Prácticas de Manufactura de
Dispositivos Médicos expedidas por el Ministerio de la Protección Social.
Concepto Técnico de las Condiciones Sanitarias: Es el documento expedido por el
Instituto Nacional de Vigilancia de Medicamentos y Alimentos - INVIMA -, en el que consta
el cumplimiento de las condiciones higiénicas, técnicas, locativas, de dotación, recursos
humanos y de control de calidad que garantizan el buen funcionamiento del
establecimiento fabricante, así como la capacidad técnica y la calidad de los productos
que allí se elaboran, el cual regirá hasta tanto se certifique el Cumplimiento de las Buenas
Prácticas de Manufactura de Dispositivos Médicos -BPM-
Dispositivo Médico Activo: Cualquier dispositivo médico cuyo funcionamiento dependa de
una fuente de energía eléctrica o de cualquier fuente de energía distinta de la generada
directamente por el cuerpo humano o por la gravedad, y que actúa mediante la conversión
de dicha energía. No se considerarán dispositivos médicos activos, los productos
sanitarios destinados a transmitir, sin ninguna modificación significativa, energía,
sustancias u otros elementos de un dispositivo médico activo al paciente.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Dispositivo Médico Activo Terapéutico: Cualquier dispositivo médico activo utilizado sólo o
en combinación con otros dispositivos médicos, destinado a sostener, modificar, sustituir o
restaurar funciones o estructuras biológicas en el contexto del tratamiento o alivio de una
enfermedad, lesión o deficiencia.
Dispositivo Médico Alterado: Es aquel que se encuentre inmerso en una de las siguientes
situaciones: a) Cuando sin el lleno de los requisitos señalados en el presente decreto, se
le hubiere sustituido, sustraído total o parcialmente, o reemplazado los elementos
constitutivos que forman parte de la composición o el diseño oficialmente aprobado, o
cuando se le hubieren adicionado sustancias o elementos que puedan modificar sus
efectos o sus características funcionales fisicoquímicas o microbiológicas. a) Cuando sin
el lleno de los requisitos señalados en el presente decreto, hubiere sufrido
transformaciones en sus características funcionales, fisicoquímicas, biológicas y
microbiológicas, por causa de agentes químicos, físicos o biológicos. b) Cuando se
encuentre vencida la fecha de expiración correspondiente a la vida útil del dispositivo
médico, cuando aplique. c) Cuando no corresponda al autorizado por la autoridad
sanitaria o se hubiere sustituido el original, total o parcialmente. d) Cuando por su
naturaleza, no se encuentre almacenado o conservado con las debidas precauciones. e)
Cuando se altere el diseño original o la composición del dispositivo médico.
Dispositivo Médico Combinado: Se considera dispositivo médico combinado, un
dispositivo que forme con un fármaco, un solo producto destinado a ser utilizado
exclusivamente en esta combinación. Si la función principal tiene una acción
farmacológica, será evaluado bajo las disposiciones del Decreto 677 de 1995 o las
normas que lo modifiquen, adicionen o sustituyan. Si la función principal es la de ser
dispositivo y la del fármaco, accesoria, se regirá por lo dispuesto en el presente decreto
con la verificación de calidad y seguridad del medicamento.
Dispositivo Médico Destinado a Investigaciones Clínicas: Es cualquier dispositivo médico
para ser utilizado por un facultativo especialista, en investigaciones efectuadas en un
entorno clínico humano adecuado.
Dispositivo Médico Fraudulento: Aquel que se comercializa sin cumplir con los requisitos
exigidos en las disposiciones técnicas y legales que lo regulan, o aquel que es fabricado,
ensamblado total o parcialmente en Colombia sin el respectivo registro sanitario o permiso
de comercialización.
Dispositivo Médico Implantable: Cualquier dispositivo médico diseñado para ser
implantado totalmente en el cuerpo humano o para sustituir una superficie epitelial o la
superficie ocular mediante intervención quirúrgica y destinado a permanecer allí después
de la intervención por un período no menor de treinta (30) días.
Dispositivo Médico Invasivo: El que penetra parcial o completamente en el interior del
cuerpo, bien por un orificio corporal o bien a través de la superficie corporal.
Dispositivo Médico Invasivo de Tipo Quirúrgico: Dispositivo médico invasivo que penetra
en el interior del cuerpo a través de la superficie corporal por medio de una intervención
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
quirúrgica. Para los efectos del presente decreto, los dispositivos médicos distintos de los
aludidos en esta definición y cuya penetración no se produzca a través de uno de los
orificios corporales reconocidos, serán considerados productos invasivos de tipo
quirúrgico.
Dispositivo Médico Quirúrgico Reutilizable: Instrumento destinado a fines quirúrgicos para
cortar, perforar, cerrar, escarificar, raspar, pinzar, retraer, recortar u otros procedimientos
similares, sin estar conectado a ningún dispositivo médico activo y que puede volver a
utilizarse una vez efectuados todos los procedimientos pertinentes.
Dispositivo Médico para Uso Humano: Se entiende por dispositivo médico para uso
humano, cualquier instrumento, aparato, máquina, software, equipo biomédico u otro
artículo similar o relacionado, utilizado sólo o en combinación, incluyendo sus
componentes, partes, accesorios y programas informáticos que intervengan en su
correcta aplicación, propuesta por el fabricante para su uso en: a) Diagnóstico,
prevención, supervisión, tratamiento o alivio de una enfermedad. b) Diagnóstico,
prevención, supervisión, tratamiento, alivio o compensación de una lesión o de una
deficiencia. c) Investigación, sustitución, modificación o soporte de la estructura anatómica
o de un proceso fisiológico. d) Diagnóstico del embarazo y control de la concepción. e)
Cuidado durante el embarazo, el nacimiento o después del mismo, incluyendo el cuidado
del recién nacido. f) Productos para desinfección y/o esterilización de dispositivos
médicos. Los dispositivos médicos para uso humano, no deberán ejercer la acción
principal que se desea por medios farmacológicos, inmunológicos o metabólicos.
Dispositivo Médico o Equipo Biomédico Vital No Disponible: Son aquellos indispensables
e irremplazables para salvaguardar la vida o aliviar el sufrimiento de un paciente o grupo
de pacientes, y que por condiciones de baja rentabilidad en su comercialización, no se
encuentran disponibles en el país o las cantidades no son suficientes
Dispositivos con Superficie de Contacto: Son aquellos que incluyen contacto con piel,
membrana mucosa y superficies abiertas o comprometidas.
Dispositivos de Comunicación Interna y Externa: Incluyen los dispositivos que entran en
contacto directo con la corriente sanguínea o sangre, fluidos corporales o aquellos que se
comunican con tejidos, huesos y con el sistema pulpa / dentina.
Dispositivo Médico Terminado: Es el que se encuentra en su empaque definitivo, apto
para ser usado y listo para su distribución comercial.
Dispositivo Médico Sobre Medida: Todo dispositivo fabricado específicamente, siguiendo
la prescripción escrita de un profesional de la salud, para ser utilizado por un paciente
determinado.
Equipo Biomédico: Dispositivo médico operacional y funcional que reúne sistemas y
subsistemas eléctricos, electrónicos o hidráulicos, incluidos los programas informáticos
que intervengan en su buen funcionamiento, destinado por el fabricante a ser usado en
seres humanos con fines de prevención, diagnóstico, tratamiento o rehabilitación. No
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
constituyen equipo biomédico, aquellos dispositivos médicos implantados en el ser
humano o aquellos destinados para un sólo uso.
Equipo Biomédico de Tecnología Controlada: Son aquellos dispositivos médicos
sometidos a un control especial, por estar incluidos en alguna de las siguientes
situaciones: a) De acuerdo a su clasificación de alto riesgo y el grado de vulnerabilidad
asociado a estos dispositivos; así como los derivados del diseño, fabricación, instalación,
manejo y su destino previsto. b) Los prototipos que conlleva a nuevos desarrollos
científicos y tecnológicos. c) Los que sean objeto de control de la oferta mediante la
utilización de estándares que permitan la distribución eficiente de la tecnología, por zonas
geográficas en el país, según los parámetros del artículo 65 de la Ley 715 de 2001. d)
Que corresponda a equipo usado o repotenciado. e) Que para su adquisición, instalación
y utilización requieren de una inversión superior a los 700 salarios mínimos legales
vigentes, sean clasificados IIb y III conforme a lo establecido en el presente decreto y se
encuentren bajo los parámetros del artículo 65 de la Ley 715 de 2001. El Ministerio de la
Protección Social podrá, a través de acto administrativo, clasificar como equipos
biomédicos de tecnología controlada, además de los enunciados en el presente artículo, a
los equipos de las clases I y IIa previstas en el presente decreto, cuando las necesidades
del Sector así lo requieran.
Equipo Biomédico Nuevo: Se aplica a aquellos equipos que no han sido usados y que no
tengan más de dos (2) años desde la fecha de su fabricación.
Equipo Biomédico en Demostración: Es aquel equipo biomédico nuevo, que se utiliza para
promover la tecnología. Los equipos biomédicos en demostración importados pueden ser
nacionalizados en los términos y condiciones establecidas en la normatividad aduanera
para la modalidad de importación temporal y sólo pueden ser certificados por su
fabricante o su representante en Colombia.
Equipo Biomédico Usado: Incluye todos los equipos que han sido utilizados en la
prestación de servicios y/o en procesos de demostración, que no tienen más de cinco (5)
años de servicio desde su fabricación o ensamble.
Equipo Biomédico Repotenciado: Incluye todos los equipos que han sido utilizados en la
prestación de servicios de salud o en procesos de demostración, en los cuales, y que
parte de sus subsistemas principales, han sido sustituidos con piezas nuevas por el
fabricante o el repotenciador autorizado por el fabricante y que cumplen con los requisitos
especificados por éste y las normas de seguridad bajo el cual fue construido.
Equipo Biomédico Prototipo: Incluye todos aquellos que se encuentran en fase de
experimentación que aún no se han empleado en la prestación de servicios o en
demostraciones y que no cuentan con el certificado de venta libre expedido por el
organismo nacional competente o su homólogo en el país de origen.
Estabilidad: Propiedad del dispositivo médico de mantener sus características originales
en el tiempo de vida útil dentro de las especificaciones establecidas de calidad.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Estudio Clínico: Cualquier investigación que se realice en seres humanos con intención de
descubrir o verificar los efectos clínicos o cualquier otro efecto de los dispositivos médicos
y/o identificar cualquier reacción adversa, con el objeto de comprobar su seguridad y/o
eficacia.
Etiqueta: Es toda información impresa escrita o gráfica adherida que acompañe el
dispositivo médico.
Fabricante: Es la persona natural o jurídica responsable del diseño, fabricación, empaque
acondicionamiento y etiquetado de un dispositivo médico. El fabricante será el
responsable del producto final, independientemente que las etapas mencionadas sean
hechas por la misma persona o en su nombre, por un tercero.
Fecha de Expiración o Caducidad: Es la que indica el tiempo máximo dentro del cual se
garantizan las especificaciones de calidad de un producto establecidas para su utilización.
Finalidad Prevista: La utilización a la que se destina el dispositivo médico según las
indicaciones proporcionadas por el fabricante en el etiquetado, las instrucciones de
utilización y/o material publicitario, las cuales deben ser acordes con las autorizadas en el
respectivo registro sanitario o en el permiso de comercialización.
Importación Temporal de Equipo Biomédico a Corto Plazo: Es aquella que se realiza
cuando el equipo biomédico se importa para atender una finalidad específica que
determine su corta permanencia en el país. El plazo máximo de importación será de seis
(6) meses contados a partir del levante de la mercancía, prorrogables por la autoridad
aduanera por tres (3) meses más.
Importación Temporal de Equipo Biomédico a Largo Plazo: Es aquella que se realiza
cuando se trate de equipo biomédico contemplado como un bien de capital, sus piezas y
accesorios necesarios para su normal funcionamiento que vengan en el mismo embarque.
El plazo máximo de esta importación será de cinco (5) años contados a partir del levante
de la mercancía.
Incidente adverso: Daño o potencial riesgo de daño no intencionado al paciente, operador
o medio ambiente que ocurre como consecuencia de la utilización de un dispositivo
médico.
Inserto: Es cualquier material impreso, digitalizado o gráfico que contiene instrucciones
para su almacenamiento, utilización o consumo seguro del dispositivo médico.
Lote: Una cantidad definida de materia prima, material de envasado o producto procesado
en un sólo proceso o en una serie de procesos, de tal manera que pueda esperarse que
sea homogéneo. En el caso de un proceso continuo de fabricación, el lote debe
corresponder a una fracción definida de la producción, que se caracterice por la
homogeneidad que se busca en el dispositivo médico. El lote puede ser subdividido.
Modelo: Es la designación mediante números, letras o su combinación con la cual se
identifica el diseño y la composición de un equipo biomédico.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Número de Lote o serie: Designación (mediante números, letras o ambos) del lote o serie
de dispositivos médicos que, en caso de necesidad, permita localizar y revisar todas las
operaciones de fabricación e inspección practicadas durante su producción y permitiendo
su trazabilidad.
Permiso de Comercialización para Equipo Biomédico de Tecnología Controlada: Es el
documento público expedido por el Instituto Nacional de Vigilancia de Medicamentos y
Alimentos - INVIMA - previo al procedimiento tendiente a verificar el cumplimiento de los
requisitos técnico - legales establecidos en el presente decreto, el cual faculta a una
persona natural o jurídica para producir, comercializar, importar, exportar, ensamblar,
procesar, expender o vender un equipo biomédico controlado.
Precauciones: Medidas de seguridad que se deben cumplir al usar todo dispositivo
médico.
Referencia: Variante cualitativa o de diseño de un producto, empleado para un mismo uso
y que corresponde a un mismo titular y fabricantes.
Registro Sanitario: Es el documento público expedido por el Instituto Nacional de
Vigilancia de Medicamentos y Alimentos - INVIMA - previo el procedimiento tendiente a
verificar el cumplimiento de los requisitos técnico - legales y sanitarios establecidos en el
presente decreto, el cual faculta a una persona natural o jurídica para producir,
comercializar, importar, exportar, envasar, procesar, expender y/o almacenar un
dispositivo médico.
Seguridad: Es la característica de un dispositivo médico, que permite su uso sin mayores
posibilidades de causar efectos adversos.
Semielaborar: Todo proceso de fabricación que permita la obtención de un dispositivo
médico hasta su envase o empaque.
Servicio de Soporte Técnico: Son todas las actividades realizadas para asegurar el buen
funcionamiento del equipo biomédico, involucrando aquellas consideradas como de
mantenimiento preventivo, correctivo y verificación de la calibración, entre otras.
Sistema Nervioso Central: Para efectos de este decreto se entiende como sistema
nervioso central, el encéfalo, la médula espinal y las meninges.
Sistema Circulatorio Central: Corresponde a los siguientes vasos: arteria pulmonar, aorta
ascendente, arterias coronarias, arteria carótida común, arteria carótida externa e interna,
arterias cerebrales, tronco braquiocefálico, vena cordis (coronaria mayor y senocoronaria),
vena pulmonar, vena cava superior e inferior.
Tarjeta de Implante: Documento donde se registra el nombre y modelo del dispositivo
médico, número de lote o número de serie, dirección del fabricante, el nombre de la
institución en donde se realizó el implante y la fecha del mismo, así como la identificación
del paciente.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Tecnovigilancia: Es el conjunto de actividades que tienen por objeto la identificación y la
cualificación de efectos adversos serios e indeseados producidos por los dispositivos
médicos, así como la identificación de los factores de riesgo asociados a estos efectos o
características, con base en la notificación, registro y evaluación sistemática de los
efectos adversos de los dispositivos médicos, con el fin de determinar la frecuencia,
gravedad e incidencia de los mismos para prevenir su aparición.
Uso a Corto Plazo: Destinado normalmente a utilizarse de forma continua durante un
período de hasta treinta (30) días.
Uso Prolongado: Destinado normalmente a utilizarse de forma continua durante un
período de más de treinta (30) días.
Uso Transitorio: Destinado normalmente a utilizarse de forma continua durante menos de
sesenta (60) minutos.
2. Clasificación de los dispositivos médicos
La clasificación de los dispositivos médicos realizada por el fabricante se fundamenta en
los riesgos potenciales relacionados con el uso y el posible fracaso de los dispositivos con
base en la combinación de varios criterios tales como, duración del contacto con el
cuerpo, grado de invasión y efecto local contra efecto sistémico.
Se deberá establecer la clasificación de los dispositivos médicos siguiendo las reglas,
dentro de las siguientes clases:
Clase I: Son aquellos dispositivos médicos de bajo riesgo, sujetos a controles generales,
no destinados para proteger o mantener la vida o para un uso de importancia especial en
la prevención del deterioro de la salud humana y que no representan un riesgo potencial
no razonable de enfermedad o lesión.
Clase IIa: Son los dispositivos médicos de riesgo moderado, sujetos a controles
especiales en la fase de fabricación para demostrar su seguridad y efectividad.
Clase IIb: Son los dispositivos médicos de riesgo alto, sujetos a controles especiales en el
diseño y fabricación para demostrar su seguridad y efectividad.
Clase III: Son los dispositivos médicos de muy alto riesgo sujetos a controles especiales,
destinados a proteger o mantener la vida o para un uso de importancia sustancial en la
prevención del deterioro de la salud humana, o si su uso presenta un riesgo potencial de
enfermedad o lesión.
Criterios de clasificación.
La aplicación de las reglas de clasificación se regirá por la finalidad prevista de los
dispositivos médicos:
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
a) Si un dispositivo médico se destina a utilizarse en combinación con otro dispositivo
médico, las reglas de clasificación se aplicarán a cada uno de los productos por separado
del producto con el que se utilicen.
b) Los soportes informáticos que sirvan para manejar un producto o que tengan influencia
en su utilización se incluirán automáticamente en la misma categoría.
c) Si un dispositivo médico no se destina a utilizarse exclusiva o principalmente en una
parte específica del cuerpo, se considerará para la clasificación, su utilización especifica
más crítica.
d) Si para el mismo dispositivo médico, son aplicables varias reglas teniendo en cuenta
las funciones que le atribuye el fabricante, se aplicarán las reglas que conduzcan a la
clasificación más elevada.
Reglas de clasificación.
Para clasificar un dispositivo médico se tendrán en cuenta las siguientes reglas:
A. DISPOSITIVOS MÉDICOS NO INVASIVOS
Regla 1. Todos los dispositivos médicos no invasivos se incluirán en la clase I, salvo que
les sean aplicables algunas de las reglas siguientes.
Regla 2. Todos los dispositivos médicos no invasivos destinados a la conducción o
almacenamiento de sangre, fluidos o tejidos corporales, líquidos o gases destinados a una
perfusión, administración o introducción en el cuerpo, harán parte de la clase IIa; siempre
que: a) Puedan conectarse a un dispositivo médico activo de la clase IIa o de una clase
superior. b) Estén destinados a ser utilizados para el almacenamiento o canalización de
sangre u otros fluidos o para el almacenamiento de órganos, partes de órganos o tejidos
corporales. En todos los demás casos se incluirán en la clase I.
Regla 3. Todos los dispositivos médicos no invasivos destinados a modificar la
composición biológica o química de la sangre, de otros fluidos corporales o de otros
líquidos destinados a introducirse en el cuerpo se incluirán en la clase IIb, salvo si el
tratamiento consiste en filtración, centrifugación o intercambios de gases o de calor, en
cuyo caso, se incluirán en la clase IIa.
Regla 4. Todos los dispositivos médicos no invasivos que entren en contacto con la piel
lesionada, se clasificarán en: a) La clase I, si están destinados a ser utilizados como
barrera mecánica para la compresión o para la absorción de exudados. b) La clase IIb, si
se destinan principalmente a utilizarse con heridas que hayan producido una ruptura de la
dermis y sólo pueden cicatrizar por segunda intención. c) La clase IIa, en todos los demás
casos, incluidos los dispositivos médicos destinados principalmente a actuar en el
microentorno de una herida.
B. DISPOSITIVOS MÉDICOS INVASIVOS
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Regla 5. Todos los dispositivos médicos invasivos en relación con los orificios corporales,
salvo los dispositivos médicos invasivos de tipo quirúrgico, que no estén destinados a ser
conectados a un dispositivo médico activo, se incluirán en: a) La clase I, si se destinan a
un uso transitorio. b) La clase IIa, si se destinan a un uso a corto plazo, salvo si se utilizan
en la cavidad oral hasta la faringe, en el conducto auditivo externo hasta el tímpano o en
una cavidad nasal, en cuyo caso, si incluirán en la clase I. c) La clase IIb, si se destinan a
un uso prolongado, salvo si se utilizan en la cavidad oral hasta la faringe, en el conducto
auditivo externo hasta el tímpano o en una cavidad nasal, y no pueden ser absorbidos por
la membrana mucosa, en cuyo caso, se incluirán en la clase IIa. d) Todos los productos
invasivos en relación con los orificios corporales, salvo los productos invasivos de tipo
quirúrgico, que se destinen a conectarse a un producto activo de la clase IIa o de una
clase superior, entrarán en la clase IIa.
Regla 6. Todos los dispositivos médicos invasivos de tipo quirúrgico destinados a un uso
transitorio se incluirán en la clase IIa, salvo que: a) Sean instrumentos quirúrgicos
reutilizables, en cuyo caso, se incluirán en la clase I. b) Se destinen a suministrar energía
en forma de radiaciones ionizantes, en cuyo caso, se incluirán en la clase IIb. c) Se
destinen a ejercer un efecto biológico o a ser absorbidos totalmente o en gran parte, en
cuyo caso, se incluirán en la clase IIb. d) Se destinen a la administración de
medicamentos mediante un sistema de suministro, sí ello se efectúa de manera
potencialmente peligrosa teniendo en cuenta el modo de aplicación, en cuyo caso, se
incluirán en la clase IIb. e) Se destinen específicamente a diagnosticar, vigilar o corregir
una alteración cardiaca o del sistema circulatorio central por contacto directo con estas
partes del cuerpo, en cuyo caso, se incluirán en la clase III.
Regla 7. Todos los dispositivos médicos invasivos de tipo quirúrgico destinados a un uso
a corto plazo se incluirán en la clase IIa, salvo que tengan por finalidad: a) Suministrar
energía en forma de radiaciones ionizantes, en cuyo caso, se incluirán en la clase IIb. b)
Experimentar modificaciones químicas en el organismo, salvo si los productos se colocan
dentro de los dientes, o administrar medicamentos, en cuyo caso, se incluirán en la clase
IIb. c) Específicamente diagnosticar, vigilar o corregir una alteración cardiaca o del
sistema circulatorio central por contacto directo con estas partes del cuerpo, en cuyo
caso, se incluirán en la clase III. d) Utilizarse, específicamente, en contacto directo con el
sistema nervioso central, en cuyo caso, se incluirán en la clase III e) Ejercer un efecto
biológico o ser absorbidos, totalmente o en gran parte, en cuyo caso, se incluirán en clase
III.
Regla 8. Todos los dispositivos médicos implantables y los dispositivos médicos invasivos
de uso prolongado de tipo quirúrgico, se incluirán en la clase IIb salvo que se destinen a:
a) Colocarse dentro de los dientes, en cuyo caso, se incluirán en la clase IIa. b) Utilizarse
en contacto directo con el corazón, el sistema circulatorio central o el sistema nervioso
central, en cuyo caso, se incluirán en la clase III. c) Ejercer un efecto biológico o ser
absorbidos totalmente o en gran parte, en cuyo caso, se incluirán en la clase III. d) Sufrir
modificaciones químicas en el organismo, salvo si los productos se colocan dentro de los
dientes, o a la administración de medicamentos, en cuyo caso, se incluirán en la clase III.
C. REGLAS ADICIONALES APLICABLES A LOS DISPOSITIVOS MÉDICOS ACTIVOS
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Regla 9. Todos los dispositivos médicos terapéuticos activos destinados a administrar o
intercambiar energía se incluirán en la clase IIa, salvo si sus características son tales que
puedan administrar energía al cuerpo humano o intercambiarla con el mismo, de forma
potencialmente peligrosa, teniendo en cuenta la naturaleza, la densidad y el punto de
aplicación de la energía, en cuyo caso, se incluirán en la clase IIb. Todos los dispositivos
médicos activos destinados a controlar el funcionamiento de los productos terapéuticos
activos de la clase IIb o destinados a influir directamente en el funcionamiento de dichos
productos se incluirán en la clase IIb.
Regla 10. Todos los dispositivos médicos activos con fines de diagnóstico se incluirán en
la clase IIa, siempre que: a) Se destinen a suministrar energía que vaya a ser absorbida
por el cuerpo humano, caso en el cual, son excluidos los productos cuya función sea la
iluminación del organismo del paciente en el espectro visible. b) Se destinen a crear una
imagen de la distribución in vivo de fármacos radiactivos. c) Se destinen a permitir un
diagnóstico directo o la vigilancia de procesos fisiológicos vitales, a no ser que se destinen
específicamente a la vigilancia de parámetros fisiológicos vitales, cuando las variaciones
de esos parámetros, por ejemplo, las variaciones en el funcionamiento cardíaco, la
respiración, la actividad del sistema nervioso central, puedan suponer un peligro
inmediato para la vida del paciente, en cuyo caso, se incluirán en la clase IIb. d) Los
dispositivos médicos activos destinados a emitir radiaciones ionizantes y que se destinen
a la radiología con fines diagnósticos y terapéuticos, incluidos los productos para controlar
o vigilar dichos productos, o que influyan directamente en el funcionamiento de los
mismos, se incluirán en la clase IIb.
Regla 11. Todos los dispositivos médicos activos destinados a administrar medicamentos,
líquidos corporales u otras sustancias al organismo, o extraerlos del mismo, se incluirán
en la clase IIa, salvo que ello se efectúe de forma potencialmente peligrosa, teniendo en
cuenta la naturaleza de las sustancias, la parte del cuerpo de que se trate y el modo de
aplicación, en cuyo caso, se incluirán en la clase IIb.
Regla 12. Todos los demás dispositivos médicos activos se incluirán en la clase I.
D. REGLAS ESPECIALES
Regla 13. Todos los dispositivos médicos que incorporen como parte integral una
sustancia que, si se utilizara independientemente, pudiera considerarse como un
medicamento y que pueda ejercer sobre el cuerpo humano una acción accesoria a la de
los dispositivos médicos, se incluirán en la clase III.
Regla 14. Todos los dispositivos médicos utilizados con fines anticonceptivos o para la
prevención de la transmisión de enfermedades transmisibles por contacto sexual, se
considerarán dispositivos médicos de la clase IIb, a menos que sean dispositivos médicos
implantables o invasivos de uso prolongado, en cuyo caso, se incluirán en la clase III.
Regla 15. Todos los productos destinados específicamente a usos de desinfección,
limpieza, enjuague o, en su caso, a la hidratación de lentes de contacto, se incluirán en la
clase IIb. Todos los productos que se destinen específicamente a la desinfección de
dispositivos médicos, se incluirán en la clase IIa. La presente regla no se aplicará a
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
productos destinados a la limpieza de dispositivos médicos que no sean lentes de
contacto mediante acción física.
Regla 16. Los dispositivos médicos no activos destinados específicamente al registro de
imágenes radiográficas de diagnóstico, se incluirán en la clase IIa.
Regla 17. Todos los dispositivos médicos elaborados utilizando tejidos animales o
derivados de los mismos que hayan sido transformados en inviables, se incluirán en la
clase III, excepto en los casos en que los dispositivos médicos estén destinados a entrar
en contacto únicamente con piel intacta.
Regla 18. No obstante lo dispuesto en otras reglas, las bolsas para sangre se incluirán en
la clase IIb.
3. Tecnovigilancia
La evolución de la ciencia y la tecnología ha generado un elevado número de recursos
diagnósticos, curativos, de rehabilitación, promocionales, preventivos, de investigación,
reemplazo o modificación; que de una u otra manera han contribuido a mejorar la atención
y los indicadores de salud en el mundo. Sin embargo, la aparición de nuevas tecnologías
sanitarias trae consigo un incremento en los costos de los servicios de salud y
consecuentemente mayores dificultades en el acceso.
Siendo función de los sistemas de salud, garantizar el acceso, la calidad y uso apropiado
de éstos recursos estratégicos para la salud, se hace necesario no solamente conocer
¿de qué recursos estamos hablando?, sino también de su fabricación, su regulación, su
cadena de suministro, su uso apropiado, así como evaluar su eficacia, costo efectividad y
seguridad para poder seleccionar aquellos que se conviertan en esenciales para la
atención de la población, disminuyendo riesgos para la salud y costos para los sistemas
sanitarios.
La gran complejidad que cada día muestran equipos, instrumentos, reactivos de
diagnóstico y diversos elementos de uso en la medicina, hace más necesario su
conocimiento y su vigilancia, es por esto que en la década pasada apareció la
tecnovigilancia, como una estrategia de control y seguimiento a la diversidad de
tecnología al alcance de la medicina.
La Tecnovigilancia, se realiza en forma subsecuente al registro sanitario de una nueva
tecnología, y no viene a ser más que el conjunto de métodos y observaciones que
permiten investigar eventos e incidentes adversos previos o posteriores a la utilización de
un producto sanitario. Con el fin de evitar daño al paciente, al operador, al profesional o al
medio ambiente que rodea al equipo o instrumento.
La Asamblea Mundial de la Salud, mediante resolución WHA60.29, encargó al Equipo de
Imaginología de Diagnóstico y Dispositivos Médicos del Departamento de Tecnologías
Sanitarias Esenciales, trabajar por garantizar el acceso, calidad y uso mejores de
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
dispositivos médicos seguros y adecuados, de conformidad con lo previsto en la reforma
de la atención primaria de salud.
Como consecuencia, la OMS/OPS ha señalado estrategias clave para estos últimos años,
entre las que ha considerado el Proyecto sobre Dispositivos Médicos Prioritarios, la
Encuesta Nacional para consolidación global y la Iniciativa Mundial sobre tecnologías
sanitarias, que incluye la formulación de políticas e instrumentos de gestión sobre
tecnologías sanitarias y la selección de tecnologías innovadoras.
Hoy existen enormes posibilidades de extender coberturas de servicios de salud gracias a
los desarrolios científicos y tecnológicos, que hacen que se conozcan y usen gran
cantidad de tecnologías a beneficio de la salud de la población y que pueden mejorar
extraordinariamente el acceso, la eficiencia y la equidad de la producción social de la
salud, con acciones de carácter ambulatorio, comunitario, y hospitalario.
Para esto es necesario, que nuestros recursos humanos sean competentes en regular,
gestionar, planificar, adquirir, suministrar, usar y vigilar eficientemente esta gran variedad
de tecnologías en pro de la salud de la población.
Palabras del Dr. Fernando Leanes, Representante OPS/OMS en el Perú, Curso
Internacional: Tecnovigilancia y Regulación en Dispositivos Médicos, Lima 2012
Qué es la tecnovigilancia
Se define como el conjunto de actividades que tienen por objeto la identificación y la
cualificación de eventos e incidentes adversos serios e indeseados producidos y/o
asociados con los dispositivos médicos, así como la identificación de los factores de
riesgo asociados a estos, con base en la notificación, registro y evaluación sistemática,
con el fin de determinar la frecuencia, gravedad e incidencia de los mismos para prevenir
su aparición.
La Tecnovigilancia debe ayudar a la identificación, prevención y resolución de los eventos
o incidentes relacionados con el uso de los Dispositivos Médicos por medio de la
evaluación de la causalidad y la gestión del riesgo con el fin de disminuir la carga
de morbi-mortalidad.
Objetivo de la Tecnovigilancia
Objetivo Principal:
Realizar la identificación, recolección, evaluación y seguimiento permanente de los
eventos o incidentes adversos que presentan los dispositivos médicos antes o durante su
uso por medio de la gestión del riesgo con el fin de mejorar la protección de la salud y la
seguridad de los pacientes y personal asistencial coordinando acciones con las
autoridades para tomar las medidas que sean necesarias.
Objetivos Específicos:
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
• Desarroliar actividades de promoción, prevención y formación con las instituciones de
salud del departamento públicas y privadas.
• Realizar seguimiento y gestión de los informes de seguridad, alertas y reportes que se
generan.
• Desarroliar, mantener y fortalecer la Red de Tecnovigilancia.
• Proponer y aplicar las medidas de prevención, vigilancia, control y/o seguimiento a los
casos de eventos adversos detectados.
• Desarroliar e implementar planes y programas de vigilancia y seguimiento activo sobre
dispositivos médicos que supongan alto riesgo de generación de eventos en dispositivos
médicos.
• Transmitir de manera inmediata a la autoridad todo reporte de evento o de incidente
adverso serio cuando es del caso.
• Tomar las medidas de mejoramiento con respecto a los eventos presentados en las
Instituciones Prestadoras de Servicios de Salud y profesionales de la salud.
• Ejecutar las medidas de mejoramiento respecto a los eventos presentados en las
instituciones prestadoras de servicios de salud y profesionales de la salud.
• Implementar y garantizar la continuidad de los mecanismos para identificar, recolectar y
gestionar información sobre eventos a nivel territorial, manteniendo los soportes
estructurales, informáticos y documentales necesarios para el buen desarrolio del
programa en concordancia con lo establecido por el Centro Nacional de Referencia.
Programa Nacional de Tecnovigilancia
El Programa Nacional de Tecnovigilancia se configura como un sistema de vigilancia post-
mercado, constituido por el conjunto de instituciones, normas, mecanismos, procesos,
recursos financieros, técnicos y de talento humano que interactúan para la identificación,
recolección, evaluación, gestión y divulgación de los eventos o incidentes adversos no
descritos que presentan los dispositivos médicos durante su uso, la cuantificación del
riesgo y la realización de medidas en salud pública, con el fin de mejorar la protección de
la salud y la seguridad de los pacientes, usuarios y todo aquel que se vea implicado
directa o indirectamente con la utilización del dispositivo.
Los principios que rigen el Programa Nacional de Tecnovigilancia son los siguientes:
1. Articulación entre los actores del Programa Nacional de Tecnovigilancia.
2. Información veraz, oportuna y confidencial
3. Formación e información permanente de los actores involucrados
4. Trazabilidad de los dispositivos médicos
5. Sensibilidad y representatividad
Vídeos de apoyo
- Tecnovigilancia y la seguridad del paciente
https://www.youtube.com/watch?v=INkHaruBuE4
Material de apoyo para el estudiante
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
Guía para la implementación del Programa Nacional de Tecnovigilancia en el Hospital
General de Medellín. Catalina Vásquez Franco, Mauricio Pérez Trujillo. Revista Ingeniería
Biomédica. 2010.
Tecnovigilancia y Dispositivos Médicos. COHAN, Medellín
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
GUÍAS DE AUTOAPRENDIZAJE
Estas guías te permitirán complementar los temas observados sobre esta
competencia, te sugerimos investigar y desarrollarlas como parte del proceso de
aprendizaje.
El material de esta guía se evalúa en los cuestionarios, los cuales corresponden al
total de nota, de ahí la importancia de desarrollar los
GUÍA Nº 1
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente.
Unidad de Aprendizaje: Normativa legal vigente relacionada con prohibiciones y
obligaciones durante la dispensación. Tipo de información de acuerdo con la dirección
técnica del servicio farmacéutico.
Unidad de Aprendizaje: Procesos especiales de fármacovigilancia y tecnovigilancia.
Unidad de Aprendizaje: Manual de condiciones esenciales y procedimientos de la
institución.
1. De acuerdo con el Decreto 780 de 2016, realice un cuadro comparativo en el que se
muestre:
a. Realice un cuadro comparativo en el que se muestren las obligaciones y
prohibiciones del dispensador
a. Qué tipo de información puede suministrar de acuerdo con su formación académica
(auxiliar de servicio farmacéutico, regente de farmacia, químico farmacéutico).
2. Investigué qué es y para qué sirve el programa de seguridad del paciente
3. Defina:
a. Incidente adverso
b. Evento adverso
c. Complicación
4. ¿Cómo se clasifican los reportes de eventos/incidentes adversos?
5. Investigue qué es farmacovigilancia y todo lo referente con el reporte de casos de este
tipo.
6. Investigue qué es tecnovigilancia, y todo lo referente con el reporte de casos de este
tipo.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
7. Investigue qué es un error de medicación y cómo se clasifican.
8. ¿Cuáles son los errores de medicación que puede cometer usted como dispensador?,
¿qué puede hacer para minimizar los errores de medicación que son de su
competencia?
9. Realice un breve resumen (en mapa conceptual) del contenido del Manual de
condiciones esenciales, especialmente en lo referente a los procesos del servicio
farmacéutico.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
GUÍA Nº 2
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente.
Unidad de Aprendizaje:
Conceptos básicos de farmacología: farmacocinética farmacodinamia
Grupos terapéuticos: uso adecuado, contraindicaciones, advertencias.
Farmacología de analgésicos
1. Defina:
a. Dolor
b. Inflamación
c. Analgesia
2. Investigue para cada uno de los siguientes grupos de medicamentos definición,
mecanismos de acción, clasificación, proceso ADME, indicaciones, contraindicaciones,
principales efectos secundarios y reacciones adversas, nombres comerciales y
productos disponibles en el mercado colombiano:
a. AINES
b. Inhibidores de la ciclooxigenasa II
c. Analgésicos opioides
3. Investigue qué otros analgésicos existen y mencione para estos la misma información
del punto anterior.
Farmacologia de anti-histamínicos
1. Investigue y defina:
a. Histamina d. Reacción alérgica
b. Receptores de histamina e. Shock anafiláctico
c. Funciones de la histamina en el organismo
2. Investigue para cada uno de los siguientes grupos de medicamentos definición,
mecanismos de acción, clasificación, proceso ADME, indicaciones, contraindicaciones,
principales efectos secundarios y reacciones adversas, nombres comerciales y
productos disponibles en el mercado colombiano:
a. Antagonistas de los receptores H1 (antihistamínicos)
b. Antagonistas de los receptores H2
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 77 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
GUÍA Nº 3
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente,
Unidad de Aprendizaje:
Conceptos básicos de farmacología: farmacocinética farmacodinamia
Grupos terapéuticos: uso adecuado, contraindicaciones, advertencias.
Farmacología del sistema cardiovascular
1. Defina:
a. Hipertensión arterial
b. Cifras tensionales normales
c. Factores de riesgo asociados
2. Anatomía y fisiología del sistema cardiovascular
a. Investigué cómo es el funcionamiento del sistema cardiovascular y cada uno de los
órganos que lo conforman.
b. Realice un dibujo en el que se muestre cómo está conformado el sistema
cardiovascular y las partes de los diferentes órganos.
3. Investigue para cada uno de los siguientes grupos de medicamentos definición,
mecanismos de acción, clasificación, proceso ADME, indicaciones, contraindicaciones,
principales efectos secundarios y reacciones adversas, nombres comerciales y
productos disponibles en el mercado colombiano:
a. Diuréticos
b. Betabloqueadores
c. Calcioantagonistas
d. Inhibidores de enzima convertidora de angiotensina
e. Bloqueadores selectivos de receptores de angiotensina II
f. Otros fármacos antihipertensivos (Minoxidil, Nitritos y Nitratos, Vasodilatadores,
otros)
g. Antianginosos
h. Antiarrítmicos
i. Inotrópicos (digitálicos)
j. Hipolipemiantes
k. Hipoglicemiantes
l. Anticoagulantes
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 78 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
GUÍA Nº 4
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente,
Unidad de Aprendizaje:
Conceptos básicos de farmacología: farmacocinética farmacodinamia
Grupos terapéuticos: uso adecuado, contraindicaciones, advertencias.
Farmacología de los antiinfecciosos
1. La célula
a. Realice un dibujo de la célula eucariota y otro de la célula procariota en los que se
muestren todas sus partes
b. Realice un cuadro comparativo entre las dos células
2. Investigue y defina:
a. Infección y tipos de infecciones f. Antibiótico
b. Bacteria y tipos de bacterias g. Antimicótico
c. Hongo y tipos de hongos h. Antiretroviral
d. Virus y tipos de virus i. Antiparasitario
e. Parásito y su clasificación
3. Investigue para cada uno de los siguientes grupos de medicamentos definición,
mecanismos de acción, clasificación, proceso ADME, indicaciones, contraindicaciones,
principales efectos secundarios y reacciones adversas, nombres comerciales y
productos disponibles en el mercado colombiano:
a. Antibióticos Betalactámicos
b. Monobactámicos y Carbapenémicos
c. Inhibidores de la betalactamasa
d. Glucopéptidos
e. Aminoglucósidos
f. Anfenicoles
g. Lincosamidas
h. Macrólidos
i. Tetraciclinas
j. Quinolonas
k. Sulfamidas
l. Otros: Vancomicina, Daptomicina, Linezolide, Tigeciclina.
m.Antimicóticos
n. Antimaláricos
o. Antiparasitarios
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 79 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
p. Antiretrovirales
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 80 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
GUÍA Nº 5
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente,
Unidad de Aprendizaje:
Conceptos básicos de farmacología: farmacocinética farmacodinamia
Grupos terapéuticos: uso adecuado, contraindicaciones, advertencias.
Farmacología sistema gastrointestinal
1. El sistema gastrointestinal
a. Realice un dibujo del sistema gastrointestinal en el que se muestren los órganos y
todas sus partes
b. Investigue y explique la fisiología del sistema gastrointestinal.
2. Investigue y defina:
j. Gastritis
k. Úlcera péptica
l. Dispepsia
m. Reflujo gastroesofágico
n. Diarrea
o. Estreñimiento
3. Investigue para cada uno de los siguientes grupos de medicamentos definición,
mecanismos de acción, clasificación, proceso ADME, indicaciones, contraindicaciones,
principales efectos secundarios y reacciones adversas, nombres comerciales y
productos disponibles en el mercado colombiano:
a. Antagonistas de receptores H2
b. Inhibidores de la bomba de protones
c. Antiácidos
d. Antieméticos y procinéticos
e. Laxantes
f. Antidiarreicos
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 81 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
GUÍA Nº 6
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente.
Unidad de Aprendizaje:
Conceptos básicos de farmacología: farmacocinética farmacodinamia
Grupos terapéuticos: uso adecuado, contraindicaciones, advertencias.
Farmacología del sistema nervioso
4. El sistema nervioso
a. Realice un dibujo del sistema nervioso central en el que se muestre los órganos y
todas sus partes
b. Investigue y explique la anatomía, fisiología y clasificación del sistema nervioso.
c. Realice un dibujo de la neurona y sus partes y explique su función.
5. Investigue y defina:
p. Sedación
q. Anestesia
r. Principios generales de la anestesia
s. Tipos de anestesia y medicamentos empleados para anestesia
t. Premedicación anestésica
u. Enfermedades que afectan el sistema nervioso central
6. Investigue para cada uno de los siguientes grupos de medicamentos definición,
mecanismos de acción, clasificación, proceso ADME, indicaciones, contraindicaciones,
principales efectos secundarios y reacciones adversas, nombres comerciales y
productos disponibles en el mercado colombiano:
a. Anti parkinsonianos
b. Antimigrañosos
c. Antipsicóticos o neurolépticos
d. Ansiolíticos e hipnóticos
e. Antidepresivos y antimaniacos
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 82 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
GUÍA Nº 7
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 01: Brindar información de productos farmacéuticos según
normativa legal vigente.
Unidad de Aprendizaje:
Conceptos básicos de farmacología: farmacocinética farmacodinamia
Grupos terapéuticos: uso adecuado, contraindicaciones, advertencias.
1. Definir:
a. Indicación
b. Contraindicación
c. Interacción
d. advertencias.
2. Medicamentos OTC y de venta bajo fórmula médica
a. ¿Qué significa OTC?
b. ¿Qué medicamentos se denominan OTC?
c. ¿Qué significa “venta bajo fórmula médica?
d. ¿Qué medicamentos son de venta bajo formula médica?
e. ¿Cómo se diferencian los medicamentos OTC de los de venta bajo fórmula médica y
cómo se almacenan?
f. Investigue qué medicamentos son de venta estricta con formula médica.
g. Realice un cuadro en el que se relacionen5 medicamentos de venta bajo formula
médica, 5OTC y 5 dispositivos médicos; debe registrar nombre genérico, nombres
comerciales (por lo menos 2), presentación, sus indicaciones, contraindicaciones y
advertencias.
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
CÓDIGO FTM03-17
GUIAS DE ESTUDIO PROGRAMA VERSIÓN 0
SISTEMA DE
TÉCNICO LABORAL EN
GESTIÓN DE PÁGINA: 83 de 1
CALIDAD AUXILIAR DE FARMACIA
VIGENTE DESDE: Mayo 2 de 2011
GUÍA Nº 8
Norma de Competencia 230101021: Dispensar productos farmacéuticos según
disposiciones legales vigentes.
Elemento de competencia 02: Entregar productos farmacéuticos de acuerdo con la
prescripción médica y disposiciones legales vigentes.
Unidad de Aprendizaje: Medicamentos de control especial
Medicamentos de control especial
1. Defina:
a. Medicamentos de control especial
b. Medicamentos de control especial monopolio del estado
c. Sustancias narcóticas
2. Investigue la resolución 1478 de 2006 y sus modificaciones
a. Realice un mapa conceptual sobre los requisitos requeridos para manejar
medicamentos de control especial en una farmacia y en una droguería.
b. ¿Cuáles son las normas de prescripción para los medicamentos de control especial?
c. ¿Cuáles son las prohibiciones que tienen los medicamentos de control especial?
d. ¿Qué aspectos se deben tener en cuenta para la dispensación y venta de
medicamentos de control especial?
e. ¿Cuáles son sus responsabilidades, como auxiliar de servicio farmacéutico, en el
manejo de medicamentos de control especial?
f. ¿Cuáles son las infracciones y sanciones en las que se puede incurrir en el manejo
de medicamentos de control especial?
g. ¿Cómo se realiza la disposición final, ya sea por avería o por vencimiento, para los
medicamentos de control especial?
Material exclusivo de la ESCUELA LATINOAMERICANA DE FARMACIA, PROHIBIDA SU
REPRODUCCIÓN PARCIAL O TOTAL
También podría gustarte
- Purpura H..Documento7 páginasPurpura H..Lay-Fun Vet100% (3)
- Eett SieDocumento23 páginasEett SieLobojAún no hay calificaciones
- Realizar El ExamenDocumento11 páginasRealizar El ExamenPOLICARPIA VAZQUEZ MENDOZAAún no hay calificaciones
- Poe de Recepcion y Validacion de Recetas - 1Documento3 páginasPoe de Recepcion y Validacion de Recetas - 1Angie Espinoza UribeAún no hay calificaciones
- Exposición - Buenas Prácticas de Dispensación Diana Pilar Basilio Leandro .Documento19 páginasExposición - Buenas Prácticas de Dispensación Diana Pilar Basilio Leandro .Nair Estefani Hancco CruzAún no hay calificaciones
- Procedimientos Operativos Hospital TambobambaDocumento48 páginasProcedimientos Operativos Hospital TambobambaFlavio Mamani Huaihua100% (1)
- Director Técnico REQUISITOSDocumento8 páginasDirector Técnico REQUISITOSthania adela fernandez zuloetaAún no hay calificaciones
- Buenas Practicas de DispensacionDocumento86 páginasBuenas Practicas de DispensacionLiliana Tello PortillaAún no hay calificaciones
- Poes 12Documento3 páginasPoes 12Mariela Livia MoralesAún no hay calificaciones
- Diapositivas Buenas Practicas de AlmacenamientoDocumento63 páginasDiapositivas Buenas Practicas de AlmacenamientoemilyAún no hay calificaciones
- INFOGRAFIA Micro PDFDocumento2 páginasINFOGRAFIA Micro PDFteresa gutierrez100% (1)
- Alerta Digemid #001 - 2022: Anvisa Comunica La Falsificación Del Producto TECENTRIQ (Atezolizumab) 1200mg/20mLDocumento74 páginasAlerta Digemid #001 - 2022: Anvisa Comunica La Falsificación Del Producto TECENTRIQ (Atezolizumab) 1200mg/20mLaliAún no hay calificaciones
- Seguimiento Farmacoterapeutico PersonalizadoDocumento24 páginasSeguimiento Farmacoterapeutico PersonalizadoNemo Pumashonco Chávez100% (1)
- FARMACOVIGILANCIADocumento18 páginasFARMACOVIGILANCIAJeny Ely Alarcon Gomez0% (1)
- Poes Botica NBDocumento26 páginasPoes Botica NBtrabiesoAún no hay calificaciones
- DS No 023-2001 Reglamento de Estupefacientes, Psicotrópicos y Otras SustanciasDocumento33 páginasDS No 023-2001 Reglamento de Estupefacientes, Psicotrópicos y Otras SustanciasAlfonso Bendezu0% (1)
- Manual de Buenas Practicas de DispensacionDocumento31 páginasManual de Buenas Practicas de DispensacionWalter MendozaAún no hay calificaciones
- Buenas Prácticas de Almacenamiento en Farmacias de losEE. SS.Documento51 páginasBuenas Prácticas de Almacenamiento en Farmacias de losEE. SS.LY SHARMELY OVALLE AGUIRREAún no hay calificaciones
- 6 Adquisicion y Recepcion de Productos Farmaceuticosdispositivos Medicos y Productos SanitariosDocumento10 páginas6 Adquisicion y Recepcion de Productos Farmaceuticosdispositivos Medicos y Productos SanitariosJoselyn VillanoAún no hay calificaciones
- Historia Industria FarmacéuticaDocumento44 páginasHistoria Industria FarmacéuticaFonque Sebastian100% (1)
- Manual de Buenas Prácticas de Distribución y Transporte de Productos FarmacéuticosDocumento2 páginasManual de Buenas Prácticas de Distribución y Transporte de Productos FarmacéuticosGilmer Jara Vásquez0% (1)
- EvaluacionDocumento17 páginasEvaluacionpatty tsAún no hay calificaciones
- 1 Perfil FarmacoterapeuticoDocumento6 páginas1 Perfil FarmacoterapeuticoIrmacinaAún no hay calificaciones
- Mapa Conceptual PDFDocumento2 páginasMapa Conceptual PDFSalgado JesúsAún no hay calificaciones
- SEM 9 Y 10 Buenas Practicas de DispensacionDocumento44 páginasSEM 9 Y 10 Buenas Practicas de DispensacionarlethAún no hay calificaciones
- Farmacia Hospitalaria P1Documento151 páginasFarmacia Hospitalaria P1Mariana Lasso100% (1)
- POE Entrega A Domicilio BOTICA WELLNESS PHARMADocumento8 páginasPOE Entrega A Domicilio BOTICA WELLNESS PHARMAerika1707Aún no hay calificaciones
- Procedimientos de Dosis UnitariaDocumento18 páginasProcedimientos de Dosis UnitariaVladimir Condori Melgar100% (1)
- Tecnovigilancia. Zhenia Solis PDFDocumento26 páginasTecnovigilancia. Zhenia Solis PDFRicardo Robles100% (1)
- Semana 16 Farmacias InclusivasDocumento31 páginasSemana 16 Farmacias InclusivasLuis Taipe SanchezAún no hay calificaciones
- Proceso de Certificacion de Farmacias y Boticas en Buenas Practicas de Oficina FarmaceuticaDocumento30 páginasProceso de Certificacion de Farmacias y Boticas en Buenas Practicas de Oficina Farmaceuticavizcaino20Aún no hay calificaciones
- Buenas Practicas de PrescripcionDocumento16 páginasBuenas Practicas de PrescripcionCaroltorres07Aún no hay calificaciones
- Qué Es Una DrogueríaDocumento2 páginasQué Es Una DrogueríakarlyAún no hay calificaciones
- FarmacovigilanciaDocumento28 páginasFarmacovigilanciaDIEGO RIOSAún no hay calificaciones
- Tecnovigilancia 1ra Parte - 05.06.18 PDFDocumento24 páginasTecnovigilancia 1ra Parte - 05.06.18 PDFyEMPAC RegulatorioAún no hay calificaciones
- Tramite de DrogueriaDocumento2 páginasTramite de DrogueriaEduard CBAún no hay calificaciones
- Norma de ..Documento10 páginasNorma de ..Milagros Trujillo MuchaAún no hay calificaciones
- Atención Farmaceutica 1Documento33 páginasAtención Farmaceutica 1Elias ReevesAún no hay calificaciones
- Silabus Tecnicas de Transformacion de Materias Primas 2014Documento4 páginasSilabus Tecnicas de Transformacion de Materias Primas 2014Cesar Giancarlo Jimenez Tellez88% (8)
- Actividad 2 - Taller Recepcion y Almacenamiento N°1Documento1 páginaActividad 2 - Taller Recepcion y Almacenamiento N°1ramiro100% (1)
- Requisitos para Aperturar Una Farmacia o Botica JMD2016Documento89 páginasRequisitos para Aperturar Una Farmacia o Botica JMD2016davidAún no hay calificaciones
- Venta y Dispensacion 2do ExamenDocumento8 páginasVenta y Dispensacion 2do ExamenJaviluz SuxaAún no hay calificaciones
- Calendula OfficinalisDocumento4 páginasCalendula OfficinalisLia Gabriela GonzálezAún no hay calificaciones
- Bpa en EeffDocumento33 páginasBpa en EeffAnonymous MunIEkQ6hAún no hay calificaciones
- AminorexDocumento2 páginasAminorexAlberto Antonio Alvarez AlvaradoAún no hay calificaciones
- Check List SDMDUDocumento2 páginasCheck List SDMDUAmba GuevaraAún no hay calificaciones
- POESDocumento10 páginasPOESleviAún no hay calificaciones
- EXAMEN FINAL DE LEGISLACIÓN FARMACEUTICA-apaesteguiDocumento3 páginasEXAMEN FINAL DE LEGISLACIÓN FARMACEUTICA-apaesteguiMilagros Ruiz paredesAún no hay calificaciones
- Buenas Practicas de PrescripcionDocumento6 páginasBuenas Practicas de PrescripcionVictor Bohorquez FloresAún no hay calificaciones
- Manejo y Llenado de LibrosDocumento10 páginasManejo y Llenado de LibrosvladimirAún no hay calificaciones
- Verificación de RecetasDocumento7 páginasVerificación de RecetasKarenAún no hay calificaciones
- 09 POEs - PSICOTROPICOS Lista IVBDocumento10 páginas09 POEs - PSICOTROPICOS Lista IVBsaydavelconAún no hay calificaciones
- Internado FARMACIADocumento81 páginasInternado FARMACIAJessica Benavides BermudezAún no hay calificaciones
- Mof FarmaciaDocumento11 páginasMof FarmaciaJOBAún no hay calificaciones
- Pasos para Crear FarmaciaDocumento4 páginasPasos para Crear FarmaciaMiguel Diaz SotoAún no hay calificaciones
- MP Droguería Andre'sDocumento75 páginasMP Droguería Andre'sKarolina MesaAún no hay calificaciones
- BOT - POE013 Productos Refrigerados 1Documento4 páginasBOT - POE013 Productos Refrigerados 1NIL CHARLIE MARAÑON PINTOAún no hay calificaciones
- Manual de Organización y Funciones Botica Salud y VidaDocumento12 páginasManual de Organización y Funciones Botica Salud y VidaJosé Gutiérrez ParvinaAún no hay calificaciones
- Cuestionario 2Documento2 páginasCuestionario 2Alejandra Cordova100% (1)
- Dispensar Medicamentos - Material de EstudioDocumento83 páginasDispensar Medicamentos - Material de EstudioDEINER DE JESUS PEREZ MEZAAún no hay calificaciones
- Guía Módulo 3 Introducción A La FarmacologíaDocumento20 páginasGuía Módulo 3 Introducción A La Farmacologíaramon edickson placencia encarnacionAún no hay calificaciones
- Actividad 2 Modulo 2 - Jerry GomezDocumento17 páginasActividad 2 Modulo 2 - Jerry GomezJerry LawrenceAún no hay calificaciones
- Blog de Información Plantas Medicinales SupleDocumento1 páginaBlog de Información Plantas Medicinales SupleGuadalupe Razo PadillaAún no hay calificaciones
- M.rodriguez.-Conoces A Los MicroorganismosDocumento5 páginasM.rodriguez.-Conoces A Los MicroorganismosMaria del Carmen Rodriguez VillalbaAún no hay calificaciones
- Protec LifeDocumento4 páginasProtec LifeKarol MabelAún no hay calificaciones
- 1 Material de Apoyo y Complementario - Nivel II en MicrobiologiaDocumento5 páginas1 Material de Apoyo y Complementario - Nivel II en MicrobiologiaMariana GonzálezAún no hay calificaciones
- Triptico Energy 2013 CorrectoDocumento2 páginasTriptico Energy 2013 CorrectoEnergy EspañaAún no hay calificaciones
- Matriz 4 - 8 Sesiones-Descripción de La Problemática y CríticaDocumento10 páginasMatriz 4 - 8 Sesiones-Descripción de La Problemática y Críticamicke vegaAún no hay calificaciones
- TEC Toma CitologiaDocumento26 páginasTEC Toma CitologiaArled Losada VargasAún no hay calificaciones
- Trombocitopenia PDFDocumento53 páginasTrombocitopenia PDFFrancesca A MedranoAún no hay calificaciones
- JESUS MASTACHE ROMAN No (Recuperado Automáticamente)Documento10 páginasJESUS MASTACHE ROMAN No (Recuperado Automáticamente)Giovanni Bonilla BenítezAún no hay calificaciones
- Esquizofrenia - Thomas Szasz PDFDocumento1001 páginasEsquizofrenia - Thomas Szasz PDFLauraLabadie67% (3)
- Bases de La Convocatoria #02 2021 D.L. 1057 Cas R.O.Documento43 páginasBases de La Convocatoria #02 2021 D.L. 1057 Cas R.O.myg305Aún no hay calificaciones
- Ft-061 Benzatidelt 2.4Documento9 páginasFt-061 Benzatidelt 2.4JOSE LUIS CERONAún no hay calificaciones
- Síndrome de AlströmDocumento8 páginasSíndrome de AlströmGiuliana RidolfiAún no hay calificaciones
- Cutaneous Loxoscelism - En.esDocumento1 páginaCutaneous Loxoscelism - En.esmetafan_1Aún no hay calificaciones
- COLELITIASISDocumento1 páginaCOLELITIASISmargori stefaniAún no hay calificaciones
- Hipertensión GESDocumento17 páginasHipertensión GESOshis18Aún no hay calificaciones
- El Médico Veterinario y Su Función Hacia Los Animales DomésticosDocumento4 páginasEl Médico Veterinario y Su Función Hacia Los Animales DomésticosPianka SpAún no hay calificaciones
- Cote Lizcano Adriana Carolina 2021Documento40 páginasCote Lizcano Adriana Carolina 2021Jennifer AlvearAún no hay calificaciones
- Enfermedades Parasitarias de Los Animales Domesticos PDFDocumento757 páginasEnfermedades Parasitarias de Los Animales Domesticos PDFPaula ParissiAún no hay calificaciones
- Cadena EpidemiológicaDocumento12 páginasCadena EpidemiológicaFernando RuedaAún no hay calificaciones
- Preguntas Mas Frecuentes CartillasDocumento37 páginasPreguntas Mas Frecuentes CartillasLidia Cruz MartinezAún no hay calificaciones
- Anticonceptivos (Yuri)Documento20 páginasAnticonceptivos (Yuri)Yuri Michael Paredes SalcedoAún no hay calificaciones
- Tipos de AbortoDocumento6 páginasTipos de AbortoYorlett Rivera GonzalezAún no hay calificaciones
- Conociendo La MarihuanaDocumento16 páginasConociendo La MarihuanaPatricia Peñalver HernandezAún no hay calificaciones
- CefaleaDocumento5 páginasCefaleaCarolina Velasco de CampoverdeAún no hay calificaciones
- Informe de Laboratorio de Biología1Documento5 páginasInforme de Laboratorio de Biología1Menaly Luzuriaga MoranAún no hay calificaciones
- Sindrome DiarreicoDocumento33 páginasSindrome DiarreicoIan SanCasAún no hay calificaciones
- Ficha Acumulativa de Estudiante Aplicar A Padre de FamiliaDocumento4 páginasFicha Acumulativa de Estudiante Aplicar A Padre de FamiliaIsidro PincayAún no hay calificaciones