100% encontró este documento útil (1 voto)
662 vistas15 páginas1 Reconocimiento de Azucares Reductores
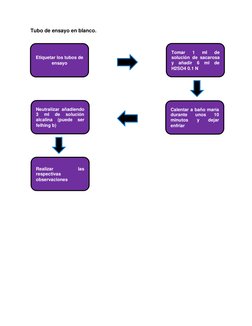
El documento describe una práctica de laboratorio para identificar azúcares reductores. Los estudiantes etiquetaron tubos de ensayo y realizaron pruebas con soluciones de sacarosa, fructosa, glucosa y maltosa usando reactivos de Fehling y calentamiento. La glucosa y la fructosa dieron resultados positivos, indicando que son azúcares reductores, mientras que la sacarosa y la maltosa dieron resultados negativos.
Cargado por
VICTOR ALEJANDRO ROMERO RUIZDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
100% encontró este documento útil (1 voto)
662 vistas15 páginas1 Reconocimiento de Azucares Reductores
El documento describe una práctica de laboratorio para identificar azúcares reductores. Los estudiantes etiquetaron tubos de ensayo y realizaron pruebas con soluciones de sacarosa, fructosa, glucosa y maltosa usando reactivos de Fehling y calentamiento. La glucosa y la fructosa dieron resultados positivos, indicando que son azúcares reductores, mientras que la sacarosa y la maltosa dieron resultados negativos.
Cargado por
VICTOR ALEJANDRO ROMERO RUIZDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd