Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Valorizaciones Con Indicadores: Determinacion de Carbonatos y Fosfatos
Cargado por
Santiago CazorlaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Valorizaciones Con Indicadores: Determinacion de Carbonatos y Fosfatos
Cargado por
Santiago CazorlaCopyright:
Formatos disponibles
LABORATORIO DE QUMICA ANALTICA - UNIVERSIDAD DEL VALLE
VALORIZACIONES CON INDICADORES: DETERMINACION DE CARBONATOS Y FOSFATOS
19 de Octubre de 2016. Departamento de Qumica Universidad del Valle.
Palabras clave: Valoracin, Indicadores, Carbonatos.
Resumen. Mediante la valoracin de dos indicadores, en este caso la fenolftalena y el naranja de
metilo, se determina cuantitativamente la composicin de mezclas de carbonatos en una muestra
acuosa, para el primer punto de equivalencia se utiliz fenolftalena y para el segundo el naranja de
metilo. En la determinacin que se realiz en el mismo vaso se encontr
NaOH , Na2 CO3 y NaHCO 3 . Para cada solucin se calcul la concentracin en mg/mL.
Introduccin. El ion carbonato es un ion
bifuncional esto quiere decir se lleva a cabo una
neutralizacin en dos etapas tmese como
ejemplo un cido H2A el cual se disocia primero
en HA- y luego en A= debido a esto se debe tener
en cuenta que hay presentes dos constantes de
disociacin diferentes una K1 y K2 las cuales son
una muy diferente a la otra ya que una primera
disociacin fuerte y la otra no es tan fuerte (1).
Para este tipo de titulacin se suele titular con
dos indicadores ya que primero se debe tener en
cuenta una disociacin para despus poder tener
en cuenta la segunda disociacin en la cual se
debe usar un indicador diferente un ejemplo de
esto se pudo notar en la prctica donde primero
se titul con el indicador fenolftalena llevando de
un medio bsico a uno bsico para despus de
encontrar el viraje poder llevar a cabo una
segunda titulacin pero utilizando naranja de
metilo pero poder determinar el punto final de la
segunda disociacin para poder cuantificar los
carbonatos los cuales reaccionan por completo
con el HCl que titula dando lugar al H2CO3.
sln0,1 mmol HCl
36,45 mg HCl
1 mL sln
100mg muestra
1mmol HCl
37 mg HCl
1000 mg
100 mL
1,189 g
Para calcular la concentracin real del HCl, se
utiliz el peso del carbonato de sodio como
estndar primario multiplicado por la relacin
estequiometria de la reaccin carbonato de sodio
y HCl (2:1) y por ltimo se multiplica por el
volumen gastado de HCl.
La reaccin qumica que se llev a cabo es:
Na2 CO 3+ 2 HCl 2 NaCl+ H 2 CO 3
H 2 CO 3 H 2 O+CO 2
A continuacin se encuentran los datos de la
estandarizacin del HCl.
Tabla 1. Datos de estandarizacin HCl.
Volumen HCl
estandarizad
o
(
Na 2 CO 3 Volumen de
HCl
gastado
(mg)
mL 0,1 mL
Resultados y discusin.
Para la valoracin de cada solucin problema
hasta el viraje del indicador, se utiliz una
solucin de HCl 0,1 M. Se prepar la solucin
usando 0,82 mL de HCl en 100 mL de agua.
=1,189 g /mL
%P/ P=37
20,5
mL 0,1 mL
100
14,7
Estandarizacin de la solucin de HCl
[ HCl ] =
100 mg Na 2 CO3
20,5mL HCl
)(
1 mmol Na2 CO3
105.99 mg Na2 CO3
)(
1 mmol HC
1 mmol Na 2 C
LABORATORIO DE QUMICA ANALTICA - UNIVERSIDAD DEL VALLE
Se realiza una tabla con la relacin de
volmenes en el anlisis de mezclas de
carbonatos.
Tabla 2. Relacin de volmenes en el anlisis de
mezclas
de
carbonatos
que
contiene
,CO 3 , HCO3
solos o en mezclas compatibles (
OH
Anlisis de carbonatos en un mismo vaso
A continuacin se realiza una tabla donde se
pueden observar los volmenes usados en las
titulaciones.
Tabla 4. Volmenes anlisis de carbonatos en un
mismo vaso.
Muestr
a
+CO 3
CO3 + HCO3
OH ,
mL 0,1 mL
A
B
C
Componentes
de la muestra
Relacin entre volmenes
de indicadores en la
titulacin de volmenes
iguales de muestra
Fenolftalena(f) y Naranja
de Metilo (nm)
NaOH
V f =V nm
Na2 CO 3
1
V f = V nm
2
NaHCO3
V f =0 ; V nm >0
NaOH + Na2 CO 3
1
V f > V nm
2
Fenolftalena
Naranja
Metilo
[1]
de
3,1-4,4
Solucin A
Los mL de HCl gastado en la valorizacin de los
indicadores tienen concentracin 0,0460 M
1
V f > V nm contiene NaOH+ Na 2 CO 3
2
(Vf -Vnm) titula
Na 2 CO 3
HCO3 proveniente de CO3
+ HCO3
CO3 + H
mmol HCO 3 =mmol
Tabla 3. Puntos de viraje de los indicadores acidobase utilizados.
Color
cido
Incolo
ro
Rojo
10
8,3
6,8
El Vf titula NaOH y
Para realizar el anlisis es necesario tener en
cuenta los puntos de viraje de los indicadores
utilizados.
pH
viraje
8,0-9,8
12,3
13,5
0,2
Na 2 CO 3+ NaHCO 3
1
V f < V nm
2
Indicador
Volumen (mL) de HCl gastado
con indicador
Fenolftaleina Naranja de Metilo
(
( mL 0,1 mL
Color bsico
Rojo
mmol
CO3 = (Vf -Vnm)*MHCl
CO3 = (12,3-10)*0,0460=0,1058
0,1058 mmol Na2 CO3
105,988 mg Na2 CO3
5 mL
mg
=2,24
Na C
1 mmol Na2 CO 3
mL 2
El Vf titula NaOH y
Na 2 CO 3
mmol NaOH+mmol
CO3 = Vf *MHCl
Anaranjado
LABORATORIO DE QUMICA ANALTICA - UNIVERSIDAD DEL VALLE
=12,3*0,0460=0,5658
mmol NaOH=0,5658-0,1058=0,46 mmol NaOH
0,46 mmol NaOH
40 mg NaOH
5 mL
mg
=3,68
NaOH
1 mmol NaOH
mL
mol HCl
( 0.0460
1000 mL sln )
2
+ mol CO3
mol OH
6,21 x 104 moles=
6,21104 mol3,818104 moles
4
2,39210 mol NaOH
Solucin B
Los mL de HCl gastados con indicador
fenolftalena se encuentran en la tabla 4.
Las especies presentes que se deducen de la
tabla 2 en la solucin fueron NaOH y Na 2CO3,
entonces:
Con la fenolftalena se titulan los iones OH- y
CO32-
13,5 mL HCl
mg Na2 CO 3
1
=8,09
5.0 mL sln B
mL
2.3104 mol NaOH
39.997 x 10 mg NaOH
1 mol NaOH
( 5.0 mL1 sln B )=1,8410
mgNaOH
mL
Solucin C
Segn la tabla 2 la especie presente en la
solucin era NaHCO3.
Fenolftalena
0,2 mL HCl
mol HCl
( 0.0460
1000 mL sln )(
1mol Na2 CO3
1mol HCl
9,210 mol Na2 CO3
Con el naranja de metilo se titula el ion
HCO3
bicarbonato
procedente
disolucin del ion carbonato
8,3 mL HCl
0.0460 mol HCl
1000 mL sln
de
la
Con las moles de anteriores se procede a hallar
concentracin de Na2CO3 as
9,2 x 10
3
105.99 x 10 mg Na2 CO 3
( 6 mol Na2 CO 3)
1 mol Na2 CO 3
CO3 .
)(
1 mol NaH CO3
1 mol HCl
( 5.0 mL1 sln C )=0,1950
3.818 10 moles NaH CO 3
Las moles de NaHCO3 pueden convertirse
estequiometricamente con las de NaCO 3,
entonces se hall la concentracin del NaCO 3 y
las moles y concentracin del NaOH.
105.99 x 103 mg Na 2 CO3
3.818 x 10 mol N a2 CO3
1 mol Na 2 CO 3
4
mg Na2 CO 3
mL
Naranja de metilo
6,8 mL HCl
0.0460 mol HCl
1000 mL sln
3,128104 mol NaH CO3
() 1 mol1molNaHHClCO )
3
LABORATORIO DE QUMICA ANALTICA - UNIVERSIDAD DEL VALLE
As ya teniendo las moles anteriores se hall la
concentracin de HCO3.
3,128 x 10
3
84,00810 mg NaH CO3
( 4 mol NaH CO3 )
1 mol NaH C O3
( 5.0 mL1 sln C )=5,255
mg NaH CO3
mL
Tabla 3. Volmenes anlisis de carbonatos en vasos
separados
Volumen (mL) de HCl gastado
con indicador
Fenolftalena + Naranja
de
25 mL Agua
Metilo+ 50 mL
(
agua
(
mL 0,1 mL
A
B
C
11
8,8
1,3
0.0460 mol HCl
1000 mL sln
mg Na2 CO3
1
=10,73
5.0 mL sln A
mL
22,2 mL HCl
mol HCl
( 0.0460
1000 mL sln )(
1mol NaH CO3
1 mol HCl
1,02103 mol NaH CO 3
Se procede a hallar las moles reales de HCO3- en
la segunda titulacin.
5,06104 mol HCO3
1.02103 mol HCO 3
mL 0,1 mL
5,14104 mol HCO3
22,2
12
7
Debido a que se utilizaron las mismas soluciones
para el anlisis en vasos separados, ya se sabe
que especies se encuentran en cada solucin.
Solucin A
Con fenolftalena
11 mL HCl
Con naranja de metilo
Anlisis de carbonatos en vasos separados
A continuacin se realiza una tabla donde se
pueden observar los volmenes usados en las
titulaciones.
Muestr
a
5,0610
105,99mg Na2 CO 3
( 4 mol Na2 CO3 )
1 mol Na2 CO 3
)(
1 mol Na2 CO3
1 mol HCl
Con las moles halladas se puede calcular la
concentracin del segundo soluto as:
84.008 x 10 mg NaH CO 3
5,1410 mol NaH CO 3
1 mol NaH CO 3
4
mg NaH CO 3
1
=8.64
5.0 mL sln A
mL
5,0610 mol Na 2 CO 3
Ya con las moles de Na2CO3 se puede hallar la
concentracin
Solucin B
En este proceso se titulan los iones OH - y CO32,
como en el otro procedimiento:
Fenolftalena
LABORATORIO DE QUMICA ANALTICA - UNIVERSIDAD DEL VALLE
8,8 mL HCl
3
4,048104 moles1,472104 mol CO
mol HCl
( 0.0460
1000 mL sln )
2
+mol CO 3
mol OH
4,048 104 moles=
2.57104 mol NaOH
Con este dato
concentracin
2.57104 mol NaOH
Se lleva a cabo el mismo clculo con el indicador
naranja de metilo
se
2+ mol HCO3
+mol CO 3 )
mol OH
1.3 mL HCl
la
39.997 x 103 mg NaOH
1 mol NaOH
mol HCl
( 0.0460
1000 mL sln )(
1mol Na2 CO3
1mol HCl
5,98105 mol Na 2 CO 3
Se halla la concentracin de Na2CO3
5,52104 moles4,048 x 104 moles
5,98 x 10
3
105.99 x 10 mg Na 2 CO 3
5
mol
Na
CO
(
2
3)
1 mol Na 2 CO 3
1,472104 mol HCO3
Ya que las moles del NaHCO3 se pueden hacer
estequiometricamente equivalentes a las de
Na2CO3, entonces se puede hallar la
concentracin del Na2CO3.
mg Na2 CO 3
1
=3,12
5.0 mL sln B
mL
Para hallar las moles de NaOH se sustituyeron
las moles del ion carbonato y se despejaron:
mg Na2 CO 3
1
=1,27
5.0 mL sln C
mL
105.99 x 103 mg Na2 CO 3 Naranja de metilo
1,472 x 10 mol Na2 CO 3
1 mol Na2 CO3
0.0460 mol HCl
7 mL HCl
1000 mL sln
hallar
Solucin C
Fenolftalena
Se hallan las moles de NaHCO3 as:
puede
( 5.0 mL1 sln B )=2,05 mgNaOH
mL
0.0460 mol HCl
12 mL HCl
=5,52104 moles
1000 mL sln
ya
)(
1 mol NaH CO3
1 mol HCl
3.22104 mol NaH CO3
Con esas moles encontradas se puede hallar la
concentracin del NaHCO3
LABORATORIO DE QUMICA ANALTICA - UNIVERSIDAD DEL VALLE
3.22 x 10
3
84.004 x 10 mg NaH CO3
4
mol
NaH
CO
(
3)
1 mol NaH CO 3
mg NaH CO3
1
=5,40
5.0 mL sln C
mL
Discusin de resultados
Se titularon muestras de soluciones acuosas
desconocidas las cuales se supone deben
contener el Ion CO3 las cuales fueron la
sustancia A, B y C para esto se evaluaron 5 mL
de cada una de las tres sustancias de manera
individual y de dos mtodos 5 mL se titularon en
un solo vaso mientras otros 5 mL se llevaron a
cabo en 2 vasos para esto se titul con un con
cido clorhdrico el cual reaccionaria con el ion
carbonato el cual se encontrara en medio
alcalino al momento de llevar acabo la primer
reaccin se pudo observar mediante el indicador
de fenolftalena que cuando todos los CO3
reaccionan con el cido el medio se torna
traslucido lo que significa que en ese momento
tengo en solucin HCO3 de esta manera se
procede a evaluar con naranja de metilo el cual
evala que tana acido se tornara al seguir
agregando cido clorhdrico ya que el HCO3
reacciona con los iones H+ presentes en el medio
de y esta manera llega a formar H2CO3 en el
momento en que sucede esto el indicador Nara
de metilo llega a su viraje.
En este mtodo se puede tener presente que es
mejor realizar la medicin en un solo vaso que en
dos ya que de la segunda manera se puede
producir un error sistemtico de manera ms fcil
que cuando se trabaja en un mismo vaso.
Hay que tener en cuenta que cuando se lleva un
volumen relativamente grande hay una presencia
de iones OH- en el medio en una cantidad que no
puede ser despreciada por lo que no se
consideran los iones OH- que son aportados por
en agua en este momento. Segn la valoracin
se pudo determinar que la solucin A esta
compuesta principal mente de una mezcla entre
CO3 en su mayora y HCO 3 esto debido al
volumen que se gast y teniendo en cuenta la
relacin que existe entre los indicadores. En la
solucin B se tiene presente que hay presencia
de Iones OH- y NaCO3 por que el volumen que
se gast en la titulacin con la fenolftalena fue el
doble del que se gast con el naranja de metido.
Teniendo en cuenta la gran diferencia de
volumen que se gast para llevar acabo el viraje
en el naranja de metilo y el poco volumen que se
gast en el viraje para la fenolftalena se
concluy que la solucin C est compuesta
principalmente de NaHCO3.
Conclusiones
Al titular el ion carbonato con un cido fuerte se
debe tener en cuenta la naturaleza bifuncional de
este; Los indicadores son sumamente tiles para
saber cundo termina de reaccionar el ion con el
cido fuerte.
Bibliografa
[1] Harold F Walton, Jorge reyes. Anlisis
qumico e instrumental moderno. Editorial reverte
S.A. Barcelona 2006 capitulo 7 Pag 23 a 26
[2] GLEN.BROWN. Qumica cuantitativa. 1ra
edicin. Editorial reverte S.A. Barcelona 1967.
Captulo 7. Indicadores qumicos para reacciones
de neutralizacin. Pg.: 206-213.
También podría gustarte
- Aprendizajes Esperados de La Materia de Español y MatematicasDocumento44 páginasAprendizajes Esperados de La Materia de Español y MatematicasToñOo Castrillo100% (4)
- Sintesis de Un Compuesto de Coordinacion Cloruro de Hexaamin Cobalto IIIDocumento9 páginasSintesis de Un Compuesto de Coordinacion Cloruro de Hexaamin Cobalto IIICristobal Alexander Coto VelazquezAún no hay calificaciones
- Práctica 4 - Titulación Ácido-BaseDocumento6 páginasPráctica 4 - Titulación Ácido-BaseMaria CastilloAún no hay calificaciones
- Informe #8Documento4 páginasInforme #8Mateo Martínez ValenciaAún no hay calificaciones
- Informe-Volumetria de Precipitacion, Curvas de Valoracion - Volumetria de Formacion de Complejos (Autoguardado)Documento17 páginasInforme-Volumetria de Precipitacion, Curvas de Valoracion - Volumetria de Formacion de Complejos (Autoguardado)jairo guerreroAún no hay calificaciones
- CR (Acac) 3Documento2 páginasCR (Acac) 3Davis Bernardo0% (2)
- PrecipitaciónDocumento1 páginaPrecipitaciónIsa MarAún no hay calificaciones
- Carbonatos y Fosfatos Informe 0956956Documento7 páginasCarbonatos y Fosfatos Informe 0956956Jose_Warrner_H_7234Aún no hay calificaciones
- An Alisis de Una Mezcla de Carbonato y BicarbonatoDocumento11 páginasAn Alisis de Una Mezcla de Carbonato y BicarbonatoRicardo PardeyAún no hay calificaciones
- Informe #03 Isomeros GeometricosDocumento7 páginasInforme #03 Isomeros GeometricosJoHana BolañosAún no hay calificaciones
- INFODocumento6 páginasINFOsandraAún no hay calificaciones
- Determinacion Del Contenido de Calcio en Una Caliza Mediante Volumetria Redox Con Pergamanato de PotasioDocumento4 páginasDeterminacion Del Contenido de Calcio en Una Caliza Mediante Volumetria Redox Con Pergamanato de Potasionepertorres6169100% (1)
- INFORME-Solucion de Tiosulfato de SodioDocumento8 páginasINFORME-Solucion de Tiosulfato de SodioJosé MolinaAún no hay calificaciones
- Informe 1 - 4° SemestreDocumento7 páginasInforme 1 - 4° SemestreJohan Lf CalderonAún no hay calificaciones
- Isomeros FinalDocumento5 páginasIsomeros FinalJohanna GalanAún no hay calificaciones
- Crecimiento de Cristales Olga LuciaDocumento7 páginasCrecimiento de Cristales Olga Luciadinobile10Aún no hay calificaciones
- Determinacion Del Contenido de Hipoclorito de Sodio en Un Producto Comercial y El Contenido de Yodo en Un Anticeptico BucalDocumento7 páginasDeterminacion Del Contenido de Hipoclorito de Sodio en Un Producto Comercial y El Contenido de Yodo en Un Anticeptico BucalAlejandro Lara ResendízAún no hay calificaciones
- Examen Preliminar P - CLOROANILINADocumento4 páginasExamen Preliminar P - CLOROANILINAAlejandra ZeaAún no hay calificaciones
- Laboratorio de Química Analítica ClorurosDocumento5 páginasLaboratorio de Química Analítica ClorurosKatherine CendalesAún no hay calificaciones
- Informe 4. Titulaciones de Precipitación FINALxDocumento5 páginasInforme 4. Titulaciones de Precipitación FINALxCamiloAún no hay calificaciones
- Isomeros GeometricosDocumento6 páginasIsomeros GeometricosSebastián Tovar Molina100% (1)
- VOLUMETRÍA REDOX Permanganato FINAL Gaby JohanDocumento4 páginasVOLUMETRÍA REDOX Permanganato FINAL Gaby JohanGABRIELA ANDREA VELEZ CERONAún no hay calificaciones
- Informe #7 Valoraciones Por Formación de ComplejosDocumento5 páginasInforme #7 Valoraciones Por Formación de ComplejosLinaRodriguez0126Aún no hay calificaciones
- Determinación Gravimetrica Del NíquelDocumento5 páginasDeterminación Gravimetrica Del NíquelSamuel Fernando DelgadoAún no hay calificaciones
- Determinaciòn de La Constante de Equilibrio de Una Reaccion HomogeneaDocumento6 páginasDeterminaciòn de La Constante de Equilibrio de Una Reaccion HomogeneaJonatan David75% (4)
- Volumetría Por Formación de Precipitados (Ramos)Documento5 páginasVolumetría Por Formación de Precipitados (Ramos)Alex LumbardoAún no hay calificaciones
- Síntesis Análisis Hidratos Oxalatos Metálicos Grupo 2Documento7 páginasSíntesis Análisis Hidratos Oxalatos Metálicos Grupo 2Mayra Alejandra Balanta RamirezAún no hay calificaciones
- Guía de Seminarios Química Inorgánica - 2020 - FINAL ENVIADADocumento95 páginasGuía de Seminarios Química Inorgánica - 2020 - FINAL ENVIADADiego Moya100% (1)
- Analisis GravimetricoDocumento13 páginasAnalisis GravimetricoDavidAún no hay calificaciones
- Informe 09Documento11 páginasInforme 09Nicolh EnríquezAún no hay calificaciones
- Informe de La Parra 1Documento4 páginasInforme de La Parra 1Foxy4DAún no hay calificaciones
- Sintesis de Isomeros GeometricosDocumento19 páginasSintesis de Isomeros GeometricosJUAN DANIEL GIRALDO MUÑOZAún no hay calificaciones
- Determinación de Cloruro en Orina y en Un Suero Fisiológico Mediante Metodo Argentometrico y Método de Electrodo Selectivo de Iones CloruroDocumento8 páginasDeterminación de Cloruro en Orina y en Un Suero Fisiológico Mediante Metodo Argentometrico y Método de Electrodo Selectivo de Iones CloruroJuan Carlos Portillo Villarruel100% (1)
- Yoduro de CobreDocumento5 páginasYoduro de Cobrealejandro harukar100% (1)
- Titulaciones ArgentométricasDocumento4 páginasTitulaciones Argentométricasnata fallaAún no hay calificaciones
- 10 CDocumento6 páginas10 CJuan PabloAún no hay calificaciones
- Ejercicios Clase 8Documento60 páginasEjercicios Clase 8marcosAún no hay calificaciones
- Determinación de Hierro (Practica Nº3) IMPRIMIRDocumento8 páginasDeterminación de Hierro (Practica Nº3) IMPRIMIRJean Pierre Cirilo SosaAún no hay calificaciones
- Determinacion de La Curva de Solubilidad FINALDocumento10 páginasDeterminacion de La Curva de Solubilidad FINALmariaAún no hay calificaciones
- 2010 - PROBLEMAS CLASE 2010 Página WebDocumento7 páginas2010 - PROBLEMAS CLASE 2010 Página Webph0714Aún no hay calificaciones
- Guia Titulacion Complejometrica 2S 2019 532326Documento2 páginasGuia Titulacion Complejometrica 2S 2019 532326Kristofer Bonilla0% (1)
- Volumetría Por PrecipitaciónDocumento4 páginasVolumetría Por PrecipitaciónbyronAún no hay calificaciones
- Determinacion Del Contenido de Nitrog No Por El M Todo de MicroKjeldahlDocumento5 páginasDeterminacion Del Contenido de Nitrog No Por El M Todo de MicroKjeldahlLeonel Luna NawnesterAún no hay calificaciones
- Ácidos y Bases, Valoracion de Acido Clorhidrico y de Hidroxido de Sodio Por Titulacion PDFDocumento6 páginasÁcidos y Bases, Valoracion de Acido Clorhidrico y de Hidroxido de Sodio Por Titulacion PDFJhon Cristian Urrego RodriguezAún no hay calificaciones
- 27 Sintesis FerrofluidoDocumento6 páginas27 Sintesis FerrofluidoJuan David Benitez MonroyAún no hay calificaciones
- Valorizaciones IndicadoresDocumento10 páginasValorizaciones IndicadoresmariaAún no hay calificaciones
- CUESTIONARIODocumento3 páginasCUESTIONARIOJuan Miguel VelezAún no hay calificaciones
- 4 Preparación y Caracterización Del Cis y Trans-Diclorobisetilendiaminocobalto (III)Documento10 páginas4 Preparación y Caracterización Del Cis y Trans-Diclorobisetilendiaminocobalto (III)Javier Mauricio Posada CabreraAún no hay calificaciones
- PrecipitacionDocumento17 páginasPrecipitacionKarina Caudillo GamezAún no hay calificaciones
- Práctica ComplejometríaDocumento3 páginasPráctica Complejometríastick9510100% (1)
- Reporte Fisico QuimicaDocumento8 páginasReporte Fisico QuimicaFelipe VilchesAún no hay calificaciones
- Nomenclatura de AlcoholesDocumento9 páginasNomenclatura de AlcoholesCristian Edwin Machaca RamosAún no hay calificaciones
- Analisis de Cationes Del Tercer GrupoDocumento7 páginasAnalisis de Cationes Del Tercer GrupoYessenia AlejoAún no hay calificaciones
- Determinación de Carbonato y Bicarbonato en Una MuestraDocumento2 páginasDeterminación de Carbonato y Bicarbonato en Una MuestraSantiago MoralesAún no hay calificaciones
- Informe - Volumetría Porprecipitación ArgentométricaDocumento5 páginasInforme - Volumetría Porprecipitación ArgentométricaSergio CaminosAún no hay calificaciones
- Lab 2. Soluciones AmortiguadorasDocumento4 páginasLab 2. Soluciones AmortiguadorasRoger RamosAún no hay calificaciones
- YodometriaDocumento6 páginasYodometriaAndres MorenoAún no hay calificaciones
- Determinación Del Contenido de Hipoclorito Sódico en UnDocumento6 páginasDeterminación Del Contenido de Hipoclorito Sódico en UnLuisa SandovalAún no hay calificaciones
- Cálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaDe EverandCálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaCalificación: 5 de 5 estrellas5/5 (1)
- Determinación de Carbonatos y Fosfatos en Una Muestra AcuosaDocumento12 páginasDeterminación de Carbonatos y Fosfatos en Una Muestra Acuosachelsea00001Aún no hay calificaciones
- Valoraciones Con Dos IndicadoresDocumento17 páginasValoraciones Con Dos IndicadoresJennifer MacaAún no hay calificaciones
- Historia de La MecánicaDocumento4 páginasHistoria de La Mecánicadiegodimei33% (3)
- Concreto Armado 1Documento38 páginasConcreto Armado 1Pamela YupanqAún no hay calificaciones
- Introduccion A La Mecanica CuanticaDocumento66 páginasIntroduccion A La Mecanica CuanticaLevi ZufAún no hay calificaciones
- Crossover 3vias 2Documento7 páginasCrossover 3vias 2Cecilia CondeAún no hay calificaciones
- 1 Técnicas de Control para Sistemas SISO No Clásicos - (YA)Documento28 páginas1 Técnicas de Control para Sistemas SISO No Clásicos - (YA)tirat_aunpozoAún no hay calificaciones
- Primer Examen de RankingDocumento5 páginasPrimer Examen de RankingJCamposanoGCAún no hay calificaciones
- Etm - Lampara Fluoresc T9Documento80 páginasEtm - Lampara Fluoresc T9franklinAún no hay calificaciones
- Anexo1 - Plantilla - Entrega - Tarea 1Documento26 páginasAnexo1 - Plantilla - Entrega - Tarea 1Mariana PinedaAún no hay calificaciones
- HistoryDocumento2 páginasHistoryBryan Briceño ChihuanAún no hay calificaciones
- P 1Documento3 páginasP 1laumedinaAún no hay calificaciones
- Tema 3 - Estatica Del Cuerpo RigidoDocumento22 páginasTema 3 - Estatica Del Cuerpo RigidoDaniel Garcia0% (1)
- Ensayo 1Documento4 páginasEnsayo 1Andrea Flores AcflAún no hay calificaciones
- Practica #3 Alcalinos TerreosDocumento3 páginasPractica #3 Alcalinos TerreosKath MedaAún no hay calificaciones
- ALGEBRA Producto Académico 3Documento4 páginasALGEBRA Producto Académico 3HERBERT AMADEUS FERNANDEZ ROSALESAún no hay calificaciones
- Riesgos de Choque ElectricoDocumento25 páginasRiesgos de Choque Electricotiburon53Aún no hay calificaciones
- Fisiología de La OclusiónDocumento20 páginasFisiología de La OclusiónJorgeBetancourt100% (1)
- Fisica (Dinamica Lineal y Rozamiento - Trabajo Mecanico y Potencia Mecanica)Documento2 páginasFisica (Dinamica Lineal y Rozamiento - Trabajo Mecanico y Potencia Mecanica)Edson Luis Egusquiza CordovaAún no hay calificaciones
- Tabla de Funciones de Bessel y Raíces de Ecuaciones Trascendentes RelacionadasDocumento1 páginaTabla de Funciones de Bessel y Raíces de Ecuaciones Trascendentes RelacionadasFernando Vidal OlmosAún no hay calificaciones
- Laboratorio # 3 (Fuerza Sobre Superficies Planas)Documento3 páginasLaboratorio # 3 (Fuerza Sobre Superficies Planas)Juan Jose Perez0% (1)
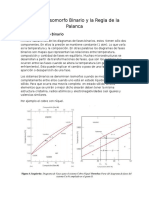
- Sistema Isomorfo Binario y La Regla de La PalancaDocumento3 páginasSistema Isomorfo Binario y La Regla de La PalancaCarlos Abraham Paniahua Pérez100% (1)
- Mapa ConceptualDocumento6 páginasMapa ConceptualNelida Galindo MendezAún no hay calificaciones
- Preparatorio 7 Lizeth SigchaDocumento16 páginasPreparatorio 7 Lizeth SigchaChristopher Castro DavilaAún no hay calificaciones
- Reporte 3 - 4 Cizallamiento y AplastamientoDocumento24 páginasReporte 3 - 4 Cizallamiento y AplastamientoArturo PinedaAún no hay calificaciones
- Anàlisis Matemàtico II - UTP-2013-IIDocumento15 páginasAnàlisis Matemàtico II - UTP-2013-IIJhon Torres CastilloAún no hay calificaciones
- Manual de Soldadura Oerlikon EXSA S.A.Documento146 páginasManual de Soldadura Oerlikon EXSA S.A.Leo Garcia Diaz100% (1)
- Procedimiento Hot TapDocumento6 páginasProcedimiento Hot Tapalex navarreteAún no hay calificaciones
- LABORATORIO de FÍSICA III - Curvas EquipotencialesDocumento24 páginasLABORATORIO de FÍSICA III - Curvas EquipotencialesJorge Andres Naveros100% (1)
- Manual de Instrucciones y Mantenimiento - Equipos AlternosDocumento35 páginasManual de Instrucciones y Mantenimiento - Equipos AlternosJesus CondoriAún no hay calificaciones