Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Curva de absorción binaria
Cargado por
Francisco Jiménez BarrónTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Curva de absorción binaria
Cargado por
Francisco Jiménez BarrónCopyright:
Formatos disponibles
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
TECNOLGICO NACIONAL DE
MXICO
INSTITUTO TECNOLGICO DE MINATITLN
Prctica No.3
Curva de absorcin de una mezcla binaria.
Alumnos.Diana del Carmen Jimnez Lpez
Vianey Ostos Santos
ngel Francisco Jimnez Barrn
Juana del Carmen Mrquez Gmez
Jonathan Lemuel Morales Osorio
Nmero de quipo:
2B
Catedrtico:
M.C. Gabriela Garca Rodrguez
Materia.Anlisis Instrumental
Carrera:
Ingeniera Qumica
Minatitln, Ver a 28 de Abril 2016.
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
Objetivo.
Comprobar que la absorbancia de una mezcla binaria a determinadas longitudes
de onda es igual a la suma de las absorbancias de cada componente que
conforma dicha mezcla.
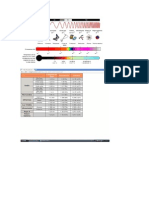
Marco terico.
Imaginemos un dispositivo experimental como el de la siguiente Figura 3.
Disponemos de una fuente emisora de radiacin electromagntica (lmpara), unos
sistemas
de
enfoque
(rendijas)
para
hacer
que
la
radiacin
incida
perpendicularmente a la muestra, un dispositivo que permita seleccionar la
longitud de onda que incide sobre la muestra (red de difraccin) y un sistema
electrnico de medida de intensidad de luz.
Imaginemos tambin que hacemos dos medidas de la intensidad de luz:
1) La primera medida la muestra ser una disolucin con la misma matriz que el
analito que deseemos determinar pero en ausencia de ste (disolucin blanco). La
intensidad de radiacin (luz) que llega al lector ser
2) La segunda medida se har en presencia del analito (cromforo) que deseemos
estudiar. En este caso la intensidad de luz que llega al lector ser I. Como
trabajamos con analitos que absorben radiacin a la longitud de onda que
selecciona la red de difraccin, lgicamente
Existen dos maneras de expresar la relacin entre I e Io. La relacin directa se
denomina transmitancia (T), mientras que se denomina absorbancia al logaritmo
con signo cambiado de la transmitancia. La absorbancia es un trmino
actualmente mucho ms utilizado que la transmitancia.
La expresin matemtica de ambos parmetros es:
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
La ley de Lambert-Beer establece que la absorbancia est directamente
relacionada con las propiedades intrnsecas del analito, con su concentracin y
con la longitud de la trayectoria del haz de radiacin al atravesar la muestra. La
expresin matemtica de la ley de Lambert-Beer es:
A= C.
.L
donde:
A = Absorbancia de la muestra
C = Concentracin del cromforo
L = Longitud del paso ptico que contiene la muestra.
= Absorptividad molar. Depende del cromforo en si mismo, de la
y de las
condiciones de medida (pH, T...). Ya que la absorbancia es adimensional las
unidades son concentracin-1 longitud-1.
Actividades pre-laboratorio.
Investigu y de respuesta brevemente a las siguientes preguntas
a. Explique brevemente la propiedad aditiva de la Ley de Beer establece para
la absorbancia, indicando las aplicaciones principales de esta propiedad.
b. Represente el sistema de ecuaciones que se pueden plantear con base en
la Ley de Beer, para una mezcla binaria cuya concentracin de
componentes se quiere determinar. Indique el significado de cada variable.
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
Equipo, materiales y reactivos.
Equipo
Reactivos y soluciones
4 vasos de precipitado de 50 ml
1 pipeta volumtrica de 3 ml
1 pipeta volumtrica de 2 ml
1 pipeta volumtrica de 1 ml
1 perilla
1 pizeta de agua destilada
3 celdas de metacrilato de 1 cm
KMnO4
cido
K2Cr2O7 5x10-4 M en medio
cido
Mezcla binaria de KMnO4 y
5x10-4 M en medio
K2Cr2O7
Metodologa
1. Encender el espectofotometro UV-VIS marca Genesys 20. Esperar 30
minutos para que la lampara alcance su mxima intensidad
2. En dos vasos de precipitado de 50 ml depositar por separado 5 ml de
K2Cr2O7 5x10-4 M y KMnO4 5x10-4 M, ambas soluciones preparadas en
medio cido
3. Correr el espectro de absorcin de K2Cr2O7 5x10-4 M en medio cido,
desde un valor de 330 con un barrido de 20 en 20 hasta 590 nm.
4. Correr el espectro de absorcin de KMnO4 5x10-4 M en medio cido en el
mismo rango indicado en el punto anterior
5. Identificar la longitud de onda a la cual se obtiene el mximo valor de
absorbancia de nada una de las soluciones.
6. Preparar una mezcla binaria de las soluciones analizadas, de acuerdo a las
indicaciones del profesor.
7. Correr el espectro de la mezcla de KMnO4 y K2Cr2O7 a las longitudes de
onda identificadas en el punto 5, determinando los valores de absorbancia
I.
obtenidos
Calculo, resultados y actividades pos-laboratorio
De manera individual:
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
1. Elaborar
las
tablas
de
longitud
de
onda
contra
absorbancia
correspondientes a cada una de las soluciones
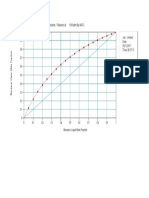
2. En un papel milimtrico, graficar las curvas de absorcin de las respectivas
soluciones.
3. Calcular el coeficiente de Absortividad molar del KMnO4 y K2Cr2O7 a cada
una de las longitudes de onda identificadas en el punto 5 de la metodologa.
4. Utilizar el sistema de ecuaciones necesario para obtener la concentracin
de los componentes que conforman la mezcla binaria.
5. Qu observaciones puede realizar en relacin a las longitudes de onda
analtica identificadas en la prctica No. 2, cuando se obtuvieron los
espectros de absorcin de KMnO4 y K2Cr2O7 utilizando agua destilada
como disolvente, comparadas con los valores de longitud de onda analtica
obtenidos utilizando como disolvente un medio cido? Si hubo cambio en
los valores mencionados, qu tipo de desplazamiento se present?.
6. Formular sus conclusiones.
7. Reportar la informacin anterior en la bitcora personal y en el reporte por
equipo.
DESARROLLO
1.- Lo primero que hicimos fue Encender el espectrofotmetro UV.-VIS Marca
Genesys 20. Esperamos 30 minutos para que la lmpara alcance su mxima
intensidad.
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
2.- Escogimos el material y lo ms importante elegimos nuestras celdas que es
parte fundamental para la prctica.
3.- Limpiamos bien nuestras celdas con un pao suave y con guantes de ltex
para obtener mejores resultados
4.-Posteriormente en nuestro vaso de precipitado de 50 mL colocamos 5 mL de
cido sulfrico 0.2 N que sera nuestra solucin en blanco.
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
5.- En los siguientes vasos de precipitado 2 vasos de precipitado colocamos en
uno dicromato de potasio 5ml y en el segundo permanganato de potasio 5 ml.
6.- Cuidadosamente colocamos el dicromato de potasio y el permanganato en
celdas para nuestro espectrofotmetro y el cido sulfrico en otro que sera
nuestro blanco.
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
7.-Nos dirigimos al rea que se encuentra nuestro espectrofotmetro y colocamos
nuestro espectrofotmetro en 330 y comenzamos nuestra longitud de onda con el
blanco.
8.- cuando llegamos a la longitud de onda de 490 nos dirigimos dos integrantes a
hacer nuestra mezcla binaria
9.- Nuestra mezcla binaria le agregamos 2 ml de KMnO4 y 6ml de K2Cr2O7.
10.-Una vez terminado el anlisis se depositan los residuos en sus respectivos
lugares, as mismo se enjuagan las celdas con agua destilada. No se deben de
raya, deben ser secadas cuidadosamente y no deben dejar con residuos.
11.-Se determina la concentracin de ambos componentes de las mezclas, as
como sus absortividades molares y tambin la composicin porcentual de cada
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
componente en la mezcla por medio de nmero de moles. Estos de muestra en el
apartado clculos y resultados.
RESULTADOS
Valor de absorbancia
Longitud de onda
330
350
370
390
410
430
450
470
490
510
530
550
570
590
KMnO4
0.252
0.228
0.188
0.144
0.122
0.111
0.108
0.125
0.169
0.233
0.274
0.255
0.156
0.056
Longitud de onda analtica de k2Cr2O7
Longitud de onda analtica de KMno4
K2CrO7
0.461
0.647
0.496
0.256
0.115
0.095
0.093
0.065
0.036
0.016
0.005
0.002
0.002
0.002
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
Absorbancia de nuestra mezcla binaria
Longitud de onda
analtica
Absorbancia
350
.528
550
0.155
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
CONCLUSIN
Vianey Ostos santos: Esta conclusin es muy interesante ya que aprendimos
ms sobre la absorcin. Realizamos un sistema de ecuaciones que nos permiti
obtener la concentracin de los componentes. Es importante conocer la ley de
Beer y sus aplicaciones, tambin esta prctica nos permiti conocer ms sobre el
tipo de celdas y el espectrofotmetro.
ngel Francisco Jimnez Barrn: En esta prctica pudimos comprobar la ley de
Beer ya que se conoci y utiliz una tcnica de aplicacin para lograr determinar la
concentracin de una muestra de concentracin desconocida a partir de su
absorbancia, la longitud de su camino ptico y su coeficiente de extincin
molecular. Por esta razn es importante conocer estas tcnicas, leyes y
formulaciones ya que si se tienen estas bases para conocer algunas sustancias
desconocidas, con estas bases se puede determinar concentracin, absorbancia,
coeficiente de extincin molecular e incluso la transmitancia de una solucin.
TECNOLGICO NACIONAL DE MXICO INSTITUTO TECNOLGICO
DE MINATITLN
Bibliografa.
https://www.scribd.com/doc/20250768/Espectrofotometria-en-Una-Mezcla-
de-Dos-Componentes
http://www.quimicaorganica.org/espectroscopia-visible-ultraviolata/733ecuacion-de-lambert-beer.html
También podría gustarte
- Analisis Instrumental 1-2Documento15 páginasAnalisis Instrumental 1-2Marco Mosquera MarínAún no hay calificaciones
- Determinación espectrofotométrica de hierro en muestrasDocumento9 páginasDeterminación espectrofotométrica de hierro en muestrasMijael AlvaroAún no hay calificaciones
- PRÁCTICA NO. 3 AIIQ ENE-JUN 2022Documento2 páginasPRÁCTICA NO. 3 AIIQ ENE-JUN 2022jcasares888Aún no hay calificaciones
- Práctica No. 3 Aiiq Ene-Jun 2020Documento2 páginasPráctica No. 3 Aiiq Ene-Jun 2020Tadeo RipoolAún no hay calificaciones
- Práctica 2Documento4 páginasPráctica 2Paz Ortega AndradeAún no hay calificaciones
- Practica #01 - EspectrofotometriaDocumento4 páginasPractica #01 - EspectrofotometriaSILVIA ROSARIO CHALCO MENDOZAAún no hay calificaciones
- Espectro ElectromagneticoDocumento25 páginasEspectro ElectromagneticoianelAún no hay calificaciones
- Informes LaboratorioDocumento12 páginasInformes LaboratorioDiana Catalina Castiblanco Soriano100% (1)
- Análisis espectroscófico de compuestos químicosDocumento4 páginasAnálisis espectroscófico de compuestos químicoscarlos cuervoAún no hay calificaciones
- Reporte de Instrumental-Practica 5 - Equipo 3Documento11 páginasReporte de Instrumental-Practica 5 - Equipo 3Isaac GutiérrezAún no hay calificaciones
- Práctica No. 5 Curva Mezcla Binaria Ene-Jun 2023Documento2 páginasPráctica No. 5 Curva Mezcla Binaria Ene-Jun 2023dafne gutierrezAún no hay calificaciones
- Practica No 6 Ni y CoDocumento3 páginasPractica No 6 Ni y CoMoises PcAún no hay calificaciones
- Practica No6 Ni y CoDocumento3 páginasPractica No6 Ni y CoStebanContrerasAún no hay calificaciones
- Colorimetría UV-VisDocumento5 páginasColorimetría UV-VisHaruka KouAún no hay calificaciones
- Cuaderno de Practica de Analisis de Enrique Sanchez CebrianDocumento27 páginasCuaderno de Practica de Analisis de Enrique Sanchez Cebrianquique 657Aún no hay calificaciones
- EspectrofotometríaDocumento10 páginasEspectrofotometríaMarya ValentineAún no hay calificaciones
- Práctica Clasificada de Laboratorio N 2 Espectrofotometría - 2021-QBIDocumento11 páginasPráctica Clasificada de Laboratorio N 2 Espectrofotometría - 2021-QBIYuriy KosinskyyAún no hay calificaciones
- Guía Instrumentación 2023Documento24 páginasGuía Instrumentación 2023AngélicaAún no hay calificaciones
- Manual Laboratorio QAIIIDocumento28 páginasManual Laboratorio QAIIIMiguel Angel DzibAún no hay calificaciones
- INFORME 10 - Espectroscopía (MN y CR)Documento22 páginasINFORME 10 - Espectroscopía (MN y CR)Kevin Paul ÑiquenAún no hay calificaciones
- (P) Lectura 1 - EspectrofotometriaDocumento10 páginas(P) Lectura 1 - EspectrofotometriaArianna CornejoAún no hay calificaciones
- Practica No. 3 ESPECTROFOTOMETRÍA: CURVAS DE ABSORCIÓNDocumento12 páginasPractica No. 3 ESPECTROFOTOMETRÍA: CURVAS DE ABSORCIÓNFanny Torres Ortiz0% (1)
- Determinación de La Concentración de MPDocumento4 páginasDeterminación de La Concentración de MPJatziri Tapia OchoaAún no hay calificaciones
- Práctica 13. Valoraciones Potenciométricas de Compuestos Que Forman PrecipitadosDocumento20 páginasPráctica 13. Valoraciones Potenciométricas de Compuestos Que Forman PrecipitadosJossep Dady Cervantes SierraAún no hay calificaciones
- Informe 2 Quimica Organica 3Documento17 páginasInforme 2 Quimica Organica 3carlos19895Aún no hay calificaciones
- Pratica Espectrofotometria UNIADocumento10 páginasPratica Espectrofotometria UNIAKelly Panduro Hoyos100% (1)
- Cuestionario Asegurar II Resultado de Aprendizaje 2 Análisis EspectrofotométricosDocumento9 páginasCuestionario Asegurar II Resultado de Aprendizaje 2 Análisis EspectrofotométricosCharly RinconAún no hay calificaciones
- Practica #02 - Espectrofotometria - Metodo Analitico - Determinacion de La Concentracion de Una Muestra Problema 1Documento6 páginasPractica #02 - Espectrofotometria - Metodo Analitico - Determinacion de La Concentracion de Una Muestra Problema 1WALTER ISAAC VALLEJOS CAMACHOAún no hay calificaciones
- Informe 2. Analisis InstrumentalDocumento28 páginasInforme 2. Analisis InstrumentalJherson ZelayaAún no hay calificaciones
- Lab 9 Mesa 3Documento9 páginasLab 9 Mesa 3Rico Cacho PortuánoAún no hay calificaciones
- Práctica 3 Emya RRL DRM 3iv6bDocumento16 páginasPráctica 3 Emya RRL DRM 3iv6bdannyromosso18Aún no hay calificaciones
- Laboratorio 3. 4T3-IQDocumento15 páginasLaboratorio 3. 4T3-IQÁlvaro Chamorro CalixtoAún no hay calificaciones
- Informe QA 9Documento13 páginasInforme QA 9Jhoana Alexandra Lévano LévanoAún no hay calificaciones
- QAI - Práctica 3Documento6 páginasQAI - Práctica 3ffferrrfzuritaaAún no hay calificaciones
- PRÁCTICA 3 Mezclas Binarias PDFDocumento3 páginasPRÁCTICA 3 Mezclas Binarias PDFFranklin AjcholonAún no hay calificaciones
- Practica 5 Instrumental PDFDocumento10 páginasPractica 5 Instrumental PDFCamila Arisleidys QuezadaAún no hay calificaciones
- Practica 9Documento13 páginasPractica 9Juan Carlos Castillo ZamoraAún no hay calificaciones
- Fundamentos de Espectrofotometría y Curva PatrónDocumento19 páginasFundamentos de Espectrofotometría y Curva PatrónSofia Ojeda75% (4)
- Practica 3Documento11 páginasPractica 3angelesAún no hay calificaciones
- Cuadernillo de Prácticas U4Documento11 páginasCuadernillo de Prácticas U4RUTH0% (1)
- Análisis Espectrofotométrico - Erick YupaDocumento12 páginasAnálisis Espectrofotométrico - Erick YupaErick YupaAún no hay calificaciones
- G.p.bioquimica y NutricionDocumento68 páginasG.p.bioquimica y NutricionKen Beeler Tolentino GuzmanAún no hay calificaciones
- Practica #1 - QCBDocumento17 páginasPractica #1 - QCBANGEL RAMON PACHECO PLASCENCIAAún no hay calificaciones
- Informe 02 Instrumental.Documento10 páginasInforme 02 Instrumental.Joel LizanoAún no hay calificaciones
- Instrumental Uv Vis 2Documento3 páginasInstrumental Uv Vis 2LENIN SAMUEL ALARCON PRIETOAún no hay calificaciones
- Lab Espectrofotometría VisibleDocumento3 páginasLab Espectrofotometría VisibleErick Grimaldo0% (1)
- Practica 2 Analisis Instrum2do ParcialDocumento9 páginasPractica 2 Analisis Instrum2do ParcialBraulio AvilaAún no hay calificaciones
- Espectrofotometría y colorantesDocumento23 páginasEspectrofotometría y colorantesAaronAún no hay calificaciones
- Práctica No 6 Longitud de Onda de Mayor Absorbancia para El CobaltoDocumento8 páginasPráctica No 6 Longitud de Onda de Mayor Absorbancia para El CobaltoCristy VeLaAún no hay calificaciones
- Practica N 1Documento7 páginasPractica N 1Isabelle casanova ledezmaAún no hay calificaciones
- UntitledDocumento9 páginasUntitledVanessa Labán QuispeAún no hay calificaciones
- Fotocolorimetria 2Documento9 páginasFotocolorimetria 2Germán Guerra Fernández0% (1)
- Espectrofotometría I3-: Determinación ε a partir de curva patrónDocumento9 páginasEspectrofotometría I3-: Determinación ε a partir de curva patrónMontse MoMo Mtz100% (1)
- Determinación de longitudes de onda máximasDocumento3 páginasDeterminación de longitudes de onda máximasSteward FloresAún no hay calificaciones
- Informe EspectrofotometríaDocumento11 páginasInforme EspectrofotometríaFiorella Danna AsenjoAún no hay calificaciones
- Practica 2 Bioquimica PDFDocumento5 páginasPractica 2 Bioquimica PDFlou_sheeriectionerAún no hay calificaciones
- Curva calibración MnO4- espectrofotometríaDocumento3 páginasCurva calibración MnO4- espectrofotometríadafne gutierrezAún no hay calificaciones
- Nalisis Cuantitativo de Una Mezcla de Permanganato y Dicromato Potásicos Por Espectrofotometria UvDocumento5 páginasNalisis Cuantitativo de Una Mezcla de Permanganato y Dicromato Potásicos Por Espectrofotometria UvHernan DmgzAún no hay calificaciones
- Análisis inorgánico cualitativo sistemáticoDe EverandAnálisis inorgánico cualitativo sistemáticoCalificación: 4.5 de 5 estrellas4.5/5 (2)
- Sensores electroquímicos: Teoría y aplicacionesDe EverandSensores electroquímicos: Teoría y aplicacionesAún no hay calificaciones
- Proceso de Ontencion de h2s04Documento3 páginasProceso de Ontencion de h2s04Francisco Jiménez BarrónAún no hay calificaciones
- E Vapor AdoresDocumento14 páginasE Vapor AdoresFrancisco Jiménez BarrónAún no hay calificaciones
- Simulacion de ChecadDocumento7 páginasSimulacion de ChecadFrancisco Jiménez BarrónAún no hay calificaciones
- Absorción Presentacion Equipo 5Documento20 páginasAbsorción Presentacion Equipo 5Francisco Jiménez BarrónAún no hay calificaciones
- Diametro de Una TuberiaDocumento2 páginasDiametro de Una TuberiaFrancisco Jiménez BarrónAún no hay calificaciones
- Volumen Reactor LotesDocumento8 páginasVolumen Reactor LotesFrancisco Jiménez BarrónAún no hay calificaciones
- AntoineDocumento5 páginasAntoineJorgeh Ivanh Lopezh EzquivelhAún no hay calificaciones
- TareasDocumento1 páginaTareasjaredAún no hay calificaciones
- Metodos Numericos Mas Usuales en QuimicaDocumento59 páginasMetodos Numericos Mas Usuales en QuimicaCarlos ValdiviesoAún no hay calificaciones
- Codigo o Sintaxis Ejercicio MatlabDocumento13 páginasCodigo o Sintaxis Ejercicio MatlabFrancisco Jiménez BarrónAún no hay calificaciones
- Curva de Equilibrio Benceno ToluenoDocumento1 páginaCurva de Equilibrio Benceno ToluenoFrancisco Jiménez BarrónAún no hay calificaciones
- Programador Riego Instrucciones PDFDocumento24 páginasProgramador Riego Instrucciones PDFJoseph FitzgeraldAún no hay calificaciones
- CatalogoProductosSiemens MAY2015Documento188 páginasCatalogoProductosSiemens MAY2015UcCouohMartínAún no hay calificaciones
- Cuadernillo No. 1 de Artistica 6 Los Colores PrimariosDocumento2 páginasCuadernillo No. 1 de Artistica 6 Los Colores PrimariosAlexander arenasAún no hay calificaciones
- Teoria Del ColorDocumento4 páginasTeoria Del ColorGustavo Salomón Tindal CondeAún no hay calificaciones
- Caminata Química. Ensayo A La LlamaDocumento1 páginaCaminata Química. Ensayo A La LlamaAlex FernandezAún no hay calificaciones
- Nuevo Catálogo de Iluminación TBCinDocumento320 páginasNuevo Catálogo de Iluminación TBCinMarcos BarrosAún no hay calificaciones
- Los 7 contrastes del color según Johannes IttenDocumento23 páginasLos 7 contrastes del color según Johannes Ittenyajaimi67% (3)
- Historia de Los ColoresDocumento4 páginasHistoria de Los ColoresMichael Andres IndAún no hay calificaciones
- Ets QuimicaDocumento7 páginasEts QuimicaDanielaAún no hay calificaciones
- EPPSDocumento829 páginasEPPSCarlos Eduardo Niño ArroyoAún no hay calificaciones
- Capítulo 2. Percepción Del Color2021. PSICOLOGÍA PERCEPCIÓN. CURSO 2. GRADO PSICOLOGIA UNEDDocumento29 páginasCapítulo 2. Percepción Del Color2021. PSICOLOGÍA PERCEPCIÓN. CURSO 2. GRADO PSICOLOGIA UNEDMariaAún no hay calificaciones
- Catalogo San JustoDocumento14 páginasCatalogo San JustoHiper StockAún no hay calificaciones
- Plantilla Abono CTS 2018Documento34 páginasPlantilla Abono CTS 2018COLLPA PAREDES WALTERAún no hay calificaciones
- Propagación de OndasDocumento37 páginasPropagación de OndasFrancisco Javier Jimenez FernandezAún no hay calificaciones
- Informe 5Documento19 páginasInforme 5Joelitho Carrasco LeonAún no hay calificaciones
- Colorear Leyendo ACT2Documento9 páginasColorear Leyendo ACT2Yanell MatadamasAún no hay calificaciones
- Cómo Sobrevivir A Las Profecías Del Año 2012Documento328 páginasCómo Sobrevivir A Las Profecías Del Año 2012Flor D María Mora100% (3)
- 6 Modelos de Propagación Tierra Plana (2-Rayos)Documento38 páginas6 Modelos de Propagación Tierra Plana (2-Rayos)byronsmart100% (1)
- Radio Enlace Piura - Huancabamba Trabajo 3Documento24 páginasRadio Enlace Piura - Huancabamba Trabajo 3Arnol Sayas ZubietaAún no hay calificaciones
- Catalogo de LamparasDocumento2 páginasCatalogo de LamparasMaria Del Carmen Arizmendi CastilloAún no hay calificaciones
- YARIDocumento3 páginasYARIdenis max cotrinaAún no hay calificaciones
- Ibnorca Anteproyecto de Norma Boliviana Apnb 1412001Documento9 páginasIbnorca Anteproyecto de Norma Boliviana Apnb 1412001mxnuel750% (1)
- CielabDocumento3 páginasCielabMeli RomeroAún no hay calificaciones
- F Ondas Electromagneticas Fisica ModernaDocumento3 páginasF Ondas Electromagneticas Fisica ModernaGerardo Manrique TelloAún no hay calificaciones
- Proyecto Final Óptica y OndasDocumento6 páginasProyecto Final Óptica y OndasTARAZONA VELEZ VALERIAAún no hay calificaciones
- Modos de PropagaciónDocumento4 páginasModos de PropagaciónCarlos GilAún no hay calificaciones
- UNI-Examen Fisica 2008 I - SolucionarioDocumento12 páginasUNI-Examen Fisica 2008 I - Solucionarioprofe.alex100% (2)
- Metodos Espectrometricos de AnalisisDocumento98 páginasMetodos Espectrometricos de AnalisisValeria PerezAún no hay calificaciones
- Brillemos Juntos: Campaña 10Documento200 páginasBrillemos Juntos: Campaña 10Jein OñaAún no hay calificaciones
- Compendio Expresión Visual 2023 - 230620 - 082256Documento206 páginasCompendio Expresión Visual 2023 - 230620 - 082256Walter AlvearAún no hay calificaciones