Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Manual de Bioquimica
Manual de Bioquimica
Cargado por
Javier SolisDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Manual de Bioquimica
Manual de Bioquimica
Cargado por
Javier SolisCopyright:
Formatos disponibles
NDICE
BIOQUMICA................................................................................................. 1
I. CLULA..................................................................................................... 2
II. AGUA........................................................................................................ 8
III. AMINOCIDOS.......................................................................................13
IV. ENZIMAS Y COENZIMAS.......................................................................17
V. INTRODUCCIN AL METABOLISMO.................................................... 20
VI. CARBOHIDRATOS................................................................................ 27
VII. LPIDOS................................................................................................ 35
BIBLIOGRAFA............................................. ..............................................39
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
BIOQUMICA
La Bioqumica juega un papel trascendental
en todas las reas de Ciencias de la
Salud.
Gran parte de las enfermedades son
consecuencia de alteraciones moleculares
en clulas, rganos o tejidos. Se requieren
slidos fundamentos bioqumicos para
entender su fisiopatologa, llegar al
diagnstico y desarrollar una teraputica
apropiada.
La bioqumica es la
qumica de la vida.
La bioqumica puede definirse de manera
ms formal como la ciencia que se
ocupa de la base qumica de la vida (del
griego, bios: vida). La clula es la unidad
estructural de los sistemas vivientes. La
consideracin de este concepto conduce
a una definicin funcional de la bioqumica
como la ciencia que se ocupa de los
constituyentes qumicos de las clulas
vivas y de las reacciones y procesos que
experimentan. Con esta definicin, la
bioqumica abarca extensas reas de la
biologa celular, la biologa molecular y la
gentica moIecular.
El campo de la bioqumica es tan amplio
como la vida misma. Dondequiera
que hay vida, se producen procesos
qumicos. Los bioqumicos los estudian
en microorganismos, vegetales, insectos,
peces, aves, mamferos y en el ser
humano.
El hecho de que la Bioqumica sea la ciencia
que estudia la vida a nivel molecular como
1
Curso Propedutico
ciencia fundamental y necesaria para otras
disciplinas que se ocupan del fenmeno
vital. As, la Anatoma, Histologa, Fisiologa
y otras materias relacionadas adquieren otra
dimensin cuando el estudio macroscpico,
relacionado a estas reas de conocimiento
morfolgicas y funcionales, se desarrolla
de forma paralela al enfoque molecular que
proporciona la Bioqumica.
As mismo, otras disciplinas como la
Microbiologa, Gentica, Embriologa,
Fisiologa, Neuroqumica y otras ciencias
implicadas en los fenmenos vitales,
necesitan del lenguaje bioqumico para
profundizar adecuadamente.
La Bioqumica es la piedra angular sobre
las que se apoyan todas y cada una de las
ciencias relacionadas con la vida.
Figura 1 Ejemplos de la avenida bidireccional que conecta la
bioqumica y la medicina. El conocimiento de las molculas
bioqumicas mostradas en la parte superior del diagrama
ha esclarecido el entendimiento de las enfermedades
mostradas en la mitad inferior y, a la inversa, los anlisis de las
enfermedades que se muestran abajo han aclarado muchas
reas de la bioqumica.
Antologa de Bioqumica / 1era. Edicin 2015
Lgica Molecular de la Vida
A pesar de la gran diversidad de todos los
organismos vivos, todos son semejantes a
nivel qumico y celular.
Todos los seres vivos estn constituidos
cualitativa y cuantitativamente por los
mismos elementos qumicos.
De todos los elementos que se encuentran
en la corteza terrestre, slo 30 son
componentes de los seres vivos. Se
denominan
bioelementos
aqullos
elementos que forman parte de los seres
vivos.
Se denominan Biolelementos a los
elementos qumicos que constituyen los
seres vivos. Tambin reciben el nombre
de elementos biogenticos y pueden ser
clasificados segn su abundancia en tres
grandes grupos. Fig. 1-2
1. Biolementos primarios : H, O, C, N.
Son los ms abundantes, representan
un 99.3% del total de tomos del cuerpo
humano. El Hidrgeno, el que ms abunda,
junto con el oxgeno, ya que forman parte
del agua.
2. Bioelementos secundarios : Ca,
P, K, S, Na, Cl, Mg, Fe.
Constituyen
prcticamente el 0.7% del total de tomos
del cuerpo humano.
3. Oligoelementos: Mn, I, Cu, Co, Zn, F,
Mo, Se, y otros. Aparecen slo en trazas
o en cantidades mnimas, pero an as,
su presencia es esencial para el correcto
funcionamiento del organismo. Su ausencia
determina la aparicin de enfermedades
carenciales o sntomas de dficit.
Q. F. B. Melba Fernndez Rojas
vivos. Atendiendo a su naturaleza qumica,
se pueden clasificar las biomolculas en
dos grandes grupos :
1. Biomolculas inorgnicas : Agua
(la biomolcula ms abundante). Gases
(oxgeno, dixido de carbono). Sales
inorgnicas (aniones, como fosfato y
bicarbonato, y cationes como amonio)
2. Biomolculas orgnicas : Glcidos
(glucosa, glucgeno). Lpidos (triglicridos,
colesterol). Protenas (enzimas, hemoglobina).
cidos nuclicos (ADN, ARN). Metabolitos
(cido pirvico, cido lctico).
Segn la especializacin de cada tejido,
existe una diferente distribucin celular
cualitatita y cuantitativa de las biomolculas,
siendo la ms abundante , el agua.
Figura 2 Biolelementos qumicos que constituyen los seres vivos.
Anlogamente a lo que ocurre con los
bioelementos, las Biomolculas son las
molculas constituyentes de los seres
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD I:CLULA
Conceptos de Clula,
Tejido y rgano
biolgico superior a tejido pero inferior a
sistema.
Clula
La clula es la unidad de organizacin
(estructura) y funcin bsica de la vida
en todos los organismos. Proceden de la
divisin de otra clula preexistente, siendo
idntica a esta gentica, estructural y
funcionalmente. Las semejanzas bsicas
entre su estructura y composicin molecular
proporcionan evidencias que todas las
clulas tiene un origen evolutivo comn
(Figura 1.1).
Tipos de clula
Las clulas se pueden clasificar en dos
grandes grupos: Eucariotas y Procariotas.
La procariota es una clula sin ncleo celular
diferenciado, es decir, su ADN no est
confinado en el interior de un ncleo, si no
libremente en el citoplasma (ej. Bacterias)
y carece de organelos. En contraste, la
clula eucariota es compleja y altamente
organizada, contienen organelos rodeados
de membrana con funciones especficas que
se encuentran en el citoplasma. Presentan
un ncleo prominente que contiene el 99%
del cdigo gentico, el ADN.
Organelos de las
clulas eucariotas
Figura 1.1 Organizacin Celular.
Tejido
En biologa se llama tejido a una estructura
constituida por un conjunto organizado
de clulas diferenciadas, ordenadas
regularmente, que realizan un trabajo
fisiolgico coordinado. Esta estructura
forma un nivel superior de organizacin
biolgica superior a la clula.
rgano
Un rgano es una agrupacin de diversos
tejidos que forman una unidad estructural
encargada del cumplimiento de una funcin
determinada. Se encuentra en un nivel
3
Curso Propedutico
Las clulas eucariotas tienen un volumen
superior al de las clulas procariotas,
entre 1000 y 10 000 veces, contienen
numeroso organitos membranosos y no
membranosos, todos ellos contenidos en
los lmites establecidos por la membrana
plasmtica. En este apartado se har
nfasis en los organelos ms relevantes
(Figura 1.2).
Ncleo
En este organelo se encuentra la
informacin gentica, el ADN, por lo que su
duplicacin se lleva a cabo en el ncleo,
proceso que est regulado por diversas
enzimas y protenas especializadas. La
transcripcin tambin se efecta en el
ncleo.
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
modificacin y ensamblaje de protenas.
Figura 1.2 Clula Eucariota.
Retculo Endoplasmtico
Consta de una red de membranas internas
paralelas que envuelven al ncleo y se
extienden hacia muchas regiones del
citoplasma y estn conectadas entre s.
Existen dos tipos de retculo: Liso (REL) y
rugoso (RER).
El RER se considera como una extensin de
la membrana nuclear, presenta numerosos
ribosomas en su superficie externa. El RER
tiene una funcin principal en la sntesis,
Figura 1.3 Retculo Endoplsmico.
El REL presenta continuidad con el
RER, tienen apariencia tubular y son de
superficie lisa (no presentan ribosomas).
El REL es el sitio principal de sntesis de
lpidos necesarios para la formacin de
membranas celulares. Es un centro de
desintoxicacin puesto que efecta la
transformacin qumica de drogas lo que
permite eliminar compuestos txicos. En
clulas animales, el REL sintetiza hormonas
a partir de colesterol (Figura 1.3).
Aparato de Golgi
Est formado por una serie de sacos
membranosos aplanados y apilados
llamados cisternas, cada cisterna tiene
un espacio interno (luz) Cada apilamiento
del complejo de Golgi consiste en 3 zonas
denominadas caras cis (superficie de
entrada), trans (superficie de salida) y
regin media ubicada entre ambas caras.
Por lo general la cara cis se localiza prxima
al RER y recibe protenas procedentes
del RER. La cara trans est ms prxima
a la membrana plasmtica y clasifica,
empaqueta y distribuye las proteinas
maduras segn su destino; el carbohidrato
de las glicoprotenas puede constituir una
seal de clasificacin (Figura 1.4).
Figura 1.4 Aparato de Golgi.
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Lisosomas
Son organelos esfricos que se encuentran
dispersos en el citoplasma de la mayora
de las clulas animales, se encuentran
rodeados por una nica membrana y
estn llenos de enzimas digestivas que
se sintetizan en el RER. Las enzimas
hidrolizan macromolculas complejas por
lo que se liberan los monmeros que los
componen y son reutilizados por la clula.
En condiciones normales, los lisosomas
degradan membranas y organelos que
han han dejado de funcionar en la clula
(autofagia).
Mitocondria
Las mitocondrias presentan doble membrana:
externa e interna. La membrana externa es
permeable a molculas pequeas e iones.
La membrana interna esta plegada
Q. F. B. Melba Fernndez Rojas
formando crestas que aumentan el rea
de superficie, es impermeable a la mayora
de las molculas o iones y est separada
de la membrana externa por un espacio
intermembrana.
La membrana interna rodea la matriz
mitocondrial, una solucin acuosa muy
concentrada de enzimas (ciclo de Krebs) e
intermediarios qumicos. La matriz contiene
al menos un ADN mitocondrial circulante
de doble hlice, que contiene 1% de la
informacin gentica de la clula.
La mitocondria es el centro de respiracin
aerobia de la clula, esta respiracin ocurre
en la membrana interna mitocondrial y la
matriz mitocondrial. En la mitocondria se
sintetiza ATP que es la moneda energtica
de la clula, es la fuente de energa
mediante la cual las clulas pueden realizar
sus tareas vitales. Tienen una funcin
importante en la muerte celular programada
(apoptosis) Figura 1.5.
El Citoesqueleto
Es un armazn tridimensional que est
presente en el citoplasma, proporciona
a la clula resistencia mecnica, forma y
capacidad de movimiento. Participa en
la divisin celular y en el transporte de
materiales dentro de la clula.
Est formado por tres tipos de filamentos:
microtbulos,
microfilamentos
y
filamentos intermedios. Los microtbulos
y los microfilamentos estn formados
por subunidades globulares de protenas
dispuestas en forma de perla que se
pueden ensamblar y desensamblar
rpidamente.
Figura 1.5 Mitocondria.
Curso Propedutico
Los filamentos intermedios estn formados
por subunidades fibrosas de protena y son
ms estables que los otros dos.
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Todas las clulas eucariotas tienen
microtbulos y microfilamentos, solo algunos
de animales tienen filamentos intermedios
(Figura 1.6).
Figura 1.6 Citoesqueleto.
Cuadro 1.1 Principales funciones de los organelos celulares.
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Cuadro 1.2 Jerarqua Molecular.
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD II:AGUA
Importancia biomdica
El 71% de la superficie terrestre esta
cubierta por agua y el 97% est en los
ocanos. En los seres vivos,
el agua
representa el 70% del peso total. Es la
nica sustancia que podemos encontrar
en la tierra de forma natural como slido
(hielo), lquido o gas (vapor de agua).
Gracias a sus propiedades fisicoqumicas
permite la vida en nuestro planeta.
El agua, una molcula notablemente
esencial para la vida, solubiliza y modifica
las caractersticas de biomolculas como
cidos nucleicos, protenas y carbohidratos
al formar puentes de hidrgeno con sus
grupos funcionales.
Tiene una propension leve a disociarse
hacia iones hidroxido y protones.
La concentracion de protones, o acidez,
de soluciones acuosas por lo general se
reporta usando la escala de pH.
La homeostasis, conservacin de la
composicin del medio interno que es
esencial para la salud, incluye considerar
la distribucin del agua en el cuerpo
y la preservacin del pH as como de
concentraciones electrolticas apropiadas.
En el cuerpo, el agua puede encontrarse
en un compartimento intracelular y otro
extra-celular. Dos terceras partes del agua
corporal total (55 a 65% del peso corporal
en varones y alrededor de 10% menos
en mujeres) es lquido intracelular. Del
lquido extracelular remanente, el plasma
sanguneo constituye cerca de 25 por
ciento.
La regulacin del equilibrio hdrico depende
de mecanismos hipotalmicos para
controlar la sed, de la hormona antidiurtica
y de la retencin o excrecin del agua por
los riones. Los estados de deplecin de
agua y exceso de Iquido corporal son
bastante comunes. En muchos casos se
acompaan de deficiencia o exceso de
sodio. La deplecin hdrica puede deberse
a una disminucin de la ingestin de
lquidos o bien un incremento de la prdida.
Las causas de exceso de agua corporal se
deben al incremento en la ingestin.
La conservacin del lquido extracelular
dentro de un pH entre 7.35 y 7.45,
en donde el sistema amortiguador de
bicarbonato tiene una funcin importante,
es esencial para la salud. Las alteraciones
del equilibrio cido-bsico se diagnostican
en el laboratorio clnico por medicin del
pH de la sangre arterial y el contenido de
CO2 en la sangre venosa. Las causas
de la acidosis (pH sanguneo < 7.35)
incluyen cetoacidosis diabtica y acidosis
lctica; mientras que las de la alcalosis (pH
sanguneo > 7.45) comprenden el vmito
de contenido gstrico o el tratamiento con
ciertos diurticos.
Estructura de la molcula del agua
La molcula del agua es un tetraedro
irregular con oxgeno en el centro.
Los dos enlaces con hidrgeno se dirigen
hacia dos vrtices del tetraedro, en tanto
que los electrones no compartidos del
oxgeno en el orbital 2sp3 ocupan los dos
vrtices restantes.
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
El ngulo entre los dos tomos de hidrgeno
(105 grados) es algo menor que el ngulo
del tetraedro (109.5 grados), formando una
figura geomtrica ligeramente asimtrica.
Q. F. B. Melba Fernndez Rojas
formar puentes de hidrgeno con el agua
(por ejemplo, compuestos con radicales
4N o SH, aminas, steres, aldehdos y
cetonas) se solvatan con facilidad lo que
por su solubilidad en agua aumenta.
Grupos apolares como aquellos presentes
en hidrocarburos no tienen capacidad para
formar uniones hidrgeno y, por tanto, son
insolubles en agua.
Figura 2.1 La molcula de agua tiene forma tetradica.
Un nucleo de hidrogeno parcialmente
desprotegido, unido de manera covalente
a un atomo de oxigeno que extrae electrn,
puede interactuar con un par de electrones
no compartidos sobre otro atomo de oxigeno
para formar un enlace de hidrogeno. Dado
que las moleculas de agua tienen estas dos
caracteristicas, la formacion de enlaces de
hidrogeno favorece la autoasociacion de
moleculas de agua hacia disposiciones
ordenadas.
La mayora de las Biomolculas establecen
un modelo estructural que maximiza
las oportunidades para la formacion de
interacciones de carga dipolo, dipolodipolo,
y formacion de enlaces de hidrogeno,
favorables desde el punto de vista
energetico entre grupos polares sobre la
biomolecula y el agua. Tambien minimiza
contactos desfavorables desde el punto
de vista energetico entre el agua y grupos
hidrofobicos.
La propiedad del agua de servir como
solvente para iones y numerosas molculas
orgnicas se debe a su carcter bipolar
y a su capacidad para formar puentes de
hidrgeno. Las molculas que pueden
Curso Propedutico
Figura 2.2 Izquierda: asociacin de dos molculas de agua
dipolares mediante un enlace de hidrgeno (lnea punteada).
Derecha: agrupacin de cuatro molculas de agua con enlaces
de hidrgeno. Note que el agua puede servir de manera
simultnea como donador y como aceptor de hidrgeno.
La estructura del agua es
distinta en respuesta al estado
de agregacin en el que se
encuentre:
Figura 2.3 Estructuras de los estados del agua.
En estado slido, las molculas de agua
son capaces de formar cuatro puentes de
hidrgeno por que las molculas de agua se
encuentran restringidas en su movimiento.
A temperatura ambiente y a la presin
de la atmsfera, las molculas de agua
estn desorganizadas y en un continuo
Antologa de Bioqumica / 1era. Edicin 2015
movimiento, de modo que forman en
promedio 3,4 puentes de hidrgeno con las
molculas vecinas (Figura 2.3).
Como muchos otros compuestos, el agua
mantiene ciertas propiedades fsicoqumicas de gran importancia (Cuadro 2.1).
Masa molecular
Punto de fusin
Punto de ebullicin
Densidad a 4 C
Densidad a 0 C
Q. F. B. Melba Fernndez Rojas
superficie. De esta manera, los cuerpos y
algunos animales como moscos o araas
pueden desplazarse sobre la superficie del
agua (Figura 2.4).
18 Dalton (Da)
0 C
100 C
1g/cm3
097 g/cm3
Cuadro 2.1 Propiedades importantes del agua.
Algunas propiedades del agua
le confieren importancia en
funciones biolgicas vitales:
Gracias a su capacidad de mantenerse
liquida a temperatura ambiente y a su
propiedad de solvente universal, acta
como un medio de transporte de sustancias
en el organismo.
Adems, su alto calor de vaporizacin
(energa necesaria para romper puentes
de hidrgeno para el cambio de estado) y
su alto calor especfico (energa necesaria
para elevar su temperatura 1 C) la
convierten en mecanismo termorregulador
por excelencia, absorbiendo el exceso de
calor o cediendo energa si es necesario,
de tal manera que ayuda a mantener la
temperatura corporal el organismo.
Otras propiedades importantes:
La estructura del agua en la interfase aguaaire (como en los ros) no estn sujetas
a fuerzas de atraccin semejante es en
todas direcciones, de modo que el agua
tiene una resistencia para aumentar su
Figura 2.4 Tensin superficial del agua.
En relacin con las molculas de agua,
se dice que puede establecer diferentes
tipos de interacciones dependiendo de la
naturaleza del compuesto con el que se
quiera interactuar:
1.- Interacciones hidrofbicas:
Alude a la tendencia de compuestos no
polares a autoasociarse en un ambiente
acuoso. La autoasociacion minimiza la dis
rupcion de interacciones desfavorables
desde el punto de vista energetico entre
las moleculas de agua circundantes,
impidiendo el establecimiento de mas
puentes de hidrgeno.
2.- Interacciones electroestticas:
Interacciones entre grupos cargados
ayudan a dar forma a la estructura
biomolecular. Las interacciones electrostaticas entre grupos con carga opuesta dentro
de biomoleculas se denominan puentes de
sal.
Curso Propedutico
10
Antologa de Bioqumica / 1era. Edicin 2015
3.- Fuerzas de van der Waals:
Surgen por atracciones entre dipolos
transitorios generados por el movimiento
rapido de electrones de todos los atomos
neutros.
Q. F. B. Melba Fernndez Rojas
El plasma; es el componente lquido de la
sangre; est contenido dentro del sistema
vascular (arterias y venas) y contribuye con
un total de 3 litros, lo que constituye un 5%
del peso corporal.
Los lquidos del cuerpo humano se dividen :
Segn su polaridad en agua, los
compuestos pueden clasificarse:
Lquido intracelular (dentro de las clulas):
todo el lquido que est dentro de las clulas,
el mayor compartimiento lquido, contiene
aproximadamente 25 litros y constituye
cerca del 40% del peso corporal.
Polares (hidroflicas): contienen grupos
funcionales con enlaces covalentes
polares (Enlaces OH en alcoholes, -N-H
de las aminas, etc) formando puentes de
hidrgeno con agua.
Cuadro 2.2 Propiedades del agua y funciones biolgicas.
Lquido intersticial o extracelular (fuera
de las clulas): todo el lquido que baa a
las clulas y por supuesto todo material
que entre o salga de estas, debe cruzar
este compartimiento que contiene un
volumen total de 12 litros y constituye
aproximadamente el 15% del peso corporal.
Incluye el plasma
11
Curso Propedutico
No polares: contienen enlaces covalentes
no polares (C-H en hidrocarburos etc) que
no forman puentes de hidrgeno con el
agua.
Anfipticas: Parte de la molcula
interaccina con el agua porque contiene
enlaces covalentes polares y la otra parte
Antologa de Bioqumica / 1era. Edicin 2015
no, por cuanto tiene enlaces covalentes no
polares.
Las moleculas de agua muestran
una tendencia leve pero importante
a disociarse.
La capacidad del agua para ionizarse, si bien
es leve, tiene importancia fundamental para
la vida. Dado que el agua tiene la capacidad
de actuar como un acido y como una base,
su ionizacion puede representarse como
una transferencia de proton intermolecular
que forma un ion hidronio (H3O+) y un ion
hidroxido (OH):
Q. F. B. Melba Fernndez Rojas
Los valores de pH bajos corresponden a
concentraciones altas de H+, y los valores
de pH altos corresponden a concentraciones
bajas de H+. Los acidos son donadores
de protones y las bases son aceptores de
protones. Los acidos fuertes (p. ej., HCl,
H2SO4) se disocian por completo hacia
aniones y protones, incluso en soluciones
fuertemente acidicas (pH bajo); por su
parte, los acidos debiles se disocian solo
en parte en soluciones acidicas. De modo
similar, las bases fuertes (p. ej., KOH,
NaOH) no asi las bases debiles (p. ej.,
Ca[OH]2) estan por completo disociadas
a pH alto.
H O + H O H O+ + OH 223
El proton transferido en realidad se relaciona
con una agrupacin de moleculas de agua.
Los protones existen en solucion no solo
como H3O+, sino tambien como multimeros
tipo H5O2+ y H7O3+. Sin embargo, el
proton se representa de manera sistematica
como H+, aun cuando de hecho esta muy
hidratado.
El PH es el logaritmo negativo De la
concentracin de ion hidrgeno:
El termino pH fue introducido en 1909
por Sorensen, quien lo definio como el
logaritmo negativo de la concentracion de
ion hidrogeno:
pH = log [H]
Esta definicion, si bien no es rigurosa,
es suficiente para muchos propositos
bioquimicos; a fin de calcular el pH de una
solucion: 1. Se calcula la concentracion
de ion hidrogeno [H+]. 2. Se calcula el
logaritmo base 10 de [H+]. 3. El pH es el
negativo del valor que se encuentra en el
paso 2.
Curso Propedutico
12
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD III: AMINOCIDOS
Y PROTENAS
Adems de proporcionar las unidades
monmero para sintetizar las cadenas
polipeptdicas largas de protenas, los
L--aminocidos, participan en funciones
celulares diversas transmisin nerviosa,
biosntesis de porfirinas, purinas, pirimidinas
y urea .Los polmeros cortos de aminocidos
llamados pptidos desempean funciones
importantes en el sistema neuroendocrino
hormonas, factores liberadores de hormona,
neuromoduladores o neurotransmisores .
Los seres humanos carecen de la capacidad
para sintetizar 10 a 20 L--aminocidos
comunes en cantidades adecuadas
para el crecimiento y mantener la salud.
No sorprende que defectos genticos
en el metabolismo de los aminocidos
puedan conducir a trastornos graves
(fenilcetonuria y Enf. De la orina de jarabe
de maple). La dieta del ser humano debe de
contener cantidades adecuadas de estos
aminocidos esenciales (desde el punto
de vista nutricional). Las protenas del ser
humano solo contienes L--aminocidos,
los microorganismos hacen uso extenso de
D- -aminocidos (Figura 3.1).
En las Protenas Solo
Existen L- - Aminocidos
Si bien algunos aminocidos de protenas
son dextrorrotatorios y otros levorrotatorios,
todos comparten la configuracin gentica
absoluta de L- gliceraldehido, y asi, son L-aminoacidos (Cuadro 3.1).
Formacin del Enlace Peptdico
El enlace peptdico es un enlace amida que
se establece entre el grupo - carboxilo de
un aminocido y el grupo -amino del otro
aminocido (Figura 3.2).
Todos los pptidos tienen un grupo
-amino libre en un extremo, a la izquierda,
(Nterminal) y un grupo - carboxilo libre
en el otro, a la derecha (C-terminal), que
pertenece a l ltimo aminocido aadido a
la cadena.
Figura 3.2 Formacin del enlace peptdico.
Figura 3.1 Estructura del Aminocido.
13
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Cuadro 3.1 L- Aminocidos presentes en protenas
Curso Propedutico
14
Antologa de Bioqumica / 1era. Edicin 2015
Los Grupos Funcionales Dictan
las Reacciones Qumicas de los
Aminocidos
Cada grupo funcional de un aminocido
muestra todas sus reacciones qumicas
caractersticas. Para grupos de cido
carboxlico, tales reacciones incluyen la
formacin de esteres, amidas y anhidricos
acidos-, en el caso de los grupos amino,
comprende
acilacion,
amidacion
y
esterificacin; en tanto que para grupos OH
y SH, conlleva oxidacin y esterificacin.
Figura 3.4 Nomenclatura de las protenas.
15
Curso Propedutico
Q. F. B. Melba Fernndez Rojas
La reaccin de mayor importancia de los
aminocidos es la formacin de un enlace
pptido (Figura 3.4).
3.3 rdenes de la Estructura
de las Protenas
Niveles de organizacin estructural de las
protenas.
Los niveles de organizacin estn
dictados por la secuencia de aminocidos.
Se estabilizan por interacciones entre los
grupos R de la protena, pueden ser:
- No covalentes: puentes de hidrgeno,
atraccin electrosttica (puente salino) e
hidrofbicas
- Covalentes: puentes de disulfuro entre
otros
- Formacin de puentes hidrgeno entre
los grupos C=O y N-H de los enlaces
peptdicos (estructura secundaria).
Antologa de Bioqumica / 1era. Edicin 2015
Los Cuatro rdenes de
Estructura de las Protenas
La naturaleza modular de la sntesis y
el plegamiento de las protenas estn
incorporados en el concepto de rdenes
de estructura de protena: estructura
primaria, la secuencia de aminocidos
en una cadena polipeptdica; estructura
secundaria, el plegado de segmento de
polipptidos cortos (3 a 30 residuos) y
contiguos, hacia unidades ordenadas de
manera geomtrica; estructura terciaria,
el montaje de unidades estructurales
secundaria hacia unidades funcionales de
mayor tamao como el polipptido maduro
y los dominios que lo componen y, por
ltimo, estructura cuaternaria, el nmero
y los tipos de unidades polipeptdicas de
protenas oligomricas y su disposicin
espacial (Cuadro 3.2).
Q. F. B. Melba Fernndez Rojas
una conformacin nica a pH fisiolgico,
dictada por la secuencia de aminocidos.
La estructura 3D nica es la responsable
de la funcin biolgica y se conoce como
conformacin o protena nativa.
Las protenas mantienen la conformacin
nativa a pH fisiolgico y a la temperatura
del organismo. Ej: La mioglobina.
Estructura Cuaternaria
La estructura cuaternaria define la
composicion polipeptidica de una proteina
y, para una protena oligomerica, las
relaciones espaciales entre sus protomeros
o subunidadedes. Ej: hemoglobina, queratina, fibras de la seda.
Estructura Primaria
Secuencia de aminocidos de una
cadena polipeptdica.
Se escribe del N- al C-terminal.
Estructura Secundaria
Es la conformacin local de secuencias de
residuos de aminocidos en un polipptido.
Se distinguen tres clases de estructura
secundaria: Hlice, Lmina plegada y
vueltas-.
Cuadro 3.2 Estructura de las protenas.
La estructura secundaria se estabiliza por
puentes de hidrgeno entre los grupos
carbonilo (C=0) y NH de los enlaces
peptdicos.
Estabilizadas por puentes de hidrgeno
entre todos los grupos C=O y N-H de los
enlaces peptdicos.
Estructura Terciaria
Estructura 3-D de un polipptido.
Resulta del plegamiento del polipptido con
sus elementos de estructura secundaria en
Curso Propedutico
16
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD IV: ENZIMAS
Y COENZIMAS
Propiedades generales
de las enzimas
La mayora de las reacciones qumicas
celulares presenta una elevada energa libre
de activacin (energa mnima necesaria
para que se produzca la reaccin). En
consecuencia dichas reacciones en las
clulas son muy lentas (Figura 4.1).
(sustratos), originando as productos.
A la regin donde se une el sustrato y ocurre
la conversin del sustrato en producto se le
llama: sitio activo (Figura 4.2).
Las enzimas y coenzimas son catalizadores
biolgicos de naturaleza proteica que son
producidas por las clulas mediante la
expresin de los genes en el ADN, y que
aceleran la reaccin segn las necesidades
de la clula, y as acortan el tiempo para
alcanzar el equilibrio sin alterarlo.
Figura 4.2 Reacciones Enzimticas.
Las enzimas son altamente especficas.
Esto quiere decir, que no se unen a un
sustrato que no le corresponde.
La especificidad del sitio activo se refiere
a la capacidad de seleccin del sustrato
por la enzima. Varios factores contribuyen
a esta propiedad: la 3D del sitio activo,
caractersticas qumicas del sitio activo y la
estructura del sustrato (Figura 4.3).
Figura 4.1 Activacin de las enzimas.
Presentan estructura primaria, secundaria
y terciaria, y en algunas ocasiones, pueden
presentar estructura cuaternaria. Las
enzimas presentan una conformacin nativa
biolgicamente activa a pH fisiolgico.
Las enzimas actan sobre los reactantes
17
Curso Propedutico
Dentro de una clula hay cientos de enzimas
distintas. La especificidad hace que dentro
de un mismo compartimiento subcelular
puedan tener lugar, a la vez, cientos de
reacciones distintas sin que se confundan.
Existe un modelo, llamado modelo de
Fischer, que es conocido como llave
Antologa de Bioqumica / 1era. Edicin 2015
cerradura y explica que la enzima viene a
ser como una llave que slo est destinada
a abrir una cerradura.
Sin embargo, En 1958, Daniel Koshland
sugiere una modificacin al modelo de la
llave-cerradura: las enzimas son estructuras
bastante flexibles y as el sitio activo podra
cambiar su conformacin estructural por la
interaccin con el sustrato.
Q. F. B. Melba Fernndez Rojas
Ligasas: Permiten la unin de dos molculas
simultneamente a la degradacin de ATP
u otro enlace qumico, con la liberacin de
energa necesaria.
Factores que afectan la
actividad enzimtica
La actividad de las enzimas puede ser
regulada.
Algunas enzimas requieren cofactores en
el sitio activo para efectuar su actividad
biolgica. Estos pueden ser de dos clases:
1. Elemento inorgnico (Fe2+, Mg2+,
Cu2+ )
2. Molcula orgnica [coenzima] (FMN,
FAD, NAD+, CoASH)
Figura 4.3 Especificidad Enzimtica.
Clasificacin de las enzimas
Las enzimas se pueden clasificar en:
Oxidorreductasas: Relacionadas con
reacciones de xido-reduccin.
Transferasas: Catalizan el traspaso de
grupos qumicos, menos hidrgeno y
oxgeno. Ejemplos son metiltransferasas,
aciltransferasas, glucosiltransferasas
Hidrolasas: Tienen la capacidad de
introducir los elementos del agua en el
sustrato atacado, produciendo hidrlisis. Son
las esterasas, fosfatasas y glicosidasas.
Liasas: Catalizan la introduccin o eliminacin
de un grupo qumico a una doble ligadura.
Isomerasas: catalizan diversos tipos de
isomerizacin.
Cualquiera de los dos cofactores puede
estar unido a la enzima de manera dbil
(cosustrato) o de manera estrecha (grupo
prosttico).
La formacin del complejo enzima-sustrato
es intervenido por mltiples interacciones
individuales dbiles que liberan una
pequea cantidad de energa libre,
conocida como energa de enlazamiento.
Entre estas puede estar, el efecto del pH,
la temperatura o la concentracin de la
enzima:
El pH en el cual la velocidad de la reaccin
es mxima se denomina pH ptimo, que
generalmente vara entre 6 y 8.
La temperatura ptima es la de nuestro
cuerpo, entre 35 a 37 C. El incremento
de temperatura, aumenta la energa de
las molculas y favorece las reacciones
enzimticas. Pero, si se incrementa
demasiado la temperatura, la estructura
secundaria, terciaria y cuaternaria, se
pueden desestabilizar, y ocasionar una
prdida de la actividad.
Curso Propedutico
18
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Existen sustancias que impiden la funcin
de las enzimas. Son llamados inhibidores.
Existen inhibidores por competencia (que
tienen la forma del sustrato, y se sita en
el sitio del mismo en la enzima) y por no
competencia (bloquea los sitios activos de
una enzima de modo irreversible).
Anlisis enzimtico en
diagnstico de enfermedades
paperas
Fosfatasa cida: cncer de prstata,
enfermedad de Gaucher, mieloma
mltiple, cncer de hueso, hepatitis,
destruccin de plaquetas.
Fosfatasa alcalina: enfermedades
hepticas, metstasis de hueso,
leucemia y tumores.
TGP y ALT: enfermedad hepatocelular,
cirrosis, tumor metastsico, ictericia,
hepatitis y congestin heptica.
TGO y AST: necrosis, infarto y
enfermedades hepticas. Aumenta tras
12 horas de infarto y disminuye pasados
5 das.
Creatina fosfoquinasa:
muscular de Duchenne.
distrofia
Deshidrogenasa lctica DHL: infartos
al miocardio. Se eleva al 3 da del infarto
y se normaliza de 5 a 10 das despus..
19
Curso Propedutico
Aldolasa: Distrofia muscular
Lipasa: Se eleva en trastornos hepticos.
Colinesterasa: Sndrome nefrtico
La presencia de una actividad enzimtica
elevada en el plasma puede indicar
una lesin tisular, que se muestra por la
liberacin de enzimas en el plasma. Los
ejemplos ms comunes son:
Amilasa: Pancreatitis,
intoxicacin alcohlica.
CPK: Se utiliza para dx de infarto al
miocardio. Aumenta de 4 a 6 horas y
disminuye a los 2 o 3 das. Tambin
aumenta en la distrofia muscular.
Ceruloplasmina: Enfermedad de Wilson
y degeneracin hepatolenticular.
Gammaglutamil transferasa GGT: Se
eleva en todo tipo de trastorno heptico.
Es la enzima ms sensible de todas.
Troponinas: este es un complejo de
tres protenas comprendidas en la
contraccin muscular en los msculos
estriado y cardaco, no en el liso.
Proporciona indicadores sensibles
y especficos de dao del msculo
cardaco.
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD V: INTRODUCCIN
AL METABOLISMO
Metabolismo y leyes de la
termodinmica en sistemas
biolgicos
Los seres vivos son mquinas qumicas,
obtienen sus componentes y energa
mediante reacciones qumicas. Al conjunto
de reacciones qumicas en un ser vivo se
denomina metabolismo. El metabolismo
est constituido por dos procesos:
catablico y anablico. El catabolismo,
tambin llamado reaccin exergnica, es
un proceso acompaado de prdida de
energa, en tanto que el anabolismo, o
reaccin endergnica es acompaada por
ganancia de energa (Figura 5.1).
sus alrededores, permanece constante.
Eso implica que dentro de un sistema total,
la energa no se pierde ni se gana durante
cambio alguno, pero si se puede transferir
de una porcin del sistema a otra.
Figura 5.2 Sistemas Biolgicos.
La segunda ley establece que para que
un proceso ocurra de manera espontnea,
es necesario que la entropa total de un
sistema aumente.
Figura 5.1 Metabolismo.
Los sistemas biolgicos se conforman a las
leyes generales de la termodinmica. La
bioenergtica o termodinmica bioqumica
es el estudio de los cambios de energa
que acompaan a reacciones bioqumicas
(Figura 5.2).
La primera ley de la termodinmica establece
que la energa total de un sistema, incluso
La entropa es la extensin de trastorno o
de aleatoriedad del sistema y alcanza su
punto mximo conforme logra el equilibrio.
Oxidaciones Biolgicas
Desde el punto de vista qumico, la oxidacin
se define como la perdida de electrones,
en tanto que la reduccin es la ganancia
de electrones. De este modo, la oxidacin
siempre se acompaa de reduccin de un
aceptor de electrones.
Curso Propedutico
20
Antologa de Bioqumica / 1era. Edicin 2015
La reaccin REDOX se refiere a la prdida
de un electrn por una especie qumica
(oxidacin) y la ganancia de electrones por
otra (reduccin). La molcula donadora de
electrones se conoce como agente reductor
y a la molcula aceptora se le denomina
como agente oxidante.
Las enzimas comprendidas en oxidacin
y reduccin reciben el nombre de
oxidorreductasas y se clasifican en cuatro
grupos: oxidasas, deshidrogenasas,
hidroperoxidasas y oxigenasas.
Cadena respiratoria y
Fosforilacin oxidativa
La cadena respiratoria consiste de un
conjunto de transportadores de electrones
situados en la membrana interna mitocondrial.
La respiracin esta acoplada a la generacin
del intermediario de alta energa, ATP, por
medio de fosforilacin oxidativa. Diversos
frmacos (ej. Amorbital) y venenos (ej.
Cianuro, monxido de carbono) inhiben la
fosforilacin oxidativa.
Una unidad de respiracin mitocondria
consiste en una cadena respiratoria y una
ATP sintasa, enzima responsable de la
sntesis de ATP.
Q. F. B. Melba Fernndez Rojas
Los componentes de la cadena respiratoria
estn contenidos en cuatro complejos, los
electrones fluyen por la cadena a travs de
un intervalo REDOX desde NAD+/NADH
hacia O/2HO y pasan por tres complejos
protenicos (Figura 5.3).
1. NADH-Q oxidorreductasa (complejo
I), donde se transfieren electrones desde
NADH hacia la coenzima Q (ubiquinona).
2. Q- Citocromo c oxidorreductasa (complejo
III), que pasa electrones hacia el Citocromo c.
3. Citocromo c oxidasa recibe los electrones
de Citocromo c y de aqu se completa la
cadena, pasa los electrones hacia O y
hace que se reduzca a HO.
Algunas sustancias con potenciales
redox ms positivos que NAD+/NADH
(ej. Succinato) pasan electrones hacia
Q (ubiquinona) por medio de un cuarto
complejo, la Succinato- Q reductasa
(complejo II), en lugar de mediante el
complejo I. Los cuatro complejos estn
embebidos en la membrana mitocondria
interna, pero Q y Citocromo c son mviles.
El flujo de electrones a travs de los
complejos I, III y IV da por resultado el
bombeo de protones desde la matriz
Figura 5.3 Cadena Respiratoria.
21
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
a travs de la membrana mitocondria
interna hacia el espacio intermembrana.
El flujo de electrones por la cadena
respiratoria genera ATP por medio
de fosforilacin oxidativa. La teora
quimiosmtica postula que los dos procesos
estn acoplados mediante un gradiente de
protn a travs de la membrana interna,
de manera que la fuerza motriz de protn
causada por la diferencia de potencial
electroqumico impulsa el mecanismo de
sntesis de ATP mediante la bomba de
protones generada por los complejos I, III y IV.
Dado que la membrana mitocondria interna
es impermeable a protones, stos se
acumulan en el espacio intermembrana, lo
que crea la fuerza motriz de protn predicha
por la teora quimiosmtica.
La fuerza motriz de protn impulsa una ATP
sintasa ubicada en la membrana que en
presencia de Pi (fosfato inorgnico) + ADP
forma ATP. La ATP sintasa esta embebida
en la membrana mitocondria interna, junto
con los complejos de la cadena respiratoria
(marcado como complejo V en la figura
siguiente). Varias subunidades de la
protena forman una estructura parecida a
bola alrededor de un eje conocido como F,
que se proyecta hacia la matriz y contiene
el mecanismo de fosforilacin. F est fijo
a un complejo de protena de membrana
conocido como F, que tambin consta de
varias subunidades protenicas. F abarca
la membrana y forma un canal de protones.
El flujo de estos ltimos a travs de F hace
que rote, lo que impulsa la produccin de
ATP en el complejo F1 (Figura 5.4).
Se cree que esto sucede por un mecanismo
de cambio de unin, en el cual, a medida
que el eje rota, la conformacin de las
subunidades en F1 cambia desde una
Q. F. B. Melba Fernndez Rojas
que se une con firmeza al ATP hacia una
que libera ATP y se une a ADP y Pi, de
modo que puede formarse el siguiente
ATP. El ATP resultante se ha denominado
la moneda de energa de la clula. Figura
5.6
Figura 5.4 Fosforilacin Oxidativa.
Muchos venenos inhiben la cadena
respiratoria. Los barbitricos, como el
amorbarbital, inhiben el transporte de
electrones mediante el complejo I. La
antimicina A y el dimercaprol inhiben en el
complejo III. Los venenos clsicos H2S,
monxido de carbono y cianuro inhiben al
complejo IV, y en consecuencia, pueden
suspender por completo la respiracin.
El malonato es un inhibidor competitivo
del complejo II. El atractilsido inhibe la
fosforilacin oxidativa mediante la inhibicin
del transportador de ADP hacia dentro de
la mitocondria, y de ATP hacia fuera de
ella. El antibitico oligomicina bloquea por
completo la oxidacin y la fosforilacin al
bloquear el flujo de protones por medio de la
ATP sintasa. Los desacopladores disocian
la oxidacin en la cadena respiratoria, de la
fosforilacin. Estos compuestos son txicos
in vivo, lo que hace que la respiracin se
torne incontrolada. El desacoplador mas
usado es el 2,4-dinitrofenol.
Curso Propedutico
22
Antologa de Bioqumica / 1era. Edicin 2015
Figura 5.5 Mitocondria y Cadena Respiratoria.
Figura 5.6 Teora Quimiosmtica de Mitchell.
23
Curso Propedutico
Q. F. B. Melba Fernndez Rojas
Antologa de Bioqumica / 1era. Edicin 2015
Ciclo de Krebs
El ciclo del cido ctrico o ciclo de los cidos
tricarboxlicos, esta ruta metablica es la
tercera etapa de la respiracin celular, el
proceso de energa en las clulas. Forma
parte de la repiracin aerobia, requiere de
oxgeno, y se desarrolla entre los procesos
de gluclisis y cadena respiratoria; es una
secuencia de reacciones en las mitocondrias
que oxidan la porcin acetilo de la acetilCoA y reducen coenzimas que se reoxidan
por medio de la cadena de transporte de
electrones, enlazada a la formacin de
ATP. El ciclo de krebs es la va comn final
para la oxidacin de carbohidratos, lpidos
y protenas ya que se metabolizan hacia
acetil-CoA o intermediarios del ciclo (Figura
5.7 y 5.8).
La descarboxilacin oxidativa del piruvato
es un paso anterior al propio ciclo de Krebs.
Durante la gluclisis en el citoplasma se
produce el piruvato, que pasa por una etapa
de transicin para convertirse en acetil CoA
para que pueda entrar en el ciclo.
El piruvato pasa del citoplasma en las
mitocondrias donde el complejo enzimtico
piruvato deshidrogenasa lo convierte en
acetil coA.
La transformacin del piruvato en acetil
CoA es de gran importancia ya que une la
gluclisis y el ciclo de Krebs
El ciclo empieza con la reaccin entre
la porcin acetilo de la acetil-CoA y el
oxaloacetato, lo que forma citrato. Las
reacciones siguientes se liberan dos
molculas de CO2 y se regenera el
oxaloacetato. Este proceso es aerobio;
requiere oxgeno como el oxidante final
de las coenzimas reducidas. Las enzimas
del ciclo estn ubicadas en la matriz
Q. F. B. Melba Fernndez Rojas
mitocondrial donde tambin se encuentran
con las enzimas y coenzimas de la cadena
respiratoria.
Figura 5.7 Ciclo de Krebs
Reaccin 1
La reaccin inicial entre la acetil-CoA y
el oxaloacetato para formar citrato est
catalizada por la citrato sintasa.
Reaccin 2
La enzima aconitasa isomeriza el citrato
hacia isocitrato; esta reaccin ocurren
en 2 pasos: deshidratacin hacia cisaconitato, y rehidratacin hacia isocitrato.
El veneno fluoroacetato es txico por
que la fluoroacetil-CoA se condensa con
oxaloacetato para formar fluorocitrato, que
inhibe la aconitasa, lo que hace que se
acumule el citrato.
Reaccin 3
El isocitrato pasa por deshidrogenacin
catalizada por la isocitrato deshidrogenasa
para formar, en un inicio, oxalosuccinato,
que permanece unido a la enzima y pasa por
descarboxilacin hacia -cetoglutarato.
Curso Propedutico
24
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Reaccin 4
El -cetoglutarato pasa por descarboxilacin
oxidativa en una reaccin catalizada por un
complejo de mltiples enzimas. El complejo
de -cetoglutarato deshidrogenasa origina
la formacin de succinil-CoA. La arsenita
inhibe la reaccin, lo que hace que se
acumule el sustrato, -cetoglutarato.
Reaccin 6
La primera reaccin de deshidrogenacin,
que formar fumarato, es catalizada por la
succinato deshidrogenasa.
Reaccin 7
La fumarasa cataliza la adicin de de agua
a travs del doble enlace del fumarato, lo
que produce malato.
Reaccin 5
La succinil-CoA se convierte en Succinato
mediante la enzima succinato tiocinasa.
Reaccin 8
La malato deshidrogenasa convierte al
malato en oxaloacetato.
Cada vuelta del ciclo genera 12 ATP (Figura
5.9).
Figura 5.8 Destino final de Acetil CoA
25
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Figura 5.9 Ciclo de Krebs
Curso Propedutico
26
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD VI:
CARBOHIDRATOS
Importancia biomdica
las gluco- protenas y los proteoglucanos.
Los carbohidratos son la fuente primaria de
energa qumica necesaria para el correcto
funcionamiento celular. Adems de su
funcin como proveedores de energa,
los carbohidratos forman parte de los
materiales de construccin de diversos
constituyentes celulares.
Para la conversin de glucosa en energa
til para la clula (ATP), esta tiene que ser
oxidada a partir de procesos metablicos con
ayuda de diversos complejos enzimticos.
Las fallas en los mecanismos de regulacin
del metabolismo, deficiencias enzimticas
y diversos desequilibrios a nivel celular
relacionados con la conversin glucosa>energa se relacionan con diversas
enfermedades tales como diabetes
mellitus, galactosemia, enfermedades
por deposito de glucogeno, e intolerancia
a la lactosa.
En la economa de la clula, los carbohidratos
sirven como combustible. Los carbohidratos
que son utilizados directamente por la
clula para esta funcin son carbohidratos
que, de acuerdo a su tamao y con ayuda
del sistema de transporte activo, pueden
atravesar la membrana plasmtica para
que puedan transformarse en energa til
para la clula. La glucosa es el carbohidrato
ms importante; casi todo el carbohidrato
de la dieta se absorbe hacia el torrente
sanguneo como glucosa formada a partir
de otros carbohidratos ms complejos
(hidrlisis del almidn y disacridos de la
dieta).
As, la glucosa es el principal combustible
metablico de mamferos (excepto de los
rumiantes), y un combustible universal del
feto durante el embarazo. Una vez que ha
cumplido con su papel de principal proveedor
de energa , el organismo es capaz de
transformarla a otros carbohidratos que
tienen funciones altamente especificas,
por ejemplo, glucgeno para almacenaje;
ribosa en los cidos nucleicos; galactosa
en la lactosa de la leche y en ciertos lpidos
complejos y, combinada con protenas en
27
Curso Propedutico
Los carbohidratos estn compuestos por
unidades ms simples a su estructura
completa. Estas unidades de carbono
pueden unirse (polimerizarse) para producir
molculas complejas mas grandes que, a
su vez, pueden separarse de nuevo para
producir sus unidades bsicas de formacin
a voluntad de la propia clula.
Los procesos de sntesis (construccinpolimerizacin) y degradacin (separacin)
del metabolismo de los carbohidratos
pueden entenderse a partir de la clasificacin
de los carbohidratos en base a el numero
de unidades de carbono que lo conforman.
Clasificacin de los
Carbohidratos
1.- Monosacridos: son aquellos carbohidratos
que no pueden ser hidrolizados en molculas
ms sencillas.
Antologa de Bioqumica / 1era. Edicin 2015
Pueden subdividirse en
triosas, tetrosas, pentosas,
hexosas, heptosas u
octosas, dependiendo de
la cantidad de tomos de
carbn que contengan;
y como aldosas y cetosas dependiendo si
tienen o no grupo aldehido o cetona en su
estructura.
2.- Disacridos: Se producen de dos
molculas del mismo o de diferentes
monosacridos cuando se unen entre
si: ejemplos de estos compuestos son la
maltosa, que produce dos molculas de
glucosa, y la sucrosa, que produce una
inolcula de glucosa y una de fructosa
(Figura 6.1).
Q. F. B. Melba Fernndez Rojas
disacridos
cuya
estructura
est
conformada por dos monmeros, uno de
ellos o ambos, glucosa. Al ser hidrolizados,
estos disacridos se degradan hacia
glucosa que puede ser utilizada para
obtencin de energa.
3.- Oligosacaridos: son productos de
condensacion de 3 a 10 monosacaridos.
Casi ninguno es digerido por las enzimas
del ser humano.
4.- Polisacaridos: Son productos de
condensacion de mas de 10 unidades
de monosacaridos; los ejemplos son los
almidones y las dextrinas, que pueden
ser polimeros lineales o ramificados. Los
polisacaridos a veces se clasifican como
hexosanos o pentosanos, dependiendo
de la identidad de los monosacaridos
que los constituyen (hexosas y pentosas,
respectivamente) Figura 6.2.
Figura 6.1 Estructura de la Lactosa. Disacrido..
Estos disacridos tienen diferentes funciones
especficas:
1) Algunos son azcares reductores
2) Son necesarios en la dieta ya que son
fuente de energa
3) Para utilizarlos como fuente de
energa, los disacridos son hidrolizados
por enzimas que tapizan el intestino
delgado
4) La hidrolisis de los disacridos puede
dar lugar a la formacin de glucosa,
fructosa, galactosa, que son la fuente de
energa inmediata para las clulas.
El punto 4) puede explicarse gracias a esta
clasificacin. La fructosa y galactosa son
Figura 6.2 Diferentes tipos de Polisacaridos.
Ademas de almidones y dextrinas, los
alimentos contienen una amplia variedad
de otros polisacaridos que se conocen
en conjunto como polisacaridos no
almidon; las enzimas de ser humano no
los digieren, y son el principal componente
de la fibra en la dieta. Los ejemplos son
celulosa (un polimero de glucosa) de
paredes de celulas vegetales, e inulina (un
polimero de fructosa), el carbohidrato de
almacenamiento en algunos vegetales.
Curso Propedutico
28
Antologa de Bioqumica / 1era. Edicin 2015
En la tabla 6.1 se pueden observar
diversas funciones de los polisacridos en
la naturaleza y el cuerpo humano.
Metabolismo de carbohidratos:
Digestin.
Los carbohidratos de la dieta de los que los
humanos tomamos energa entran en el
organismo en una forma compleja, en forma
de monosacridos, disacridos, polmetros
de almidn (amilasa y amilopectina) y
glicgeno. El polmero celulosa (tambin
formado por glucosas) tambin es
consumido pero no digerido.
Q. F. B. Melba Fernndez Rojas
Tabla 6.1 Funcin de los Polisacaridos.
de la amilasa lingual est limitada a la boca
y esfago; es virtualmente inactivada por el
pH ms fuerte del estomago.
Una vez que la comida ha llegado al
estmago, la hidrlisis cida contribuye a la
degradacin: proteasas y lipasas gstricas
ayudan a la digestin de la comida. La
mezcla de las secreciones gstricas, saliva,
y comida se llama colectivamente quimo, y
se mueve hacia el intestino delgado (Figura
6.3).
El primer paso en el metabolismo de los
carbohidratos que se pueden digerir es
la conversin de grandes polmeros a
estructuras ms simples, formas solubles
que puedan ser transportados a travs
del intestino para ser distribuidos a los
tejidos. La digestin de los polmeros de
carbohidratos se inicia en la boca.
La saliva tiene un pH un poco acdico 6.8 y
contiene a la amilasa lingual que inicia la
degradacin de los carbohidratos. La accin
29
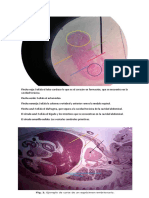
Curso Propedutico
Fig. 6.3 Digestin y Absorcin de Nutrientes
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
Figura 6.4 Catabolismo y Anabolismo de Nutrientes.
La enzima ms importante para degradar
los polmeros de carbohidratos en el
intestino delgado es la -amilasa. Esta
enzima es secretada por el pncreas y
tiene la misma actividad que la amilasa
de la saliva, produciendo disacridos y
trisacridos. Estos ltimos son convertidos
a
monosacridos
por
sacaridasas
intestinales, incluyendo maltasas, que
hidrolizan di- y tri-sacridos, y las enzimas
ms especificas las disacaridasas,
sucrasa, lactasa, y trealasa. El resultado
neto es la conversin casi completa
de los carbohidratos digeribles a sus
componentes monosacridos. La glucosa
resultante y otros carbohidratos simples
son transportados a travs del epitelio
intestinal a la vena portal heptica y luego a
las clulas hepticas y a otros tejidos. Ah,
estos azucares simples son convertidos a
cidos grasos, aminocidos, y glicgeno, o
sino oxidados por varias vas metablicas
celulares (Figura 6.4).
La glucosa se fosforila para poder entrar
a cualquier va metablica a glucosa 6
fosfato, donde :
1. Podr utilizarse como combustible para
el metabolismo aerbico o anaerbico en
el caso del msculo; o bien convertirse
en glucosa libre en el hgado y liberarse
seguidamente a la sangre.
2. Almacenarse en forma de glucgeno
en el hgado.
3. Procesarse por la va de las Pentosa
Fosfato.
Curso Propedutico
30
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
sirven como combustible y son oxidados
para pasar a CO2 y Agua, proceso durante
el cual se libeTa energa en forma de ATP
(Adenosin trifosfato).
Figura 6.5 Estructura del ATP.
Figura 6.4 Destinos de la glucosa 6-fosfato. La glucosa
6-fosfato procedente del glucgeno puede (1) utilizarse como
combustible para el metabolismo aerbico o anaerbico somo
sucede, por ejemplo, en el msculo; (2) convertirse en glucosa
libre en el hgado y liberarse seguidamente a la sangre; (3)
procesarse por la va de las pentosas fosfato para producir
NADPH o ribosa en diversos tejidos.
Glucolisis: Metabolismo
de la glucosa.
Como hemos mencionado anteriormente,
la glucosa es un carbohidrato esencial en
la dieta ya que al pasar por un proceso de
oxidacin es capaz de aportar de la energa
necesaria para realizar todas las funciones
biolgicas. La oxidacin es un proceso
mediante en el cual se aaden molculas
de oxgeno a una molcula o bien se le
extraen electrones, por lo que no siempre
la oxidacin es vinculada al oxgeno. Estos
procesos requieren de alguna manera
el transporte de oxgeno y electrones
de un lugar a otro. As , toda reaccin de
oxidacin debe acompaarse de reduccin
(eliminacin de oxgeno o adhesin de
hidrgeno o electrones a una sustancia)
En el cuerpo humano, los carbohidratos
31
Curso Propedutico
El ATP puede compararse a un acumulador
cargado con energa disponible para
el trabajo celular. De manera que al
proporcionar la energa, el ATP cede
electrones para permitir las reacciones
metablicas, y se oxida hacia una molcula
mas sencilla conocida como ADP (Adenosin
Difosfato).
Al romper los enlaces entre los grupos
fosfato de la molcula de ATP existe
liberacin de energa asimilada por la
clula.
La obtencin de energa se da a partir de
3 o 4 pasos importantes, uno despus de
otro, trabajando como un metabolismo en
cadena para la formacin de ATP:
Figura 6.6 Transporte de a Energa del ATP y formacin de ADP
despus de ceder electrones.
Antologa de Bioqumica / 1era. Edicin 2015
1. Glucolisis (oxidacin de la glucosa)
2. Formacin de Acetil CoA
3. Ciclo del cido ctrico (Ciclo de
Krebs)
4. Cadena respiratoria (Fosforilacin
Oxidativa)
De tal manera que podemos definir a la
Glucolisis como el proceso metablico por
el cual la clula es capas de obtener ATP a
partir de la oxidacin de la glucosa.
Q. F. B. Melba Fernndez Rojas
produce por un aumento de la produccin
de Lactato a travs de Glucolisis (Figura
6.6).
A traves de diversos complejos enzimticas,
la molcula de glucosa ser oxidada, y los
electrones perdidos se unirn a diversas
molculas que los transportarn para
transformarlos en ATP (Cuadro 6.1).
La glucosa es oxidada a lactato o piruvato.
Bajo condiciones aerbicas, el producto
dominante en la mayora de tejidos es el
piruvato y la va metablica se conoce
como gliclisis aerbica.
La capacidad de la glucolisis para
proporcionar ATP en ausencia de oxigeno
tiene especial importancia, porque esto
permite al musculo estriado tener un
desempeno a cifras muy altas de gasto
de trabajo cuando el aporte de oxigeno es
insuficiente, y permite a los tejidos sobrevivir
a episodios de anoxia.
Las enfermedades en las cuales hay
deficiencia de las enzimas de la glucolisis
(p. ej., piruvato cinasa) se observan sobre
todo como anemias hemoliticas o, si el
defecto afecta el musculo estriado (p.
ej., fosfofructocinasa), como fatiga. En
las celulas cancerosas en crecimiento
rapido, la gluclisis procede a un indice
alto, formando grandes cantidades de
piruvato, el cual es reducido hacia lactato y
exportado. Esto produce un ambiente local
hasta cierto punto acido benfico para el
desarrollo del tumor. La acidosis lactica se
Figura 6.6 Gluclisis.
Metabolismo del Glucgeno.
Se dice que una vez que la clula satisface
sus necesidades de aporte energtico, esta
es capaz de almacenar la glucosa restante
para utilizarla en un momento en el que
Figura 6.7 Sntesis del Glucgeno.
Curso Propedutico
32
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
se detenga la ingesta calrica o bien se
requiera energa extra (Figura 6.7).
Si el azcar (glucosa) en la clula no
es utilizada de inmediato, puede salir
y perderse. En cambio, si se retiene,
contribuye a aumentar la presin osmtica
en la clula.
Para almacenarla y evitar que se pierda,
la glucosa debe ser convertida en una
forma estructural en la que no pueda
pasar por la membrana y no pueda salir.
La clula almacena carbohidratos en forma
de molculas grandes e insolubles como
almidn y glucgeno. Para convertirse en
glucgeno y quedar almacenada, complejos
multienzimticos se encargan de ramificar
grandes cantidades de monmeros de
glucosa en una estructura compleja que
permite su almacenamiento, principalmente
en el msculo.
El glucogeno hepatico funciona para
almacenar glucosa y exportarla para
mantener la concentracion de glucosa en
sangre durante el estado de ayuno.
La concentracion de glucogeno en el higado
es de alrededor de 450 mM despues de una
comida; disminuye a alrededor de 200 mM
tras ayuno de toda la noche; luego de 12 a
18 horas de ayuno, el glucogeno hepatico
esta agotado casi en su totalidad (Figura
6.8).
Gluconeognesis:
En ocasiones, los niveles de energa
requeridos por la clula son tan altos que
la energa aportada por la glucosa no es
suficiente. Despus de haber destinado toda
la glucosa disponible para la obtencin de
energa y al acabar las reservas del cuerpo
(glucgeno almacenado), el organismo
es capaz de utilizar otras Biomolculas
adquiridas en la dieta, transformndolas
primero en intermediarios capaces de
cumplir con el aporte de energa que el
cuerpo necesita. De tal manera, que tras
un ayuno prolongado de 24 horas, el
organismo comenzar a consumir todas
sus reservas no solo de carbohidratos, si no
tambin de lpidos y protenas esenciales
para el funcionamiento celular.
Figura 6.8 Glucognesis
33
Curso Propedutico
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
De tal manera que aminocidos, cidos
grasos y glicerol que son productos
de la digestin de lpidos y protenas,
pueden ser transformados por diversas
vas gluconeognicos en tres puntos
principales:
1) Formacin de piruvato: capaz de
convertirse en Acetil CoA y entrar al ciclo
de Krebs para producir energa
2) Acetil CoA: que se dirija a Krebs.
3) Intermediarios del ciclo de Krebs:
para dar mas energa.
Curso Propedutico
34
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
UNIDAD VII:LPIDOS
Los lpidos son un grupo de compuestos
heterogneo, que incluye grasas, aceites,
esteroides, ceras y compuestos relacionados
ms por sus propiedades fsicas que por
sus propiedades qumicas.
Tienen la propiedad comn de ser:
1) relativamente insolubles en agua
2) solubles en solventes no polares
Son importantes constituyentes de la dieta
no slo debido a su alto valor energtico,
sino tambin debido a las vitaminas
liposolubles y los cidos grasos
esenciales contenidos en la grasa de
alimentos naturales.
Las combinaciones de lpido y protena
(lipoprotenas) sirven como el medio para
transportar lpidos en la sangre. Los
lpidos tienen funciones esenciales en la
nutricin y la salud, y el conocimiento de
la bioqumica de los lpidos es necesario
para entender muchas enfermedades
biomdicas.
8.1 Clasificacin de Lpidos
1. Lpidos simples: steres de cidos
grasos con diversos alcoholes.
Grasas: steres de cidos grasos con
glicerol. Los aceites son grasas en el
estado lquido.
Ceras: steres de cidos grasos
con alcoholes monohdricos de masa
molecular relativa (peso molecular) ms
alta.
2. Lpidos complejos: steres de cidos
grasos que contienen grupos adems de
un alcohol y un cido graso.
35
Curso Propedutico
Fosfolpidos: lpidos que contienen,
adems de cidos grasos y un alcohol,
un residuo cido fosfrico. A menudo
poseen bases que contienen nitrgeno
y otros sustituyentes, por ejemplo, en los
glicerofosfolpidos el alcohol es glicerol,
y en los esfingofosfolpidos el alcohol es
la esfingosina.
Glucolpidos (glucoesfingolpidos):
lpidos que contienen un cido graso,
esfingosina y carbohidrato.
Otros lpidos complejos: lpidos como
sulfolpidos y aminolpidos.
Las lipoprotenas tambin pueden
colocarse en esta categora.
3. Lpidos precursores y derivados:
comprenden cidos grasos, glicerol,
esteroides, otros alcoholes, aldehdos
grasos, cuerpos cetnicos.
Unidad Organizacional de
los Lpidos: el cido Graso
Son cidos carboxlicos, contienen un
grupo carboxilo en el tomo de C1.
Se comportan como cidos dbiles.
La cadena hidrocarbonada consiste de 4 a
36 tomos de carbono.
Existen dos tipos de cidos grasos segn
la presencia o no de dobles enlaces en la
cadena hidrocarbonada:
cidos grasos saturados sin dobles
enlaces
cidos grasos insaturados con dobles
enlace (Figura 7.1).
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
temperatura ambiente (25oC).
Son rigidos.
Figura 7.1 Clasificacin de los cidos grasos.
Los cidos Grasos Saturados no
Contienen Dobles Enlaces
Los cidos grasos saturados pueden
imaginarse como basados en cido actico
(CH3COOH) en la cual se agrega de
manera progresiva CH2 entre los
grupos CH3 y COOH terminales.
Figura 7.2 cidos Grasos
Saturados
Presentan
conformacin
extendida.
Rotan alrededor de
los enlaces carbono
-carbono sencillos.
Forman
agregados estables
(empaquetamiento).
(Figura 7.2).
Estabilizan los agregados por interacciones
de Van der Waals entre las cadenas
hidrocarbonadas.
Presentan elevado punto de fusin (Tm);
se requieren elevadas temperaturas para
separar los cidos grasos del agregado.
Tienen consistencia slida a
Los cidos Grasos Insaturados
Contienen Uno o Ms
Enlaces Dobles
No presentan
conformacin
extendida, el
doble enlace
introduce un ngulo
en la estructura
de la cadena
hidrocarbonada.
Todos los
enlaces sencillos
Figura 7.2 cidos Grasos
carbono- carbono
Insaturados.
pueden rotar, excepto el comprometido
en el doble enlace.
No se pueden empaquetar tan fcilmente
como los cidos grasos saturados,
sus interacciones son ms dbiles.
Presentan bajo punto de fusin (Tm), se
requieren bajas temperaturas para separar
los cidos grasos del agregado.
Presentan consistencia de blanda a
lquida
a temperatura ambiente.
No son rgidos (Figura 7.3).
Los cidos grasos insaturados, pueden
subdividirse como sigue:
1. cidos monoinsaturados (monoetenoide,
monoenoico) que contienen un doble
enlace.
2. cidos poliinsaturados (polietenoide,
polienoico), que contienen dos o ms
dobles enlaces.
3. Eicosanoides: estos compuestos,
derivados de cidos grasos polienoicos
eicosa
(20
carbonos),
incluyen
prostanoides, leucotrienos (LT) y
lipoxinas (LX).
Curso Propedutico
36
Antologa de Bioqumica / 1era. Edicin 2015
Los prostanoides comprenden
prostaglandinas (PG), prostaciclinas
(PGI) y tromboxanos (TX).
Los lpidos tienen la propiedad comn
de ser relativamente insolubles en agua
(hidrofbicos) pero solubles en solventes
no polares.
Los lpidos anfipticos tambin contienen
uno o ms grupos polares, lo que hace
que sean idneos como constituyentes de
membranas en interfases lpidoagua.
Los lpidos de gran importancia fisiolgica
son los cidos grasos y sus steres, junto
con el colesterol y otros esteroides.
8.2 Metabolismo de los lpidos.
Digestion y absorbcion de grasas.
El objetivo primario de la digestin de los
lpidos es hacerlos hidromiscibles y puedan
absorberse a travs de las microvellosidades
intestinales que estn recubiertas por una
capa acuosa. La separacin mecnica de
los lpidos comienza en el estmago por
efecto de los movimientos peristlticos,
contina en el duodeno a donde llega
una grosera emulsin de grasa que se ir
hidrolizando gracias a la accin combinada
de las lipasas pancreticas y de las sales
biliares, facilitando la accin de las enzimas
pancreticas.
La hidrlisis de los triglicridos aun as no
es total sino que se forman unas micelas
de monoglicridos, cidos grasos y cidos
biliares, transportan los lpidos hasta las
clulas de la mucosa intestinal donde son
posteriormente absorbidas.
Absorcin intestinal de los lpidos
Los fosfolpidos y los cidos grasos
37
Curso Propedutico
Q. F. B. Melba Fernndez Rojas
procesados son digeridos y absorbidos
a travs de la pared del intestino. La bilis
secretada por el hgado y las secreciones
pancreticas (ricas en enzimas y en especial
las lipasas pancreticas y bicarbonato)
se mezclan con el contenido del intestino
delgado. Las secreciones biliares en
especial los cidos glicoclico, tauroclico
y clico son esenciales para preparar los
lpidos para absorcin, formando partculas
mezclables con agua que pueden entrar
en las clulas intestinales. En las clulas
intestinales la mayor parte de los cidos
grasos se ligan con glicerol (proveniente
de la glucosa de la sangre) para formar
triglicridos.
Los triglicridos, algunos cidos grasos
libres, colesterol y otras sustancias
relacionadas con lpidos se recubren con
protenas para formar lipoprotenas ricas en
triglicridos, tambin llamados lipoprotenas
de baja densidad. Las lipoprotenas ricas en
triglicridos entran en los vasos linfticos
y de all pasan al canal torcico (donde el
sistema linftico se conecta con la sangre)
y as llegan a la sangre. En contraste con la
mayora de nutrientes absorbidos en el tracto
gastrointestinal los lpidos absorbidos no
van al hgado sino que entran directamente
a la circulacin general. As los lpidos
absorbidos pueden ser utilizados por todos
los tejidos del cuerpo sin ser procesados
por el hgado.
Catabolismo de los lpidos
El principal mecanismo de obtencin de
energa de los lpidos (sustancias con muy
alto valor calrico) lo constituye la oxidacin
de los cidos grasos, que se obtienen de los
triglicridos mediante hidrlisis por lipasas
especficas. stos siempre podrn entrar
en el ciclo de Krebs, por lo que cuanto ms
largo sea el cido graso mayor cantidad de
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
energa se obtendr en su oxidacin.
En el caso de los mamferos, los cidos
grasos (en forma de triglicridos) tienen
una importancia capital como almacn y
fuente de energa. El principal mecanismo
de obtencin de energa de los lpidos lo
constituye la llamada beta-oxidacin de los
cidos grasos. Los cidos grasos se unirn
a una molcula de coenzima A (CoA) en el
citoplasma, quedando activados como acilCoA.
De esta forma pasan a la mitocondria,
donde sufren el proceso denominado
b-oxidacion. Los cidos grasos se oxidan
completamente hasta dixido de carbono y
agua. El resultado de cada ciclo oxidativo
de la beta-oxidacin de los cidos grasos
es la formacin de equivalentes reductores
(FADH2 y NADH), una molcula de
acetil-coenzima A y una molcula de acilcoenzima A dos carbonos ms corta. El
acetil-coenzima A se incorpora al ciclo de
Krebs para continuar su degradacin.
Curso Propedutico
38
Antologa de Bioqumica / 1era. Edicin 2015
Q. F. B. Melba Fernndez Rojas
BIBLIOGRAFA
1.- Bioqumica Ilustrada Harper
Robert K. Murray, David A. Bender, Kathleen M. Botham, Peter J. Kenelly, Rodwell
Victor W, P. Anthony Weil
29 a edicin
Mc Graw Hill
2.- Bioqumica de Laguna
Jos Laguna, Enrique Pia
5a edicin
Manual Moderno
3.- Lippincotts Ilustrated Reviews : Bioqumica
Richard A. Harvey, Ph. D., Denise R. Ferrier, Ph.D
5a edicin
Wolters Kluwer Health
39
Curso Propedutico
También podría gustarte
- Práctica 3. Tejido Conjuntivo OrdinarioDocumento5 páginasPráctica 3. Tejido Conjuntivo OrdinarioJesus Eduardp HernandezAún no hay calificaciones
- Taller - 2 MoleculasDocumento6 páginasTaller - 2 MoleculasSteven Leyton100% (1)
- Sangre y Renal. Fis. AplicadaDocumento17 páginasSangre y Renal. Fis. AplicadaMaEs PegueroAún no hay calificaciones
- CLASE 7.B. Atributos Especiales Del Sistema Del LinfocitoDocumento21 páginasCLASE 7.B. Atributos Especiales Del Sistema Del LinfocitoValeria Ponce MurilloAún no hay calificaciones
- Presentación Tejido Cartilaginoso 2020Documento15 páginasPresentación Tejido Cartilaginoso 2020Jean-Ull Nimes-SimoneAún no hay calificaciones
- Torax Anterior: 6ta Costal Reborde CostaDocumento1 páginaTorax Anterior: 6ta Costal Reborde CostaAna Cecilia MantillaAún no hay calificaciones
- Perfiles HematologicosDocumento4 páginasPerfiles HematologicosDaniel ValenciaAún no hay calificaciones
- Reumatologia Historia Clinica de Artritis Septica y Artrosis p1Documento8 páginasReumatologia Historia Clinica de Artritis Septica y Artrosis p1JAMMILETH LENNY SALVATIERRA GUTIERREZAún no hay calificaciones
- Copia de Programa Infectologia 2019-2Documento207 páginasCopia de Programa Infectologia 2019-2Yakayri FriasAún no hay calificaciones
- Lecturas PDFDocumento114 páginasLecturas PDFAlex AcostaAún no hay calificaciones
- Túnica Íntima, Media y Adventicia.. DiapositivasDocumento5 páginasTúnica Íntima, Media y Adventicia.. DiapositivasAlicia Chavez CernaAún no hay calificaciones
- Programa Fisiologia Celular. Plan 14Documento27 páginasPrograma Fisiologia Celular. Plan 14Nicole CorderoAún no hay calificaciones
- EXPERRIMENTO 13 Endogrino GrupalDocumento16 páginasEXPERRIMENTO 13 Endogrino GrupalSHEILA CESPEDESAún no hay calificaciones
- Slide - Apendicitis AgudaDocumento73 páginasSlide - Apendicitis AgudaGabrielly CristiniAún no hay calificaciones
- El Corazon EnsayoDocumento4 páginasEl Corazon Ensayomilagros rinconAún no hay calificaciones
- Apuntes Antropología MédicaDocumento8 páginasApuntes Antropología MédicaMarcelo Rojas DuarteAún no hay calificaciones
- Plexo CeliacoDocumento3 páginasPlexo CeliacoAlezie Roosevelt Paul GarciaAún no hay calificaciones
- Configuración Interna Del Cráneo y Cavidades de La CaraDocumento3 páginasConfiguración Interna Del Cráneo y Cavidades de La CaraLuisa Albania Casilla Mancebo100% (1)
- Función RenalDocumento4 páginasFunción RenalHernández Arroyo RodrigoAún no hay calificaciones
- Microambiente MedularDocumento11 páginasMicroambiente MedularGido Cliner Quispe FernandezAún no hay calificaciones
- Membrana PlasmáticaDocumento20 páginasMembrana PlasmáticaJr EscobarAún no hay calificaciones
- Relacion Medico Paciente SociedadDocumento6 páginasRelacion Medico Paciente SociedadKevin GiraldoAún no hay calificaciones
- Oncologia Conceptos 1Documento6 páginasOncologia Conceptos 1angeli yamilex zarzuela bocio100% (1)
- Generalidades de Los TejidosDocumento6 páginasGeneralidades de Los TejidosJuan Antonio100% (2)
- EspermatobiosDocumento4 páginasEspermatobiosAndrés VillanuevaAún no hay calificaciones
- Lab 3 Reflejos V 2020Documento14 páginasLab 3 Reflejos V 2020Angie IzaguirreAún no hay calificaciones
- 2do Parcial Transcripcion Notas de Voz Anestesiologia UASDDocumento12 páginas2do Parcial Transcripcion Notas de Voz Anestesiologia UASDFidel CastilloAún no hay calificaciones
- Proy Nom 015 Ssa2 2018Documento30 páginasProy Nom 015 Ssa2 2018Javier Orozco100% (1)
- Farmacologia I - Unidad IIIDocumento102 páginasFarmacologia I - Unidad IIIadrngilson11Aún no hay calificaciones
- 7 - Conferencia Enfoque Epidemiologico de Las DiarreasDocumento11 páginas7 - Conferencia Enfoque Epidemiologico de Las DiarreasMarcusAún no hay calificaciones
- El Maravilloso Cerebro HumanoDocumento3 páginasEl Maravilloso Cerebro HumanoCristiano CorreaAún no hay calificaciones
- TRIPLOIDÍADocumento6 páginasTRIPLOIDÍAvelichek67% (3)
- Importancia de La InmunogeneticaDocumento1 páginaImportancia de La InmunogeneticaZeynara ZapataAún no hay calificaciones
- Proyecto de Investigacion de Histologia YANETTDocumento30 páginasProyecto de Investigacion de Histologia YANETTjuliocesar100% (10)
- Exploracion de Sistema CardiovascularDocumento53 páginasExploracion de Sistema CardiovascularValeria MoraAún no hay calificaciones
- Patologia GalenicaDocumento4 páginasPatologia GalenicaJaimecesar Ch MAún no hay calificaciones
- 4 A 8 Semana de Desarrollo EmbrionarioDocumento2 páginas4 A 8 Semana de Desarrollo EmbrionarioYesenia Nayeli Bellot MontañoAún no hay calificaciones
- Resumen Del Capitulo 2 y 3 Guyton y HallDocumento7 páginasResumen Del Capitulo 2 y 3 Guyton y HallEdward ArredondoAún no hay calificaciones
- Componentes Químicos Del Líquido Intracelular y ExtracelularDocumento28 páginasComponentes Químicos Del Líquido Intracelular y Extracelularelaine16080% (1)
- Ruta de La Vida 4 DemorasDocumento44 páginasRuta de La Vida 4 DemorasMario Fernando Villota Esparza0% (1)
- Diferencias Video 8 y 9 - Tarea #5 - BiofísicaDocumento5 páginasDiferencias Video 8 y 9 - Tarea #5 - BiofísicaDiego Carrera100% (1)
- Diabetes Insípida FisiologíaDocumento13 páginasDiabetes Insípida FisiologíaFiorella YavarAún no hay calificaciones
- Historia de La FisiologiaDocumento3 páginasHistoria de La Fisiologiamari barrientosAún no hay calificaciones
- Parcial de NucleoDocumento5 páginasParcial de NucleoMelissa LukasiewiczAún no hay calificaciones
- Programa de Bio IIDocumento3 páginasPrograma de Bio IICarlenis RamosAún no hay calificaciones
- Qué Es La TerologiaDocumento8 páginasQué Es La TerologiaAlexandra EAAún no hay calificaciones
- Corazón Como BombaDocumento4 páginasCorazón Como BombaMary ElisaAún no hay calificaciones
- Resumen Histología Bloque 1Documento75 páginasResumen Histología Bloque 1Winny Wen WenAún no hay calificaciones
- Patologia de Musculo EstriadoDocumento17 páginasPatologia de Musculo Estriadojose A100% (2)
- Región SupramesocólicaDocumento12 páginasRegión SupramesocólicaJaviera AriasAún no hay calificaciones
- Células AtipicasDocumento4 páginasCélulas AtipicasMontse Medina100% (3)
- Patrones No ClasicosDocumento5 páginasPatrones No ClasicosMiguel Angel Acosta ReinosoAún no hay calificaciones
- Guía Paso A Paso para Describir Las Fracturas en La RadiografíaDocumento21 páginasGuía Paso A Paso para Describir Las Fracturas en La RadiografíaYaely SosaAún no hay calificaciones
- Insuficiencia RenalDocumento16 páginasInsuficiencia RenalPaulina Rosas GleasonAún no hay calificaciones
- 5ta Clase Practica de Embriologia - ApuntesDocumento15 páginas5ta Clase Practica de Embriologia - ApuntesGuillermo Peralta LópezAún no hay calificaciones
- Plexo Cervical y BraquialDocumento7 páginasPlexo Cervical y BraquialAlexJoshep CoKaAún no hay calificaciones
- Resumen de Embriología Regulacion MolecularDocumento5 páginasResumen de Embriología Regulacion MolecularJeisson Jauregui100% (1)
- BHCDocumento11 páginasBHCAndy ArreguiinAún no hay calificaciones
- Control de La Osmolaridad y de La Concentración de Sodio Del Líquido ExtracelularDocumento3 páginasControl de La Osmolaridad y de La Concentración de Sodio Del Líquido ExtracelularIrma TaipeAún no hay calificaciones
- Texto Bioquimica 2022Documento130 páginasTexto Bioquimica 2022jhossepcondorimamaniAún no hay calificaciones
- Biología Molecular y Celular: Una guía introductoria para aprender Biología Celular y MolecularDe EverandBiología Molecular y Celular: Una guía introductoria para aprender Biología Celular y MolecularAún no hay calificaciones
- Bioquimica, Trabajo 2.Documento11 páginasBioquimica, Trabajo 2.Litzy IsabelAún no hay calificaciones
- TA80112 La Alimentacion y Nutricion AnimalDocumento9 páginasTA80112 La Alimentacion y Nutricion AnimalCristian ChavarriaAún no hay calificaciones
- Que Es Una Biomolécula ExposicionDocumento4 páginasQue Es Una Biomolécula ExposicionMARIA USTARIZ FRAGOZOAún no hay calificaciones
- Biomoléculas Orgánicas 4Documento4 páginasBiomoléculas Orgánicas 4Deyvi MsAún no hay calificaciones
- Libro Del MinisterioDocumento5 páginasLibro Del Ministerioesteban estevezAún no hay calificaciones
- Biolelementos y Ciclos GeoquimicosDocumento33 páginasBiolelementos y Ciclos GeoquimicosJesus TrujilloAún no hay calificaciones
- Clase 1 Celula Planos GeneralidadesDocumento78 páginasClase 1 Celula Planos GeneralidadesAna Fabiola Mosqueda DiazAún no hay calificaciones
- 4°sec - UNIDAD 1 - ACTIVIDAD 3 (CyT Explica 2024) - Los Carbohidratos y Las ProteínasDocumento7 páginas4°sec - UNIDAD 1 - ACTIVIDAD 3 (CyT Explica 2024) - Los Carbohidratos y Las ProteínaskarurocorreoAún no hay calificaciones
- Programa Curricular para La Primera Unidad de Ciencia y Tecnologia Cuarto Grado 2019Documento9 páginasPrograma Curricular para La Primera Unidad de Ciencia y Tecnologia Cuarto Grado 2019juilianrtAún no hay calificaciones
- Cuestionario CarbohidratosDocumento4 páginasCuestionario CarbohidratosRoque EStradaAún no hay calificaciones
- Examen de Entrada 4 y 5to Sec BiologíaDocumento7 páginasExamen de Entrada 4 y 5to Sec BiologíaMily Malú Miluska Chávez GamarraAún no hay calificaciones
- Relación Entre Bioelementos y BiomoleculasDocumento7 páginasRelación Entre Bioelementos y BiomoleculasAngie QuirozAún no hay calificaciones
- Nociones de BioquimicaDocumento7 páginasNociones de BioquimicaMichelle EscobarAún no hay calificaciones
- Ciencias Naturales Guía 10Documento225 páginasCiencias Naturales Guía 10Teonila57% (7)
- PNP 7 BiologiaDocumento20 páginasPNP 7 BiologiaYerson Lopez100% (1)
- Cuadernillo Introductorio 2022-BiologiaDocumento51 páginasCuadernillo Introductorio 2022-BiologiaMartin VeglienzoneAún no hay calificaciones
- Bioelementos y Biomoléculas InorgánicasDocumento43 páginasBioelementos y Biomoléculas InorgánicasJohana Ninaja AlferezAún no hay calificaciones
- Carpeta DigitalDocumento21 páginasCarpeta Digitalperla diazAún no hay calificaciones
- Preguntas de BiologiaDocumento3 páginasPreguntas de BiologiaManuel Orlando Zamata SanchezAún no hay calificaciones
- Sales MineralesDocumento12 páginasSales MineralesDaniel Ibáñez FuentesAún no hay calificaciones
- Ejercicio1 Unidad1Documento3 páginasEjercicio1 Unidad1Eyleen MandonAún no hay calificaciones
- Unidad 02 - Biomoleculas OrganicasDocumento9 páginasUnidad 02 - Biomoleculas OrganicasIsmael Cabello CarrilloAún no hay calificaciones
- Tema 5Documento6 páginasTema 5doloresAún no hay calificaciones
- Biomoléculas y Ciclos BiogeoquímicosDocumento13 páginasBiomoléculas y Ciclos BiogeoquímicosDoccccccccccAún no hay calificaciones
- Práctica #1. Composición Química de La Materia VivaDocumento17 páginasPráctica #1. Composición Química de La Materia VivaMerlin Alberto Encarnacion de los Santos100% (1)
- ECA 1 Temas de Biología ContemporáneaDocumento11 páginasECA 1 Temas de Biología ContemporáneavicjoaquinAún no hay calificaciones
- La Materia Viva III ClaseDocumento43 páginasLa Materia Viva III ClaseAlexandra Pastor TarrilloAún no hay calificaciones
- Bioelementos para Que Sirven y Cual Es Su Función en El CuerpoDocumento4 páginasBioelementos para Que Sirven y Cual Es Su Función en El CuerpoKaren V. ArceAún no hay calificaciones
- Taller 1° BioqumicaDocumento5 páginasTaller 1° BioqumicaElizabeth VidalAún no hay calificaciones