Documentos de Académico
Documentos de Profesional
Documentos de Cultura
11 Estudios Pre y Clinicos
11 Estudios Pre y Clinicos
Cargado por
Betsy Villafan0 calificaciones0% encontró este documento útil (0 votos)
9 vistas20 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
9 vistas20 páginas11 Estudios Pre y Clinicos
11 Estudios Pre y Clinicos
Cargado por
Betsy VillafanCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 20
1
Estudios Pre-clnicos y Clnicos
Roco Ramrez Herrera Norma Edith Soto Ruz
Dictaminadoras Especializadas
DIRECCIN EJECUTIVA DE AUTORIZACIN DE PRODUCTOS Y ESTABLECIMIENTOS
2
ESTUDIOS PRECLNICOS
Conjunto de estudios para el desarrollo de un medicamento que se
efectan in vitro o en animales de experimentacin y que se disean
para obtener la informacin necesaria para decidir si se justifican
estudios ms amplios en seres humanos, sin exponerlos a riesgos
injustificados.
3
ESTUDIOS PRECLNICOS
Se requieren para:
Molculas nuevas.
Vacunas.
Hurfanos.
Articulo 167 de Fraccin I inciso C del Reglamento de Insumos Para la Salud.
Artculos 62, 65, 66, 67. Capitulo II Dela investigacin Farmacolgica del Reglamento de la Ley General de
Salud en Materia de Investigacin en Materia de Salud.
4
ESTUDIOS PRECLNICOS
Estudios preclnicos
Especies animales utilizadas (dos roedor y un no roedor).
Estudios toxicolgicos.
Toxicologa general: Aguda, Subaguda, Crnica.
Toxicidad aguda: Exposicin a una sola dosis mnima y dosis Letal DL50. El objetivo es
obtener datos sobre los efectos producidos en el animal despus de una nica exposicin del
material de ensayo.
Toxicidad Subaguda: Exposicin de dosis repetidas en un periodo de tiempo. El objetivo es
obtener los efectos adversos que ocurren como resultado de una dosis diaria repetida de una
sustancia qumica, o exposicin a una sustancia qumica durante parte del ciclo de vida de un
organismo (generalmente, no excede 10%). Con animales experimentales, el perodo de
exposicin puede variar de unos pocos das a seis meses.
5
ESTUDIOS PRECLNICOS
Toxicidad Crnica:
Son los estudios en donde se observa los efectos adversos que ocurren como resultado de
dosis repetidas con una sustancia qumica sobre una base diaria, o exposicin a la sustancia
qumica durante la mayor parte de vida de un organismo (generalmente, ms del 50%). Con
animales experimentales, esto generalmente significa un perodo de exposicin de ms de
tres meses. Los estudios con exposicin crnica durante dos aos, se hacen con ratas o
ratones para evaluar el potencial carcinognico de las sustancias qumicas.
Carcinogenicidad:
Son los estudios en donde se observa la propiedad de producir cncer en animales. Observa
la incidencia de los tumores espontneos.
Genotoxicidad :
Son los estudios en donde se observa la capacidad para causar dao al material gentico; el
dao puede ser de tipo mutgeno o carcingeno. Pueden identificar agentes mutagnicos y
cuantificar el peligro que estos pueden representar en cuanto inductores de dao gentico
trasmisible por herencia.
6
ESTUDIOS PRECLNICOS
ESTUDIOS DE TERATOGENICIDAD
Estudio de los efectos de las sustancias qumicas en los sistemas
reproductivos y neuroendocrinos del adulto y el embrin, el feto, el neonato
y el mamfero prepuberal.
Proporciona informacin sobre el comportamiento de acoplamiento
fertilidad, progreso del embarazo y posparto.
Hay sustancias que pasan la barrera placentaria que puede influir
directamente en el desarrollo y sobrevivencia del embrin in tero.
7
Problemtica que ha existido en mltiples solicitudes:
Omisin de la informacin.
Informacin incompleta o no concluyente.
No presentan la traduccin de la informacin.
La informacin de farmacodinamia y farmacocintica no es congruente con los
estudios preclnicos.
ESTUDIOS PRECLNICOS
8
Es aceptable:
a. Resumen de estudios farmacodinmicos.
Mecanismos de accin
b. Resumen de estudios farmacocinticos.
Absorcin, distribucin, vida media, concentracin mxima, excrecin.
c. Resumen de Toxicologa
Subaguda.
Aguda o
Crnica de la reproduccin, genotoxicidad, mutagenidad y teratogenicidad.
Deben ser presentados en idioma de origen con traduccin al espaol.
ESTUDIOS PRECLNICOS
9
ESTUDIOS CLNICOS
Cualquier estudio sistemtico que emplea un diseo elaborado
cuidadosamente para efectuarse en sujetos humanos, sean estos
voluntarios sanos o voluntarios enfermos y que respeta los principios
ticos contenidos en la Declaracin de Helsinki.
En general, cualquier estudio que se efecta en seres humanos.
10
ESTUDIOS CLNICOS
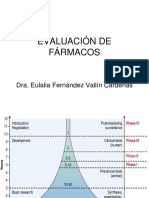
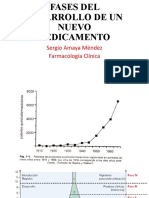
Fases de los ensayos clnicos.
Existen 4 fases de ensayos clnicos.
La Investigacin de Nuevos Frmacos/Medicamentos se puede
evaluar en 2 o ms fases simultneamente en diferentes ensayos
clnicos.
11
ESTUDIOS CLNICOS
Fases de los ensayos clnicos.
Fase I. Son estudios de seguridad iniciales de un nuevo medicamento,
usualmente conducido en voluntarios sanos.
Se pueden evaluar diversos rango de dosis.
Se pueden hacer en pacientes con enfermedad cuando el mecanismo
de accin del medicamento o aspectos ticos as lo requieran (VIH o
cncer).
Estudios de farmacocintica son considerados usualmente de fase I
12
ESTUDIOS CLNICOS
Fase II a
Ensayos clnicos (pilotos) para evaluar eficacia y seguridad en
poblacin seleccionada de pacientes con la enfermedad o condicin a
ser tratada, diagnosticada o prevenida.
Los objetivos pueden ser:
Dosis-respuesta, tipo de paciente, frecuencia de dosis, o preguntas
de seguridad y eficacia
13
ESTUDIOS CLNICOS
Fase II b
Ensayos bien controlados para evaluar eficacia y seguridad en
pacientes que sufren de la condicin o enfermedad.
Son los estudio clnico que usualmente representan la demostracin
ms rigurosa de la eficacia de un frmaco. Son los llamados estudios
pivote
14
ESTUDIOS CLNICOS
Fase III a.
Ensayos que se realizan despus de que se demostr la eficacia del
frmaco, pero antes del sometimiento regulatorio de autorizacin
sanitaria.
Estudios en pacientes a donde va dirigido el frmaco.
+ datos de eficacia y seguridad + nmero de pacientes.
Estudios controlados y no controlados, grupos de pacientes con
condiciones especiales (p. ej. Insuficiencia renal).
Proveen informacin muy importante para la IPP y etiquetado en
general
15
ESTUDIOS CLNICOS
Fase III b.
Estudios clnicos que se realizan despus del sometimiento regulatorio
y dossiers relacionados, pero antes de que sea aprobado y lanzado.
Estudios de calidad de vida.
16
ESTUDIOS CLNICOS
Fase IV
Ensayos conducidos posterior al lanzamiento del frmaco
Provee datos adicionales de eficacia y seguridad
Diferentes formulaciones, dosis, duracin de Tx, interacciones con
otros, y comparaciones.
Grupos poblacionales (edad, raza, gnero)
Crtico para recoger datos de seguridad
17
ESTUDIOS CLNICOS
18
Problemtica que ha existido en mltiples solicitudes:
Informacin incompleta.
No presentan la traduccin de la informacin.
Presentan estudios clnicos sin concluir.
ESTUDIOS CLNICOS
19
Es aceptable:
a. Resumen del estudio clnico Fase I.
b. Resumen del estudio clnico Fase II.
c. Resumen del estudio clnico Fase III.
d. Reporte periodico de seguridad (Fase IV) cuando aplique.
Cuando se comercializa en otro pas.
e. Resumen de estudios riesgo-beneficio para combinaciones.
Resumen de genotoxicidad, teratogenicidad y mutagenicidad
Deben ser presentados en idioma de origen con traduccin al espaol..
ESTUDIOS CLNICOS
Roco Ramrez Herrera
Norma E. Soto Ruz
ramirezh@cofepris.gob.mx
: 52 (55) 5080 5200
También podría gustarte
- Ciclo Hirn..Documento8 páginasCiclo Hirn..Axel GuerreroAún no hay calificaciones
- Nuevos usos para viejos medicamentosDe EverandNuevos usos para viejos medicamentosAún no hay calificaciones
- 1.bases Científicas para El Desarrollo y La Utilización de Los Medicamentos - Ensayos ClínicosDocumento31 páginas1.bases Científicas para El Desarrollo y La Utilización de Los Medicamentos - Ensayos ClínicosFrank Gonzalez0% (2)
- Etapas de Ensayos ClínicosDocumento5 páginasEtapas de Ensayos ClínicosjorgeosmarrAún no hay calificaciones
- Clase 15 UnidDocumento36 páginasClase 15 UnidMaria Claudia Soto PrudencioAún no hay calificaciones
- Evaluación Clínica de Farmacos NuevosDocumento34 páginasEvaluación Clínica de Farmacos NuevosVõ Nguyên GiápAún no hay calificaciones
- Discernimiento FarmacologicoDocumento49 páginasDiscernimiento FarmacologicoJesus RamirezAún no hay calificaciones
- 5 Investigacion ClinicaDocumento68 páginas5 Investigacion ClinicaCarolina Suarez DiazAún no hay calificaciones
- Clase 9 FarmacoDocumento60 páginasClase 9 Farmacosoledad romeroAún no hay calificaciones
- Investigación y Desarrollo de Nuestro FármacosDocumento7 páginasInvestigación y Desarrollo de Nuestro FármacosPier Michell Lopez RuizAún no hay calificaciones
- BIOFARMACIA-semana 1Documento28 páginasBIOFARMACIA-semana 1Deivi Huaman BurgosAún no hay calificaciones
- Unidad 2. - Desarrollo de Nuevos FarmacosDocumento30 páginasUnidad 2. - Desarrollo de Nuevos FarmacosRIgoberto Paez50% (2)
- TEMA 4 Vias Administ e Investigación ClínicaDocumento26 páginasTEMA 4 Vias Administ e Investigación ClínicaJoel Donato Barrientos ValdezAún no hay calificaciones
- Biofarmacia y La Evaluacion de MedicamentosDocumento52 páginasBiofarmacia y La Evaluacion de MedicamentosMoniGuzmánAún no hay calificaciones
- Desarrollo de Un FarmacóDocumento15 páginasDesarrollo de Un FarmacóMF MFAún no hay calificaciones
- Cuestionario de FarmacologíaDocumento6 páginasCuestionario de FarmacologíaFlores Mendez GregorioAún no hay calificaciones
- Estudios Preclínicos y ClínicossDocumento6 páginasEstudios Preclínicos y ClínicossAgustina MaurerAún no hay calificaciones
- TOXICOLOGIADocumento34 páginasTOXICOLOGIAEUGENIO VEGAAún no hay calificaciones
- Abp 5Documento9 páginasAbp 5a.moralesAún no hay calificaciones
- Ensayo Clínico 2018Documento17 páginasEnsayo Clínico 2018VanessaMendozaAún no hay calificaciones
- Unidad 5 Posgrado RegulatoriosDocumento62 páginasUnidad 5 Posgrado RegulatoriosMir AvAún no hay calificaciones
- Ética de La Investigación ClínicaDocumento12 páginasÉtica de La Investigación ClínicaCaro SierraAún no hay calificaciones
- Farmacología Clínica. Desarrollo de Nuevos MedicamentosDocumento7 páginasFarmacología Clínica. Desarrollo de Nuevos Medicamentosismarcos666Aún no hay calificaciones
- PRODUCCION O FABRICACION DE UN MEDICAMENTO. SiDocumento8 páginasPRODUCCION O FABRICACION DE UN MEDICAMENTO. SiJONATHAN GONZALEZ ROBAYOAún no hay calificaciones
- BiofarmaciaDocumento9 páginasBiofarmaciaMaria claret Ayma quijadaAún no hay calificaciones
- FarmacovigilanciaDocumento17 páginasFarmacovigilanciarosana keAún no hay calificaciones
- Clase Iv - Investigacion FarmacosDocumento43 páginasClase Iv - Investigacion FarmacosNicole Alexandra Garavito Nu�ezAún no hay calificaciones
- Cuestionario 9 METODOLOGIA DE LAS CIENCIASDocumento6 páginasCuestionario 9 METODOLOGIA DE LAS CIENCIAStaniaabarca94Aún no hay calificaciones
- Anexos Fases de La Investigación Cientifica para Aprobar La Vacuna RusaDocumento38 páginasAnexos Fases de La Investigación Cientifica para Aprobar La Vacuna RusaKristian floresAún no hay calificaciones
- Farmacologia Investigacion (I+d)Documento9 páginasFarmacologia Investigacion (I+d)frankoom orlando MendozaAún no hay calificaciones
- Proceso Aprobacion FarmacoDocumento9 páginasProceso Aprobacion FarmacoRocio DelgadoAún no hay calificaciones
- Curso Enfermeria InvestigacionDocumento25 páginasCurso Enfermeria InvestigacionFortunato BonillaAún no hay calificaciones
- Investigación Aprobacion FarmacoDocumento12 páginasInvestigación Aprobacion FarmacoLuis DominguezAún no hay calificaciones
- Farmaco, Como Se Hace U Nuevo MedDocumento5 páginasFarmaco, Como Se Hace U Nuevo MedClaudia CansecoAún no hay calificaciones
- Fases Investigacion Nuevos Farmacos PDFDocumento25 páginasFases Investigacion Nuevos Farmacos PDFYsabelAdelaTaypeValenciaAún no hay calificaciones
- Etapas en El Desarrollo de FarmacoDocumento2 páginasEtapas en El Desarrollo de FarmacoMariajosé RebolledoAún no hay calificaciones
- 1726 8958 RMCMLP 28 01 59Documento5 páginas1726 8958 RMCMLP 28 01 59Angelica SuarezAún no hay calificaciones
- Cuestionario 2 BelenDocumento3 páginasCuestionario 2 BelenBelen AlarconAún no hay calificaciones
- Proceso de InvestigaciónDocumento7 páginasProceso de InvestigaciónFer HernandezAún no hay calificaciones
- Investigación ClínicaDocumento4 páginasInvestigación ClínicaAbril MarcoliniAún no hay calificaciones
- Fases Del Desarrollo de Un MedicamentoDocumento37 páginasFases Del Desarrollo de Un MedicamentoMariajose Ceballos SalazarAún no hay calificaciones
- TEMA 2 Completo + LibroDocumento8 páginasTEMA 2 Completo + Libroal436796Aún no hay calificaciones
- 6 7Documento5 páginas6 7Alejandra Urrutia100% (1)
- Garcia Patiño Jesus 1652 Etapas de Investigación de Un Nuevo Fármaco Hasta Su Distribución en El MercadoDocumento4 páginasGarcia Patiño Jesus 1652 Etapas de Investigación de Un Nuevo Fármaco Hasta Su Distribución en El MercadoJesus Garcia PatiñoAún no hay calificaciones
- BIOÉTICADocumento8 páginasBIOÉTICAJosé Alexander Silva CruzAún no hay calificaciones
- Principios Bioeticos en Terapia Genica en MéxicoDocumento15 páginasPrincipios Bioeticos en Terapia Genica en Méxicomiguel angelAún no hay calificaciones
- Evaluacion de AO1 de Farmacologia I FRANNYS INFANTEDocumento11 páginasEvaluacion de AO1 de Farmacologia I FRANNYS INFANTEeguevara66677Aún no hay calificaciones
- 2 Fases Del Desarrollo de Nuevos FármacosDocumento22 páginas2 Fases Del Desarrollo de Nuevos FármacosdiegoAún no hay calificaciones
- Carátula Trabajo PrácticoDocumento6 páginasCarátula Trabajo PrácticoBrenda RíosAún no hay calificaciones
- Proceso Aprobacion Farmaco PDFDocumento9 páginasProceso Aprobacion Farmaco PDFIvt RomeroAún no hay calificaciones
- Guia de Estudio I Parcial, I Periodo Del 2019Documento18 páginasGuia de Estudio I Parcial, I Periodo Del 2019Cortes AshlyAún no hay calificaciones
- Prácticas Bloque 1 PDFDocumento186 páginasPrácticas Bloque 1 PDFFernandaLizbethPerezAún no hay calificaciones
- Fases de La Investigación ClínicaDocumento20 páginasFases de La Investigación ClínicaisaacAún no hay calificaciones
- Evaluacion de AO1 de Farmacologia I DENY REYESDocumento10 páginasEvaluacion de AO1 de Farmacologia I DENY REYESeguevara66677Aún no hay calificaciones
- Farmacología ClínicaDocumento15 páginasFarmacología ClínicaWilianny RomeroAún no hay calificaciones
- Desarrollo de Los Farmacos PDFDocumento4 páginasDesarrollo de Los Farmacos PDFAna Lilia Martínez MartínezAún no hay calificaciones
- Conceptes Assajos ClínicsDocumento17 páginasConceptes Assajos ClínicsAlma CarracedoAún no hay calificaciones
- Desarrollo de Un FármacoDocumento5 páginasDesarrollo de Un FármacoPatricia PerezAún no hay calificaciones
- Principales procedimientos quirúrgicos CMG 6De EverandPrincipales procedimientos quirúrgicos CMG 6Aún no hay calificaciones
- Ciencia regulatoria: Medicamentos bio y su relevancia para la saludDe EverandCiencia regulatoria: Medicamentos bio y su relevancia para la saludAún no hay calificaciones
- La historia clínica para médicoblastos: Material de apoyo. Tomo IIDe EverandLa historia clínica para médicoblastos: Material de apoyo. Tomo IIAún no hay calificaciones
- Curso de Operacion PTAR CUCEI.Documento54 páginasCurso de Operacion PTAR CUCEI.JoseCastilloAún no hay calificaciones
- Influencia Del Solvente en El Espectro Uv PDFDocumento45 páginasInfluencia Del Solvente en El Espectro Uv PDFJoseCastilloAún no hay calificaciones
- Iso9001 2008 PDFDocumento41 páginasIso9001 2008 PDFBrian ChavezAún no hay calificaciones
- Nom - 177 - Ssa1 - 2013Documento64 páginasNom - 177 - Ssa1 - 2013JoseCastilloAún no hay calificaciones
- Liberar Lumia 710Documento15 páginasLiberar Lumia 710JoseCastilloAún no hay calificaciones
- Liberar Lumia 710Documento15 páginasLiberar Lumia 710JoseCastilloAún no hay calificaciones
- Decoracion Mural - ListaDocumento74 páginasDecoracion Mural - ListaArelyACAún no hay calificaciones
- PlandenegociosDocumento130 páginasPlandenegociosaraceli venturaAún no hay calificaciones
- Informe Practica de Laboratorio N1Documento3 páginasInforme Practica de Laboratorio N1OscarDucuara100% (1)
- BCPaniDocumento192 páginasBCPanimauro guerraAún no hay calificaciones
- Ricce Torres - Robles CoronelDocumento93 páginasRicce Torres - Robles CoronelRONALD ALEXIS SILUPU BEDRIÑANAAún no hay calificaciones
- El Estúpido y Pornográfico Fracaso de Las Gatitas SiniestrasDocumento146 páginasEl Estúpido y Pornográfico Fracaso de Las Gatitas SiniestrasG A Robles CastroAún no hay calificaciones
- Informe Del Molino de Moscopan y Molino de CaldasDocumento3 páginasInforme Del Molino de Moscopan y Molino de CaldasJuliana fernandezAún no hay calificaciones
- Analisis WifiDocumento110 páginasAnalisis WifiMarco Antonio Pérez TorresAún no hay calificaciones
- Hora Santa 12-01-2023Documento2 páginasHora Santa 12-01-2023Isc Jose Carlos Hernandez SantiagoAún no hay calificaciones
- Laboratorio - Guia 1 - ExtracciónDocumento3 páginasLaboratorio - Guia 1 - ExtracciónAnto La TorreAún no hay calificaciones
- SULFAS y Anticepticos UrinariosDocumento40 páginasSULFAS y Anticepticos UrinariosAnonymous 5RhHmNmgJAún no hay calificaciones
- Trabajo Institucional Yesenia OrtizDocumento9 páginasTrabajo Institucional Yesenia OrtizYesenia Ortiz rojasAún no hay calificaciones
- Calculo de Fundaciones para Postes Normales Supercemento Rev1Documento11 páginasCalculo de Fundaciones para Postes Normales Supercemento Rev1Andrés AndretichAún no hay calificaciones
- MEZCLASDocumento11 páginasMEZCLASRoberto SantiagoAún no hay calificaciones
- CBA-PT-01 Topografia y GeoreferenciacionDocumento5 páginasCBA-PT-01 Topografia y Georeferenciacionangelo bszAún no hay calificaciones
- Caballería en Campaña de AntofagastaDocumento32 páginasCaballería en Campaña de AntofagastaPaginas Heroicas de la Guerra del PacificoAún no hay calificaciones
- EstadisticaDocumento18 páginasEstadisticaRoselin HernandezAún no hay calificaciones
- Catalogo Scotia Julio 2018Documento32 páginasCatalogo Scotia Julio 2018Julio CesarAún no hay calificaciones
- Unity TempleDocumento6 páginasUnity TemplesergioAún no hay calificaciones
- La Agricultura Orgánica SustentableDocumento5 páginasLa Agricultura Orgánica SustentableKaryagus D GarciaAún no hay calificaciones
- I-2020 Taller Sistema GaseosoDocumento2 páginasI-2020 Taller Sistema GaseosoGeraldinecarAún no hay calificaciones
- El Crimen Fue en Granada (Comentario Hautatzen)Documento3 páginasEl Crimen Fue en Granada (Comentario Hautatzen)aa aaAún no hay calificaciones
- Psicoendocrinología y Sistema EndócrinoDocumento1 páginaPsicoendocrinología y Sistema EndócrinoEuniké NietoAún no hay calificaciones
- Caso 2 Trabajo AuditoriaDocumento10 páginasCaso 2 Trabajo AuditoriaDiana Estefany Gonzáles FloresAún no hay calificaciones
- Astymin 2Documento9 páginasAstymin 2La Verdad TierraAún no hay calificaciones
- Desarrollo de Nuevos Productos Unidad IDocumento52 páginasDesarrollo de Nuevos Productos Unidad IRamiro100% (1)
- Norma Iso 9249Documento6 páginasNorma Iso 9249diegoAún no hay calificaciones
- Caracst. CerámicasDocumento12 páginasCaracst. CerámicasmoliloliAún no hay calificaciones
- Acta de Entrega de Vivienda KarelysDocumento92 páginasActa de Entrega de Vivienda KarelysAnaMilenaNobleAún no hay calificaciones