Documentos de Académico
Documentos de Profesional
Documentos de Cultura
7 Termot Exergia 2010 11
7 Termot Exergia 2010 11
Cargado por
corvettexpTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
7 Termot Exergia 2010 11
7 Termot Exergia 2010 11
Cargado por
corvettexpCopyright:
Formatos disponibles
7_ANLISIS DE LA 2 LEY: EXERGA
7.1 NOCIN DE EXERGA
7.2 EXERGA: SISTEMAS CERRADOS
Trabajo til e Irreversibilidad
7.3 EXERGA: SISTEMAS ABIERTOS
Exerga de flujo
7.4 EFICIENCIA EXERGTICA
Transferencia de exerga
7.1 NOCIN DE EXERGA
El sistema interacciona con el entorno (alrededores + ambiente). La interaccin del
sistema-alrededores cambia las propiedades de ambos. La interaccin con el
ambiente, normalmente un bao, no modifica las propiedades de este (naturalmente
pueden cambiar las propiedades extensivas del ambiente).
Por lo tanto el ambiente se caracteriza por sus las propiedades intensivas T
0
, p
0
, h
0
, s
0
,
invariables. Adems se supone el ambiente sin cambios de energa cintica y con
energa potencial cero.
El objetivo del problema es disear el sistema para obtener el mximo trabajo real de
esas interacciones. El mximo trabajo terico est determinado por la segunda ley de
la termodinmica que exige que las interacciones sigan un proceso REVERSIBLE.
Las irreversibilidades slo se pueden producir en el sistema y alrededores.
Ambiente
Sistema
cerrado
Alrededores
0 , 0 ,..., ,
0 0
= = vel z T p
,... , , , , , vel z S V T p
Entorno
W
Definiciones de alrededores y ambiente.
Ambiente
Sistema
cerrado
Alrededores
0 , 0 ,..., ,
0 0
= = vel z T p
,... , , , , , vel z S V T p
Entorno
W
W
CENTRAL
ELECTRICA
Aire
Combustible
0 =
T T
Q W
T T T T
W W Q E = =
amb amb amb
V p S T U =
0 0
) (
0
E E E E E E
amb amb T
+ = + =
) (
0
V V V V
amb
= =
T g T g T T
S S T dQ S
, ,
/ = + =
) (
0
S S S S S S
amb amb T
+ = + =
T g T
S T S S T V V p U E W
, 0 0 0 0 0 0
) ( ) ( ) ( + =
mximo T
W
,
=
= EXERGA
Irre
0
0 , 0 ,..., ,
0 0
= = vel z T p
0 , 0
,... , , , ,
0 0 0 0 0
= = vel z
U S V T p
+
MXIMO TRABAJO EXERGA _ = =
Estado muerto
del sistema
NO NEGATIVO
NO SE CONSERVA
SISTEMA CERRADO
AMBIENTE DADO
Ambiente
Sistema
cerrado
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
,... , , , ,
vel z
E S V T p
Definicin de exerga (o disponibilidad).
) ( ) ( ) (
0 1 0 0 1 0 0 1 1
S S T V V p U E + =
) ( ) ( ) (
0 2 0 0 2 0 0 2 2
S S T V V p U E + =
) ( ) ( ) (
1 2 0 1 2 0 1 2
S S T V V p E E + =
2 _ _ 1 _ _ _ a de yendo REV
W =
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
, , , ,
1 1
1 1 1 1
vel z
S V T p
0 , 0
,... , , ,
0 0 0 0
= = vel z
S V T p
+
2 _ _ 1 _ _ _
_ _ _
a de yendo
obtenerse podra que mximo
W =
1
2 _ 1 _ max_ 2 1 a de
W = =
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
, , , ,
2 2
2 2 2 2
vel z
S V T p
0 , 0 ,..., ,
0 0
= = vel z T p
Molino: 12m envergadura (radio=6m)
Viento: 10m/s
kg kJ
s m vel
/ 05 . 0
2
/ 100
2
2 2 2
1
= = =
Densidad aire: 1.18Kg/m
3
Ambiente: T
0
=298K, p
0
=101kPa
s Kg s m m m kg Av m / 1334 / 10 6 / 18 . 1
2 2 3
= = =
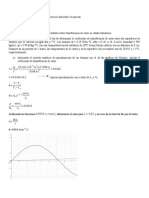
kW m Potencia 7 . 66 max _ = =
Ejemplo 31
Potencia mxima del molino?
1 max
max max _
= = = m w m W Potencia
) ( ) ( ) (
0 1 0 0 1 0 0 1 1
s s T v v p u e + = ) ( ) ( ) (
0 1 0 0 1 0 0
1
1 1
s s T v v p u e e u
p c
+ + + =
1 c
e =
Sistema: estado inicial viento vel=10m/s estado muerto vel=0 m/s
mxima potencia mxima trabajo proceso reversible
0 0
,T p
0
,... ,
1
0 0
vel
T p aire
0 0
,T p
0
,... ,
0 0
= vel
T p aire
Ejemplo 32
s kJ Q genera que K T con HORNO
horno
/ 3165 _ _ 1111 _ _ = =
K T 298
0
=
732 . 0 / 1 / 1
0
= =
horno H L
T T T T
kW W 2317 =
K T
polo
270 = Estado muerto diferente
Q
H
Q
L
W
H L rev
H L
H
T T
Q Q
Q
W
/ 1 ...
/ 1
= =
= =
Exerga por unidad de tiempo del calor en el horno?
H H L
REV Q T T W W
= = ) / 1 ( max
usando una mquina trmica reversible entre la T del horno y T ambiental
kW 2317 =
kW 2396 =
Exerga = mximo trabajo obtenible del calor
Aqu el horno no llega al equilibrio con el
ambiente ya que la temperatura del
horno se mantiene fija. Observe que no
se pide la exerga del horno sino la del
calor producido.
0 0
,T p
Q
0 0
,T p
Ejemplo 33
2450cm
3
7 bar
867C
aire
p
0
=1.013bar
T
0
=27C
Exerga especfica de los
gases de combustin?
) ( ) ( ) (
0 1 0 0 1 0 0 1 1
s s T v v p u e + =
1 1
u e =
Tablas
Aire como gas ideal, se
desprecian los cambios de
las energas cintica y
potencial
1
0
ln
p
p
R s s
o
=
Tablas
0 0 0
RT v p =
1 1 1
/ p RT v =
kg kJ / 91 . 368 =
Esta exerga no hace nada de trabajo: W
T
=0
0 ) ( ) ( ) (
, 0 , 0 0 0 0 0 0
= = + =
T g T g T
s T s T s s T v v p u e w kg kJ S T
T g
/ 91 . 368
, 0
=
Motores turboalimentados
Ejemplo 34
Cambio de exerga especfica?
Agua
Proceso lento: reversible internamente entropa generada=0
vapor
saturado
Q
W
lquido
saturado
a 100C
p
v
1 2
p
0
=1.014bar
T
0
=20C
) ( ) ( ) (
1 2 0 1 2 0 1 2
s s T v v p u u + =
Tablas .... , ,
2 1 2 g f g
v v u u u u = = =
kg kJ / 484 =
kg kJ antes que igual / 484 ... _ _ ... = =
W
Agitacin
Ahora:
1 2
... _ _ ... s s antes que igual s = =
Mismos estados
inicial y final
Proceso no lento: irreversible entropa generada 0
Se obtendr menor trabajo que el caso anterior.
7.2 EXERGA: SISTEMAS CERRADOS
0
0
=
g
S T I Irrev
W Q Q E E + =
0 1 2 g
S T Q T Q S S + + = / /
0 0 1 2
0 , 0 ,..., ,
0 0
= = vel z T p
0 , 0
,... , , , ,
0 0 0 0 0
= = vel z
S E V T p
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
,... , , , ,
2 2
2 2 2 2 2
vel z
S E V T p
T
SISTEMA CERRADO CON UN BAO:
0 2 1
) ( Q Q E E W + + =
g
S T T QT S S T Q
0 0 1 2 0 0
/ ) ( =
g
S T Q
T
T
S S T E E
0
0
2 2 0 2 1
) 1 ( ) ( ) ( + =
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
,... , , , ,
1 1
1 1 1 1 1
vel z
S E V T p
T
g til
S T Q
T
T
S S T V V p E E W
0
0
2 2 0 2 1 0 2 1
) 1 ( ) ( ) ( ) ( + + =
g til real
S T Q
T
T
W
0
0
,
) 1 ( + =
Q
T
T
W
til rev
) 1 (
0
,
+ =
W
0
Q
Q
Aqu slo estn las
irreversibilidades del sistema.
Las nicas que existen en el
presente caso.
Ambiente y alrededores son baos
) (
1 2 0
V V p W W
til
=
+
Definicin de trabajo til:
0
0
=
g
S T I Irrev
W Q Q E E + =
0 1 2 g
S T dQ T Q S S + + =
/ /
0 0 1 2
0 , 0 ,..., ,
0 0
= = vel z T p
0 , 0
,... , , , ,
0 0 0 0 0
= = vel z
S E V T p
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
,... , , , ,
2 2
2 2 2 2 2
vel z
S E V T p
final
T
SISTEMA CERRADO INTERACTUANDO CON UN SISTEMA QUE NO ES UN BAO:
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
,... , , , ,
1 1
1 1 1 1 1
vel z
S E V T p
g til real
S T dQ
T
T
W
0
0
,
) 1 ( + =
+ = dQ
T
T
W
til rev
) 1 (
0
,
W
0
Q
Q
Aqu slo estn las
irreversibilidades
del sistema
Alrededores: no es un bao
OJO: en este caso no son las nicas
irreversibilidades. En los alrededores
tambin puede haber irreversibilidades y
por tanto se generacin de entropa.
inicial
T
+
g
k
k
k
til real
S T Q
T
T
W
0
0
,
) 1 ( + =
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
, , ,
1 1
1 1 1
vel z
V T p
W
0
Q
} {
k
Q
} {
k
T
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
, , , ,
2 2
2 2 2 2
vel z
S V T p
} {
k
T
0 , 0 ,..., ,
0 0
= = vel z T p
0 , 0
,... , , ,
0 0 0 0
= = vel z
S V T p
+ =
k
k
k
til rev
Q
T
T
W ) 1 (
0
,
g
k
k
k
til real
S T dQ
T
T
W
0
0
,
) 1 ( + =
+ =
k
k
k
til rev
dQ
T
T
W ) 1 (
0
,
g til real
S T Q
T
T
W
0
0
,
) 1 ( + =
Q
T
T
W
til rev
) 1 (
0
,
+ =
Ahora
+
SISTEMA CERRADO CON VARIOS BAOS:
SISTEMA CERRADO INTERACTUANDO CON VARIOS SISTEMAS QUE NO SON BAOS:
g til real
S T dQ
T
T
W
0
0
,
) 1 ( + =
+ = dQ
T
T
W
til rev
) 1 (
0
,
Ahora
EN TODOS LOS CASOS S
g
ES LA IRREVERSIBILIDAD GENERADA SOLAMENTE EN EL SISTEMA
) ( ) ( ) (
1 2 0 1 2 0 1 2
S S T V V p E E + =
k REV
k
T
T
,
0
1 =
[ ]
g
k
k
k
S T V V p W dQ
T
T
0 1 2 0
2
1
0
) ( ) 1 ( =
[ ]
g
k
k
k
S T V V p W Q
T
T
0 1 2 0
0
) ( ) 1 ( =
Transferencia de
exerga debida al
trabajo
Transferencia de
exerga debida al
calor
Prdida de exerga
en la transferencia
debida a la
irreversibilidad
Cuando slo se
intercambia
energa trmica
con el ambiente
(slo k=0) no hay
transferencia de
exerga calrica.
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
, , , ,
1 1
1 1 1 1
vel z
S V T p
,...
k
T
0 , 0 ,..., ,
0 0
= = vel z T p
0 , 0
,... , , ,
0 0 0 0
= = vel z
S V T p
0 , 0 ,..., ,
0 0
= = vel z T p
,... ,
, , , ,
2 2
2 2 2 2
vel z
S V T p
,...
k
T
+
Transferencia de exerga.
) ( ) ( ) (
1 2 0 1 2 0 1 2
S S T V V p E E + =
g til real
S T Q
T
T
W
0
0
,
) 1 ( + =
[ ]
g
k
k
k
S T V V p W Q
T
T
0 1 2 0
0
) ( ) 1 ( =
+ = S T V p E
0 0
g til real S T Q
T
T
W
+ =
0
0
, ) 1 (
g
k
k
k
S T V p W Q
T
T
=
0 0
0
) 1 (
Observaciones:
) (
1 2 0
V V p W W
til
=
g til
S T Q
T
T
W
0
0
) 1 ( + =
En trminos del proceso seguido
En trminos de los estados
inicial y final
g
S T V V p W Q
T
T
0 1 2 0
0
)] ( [ ) 1 ( = ) ( ) ( ) (
1 2 0 1 2 0 1 2
S S T V V p E E + =
De la definicin
) ( ) ( ) (
0 0 0 0 0
S S T V V p U E + =
) ( ) ( ) ( /
0 0 0 0 0
s s T v v p u e m + = =
Exerga especfica
7.3 EXERGA: SISTEMAS ABIERTOS
,... ,
0 0
T p
,... ,
, , , ,
1 1
1 1 1 1
vel z
S V T p
,... ,
0 0
T p
0
,... 0 , 0
, , , ,
0 0 0 0
=
= =
flujos
vel z
S V T p
+
Definicin de exerga de flujo:
) ( ) ( ) ( ) (
0 0 0 0 0 0
p p V S S T V V p U E
A A A A A A
+ + =
Exerga asociada al
trabajo de flujo en A
Exerga
A
que
lleva el flujo en A
) ( ) (
0 0 0
S S T
A A
=
A
A B B
Exerga asociada al flujo: EXERGA DE FLUJO
EXERGA DE FLUJO especfica: [ ] ) ( ) ( /
0 0 0
s s T m = =
) ( ) (
0 0 0
S S T
B B B
=
,... ,
0 0
T p
,... ,
, , , ,
1 1
1 1 1 1
vel z
S V T p
k
T
,... ,
0 0
T p
0
,... 0 , 0
, , , ,
0 0 0 0
=
= =
flujos
vel z
S V T p
+
[ ] ) ( ) ( ) (
0 0 0 0 0
s s T v v p u e m m + = =
SISTEMAS CERRADOS
+
=
salidas
j
j
entradas
i
i g
k
k
k
m m S T V p W Q
T
T
0 0
0
) ) 1 (
SISTEMAS ABIERTOS
,... ,
0 0
T p
,... ,
, , , ,
2 2
2 2 2 2
vel z
S V T p
k
T
[ ] ) ( ) (
0 0 0
s s T m m = =
[ ]
+ + = =
salidas
j j
entradas
i i g
k
k
k
til
m m S T Q
T
T
V p W W
0
0
2 1 0
) 1 ( ) ( )
EXERGA EXERGA DE FLUJO
Trabajo til en sistemas abiertos:
SI EN LOS ALREDEDORES HAY EL SISTEMA CON SISTEMAS QUE NO SON BAOS LOS TRMINOS TRMICOS
CORRESPONDIENTES SON INTEGRALES.
En TODOS LOS CASOS S
g
ES LA IRREVERSIBILIDAD GENERADA SOLAMENTE EN EL SISTEMA
% 50
600
300
1 1 = = =
H
L
rev
T
T
Q
H
Q
L
W
600K
300K
% 30 =
Q
H
Q
L
W
1000K
300K
% 30 =
60 . 0
50
30
= = =
rev
II
% 70
1000
300
1 1 = = =
H
L
rev
T
T
43 . 0
70
30
= = =
rev
II
Necesidad de una definicin de eficiencia asociada a la exerga: un ejemplo.
7.4 EFICIENCIA EXERGTICA
rev
II
exergtica eficiencia
= _
I
=
Otro ejemplo,
(W=0 & estado
estacionario).
Q
H
Q
til
til
T
H
T
a
T
Q
a
0 = = W Q Q Q U
a u H a u H
Q Q Q + =
Aqu las Q en
valor absoluto
H
u
I
Q
Q
=
0 ) 1 (
0 0
0
=
g
k
k
k
S T V p W Q
T
T
Punto de vista
de la 1 LEY:
Punto de vista
de la 2 LEY:
g
a
a
u
u
H
H
S T Q
T
T
Q
T
T
Q
T
T
=
0
0 0 0
) 1 ( ) 1 ( ) 1 (
g
a
a
u
u
H
H
S T Q
T
T
Q
T
T
Q
T
T
+ + =
0
0 0 0
) 1 ( ) 1 ( ) 1 (
Exerga
entrante
Exerga
perdida
Exerga
utilizada
(hasta este
punto)
Otro ejemplo,
(W=0 & estado
estacionario).
Q
H
Q
til
til
T
H
T
a
T
Q
a Aqu las Q en
valor absoluto
H
u
I
Q
Q
=
g
a
a
u
u
H
H
S T Q
T
T
Q
T
T
Q
T
T
+ + =
0
0 0 0
) 1 ( ) 1 ( ) 1 (
Exerga
entrante
Exerga
perdida
Exerga
utilizada
(hasta este
punto)
H H
u u
II
Q T T
Q T T
=
) 1 (
) 1 (
0
0
) 1 (
) 1 (
0
0
H
u
I II
T T
T T
=
1 1 _ < =
II I
si Incluso
II
til
T
0
1
Calefaccin
Generador de vapor
Horno industrial
Mquinas trmicas:
rev
II
ex eficiencia
= . _
Dispositivos que producen trabajo:
rev
real
II
W
W
ex eficiencia = _
Dispositivos que consumen trabajo:
real
rev
II
W
W
ex eficiencia = _
real
H
real BC
rev
H
rev BC
W
Q
COP
W
Q
COP = =
, ,
,
rev BC
real BC
COP
COP
,
,
=
= =
I I
disponible Exerga
obtenida Exerga
exergtica eficiencia
II
1
_
_
_
(Tambin se llama eficacia)
T g T
S T S S T V V p U E W
, 0 0 0 0 0 0
) ( ) ( ) ( + =
I =
Ejemplo 35
s kJ Q K T
H
/ 500 1200 = =
s kJ W K T / 180 300
0
= =
75 . 0 / 1
0
= =
H rev
T T
kW Q rev W
rev
375 ) ( = =
kW real W rev W S T I
g
195 ) ( ) (
0
= = =
Q
H
Q
L
W
? ? ?
til rev
W I W
= = W til W V ) ( 0
= Q
T
T
W
H
rev ) 1 (
0
kW 375 =
kW 375 =
dado ambiente el para
le irremadiab perdida kW
_ _ _
_ _ 125
k
W
Q
5
0
0
=
kW I 195 =
kW W 180 =
Anlisis exergtico de una mquina trmica
Visto desde el fluido de la mquina
g H
H
L
L
f til
S T Q
T
T
Q
T
T
V p W W
0
0 0
0
) 1 ( ) 1 ( + + = =
kW real W rev W I 195 ) ( ) ( = =
kW
H
Q de 375 _ =
Visto desde Q
H
Ejemplo 36
=
=
0 ,
,
) 1 ( ) (
0
T T
T
Fe
Fe
final Fe
inicial Fe
mcdT
T
T
rev W
kJ
T
T
Ln mcT T T mc rev W
ini Fe
ini Fe
8191 ) ( ) (
0
,
0 0 ,
= =
kJ T T mc Q
ini Fe ambiente al
38925 ) (
0 , _
= =
kg m 500 =
K T 300
0
=
Fe
dQ
H
dQ
L
dW
Fe
Fe
rev
T
T
dQ
rev dW
0
1
) (
=
=
=
=
0 ,
,
) 1 ( ) (
0
T T
T
Fe
Fe
final Fe
inicial Fe
dQ
T
T
rev W
kgK kJ c / 45 . 0 =
kJ 8191 =
dado ambiente el para
lemente irremadiab
perdidos kJ
_ _ _
_ _ 30734
kJ I 8191 =
k
J
Q
a
m
b
i
e
n
t
a
l
3
8
9
2
5
_
=
Anlisis exergtico de una masa de hierro que se deja enfriar
K T
inicial Fe
473
,
=
Exerga inicial del hierro: mximo trabajo obtenible con una mquina trmica
Fe Fe
kJ W
REV Fe
8191 = =
0 =
real
W
kJ I W W
real rev
8191 = =
kJ S T dQ
T
T
Q
T
T
W
g H
H
L
L
f rev
8191 ) 1 ( ) 1 (
0
0 0
= + + =
Visto desde el fluido de la mquina
Fe
dQ
H
dQ
L
dW
Fe
Fe
dQ
T
T
rev dW ) 1 ( ) (
0
=
Ejemplo 37
kJ T T mc Q
casa ini Fe te directamen casa la a
925 . 38 ) (
, _ _ _
= =
kgK kJ c / 45 . 0 =
0 I
dW
Fe
dQ
H
dQ
L
casa
kJ rev W 191 . 8 ) ( =
kJ kJ kJ Q
Fe
casa la a
734 . 30 191 . 8 925 . 38
_ _
= =
6 ' 13
300 / 278 1
1
/ 1
1
) ( =
=
H L
BC
T T
rev COP
dW
dQ
COP
BC
H
BC
=
kJ rev W Q Q
BC
casa la a
BC
H
398 . 111 ) ( 6 . 13
_ _
= = =
kJ Q
Total
casa la a
132 . 142 ...
_ _
= =
K T T
calle
278
0
= =
K T
casa
300 =
Kg m 500 =
calle
BC
H
dQ
BC
L
dQ
K T
inicial Fe
473
,
=
?
_ _ _ casa la a mximo
Q
casa la a mximo te directamen casa la a
Q Q
_ _ _ _ _ _
<
(Ojo, ahora T
0
es diferente al ej. Anterior)
H L
H
BC
Q Q W
Q
Energtico Coste
Deseada Energa
COP
/ 1
1
_
_
= = =
7 . 26
294 / 283 1
1
/ 1
1
,
=
=
H L
rev BC
T T
COP
K T
calle
283 =
K T
casa
294 =
1 =
BC
COP
W
W
eficiencia
rev
II
= % 7 . 3 037 . 0
7 . 26
1
,
,
= = = =
rev BC
real BC
COP
COP
Ejemplo 38
real BC H
rev BC H
COP Q
COP Q
,
,
/
/
=
Eficiencia exergtica de una bomba de calor
Ejemplo 39
MPa p 1
1
=
kPa p 200
2
=
C T 300
1
=
C T 150
2
=
agua de vapor _ _ Kg m 05 . 0 =
kJ Q 2 =
?
II
? I
C T 25
0
= kPa p 100
0
=
kJ S S T V V p U U 0 . 35 ) ( ) ( ) (
0 1 0 0 1 0 0 1 1
= + =
s v u , ,
de los estados inicial y final: tablas
de vapor sobrecalentado
0 0 0
, , s v u
del estado muerto: tabla de agua
lquida o valores de saturacin a la misma
temperatura.
kJ 4 . 25 ....
2
= =
kJ kJ W
til rev
6 . 9 ) 4 . 25 0 . 35 (
2 1 .
= = = =
kJ U Q W
real
8 . 8 = =
kJ V p W W
real real til
3 . 5
0 ,
= = kJ kJ W W I
real til til rev
3 . 4 ) 3 . 5 6 . 9 (
, ,
= = =
Tambin: kJ
T
Q
S T S T I
gen
3 . 4 ) (
0
0 0
= = =
rev
real til
II
W
W
eficiencia
,
= % 2 . 55 552 . 0
6 . 9
3 . 5
= = =
kJ
kJ
) 33 ( ) ( C c T c c
V V V
= Aire=gas ideal (Tablas)
) (
0
0 0
T
Q
S T S T I
gen
= =
= S
kJ I 679 . 20 =
Proceso reversible entre los
mismos estados inicial y final
V p U S T W
rev
= =
0 0
U U Q W
real
= =
? ?_ ?_
, , real til rev til
W W I
kJ T mc S T
v
055 . 1
0
= =
kJ T mc
v
734 . 21 = =
S T =
0
1
2
2
1
T
T
Ln mc
T
dT mc
v
v
= =
2
1
T
dQ
Ejemplo 40
kPa p 138
1
=
C T 21
1
=
W
C T 21
0
= C T 21
0
=
aire
C T 54
2
=
Kg m 91 . 0 =
Q
H
Q
L
W
C T 54
2
=
C T 21
1
=
kJ T mc U Q
v H
7 . 21 = = =
Calor necesario para subir a T=54C:
H H L
H
BC
T T dQ dQ dW
dQ
COP
/ 1
1
/ 1
1
0
= =
H H rev
dQ T T dW ) / 1 (
0
=
=
=
=
=
= =
2
1
2
1
) / 1 ( ) / 1 (
0 0
T T
T T
H V H
T T
T T
H H rev
H
H
H
H
dT mc T T dQ T T W
kJ kJ kJ
T
T
Ln T mc T T mc W
V V rev
05 . 1 68 . 20 70 . 21 ) (
1
2
0 1 2
= = =
W til W V = = ) ( 0
Tambin usando:
I W W
real rev
=
kJ I 679 . 20 =
kJ W
rev
05 . 1 =
kJ W
real
734 . 21 =
Ejemplo 40
kPa p 138
1
=
C T 21
1
=
W
C T 21
0
= C T 21
0
=
aire
C T 54
2
=
Kg m 91 . 0 =
Q
H
Q
L
W
C T 54
2
=
C T 21
1
=
kJ W
rev
05 . 1 =
Kg m
Fe
5 =
K T
inicial Fe
623
,
=
U W Q =
Agua: lquido incompresible
Capacidades del agua y hierro obtenidas de las tablas
0 = + =
Fe Fe Fe agua agua agua
T m c T m c
Kg m
agua
100 =
K T T
final agua
303 =
K T T
final Fe
623 =
K T
final
7 . 304 =
kJ V p U S T
agua agua agua agua
8 . 69
1 0 1 1 0 1
= =
kJ V p U S T
Fe Fe Fe Fe
2 . 245
1 0 1 1 0 1
= =
) 623 (
0
K T c m
Fe Fe
K
T
Ln T c m
Fe Fe
623
0
0
kJ
Fe agua inicial
315
1 1
= + =
kJ
agua
2 . 95 ...
2
= =
kJ
Fe
5 . 0 ...
2
= =
kJ
Fe agua final
7 . 95
2 2
= + =
kJ W W I
final inicial real til rev til
3 . 219
, ,
= = =
K T 293
0
=
K T
agua
303 =
Fe
kPa p 100
0
=
Q
? I
K
T
Ln T c m
a a
303
0
0
) 303 (
0
K T c m
a a
Ejemplo 41
Proceso reversible entre los
mismos estados inicial y final
W til W V = = ) ( 0
OJO: El sistema (Fe+agua) no intercambia Q con
nadie, es cerrado, as que W
rev
=
1
-
2
+nada
3
1
01 . 0 m V =
3
2
02 . 0 m V =
Argon=gas ideal
= =
2
1
1 1
2
1
dV
V
V p
pdV W
real
?
,til real
W ? I
) / 1 ( ) 2 , 1 ( ) 2 , 1 (
0 , B til rev
T T Q W + =
) / 1 ( ) ( ) (
0 2 1 0 2 1 0 2 1 B
T T Q S S T V V p U U + + =
K T 300
0
=
kPa p 100
0
=
Argon
K T 400
1
=
kPa p 350
1
=
K T
B
1200 =
kJ V p dV p W 1
0
2
1
0 0
= = =
kJ W W W
til real
43 . 1
0 ,
= =
0
W
2
1 B
T
dQ
real
W Q Q U + =
0
W Q = kJ 43 . 2 =
2
1
T
dQ
+
=
2
1
T
dW dU
?
2 1
S S
! ! ! S <
Camino reversible entre 1
y 2: la misma isoterma
pero con infinitos baos
=
2
1
T
pdV
1
2
2
1
V
V
RLn
V
RdV
= =
K kJ
T
W
rpido ms / 00608 . 0 _ = =
T
W
T
0
=
kJ W
til rev
64 . 2 ... ) 2 , 1 (
,
= = kJ W W I
til real til rev
21 . 1 ) 2 , 1 ( ) 2 , 1 (
, ,
= =
Ejemplo 42
const RT pV = =
Proceso cuasiesttico isotermo
kJ
V
V
Ln V p 43 . 2
1
2
1 1
= =
no reversible!!!
3
1
01 . 0 m V =
3
2
02 . 0 m V =
Argon=gas ideal
?
,til real
W ? I
) / 1 ( ) ( ) ( ) 2 , 1 (
0 2 1 0 2 1 0 2 1 , B til rev
T T Q S S T V V p U U W + + =
K T 300
0
=
kPa p 100
0
=
Argon
K T 400
1
=
kPa p 350
1
=
K T
B
1200 =
0
W
2
1 B
T
dQ
real
W Q Q U + =
0
W Q =
?
2 1
S S
! ! ! S <
T
W
T
0
=
) 2 , 1 ( ) 2 , 1 (
, , til real til rev
W W I =
Ejemplo 42
continuacin
const RT pV = =
Proceso cuasiesttico isotermo
0 ,
W W W
til real
=
) ( ) / 1 (
0 0 0 0
W W T T W
T
W
T W I
B
+ + = ) (
0
B
T
W
T
W
T =
) (
B
g
T
W
T
W
S =
+ =
2
1
g
B
S
T
dQ
S
=
2
1 B
g
T
dQ
S S
Evaluacin alternativa de
g
S T I
0
=
=
2
1
1
dQ
T T
W
B B
T
Q
T
W
= . ..........
B
T
W
T
W
=
vapor de
Turbina
_
C T 450
1
=
MPa p 3
1
=
C T 25
0
=
kPa p 100
0
=
C T 150
2
=
MPa p 2 . 0
2
=
?
W
s kg m / 8 =
kW Q 300 =
De las tablas se obtiene h y s para el estado de
entrada (vapor sobrec., h
1
y s
1
) de salida (vapor
sobrec. h
2
y s
2
) y el estado muerto (agua lquida,
h
0
y s
0
).
1 Ley: ) ( 0
p c
real e e h m W Q + + =
kW Wreal 4302 ... = =
1 2
h h h =
? max
W ? I
= = =
) ( ) (
2 0 2 1 0 1
max s T m s T m W W rev
)) ( (
2 1 0 2 1
s s T h h m =
kW 5069 ... = =
849 . 0 ... = = =
rev
real
II
W
W
?
II
kW W W I
real rev
767 ... = = =
?
1 _ vapor
1
2
1 0 1 0 0 1
2 / ) ( gz vel s s T h h + + = kg kJ / 1238 ... = =
434 . 0
1
=
m
Wreal
Se obtiene el 43.4%
del flujo de exerga del
vapor de entrada
Ejemplo 43
+ + =
salidas
j
j
entradas
i
i
k
k
k
rev m m Q
T
T
W ) 1 (
0
[ ] [ ] = = =
) ) ( ) ( ( ) (
0 2 0 0 2 0 1 0 0 1 2 1
s s T s s T m m
512 . 0
1
=
m
Wrev
El mximo que podra
obtenerse del flujo de exerga
del vapor de entrada es el
51.2%
C T 10
1
=
C T 21
0
= kPa p 101
0
=
C T 116
2
=
s kJ Q / 17 . 3 =
C T 54
3
=
kPa p
agua
138 =
s kg m / 27 . 2 1 =
I
Conservacin de masa y energa:
= +
3 2 1
m m m
p c
real e e h m h m h m W Q + + =
3 3 2 2 1 1
0
Despreciables
h de las tablas
) ( ) ( ) (
3 0 3
3
2 0 2
2
1 0 1
1 s T h m s T h m s T h m + =
s de las tablas
s kJ / 69 . 80 =
s kJ W W I real rev / 69 . 80 = =
g S T I
=
0
sK kJ S g / 274 . 0 =
Tambin:
0
T
Q
s m s m S
Entradas
i
i
Salidas
j
j
g
=
sK kJ / 274 . 0 =
s kg m / 17 . 0
2
=
s kg m / 44 . 2
3
=
Ejemplo 44
[ ] [ ] [ ] = + = + =
) ( ) ( ) (
0 3 0 0 3
3
0 2 0 0 2
2
0 1 0 0 1
1
3
3
2
2
1
1 s s T m s s T m s s T m m m m
= + + + =
) ( ) ( ) ( ) )( (
3 0 3
3
2 0 2
2
1 0 1
1
0 0 0
3 2 1 s T m s T m s T m s T m m m
+ + = =
Salidas
j j
Entradas
i i s g
k
k
k
VC
s m s m S
T
Q
S
,
0
+ + =
salidas
j
j
entradas
i
i
k
k
k
rev m m Q
T
T
W ) 1 (
0
También podría gustarte
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Runge Kutta de Orden 4 para Sistemas Aplicado A Circuitos ElectricosDocumento5 páginasRunge Kutta de Orden 4 para Sistemas Aplicado A Circuitos ElectricosJhulian Villafuerte100% (1)
- Control e Instrumentación de Procesos Químicos:) 2 T (Bu VT DT DV VDocumento67 páginasControl e Instrumentación de Procesos Químicos:) 2 T (Bu VT DT DV VRenzo PinedoAún no hay calificaciones
- VI. - Conducción de Calor Transitoria en Sólidos SemiinfinitosDocumento13 páginasVI. - Conducción de Calor Transitoria en Sólidos SemiinfinitosFrancisco González De Brito100% (3)
- Temas de Exposicion 3.4 3.5 y 3.6Documento7 páginasTemas de Exposicion 3.4 3.5 y 3.6Ulises Cortés LópezAún no hay calificaciones
- Termodinamica UdeMM - 7Documento20 páginasTermodinamica UdeMM - 7Martin Javier RadogowskiAún no hay calificaciones
- C03-Linealización y Función de Transferencia PDFDocumento56 páginasC03-Linealización y Función de Transferencia PDFEnrique VidalAún no hay calificaciones
- 07-Equilibrio Termodinaì - MicoDocumento16 páginas07-Equilibrio Termodinaì - MicoLOBOBLOXYT EL CRAK2000Aún no hay calificaciones
- Trabajo AychoDocumento10 páginasTrabajo AychoNi AnAún no hay calificaciones
- Ecuaciones DifDocumento4 páginasEcuaciones DifDaniel CabreraAún no hay calificaciones
- 13.2 Ejercicios 1Documento18 páginas13.2 Ejercicios 1Joe Marco Fiestas AmayaAún no hay calificaciones
- Taller Ecuaciones Diferenciales UDDocumento4 páginasTaller Ecuaciones Diferenciales UDFredy ParraAún no hay calificaciones
- Practica de Ecuaciones DiferencialesDocumento7 páginasPractica de Ecuaciones DiferencialesJorge Armando Ocampo MedinaAún no hay calificaciones
- Módulo Viii - Segundo Principio de La TermodinámicaDocumento28 páginasMódulo Viii - Segundo Principio de La TermodinámicaIsaac MuñozAún no hay calificaciones
- Labo Alterna Part1Documento7 páginasLabo Alterna Part1Luis Alberto Valverde SánchezAún no hay calificaciones
- Exergia3 ApunteDocumento16 páginasExergia3 ApunteOsvaldo RodriguezAún no hay calificaciones
- Formulario de EDDPDocumento4 páginasFormulario de EDDPmonicaAún no hay calificaciones
- LaplaceDocumento63 páginasLaplaceAlejandro Salinas LauraAún no hay calificaciones
- 1585698262.T - 1 - Combinacion Del Primer y Seg PrincipioDocumento38 páginas1585698262.T - 1 - Combinacion Del Primer y Seg PrincipioPedro InsaurraldeAún no hay calificaciones
- Trabajo Domiciliario 1Documento11 páginasTrabajo Domiciliario 1Monin Bernaola CamposAún no hay calificaciones
- Cambio de Variables Integrales DoblesDocumento11 páginasCambio de Variables Integrales DoblesVictor Azua PobleteAún no hay calificaciones
- EO51E 13avaSEMANA 03 EST NO ESTACONARIODocumento5 páginasEO51E 13avaSEMANA 03 EST NO ESTACONARIOALDO MORALESAún no hay calificaciones
- Final FluidosDocumento8 páginasFinal FluidosJohn Beker Espinoza VelasquezAún no hay calificaciones
- Act.4 ModeladoDocumento6 páginasAct.4 ModeladoDaniel MonroyAún no hay calificaciones
- Tarea 4.3 CVDocumento18 páginasTarea 4.3 CVFernando LemusAún no hay calificaciones
- Semincc, CADocumento6 páginasSemincc, CAalexandra perezAún no hay calificaciones
- Calculos. Trabajo Final. 201015 - 100Documento9 páginasCalculos. Trabajo Final. 201015 - 100omarcb10Aún no hay calificaciones
- Simulación de Un Intercambiador de CalorDocumento7 páginasSimulación de Un Intercambiador de CalorJazmin Flores MondragónAún no hay calificaciones
- Ejercicios de CircuitosDocumento11 páginasEjercicios de CircuitosOskarDarioAún no hay calificaciones
- Resolución Ej. 3 CinéticaDocumento3 páginasResolución Ej. 3 CinéticaSimon AbadovskyAún no hay calificaciones
- Formulario de ElectromagnetismoDocumento1 páginaFormulario de ElectromagnetismoAndrés YáñezAún no hay calificaciones
- Asignación 5Documento4 páginasAsignación 5Grecia Cajigas VelásquezAún no hay calificaciones
- Solución para La Ecuación de Calor Por Transformada de LaplaceDocumento6 páginasSolución para La Ecuación de Calor Por Transformada de Laplacemary pinzonAún no hay calificaciones
- Clase 4Documento8 páginasClase 4botametunosegaAún no hay calificaciones
- Problemas Sistemas de PotenciaDocumento73 páginasProblemas Sistemas de PotenciaKaren Marcela Mantilla Botello100% (2)
- Exergía-Abiertos 2014B PDFDocumento60 páginasExergía-Abiertos 2014B PDFPili TaAún no hay calificaciones
- 38 - Omaira Martinez - Fase 4Documento9 páginas38 - Omaira Martinez - Fase 4ANDRES FELIPE GUTIERREZ HUERTASAún no hay calificaciones
- Calculo Integral Ejercicios 2, 3 y 4Documento9 páginasCalculo Integral Ejercicios 2, 3 y 4luis hoyos100% (1)
- Matematicas Avanzadas - Actividad 4Documento17 páginasMatematicas Avanzadas - Actividad 4Luis Miguel Perez Pertuz0% (1)
- Deber para El Final Del Semestre Circuitos 2Documento18 páginasDeber para El Final Del Semestre Circuitos 2ronnyAún no hay calificaciones
- Muestreo de Aceptación Por Variables12Documento7 páginasMuestreo de Aceptación Por Variables12Andrea GFloresAún no hay calificaciones
- Formularios Fisica y CalculoDocumento3 páginasFormularios Fisica y Calculosimplemente1968Aún no hay calificaciones
- Entropia Termodinamica PPT CumpaDocumento32 páginasEntropia Termodinamica PPT CumpaDaniel LopezAún no hay calificaciones
- Codigo V15284373 326Documento9 páginasCodigo V15284373 326HEDDIE ELIZABETH MONASTERIO MEDINAAún no hay calificaciones
- Problemas Capitulo 10 y 11Documento12 páginasProblemas Capitulo 10 y 11coolkid23Aún no hay calificaciones
- Automatico Tema 1Documento17 páginasAutomatico Tema 1Victor Rebollal MendoAún no hay calificaciones
- Sistemas Muestreados y DiscretosDocumento30 páginasSistemas Muestreados y DiscretosRobert Andrew CabAún no hay calificaciones
- Problema 11 Circuitos 2 TrifasicosDocumento7 páginasProblema 11 Circuitos 2 TrifasicosxrexAún no hay calificaciones
- INTRODUCCIÓNDocumento22 páginasINTRODUCCIÓNISAI HUACHOS BENDEZUAún no hay calificaciones
- Parcial 11 ResolucionDocumento5 páginasParcial 11 ResolucionFede CasconAún no hay calificaciones
- Taller 7 FísicaDocumento5 páginasTaller 7 FísicaRoberto SuárezAún no hay calificaciones
- Tarea y Practica 10 Transformacion AdiabaticaDocumento10 páginasTarea y Practica 10 Transformacion AdiabaticaDelaia Nicole Ulloa AriasAún no hay calificaciones
- LaplaceDocumento4 páginasLaplacedantejbmAún no hay calificaciones
- ParcialOndas 2015-1Documento1 páginaParcialOndas 2015-1Brayan Camilo Estrada RamosAún no hay calificaciones
- 12 Movimiento Unidireccionales de LiquidosDocumento6 páginas12 Movimiento Unidireccionales de LiquidosBentura VenturaAún no hay calificaciones
- Ecuaciones Diferenciales ParcialesDocumento41 páginasEcuaciones Diferenciales ParcialesHebertMendezValdezAún no hay calificaciones
- Ejercicio 1 Sistema de Varios Grados de LibertadDocumento12 páginasEjercicio 1 Sistema de Varios Grados de LibertadRommel GuzmanAún no hay calificaciones
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaDe EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaAún no hay calificaciones
- Solucion Prueba de Nivelacion FM 2017 18Documento9 páginasSolucion Prueba de Nivelacion FM 2017 18Jorge Perez GarciaAún no hay calificaciones
- Tmm18 Practica5 Winmecc VelocidadesDocumento1 páginaTmm18 Practica5 Winmecc VelocidadesJorge Perez GarciaAún no hay calificaciones
- Presa BovedaDocumento13 páginasPresa BovedaJorge Perez GarciaAún no hay calificaciones
- Simulacro Examen Cinematica 1718 Solucion AcelDocumento1 páginaSimulacro Examen Cinematica 1718 Solucion AcelJorge Perez GarciaAún no hay calificaciones
- Simulacro Examen Cinematica 1718 Solucion VelocDocumento1 páginaSimulacro Examen Cinematica 1718 Solucion VelocJorge Perez GarciaAún no hay calificaciones
- ArmadurasDocumento37 páginasArmadurasJorge Perez Garcia100% (2)
- Segundo Parcial Resistencia de MaterialesDocumento8 páginasSegundo Parcial Resistencia de MaterialesJorge Perez Garcia0% (1)
- Estatica SRDocumento4 páginasEstatica SRJorge Perez GarciaAún no hay calificaciones
- Examenes AlgoritmicoDocumento35 páginasExamenes AlgoritmicoJorge Perez GarciaAún no hay calificaciones
- Carga Barco ContenedoresDocumento3 páginasCarga Barco ContenedoresJorge Perez GarciaAún no hay calificaciones
- 5EjProba 11-12 PDFDocumento18 páginas5EjProba 11-12 PDFJorge Perez Garcia0% (1)
- Visita HormicretoDocumento6 páginasVisita HormicretoAnaAún no hay calificaciones
- Lab. #6 Permeabilidad UTPDocumento8 páginasLab. #6 Permeabilidad UTPJose LopezAún no hay calificaciones
- Analisis de FluidosDocumento45 páginasAnalisis de FluidosGarcia ManuelAún no hay calificaciones
- Experiencia n2Documento4 páginasExperiencia n2Carlos Gormas PoloAún no hay calificaciones
- Problemas de Meteorología GeneralDocumento10 páginasProblemas de Meteorología Generaljamara74Aún no hay calificaciones
- Mentefactos Transporte Pasivo y OrganeloDocumento2 páginasMentefactos Transporte Pasivo y OrganeloAndrea Molano DuarteAún no hay calificaciones
- Problemas de Selectividad de Matem Aticas Aplicadas A La Ciencias Sociales Comunidad de Madrid (Enunciados)Documento103 páginasProblemas de Selectividad de Matem Aticas Aplicadas A La Ciencias Sociales Comunidad de Madrid (Enunciados)Ignacio MarínAún no hay calificaciones
- Ciclos de RefrigeraciónDocumento3 páginasCiclos de RefrigeraciónAnonymous jQreDXWVjAún no hay calificaciones
- Cálculo deDocumento3 páginasCálculo derobertocarlos88Aún no hay calificaciones
- INFORME de Entalpia de Fusion Del HieloDocumento18 páginasINFORME de Entalpia de Fusion Del HieloAlvaro TurizoAún no hay calificaciones
- Corte y TerraplenDocumento13 páginasCorte y TerraplenWilliams FontalbaAún no hay calificaciones
- Cuadro Comparativo de FibrasDocumento1 páginaCuadro Comparativo de FibrasIvan CarmannAún no hay calificaciones
- Herramientas Cualimétricas IIDocumento13 páginasHerramientas Cualimétricas IILu VercelloneAún no hay calificaciones
- Vitamina CDocumento3 páginasVitamina CkaterineAún no hay calificaciones
- Ejercicios Resueltos Sistema Hierro - CarDocumento3 páginasEjercicios Resueltos Sistema Hierro - CarJeffer Alexander Arbildo BalrodanoAún no hay calificaciones
- Secretaria de Comunicaciones y Transportes - GlosarioDocumento40 páginasSecretaria de Comunicaciones y Transportes - Glosarioandy7sixAún no hay calificaciones
- QC-215-ET-05-Concreto ArmadoDocumento17 páginasQC-215-ET-05-Concreto ArmadoAzucena Reyes HaroAún no hay calificaciones
- 4 Apuntes Elementos FinitosDocumento11 páginas4 Apuntes Elementos FinitosDilson Loaiza CruzAún no hay calificaciones
- Color en La ArquitecturaDocumento41 páginasColor en La ArquitecturaDiana GisAún no hay calificaciones
- Biometro BovisDocumento5 páginasBiometro BovisYOSOYEXITOSO100% (2)
- Función de Un Diodo 1N4148: 1k OhmiosDocumento9 páginasFunción de Un Diodo 1N4148: 1k OhmiosLuis Angel Salas VelasquezAún no hay calificaciones
- Servicio Comunitario IutvalDocumento47 páginasServicio Comunitario IutvalJoseAún no hay calificaciones
- Integrales TriplesDocumento5 páginasIntegrales Triplesslade18Aún no hay calificaciones
- Catalogo Woo & WilkinsDocumento136 páginasCatalogo Woo & WilkinsJose Amaro GonzalezAún no hay calificaciones
- Trabajo de Caminos II - Mantenimiento de Carreteras (Grupal)Documento191 páginasTrabajo de Caminos II - Mantenimiento de Carreteras (Grupal)Gerson Andre Morales Ramirez100% (1)
- Vision Artificial MatematicaDocumento8 páginasVision Artificial MatematicaZavaleta Hoyos MaryanAún no hay calificaciones
- 2 - EncajadoDocumento7 páginas2 - EncajadoNancy ChoquehuancaAún no hay calificaciones
- Guión P Animación-Saenz ValienteDocumento48 páginasGuión P Animación-Saenz ValienteRaúl Querci0% (1)
- Trabajo Experimental FenomenosDocumento37 páginasTrabajo Experimental FenomenosEdwin Cirilo ChaucaAún no hay calificaciones