Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Manual 2019-2
Cargado por
javierTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Manual 2019-2
Cargado por
javierCopyright:
Formatos disponibles
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Instituto Politécnico Nacional
UNIDAD PROFESIONAL INTERDISCIPLINARIA DE
INGENIERÍA CAMPUS GUANAJUATO
MANUAL DE PRÁCTICAS DE LA MATERIA:
QUÍMICA BÁSICA
CORRESPONDIENTES AL LABORATORIO:
QUÍMICA I Y QUÍMICA II
ÚLTIMA ACTUALIZACIÓN: JUNIO 2019
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 1
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Índice
Pág.
Índice
Práctica 1. Introducción al laboratorio de química 3
Práctica 2. Introducción al trabajo experimental 7
Práctica 3. Color a la llama de iones metálicos 9
Práctica 4. Propiedades físicas del enlace químico: conductividad 13
Práctica 5. Estado sólido: formación de cristales 18
Práctica 6. Obtención de una resina fenólica 23
Práctica 7a. Elaboración de un plástico reforzado 26
Práctica 7b. Obtención de una espuma flexible (poliuretano) 29
Práctica 7c. Encapsulado 32
Práctica 8. Identificación de polímeros 35
Práctica 9. Óxido ‐ reducción 41
Práctica 10. Celdas voltaicas 45
Práctica 11. Recubrimiento electrolítico 51
Índice de Anexos
Anexo 1. Rúbrica de bitácora 57
Anexo 2. Rúbrica de reporte 58
Anexo 3. Tabla general de propiedades de polímeros 59
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 2
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1. Introducción al laboratorio de Química
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivos:
a) Conocer el reglamento del laboratorio.
b) Conocer las políticas de evaluación y acreditación del laboratorio de Química Básica.
c) Identificar las áreas de trabajo experimental, los espacios asignados para equipos de
laboratorio y residuos químicos.
1.2 Fundamento teórico:
El laboratorio de Química es un espacio acondicionado especialmente para la experimentación,
realización de prácticas y proyectos de investigación, es por ello, que este espacio cuenta con el
equipamiento, material y reactivos necesarios para lograr el adecuado aprendizaje práctico del
alumno respecto al área de las ciencias químicas.
Con la finalidad de cumplir los objetivos de cada práctica en los tiempos establecidos, y, sobre todo,
conservando la integridad física de los alumnos, se cuenta con un reglamento de laboratorio, el cual
se resume a continuación:
Medidas de seguridad:
a) Se requiere el uso de bata de algodón (de manga larga y de preferencia que llegue hasta la
rodilla) debe de estar abrochada todo el tiempo y se debe de poner afuera del laboratorio.
b) Se requiere el uso de lentes de seguridad durante toda la sesión. En caso de que utilices
lentes de graduación no requerirás el uso de lentes de seguridad adicionales. Por otra parte,
está prohibido el uso de lentes de contacto. El uso de lentes de seguridad no será
necesario en el caso de que la sesión sea teórica, lo cual te será indicado previamente por
tu profesor y esto estará de acuerdo con el calendario de prácticas.
c) Se te recomienda usar ropa adecuada para el trabajo en el laboratorio de química,
preferentemente pantalón de mezclilla y zapato cerrado. Por el contrario, no se te permitirá
trabajar en el laboratorio si acudes vestido con short, bermudas, pants u otra prenda similar,
tampoco podrás trabajar en el laboratorio si el pantalón tiene agujeros. Los zapatos que uses
no deben llevar tacón, y tampoco se te permitirá trabajar en el laboratorio calzando sandalias,
huaraches, tenis de tela o similares.
d) Si usas el cabello largo, para trabajar en el laboratorio deberás recogerlo en una “cola de
caballo”, si el pelo es muy largo puedes enredarlo sobre la base o debes de conservarlo
siempre en la espalda.
e) Las uñas deben estar cortas y sin pintar. Este punto no aplica en caso de que la sesión sea
teórica, lo cual te será indicado previamente por tu profesor y esto estará de acuerdo con el
calendario de prácticas.
f) No está permitido introducir alimentos y bebidas dentro del laboratorio, de la misma manera
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 3
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
está prohibido ingerir bebidas dentro del laboratorio, así como comer cualquier alimento
independientemente de si se trata de dulces, galletas, chicles, etcétera.
g) Debes conocer la ubicación exacta y el modo de empleo del equipo de seguridad del
laboratorio (extintores, lavaojos, campanas de extracción, botiquín, regaderas, manta
antifuego, etc.)
La materia de química básica consta de la sesión teórica, que se imparte en el aula de clase, y la
sesión práctica, que se lleva a cabo en el Laboratorio de Química. Para poder aprobar la materia es
requisito aprobar la parte de laboratorio, para ello es indispensable trabajar de forma eficiente y
asistir a las prácticas de laboratorio. A continuación, se describen los requisitos para tener derecho a
entrar y/o permanecer en el laboratorio.
Puntualidad y asistencia
h) El tiempo de tolerancia para llegar al laboratorio es de 10 min, sin embargo, es el tiempo
asignado para que un representante del grupo llene el vale de material y cada equipo de
laboratorio revise su material de laboratorio, entregue una credencial en garantía y se lleve
su material a su mesa. Después de llevarse el material no se aceptan reclamaciones al técnico
de laboratorio.
i) Debes presentarte en el laboratorio con la vestimenta adecuada (revisar el punto de
medidas de seguridad)
j) Llevar bitácora de forma individual, sin embargo, se revisará una bitácora por equipo, si la
bitácora revisada no cumple con los requisitos necesarios todo el equipo de laboratorio
deberá abandonar la sesión de laboratorio. La bitácora debe de contener lo siguiente:
a. Índice actualizado
b. Fecha
c. Nombre y número de la práctica
d. Objetivo
e. Cuestionario pre-laboratorio contestado
f. Materiales, equipos y reactivos
g. Metodología con dibujos (no transcribir la metodología del protocolo, deben ser
dibujos y se pueden escribir palabras claves para que sean más claras las
instrucciones)
h. Deberá de contar con resultados y discusión de la práctica anterior.
i. Revisa la rúbrica de bitácora que se encuentra en la parte de anexos para que puedas
contar con la información más detallada del contenido solicitado.
k) Deberás de realizar las actividades programadas en el protocolo de prácticas y tu
comportamiento debe de ser el adecuado para poder permanecer en la sesión de laboratorio
(revisar el punto de actividades y comportamiento).
NOTA: En todos los casos que el alumno no entre a la sesión de laboratorio, no haya tenido
derecho a entrar o permanecer en la sesión, no se podrá reponer la sesión y la calificación
obtenida será de cero.
El desempeño en el laboratorio es fundamental para lograr el aprendizaje establecido, es por ello que
las actividades que realices deben ir de acuerdo a lo marcado en el protocolo de práctica. A
continuación, se especifica como debes desempeñarte durante la sesión:
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 4
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Actividades y comportamiento:
l) No realices experimentos sin previa autorización, puede ser peligroso. No hagas
combinaciones de reactivos que no estaban establecidos en el protocolo de práctica. No
manipules equipos que no indique el protocolo, y si debes de utilizar algún equipo en la
sesión de laboratorio tu profesor te dará instrucciones de cómo utilizarlo.
m) Debes de mantener orden dentro de tu área de trabajo. Los bancos deben de mantenerse
en su lugar y la mesa debe de estar limpia (sin: laptop, celulares, cartucheras, hojas sueltas).
Al terminar la sesión de laboratorio deberás de cerciorarte de que tu mesa haya quedado
limpia, al igual que las áreas comunes (campana de extracción, balanza analítica y tarjas) y
los bancos deberán estar en el lugar que les corresponde.
n) El uso de celular durante la sesión será exclusivamente para tomar fotos de los experimentos
y consultar datos necesarios para el desarrollo de la práctica y sí y sólo sí el profesor te lo
solicita y/o autoriza. Está prohibido mensajear, revisar redes sociales, hacer o recibir
llamadas.
o) Si debes salir del laboratorio por algún motivo justificable, deberás indicarlo al profesor
responsable. Si hay alguna ausencia de laboratorio sin previa autorización se tomará como
inasistencia.
p) El trabajo de laboratorio se permite sólo durante el horario establecido para el mismo y bajo
la supervisión directa de tu profesor.
q) Ten la precaución de nunca contaminar un frasco de reactivo. Asimismo, todo el material
que entre en contacto con un reactivo deberá estar limpio y seco. En caso de que sobrara
alguna cantidad de reactivo, pregunta a tu profesor que hacer con este.
r) Reporta al profesor y/o técnicos de laboratorio cualquier accidente y daño por insignificante
que parezca.
s) El derrame de cualquier sustancia debe ser limpiado de inmediato empleando el método
correcto, repórtalo al profesor para que te indique cuál es la manera adecuada de limpiar el
derrame.
t) Los desechos generados durante la sesión de práctica tienen un contenedor específico, si
tienes dudas pregunta a tu profesor cuál es. Nunca debes de depositar los desechos en la
tarja.
u) Diez minutos antes de finalizar la sesión de laboratorio, los alumnos deberán entregar los
equipos y materiales limpios y secos, y en las mismas condiciones en que lo recibió. Después
de lavar el material, éste se deberá de atomizar con alcohol para favorecer el secado del
mismo.
v) En caso de ruptura de material de laboratorio o desperfecto de algún equipo, el alumno
deberá llenar el vale correspondiente y dejará una credencial en garantía. La reposición del
daño se deberá de hacer en un tiempo máximo de 15 días naturales. El material deberá tener
las mismas características y marca de aquel correspondiente al adeudo generado.
w) Cuando un alumno no cumpla con los reglamentos establecidos, dado que pone en riesgo su
seguridad y la de sus compañeros, se hará acreedor a la expulsión del laboratorio y
automáticamente su práctica quedará anulada.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 5
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Evaluación y acreditación del laboratorio de Química Básica:
La calificación mínima aprobatoria, para el laboratorio de Química Básica, es de 6.0. Es requisito
aprobar el laboratorio para aprobar la materia de Química Básica. La evaluación se realiza con la
siguiente ponderación:
100 % Examen de laboratorio. El profesor te dirá la fecha de realización, el cual,
generalmente debe ser antes del examen departamental. El examen es individual y a
bitácora abierta.
0 % Bitácora de laboratorio. Se trabaja de forma individual y es requisito para
entrar al laboratorio. No puede llevar hojas pegadas.
Nota: En caso de inasistencia la calificación obtenida en esa ocasión es cero, en caso de existir una
justificación deberás de tratarlo con tu profesor lo más pronto posible.
Instalaciones del laboratorio de Química.
Como ya se ha mencionado, el laboratorio de Química no es un lugar peligroso si se trabaja
correctamente, de acuerdo a las medidas de seguridad y los protocolos de práctica. Para que puedas
trabajar con mayor seguridad ubica en tu laboratorio donde se encuentran físicamente los siguientes
componentes:
Lavaojos
Regaderas de emergencia
Manta antifuego
Campana de extracción
Extinguidores
Bidones de desechos de reactivos
Salidas de emergencia
Punto de reunión
Área de entrega de material de laboratorio
Área de equipos
Área de entrega de reactivos para la práctica actual
Mesas de trabajo
Tarjas
Gavetas
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 6
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
2. Introducción al trabajo experimental
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
El alumno conocerá el material básico de laboratorio y lo empleará en operaciones químicas
elementales.
1.2 Fundamento teórico:
Existen muchos materiales de laboratorio, algunos de ellos se deben de emplear en experimentos
muy particulares, sin embargo, hay otros de uso muy común y frecuentemente se utilizan en las
sesiones de prácticas de laboratorio, por lo anterior, es indispensable que el alumno pueda identificar
estos materiales, ya que al dominarlos puede llegar a seleccionarlos y manejarlos adecuadamente,
con lo que desarrollará la habilidad necesaria para realizar las prácticas incluidas en este manual.
1.3 Trabajo Pre-laboratorio
1. Investiga los pictogramas alusivos a las siguientes características que puede tener un reactivo
químico: explosivo, oxidante, inflamable, tóxico, irritante, corrosivo, peligroso para el ambiente.
2. Identifique cada uno de los materiales con los que va a trabajar, haga un dibujo en su bitácora de
cada uno de ellos.
3. Investiga cuantas clases de fuego existen y que clase de extintor se debe de usar para cada caso.
4. ¿Cuál es la información que debe de tener una etiqueta de un reactivo de laboratorio?
1.4 Desarrollo experimental
a) Medidas de seguridad
Utilizar bata.
Utilizar lentes de seguridad.
b) Materiales
2 Manguera de látex 1 Pinzas para termómetro Conexiones de vidrio
2 Tubos de ensaye 1 Embudo de filtración 1 Pizeta
1 Pipeta de 1 mL 2 Pinzas de tres dedos 1 Anillo metálico
1 Pipeta de 10 mL 1 Vaso de precipitado de 100 mL 1 Propipeta
1 Probeta de 25 mL 1 Matraz Kitazato 1 Charola metálica
1 Termómetro 1 Embudo Buchner 1 Espátula metálica
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 7
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1 Agitador de vidrio 2 Papel filtro 2 Soporte universal
1 Gradilla 1 Matraz volumético de 100 mL 1 Tela de asbesto
1 Mechero de Bunsen 2 Nuez 1 Tripie
1 Embudo de separación 1 Vidrio de Reloj 1 Mortero
Balanza analítica
c) Reactivos
Cloruro de sodio (NaCl) Frascos de reactivos diversos
d) Procedimiento
1. Clasifique los materiales de laboratorio en: material de soporte, material de vidrio y misceláneo.
Dentro de los materiales de vidrio clasifíquelos en: para medir y para contener.
2. Observe los reactivos que se le proporcionaron identifique el rombo de seguridad y anote en su
bitácora la información proporcionada.
3. Con el material de laboratorio proporcionado, monte los siguientes sistemas:
a) Filtración al vacío e) Calentamiento de un líquido a
determinada temperatura (simulación de 2
b) Filtración por gravedad
horas)
c) Decantación
f) Disolver 2 g de NaCl en 20 mL de agua y
d) Separación de dos líquidos
calentar a 40°C.
(extracción)
4. Seleccione uno de los sistemas anteriores, y realice, en su bitácora, el diagrama de flujo (con
dibujos).
5. Mida 100 mL de agua corriente con un vaso de precipitados y colóquelos en el matraz volumétrico.
Anote sus conclusiones.
6. Mida 25 mL con pipeta y colóquelos en una probeta, luego en el vaso de precipitado. Anote sus
conclusiones. Diga por que no utilizaría el matraz kitazato para medir un líquido.
1.6 REFERENCIAS BIBLIOGRAFICAS.
Rodríguez Esparza B.E., Romero Robles L.E.; Manual de laboratorio de Química para
Ingenierias. Primera Edición. Pearson Educación 2015. México.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 8
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
3. Color a la llama de iones metálicos
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
Identificar elementos de la tabla periódica a través de ensayo a la flama de varias sales metálicas.
1.2 Fundamento teórico:
En la llama de un mechero de gas pueden distinguirse dos partes bien diferenciadas: una interior, de
color azulado (zona de reducción) y baja temperatura, donde hay defecto de oxígeno y la combustión
del gas es incompleta. Su zona central está constituida por gases sin arder. La zona exterior, incolora
y de gran poder calorífico es la zona de oxidación y en ella la combustión de los gases es completa.
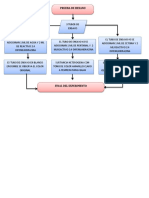
Bunsen distingue en la llama seis zonas fáciles de localizar base de la llama (A), que es la utilizada
para realizar el ensayo de coloración a la llama, zona de fusión (S), localizada en el centro de la
envoltura oxidante, zonas superior (E) e inferior (F) de reducción y zonas superior (C) e inferior (D)
de oxidación (Esquema 1). Todas estas zonas de la llama bunsen pueden modificarse regulando las
entradas de aire y/o de gas.
Cuando los átomos de un elemento se excitan, algunos de sus electrones "saltan" a niveles u orbitales
superiores de los que caen rápidamente a su posición inicial emitiendo una radiación luminosa
característica y visible. Así, en el caso de muchos elementos la temperatura de la llama oxidante de
un mechero de gas es suficiente para producir esa excitación de los electrones, que al emitir la
radiación característica, harán que la llama aparezca coloreada.
Esta llama no es capaz de excitar a los electrones de un átomo llevándolos a todos los orbitales
vacantes, sino que solamente es capaz de originar saltos electrónicos entre orbitales cercanos, lo que
hace que cada elemento emita un solo tipo de luz, pudiendo identificarse por ella. En esta práctica
vamos a comprobar la energía que emiten los electrones de diferentes elementos al caer desde una
órbita a otra de menor energía, para lo cual observaremos las diferencias de color de la luz emitida
cuando estos elementos se introducen en la llama de un mechero de gas.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 9
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Esquema 1. Partes de la llama del mechero
1.3 Trabajo Pre-laboratorio
1. Investigue qué son los espectros electromagnético, de emisión y de absorción.
2. ¿Por qué cada elemento tiene un espectro de líneas característico?
3. ¿Qué es un fotón?, ¿Por qué se dice que la luz tiene una naturaleza dual?
4. ¿Cómo se relaciona la pregunta anterior con las llamadas series de Balmer, Paschen, Lyman y
Brackett?
5. ¿Cuáles saltos del electrón de un átomo de hidrógeno generan radiación que aparece en el espectro
visible?
1.4 Desarrollo experimental
a) Medidas de seguridad
Utilizar bata.
Utilizar lentes de seguridad.
Manipular con cuidado el mechero de Fisher y de acuerdo a las indicaciones del personal responsable
de la práctica.
Limpiar con una franela húmeda el lugar donde se ha esparcido las disoluciones.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 10
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
b) Materiales
1 Mechero Fisher 1 Atomizador con metanol puro
1 Atomizador por reactivo
c) Reactivos
Cloruro de litio (LiCl) Cloruro de bario (BaCl2) Ácido bórico (B(OH)3)
Cloruro de sodio (NaCl) Cloruro de estroncio (SrCl2) Metanol (disolvente)
Cloruro de potasio (KCl) Cloruro de cobalto II (CoCl2)
Cloruro de cobre II
Cloruro de calcio (CaCl2)
hexahidratado (CuCl2·6H2O)
d) Procedimiento
1. Adicione 5 g de cada sal al contenedor de un aspersor y llénelo con metanol.
2. Verifique que éstos atomicen finamente y que no estén tapados (especialmente con los
correspondientes al cloruro de sodio y cloruro de potasio).
3. A continuación, y sobre una mesa de laboratorio que se encuentre en una zona bien ventilada,
encienda el mechero Fischer, si es posible apague las luces, y atomice hacia la llama primeramente
el metanol puro, con el fin de que tenga una referencia del color de la llama producido por éste.
4. Trabaje con cada una de las sales, y observe la coloración obtenida. Los colores que se deben
observar son los siguientes:
Cloruro de estroncio (rojo-
Cloruro de litio (rojo profundo)
naranja)
Cloruro de sodio (amarillo- Cloruro de cobre II
naranja) hexahidratado (verde-azul)
Cloruro de potasio (violeta) Ácido bórico (verde brillante)
Cloruro de calcio (rojo-naranja) Cloruro de bario (verde pálido)
PRECAUCIONES:
La demostración debe ser llevada a cabo en un lugar ventilado y libre de material inflamable
(recipientes y bidones con disolventes, con reactivos, y atomizadores de otras muestras).
Los vapores generados no deben ser inhalados.
No todo el metanol utilizado se consume en el fuego, por lo que los restos permanecen en el lugar
de trabajo y deben de ser retirados con un trapo húmedo, el cual debe de enjuagarse continuamente.
Nunca apunte el atomizador hacia la audiencia, así que los alumnos y profesores deben de estar al
menos a dos metros de la llama.
Al finalizar la sesión de laboratorio, la mesa donde se trabajó se debe de limpiar con jabón y fibra
para evitar la acumulación de sales y disolvente en la misma.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 11
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1.5 Cuestionario Postlaboratorio
1. Investigar a que se deben los espectros de emisión observados para cada uno de los diversos
elementos químicos.
2. Investigue por qué razón las sales de los cationes metálicos ensayados son en su mayoría
cloruros. Investigue cuál es el papel que juega el anión cloruro en este proceso.
3. Busque los espectros de emisión de los elementos a los que corresponden los cationes de las
sales ensayadas, y haga un comparativo con lo observado durante la práctica.
4. Escriba una reflexión acerca de la diferencia entre el color percibido en el experimento para cada
catión y el color real emitido por los correspondientes elementos metálicos.
5. Con relación a la pregunta anterior, ¿el color observado para el ácido bórico es realmente el que
emite este compuesto al ser ensayado a la llama o se debe a un efecto fisiológico propio de la
visión humana? Lleve a cabo esta misma reflexión para el color observado con el cloruro de cobre
II, y diga por qué estamos hablando de fenómenos diferentes.
1.6 REFERENCIAS BIBLIOGRAFICAS.
Brown, Theodore & col.; Química La Ciencia Central. Novena Edición. Pearson Educación 2004.
México, D.F.
Shakhashiri, Bassam Z.; Chemical Demonstrations, A Handbook for Teachers of Chemistry.
Volume 1. 1st. Edition. Wisconsin University, 1983. EUA.
Bretz, Stacey Lowery and Vasquez Murata Mayo, Ana. Development of the Flame Test Concept
Inventory: Measuring Student Thinking about Atomic Emission. J. Chem. Educ., 2018, 95 (1), pp
17–27. DOI: 10.1021/acs.jchemed.7b00594.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 12
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
4. Propiedades Física del enlace Químico:
Conductividad
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
Relacionar el tipo de enlace de una sustancia con su capacidad para conducir la corriente eléctrica.
1.2 Fundamento teórico.
Un enlace químico es el conjunto de fuerzas que mantiene unidos a los átomos de un compuesto
químico. Para realizar la clasificación de los elementos que se encuentran en la naturaleza, han sido
consideradas dos observaciones importantes: por un lado se ha advertido que la mayoría de los
elementos, en lugar de estar puros, se hallan combinados con otros, formando una gran variedad de
compuestos; y por el otro, se ha hecho notar que hay un grupo de elementos que difícilmente se
combinan con los demás.
La conclusión que podemos obtener de lo anterior es que los elementos que no suelen combinarse
deben tener una configuración (acomodo de sus electrones) muy estable. Asimismo, que los elementos
que, en general, se encuentran combinados es porque en sus átomos no tienen tal estabilidad y buscan
una manera de tenerla, ya sea ganando, perdiendo o compartiendo electrones con otros átomos,
formando así lo que conocemos como enlaces químicos. Se reconocen dos tipos principales de enlaces, el
iónico y el covalente.
ENLACE IÓNICO. Este tipo de enlace se forma cuando un átomo pierde electrones, y al quedar
con carga positiva, forma un ion positivo o catión. Los electrones que pierde un átomo son ganados
por otro átomo, que queda cargado negativamente, convirtiéndose en un ion negativo o anión. Como
los iones que resultan tienen cargas opuestas se atraen entre sí, formando un compuesto con enlaces
de tipo iónico que no forma moléculas simples sino un arreglo en el que se alternan los iones positivos y
negativos, forman una red. Los compuestos de tipo iónico, a temperatura ambiente, son sólidos con
puntos de fusión altos.
ENLACE COVALENTE. En algunos casos, los átomos adquieren la estabilidad que buscan
compartiendo pares de electrones, formándose así un enlace covalente, en donde pueden unirse átomos
iguales o diferentes. Los compuestos con enlaces covalentes están formados por moléculas simples: a
diferencia de los iónicos, que están formados por redes de iones. Los compuestos con enlaces covalentes
son más comunes que los compuestos con enlace iónicos, y a temperatura ambiente pueden ser sólidos,
líquidos o gaseosos.
La capacidad para conducir la corriente eléctrica depende del tipo de enlace que presenta la
sustancia en cuestión. Las sustancias que contienen átomos unidos por enlaces de tipo iónico serán
capaces de conducir la corriente cuando éstos tengan libertad para moverse. En el estado sólido, estos
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 13
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
iones mantienen un lugar fijo; en cambio, cuando las sustancias están en estado líquido o disueltas, los
iones pueden moverse libremente, permitiendo así el paso de la corriente eléctrica. Tal es el caso de la
mayoría de las sales, los ácidos y las bases, los cuales cuando están en solución o fundidas, tienen la
capacidad para conducir la corriente eléctrica; a estas sustancias se les conoce como electrolitos
Hay algunas sustancias que tienen la capacidad para formar iones en una proporción limitada,
por lo que podrán conducir la corriente eléctrica de una manera mucho menos eficiente que las que
tienen gran cantidad de iones. Por ello se les conoce como electrolitos débiles. A las sustancias con
enlaces covalentes que no son capaces de conducir la corriente eléctrica ni en solución ni fundidas, se
les conoce como no electrolitos.
1.3 Cuestionario pre-laboratorio
1. Describe los principales tipos de enlace químico.
2. ¿A qué grupo de elementos (metales o no metales) pertenecen los átomos que se unen para
formar compuestos iónicos?
3. ¿A qué grupo de elementos (metales o no metales) pertenecen los átomos que se unen para
formar compuestos covalentes?
4. ¿Qué características presentan las sustancias que tienen enlaces de tipo iónico?
5. ¿Qué características presentan las sustancias que tienen enlaces de tipo covalente?
1.4 Desarrollo experimental
a) Medidas de seguridad
Utiliza bata, lentes de seguridad y cubre-bocas
Manejar con cuidado el EQUIPO PARA MEDIR CONDUCTIVIDAD
b) Materiales
(3) Vaso de precipitados 150 mL (1) Vidrio de reloj
(1) Agitador de vidrio (1) Propipeta
(1) Espátula con mango de madera (1) Probeta graduada de 50 mL
(1) Pipeta graduada de 5 mL
c) Reactivos
Ácido clorhídrico (HCl) Agua destilada (H2O) Ácido acético (CH3COOH)
Cloruro de sodio (NaCl) Sacarosa (C12H22O11) Alcohol etílico (C2H5OH)
d) Equipo
Dispositivo para conductividad
e) Materiales y reactivos que deben traer los alumnos por TODO EL GRUPO
(1) Lija de agua No. 100
100 g de NaCl
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 14
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
100 g de azúcar
250 mL de alcohol etílico (C2H5OH)
200 mL de vinagre blanco
f) Procedimiento
1. Monta el equipo de conductividad tal y como se muestra en la Figura 1.
2. Con los compuestos proporcionados, prepara las soluciones que se indican en la Tabla I de la
sección de resultados.
Sólido. Llena parcialmente un vaso con cristales. Haz una prueba de conductividad (de acuerdo con
el paso 3). Conserva una pequeña cantidad para usarla en otras pruebas.
Solución acuosa diluida -Añade 5 gramos de sólido a 30 mL de agua destilada.
Solución acuosa - Añade aproximadamente 10 gramos de sólido a 30 ml de agua destilada.
Solución alcohólica - Añade aproximadamente 1 gramo de sólido a 30 mL de alcohol.
PRECAUCIÓN: Los alcoholes pueden ser venenosos si se absorben por la piel o se inhalan. También
se pueden encender con mucha facilidad. Evita el contacto con la piel, los ojos.
Nota: etiqueta los vasos con el nombre de la sustancia y las características de la disolución.
3. Prueba si las diferentes sustancias –como se muestra en la Figura 1- conducen o no la corriente
eléctrica, conectando el aparato a la fuente de poder de bajo voltaje y sumergiendo los electrodos
en cada una de las muestras.
Aquellas muestras con las que encienda el foco son los electrolitos. Después de cada una de las
pruebas, LAVA los electrodos en un vaso con agua destilada para evitar contaminar las soluciones.
Evalúa la conductividad de cada material probado, como bueno, malo o NDC (no se detecta
conductividad). Anota tus observaciones.
PRECAUCIÓN:
NO TOQUES LOS ELECTRODOS (LAMINILLAS DE COBRE) CUANDO EL APARATO ESTÉ CONECTADO
A LA FUENTE DE PODER. YA QUE CORRES EL RIESGO DE SUFRIR UN CHOQUE ELÉCTRICO.
4. Realiza una prueba de conductividad modificando el tamaño del área de los electrodos. Repite la
prueba al menos con tres diferentes tamaños de las laminillas de cobre. Para esta prueba, utiliza una
solución concentrada de NaCl. Anota tus observaciones en la Tabla II de la sección de
resultados.
5. Al terminar la práctica, coloca el alcohol puro y todos los sólidos en la mesa de reactivos. Todas
las soluciones acuosas se pueden echar por la tarja, usando una cantidad considerable de agua.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 15
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Figura 1. Equipo de conductividad.
1.5 Resultados
Prepara tablas para anotar tus resultados.
Tabla I.
Material Conductividad Observaciones Tipo de enlace
(iónico o
covalente)
Agua destilada
Agua corriente
Alcohol
Ácido acético
Ácido clorhídrico
NaCl sólido
NaCl disolución acuosa diluida
NaCl disolución acuosa
NaCl disolución alcohólica
Azúcar sólida
Azúcar disolución acuosa diluida
Azúcar disolución acuosa
Azúcar disolución alcohólica
KNO3 sólido
KNO3 solución acuosa
Tabla II.
Experimento Área de electrodos (cm2) Conductividad Observaciones
1
2
3
1.6 Conclusiones
Como guía para que prepares el apartado de conclusiones obtenidas a partir del trabajo experimental
realizado, considera los puntos siguientes:
• Explica las similitudes y las diferencias en los resultados obtenidos para las conductividades
de los compuestos probados.
• Explica las diferencias en los resultados, usando agua destilada y agua corriente.
• ¿Cuál es la razón de usar tanto agua como alcohol como disolventes?
• Basándote en este experimento, ¿cuáles son las conclusiones a que puedes llegar en relación
con los enlaces de los sólidos estudiados?
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 16
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
• ¿Qué efecto tiene la concentración de una solución sobre su conductividad?
• Para el caso de las sustancias conductoras de la electricidad, ¿qué efecto tiene el tamaño del
área del electrodo en la conductividad observada?
1.7 Cuestionario (deberás incluirlo en el reporte de laboratorio)
1. Predice la conductividad de CaS y de KBr, usando tablas de electronegatividades y de solubilidades.
2. Según la tabla de diferencias entre las electronegatividades de los elementos (Tabla IV), escribe
la mayor posibilidad de enlace (iónico o covalente) entre los átomos siguientes:
Tabla III.
Átomos Diferencia de Enlace
electronegatividad
Na y Cl
Na y O
CyH
Cl y H (en el HCl)
CyO
C y Cl
Tabla IV. Valores de electronegatividad[1,2]
Átomo Electronegatividad
Na 0.9
Cl 3.0
K 0.8
O 3.5
C 2.5
H 2.1
3. Investiga las Leyes de Faraday. ¿Existe alguna relación entre estos principios y el experimento
realizado en el paso 4? Comenta tus observaciones.
4. ¿Cuál es la ventaja de conocer el tipo de enlace que presentan los átomos que constituyen un
material de interés tecnológico, por ejemplo?
1.8 Referencias
[1] Brown T., LeMay E., Burnsten B. Química La Ciencia Central. Novena Edición Prentice Hall, México
2004.
[2] Chang, R. Química. Novena Edición. McGraw Hill, México 2005.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 17
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
5. Estado Sólido: Formación de Cristales
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo
Obtener sólidos cristalinos e identificar los diferentes sistemas de cristalización.
1.2 Fundamento teórico
Dependiendo del acomodo que tengan sus partículas, los sólidos pueden clasificarse en dos tipos:
cristalinos y amorfos. Los sólidos cristalinos tienen las partículas acomodadas siguiendo un orden
geométrico, por lo que forman estructuras con formas bien definidas, en tanto que los amorfos (sin
forma definida) no tienen ningún orden específico.
Las diversas aplicaciones de los cristales han llevado a desarrollar una tecnología electrónica
que ha traído consigo el desarrollo en diferentes campos, tales como: la medicina, la farmacéutica,
la energética, etc. Así, monocristales de silicio que contienen trazas de ciertas sustancias se usan en
baterías solares para la operación para la operación de instrumental en satélites; cristales de ciertos
compuestos sirven para dar control de frecuencia y otros se usan en micrófonos, audífonos y en
algunos tipos de relojes.
En forma cotidiana utilizamos cristales que, debido a su tamaño, no nos es posible percibir
la regularidad de su forma a simple vista, como la sal en polvo, el azúcar “glas”, el grafito de los
lápices, los polvos para hornear, el polvo de sulfatiazol, el polvo de azufre para usos farmacéuticos,
etc. Sin embargo, el acomodo regular de sus átomos da por resultado sólidos ordenados que, a pesar
de su tamaño, son armónicos y perfectos.
Para que un cristal se forme es necesario que las partículas de la sustancia se puedan acomodar
siguiendo el patrón geométrico que es específico para cada sustancia. Cuando el sólido se disuelve en un
solvente, forma una disolución y las partículas del sólido pueden moverse libremente, de manera que
pueden encontrar el lugar que les corresponde al lado de otras partículas iguales. De este modo, al
evaporarse el solvente se puede volver a formar el cristal.
La mayoría de los cristales puede someterse a procesos de crecimiento y el tamaño que
logren alcanzar dependerá del tiempo y de la técnica utilizada. Para poder obtener cristales a partir
de una solución es necesario que esta solución esté saturada, es decir, que tenga la máxima cantidad
posible de soluto (que en este caso será el sólido que se quiere cristalizar) en una determinada
cantidad de solvente. De esta manera, si dejamos destapado el recipiente que contiene la disolución,
el solvente se evaporará poco a poco, con lo que el sólido ya no tendrá lugar en la solución, y al
quedar fuera de ella, volverá a formar cristales.
Generalmente la solubilidad de los sólidos en los líquidos se incrementa al aumentar la
temperatura, por lo que si el solvente se utiliza caliente podrá disolver una mayor cantidad de
soluto. Al enfriarse la disolución, el soluto se cristalizará, ya que a menor temperatura el solvente
no tendrá la capacidad de disolver esa cantidad de soluto. La cristalización de un sólido en solución
se puede provocar, principalmente, de dos formas:
1) por evaporación del disolvente en una solución;
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 18
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
2) por enfriamiento de soluciones que fueron saturadas en caliente.
En este experimento utilizaremos ambos procedimientos para obtener cristales de sal, y
también estudiaremos la formación de cristales por medio del fenómeno de subli mación.
1.3 Cuestionario pre-laboratorio
1. ¿Qué es un cristal?
2. ¿Cuáles son las técnicas más comúnmente utilizadas para el crecimiento de cristales? ¿Cuál es la
base o principio para aplicar tales técnicas?
3. Menciona al menos 5 usos o aplicaciones de los cristales en el campo de la aeronáutica o Sistemas
automotrices.
1.4 Desarrollo experimental
a) Medidas de seguridad
Utiliza bata
Manejar con cuidado el material de vidrio al calentarlo
b) Materiales
(4) Vaso de precipitados 50 mL (2) Vaso de precipitados 150 (2) Vaso de precipitados 250
mL mL
(2) Mechero bunsen (2) Agitador de vidrio (2) Piseta
(2)Tela de alambre con (1) Tripié (1)Soporte universal con anillo
asbesto de fierro
(1) Recipiente para baño maría
c) Reactivos
Cloruro de sodio (NaCl) Alcanfor Yoduro de potasio (KI)
Sulfato de cobre (CuSO4·5H2O) Permanganato de potasio Dicromato de potasio
(KMnO4) (K2Cr2O7)
Hielo
d) Material que tienen que traer por TODO EL GRUPO.
25 clips
2 m de hilo para coser (cortado en fragmentos de 20 cm)
12 frascos de gerber (limpios y secos)
1 Marcador
1 Cinta masking tape
12 palos de madera de aprox. 10 cm
e) Procedimiento
Parte A. Cristalización a partir de una solución, por evaporación del solvente en una
solución saturada.
1. Llena uno de los vasos con agua, hasta la mitad de su capacidad.
2. Mide una cucharadita rasa de cloruro de sodio (NaCl), y viértela en el vaso, sin agitar. Observa
que la sal se deposita en el fondo del vaso.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 19
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
3. Mezcla todo con el agitador durante un par de minutos. Vas a observar que la sal desaparece
completamente y, a la vista, el vaso aparenta tener agua completamente transparente y cristalina.
Agrega otra cucharadita de sal, y agita con el agitador hasta que desaparezca.
4. Repite la operación, hasta que observes que la sal ya no se disuelve y queda depositada en el
fondo del vaso. Agita un minuto más y deja reposar el vaso sobre la mesa. Cuando en una solución
salina ya no se puede agregar más sal porque se sedimenta, se dice que está saturada.
5. Decanta la solución, vertiendo el líquido en otro vaso, cuidando de que no pase nada de la sal que
está depositada en el fondo.
6. Ata un extremo de un hilo al lápiz y el otro al clip. Introduce el clip en el vaso con la solución, de
manera que al apoyar el lápiz acostado sobre el borde del vaso, el clip quede colgando en medio del
líquido.
7. Coloca el vaso en algún lugar, de modo que nadie lo mueva por ningún motivo. Espera unos días,
hasta una o dos semanas, y observa lo que sucede. Seguramente verás que parte de la sal se ha
depositado en el fondo del vaso, pero otra parte se habrá depositado formando cristales de sal. Es
muy probable que algunos de esos cristales tengan la forma de un cubo perfecto. Trata de estimar
cuánto miden y vuelve a observarlos al cabo de otra semana.
Los cristales seguirán creciendo. También podrás observar que los cristales se forman incluso sobre
la parte el hilo que se encuentra fuera del agua. Esto sucede porque el agua sube por el hilo, debido
a un fenómeno conocido como capilaridad, y arrastra algo de sal. Al irse evaporando el agua del hilo,
la sal que se queda en éste va formando pequeños cristales.
Parte B. Cristalización por enfriamiento de una solución que fue saturada en caliente.
1. Llena un vaso, hasta la mitad de su capacidad, con agua hirviendo.
2. Agrega una cucharadita de sal, y agita hasta que la sal se disuelva completamente. Agrega más
sal, cucharadita por cucharadita, hasta que la solución quede saturada, y viértela en otro vaso,
cuidando que no se pasen los cristales que no se disolvieron y que están depositados en el fondo.
3. Deja enfriar la disolución a temperatura ambiente (unos 15 minutos) e introduce después el vaso
en un baño de hielo.
4. Si no llegaras a observar la formación de cristales, hierve un momento tu disolución para lograr
que se evapore un poco de agua. Deja enfriar a temperatura ambiente la disolución y, más tarde,
pásala al baño de hielo.
(CUIDADO: Algunos tipos de vidrio no resisten los cambios bruscos de temperatura y se
rompen).
Notarás que, al principio, se forma un sólido con aspecto de polvo en el borde de la solución: tus
cristales están a punto de aparecer. Deja pasar un poco más de tiempo (podrán pasar hasta algunos
días, lo que depende mucho de la concentración de tu solución, y también de las condiciones del
clima).
Observarás la formación de cristales blancos, con forma de pequeños cubos, en el centro del
recipiente. Conforme el agua se evapore, aparecerán más cristales, algunos de ellos más grandes,
en los que podrás observar perfectamente la forma que tienen.
Si dejas que toda el agua se evapore, obtendrás de nuevo la sal pura, ya completamente separada
del agua.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 20
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Parte C. Cristalización por sublimación.
1. Se pueden obtener cristales de una sustancia que se sublima (es decir, que pasa directamente de
sólido a gas), y que cuando pasa de nuevo al estado sólido se cristaliza. Este es el caso del alcanfor,
a la presión atmosférica, se sublima.
2. Coloca una muestra de alcanfor en uno de los vasos de precipitados de 50 mL
3. En el otro vaso coloca hielo o agua fría hasta la marca de 10 mL
4. Coloca el vaso que contiene el alcanfor en el baño María, y cúbrelo con el vaso que contiene el
hielo (Figura 1).
5. Después de unos minutos, observarás en la base del vaso que contiene el hielo unos cristales
blancos en forma de láminas.
Figura 1. Dispositivo para la cristalización por sublimación.
Parte D. Sistemas de cristalización.
En vidrios de reloj colocar una pequeña muestra de las siguientes sustancias: cloruro de sodio,
permanganato de potasio, sulfato de cobre, dicromato de potasio y yoduro de potasio. Observar cada
una de las muestras con el microscopio o una lupa.
1.5 Análisis de resultados
• Discutir y analizar los resultados. Prepara tablas para concentrar la información y facilitar el
análisis comparativo.
• De acuerdo a las observaciones realizadas, indica la forma de los cristales y el sistema de
cristalización al que consideras que pertenecen.
• Consultando la bibliografía, indica los sistemas de cristalización a que pertenece cada
sustancia.
1.6 Conclusiones
Como guía para que prepares el apartado de conclusiones obtenidas a partir del trabajo experimental
realizado, discute si se alcanzaron los objetivos propuestos.
Compara los resultados experimentales con los teóricos
Referencias
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 21
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
[1] Brown T., LeMay E., Burnsten B. Química La Ciencia Central. Novena Edición Prentice Hall, México
2004.
[2] Garritz, A., Chamizo, J.A. Química. Addison-Wesley Iberoamericana. USA 1994.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 22
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
6. Obtención de una resina fenólica
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
Obtener una resina mediante una reacción de policondensación.
1.2 Fundamento teórico:
El término macromolécula, o polímero, se aplica a las sustancias de peso molecular elevado que están
compuestas por un gran número de unidades de bajo peso molecular, llamadas monómeros,
(normalmente mayor a 100) que se unen entre sí por medio de enlaces covalentes. Si los monómeros
que forman la macromolécula están unidos por sus extremos formando una cadena larga sin que las
distintas cadenas se encuentren unidas entre sí por enlaces covalentes, se denominan polímeros
lineales. Dichos polímeros, salvo que su peso molecular sea muy alto (mayor a 1.000.000) suelen
ser solubles en distintos disolventes y al calentarse se ablandan o se funden, por lo cual pueden
extruirse en forma de fibras o moldearse, adoptando la forma que se desee. Por ello, se dice que son
termoplásticos. Por el contrario, aquellos polímeros cuyas cadenas se encuentran entrecruzadas,
uniéndose entre sí en diversos puntos mediante enlaces covalentes, se denominan polímeros
entrecruzados o termoestables. Este tipo de polímero adopta la forma de grandes redes
tridimensionales que hacen que sean insolubles e infusibles. (Arrazola y Martínez, 2001)
La importancia de los polímeros en la industria y en la vida diaria es muy grande, cabe recordar que
las unidades estructurales (polisacáridos y proteínas) y de información (ADN y ARN) de los seres
vivos son polímeros. Así mismo, muchos de los materiales que manejamos habitualmente (bolsas y
botellas de plástico, el nylon y muchos otros tejidos) están realizados empleando materiales
poliméricos.
El proceso por el que se unen distintos monómeros para formar una macromolécula se denomina
reacción de polimerización y puede realizarse de dos formas distintas: a) polimerización por adición
y b) polimerización por condensación. Ambos tipos de reacciones han de ser capaces de continuar
indefinidamente. Siempre que reaccionen dos moléculas de monómero, el producto resultante debe
ser capaz de reaccionar con otro monómero para que la cadena pueda alargarse.
(Hernández, Martínez y Arrazola, 1996)
1.3 Trabajo Pre-laboratorio
1. Investigar qué es un polímero.
2. ¿Qué es una reacción de polimerización?
3. ¿Qué es una reacción de policondensación?
4. ¿Qué es una resina?
5. ¿Qué es la baquelita y cuáles son sus principales usos?
6. ¿Cuáles son las propiedades de un polímero termoestable?
1.4 Desarrollo experimental
a) Medidas de seguridad
• Utilizar bata, cubre bocas, guantes y lentes de seguridad
• Manipular con cuidado el mechero de bunsen, el material de vidrio caliente y los reactivos de
acuerdo a las indicaciones del personal responsable de la práctica.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 23
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
b) Materiales
Vaso de precipitados 600 mL Vaso de precipitados 100 mL
Soporte universal (2)
(2) (2)
Termómetro -20ºC – 110 ºC (2) Pinza para termómetro (2) Anillo de fierro (2)
Mechero bunsen (2) Agitador de vidrio (2) Pipeta de 5 mL (2)
Asa de alambre de cobre
Pipeta Pasteur de plástico (2) Tela de alambre con asbesto (2)
(2)
Charola de aluminio (2) Espátula metálica (1) Propipeta (1)
c) Reactivos
Resorcinol C6H4(OH)2 Ácido clorhídrico (HCl) Formaldehído (CH2O)
Hidróxido de sodio (NaOH) Agua destilada
d) Equipo
Balanza analítica Multímetro
d) Procedimiento
PROCEDIMIENTO A.
1. Pesa 2 gramos de resorcinol y colócalos en un vaso de 100 mL.
2. Agrega 3 mL de formaldehído.
3. Coloca el vaso en un baño maría y calienta manteniendo la temperatura del baño a 50°C
hasta que se hayan disuelto todos los cristales de resorcinol.
4. Agita la disolución mientras se están disolviendo los cristales.
5. Retira el agitador y en su lugar utiliza un asa de cobre.
6. Calienta el baño maría hasta 70°C (tener cuidado de no sobrecalentar).
7. Mantén esta temperatura durante 10 minutos.
8. Retira el vaso del baño maría y déjalo enfriar.
9. Cuando la mezcla se haya enfriado, agrega gota a gota hidróxido de sodio (6 M) lentamente
hasta que se efectúe la reacción (usa el alambre para extraer el plástico del vaso y guantes).
10. Observa y registra las características del producto obtenido (determinar densidad, resistencia
eléctrica, conductividad eléctrica, comportamiento al calor).
PROCEDIMIENTO B.
1. Pesa 2 gramos de resorcinol y colócalos en un vaso de 100 mL.
2. Agrega 3 mL de formaldehído.
3. Coloca el vaso en un baño maría y calienta manteniendo la temperatura del baño a 50°C
hasta que se hayan disuelto todos los cristales de resorcinol, como en el procedimiento A.
4. Retira el vaso de 100 mL del baño maría y coloca un asa de alambre de cobre.
5. Con precaución agrega ácido clorhídrico concentrado gota a gota hasta que se efectúe la
reacción. Una vez concluida la reacción, usa el asa de alambre para extraer el plástico del
vaso y cubre las manos con guantes al manipular la resina.
6. Observa y registra las características del producto obtenido.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 24
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1.5 Guía para la construcción de la sección de análisis y discusión de resultados.
• Elabora un cuadro comparativo con las características de los productos obtenidos en los dos
procedimientos
• Menciona qué tipo de plástico se formó en cada uno de los procedimientos y discute cuáles
son las diferencias entre los dos productos obtenidos.
• Investiga y discute cuáles las diferencias entre los procedimientos de preparación de la resina
fenólica.
• Discute si las propiedades de los productos obtenidos dependen del método de preparación.
• Escribe la reacción de polimerización efectuada.
• Indicar cuál es la función de cada uno de los reactivos utilizados en las reacciones efectuadas.
Al final del reporte, deberás incluir una ficha con las propiedades físicas y químicas de cada uno de
los reactivos utilizados, así como su toxicidad y precauciones para su manipulación.
1.6 REFERENCIAS BIBLIOGRAFICAS.
Arrazola, D. Flor del Monte, Martínez, V, Elsa. Química y Propiedades de los Polímeros. IPN-ESIQIE.
5ª Edición. México 2001.
Hernández, L. Heliodoro, Martínez, R. Víctor Manuel, Arrazola, D. Flor del Monte. Transformación de
Termoplásticos, Termofijos y Reciclado. Instituto Politécnico Nacional. México 1996.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 25
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
7a. Elaboración de un Plástico Reforzado
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
Conocer los diversos elementos utilizados para la fabricación de plásticos reforzados con fibra de
vidrio, utilizando el método de laminado a baja presión, a través de la obtención de una lámina de
fibra de vidrio de buena calidad.
1.2 Fundamento teórico.
Dentro del amplio mundo de los plásticos, un lugar especial es ocupado por los polímeros reforzados
debido a su amplia versatilidad, conferida por sus excelentes propiedades mecánicas y químicas, por
lo que se utilizan en el área de la construcción, en un gran número de aplicaciones que anteriormente
sólo eran cubiertas por materiales como el acero, madera, cemento, aluminio, etc.
Los productos de resina poliéster poseen óptimas propiedades físicas, mecánicas y eléctricas, sin
dejar de mencionar la buena resistencia química y a la intemperie; este tipo de materiales no están
sujetos a la corrosión eléctrica ni a otro tipo de degradación, además su fabricación representa un
costo moderado, por lo que presenta ventajas económicas ante materiales de uso tradicional.
Se le llama “laminado” a sobreponer dos o más películas de algún material y unirse con un material
adhesivo. Aunque esta denominación abarca a un gran número de materiales en la industria de los
plásticos, el término laminado también se aplica a productos estructurales formados por la
combinación de sustratos de fibra de vidrio y resinas poliéster.
Los plásticos reforzados consisten de la siguiente combinación:
• Un sistema resinoso adhesivo que normalmente incluye distintos elementos además de la
resina, los cuales pueden ser promotores, endurecedores, cargas, catalizadores,
aceleradores, retardantes al fuego, flexibilizantes, pigmentos, etc. Estos elementos son los
que proporcionan al material formado las características requeridas para su aplicación.
• Un refuerzo fibroso. Generalmente se emplea la fibra de vidrio, en sus distintas formas
(colchoneta, hojas, cuerdas y trozos); el material fibroso también puede ser de asbesto,
carbono o poliamidas principalmente, siendo la fibra de vidrio la que proporciona mejores
propiedades y facilidad de manejo al menor costo.
1.3 Cuestionario pre-laboratorio
1. Investigar las formas comerciales en las que podemos encontrar la fibra de vidrio, indicando el uso
más común para cada una de ellas.
2. ¿Qué es un plástico reforzado?
3. Investigar dos métodos de moldeo de plásticos reforzados.
4. Investigar tres resinas empleadas en la fabricación de plásticos reforzados, con sus respectivas
características.
5. ¿Cuáles son las aplicaciones que tienen los plásticos reforzados con fibra de vidrio?
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 26
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1.4 Desarrollo experimental
a) Medidas de seguridad
Utiliza bata, lentes protectores y cubre bocas
b) Materiales (proporcionados por cada equipo)
4 tablas de madera de 20 x 20 cm, recortadas simétricamente, lijadas y limpias (procurar que no
tengan capas de pintura)
1 Tijeras
2 Brochas de 2 pulgadas
2 Lijas No. 100
2 recipientes de plástico (envase de crema o yogurt) de 1 L
Nota: Todos los recipientes tienen que estar vacíos y limpios.
c) Reactivos (proporcionados por cada equipo)
Desmoldante (alcohol polivinílico)
Resina poliéster
Fibra de vidrio (colchoneta)
Catalizador
d) Procedimiento
1. Preparar las tablas aplicando en su superficie una capa de desmóldate (alcohol polivinílico).
2. Cortar la colchoneta de fibra de vidrio en cuadros de 20 cm2.
3. Mezclar 100 mL de resina y 25 gotas de catalizador.
4. Colocar una capa de resina ya preparada (paso 3) sobre una de las tablas, posteriormente colocar
el cuadro de fibra de vidrio, una vez hecho esto colocar otra capa de resina sobre la de fibra de vidrio,
evitando la formación de burbujas de aire.
5. Colocar un segundo cuadro de fibra de vidrio e impregnarla con resina.
6. Colocar la segunda tabla sobre el material y poner sobre ella un peso de alrededor de 10 Kg, para
comprimir el laminado.
7. Determinar el tiempo en el que se inicia la gelación de la resina (observar el recipiente de mezclado
de resina y catalizador).
8. Tomar la temperatura e indicar cuál es la temperatura máxima de polimerización.
9. Hacer una curva de temperatura contra tiempo.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 27
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
10. Después del curado, aproximadamente 8 horas, quitar los moldes (las tablas).
11. Limar y lijar las orillas.
12. Lavar y dejar secar.
Bibliografía
Hernández, L. Heliodoro, Martínez, R. Víctor Manuel, Arrazola, D. Flor del Monte. Transformación de
Termoplásticos, Termofijos y Reciclado. Instituto Politécnico Nacional. México 1996.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 28
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
7b. Obtención de una Espuma Flexible (Poliuretano)
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
Conocer el procedimiento e identificar los componentes necesarios para la obtención de una espuma
flexible (poliuretano).
1.2 Fundamento teórico.
Al hacer reaccionar químicamente a un poliol y un isocianato se obtendrá un poliuretano, aunque su
formulación requiere y admite múltiples variantes y aditivos.
Una de las dos materias primas principales para la elaboración de un poliuretano son los isocianatos.
De acuerdo a la estructura que presenta el isocianato es el uso y aplicación que se le va a dar, los
más empleados son TDI (espumas flexibles), MDI (espumas elastómeras).
TDI (Toluen Di-isocianato) comercialmente es un producto importante, debido a su utilización en la
fabricación de espumas flexibles, no obstante su uso se ha estado restringiendo debido a su alta
volatilidad y toxicidad.
MDI (Metano Difenil Di isocianato). Este material resulta muy atractivo debido principalmente a su
menor toxicidad y volatilidad por lo que a nivel mundial su uso se ha incrementado, principalmente
en la fabricación de elastómeros de poliuretano y de espuma rígida además de adhesivos; es el
segundo en uso a nivel comercial.
En general, los isocianatos desprenden vapores, que resultan ser muy irritantes a los ojos y a las
membranas mucosas, llegando a ocasionar ataques de asma y enfisema pulmonar. Cuando se tiene
contacto con la piel y ojos si se realiza el lavado inmediato y vigoroso no existe ningún peligro.
El otro componente indispensable para la obtención de poliuretanos, son los polioles un ejemplo de
estos es el poliol poliéster, cuya utilidad su utilidad en la formación de espumas se reconoce desde
1957. Este material es parte clave en la elaboración de diversos poliuretanos, como espumas flexibles,
espuma rígida, espuma piel integral y elastómeros.
Además de las dos materias primas principales para obtener poliuretanos, también se pueden añadir
aditivos, los cuales proporcionan ciertas propiedades específicas, aumentando la gama de productos;
entre estos aditivos tenemos catalizadores, inhibidores, retardantes a la flama, pigmentos, etc. Este
tipo de aditivos deben ser mezclados con el poliol, para posteriormente adicionarse al isocianato para
que se lleve a cabo la reacción.
Los poliuretanos del tipo espumas flexibles, como el que se obtendrá en la presente práctica, son
materiales blandos acolchonados. Algunas de sus aplicaciones son las siguientes: fabricación de
muebles (colchones, cojines, asientos y respaldos); empaque y embalaje (piezas de cristal,
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 29
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
computadoras, televisores, etc.); fabricación de automóviles (asientos, respaldos y apoyos de cabeza)
y consumo general (esponjas para baño y filtros), entre otros [1,2].
1.3 Cuestionario pre-laboratorio
1. ¿Cuáles son los principales poliuretanos fabricados en la actualidad y sus principales
aplicaciones?
2. Investigar dos procedimientos industriales para la obtención de poliuretanos (espumas
flexibles).
3. Investigar la toxicidad de los poliuretanos.
1.4 Desarrollo experimental
a) Medidas de seguridad
Utiliza bata, lentes protectores, cubre-bocas y guantes.
b) Materiales (proporcionados por cada equipo)
1 recipiente de plástico (envase de crema comestible con una capacidad de 1 kg)
1 abate lenguas
1 Frasco de vidrio (boca ancha)
2 Jeringas desechables de 10 mL
Nota: Todos los recipientes tienen que estar vacíos y limpios
c) Reactivos (proporcionados por cada equipo)
Desmoldante (alcohol polivinílico)
Componente “A” (poliol)
Componente “B” (isocianato pre-polimerizado)
d) Procedimiento
1. Lavar perfectamente el recipiente (molde) y secarlo.
2. Colocarle una capa de Desmoldante al molde.
3. Medir 10 mL del componente “A”
4. Medir 4.5 mL del componente “B”
5. Mezclar el componente “A” y “B” en un frasco de vidrio por 10 segundos.
6. Vaciar la mezcla en el recipiente (molde).
7. Dejar que se forme el poliuretano.
8. Retirar el poliuretano del molde.
1.5 Bibliografía
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 30
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
[1] Arrazola, D. Flor del Monte, Martínez, V, Elsa. Química y Propiedades de los Polímeros. IPN-
ESIQIE. 5ª Edición. México (2001).
[2] Documentación elaborada por el Instituto Mexicano del Plástico Industrial.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 31
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
7c. Encapsulado
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo:
Conocer el procedimiento de encapsulado en frío utilizando una resina termofija.
1.2 Fundamento teórico.
El encapsulado es un método derivado del vaciado cuyo fin es envolver un material con un polímero
sólido para fines de protección o de ornamento.
Uno de los métodos más antiguos de moldeo es el vaciado, que se aplica tanto para termoplásticos
como para termofijos, debido principalmente a la sencillez y economía de fabricación. Una de las
ventajas del vaciado es que se pueden utilizar insertos en la pieza moldeada, los insertos son,
generalmente, partes metálicas que van unidas a la pieza terminada siendo este uno de los principales
usos del encapsulado. Este método consiste en colocar el objeto que se desee encapsular en el molde
en la posición requerida y después se vacía la resina, la cual se deja endurecer.
El encapsulado es utilizado en la fabricación de encendido electrónico automotriz, para proteger las
partes eléctricas, de humedad, solventes calor y descargas eléctricas. El encapsulado también es
utilizado en la fabricación de adornos y mangos termofijos de algunas herramientas, logotipos,
llaveros y adornos varios.
Los catalizadores (iniciadores) empleados en encapsulado son generalmente un peróxido orgánico o
un hidroperóxido (peróxido de benzoilo, peróxido de metil-etil-cetona o MEK, peróxido de
ciclohexanona) cuya descomposición inicia la formación de los enlaces cruzados en la resina, su
presentación más común es en solución, la cual se mezcla en una proporción variable, usualmente el
catalizador activo agregado oscila entre 0.3 % y el 0.4 % del peso total de la resina.
1.3 Cuestionario pre-laboratorio
1. Investigar la utilización de las resinas siguientes:
a) Poliéster
b) Ftalato de dialilo
c) Fenólicas
d) Epóxica
e) Acrílicas
2. Investigar qué es una resina termofija y una resina termoplástica.
3. ¿Qué resina se utiliza para encapsular partes eléctricas y por qué?
4. ¿Qué diferencia existe entre catalizador e iniciador aplicado a una resina?
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 32
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1.4 Desarrollo experimental
a) Medidas de seguridad
Utilizar lentes de seguridad y cubre bocas.
b) Materiales
1 probeta graduada de 20 mL
2 abate lenguas.
1 recipiente de crema o de yogurt (1L).
1 molde
1 objeto, de preferencia metálico, para encapsular (tamaño no mayor de 2.5 cm)
1 jeringa desechable de 10 mL
Nota: Todos los recipientes tienen que estar vacíos y limpios
c) Reactivos
Resina poliéster (20 mL)
Catalizador K-2000 (10 gotas)
Pigmento líquido (2 a 5 gotas)
d) Procedimiento
1. Limpiar y secar perfectamente el objeto a encapsular.
2. Medir 10 mL de resina poliéster.
3. Colocar en el recipiente los 10 mL de resina y agregar el pigmento liquido mezclar, añadir 5 gotas
de catalizador y volver a mezclar, evitando la formación de burbujas.
4. Vaciar la resina catalizada en el molde cuidadosamente con una jeringa hasta alcanzar una altura
de 5mm dejar que gele durante 15 minutos aproximadamente.
5. Colocar el objeto a encapsular sobre la superficie gelada, posteriormente adicionar una segunda
porción de resina 10 mL, preparada con catalizador, utilizando preferentemente la jeringa para evitar
la formación de burbujas.
6. En caso de que se formen burbujas, tronarlas con la aguja de la jeringa.
7. Dejar que el encapsulado se polimerice por espacio de 48 horas.
8. Sacar la pieza encapsulada del molde sin golpearla.
9. Lijar la superficie de encapsulado, lavar y dejar secar.
10. Pulir las superficies con pulimento hasta tener una transparencia deseada, posteriormente lavar
con agua y jabón.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 33
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
1.5 Análisis de resultados
Revisar la calidad del encapsulado, evaluando los parámetros siguientes:
1) formación de burbujas;
2) pegajosidad;
3) olor;
4) transparencia;
5) colocación de la pieza.
1.6 Bibliografía
Hernández, L. Heliodoro, Martínez, R. Víctor Manuel, Arrazola, D. Flor del Monte. Transformación de
Termoplásticos, Termofijos y Reciclado. Instituto Politécnico Nacional. México 1996.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 34
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
8. Identificación de Polímeros
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivos:
a) Identificar el tipo de polímero de acuerdo a sus propiedades físicas y químicas;
b) Evaluar la variación de propiedades de diferentes polímeros;
c) Identificar el tipo de polímero de acuerdo a su símbolo de reciclaje.
1.2 Fundamento teórico:
Los polímeros son macromoléculas compuestas por series repetitivas de monómeros. Estos pueden
ser de origen natural, como la seda, celulosa, fibras de algodón, etc., o sintéticos como el
polipropileno, polietilentereftalato, poliestireno, polietileno, policloruro de vinilo, entre otros.
Los polímeros se clasifican de diversas formas y una de ellas es agruparlos en dos grandes grupos,
como termofijos y termoplásticos (plásticos). Estos últimos presentan flexibilidad al calentarse entre
80 y 100 °C, con una gran facilidad para ser moldeados sin perder sus propiedades; al superar dicha
temperatura se degradan mientras que a temperatura ambiente son sólidos y dúctiles. Por otra parte,
presentan la propiedad de arder con mucha facilidad, formando gotas y generando un olor
característico.
En la Figura No. 1 se muestra el código que identifica a los termoplásticos de mayor importancia y
uso a nivel mundial, también denominados “commodities”. Este código de identificación se adoptó
en México a partir de 1999 en la norma mexicana NMX-E-232-SCFI-1999. Además, indica la
simbología correspondiente para efectos de reciclaje y embalaje. En la Tabla I se presentan los
termoplásticos de mayor uso industrial a nivel mundial.
PET PEAD PVC PEBD
PP PS OTROS
Figura 1. Simbología utilizada para el embalaje y reciclaje de materiales poliméricos [1]
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 35
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Termofijos. Estos materiales poseen la característica de ser rígidos, debido a su estructura compleja
tipo red, una vez moldeados ya no se puede modificar su forma, es decir polimerizan
irreversiblemente, por lo tanto no son reciclables.
Debido a su composición química estos materiales no funden y al ser expuestos al fuego solo se
carbonizan, lo que indica que el polímero se ha degradado. En la Tabla 2 se mencionan algunos
ejemplos de este tipo de materiales.
Tabla 1. Principales Termoplásticos utilizados en la industria a nivel mundial.
Nombres
Plásticos Propiedades Aplicaciones
Comerciales
PEBD. Es traslucido cuyo punto
Polietileno de fusión es de 110 °C en
-De baja promedio, resistencia al
Lupolen Películas, botellas,
densidad(LDPE o rasgado, aislamiento eléctrico,
Vestolen tuberías, láminas,
PEBD) flexibles.
Bayolen artículos domésticos,
-De alta PEAD. Resistencia mecánica
Hostalen bolsas
densidad(HDPE o (rigidez, dureza y resistencia a
PEAD) la tensión) y a productos
químicos
PVC blando:
Material blando con alta
Nipolan
resistencia al desgaste.
Regulan Tubería, Conduit,
PVC duro:
Skai Cintas enrolladas y
Cloruro de polivinilo Presenta fragilidad al frío.
Hostalit adhesivas, botellas,
(PVC) Ambos plásticos presentan
Vinoflex tapicería, aislante de
inestabilidad a disoluciones
Vinol cables eléctricos
orgánicas, resistencia a ácidos,
álcalis y alcoholes. Resiste a las
llamas
Resistencia a álcalis y ácidos. Autopartes,
Hostalen
Baja absorción de humedad. recipientes, juguetes
Polipropileno Novolen
Resistencia a la fatiga. fibras, bolsas,
Luparen
pañales
Poliestireno cristal: (PS)
Buenas propiedades ópticas,
PS es usado en la
mínima absorción al agua,
fabricación de
resiste a ácidos orgánicos e
envases para:
inorgánicos, es vulnerable a
productos
ésteres, cetonas, hidrocarburos
alimenticios,
Fortareno aromáticos.
farmacéuticos y
Novodur Poliestireno Expansible:
Poliestireno cosméticos.
Lustrex Resiste temperaturas bajo cero,
Estiron pero a temperaturas alrededor
EPS es empleado en
de 88 °C, pierde sus
la edificación,
propiedades, posee poder de
especialidades
amortiguamiento, flota en el
industriales, cuerpos
agua, resiste a la mayoría de los
moldeados y envases
ácidos, soluciones alcalinas y
saladas. Sin embargo no resiste
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 36
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
a los solventes orgánicos o
aceites minerales.
Se usa como fibra
tanto industrial como
Es altamente rígido e incoloro, textil.
presenta un elevado punto de El PET es empleado
fusión de 258 °C y excelentes en la fabricación de
Kerylen
propiedades mecánicas, así botellas para:
Polietilentereftalato Trevira
como buena resistencia química. Bebidas
(PET o PETE) Versan
Las botellas de PET no permiten carbonatadas
Dacron
el paso de CO2 de ahí su Agua purificada
aplicación en el embotellado de Conservas
bebidas gaseosas. Cosméticos
Detergentes y
productos químicos
Tabla 2. Propiedades generales de las principales resinas termoestables. [2]
Principales Resinas Termoestables
Propiedades
Poliésteres
Generales Fenólicas Aminos Epoxi
insaturados
Excelente
resistencia a la
Muy buena
humedad,
Confiere baja resistencia a Buena
ácidos y
QUÍMICAS humedad las grasas resistencia
aceites, no
aceites y química
resiste
ceras
oxidantes
fuertes
Muy buenas Muy buenas Muy buenas Muy buenas
ELÉCTRICAS propiedades propiedades propiedades propiedades
eléctricas eléctricas eléctricas eléctricas
Baja
flamabilidad y
Bajo desempeño a Baja
FLAMABILIDAD baja
altas temperaturas flamabilidad
generación de
humos
Necesita calor Muy versátil,
Muy versátil no hay Necesita
PROCESAMIENTO y presión para no hay
compuestos calor y
el curado compuestos
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 37
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
volátiles durante el presión para volátiles
curado el curado durante el
curado,
excelente
adhesión al
relleno y fibras
Madera, mica, Fibra de Fibra de
REFORZAMIENTOS
hojuelas de Fibra de vidrio vidrio carbono o de
COMUNES
vidrio, fibras. celulosa vidrio.
RESISTENCIA AL
150 105-130 100-130 130
CALOR (°C)
1.3 Cuestionario pre-laboratorio
1. Investigar las propiedades químicas y físicas de los siguientes materiales:
a) Polietilen Tereftalato (PET)
b) Polietileno de alta densidad (PEAD)
c) Cloruro de Polivinilo (PVC)
d) Polietileno de baja densidad (PEBD)
e) Polipropileno (PP)
f) Poliestireno (PS)
2. Escribir el nombre de los siguientes acrónimos.
PS ____________________________________
PVC ___________________________________
PEHD __________________________________
ABS ____________________________________
3. Investigar 3 códigos de identificación de envases plásticos para reciclaje, considerando
producción y aplicaciones.
4. Indicar el nombre de los plásticos de acuerdo a los siguientes números de reciclado:
2 _____________________________________
4 _____________________________________
5 _____________________________________
4. ¿Qué es un copolímero? Mencionar 3 ejemplos de este tipo de materiales.
5. ¿Cuáles serían las posibles modificaciones que se observarían en las propiedades de un material
plástico cuando se introduzca en su estructura un sustituyente como el cloro?
1.4 Desarrollo experimental
a) Medidas de seguridad
Utiliza bata, cubre-bocas y lentes de seguridad.
Manejar con cuidado el mechero de bunsen.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 38
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
b) Materiales
(1) Vasos de precipitados de 250 (1) Mechero Bunsen (1) Agitador de vidrio
mL
(3) Vasos de precipitados de 100 (1) Pinzas para crisol (1) Espátula mango de
mL madera
c) Reactivos
NaCl (cloruro de sodio) H2O (agua destilada)
d) Material que cada equipo debe aportar
1 Botella de agua o refresco (PET)
1 Recipiente de unicel
1 Envase de yogurt o jugo (plástico)
1 Tapa para botella (plástico)
1 Muestra de rafia
1 Muestra de PVC
1 Tijeras
Nota: Todos los recipientes deben estar vacíos y limpios
e) Procedimiento
1. De cada uno los objetos de plástico de muestra cortar un pequeño trozo de aproximadamente 2
cm2.
2. Observar si el material es traslúcido, transparente u opaco.
3. Analizar sus propiedades mecánicas, y a partir de ellas determinar si es rígido, semi-rígido o
flexible.
4. Colocar en vasos de precipitados: (1) 30 mL de agua; (2) 30 mL solución concentrada de NaCl; y
(3) 30 mL solución diluida de NaCl.
5. Analizar la densidad de cada uno de los materiales colocando una pequeña muestra del material
en cada uno de los vasos y registrar sus observaciones.
6. Encender el mechero y realizar las siguientes pruebas:
a) Prueba de combustibilidad (fácil o difícil de incendiar).
b) Duración de la flama.
c) Color de la flama.
d) Color de los humos.
e) Observar si el material fundido gotea o se auto extingue.
f) Describir el olor que se produce durante la combustión del material.
7. Registrar todos los datos experimentales en tablas.
8. Realizar el conjunto anterior de pruebas a las muestras que el profesor te proporcione; tendrás
que identificar el plástico que te fue proporcionada (utiliza la información de la Tabla 2).
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 39
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
9.- Registrar los datos de su muestra en la tabla de datos experimentales.
Tabla de resultados
Duración Color
Densidad Combus Color
Plástico Mecánicas Ópticas flama flama Gotea Olor
relativa -tibilidad humo
(s)
PET
PEAD
PVC
PEAD
PP
PS
Muestra
1.5 Bibliografía
[1] Hernández, L. Heliodoro, Martínez, R. Víctor Manuel, Arrazola, D. Flor del Monte. Transformación
de Termoplásticos, Termofijos y Reciclado. Instituto Politécnico Nacional. México 1996.
[2] Arrazola, D. Flor del Monte, Martínez, V, Elsa. Química y Propiedades de los Polímeros. IPN-
ESIQIE. 5ª Edición. México 2001.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 40
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
9. Óxido – Reducción
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivos
• Comprender las reacciones de oxidación y reducción.
• Comprender las propiedades de las sustancias oxidantes y reductoras.
• Reconocer la tendencia relativa de las especies químicas para oxidarse o reducirse.
• Identificar al agente oxidante y reductor en una reacción redox.
1.2 Fundamento teórico:
El alumno realizará una revisión bibliográfica para proponer el fundamento teórico que da sustento
al trabajo experimental a realizar.
1.3 Cuestionario pre-laboratorio
1. Elabora un cuadro sinóptico para mostrar una clasificación de los diferentes tipos de reacciones
químicas.
2. ¿Qué son los potenciales estándar de reducción y cuál es su utilidad?
3. ¿Cuál es la importancia, a nivel industrial de las reacciones de óxido – reducción?
1.4 Desarrollo experimental
a) Medidas de seguridad
Utilizar bata
Utilizar cubre-bocas, lentes de seguridad y guantes
Manejar ácidos en campana de extracción
b) Materiales
Espátula metálica 1
Gradilla 1
Pinzas para tubo de ensayo 2
Tubos de ensayo 13x100 10
Pipeta Pasteur de plástico 2
Piseta 1
Probeta de 50 mL 1
Matraz Erlenmeyer de 250 mL 2
Vaso de precipitados de 100 mL. 2
Embudo de vidrio talle corto 1
Vaso de precipitados de 250 mL 1
Charola de aluminio 2
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 41
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
c) Reactivos
Disolución de bicarbonato de sodio (25% p/p) Disolución de ácido sulfúrico (5% v/v)
Alambre de cobre
Zinc en polvo
Ácido nítrico concentrado
Magnesio (en tira)
Aluminio (en hoja)
Disolución de ácido clorhídrico 1 M
Disolución de nitrato de plata 0.2 M
Disolución de nitrato de magnesio 0.2 M
Disolución de nitrato de cobre 0.2 M
Papel filtro
e) Procedimiento
Parte I. Reacciones de desplazamiento de hidrógeno (opcional)
1. Numera y etiqueta tres tubos de ensayo.
2. Coloca en cada uno de ellos una pequeña pieza del metal indicado en la Tabla 1.
3. Añade a cada uno de los tubos de cinco a diez gotas de disolución de ácido clorhídrico 1M.
4. Agita los tubos en forma circular y advierte si ocurre alguna reacción. Cuando estas
reacciones se llevan a cabo, se manifiestan cambios en el aspecto de la superficie de los
metales y se observa desprendimiento de gas.
5. Anota tus observaciones y los resultados en la Tabla 2.
Tabla 1.
Tubo No. Metal Ion Disolución
1 Mg H+ HCl
2 Zn H+ HCl
3 Cu H+ HCl
Resultados
Tabla 2.
Tubo No. Observaciones Agente oxidante Agente reductor
1
2
3
Parte II. Reacciones de desplazamiento de un metal (opcional)
1. Numera y etiqueta tres tubos de ensayo.
2. Coloca en cada uno de ellos una pequeña pieza del metal que se indica en la Tabla 3.
3. Añade a cada uno de los tubos de cinco a diez gotas de la disolución indicada.
4. Agita los tubos en forma circular y advierte si ocurre alguna reacción. Cuando estas
reacciones se llevan a cabo, se manifiestan cambios en el aspecto de la superficie de los
metales, cambios en la coloración de las disoluciones y también se puede observar la
formación de algún precipitado.
5. Anota tus observaciones y los resultados en la Tabla 4.
6. Al finalizar el experimento coloca las mezclas en el correspondiente frasco para residuos.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 42
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Tabla 3.
Tubo No. Metal Ion Disolución
1 Mg Cu2+ Cu(NO3)2
2 Cu Ag+ AgNO3
3 Zn Cu2+ Cu(NO3)2
Resultados
Tabla 4.
Tubo No. Observaciones Agente oxidante Agente reductor
1
2
3
Parte III. Serie de reacciones redox de un metal
1. Coloca de 0.1 a 0.2 g de cobre en un vaso de precipitado de 100 mL y agrega 2mL HNO3.
Realiza este procedimiento en un lugar con buena ventilación.
2. Agregar 25 mL de solución de bicarbonato de sodio al 25% en peso, hasta la formación de
un precipitado de color azul.
3. Filtrar la disolución anterior, conservando el precipitado y desechando la disolución.
4. Al precipitado se le agregan 20 mL de solución de ácido sulfúrico al 5% en volumen, hasta
que reaccione y se recibe en un vaso de 100 mL.
5. A la solución obtenida se le agregan de 0.1 a 0.2 gramos de zinc en polvo y se agita
continuamente hasta la formación de un precipitado de color rojo ladrillo o café.
1.5 Resultados
Anota todas tus observaciones con respecto a la siguiente serie de reacciones.
a) Cu + HNO3 → Cu(NO3)2 + NO + H2O
b) Cu(NO3)2 + NaHCO3 → CuCO3 + CO2 + NaNO3 + H20
c) CuCO3 + H2SO4 → CuSO4 + CO2 + H2O
d) CuSO4 + Zn → Cu + ZnSO4
Para cada una de las reacciones indica, ¿cuál es el elemento que se oxida y cuál es el elemento que
se reduce? Balancear cada ecuación.
1.6 Conclusiones
Como guía para que prepares el apartado de conclusiones obtenidas a partir del trabajo experimental
realizado, discute si se alcanzaron los objetivos propuestos.
Compara los resultados experimentales con los teóricos.
1.7 Referencias
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 43
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
[1] Brown T., LeMay E., Burnsten B. Química La Ciencia Central. Novena Edición Prentice Hall, México
2004.
[2] Garritz, A., Chamizo, J.A. Química. Addison-Wesley Iberoamericana. USA 1994.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 44
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
10. Celdas Voltaicas
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivo
Reconocer un proceso redox a través de la construcción de una celda voltaica húmeda.
1.2 Fundamento teórico
Las celdas voltaicas son dispositivos que manejan la energía liberada durante la reacción de óxido-
reducción que se produce de manera espontánea, en el cual la transferencia de electrones tiene lugar
a lo largo de un camino externo, y no directamente entre los reactivos [1]. Cualquiera que sea el
medio que se utiliza para permitir la migración de iones entre las celdas, los aniones migran con
dirección hacia el ánodo, y los cationes hacia el cátodo. No se presentará un flujo electrónico
mensurable entre los electrodos a menos que se provea un medio para que los iones se desplacen a
través de la disolución de un compartimiento de electrodo al otro, con lo cual se completa el circuito.
Por lo tanto, en toda celda voltaica, los electrones fluyen desde el ánodo por el circuito externo hacia
el cátodo. Debido a que los electrones con carga negativa fluyen del ánodo al cátodo, el ánodo de
una celda voltaica se rotula con un sigo negativo, y el cátodo con un signo positivo [2,3].
Para generar una reacción de este tipo podemos colocar un trozo de zinc metálico (Zn°) en una
solución de sulfato de cobre II (CuSO4); una capa de color rojo ladrillo y de aspecto esponjoso
empezará a formarse sobre el trozo de Zn. Al mismo tiempo, el color azul de la solución de CuSO 4
comenzará a ser cada vez más tenue, tornándose de color celeste suave. La substancia rojiza es
cobre metálico (Cu°) y las semi-reaciones que ocurren son:
Se puede observar de estas semirreacciones que los iones Cu +2 son removidos de la solución y son
reemplazados por los iones Zn+2 que son incoloros. Por consiguiente, el color azul desaparece de la
solución y cada vez se forman más iones Zn+2.
A medida que ocurre esta reacción espontánea no se puede aprovechar la energía liberada del flujo
de electrones. La reacción simplemente genera calor. Sin embargo se puede aprovechar el flujo de
electrones que acompaña a esta reacción de óxido-reducción si se separa la solución de ión Cu+2 de
la de Zn+2, colocándolas en celdas como la que se observa en la Figura 1.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 45
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Figura 1. Diagrama de una celda voltaica [2].
En un sistema como el que se muestra en la Figura 1, los e- producidos por la oxidación de Zn° deben
pasar a través del alambre conductor y llegar al electrodo que está en la solución de CuSO 4. Los e-
son captados por los iones Cu+2 y se realiza la reducción a Cu°. El flujo de electrones que circula por
el alambre externo provee de electricidad. Si bien Zn y Cu deben estar separados para obtener un
flujo útil de e-, el aislamiento completo de las dos semiceldas del sistema conducirá a un desequilibrio
de las cargas en cada uno de los electrodos y el flujo de e - cesaría pronto. Si las dos semiceldas
estuviesen totalmente aisladas y las reacciones de oxidación y reducción siguieran ocurriendo,
sucedería lo siguiente:
• Los iones Zn+2 provenientes de la disolución de la barra de Zn provocarían que la carga total de
esta solución fuese de carga (+). Esta carga (+) de la solución evitaría una posterior formación de
ión Zn+2.
• En la otra semicelda encontraríamos que cuando Cu +2 abandona la solución por transformarse en
Cu°, los iones SO4-2 provocarían que esta solución tuviese carga (-) lo que también evitaría la posterior
transformación de ión Cu+2 a Cu°.
Un flujo continuo de corriente, acompañado con una actividad química continua se realizará sólo si
se mantiene la neutralidad eléctrica en ambas semiceldas. Una forma de mantener la neutralidad
eléctrica es permitir que los iones pasen de un compartimento a otro, pero el flujo de iones no sería
tan rápido en comparación con la velocidad de las semirreacciones [1]. Un puente salino permite la
mezcla de los iones en ambas soluciones. El puente salino es generalmente un tubo lleno con un
electrolito fuerte tal como KCl o KNO3 mezclado con un soporte inerte como gelatina o algun material
poroso que permita el intercambio de los iones, como el algodón. Los cationes del puente salino se
mueven a uno de los compartimentos para compensar el exceso de cargas negativas; mientras que
los aniones del puente salino difunden al otro compartimento para neutralizar el exceso de cargas
positivas. Con lo cual, se permite un flujo continuo, tanto de los electrones a través del alambre
externo como de los iones en la solución, mientras transcurren las reacciones redox.
Los signos de los electrodos en las celdas voltaicas.
En el electrodo llamado ánodo es donde ocurre la oxidación y el electrodo donde se realiza la
reducción se llama cátodo. En la celda de nuestro ejemplo, la oxidación se realiza en el compartimento
de Zn. Por consiguiente, la barra de Zn es el ánodo y el electrodo de Cu será el cátodo, porque es
donde ocurre la reducción. Ya que los electrones son liberados (oxidación) al ánodo y extraídos del
cátodo de Cu (reducción), la barra de Zn posee un exceso de electrones comparado con la barra de
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 46
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Cu. Como resultado, tenemos que la barra de Zn es el electrodo negativo (−) y Cu es el electrodo
positivo (+). Lo cual significa, que en las celdas voltaicas, el ánodo es (−) y el cátodo es (+). Todo
lo contrario a la electrólisis.
Potencial de la celda.
La corriente eléctrica se obtiene como resultado del flujo de electrones por el alambre conductor
desde el electrodo negativo al positivo. La fuerza con que se mueven estos electrones por el alambre
se llama fuerza electromotriz o fem y se mide en Volts. Si la fem es de 1 Volt, el paso de 1 Coulomb
de corriente eléctrica es capaz de realizar 1 Joule de trabajo:
La fem de cualquier celda galvánica depende de la naturaleza de las especies químicas involucradas,
de las concentraciones de las especies que se reducirán como de las que se oxidarán y la temperatura
de la celda. A mayor tendencia o potencial de ambas semirreacciones para que ocurran
espontaneamente, mayor será la fem de la celda. Así, la fem de la celda puede llamarse también
potencial de la celda y se designa por el símbolo Ecelda.
1.3 Cuestionario pre-laboratorio
1. ¿Qué es una pila?
2. ¿Cuáles son los tipos de pilas que se pueden construir y cuál es la aplicación de cada uno? Utiliza
diagramas para mostrar la composición de cada tipo de pila.
1.4 Desarrollo experimental
a) Medidas de seguridad
Utilizar bata, cubre-bocas, guantes y lentes de seguridad
Manejar ácidos en campana de extracción y utilizar guantes
b) Material
6 vasos de precipitados de 250 mL
4 vasos de precipitados de 100 mL
2 agitadores de vidrio
1 espátula
1 electrodo de zinc
1 tubo o placa de cobre para electrodo
1 tubo o placa de aluminio para electrodo
1 juego de caimanes
1 trozo de manguera de nivel, de 15 a 20 cm
c) Reactivos
Sulfato de cobre
Cloruro de sodio
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 47
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Nitrato de potasio
Ácido acético (vinagre comercial)
Algodón
d) Equipo
1 Multímetro
e) Secuencia experimental
Experiencia I
1. Elabora el puente salino necesario para comunicar las soluciones de los electrodos, para hacer
esto, llena el trozo de manguera con una solución saturada de nitrato de potasio, tapando los
extremos con algodón; procura que no queden burbujas de aire.
2. Conecta cada uno de los electrodos con los caimanes.
3. Para el cátodo, introduce el electrodo de cobre, en una solución de sulfato de cobre concentrado.
4. Para el ánodo, introduce el electrodo de aluminio en una solución de vinagre.
5. Introduce cada uno de los extremos del trozo de manguera que contiene la solución de nitrato de
potasio, en las soluciones con los electrodos (Figura 1).
6. Conecta los extremos de los caimanes al multímetro y mide el voltaje.
7. ¿Consideras que el potencial producido puede encender una lámpara o led? Compruébalo.
Experiencia II
Repite la experiencia I realizando tu propia mezcla de soluciones y electrodos, para ello puedes
basarte en la información proporcionada en la Tabla I.
Tabla 1. Posible combinaciones de electrodos y soluciones para obtener celdas voltaicas [1].
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 48
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Mg Ag
1.5 Resultados
Reporta en el cuadro siguiente los resultados obtenidos con las diferentes celdas voltaicas
construidas.
solución
cátodo ánodo solución ánodo Ecelda
cátodo
Cobre Aluminio Sulfato de cobre vinagre
Comenta todas tus observaciones y discute los puntos siguientes:
1. ¿Cuál sería el potencial de celda sin la utilización del puente salino?
2. ¿Qué modificaciones realizarías a la celda voltaica que construiste para aumentar el potencial de
celda?
3. ¿Cuál sería el tipo de electrodos más adecuados para construir una celda voltaica?
4. ¿Qué sucedería con el potencial de celda si se agregan soluciones de diferente concentración?
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 49
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
5. ¿Qué sucedería con el potencial de celda si se agrega la misma solución a en el ánodo y el cátodo,
por ejemplo, cloruro de sodio?
1.6 Conclusiones
Las siguientes preguntas te ayudaran a realizar tus conclusiones:
¿Se cumplió el objetivo de la práctica?
¿Es importante el material del electrodo utilizado y el tipo de solución para el funcionamiento de la
celda voltaica? ¿Todas las celdas construidas generan un voltaje semejante?
1.7 Bibliografía
[1]. Santiago Heredia-Avalos, Experiencias divertidas de electroquímica casera, Rev. Eureka. Enseñ.
Divul. Cien., 2007, 4(3), pp. 506-525.
[2]. Brown, Química, la ciencia central, Novena edición, Pearson Prentice. 2004.
[3]. Ebbing, Química General, Quinta edición McGraw Hill.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 50
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
11. Recubrimiento Electrolítico
Lugar de realización: Laboratorio de Química 1, Laboratorio Química 2
Duración: 1.5 h
1.1 Objetivos
• Construir una celda electrolítica y efectuar un electrodepósito de cobre. Comprender el
funcionamiento de la celda.
• Reconocer la importancia de los procesos electroquímicos y sus aplicaciones.
• Comprender conceptos básicos de electroquímica.
1.2 Fundamento teórico
Al colocar un electrodo negativo en una cubeta electrolítica, éste se revestirá de capas de metal en
solución. Este proceso denominado galvanoplastia (en homenaje a Galvani, físico italiano que estudió
algunos fenómenos eléctricos), es utilizado para platear, cromar, niquelar, y cobrear diversos objetos.
Recubrimiento de cobre
El cobre forma la primera capa en un sistema de capas de recubrimiento, debido a que es fácil de
depositar en metales, por su elevada conductividad; la capa de cobre es muy resistente, económica
de aplicar y forma una buena base adhesiva para otros metales. En un baño ácido, el sulfato de cobre
CuSO4 representa la fuente de iones de cobre que se deposita en la superficie a recubrir. Para este
proceso se recomienda sulfato de cobre químicamente puro. El baño de cobre típico contiene sulfato
de cobre, ácido sulfúrico, iones de cloruro y aditivos de brillo.
El ácido sulfúrico sirve para aumentar la conductividad de la solución y para facilitar en cierta medida
la oxidación del ánodo de cobre; el ánodo proporciona los iones de cobre que se incorporan a la
solución. El proceso de cobre ácido se realiza a una temperatura entre 20 y 30 ° C.
En la Figura 1 se representa la disociación del sulfato de cobre en iones Cu++ y SO4--. En la disociación
del átomo de cobre transfiere dos electrones. En la electrólisis de esta sal, el ion cobre se dirige al
electrodo negativo, pierde la carga y se deposita. El ion SO4-- va al ánodo, y entonces reacciona con
agua produciendo H2SO4 y desprendiendo oxígeno.
Si se coloca como electrodo negativo un objeto cualquiera, éste se recubrirá de una capa de cobre,
es decir quedará cobrizado.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 51
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Figura 1 Celda de electrólisis.
Las reacciones para este tipo de recubrimiento son del tipo óxido-reducción y se muestran a
continuación.
Primero el sulfato de cobre se disocia:
CuSO4 → Cu 2 + + SO42 −
La oxidación de Cu° a Cu2+ se efectúa en el ánodo:
Cu → Cu 2 + + 2e
Posteriormente los iones Cu2+ se desplazan en la solución para finalmente llegar al cátodo donde se
reducen en la superficie catódica en Cu° metálico.
Cu 2 + + 2e → Cu
Antes de realizar el cobreado hay que darle algun tratamientos al material a recubrir con la finalidad
de tener un recubrimiento de buena calidad.
Los métodos mecánicos incluyen principalmente el esmerilado y pulido. Estos pasos de trabajo
eliminan asperezas o deformaciones superficiales de la pieza. El método para eliminar el aceite y la
grasa de una superficie es el desengrasado a vapor. Consiste en calentar un solvente limpiador,
generalmente hidrocarburos clorados, para obtener una fase de vapor caliente, en la que se
introducen las piezas.
El contacto entre la atmósfera y las piezas metálicas provoca la formación de capas de óxido, que
tienen que ser eliminadas antes del recubrimiento electrolítico. El decapado con ácido se utiliza para
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 52
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
eliminar impurezas y óxidos a través de un ataque químico, el cual frecuentemente se aplica después
de un lavado alcalino. Se utilizan diferentes ácidos, solos o mezclados, entre ellos se encuentran el
ácido nítrico, ácido sulfúrico, ácido clorhídrico, ácido fluorhídrico y ácido fosfórico con concentraciones
de aproximadamente 2 % en volumen.
El proceso de activado, también llamado neutralizado e inclusive decapado suave, se utiliza para
eliminar la pequeña capa de óxido que se ha formado sobre la superficie del metal una vez que la
superficie ha sido tratada o lavada en sucesivas etapas. Esa pequeña capa de óxido hace que la
superficie sea pasiva y por lo tanto mal conductora. Las soluciones empleadas son por lo general
ácidos muy diluidos.
1.3 Cuestionario pre-laboratorio
1. ¿Qué es una celda electrolítica?
2. Describir cada uno de los componentes de una celda electrolítica.
3. Describir cada una de las leyes de Faraday.
4. Investigar los principales procesos de recubrimiento utilizados en la industria y mencionar
un par de aplicaciones de cada uno de ellos.
1.4 Desarrollo experimental
a) Medidas de seguridad
Utilizar bata, cubre-bocas, lentes y guantes de seguridad
Manejar ácidos en campana de extracción
b) Materiales
Vaso de precipitados de 250 mL (1)
Piseta (1)
Caimanes (2)
Pila de 9 volts (1)
Tubo de cobre (10 cm) de 1/2 pulgada (1)
Hierro galvanizado (clavo de 2 ½ pulgadas) (1)
Pinzas para crisol (1)
Charola de aluminio (1)
Papel filtro
Lija
c) Reactivos
Disolución de ácido clorhídrico al 5%
Disolución de sulfato de cobre al 5%
Etilenglicol
Disolución de HCl 1 M
Agua destilada
d) Equipo
Balanza analítica
Multímetro
Horno (estufa)
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 53
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
e) Procedimiento
1. Lija el tubo de cobre de aproximadamente 10 cm de longitud para quitar cualquier
impureza presente en su superficie. Este tubo será el ánodo de la celda electroquímica.
2. Prepara la superficie del electrodo de hierro (clavo) lijando ligeramente la superficie a
cobrear. Limpia perfectamente el clavo, colócalo en una charola de aluminio, determina
y registra su peso.
3. Coloca por un periodo de tiempo de 10 minutos el clavo limpio en disolución de HCl al
5% (proceso de decapado), para eliminar residuos de óxidos.
4. Una vez transcurridos los 10 minutos, retira el clavo y enjuágalo con agua destilada.
5. Transfiere de 10 a 15 mL de disolución de sulfato de cobre al 5% al vaso de precipitados
(esta disolución será el electrolito de la celda). Añade una gota de ácido sulfúrico 1M a
la disolución para aumentar su conductividad eléctrica. Por último agrega 3 gotas de
etilenglicol a la disolución, para dar un poco de brillo al recubrimiento metálico.
6. Monta la celda de electrólisis de acuerdo a la guía proporcionada por la Figura 1. El clavo
de hierro es el cátodo y el tubo de cobre es el ánodo. Los electrodos no se deben tocar.
7. Por medio de los caimanes, conecta los electrodos a una pila de 9 V o a un eliminador
de baterías. El tubo de cobre, por ser el ánodo de la celda, se conecta al polo positivo de
la pila y el clavo, por ser el cátodo de la celda, se conecta al polo negativo.
8. Deja conectada la pila entre 2 y 5 minutos para permitir el paso de la corriente eléctrica
(electrólisis) hasta que el clavo tenga un recubrimiento fino de cobre. Con el multímetro,
mide la intensidad de la corriente eléctrica transmitida. Registra el tiempo exacto que la
corriente pasó a través de la celda.
9. Desconecta la pila. Sujetando el clavo con el caimán, colócalo en la charola de aluminio
(evita tocarlo). Con unas pinzas para crisol, introduce la charola de aluminio con el clavo
en un horno a 100ºC para secarlo durante 5 minutos.
10. Con las pinzas para crisol, retira la charola de aluminio del horno, déjala sobre la mesa
de trabajo y permite que se enfríe a temperatura ambiente.
11. Pesa la charola con el clavo y registra el dato.
12. Lava con agua el electrodo de cobre antes de entregarlo.
13. Coloca el residuo de la disolución de sulfato de cobre en el recipiente indicado.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 54
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
14. Después de 24 horas se puede pulir el cobreado, frotando la pieza suavemente con papel
filtro.
1.5 Resultados:
Peso de la charola de aluminio con el clavo: ____________________________________________
Peso de la charola de aluminio con el clavo recubierto de cobre: ____________________________
Peso del cobre depositado sobre el clavo: ______________________________________________
Intensidad de la corriente eléctrica transferida: _________________________________________
Tiempo que la corriente eléctrica pasó a través de la celda: ________________________________
Análisis de resultados (DEBERÁ INCLUIRSE EN EL REPORTE):
1. Aplica la ley de Faraday para calcular la cantidad teórica de cobre que se puede depositar
durante este proceso de electrólisis.
a) Determinación del número de faradays que se deben transferir en el proceso
de electrólisis para obtener un mol de cobre:
Semirreacción de reducción: Cu2+(ac) + 2e- → Cu(s)
Al transferir 2 moles de electrones se reduce 1 mol de iones Cu2+ y se produce 1 mol de
Cu.
Al transferir 2 faradays se deposita 1 mol de Cu.
b) Determinación del número de faradays (F) que fueron transferidos durante el
proceso de electrólisis:
Fórmula: F = A x t x (1F/96 500 C)
F = número de faradays transferidos durante el proceso.
A = intensidad de la corriente eléctrica (amperes).
t = tiempo (segundos) que la corriente eléctrica pasó a través de la celda.
Factor de conversión: 1 ampere (A) = 1 coulumb (C) / segundo (s)
Datos experimentales:
Intensidad de la corriente eléctrica transferida: ________________________________
Tiempo en segundos que la corriente eléctrica pasó a través de la celda: ___________
Cálculos:
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 55
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Resultado: F= _______________________
c) Determinación de la cantidad teórica de cobre que se debía depositar durante
este proceso de electrólisis.
Recordar que al transferir 2 faradays se deposita 1 mol de cobre. Considerar el número
de faradays que fueron transferidos durante este proceso de electrólisis y determinar
cuántos moles y cuántos gramos de cobre se debían depositar.
Resultado:
____________________________________ mol de Cu(s).
____________________________________ g de Cu(s).
2. Compara la cantidad de cobre depositada sobre el clavo con la cantidad teórica calculada;
¿coinciden? Si existe alguna variación, ¿a qué factores lo atribuyes?
3. ¿En qué momento se inicia el proceso de electrólisis?
4. Indica cuáles son las reacciones (balanceadas) que se efectuaron en la celda electroquímica
durante el proceso.
Ánodo (oxidación): __________________________________________________________
Cátodo (reducción): _________________________________________________________
Reacción global: ____________________________________________________________
1.6 Referencias
[1] Brown, T., LeMay E., Burnsten B., Química La Ciencia Central, 9ª. ed., Prentice Hall, México,
2004.
[2] Cervantes, B., y Ballinger, J., Chemical Technicians Reference Handbook, 1ª. ed., Trillas, México,
2011.
[3] Chang, R., Chemistry, 9ª. ed., McGraw-Hill, Nueva York, 2007.
[4] Gershon, J., Loredo, J., Manual de prácticas de química general en microescala, 3ª. Ed., McGraw-
Hill, Nueva York, 1990.
[5] Moore, J., Stanitski, C., Kotz, J., Joesten, M. y Wood, J., El mundo de la química. Conceptos y
aplicaciones, Prentice Hall, México, 2000.
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 56
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Anexo 1. Rúbrica de Bitácora
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 57
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Anexo 2. Rúbrica de Reporte
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 58
Laboratorio de:
Química Básica para Sistemas
Manual de Prácticas Automotrices y Aeronáutica
Anexo 3. Tabla General de Propiedades de Polímeros
Unidad Profesional Interdisciplinaria de Ingeniería Campus Guanajuato Página 59
También podría gustarte
- Manual Q. Basica 19Documento59 páginasManual Q. Basica 19Lira ayala Salvador AndresAún no hay calificaciones
- Manual Química Orgánica I IQ QOI 2019-II PDFDocumento58 páginasManual Química Orgánica I IQ QOI 2019-II PDFJose Emmanuel ChemaAún no hay calificaciones
- Manual Prácticas Quimica General - 2013Documento172 páginasManual Prácticas Quimica General - 2013Derek MAún no hay calificaciones
- Manual de Laboratorio QUIM 002 2023Documento62 páginasManual de Laboratorio QUIM 002 2023Texia DominguezAún no hay calificaciones
- Reconocimiento de materiales y normas de seguridad en laboratorio virtual de química generalDocumento51 páginasReconocimiento de materiales y normas de seguridad en laboratorio virtual de química generalVanessa SernaAún no hay calificaciones
- Manual de Laboratorio de Química Inorgánica2Documento73 páginasManual de Laboratorio de Química Inorgánica2mariapaniagua83Aún no hay calificaciones
- Manual de Practicas QO I IQ 2023-IDocumento60 páginasManual de Practicas QO I IQ 2023-IAlfonso BuendiaAún no hay calificaciones
- Trabajos Practicos Laboratorio Qca. Gral. Revisión 2023Documento44 páginasTrabajos Practicos Laboratorio Qca. Gral. Revisión 2023manuel19941Aún no hay calificaciones
- Informe ElectronicaDocumento3 páginasInforme ElectronicaMigue Vega CAún no hay calificaciones
- Practica de Laboratorio de Qui Mica Orgánica.Documento70 páginasPractica de Laboratorio de Qui Mica Orgánica.edwinAún no hay calificaciones
- Laboratorios de Quimica General 1Documento63 páginasLaboratorios de Quimica General 1Miguel Melillo100% (2)
- Índice:: Química IiDocumento95 páginasÍndice:: Química IiNoelia Linet Arevalo HernandezAún no hay calificaciones
- Laboratorio de Química Inorgánica (I-2022)Documento7 páginasLaboratorio de Química Inorgánica (I-2022)Mishel MijaresAún no hay calificaciones
- Protocolo de Práctica de Laboratorio de Química GeneralDocumento50 páginasProtocolo de Práctica de Laboratorio de Química GeneralAmanda SierraAún no hay calificaciones
- Laboratorio Virtual Química GeneralDocumento51 páginasLaboratorio Virtual Química GeneralJhan LiscanoAún no hay calificaciones
- Practica VirtualDocumento42 páginasPractica VirtualAngii BenavidesAún no hay calificaciones
- Manual de Prácticas de Fisicoquímica UAEMDocumento52 páginasManual de Prácticas de Fisicoquímica UAEMAxel ColinAún no hay calificaciones
- Manualquimica 17-18-1 CV, IMT, EMI, ISCDocumento49 páginasManualquimica 17-18-1 CV, IMT, EMI, ISCRicardo Hernández ReyesAún no hay calificaciones
- Manual de Técnología de Laboratorio Químico 2S 2018Documento85 páginasManual de Técnología de Laboratorio Químico 2S 2018gabrielaAún no hay calificaciones
- Manual Fisicoquimica IiDocumento34 páginasManual Fisicoquimica Iiricardo sanchesAún no hay calificaciones
- Manual Operaciones Unitarias 2 2022Documento57 páginasManual Operaciones Unitarias 2 2022Armando GuerreroAún no hay calificaciones
- Manual Lab FisicoquimicaDocumento56 páginasManual Lab FisicoquimicaFernando EsquivelAún no hay calificaciones
- Protocolo Virtual JUAN JOSE OVIEDODocumento41 páginasProtocolo Virtual JUAN JOSE OVIEDOJuan jose BaronaAún no hay calificaciones
- Manual Laboratorio Quimica II Interciclo 2022Documento40 páginasManual Laboratorio Quimica II Interciclo 2022holahola edededeAún no hay calificaciones
- Guia Actualizada 2018 de Ciencias I 1Documento198 páginasGuia Actualizada 2018 de Ciencias I 1alx rivroAún no hay calificaciones
- Laboratorio Química Orgánica IDocumento4 páginasLaboratorio Química Orgánica IAdiel PerezAún no hay calificaciones
- Quimicaanaliticaaplicada ManualpracDocumento110 páginasQuimicaanaliticaaplicada ManualpracIngeniero QuimicoAún no hay calificaciones
- Manual LFQ IQ Ene2022Documento78 páginasManual LFQ IQ Ene2022GARCIA GAMEZ JORGE ABRAHAMAún no hay calificaciones
- Materiales y seguridad en el laboratorio de químicaDocumento45 páginasMateriales y seguridad en el laboratorio de químicaJeniffer Juliana Toro OrtegaAún no hay calificaciones
- Manual de Prácticas Ingenieros Quimicos 2021aDocumento60 páginasManual de Prácticas Ingenieros Quimicos 2021aRAFAEL OCTAVIO SANCHEZAún no hay calificaciones
- Captura de Pantalla 2023-09-19 A La(s) 1.10.46Documento71 páginasCaptura de Pantalla 2023-09-19 A La(s) 1.10.46Jecsan Mendoza velazquezAún no hay calificaciones
- Guía de Prácticas 2018A PLCsDocumento66 páginasGuía de Prácticas 2018A PLCsPatricioAlexanderNajeraAún no hay calificaciones
- Protocolo de Práctica de Laboratorio de Química GeneralDocumento50 páginasProtocolo de Práctica de Laboratorio de Química GeneraldangerAún no hay calificaciones
- Manual Química Heterocíclica UNAMDocumento59 páginasManual Química Heterocíclica UNAMLorena MedinaAún no hay calificaciones
- Manual Métodos de SeparaciónDocumento77 páginasManual Métodos de SeparaciónFrancisco ArriagaAún no hay calificaciones
- Universidad de La Sabana Facultad de IngDocumento39 páginasUniversidad de La Sabana Facultad de Ingdaniel gameroAún no hay calificaciones
- Guía Práctica Laboratorio QuímicaDocumento49 páginasGuía Práctica Laboratorio QuímicaAlejandra Peña duranAún no hay calificaciones
- Protocolo VirtualDocumento57 páginasProtocolo VirtualKRAZY NETAún no hay calificaciones
- Manual Citogenetica HumanaDocumento108 páginasManual Citogenetica HumanaPab Ari FueAún no hay calificaciones
- Cuadernillo de Prácticas de Lab 2017 Ing IndustrialDocumento60 páginasCuadernillo de Prácticas de Lab 2017 Ing IndustrialAnonymous VJrftqvOQAún no hay calificaciones
- Man Qo Iv QDocumento94 páginasMan Qo Iv QJonathan C Montealegre0% (1)
- Mediciones y métodos de uso común en el laboratorio de QuímicaDe EverandMediciones y métodos de uso común en el laboratorio de QuímicaCalificación: 4.5 de 5 estrellas4.5/5 (3)
- Guía Laboratorio Química IDocumento24 páginasGuía Laboratorio Química IGiovanni José PedroAún no hay calificaciones
- Manual LFQ IQ Ene2023Documento82 páginasManual LFQ IQ Ene2023JIhhh WanAún no hay calificaciones
- Manual de Quimica 530Documento18 páginasManual de Quimica 530xime cervantesAún no hay calificaciones
- Protocolo VirtualDocumento42 páginasProtocolo VirtualJohana MoralesAún no hay calificaciones
- Protocolo Virtual Componente PracticoDocumento44 páginasProtocolo Virtual Componente PracticoYaddy RamosAún no hay calificaciones
- Materiales y seguridad en el laboratorioDocumento37 páginasMateriales y seguridad en el laboratorioLaura Melissa esAún no hay calificaciones
- Manual de Fenómenos de Transporte IIDocumento54 páginasManual de Fenómenos de Transporte IIClaudia SilvaAún no hay calificaciones
- Guía Lab QM2487 Version Octubre 2013 Hasta Practica 7Documento42 páginasGuía Lab QM2487 Version Octubre 2013 Hasta Practica 7Adolfo LizardoHeiferAún no hay calificaciones
- Introducción Al Laboratorio INO2Documento6 páginasIntroducción Al Laboratorio INO2Mary Carmen LicuonaAún no hay calificaciones
- Normatividad laboratorio bioquímica clínicaDocumento66 páginasNormatividad laboratorio bioquímica clínicaJocelyn IslasAún no hay calificaciones
- Guía Lab-Qm-Org-IDocumento70 páginasGuía Lab-Qm-Org-IMORALES PAREDES FAVIO ALEJANDROAún no hay calificaciones
- Manual Mecanica de Materiales Enero2019Documento99 páginasManual Mecanica de Materiales Enero2019Manuel SaldañaAún no hay calificaciones
- Laboratorios Virtuales de Quimica Grado 10Documento35 páginasLaboratorios Virtuales de Quimica Grado 10Jeisson GalvisAún no hay calificaciones
- Manual-Química Orgánica IDocumento40 páginasManual-Química Orgánica IUlises Carrillo MedranoAún no hay calificaciones
- Manual Lab Mecanica Fluidos 2022Documento90 páginasManual Lab Mecanica Fluidos 2022Claudia SilvaAún no hay calificaciones
- Toma de muestras y análisis in-situ. QUIE0108De EverandToma de muestras y análisis in-situ. QUIE0108Aún no hay calificaciones
- Fisicoquímica experimental para sistemas coloidales con aplicación industrialDe EverandFisicoquímica experimental para sistemas coloidales con aplicación industrialAún no hay calificaciones
- Confianza en Si MismooDocumento8 páginasConfianza en Si MismoojavierAún no hay calificaciones
- El Sentido Historico de La Filosofia Parte 1Documento22 páginasEl Sentido Historico de La Filosofia Parte 1javierAún no hay calificaciones
- El RenacimientoDocumento24 páginasEl RenacimientojavierAún no hay calificaciones
- Contrato Individual de Trabajo Por Tiempo Indeterminado 2Documento3 páginasContrato Individual de Trabajo Por Tiempo Indeterminado 2javierAún no hay calificaciones
- Guía Bitácora Química BásicaDocumento3 páginasGuía Bitácora Química BásicajavierAún no hay calificaciones
- CBTIS 60 Bachillerato TecnológicoDocumento5 páginasCBTIS 60 Bachillerato TecnológicojavierAún no hay calificaciones
- Tesis Jose Carlos UrrozDocumento137 páginasTesis Jose Carlos UrrozjavierAún no hay calificaciones
- Una Revisión Del Uso Del Hidrógeno en Motores de Encendido Por Compresión (Diésel) y Un Análisis de Su Posible Uso en Motores Duales en ColombiaDocumento21 páginasUna Revisión Del Uso Del Hidrógeno en Motores de Encendido Por Compresión (Diésel) y Un Análisis de Su Posible Uso en Motores Duales en ColombiajavierAún no hay calificaciones
- Tesis Jose Carlos UrrozDocumento137 páginasTesis Jose Carlos UrrozjavierAún no hay calificaciones
- TFG SantiagoGarciaPrieto2Documento153 páginasTFG SantiagoGarciaPrieto2javierAún no hay calificaciones
- Informe de Laboratorio Nº3 - Gravedad EspecificaDocumento7 páginasInforme de Laboratorio Nº3 - Gravedad EspecificaLucy Anais QuicañaAún no hay calificaciones
- Digrama de Flujo MDocumento3 páginasDigrama de Flujo MJose galindez cruzAún no hay calificaciones
- La ASTM G4Documento5 páginasLa ASTM G4SOSA PALACIOS HECTOR IVAN UTAAún no hay calificaciones
- Balance de EnergiaDocumento15 páginasBalance de EnergiaEric GonzalezAún no hay calificaciones
- Practica 2 (Equipos de Laboratorio)Documento40 páginasPractica 2 (Equipos de Laboratorio)pmschambillacAún no hay calificaciones
- Metabolitos SecundariosDocumento21 páginasMetabolitos SecundariosJoffre Wladimir Cerda GrefaAún no hay calificaciones
- TAJEOSDocumento27 páginasTAJEOSJose IglesiasAún no hay calificaciones
- Química IDocumento3 páginasQuímica IFasit0uAún no hay calificaciones
- Tarifas laboratorio estudios especiales 2015Documento7 páginasTarifas laboratorio estudios especiales 2015Bryam EspinozaAún no hay calificaciones
- Segunda Eval Teoria Ia - 2020Documento1 páginaSegunda Eval Teoria Ia - 2020Norman Morales MontañoAún no hay calificaciones
- 5° S17 CUADERNILLO DE ACTIVIDADES ? Esmeralda Te Enseña ? ANEXOSDocumento16 páginas5° S17 CUADERNILLO DE ACTIVIDADES ? Esmeralda Te Enseña ? ANEXOSID TlaxAún no hay calificaciones
- Cerámicas-Definición, Historia, Usos y Comparación con MetalesDocumento4 páginasCerámicas-Definición, Historia, Usos y Comparación con MetalesJeffry Trujillo HerreraAún no hay calificaciones
- Reacciones Grupos FuncionalesDocumento39 páginasReacciones Grupos FuncionalesJosë Antonio GuerreroAún no hay calificaciones
- Laboratorio N 15 Ésteres-Grupo 11Documento21 páginasLaboratorio N 15 Ésteres-Grupo 11Sady Maraz100% (1)
- Se Disuelven 180 Gramos de Sal en 800 Gramos de Agua y La Densidad de La Solución Es de 1'340 - Brainly - LatDocumento5 páginasSe Disuelven 180 Gramos de Sal en 800 Gramos de Agua y La Densidad de La Solución Es de 1'340 - Brainly - LatMarcela SilvaAún no hay calificaciones
- 1er Avance Proyecto Fisica (Grupo 02)Documento6 páginas1er Avance Proyecto Fisica (Grupo 02)Daniel Edison Castillo CachiAún no hay calificaciones
- 2da Ley Reacciones QuimicasDocumento30 páginas2da Ley Reacciones Quimicaszulema villca100% (1)
- Termoquimica. Cuaderno Ejercicios Sin SolucionesDocumento4 páginasTermoquimica. Cuaderno Ejercicios Sin SolucionesMaría del Carmen Rodríguez GarridoAún no hay calificaciones
- Análisis de parámetros físicos de calidad de aguaDocumento1 páginaAnálisis de parámetros físicos de calidad de agualorena fory100% (1)
- Tarea 1 Aplicación Procesos y Materiales en La IndustriaDocumento14 páginasTarea 1 Aplicación Procesos y Materiales en La Industriamarcela roseroAún no hay calificaciones
- Quimica - Cuestionario 1Documento3 páginasQuimica - Cuestionario 1xiomara valenciaAún no hay calificaciones
- GUIA#3 Quim Inor Fredy SuazoDocumento4 páginasGUIA#3 Quim Inor Fredy SuazoMauro CamoranoAún no hay calificaciones
- ACO Guía de Reacciones OrgánicasDocumento5 páginasACO Guía de Reacciones OrgánicasGianni D'Agostini SilvaAún no hay calificaciones
- 2 - Relaciones de FaseDocumento9 páginas2 - Relaciones de FaseFabian RodríguezAún no hay calificaciones
- TALLERUCQDocumento2 páginasTALLERUCQLuluAún no hay calificaciones
- C-Vitae Moises MichelDocumento3 páginasC-Vitae Moises MichelWilbert Méndez nietoAún no hay calificaciones
- Taller2 Sem 2 BiologiDocumento4 páginasTaller2 Sem 2 BiologiNicolasPC 25Aún no hay calificaciones
- Balances Sesion 2 02 - 2020 PDFDocumento13 páginasBalances Sesion 2 02 - 2020 PDFAlejandro Agudelo SanmartinAún no hay calificaciones
- Por qué los lípidos son solubles en solventes orgánicosDocumento1 páginaPor qué los lípidos son solubles en solventes orgánicosrubenmanuel5100% (2)
- Configuración Electrónica y Números CuánticosDocumento35 páginasConfiguración Electrónica y Números CuánticosRoy FloresAún no hay calificaciones